Method Article
Эффективный метод синтеза Пептоиды с мономерами смешанного типа Лизин / аргинин-типа и оценки их Анти-leishmanial деятельности
В этой статье
Резюме
A protocol to synthesize peptoids with mixed cationic functionality in the same sequence is presented (lysine- and arginine-type monomers). Subsequent testing of these compounds against Leishmania mexicana, the protozoan parasites that cause cutaneous leishmaniasis, is also described.
Аннотация
This protocol describes the manual solid-phase synthesis of linear peptoids that contain two differently functionalized cationic monomers. In this procedure amino functionalized 'lysine' and guanido functionalized 'arginine' peptoid monomers can be included within the same peptoid sequence. This procedure uses on-resin (N-(1-(4,4-dimethyl-2,6-dioxocyclohexylidene)ethyl) or Dde protection, orthogonal conditions to the Boc protection of lysine monomers. Subsequent deprotection allows an efficient on-resin guanidinylation reaction to form the arginine residues. The procedure is compatible with the commonly used submonomer method of peptoid synthesis, allowing simple peptoids to be made using common laboratory equipment and commercially available reagents. The representative synthesis, purification and characterization of two mixed peptoids is described. The evaluation of these compounds as potential anti-infectives in screening assays against Leishmania mexicana is also described. The protozoan parasite L. mexicana is a causative agent of cutaneous leishmaniasis, a neglected tropical disease that affects up to 12 million people worldwide.
Введение
Пептоиды (или поли N -замещенные глицинов) представляют собой класс пептидных миметиков , которые предлагают свойства , аналогичные свойствам пептиды и как таковые все чаще исследованных в лечебных и материалов применений. В пептидах, боковая цепь каждой аминокислоты соединяется с альфа-углеродом амидной цепи; в пептоиды боковые цепи сдвинуты на атоме азота позвоночника. Важно отметить, что это дает Пептоиды большую устойчивость к протеолизу.
Пептоиды обычно синтезируют с использованием метода submonomer начатую Цукермана и др., Где Пептоидные мономеры могут быть построены путем последовательной haloacetylation из с функциональностью амина , прилипшего к твердому носителю , и последующее замещение галогена с использованием первичного амина. 1 Наша группа недавно разработала адаптация к этому методу submonomer, чтобы позволить lysine- и аргинином типа Пептоидные остатки должны быть включены в тот же пептоидной последовательности для FIRST время. 2 Данное руководство твердофазный подход к пептоидной синтез использует коммерчески доступные реагенты и общее лабораторное оборудование, что делает его доступным для большинства лабораторий. Пептоиды было показано, что перспективные мероприятия в отношении широкого спектра грамотрицательных бактерий, грамположительных бактерий и видов грибов, которые сопоставимы с многими известными антимикробными пептидами. 3-9
В нашей работе Пептоиды были использованы в качестве новых противоинфекционных соединений для лечения лейшманиоза забытой тропической болезни. 5,10 лейшманиоз является эндемическим заболеванием в более чем 80 странах по всему миру , и предполагается , что более 12 миллионов человек во всем мире инфицированы. 11 заболевание вызывается простейшими паразитами, которые передаются через укусы москитов в. видов Leishmania может вызвать кожный лейшманиоз, условие , которое приводит к образованию рубцов и повреждения слизистых оболочек, или угрожающих жизни висцерального леяhmaniasis, что вызывает фатальное повреждение органа. Ни одна вакцина не является в настоящее время для этого заболевания, и существующие методы лечения полагаются на небольшое количество лекарств, которые имеют серьезные побочные эффекты. Кроме того, устойчивость к существующим лекарственным средствам является новой и серьезной проблемой , так что новые методы лечения крайне необходимы для эффективного лечения лейшманиоза в будущем. 12-16
В этих противомикробных применений, Пептоиды часто предназначены , чтобы быть амфипатический смесью катионных и гидрофобных мономеров. 3,4 Это может дать Пептоиды степень селективности по отношению к бактериальным клеткам снижают токсичность по отношению к клеткам млекопитающих, а также улучшить их активность в качестве молекулярных переносчиков . 17-20 большинство противоинфекционных пептоиды в литературе содержат катионные боковые цепи , которые являются исключительно состоящие из аминокислот либо функционализированный мономеров лизина типа или остатков аргинина типа. Пептид-Пептоидные химеры, где катионные цепи состоят из аМино кислоты лизин или аргинин, также были синтезированы с целью изучения влияния катионных групп по активности и токсичности. 21-25
Поли-лизин Пептоиды могут быть легко синтезированы с использованием коммерчески доступных Вос-защищенные амины. Поли-аргинином Пептоиды сообщили могут быть получены с использованием способа , который использует пиразол-1-карбоксамидин в качестве guanidinylation агента. 18 Тем не менее, это может быть проведена только после того, как пептоидной было отщепляют от смолы и защиты Вос на боковых цепей удалены, так каждый лизин-типа остаток в пределах последовательности, превращается в остаток аргинина. В попытке выполнить точную настройку химические и биологические свойства соединений, мы разработали метод , который позволяет двойную функциональность катионный (например, N и N Lys Arg) , которые будут включены в любой последовательности пептоидной впервые. 2
Здесь мы описываем синтеза, очистки и характеристики ТВто новые Пептоиды, которые содержат как lysine- и аргинин типа остатков в той же последовательности. Метод использует ортогональные N Бок и N -Dde защиты на смоле с пиразол-1-карбоксамидин в качестве реагента guanidinylation. Биологическая оценка этих пептоиды также описана в цитотоксичности против Leishmania Mexicana, возбудитель кожного лейшманиоза. Это обеспечивает практический метод, чтобы получить доступ к Пептоиды с двойной функциональностью катионного и для оценки их биологической активности. Ожидается, что этот метод будет способствовать синтез амфипатическими пептоиды путем пептоидной сообщества в будущем.
протокол
1. Твердофазный синтез Пептоиды
Примечание: Пептоиды синтезируются вручную с помощью процедуры submonomer синтеза в твердой фазе пептоидной. Этот метод обеспечивает высокую эффективность связывания и хороший конечный выход продукта. Синтез на твердой фазе позволяет также избыточные реагенты легко удалить в конце каждого этапа , и метод был модифицирован здесь , чтобы позволить различным функционализованные катионных мономеров (то есть, аргинин-типа и лизин типа остатков) , которые будут включены в тот же последовательность. 1,2
- Синтез линейного пептоидной
Внимание: Провести оценку безопасности перед началом синтеза. Выполнить все реакции в вытяжном шкафу и носить соответствующие средства индивидуальной защиты в зависимости от обстоятельств (то есть, одноразовые перчатки, защитные очки и лабораторный халат). Будьте особенно осторожны при использовании следующих реагентов и растворителей. Диметилформамид (ДМФ) является подозреваемым тератогенным и гichloromethane (DCM) является канцерогеном. N, N 'диизопропилкарбодиимид (DIC) и пиперидина опасны для глаз, кожи, органов дыхания через дыхательные пути и может вызвать раздражение кожи. Гидразин является канцерогеном, со смертельным исходом при вдыхании и вызывает сильные ожоги кожи или глаз. Бромуксусной кислоты также опасны для кожи, глаз и дыхательных путей и может вызвать ожоги при контакте. Трифторуксусную кислоту (ТФК) представляет собой летучую жидкость и может вызвать серьезные ожоги, так обращаться с осторожностью. Рекомендуется использовать тяжелые перчатки долг.- Добавить 0,12 г Fmoc-защищенный Каток амидную смолу (0,1 ммоль, типичная нагрузка 0,7 ммоль / г) в 20 мл с крышкой полипропиленовой реакционный сосуд с двумя фритт. Добавьте 5 мл диметилформамида (ДМФ) для набухания смолы и оставить сосуд отстояться в течение по крайней мере, 60 минут при комнатной температуре. Слить DMF с использованием твердофазного вакуумной экстракции платформы.
- Для снятия защиты группы Fmoc на набухшей смолы, добавляют 2 мл раствора пиперидина (20% в ДМФ об / об). Поместите данное судношейкер платформы при комнатной температуре (450 оборотов в минуту) и встряхивают в течение 5 мин. Удалите решение с помощью вакуумной станции.
- Повторите Fmoc снятие защиты с 2 мл раствора пиперидина и встряхивают в течение 15 мин при комнатной температуре. Слейте раствор, как и раньше.
- Промыть смолу путем добавления 2 мл ДМФА и перемешивание смолы в течение 30 сек. Слить DMF и повторить еще три раза.
- Для ацетилирования, добавляют 1 мл раствора бромуксусной кислоты (0,6 М в ДМФА) и 0,2 мл N, диизопропилкарбодиимид раствор N '(ДВС - синдром, 50% в DMF об / об). Оставьте реакционный сосуд встряхивают в течение 20 мин при комнатной температуре. Слейте раствор и промойте смолы с 2 мл ДМФ три раза.
- Для перемещения, прибавляют 1 мл раствора амина (1,5 М в ДМФ). Взболтать смолы в течение 60 мин при комнатной температуре. Слейте раствор и промойте смолы с 2 мл ДМФ три раза.
- Для добавления Аргинин типа мономера, следовать шаг 1.7. В зависимости от желаемой пептоидной последовательности, различные аминыбудет добавлено.
- Повторите шаги 1.1.4 и 1.1.5.
- Для того, чтобы включить гуанидина функционализированного мономера (то есть, N Arg), добавляют 1 мл раствора незащищенного диамина (1,5 М в ДМФА) к смоле и встряхивают в течение 60 мин при комнатной температуре.
- Слейте раствор и промойте смолы с 2 мл ДМФ три раза.
- Добавить 2-acetyldimedone (0,2 г, 1 ммоль в 0,5 мл ДМФ, 10 эквивалентов), чтобы добавить группу ДДЭ к свободному первичным амином и встряхивают в течение 60 мин при комнатной температуре. Слейте раствор и промойте смолы с 2 мл ДМФ три раза.
- Продолжить submonomer синтез, как в 1.1.4 до 1.1.7, пока желаемая последовательность выполнена. Добавить 2 мл ДМФ, чтобы вымыть смолу и повторить три раза.
- Для снятия защиты группы ДДЭ на смоле, добавляют 4 мл 2% -ного раствора гидразина (в ДМФА об / об) и встряхивают в течение 3 мин при комнатной температуре. Слейте раствор и повторить три раза.
- Слейте раствор и промойте смолы с 2 мл DMF три тРедакторы IME.
- Добавить пиразол-1-карбоксамидин (6 эквивалентов на свободный амин, то есть на N Arg мономеров, в минимальном объеме DMF) и N, N - диизопропилэтиламин или DIPEA (6 эквивалентов на свободный амин) и встряхивают при комнатной температуре в течение 60 мин ,
- Слейте раствор и промойте смолы с 2 мл дихлорметана три раза. Оставьте смолы высохнуть на воздухе в течение 10 мин, затем смолу можно хранить до расщепления (раздел 2).
- Чтобы приостановить синтез, промойте смолы с 2 мл DMF три раза. Добавьте 2 мл DMF, закупорить синтез сосуд и оставить при комнатной температуре в вытяжном шкафу.
Примечание: Синтез может быть приостановлена после того, как (может быть сформирован за исключением второго шага смещения как дикетопиперазинов) любой шаг перемещения.
- Боковой цепи снятие защиты и отщепление от смолы
- Провести тест-прилипнет, чтобы проверить ход синтеза (чистоты и массы) в любой точке в процессе синтеза после ДИСПЛЕЙцементные шаги, добавление или удаление Dde-защитной группы или после окончательной последовательности была сделана.
- Перенесите приблизительно 10 гранулы смолы из реакционного сосуда в новый 8 мл полипропиленовую спеченной картриджа.
- Добавьте 1 мл трифторуксусной кислоты коктейль скола (содержащий 95% ТФК, 2,5% H 2 O, 2,5% триизопропилсилан) и встряхивают в течение 90 мин при комнатной температуре.
- Фильтр Отщепление коктейль TFA из смолы с использованием спеченного реакционного сосуда в 10 мл круглодонную колбу.
- Упаривают коктейль расщепления с помощью роторного испарителя и растворяться образовавшееся масло в 1 мл смеси ацетонитрил / вода для представления ЖХ-МС или аналитической ВЭЖХ.
- Для окончательного расщепления: в том же пористым картридже реакции полипропилен , используемый для синтеза, добавляют 4 мл спайности коктейля TFA (95% TFA, 2,5% H 2 O, 2,5% триизопропилсилана) и крышку сосуда. Встряхивают в течение 90 мин при комнатной температуре.
- Фильтр-йе ТФК отщепление коктейль из смолы с использованием спеченного реакционного сосуда в 50 мл круглодонную колбу.
- Упаривают коктейль расщепления с помощью роторного испарителя. После того, как ТФУ был удален, продукт должен быть получен в виде масла. Для облегчения удаления TFA из этой сырой нефти, добавляют 2 мл безводного диэтилового эфира и пептоидной должен выпадать в осадок.
- Либо удалите диэтиловый эфир через пипетку и отбрасывать или испаряются с использованием роторного испарителя. осаждение Повторите диэтиловый эфир три раза.
- Растворите неочищенный пептоидной в 10 мл смеси ацетонитрил / подкисленный раствор воды (50% ацетонитрила, 0,1% ТФУ в воде об / об). Передача в предварительно взвешенную контейнере, замерзает при температуре 20 ° С и лиофилизации в виде сухого порошка.
- Провести тест-прилипнет, чтобы проверить ход синтеза (чистоты и массы) в любой точке в процессе синтеза после ДИСПЛЕЙцементные шаги, добавление или удаление Dde-защитной группы или после окончательной последовательности была сделана.
2. Характеристика и очистка
Примечание: пептоидной синтез можно контролировать и окончательный пептоидной оценивали с помощью аналитической ВЭЖХ с обращенной фазой с использованием колонки С18 и Эльectrospray масс-спектрометрии с жидкостным хроматографии (ЖХ-МС). Все ВЭЖХ растворители растворителей для ЖХ-МС должен быть свежеприготовленным.
- Аналитическую ВЭЖХ
- Взвесить 1 мг пептоидной в небольшом стеклянном флаконе. Добавить минимальный объем ацетонитрила растворять и разбавьте до 1 мл воды. Убедитесь в том, что пептоидной полностью не растворится.
- Вводят 10 мкл на аналитической ВЭЖХ (предложенный градиент 0 - 100% растворителя В в течение 30 мин, где растворитель А = 95% воды, 5% ацетонитрила, 0,05% ТФК и растворитель В = 95% ацетонитрила, 5% воды, 0,03% ТФК) , в соответствии с инструкциями изготовителя.
- Визуализируйте УФ-спектр при длине волны 220 нм.
- ESI ЖХ-МС
- Сделать 1 мг / мл раствора пептоидной как на этапе 2.1.1.
- Вводят 1 мкл к электрораспылением ЖХ-МС, чтобы определить, является ли молекулярный вес мишени пептоидной присутствует, используя инструкции производителя.
- Проверьте целевую массу пептоидной последовательности с использованием Peptподъязычная калькулятор, в соответствии с инструкциями на калькуляторе. 26 Этот веб - утилита также позволяет назначить любые удаление / продуктов присоединения видели в масс - спектре. 26
- Препаративная ВЭЖХ с обращенной фазой
- Растворите сырой Пептоиды в 2 мл подкисленной воды / ацетонитрила (95% воды, 5% MeCN, 0,1% TFA) и очищают с помощью препаративной ОФ-ВЭЖХ с использованием протокола производителя. Определить градиент, временем элюции, полученный из аналитической ВЭЖХ и количества впрыскиваемого будет зависеть от размеров столбцов.
- Визуализируйте использованием детектором при длине волны 220 нм.
- Собирают фракции в 15 мл центрифужные пробирки, замерзает при температуре 20 ° С и лиофилизации.
- Re-анализ фракций с помощью LC-MS и аналитической ВЭЖХ в соответствии с протоколом производителя. Рекомбинируют очищенные фракции.
3. Биологическое тестирование против Leishmania Mexicana Паразиты
Кауции:. Оценки безопасности должны проводиться перед началом синтеза Leishmania Mexicana классифицируется опасности группа 2 патоген в Великобритании и адекватных мер по контролю должны быть на месте до начала тестирования. Все работы должны быть выполнены в 2 -го класса безопасности микробиологические шкафа и соответствующие средства индивидуальной защиты носится в зависимости от обстоятельств (т.е. нитриловые перчатки, защитные очки и лабораторный халат).
- Субкультура паразитов
- Размораживание 1 мл -150 ° C замороженной Leishmania Mexicana M379 путем размещения флакон в водяную баню C 37 ° С в течение 30 сек.
- Передача исходного раствора до 10 мл среды насекомых Шнайдера (при рН 7,0 , дополненной 15% инактивированной нагреванием эмбриональной телячьей сыворотки и 1% пенициллина / стрептомицина) в 25 см 3 клеток колбу культуры с не вентилируемые крышкой.
- Инкубируют при 26 ° С в течение 72 ч.
- Изучение паразитов под микроскопом (400X увеличение), чтобы проверить состояние. ThEY должно быть насекомых promastigotes стадии, проциклической формы в лог-фазе с большим количеством делящихся клеток.
- Поддерживать проциклической promastigotes сублимитами культивировании паразитов до концентрации 5 × 10 5 паразитов / мл через каждые три дня. Граф клеток с использованием гемоцитометра Neubauer улучшенный.
- Трансформация L. этап Mexicana насекомых в стадии аксенными млекопитающих формы амастигота 27
- День 0: Приготовить 10 мл культуры стадии журнала паразитов на 5 х 10 5 паразитов / мл в среде насекомых Шнайдера (при рН 7,0 , дополненной 15% инактивированной нагреванием фетальной бычьей сыворотки и 1% пенициллина / стрептомицина) в 25 см 3 ячейки культуры колбу с невентилируемых крышкой.
- Инкубируют при 26 ° С в течение 48 часов.
- День 3: Перенесите 10 мл культуры в 50 мл центрифужную пробирку и центрифугируют при 447 х г в течение 5 мин.
- Слить старую среду и добавляют 10 мл среды насекомых Шнайдера (при рН 5,5, дополненной 20% чедят инактивированной фетальной телячьей сыворотки и 1% пенициллина / стрептомицина). Аккуратно ресуспендируют осадок паразитов в новой среде с помощью пипетки.
- Подсчитайте количество паразитов, использующих Нейбауера улучшенную гемоцитометра. Разбавляют до концентрации 5 × 10 5 паразитов / мл с рН 5,5 среды и передачи до 25 см 3 клеток колбу культуры.
- Инкубируют при 26 ° С в течение приблизительно 6 дней.
- День 9: Изучение паразитов под микроскопом (400X). Они должны быть в не-реплицирующейся, инфекционного метациклическим стадии промастиготы.
- Подсчитайте количество паразитов, использующих Нейбауера улучшенную гемоцитометра. Разбавляют до концентрации 5 × 10 5 паразитов / мл с рН 5,5 среды.
- Удалить 10 мл клеточной культуры и переносят в колбу для культивирования клеток. Инкубировать при 32 ° С в течение 5 дней.
- День 14: Проверьте появление паразитов под микроскопом (400X). Они должны быть в патогенной амастигота стадии, отсутствует жгутик характерЛьву promastigotes, и готов для анализа.
- Цитотоксичности на L. Mexicana аксенический amastigotes.
Примечание: Биологическая тестирование пептоиды использует высокую пропускную способность анализов, проведенных в 96-луночные планшеты. Этот протокол описывает испытание L. Mexicana аксенический amastigotes, но идентичные анализы также могут быть выполнены на этапе промастиготы паразитов в соответствующих средствах массовой информации. Соединения инкубируют с паразитами при концентрациях от 3 - 100 мкМ в течение 60 мин, а затем инкубировали в течение 24 ч следующего 10-кратного разведения. Результаты получили путем измерения флуоресценции лунки после инкубации с ресазурина на решение , основанное на жизнеспособность клеток (например, AlamarBlue).- Подготовить сложные растворы. Взвесить 1 мг конечного очищенного пептоидной продукта с использованием аналитических весов. Добавьте соответствующий объем молекулярной биологии сорта диметилсульфоксиде (ДМСО) до концентрации 5 мМ. Сделайте 6 мкл аликвоты изамерзать при температуре -20 ° C.
- Подготовить сложные решения на 96 - луночные планшеты (рекомендуемая компоновка пластины можно увидеть в разделе результатов, рисунок 6) в трех экземплярах от 100 до 3 мкМ. Добавляют 2 мкл 5 мМ исходного раствора каждого соединения в верхнем ряду (т.е. A). Добавьте 48 мкл свежей среды от насекомых Шнайдера (при рН 5,5 и 20% фетальной телячьей сыворотки (FBS), 1% пенициллина / стрептомицина (P / S)) в верхней строке, используя пипетку многоканальный. Добавьте 25 мкл среды насекомых Шнайдера для всех остальных строк (B - F).
- Проведите серийное разведение с помощью пипетки 25 мкл раствора из верхнего ряда. Добавить в строке ниже и перемешать. не Проводят разведений до последней строки, где должна быть выброшенной последнее решение 25 мкл.
- Использование амфотерицин В (5 мМ запасы) в качестве положительного контроля и ДМСО (2% раствор) в качестве отрицательного контроля в трех экземплярах.
- Приготовьте раствор паразита: передачи культуры в центрифужную пробирку объемом 50 мл и центрифуге при447 мкг в течение 5 мин. Слить старую среду и добавляют 10 мл среды Шнайдера насекомых (при рН 5,5 и 20% FBS, 1% P / S).
- Осторожно растворить осадок паразитов в новой среде с помощью пипетки и подсчета с использованием гемоцитометра Neubauer улучшенный. Разбавляют культуры до 8 × 10 6 паразитов / мл.
- Добавить 25 мкл L. Mexicana культуры в каждую лунку. Инкубируйте пластины в течение 60 мин при 32 ° С.
- Удалить пластины из инкубатора и удалить 40 мкл раствора из каждой лунки.
- Добавьте 90 мкл свежей среды и инкубируют в течение 24 ч при 32 ° С.
- Добавить 10 мкл ресазурин раствора на основе жизнеспособности клеток в каждую лунку. Выдержите в течение 4 ч при 32 ° С.
- Измерьте флуоресценцию с помощью планшет - ридера (λ ех = 540 нм, λ = 600 EM нм), в соответствии с инструкциями изготовителя. Анализ данных путем удаления среднего фона (из среды только скважин) и сравнивая флуоресценцию скважин после нормализации по отношению к Тон ДМСО контроля.
Результаты
В качестве показательного результата, синтеза и характеристики двух 12 остатков пептоиды, содержащих два мономера лизин-типа и мономеров типа два-Аргинин каждый будет описано ниже. Последующие результаты анализа цитотоксичности также показаны.
Два Пептоиды [(N nArg N SPE N SPE) (N АЭ N SPE N SPE)] 2 (а) и [(HArg N SPE N SPE N) (Lys N SPE N SPE)] 2 (б) , были синтезированы с использованием 120 мг Ринк Амид смолы каждый (загрузки = 0,79 ммоль / г). Все ацетилирования и водоизмещение стадии осуществляли, как описано выше, со всеми реагентами, приобретенные на коммерческой основе. Для этих остатков, следующие амины были использованы на стадии смещения: N ППУ (S) - (-) - альфа-метилбензиламин, N АЭ N - (трет - бутоксикарбонил) -1,2-диамinoethane, N Lys N - (трет - бутоксикарбонил) -1,4-диаминобутан. Для производных аргинина остатков, были связаны следующие незащищенные диамины: N HArg 1,4-диаминобутан или N nArg 1,2-диаминоэтан, с последующей защитой на смоле с 2-acetyldimedone (DDE-OH). После того, как вся последовательность была синтезирована, гидразин Удаление защитной группы из ДДЭ дает свободные амины в guanidinylate.
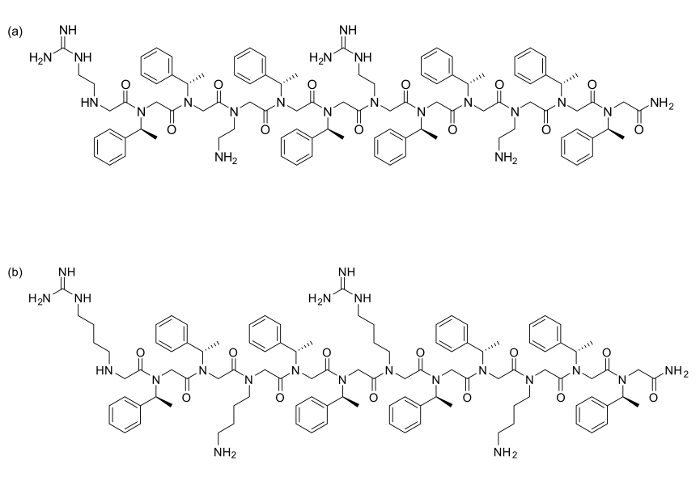
Рисунок 1. Пептоидные структуры (а) [(N nArg N спе N SPE) (N АЭ N спе N SPE)] 2 и (б) [(N HArg N спе N SPE) (N нг> Lys N спе N спе)] 2. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
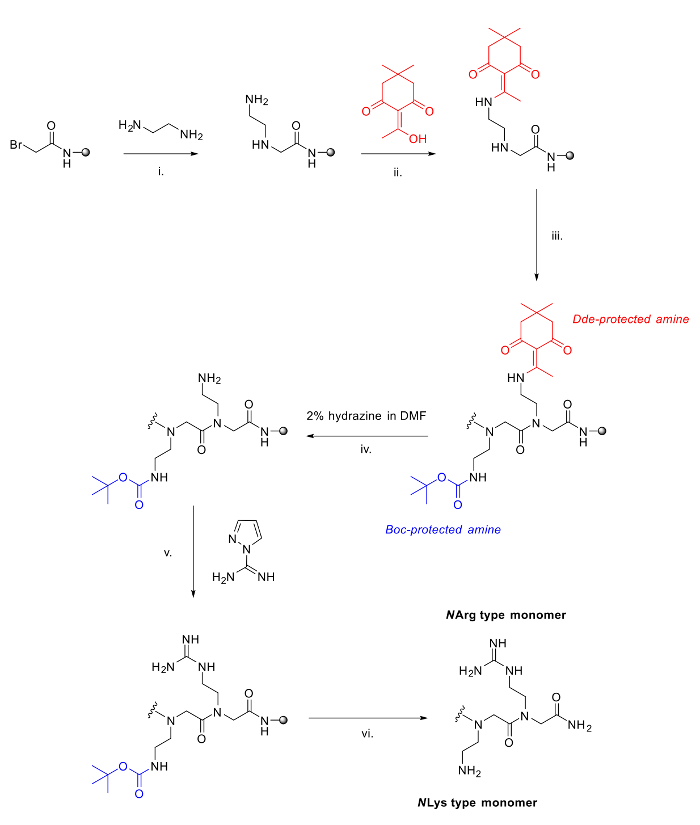
Рисунок 2. Метод , используемый для синтеза смешанных Пептоиды аргинин / лизин. I. Стандартный шаг перемещения в методе submonomer с диамина; II. Добавление ДДЭ-OH, 90 минут, чтобы защитить свободный амин; III. Дальнейшие дополнения расширить пептоидной цепочку с использованием метода submonomer; внутривенно Снятие защиты ДДЕ с использованием 2% гидразина в ДМФ; . V Guanidinylation свободного амина на смоле с пиразол-1-карбоксамидин и DIPEA в ДМФА; VI. Кислая отщепление от полимера и деблокирование с Вос групп.large.jpg "целевых =" _blank "> Пожалуйста, нажмите здесь, чтобы посмотреть увеличенную версию этой фигуры.
После отщеплени от смолы и лиофилизации, сырые продукты получают в виде белого порошка: (а) 154 мг, (б) 163 мг. Продукты очищали с помощью ОФ-ВЭЖХ, как описано с максимум 50 мг инъекции с использованием LC насос с UV-VIS детектором (λ = 250 нм) на аналитической колонке, 250 мм х 10 мм, 5 мкм; скорость потока = 2 мл / мин. Фракции, соответствующие массе мишени, объединяли и получали в виде белого порошка: (а) 54 мг (б) 65 мг, Конечный выход приблизительно 30% для фракций> 90% чистыми.
Конечное соединение идентичностей после очистки были подтверждены с помощью ЖХ-МС (смотри рисунок 3) с использованием тройной квадрупольный масс - спектрометр , снабженный UPLC и детектором Фотодиод массива. Точная масс-спектрометрия была проведена с использованием того же спектрометра на Т он [М + 2Н] 2+. Следующие вычисляются и наблюдаемые массы были найдены в близком согласии (рисунок 4): (а) рассчитывается = 896,0026 а.е.м., наблюдаемый = 896,0038 а.т.е.; (Б) рассчитывается = 952,0691 а.е.м., наблюдаемый = 952,0730 а.е.м..
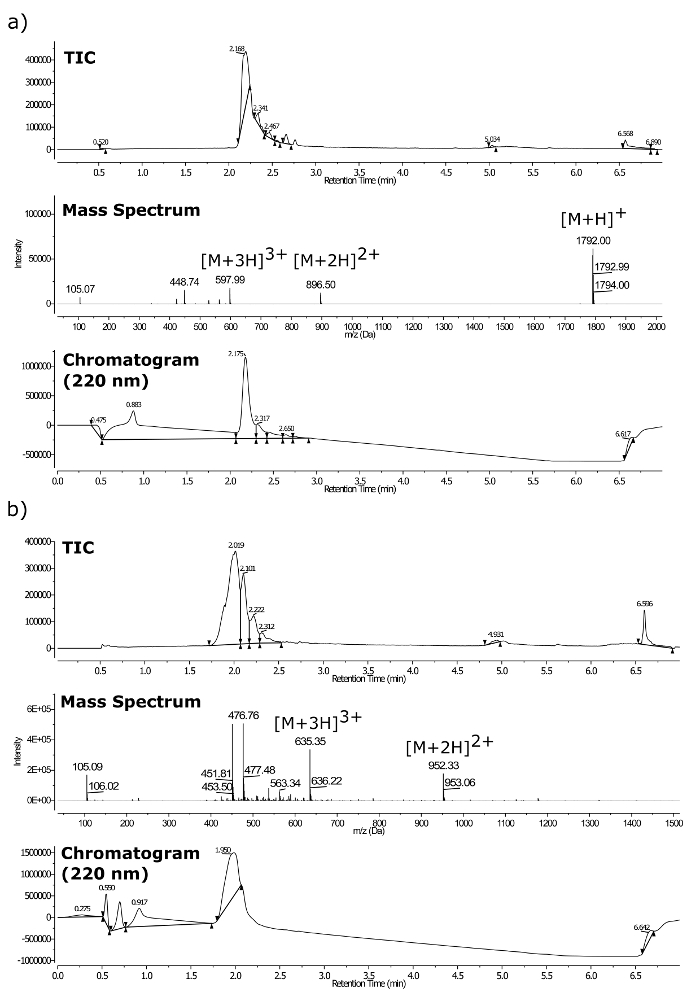
Рисунок 3. ЖХ-МС для очищенных пептоиды. (А) м / з = 1792 и (б) м / з = +1903. Там , где вершина TIC, средний спектр LC-MS, снизу УФ - хроматограммы при длине волны 220 нм. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
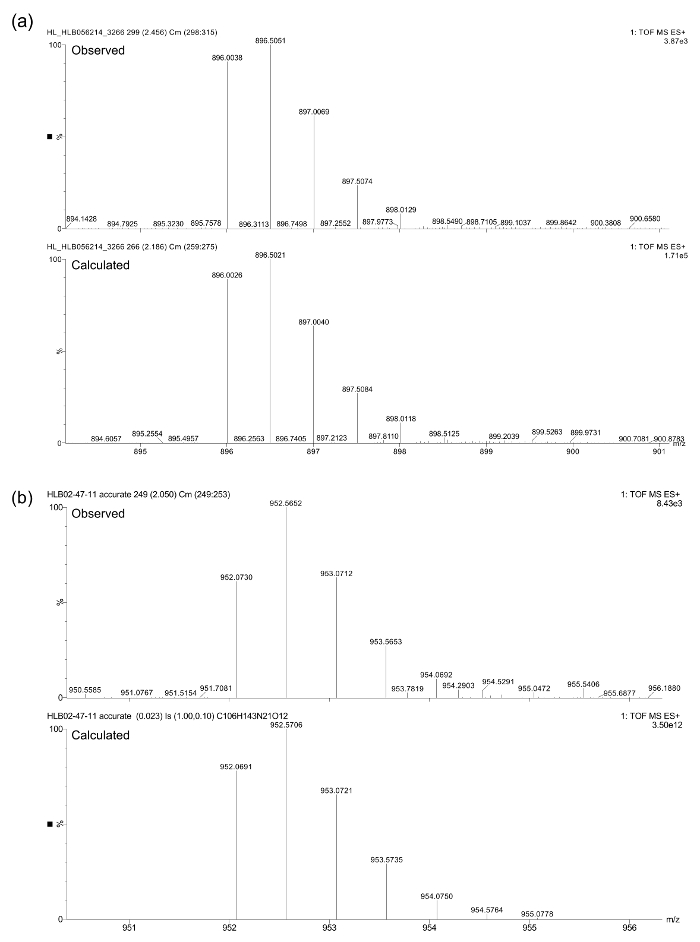
Рисунок 4. Точные данные масс - спектрометрии для пептоиды (а) и (б)."Https://www.jove.com/files/ftp_upload/54750/54750fig4large.jpg" целевых = "_blank"> Пожалуйста, нажмите здесь, чтобы посмотреть увеличенную версию этой фигуры.
чистота продукта оценивали с использованием аналитической ОФ-ВЭЖХ (LC насос с детектором UV-VIS на аналитической колонке, 4,6 мм х 100 мм, 3,5 мкм, скорость потока = 1 мл / мин), и визуализировали при 220 нм оптическую плотность амида главной цепи. на рисунке 5а и 5b показано , что соединения являются однородными.
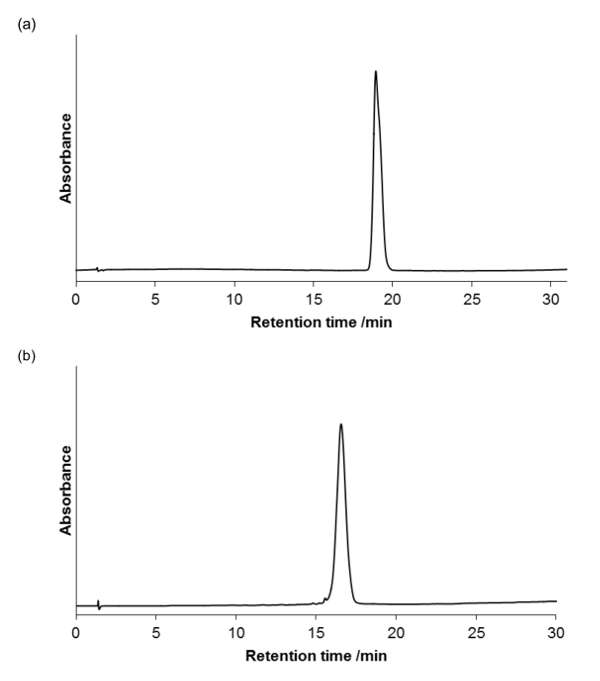
Рисунок 5. Аналитическую ВЭЖХ для очищенных пептоиды (а) и (б). Существует градиент 0-100% В в течение 30 минут, колонка печи при 40 ° C (A = 95% H 2 O, 5% MeCN, 0,05 % ТФК;. В = 95% MeCN, 5% H 2 O, 0,03% ТФК) Пожалуйста , клИк здесь, чтобы посмотреть увеличенную версию этой фигуры.
Очищенные Пептоиды (а) и (б) были испытаны в цитотоксичности против L. Mexicana аксенический amastigotes. Замороженные запасы L. Mexicana были разморожены и превращены в амастигота стадии готовности для анализа. Через 72 часа после размораживания, паразиты должны насекомых promastigotes стадии их проциклической форме, в лог-фазе с большим количеством делящихся клеток. На этой стадии паразиты могут быть преобразованы в амастигота стадии с использованием сдвига рН и температуры , описанный. 27 На 9 -й день трансформации, паразиты будут в не тиражирование инфекционной стадии метациклическими промастиготы. Наконец , в 14 -й день, паразиты должны находиться в стадии патогенного амастигота , где паразиты не хватает характерный жгутики из promastigotes. 28
Были сделаны 5 мМ исходные растворы соединений в начальной клеточной культуры ДМСО и тестировали в трех повторах набыло собрано как минимум два раза, чтобы обеспечить надежный набор данных. Представитель план 96-луночный планшет показан на рисунке 6. В конце анализа, реагент жизнеспособности клеток добавляли в каждую лунку , и флуоресценцию измеряли , как описано для расчета жизнеспособности паразитов при каждой тестируемой концентрации (см рисунок 7 ). Значения ED 50 рассчитывали как пептоидной (а)> 100 мкМ и пептоидной (б) 37 мкМ соответственно. Столбики ошибок графике, показывают, что вариации между скважинами как стандартное отклонение, и это можно увидеть, что это разумно для большинства баров.
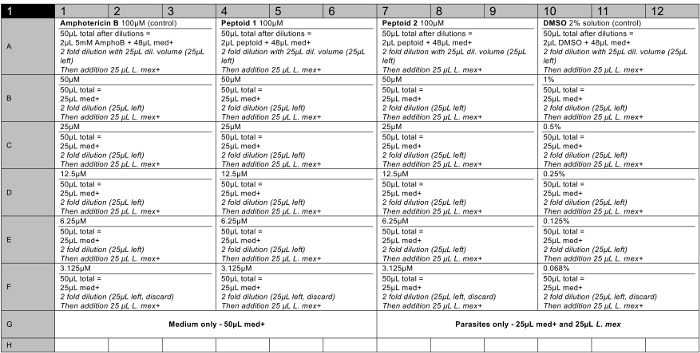
Рисунок 6. Представитель 96 также план пластина для анализа на цитотоксичность , на 2 -х пептоидной растворов ( в том числе и положительный и отрицательный контроли). Мед + = средняя (Шнайдера насекомых Среда, рН 5,5, 20% FBS, 1% P / S). Л. MEX. знак равно8 × 10 6 / мл паразитом культуры в мед +. AmphoB = 5 мМ в ДМСО. Пептоидной = 5 мМ исходного раствора в ДМСО. Пустые лунки должны содержать стерильную воду. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
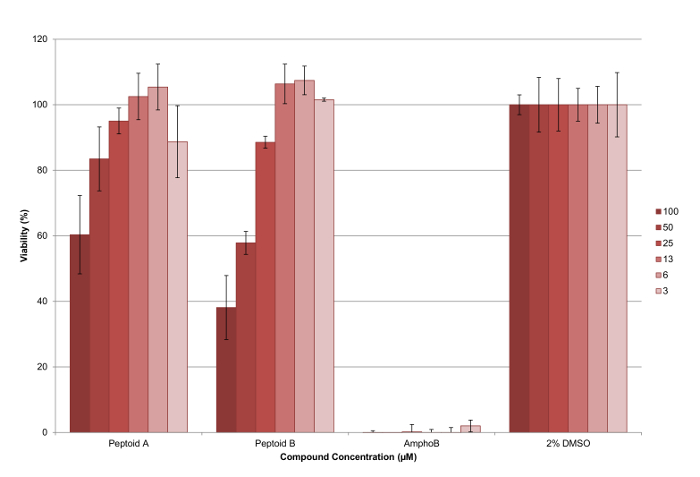
Рисунок 7. Результаты от цитотоксичности против L. MEXICANA аксенический амастигота паразиты , использующие пептоидной (а) и (б). Можно видеть , что пептоидной (б) более эффективен , чем пептоидной (а) при снижении доли жизнеспособных паразитов, причем оба соединения , обладающие дозозависимым эффектом. Столбики ошибок показывают нанесенные на график изменения между скважинами в качестве стандартного отклонения. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
Обсуждение
Пептоиды все чаще изучаются в химической биологии и лекарственных областях химии в таких областях применения , как новой терапии 3-5, их доставка агентов 18,20 и диагностические средства. 29 Как правило, эти последовательности являются катионными , чтобы обеспечить определенную степень селективности по отношению к патогену над клетки млекопитающих, способность проникать через клеточные мембраны, а также способствовать растворимости в водных системах. Существуют многочисленные примеры катионных пептоиды, которые содержат исключительно lysine- или аргинин-миметик остатки в литературе. Тем не менее, на сегодняшний день, синтез пептоиды, которые содержат оба этих катионных остатков в той же последовательности, было затруднено из-за отсутствия подходящей методики синтеза. Протокол, описанный здесь, позволяет смешанные катионные Пептоиды синтезироваться эффективным образом и весьма желательно, так как он предлагает маршрут модулировать биологические и химические свойства амфипатическими пептоиды.
нт "> Наш метод использует приспособление к обычно используемым submonomer синтеза пептоидной и допускает добавление как lysine- и аргинином типа мономеров в пределах той же последовательности. Он использует температуры в помещении, в муфтах и установили защитную группу химии, так что ожидается, что этот метод будет полезен для большинства исследовательских групп. Чтобы добавить ортогональную защиту остатка аргинина типа, незащищенная диамина добавляют при стандартных условиях замещения, а затем защищенный в 60-минутной сопряжении с Dde-ОН. разнообразие диаминов могут быть используется , которая позволяет боковые цепи от 2 до 6 углеродных атомов углерода длиной быть установлен, то есть 1,2-диаминоэтаном до 1,6-диаминогексана соответственно. защитную Dde-ОН хорошо растворяется в ДМФА , и является очень эффективным и избирательным защитную группу для первичные амины. группа Dde защита оставляет вторичные амины не зависит, например, незащищенного N - конец цепи пептоидной. 30 Одно ограничение заключается в том , что все синДиссертация была проведена вручную; Тем не менее, предполагается, что условия сопряжения, разработанные делают метод поддающийся для использования с автоматизированными пептид / пептоидной синтезаторах.На смоле Удаление защитной группы из ДДЭ-групп осуществляется с использованием 2% -ного раствора гидразина в ДМФ, чтобы оставить свободные амины, которые могут быть guanidinylated на смоле с использованием пиразол-1-карбоксамидин. Шесть эквивалентов пиразол-1-карбоксамидин и шесть эквивалентов DIPEA используют на свободный амин на смоле (например, шесть эквивалентов для каждого типа мономера N Arg быть установлен). Опять же, эта реакция является также эффективным и реагент пиразол-1-карбоксамидин имеет хорошую растворимость в DMF. По завершении реакции, как правило, рассматривается с помощью ЖХ-МС, после того, как 60 минут при комнатной температуре.
Благодаря универсальности метода submonomer, большое разнообразие первичных аминов могут быть использованы на этапе перемещения таким образом условия, возможно, должны быть оптимизированы для увеличения сцепления Эффитивности и общий выход продукта или чистота. 31 Для последовательностей , описанных выше, никаких особых условий не были необходимы для успешных соединений. Тем не менее, более длительное время перемещения или более высокие концентрации амина , могут быть использованы для проблематичных перемещений (т.е. для слабонуклеофильной или стерически громоздких амины). Некоторые амины не могут быть полностью растворимы в ДМФА, в этом случае рекомендуется , чтобы растворить их в N - метил-2-пирролидон (NMP), или других подходящих растворителей для твердофазных реакций , вместо того, чтобы, как и в предыдущем комплексного метода синтеза submonomer из пептоиды. 32 , чтобы включать мономеры, содержащие незащищенные гетероатома в боковых цепях, ацетилирование с использованием хлоруксусной кислоты , как было показано , чтобы быть эффективными другими группами. 33 Кроме того, другие смолы могут быть использованы с этим методом , чтобы получить Пептоиды с различным C Концевая функционализации. Ван смол и 2-хлортритильной хлоридные смолы обычно используются вsubmonomer синтез пептоиды. Например, этот метод был успешно использован с 2-хлортритильной хлорида смолы в нашей группе. 2 Различные твердые носители потребуется другой процедуры загрузки для Ринк Амид обсуждается здесь ( в зависимости от конкретной используемой смолы) , так что это должно быть проверено с литературой перед синтезом.
Подобно пептидного синтеза, условия для окончательного расщепления пептоидной выключения смолы также могут быть оптимизированы для конкретной последовательности. В этом протоколе, спайности коктейль ТФУ использовали (с триизопропилсилана и воды в качестве поглотителей). В Пептоиды, представленные здесь содержали только защиту Вос, которая является разумной кислотно-лабильную группу. Для того, чтобы обеспечить полное удаление защитных групп последовательностей с большей долей защищенных остатков или меньше кислоты лабильной защитной группы, более длительное время расщепления может быть необходимо (например, раз спайности свыше 2 часов , рекомендуются для последовательностей , которые содержат PBF или трет-BUТыл эфир защищенные группы). Альтернативные акцепторы могут также быть использованы для специализированных боковых цепей (например, этандитиол или 2-меркаптоэтанол, часто используются в пептиды, которые имеют серусодержащих боковые цепи, такие как цистеин или метионин).
Биологический анализ представлен стандартный тест на цитотоксичность, который может быть изменен, чтобы удовлетворить различные клеточные линии. Важно отметить, что каждый из 96-луночный планшет должен содержать достаточное количество элементов управления, чтобы обеспечить уверенность в полученных результатах. В этом случае, амфотерицин В используется в качестве положительного контроля, как это известный препарат, используемый для лечения заболевания и ДМСО используют в качестве отрицательного контроля, поскольку это растворитель, используемый, чтобы сделать растворы соединений для анализа. Если используются другие клеточные линии, альтернативные, подходящие средства управления должны быть получены и проверены перед использованием. Л. Mexicana инкубируют с пептоидной при концентрациях от 100 до 2 мкМ в течение одного часа, а затем паразит / пептоидной раствор разбавляетсяв десять раз в течение инкубации в течение ночи (т.е. скважины первоначально с 100 мкМ пептоидной запаса разбавляют до 10 мкМ).
Реагент жизнеспособность клеток добавляют в каждую лунку (10% от общего объема скважины) в конце анализа. Видимое изменение цвета наблюдается между скважинами с жизнеспособных паразитов (розовый), контрольные лунки без каких-либо жизнеспособных паразитов (синий) и спектра между промежуточными числом жизнеспособных паразитов. Флуоресценции пропорциональна числу живых клеток и соответствует метаболической активности клеток; ресазурина краситель (нефлуоресцирующего) преобразуется в флуоресцентном ресоруфина путем реакций восстановления в метаболически активных клетках. 34 В этом анализе время инкубации с реагентом жизнеспособность клеток была оптимизирована для L. Mexicana. Инкубационные раз с жизнеспособностью реагента будет изменяться для пластин высевали при различных концентрациях клеток или с различными клеточными линиями (например, этот метод также может быть использованс клетками млекопитающих). В зависимости от конкретного используемого ридере, соображения должны быть сделаны прежде, чем измерения флуоресценции принимаются. Любые пузырьки воздуха в скважинах должны быть удалены, чтобы обеспечить точные показания могут быть приняты. Некоторые читатели пластины считывают из нижней пластин, и в этом случае плоскодонных 96-луночных планшетах должны быть использованы. Другие машины могут читать из верхней части пластины, так что крышка пластины должна быть удалена перед измерением.
И, наконец, в будущем, этот протокол может быть совместима с автоматизированным синтезаторов, которые способны сделать много последовательностей параллельно. Кроме того, синтез циклических пептоиды также возможно с использованием этого метода. Этот протокол должен обеспечить исследователей практической методики синтеза, которые могут быть использованы для получения доступа к новым пептоидной подмости с обеих lysine- и аргинином типа мономеров, которые могут быть полезными во многих областях применения, в том числе материалов или лекарственных полей.
Раскрытие информации
The authors have nothing to disclose.
Благодарности
Мы благодарим инженерных и физических наук исследовательский совет (EPSRC) для финансовой поддержки (HLB). Мы также благодарим Sridevi Maalika Ramanoudjame за помощь во время съемок этой процедуры.
Материалы
| Name | Company | Catalog Number | Comments |
| Polypropylene solid phase extraction cartridges with two frits | Crawford Scientific | 12131017 and 12131015 | 20 ml and 6 ml cartridges used in this preparation |
| Trifluoroacetic acid | Tokyo Chemical Industry (Europe) | T0431-100g | >98%; CAUTION: can cause severe burns and respiratory irritation |
| N,N'-diisopropylcarbodiimide | Sigma Aldrich | 38370-100ML | >98%; CAUTION: hazardous to eyes, skin and via respiratory inhalation, may also cause sensitisation |
| Dimethylformamide | Fischer Scientific | 10346180 | HPLC grade; CAUTION: suspected teratogen |
| Acetonitrile | Fischer Scientific | 10407440 | HPLC grade |
| Dichloromethane | Fischer Scientific | 10354263 | 99.8%; CAUTION: suspected carcinogen |
| Bromacetic acid | Sigma Aldrich | 17000-100G | >99%; CAUTION: causes burns and hazardous to skin, eyes and respiratory tract |
| (S)-(-)-alpha methylbenzylamine | Sigma Aldrich | 115568-100G | 98%; CAUTION: harmful if swallowed, toxic in contact with skin, causes severe skin burns and eye damage, used to synthesise the Nspe monomer |
| N-Boc 1,4-diaminobutane | Tokyo Chemical Industry (Europe) | A1373-25g | >98%; CAUTION: causes severe skin burns and eye damage, used to synthesise the NLys monomer |
| N-Boc 1,2-diaminoethane | Tokyo Chemical Industry (Europe) | A1371-25g | >97%; CAUTION: causes severe skin burns and eye damage, used to synthesise the Nae monomer |
| 1,2-diaminobutane | Sigma Aldrich | D13208-100G | 99%; CAUTION: flammable liquid and vapour, harmful if swallowed or inhaled, toxic in contact with skin, causes severe skin burns and eye damage, used in the synthesis of the NhArg monomer |
| 1,4-diaminoethane | Sigma Aldrich | 03550-250ML | >99.5%; CAUTION: flammable liquid and vapour, harmful if swallowed or inhaled, toxic in contact with skin, causes severe skin burns and eye damage, used in the synthesis of the NnArg monomer |
| 1H-pyrazole-1-carboxamidine HCl | Sigma Aldrich | 402516-10G | as HCl salt; CAUTION: harmful if swallowed and may cause an allergic skin reaction, causes serious eye damage |
| Hydrazine monohydrate | Sigma Aldrich | 207942-5G | reagent grade; CAUTION: suspected carcinogen, fatal if inhaled and causes severe burns to skin and eyes |
| 2-acetyl dimedone | Novabiochem | 8510150005 | Dde-OH |
| Rink Amide resin | Novabiochem | 8551190005 | 100-200 mesh, high loading |
| Piperidine | Sigma Aldrich | 411027-1L | >99.5%, a controlled substance, so adequate permission must be obtained before purchase; CAUTION: highly flammable liquid and vapour, harmful if swallowed and toxic in contact with skin or if inhaled, causes severe skin burns and eye damage, harmful to aquatic life with long lasting effects |
| Triisopropylsilane | Sigma Aldrich | 233781-50G | 98%; CAUTION: flammable liquid and vapour, causes skin irritation and serious eye irritation |
| alamarBlue | ThermoFischer | DAL1025 | Not classified as hazardous |
| Schneider's Insect Medium | Sigma Aldrich | S9895-1L | Powdered, medium must be made prior to use following manafacturers instructions; allow to warm to room temperature before use in biological assays |
| 96 well plates | VWR | 734-1793 | Flat bottom (to allow fluorescence measurement from the bottom), tissue-culture treated |
| Solvent reservoirs | VWR | 613-1182 | Used with multi channel pipette |
| Multi channel pipette | Eppendorf | 3122000043 | |
| Pipette tips | Starlab Group | S1111-3810, S1113-1810, S1111-6810 | Volume of tip dependent on pipette used. 10 µl, 10 - 200 µl and 1,000 µl recommended for assays |
| 25 cm3 cell culture flasks | VWR | 734-2312 | |
| 50 ml centrifuge tubes | VWR | 525-0791 | |
| dimethylsulphoxide (molecular biology grade) | Sigma Aldrich | D8418-50ML | Not classified as hazardous |
| Heat Inactivated Fetal Bovine Serum | ThermoFischer | 10082139-100mL | Gibco |
| Penicillin/Streptomycin | ThermoFischer | 15140148-20mL | Abbreviation: P/S |
| Amphotericin B | Sigma Aldrich | 46006-100mg | Amphotericin B trihydrate, VetranalTM analytical standard |
Ссылки
- Zuckermann, R. N., Kerr, J. M., Kent, S. B. H., Moos, W. H. Efficient method for the preparation of peptoids oligo(N-substituted glycines) by submonomer solid-phase synthesis. J. Am. Chem. Soc. 114, 10646-10647 (1992).
- Bolt, H. L., Cobb, S. L. A practical method for the synthesis of peptoids containing both lysine-type and arginine-type monomers. Org. Biomol. Chem. 14, 1211-1215 (2016).
- Mojsoska, B., Zuckermann, R. N., Jenssen, H. Structure-activity relationship study of novel peptoids that mimic the structure of antimicrobial peptides. Antimicrob Agents Chemother. , (2015).
- Chongsiriwatana, N. P., et al. Peptoids that mimic the structure, function, and mechanism of helical antimicrobial peptides. Proc. Natl. Acad. Sci. USA. 105, 2794-2799 (2008).
- Eggimann, G. A., Bolt, H. L., Denny, P. W., Cobb, S. L. Investigating the Anti-leishmanial Effects of Linear Peptoids. Chem Med Chem. 10, 233-237 (2015).
- Kapoor, R., et al. Antimicrobial Peptoids Are Effective against Pseudomonas aeruginosa Biofilms. Antimicrob. Agents Chemother. 55, 3054-3057 (2011).
- Ryge, T. S., Frimodt-Moller, N., Hansen, P. R. Antimicrobial activities of twenty lysine-peptoid hybrids against clinically relevant bacteria and fungi. Chemotherapy. 54, 152-156 (2008).
- Huang, M. L., Benson, M. A., Shin, S. B. Y., Torres, V. J., Kirshenbaum, K. Amphiphilic Cyclic Peptoids That Exhibit Antimicrobial Activity by Disrupting Staphylococcus aureus Membranes. Eur. J. Org. Chem. , 3560-3566 (2013).
- Huang, M. L., Shin, S. B. Y., Benson, M. A., Torres, V. J., Kirshenbaum, K. A Comparison of Linear and Cyclic Peptoid Oligomers as Potent Antimicrobial Agents. Chem Med Chem. 7, 114-122 (2012).
- Bolt, H. L., Eggimann, G. A., Denny, P. W., Cobb, S. L. Enlarging the Chemical Space of Anti-leishmanials: a Structure-Activity Relationship Study of Peptoids against Leishmania mexicana, a Causative Agent of Cutaneous Leishmaniasis. Med Chem Comm. , (2016).
- Chon, S. Y., et al. Antibiotic overuse and resistance in dermatology. Dermatologic therapy. 25, 55-69 (2012).
- Alvar, J., et al. Leishmaniasis Worldwide and Global Estimates of Its Incidence. PLOS ONE. 7, (2012).
- Croft, S. L., Barrett, M. P., Urbina, J. A. Chemotherapy of trypanosomiases and leishmaniasis. Trends Parasitol. 21, 508-512 (2005).
- Kedzierski, L. Leishmaniasis Vaccine: Where are We Today?. J Global Infect Dis. 2, 177-185 (2010).
- Croft, S. L., Sundar, S., Fairlamb, A. H. Drug resistance in leishmaniasis. Clin Microbiol Rev. 19, 111-126 (2006).
- Huang, W., et al. Learning from Host-Defense Peptides: Cationic, Amphipathic Peptoids with Potent Anticancer Activity. PLOS ONE. 9, (2014).
- Wender, P. A., et al. The Design, Synthesis, and Evaluation of Molecules That Enable or Enhance Cellular Uptake: Peptoid Molecular Transporters. Proc. Natl. Acad. Sci. USA. 97, 13003-13008 (2000).
- Schröder, T., et al. Peptoidic Amino- and Guanidinium-Carrier Systems: Targeted Drug Delivery into the Cell Cytosol or the Nucleus. J. Med. Chem. 51, 376-379 (2008).
- Kömel, D. K., et al. Cell-penetrating peptoids: Introduction of novel cationic side chains. Eur. J. Med. Chem. 79, 231-243 (2014).
- Hein-Kristensen, L., Knapp, K. M., Franzyk, H., Gram, L. Bacterial membrane activity of α-peptide/β-peptoid chimeras: Influence of amino acid composition and chain length on the activity against different bacterial strains. BMC Microbiology. 11, 1-12 (2011).
- Su, Y., Doherty, T., Waring, A. J., Ruchala, P., Hong, M. Roles of Arginine and Lysine Residues in the Translocation of a Cell-Penetrating Peptide from (13)C, (31)P and (19)F Solid-State NMR. Biochem. 48, 4587-4595 (2009).
- Andreev, K., et al. Guanidino groups greatly enhance the action of antimicrobial peptidomimetics against bacterial cytoplasmic membranes. BBA Biomembranes. 1838, 2492-2502 (2014).
- Foged, C., et al. Cellular uptake and membrane-destabilising properties of alpha-peptide/beta-peptoid chimeras: lessons for the design of new cell-penetrating peptides. BBA Biomembranes. 1778, 2487-2495 (2008).
- Vedel, L., et al. Antiplasmodial and prehemolytic activities of alpha-peptide-beta-peptoid chimeras. Chem Bio Chem. 8, 1781-1784 (2007).
- Lear, S., Cobb, S. L. Pep-Calc.com: a set of web utilities for the calculation of peptide and peptoid properties and automatic mass spectral peak assignment. J Computer-Aided Mol Des. , 1-7 (2016).
- Bates, P. A. Complete developmental cycle of Leishmania mexicana in axenic culture. Parasitol. 108, 1-9 (1994).
- Gossage, S. M., Rogers, M. E., Bates, P. A. Two separate growth phases during the development of Leishmania in sand flies: implications for understanding the life cycle. Int J Parasitology. 33, 1027-1034 (2003).
- Seo, J., Lee, B. C., Zuckermann, R. N., Ducheyne, P. . Comp Biomaterials. 2, 53-76 (2011).
- Nash, I. A., Bycroft, B. W., Chan, W. C. Dde - A selective primary amine protecting group: A facile solid phase synthetic approach to polyamine conjugates. Tetrahedron Lett. 37, 2625-2628 (1996).
- Culf, A. S., Ouellette, R. J. Solid-phase synthesis of N-substituted glycine oligomers (alpha-peptoids) and derivatives. Molecules. 15, 5282-5335 (2010).
- Tran, H., Gael, S. L., Connolly, M. D., Zuckermann, R. N. Solid-phase Submonomer Synthesis of Peptoid Polymers and their Self-Assembly into Highly-Ordered Nanosheets. J Vis Exp. , e3373 (2011).
- Burkoth, T. S., Fafarman, A. T., Charych, D. H., Connolly, M. D., Zuckermann, R. N. Incorporation of unprotected heterocyclic side chains into peptoid oligomers via solid-phase submonomer synthesis. J. Am. Chem. Soc. 125, 8841-8845 (2003).
- Nakayama, G. R., Caton, M. C., Nova, M. P., Parandoosh, Z. Assessment of the Alamar Blue assay for cellular growth and viability in vitro. J Immunol Methods. 204, 205-208 (1997).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены