Method Article
Обнаружение горизонтального переноса генов, опосредованного природными конъюгативными плазмидами у E. coli
В этой статье
Резюме
Конъюгация опосредует горизонтальный перенос генов, мобилизуя плазмидную ДНК через две разные клетки, способствуя распространению полезных генов. В данной работе описан широко используемый метод эффективного детектирования конъюгативного переноса плазмиды, основанный на использовании дифференциальных маркеров в конъюгативной плазмиде, доноре и реципиенте для выявления трансконъюгации.
Аннотация
Конъюгация представляет собой один из основных механизмов, способствующих горизонтальному переносу генов у грамотрицательных бактерий. В данной работе описываются методы изучения мобилизации встречающихся в природе конъюгативных плазмид на примере двух встречающихся в природе плазмид. Эти протоколы основаны на дифференциальном присутствии селективных маркеров в донорской, реципиентной и конъюгативной плазмиде. В частности, описанные способы включают 1) идентификацию природных конъюгативных плазмид, 2) количественное определение скоростей конъюгации в твердой культуре и 3) диагностическое обнаружение генов устойчивости к антибиотикам и типов репликонов плазмид у трансконъюгантных реципиентов с помощью полимеразной цепной реакции (ПЦР). Описанные здесь протоколы были разработаны в контексте изучения эволюционной экологии горизонтального переноса генов для скрининга присутствия конъюгативных плазмид, несущих гены устойчивости к антибиотикам, у бактерий, обнаруженных в окружающей среде. Эффективный перенос конъюгативных плазмид, наблюдаемый в этих экспериментах в культуре, подчеркивает биологическую значимость конъюгации как механизма, способствующего горизонтальному переносу генов в целом и распространению устойчивости к антибиотикам в частности.
Введение
В 1946 году Ледерберг и Татум1 описали половой процесс у Escherichia coli K-12, который теперь известен как конъюгация. Бактериальная конъюгация - это процесс, посредством которого бактериальная клетка (донор) однонаправленно передает генетический материал другой клетке (реципиенту) путем прямого межклеточного контакта. Конъюгация широко распространена в бактериях2,3, хотя доля донорских клеток, экспрессирующих механизм конъюгации, обычно очень мала4.
Плазмиды представляют собой автономно реплицирующиеся внехромосомные элементы ДНК. В дополнение к генам, участвующим в репликации и поддержании плазмиды, плазмиды часто несут груз генов, участвующих в адаптации к экологическим проблемам, таким как тяжелые металлы или воздействие антибиотиков5. Конъюгативные плазмиды представляют собой класс плазмид с набором специализированных генов, которые позволяют их перенос в клетки-реципиенты и поддерживают их персистенцию после переноса6. Конъюгативные плазмиды варьируются по размеру от 21,8 кб до 1,35 Мб у бактерий типа Pseudomonadota (синоним Proteobacteria), со средним размером около 100 кб 5,7. Они также, как правило, имеют низкое число копий, возможно, чтобы поддерживать метаболическую нагрузку на хозяина на низкомуровне 8,9.
Типичный конъюгативный аппарат состоит из четырех компонентов: источника переноса (oriT), релаксазы, связывающего белка IV типа и системы секреции IV типа (трубчатая структура, называемая пилусом, которая позволяет донорам связываться с реципиентами)6. Только очень небольшая часть клеток, несущих конъюгативные плазмиды, экспрессируют механизм конъюгации4, но если плазмиды обеспечивают преимущество в приспособленности, трансконъюганты могут быстро расширяться в популяции. От 35% до более 80% изолятов E. coli, собранных из разных мест обитания, имеют конъюгативные плазмиды с генами, которые придают устойчивость по крайней мере к одному антибиотику10,11; Таким образом, горизонтальный перенос генов, опосредованный конъюгативными плазмидами, является основным механизмом, способствующим глобальному распространению генов устойчивости к антибиотикам12.
Эксперименты по спариванию, проведенные в лабораторных культурах, показали, что на частоту конъюгации влияет множество факторов, включая характер клеток-реципиентов, фазу роста, плотность клеток, соотношение доноров и реципиентов, проводится ли конъюгация в жидких или твердых средах, углерод, кислород, соли желчных кислот, концентрации металлов, присутствие клеток млекопитающих, температуру, рН и время спаривания13,14, 15.
В этой работе описываются протоколы для обнаружения присутствия конъюгативных плазмид в данном штамме хозяина, для количественной оценки скорости конъюгации в твердой культуре и для перепроверки их переноса в клетки-реципиенты. Эти протоколы могут быть использованы в качестве первого шага для идентификации природных конъюгативных плазмид, пригодных для исследований. Они используют минимальное количество упрощенных шагов, поскольку они предназначены для скрининга присутствия конъюгативных плазмид в бактериях, полученных из нескольких источников (экологических, комменсальных и патогенных) в масштабе (от десятков до сотен доноров).
Кроме того, показаны тесты для определения того, является ли мобилизация данной конъюгативной плазмиды независимой от антибиотика, используемого для обнаружения (т.е. релевантность гена устойчивости к антибиотикам при отборе), и для сравнения скоростей конъюгации двух конъюгативных плазмид, обнаруженных в разных изолятах окружающей среды.
Основываясь на генетическом составе соответствующих конъюгативных плазмид (плазмидный репликон и состав гена устойчивости к антибиотикам), каждый этап протокола может быть модифицирован для изучения влияния различных факторов, которые могут повлиять на скорость конъюгации.
Общий план эксперимента:
Основными компонентами, необходимыми для проведения эксперимента по спариванию, являются донорские клетки, штамм реципиента и твердые среды для выбора доноров (антибиотик А), реципиентов (антибиотик В) и трансконъюгантов (антибиотик А и В). Трансконъюганты – это клетки-реципиенты, которые стабильно поддерживают конъюгативную плазмиду донора.
Донорские клетки устойчивы к антибиотику (антибиотик А) и чувствительны к маркеру или маркерам, используемым для отбора клеток-реципиентов (антибиотик В). Геномное расположение гена устойчивости к антибиотикам (т.е. находится ли он в хромосоме или плазмиде донорской клетки) не обязательно должно быть известно априори, поскольку мобилизация маркеров устойчивости к антибиотикам к реципиенту (после прямого контакта донора-реципиента) подразумевает, что маркеры, предоставленные донором, находились в плазмиде.
Штамм-реципиент (который, как известно, принимает конъюгативные плазмиды) должен иметь стабильный селективный маркер, отсутствующий у донора; Этот селективный маркер, как правило, устойчив к антибиотику или биоциду, расположенному в хромосоме. Выбор реципиента для использования в экспериментах по спариванию имеет решающее значение, поскольку некоторые штаммы E. coli различаются по своей способности принимать конъюгативные плазмиды16.
После того, как эти компоненты установлены, любая колония, которая растет на среде с обоими антибиотиками (А и В) после контакта пары донор-реципиент, является предполагаемым трансконъюгантом (рис. 1). Это предполагает, что доноры могут расти в среде с антибиотиком А, но не могут расти в среде с антибиотиком В, и что реципиенты могут расти в среде с антибиотиком В, но не могут расти с антибиотиком А. Трансконъюгация может быть подтверждена с помощью двух диагностических тестов. Первый тест состоит из обнаружения (с помощью полимеразной цепной реакции [ПЦР], амплификации генов или других методов) генов, обнаруженных в конъюгативной плазмиде в трансконъюгантных колониях. Второй тест предполагает использование дифференциальных цветовых маркеров колоний, основанных на метаболизме лактозы. Дифференциальный цвет колонии выявляется при использовании агара Мак-Конки; Лактоза в агаре может использоваться в качестве источника ферментации микроорганизмами, ферментирующими лактозу (LAC +). Эти микроорганизмы производят органические кислоты, особенно молочную, которые снижают рН. Нейтральный красный - это индикатор pH, включенный в среду, который превращается из грязно-белого в ярко-красный/розовый, когда pH падает ниже 6,817. Таким образом, лактозоположительные штаммы E. coli производят более крупные розовые колонии на агаре МакКонки, тогда как лактозоотрицательные штаммы производят бледно-желтые и более мелкие колонии на агаре МакКонки.
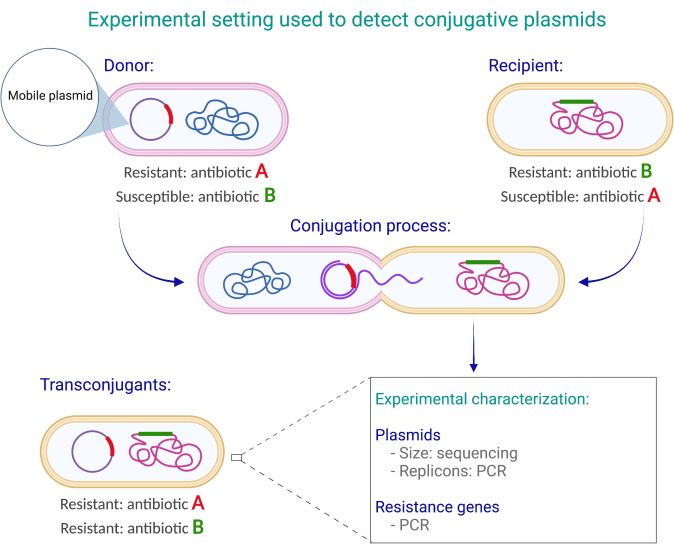
Рисунок 1: Экспериментальный дизайн, используемый для обнаружения присутствия конъюгативных плазмид в донорских штаммах. В этом примере донор несет конъюгативную плазмиду с геном устойчивости к антибиотикам, который придает устойчивость к антибиотику А, но они восприимчивы к антибиотику В. И наоборот, реципиент имеет детерминанту хромосомной резистентности, которая обеспечивает защиту от антибиотика В, но он чувствителен к антибиотику А. Трансконъюганты устойчивы к обоим антибиотикам (А и В), потому что у них есть конъюгативная плазмида донора, которая придает устойчивость к антибиотику А, и хромосома реципиента, которая обеспечивает защиту от антибиотика В. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Коэффициент конъюгации для пары донор-реципиент (в данных экспериментальных условиях) может быть рассчитан путем деления числа трансконъюгантов на количество доноров или на количество реципиентов; Первый показатель указывает на долю донорских клеток, демонстрирующих функциональную экспрессию механизма конъюгации донором16,18, а второй показатель указывает на способность реципиента принимать конъюгативные плазмиды 19,20. В этом исследовании, если не указано иное, скорость конъюгации представляет собой долю клеток-реципиентов, которые становятся трансконъюгантными (т.е. скорость на реципиента).
Здесь сообщается о двух независимых экспериментах по спариванию с участием одного реципиента кишечной палочки и двух доноров кишечной палочки. Кроме того, различные антибиотики были использованы для выбора трансконъюгантов для одного из доноров, чтобы подтвердить, что одна плазмида с множественной лекарственной устойчивостью может быть выбрана с любым из генов устойчивости к антибиотикам, обнаруженных в конъюгативной плазмиде.
Донорские и реципиентные штаммы, используемые в этой работе, были полностью секвенированы, чтобы понять все компоненты этой экспериментальной системы; Однако эти протоколы были разработаны для скрининга присутствия конъюгативных плазмид у хозяев неизвестной последовательности и могут использоваться и в этом экспериментальном контексте; Однако в этом случае соответствующие гены секвенируются в первую очередь.
Донорские и реципиентные штаммы, используемые в протоколе, следующие:
Донор 1. Кишечная палочка SW4955 был собран в озере в Батон-Руж (Лос-Анджелес, США). Он имеет конъюгативную плазмиду 134 797.н. (p134797) с репликонами IncFIC (FII) и IncFIB (AP001918). Эта конъюгативная плазмида имеет гены, которые придают устойчивость к цефалоспоринам третьего поколения (blaCTX-M-55), аминогликозидам (aac (3) -IIa и aadA1), фениколам (catA2), тетрациклинам (tet (A)), триметоприму (dfrA14) и сульфаниламидам (sul3). Полную карту p134797 см. на рисунке 2A. Кишечная палочка SW4955 является лактозоположительным, образуя розовые колонии на агаре Макконки.
Донор 2. Кишечная палочка SW7037 был собран в озере Эри (округ Оттава, штат Огайо, США). Он несет конъюгативную плазмиду 101 718.н. (p101718) с репликоном IncI1-I (Alpha). Эта конъюгативная плазмида имеет ген, который придает устойчивость к бета-лактамам (blaCMY-2). Полную карту p101718 см. на рисунке 2B. Кишечная палочка SW7037 также является лактозоположительным, образуя розовые колонии на агаре Макконки.
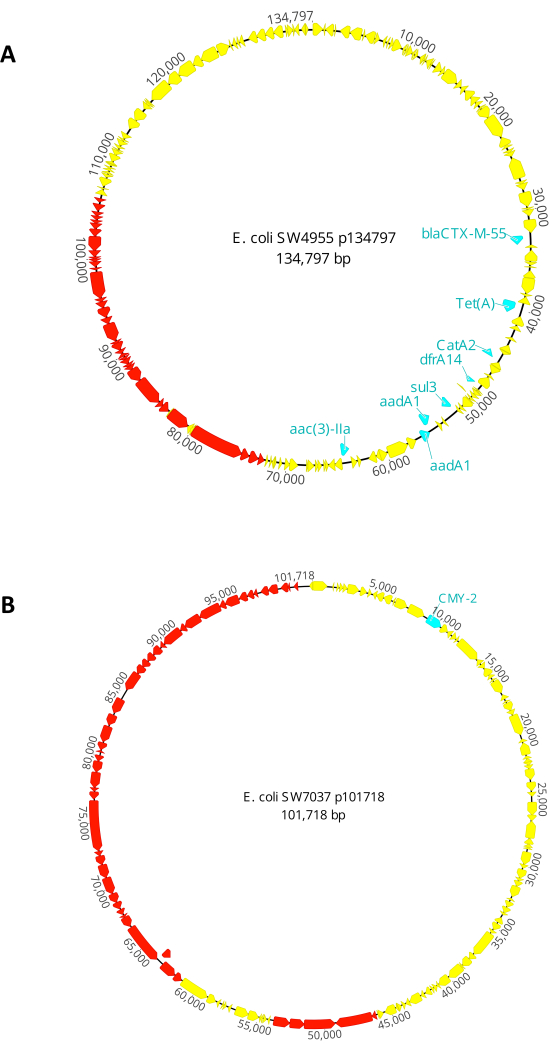
Рисунок 2: Генетическая карта конъюгативных плазмид, использованных в этом исследовании. (A) Плазмида p134797, конъюгативная плазмида, обнаруженная в штамме E. coli SW4955. (B) Плазмида p101718, конъюгативная плазмида, обнаруженная в штамме E. coli SW7037. Гены антибиотикорезистентности выделены синим цветом, а гены, относящиеся к конъюгативному аппарату, — красным. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Получатель. Кишечная палочка В качестве получателя используется LMB100. Это бесплазмидный штамм, устойчивый к рифампицину (100 мг/л) и стрептомицину (100 мг/л). Наличие резистентности к двум антибиотикам снижает вероятность возникновения мутаций резистентности у донора, которые могут помешать интерпретации результатов. Кроме того, E. coli LMB100 является лактозоотрицательным и может быть отличим от двух донорских штаммов, потому что он производит бледно-желтые и маленькие колонии (в отличие от более крупных розовых колоний) на агаре Макконки.
Если донор является лактозоотрицательным, мы рекомендуем использовать лактозо-положительного реципиента (например, E. coli J53). Штаммы LMB100 и J53 доступны для использования в других лабораториях. Отправьте запрос доктору Херардо Кортес-Кортесу вместе с адресом и номером FedEx.
Твердой средой, необходимой для отбора и подсчета доноров, реципиентов и трансконъюгантов, является агар Мак-Конки в чашках Петри диаметром 100 мм. Необходимо добавление следующих антибиотиков: (i) Носитель А: карбенициллин (100 мг/л) для подсчета доноров и обеспечения того, чтобы реципиенты не могли расти с этим антибиотиком. (ii) Носитель B: рифампицин (100 мг/л) + стрептомицин (100 мг/л) для подсчета реципиентов и обеспечения того, чтобы доноры не могли расти в этих двух антибиотиках. iii) Среда АВ: карбенициллин (100 мг/л) + рифампицин (100 мг/л) + стрептомицин (100 мг/л) для получения и подсчета трансконъюгантов. (iv) Носитель С: отсутствие антибиотиков для полосатости всех изученных изолятов.
Сравниваются скорости конъюгации конъюгативных плазмид от E. coli SW4955 и E. coli SW7037 до E. coli LMB100. Кроме того, в случае конъюгативной плазмиды p134797 (штамм SW4955) антибиотик карбенициллин (100 мг/л) заменяют гентамицином (2 мг/л), хлорамфениколом (25 мг/л), тетрациклином (10 мг/л), триметопримом (20 мг/л) или сульфаметоксазолом (100 мг/л) в последующих экспериментах, чтобы установить, оказывает ли маркер устойчивости к антибиотикам, используемый для отбора, какое-либо влияние на результаты.
протокол
1. Способ 1: Спряжение
- День 1: Проведите полосу доноров и реципиента. Полосу отдельно от запасов глицерина на среде C (агар Макконки без антибиотиков) и инкубацию в течение ночи при 37 °C.
ПРИМЕЧАНИЕ: Этот шаг необходим для того, чтобы убедиться, что эксперимент проводится с чистыми изолятами и подтвердить фенотип лактозы по цвету колоний. - День 2: Пометьте пробирку для культивирования объемом 14,0 мл для каждого донора и реципиента. Выберите по одной колонии каждого донора и реципиента и выращивайте их в течение ночи (18 часов) в отдельных культуральных пробирках объемом 14,0 мл, содержащих 2 мл бульона Мюллера Хинтона при 37 ° C и встряхивающих при 200 об/мин.
ПРИМЕЧАНИЕ: В используемых штаммах стационарная фаза достигается после ночного культивирования в течение 18 часов. - День 3: Измерьте оптическую плотность при 600 нм (OD600) ночной культуры каждого донора и реципиента (без вихря) с помощью разведения 1:10 900 мкл физиологического раствора и 100 мкл ночной культуры.
- Отрегулируйте оптическую плотность каждого донора и реципиента до 2,0 (OD600 = 2,0) стерилизованным физиологическим раствором (0,85% NaCl в воде).
ПРИМЕЧАНИЕ: Ночная культура E. coli с OD600 = 2,0 имеет 1,6 x 109 КОЕ / мл. - Маркируйте микроцентрифужную пробирку объемом 1,5 мл «сопрягательной пробиркой» с указанием донорского и реципиентного штаммов. Перенесите 500 мкл скорректированной (OD600 = 2,0) суспензии каждого донора и реципиента и поместите их в сопрягаемую трубку (эта сопрягаемая трубка будет иметь 0,8 x 109 КОЕ/мл каждого донора и реципиента). Аккуратно перемешайте сопрягаемую трубку путем инверсии.
- Центрифугируйте сопрягаемую трубку в течение 10 мин при 500 x g при комнатной температуре.
- Не нарушая гранулы, пипеткой вынимают 800 мкл конъюгационной трубки. В конъюгационной трубке должно остаться 200 мкл.
ПРИМЕЧАНИЕ: Выбросьте надосадочную жидкость в контейнер с 10% отбеливателем, чтобы инактивировать бактерии в суспензии. - Инкубируйте брачную трубку в течение 18 ч (ночь) при 37 °C в инкубаторе. Спаривание происходит во время инкубации.
ПРИМЕЧАНИЕ: Этот шаг необходимо выполнять без встряхивания, чтобы не разорвать конъюгативные пили. - В качестве отрицательного контроля проведите ночную культуру доноров на среде B и реципиентов на среде A. Инкубируйте планшеты в течение ночи при 37 ° C
- День 4: Добавьте 800 мкл физиологического раствора в сопрягаемую трубку и встряхните для ресуспендирования (это восстанавливает спаривающую смесь до 1 мл).
ПРИМЕЧАНИЕ: Вихревой распад разбивает спаривающиеся бактерии на части и гомогенизирует культуру для количественного определения КОЕ / мл. - Приготовьте разведения 1:10 (от 1 x 100 до 1 x 10-7) смеси для спаривания. Планшет 100 мкл разведений от 10-5 до 10-7 на средах A и B, а также все разведения на средах AB.
ПРИМЕЧАНИЕ: Dlution 100 относится к аккуратной трубке. - Дайте тарелкам высохнуть, прежде чем помещать их в инкубатор вверх дном. Инкубируйте пластины в течение 18 ч (на ночь) при 37 °C.
- День 5: Проверьте отрицательный контроль, чтобы убедиться, что полосы чистых ночных культур доноров не росли на носителе B, а чистая ночная культура реципиентов не росла на среде A.
- Запишите количество колоний и разведений, которые можно подсчитать:
- Подсчитайте колонии в медиа А; Это доноры. Колонии должны быть розового цвета (рис. 3А, Б).
- Подсчитайте колонии в медиа B; Это реципиенты и трансконъюганты. Колонии должны быть бледно-желтыми (рис. 3В).
- Подсчитайте колонии в медиа АВ; Это трансконъюганты. Колонии должны быть бледно-желтыми.
ПРИМЕЧАНИЕ: Выберите счетную табличку. Счетная табличка содержит от 30 до 300 колоний (более 300 колоний было бы трудно подсчитать, а менее 30 колоний считаются слишком маленьким размером выборки, чтобы представить точное представление исходного образца).
- Рассчитайте частоту конъюгации на донора или реципиента
Частота конъюгации на одного донора = (КОЕ/мл трансконъюганта [среда AB])/ (КОЕ/мл доноров [среда А]) x 100
Частота конъюгации на одного реципиента = (КОЕ/мл трансконъюганта [среда AB])/ (КОЕ/мл реципиентов и трансконъюгантов [среда B]) x 100
ПРИМЕЧАНИЕ: Частота сопряжения для этого протокола рассчитывалась как трансконъюганты, деленные на число реципиентов, умноженное на 100. Согласно литературе, результирующее количество конъюгации может быть названо частотой эксконъюганта, частотой переноса генов, частотой конъюгации, выходом рекомбинанта, эффективностью переноса плазмиды, частотой конъюгации на основе общего количества бактерий, доли трансконъюгантов, доли трансконъюгантов в популяции реципиентов, частоты трансконъюгантов, частоты конъюгации, логарифма скорости конъюгации, константы скорости передачи, скорости конъюгации на брачную пару, коэффициент сопряжения, или эффективность сопряжения20. Этот протокол относится к термину эффективность сопряжения. - Храните трансконъюганты в глицериновых запасах при температуре -80 °C. Следуйте подэтапам приготовления глицериновых бульонов.
- Выберите одну колонию трансконъюгантов и выращивайте их в течение ночи (18 часов) в культуральных пробирках объемом 5,0 мл, содержащих 2 мл бульона Мюллера Хинтона, дополненного карбенициллином (100 мг / л), при 37 ° C и встряхивании при 200 об/мин.
- Маркируют криогенные флаконы с указанием названия трансконъюганта следующим образом: Tc + имя донора + антибиотик отбора в среде А (поскольку они являются трансконъюгантами, известно, что их фоном является штамм-реципиент, который уже устойчив к стрептомицину и рифампицину, но дополнительно содержит плазмиду, несущую ген бета-лактамной резистентности); например, TcU1Carb. Добавьте непрерывные числа на случай, если необходимо сохранить более одного трансконъюганта от одного и того же донора (например, TcU1Carb1, TcU1Carb2 и т. Д.).
- Перенесите 1 мл ночной культуры в 1 мл 50% глицерина (v/v; конечная концентрация глицерина должна быть 25%) и осторожно перемешайте путем инверсии. Поместите криогенные флаконы на сухой лед на 15 минут и храните криовиалы при -80 ° C для будущих экспериментов.
- Для экстракции ДНК транснконъюганты из запасов глицерина наносят на агар Мюллера Хинтона с добавлением карбенициллина (100 мг/л) и инкубируют в течение ночи при 37 ° C; Затем следуйте рекомендациям из шага 2.1.
2. Метод 2: Полимеразная цепная реакция (ПЦР) для амплификации генов устойчивости к антибиотикам и репликонов плазмиды в трансконъюгантах E. coli
ПРИМЕЧАНИЕ: Полимеразная цепная реакция (ПЦР) была разработана доктором Кэри Маллисом в 1983 году. ПЦР зависит от специфических праймеров (короткий фрагмент ДНК, комплементарный данной последовательности ДНК, который действует как точка, в которой может протекать репликация, обычно длиной 20-40 нуклеотидов и в идеале с содержанием гуанина-цитозина 40-60%), которые отожжены на противоположные нити денатурированной двухцепочечной матрицы ДНК и расширены через термостабильную ДНК-полимеразу, Таким образом, генерируется дополнительный шаблон для следующего цикла реакций, что приводит к экспоненциальному усилению исходного шаблона21. В этом протоколе репликоны и гены резистентности, присутствующие в конъюгативных плазмидах, были амплифицированы для подтверждения переноса в трансконъюгантных клетках-реципиентах.
- Экстракция ДНК
- Чтобы обнаружить перенос генов резистентности, переносимых конъюгативными плазмидами, используйте трансконъюгантную ДНК в качестве матрицы. Используйте простую экстракцию для подготовки к фурункулу для лизиса клеточных стенок бактерий.
ПРИМЕЧАНИЕ: Простая экстракция при подготовке к фурункулу - это простой подход к лизиру клеточных стенок бактерий. Эта экстракция содержит плазмидную ДНК, смешанную с геномной ДНК, но, поскольку праймеры разработаны в соответствии с конкретными последовательностями ДНК, представляющими интерес, этот шаблон также полезен для ПЦР. Плазмиды также могут быть специально очищены, хотя выход имеет тенденцию падать с увеличением размера плазмиды22. Это удобный остановочный пункт. ДНК может храниться в течение нескольких месяцев при -20 °C.
- Чтобы обнаружить перенос генов резистентности, переносимых конъюгативными плазмидами, используйте трансконъюгантную ДНК в качестве матрицы. Используйте простую экстракцию для подготовки к фурункулу для лизиса клеточных стенок бактерий.
- ПЦР
- Учитывая, что эксперимент имеет отрицательный и положительный контроль, полезно создать пул для всех реакций в пробирке объемом 1,5 мл. Пометьте пробирку объемом 1,5 мл как «пул», а необходимые пробирки для ПЦР — с названием гена и образца (например, OXA-U1).
- Пипеткой нанесите реагенты ПЦР в следующем порядке в пробирку объемом 1,5 мл: стерильная вода, 2x Master Mix, праймеры и полимераза (кроме матричной ДНК) (см. Таблицу 1). Аккуратно перемешайте, пипеткой вверх и вниз не менее 10 раз. Держите на льду все время.
ПРИМЕЧАНИЕ: Надевайте перчатки, чтобы избежать загрязнения реакционной смеси или реагентов. Старайтесь не открывать и не смешивать реагенты и не обращаться с образцами в одной и той же зоне, чтобы предотвратить загрязнение реагентами. Поместите реагенты в ведро со льдом, чтобы подавить активность нуклеаз и неспецифический прайминг. Дайте им полностью оттаять, прежде чем запускать реакцию. Держите реагенты на льду на протяжении всего эксперимента. Taq полимераза добавляется в конце, потому что она чувствительна к изменениям pH; Он должен быть буферизован, чтобы избежать деградации или неправильного складывания. Последовательность праймеров указана в Таблице 2 - гены антибиотикорезистентности - и Таблица 3 - репликоны 23,24,25,26,27,28. - Добавьте матричную ДНК в соответствующую пробирку. Избегайте появления пузырьков и закрепляйте колпачки на пробирках для ПЦР.
- Поместите пробирки для ПЦР в термоциклер.
- Запустите программу. Обратитесь к настройкам программы, перечисленным для каждого гена в Таблице 2 (гены резистентности) и Таблице 3 (репликоны).
ПРИМЕЧАНИЕ: Установите программы ПЦР для удержания образцов при температуре 4 ° C после прогона.- Условия ПЦР для репликонов: один цикл денатурации при 94 °C в течение 5 мин, затем 30 циклов денатурации при 94 °C в течение 1 мин, отжиг при 60 °C в течение 30 с, удлинение при 72 °C в течение 1 мин и окончательное продление одного цикла при 72 °C в течение 5 мин.
ПРИМЕЧАНИЕ: Это условия, стандартизированные Carattoli et al.29.
- Условия ПЦР для репликонов: один цикл денатурации при 94 °C в течение 5 мин, затем 30 циклов денатурации при 94 °C в течение 1 мин, отжиг при 60 °C в течение 30 с, удлинение при 72 °C в течение 1 мин и окончательное продление одного цикла при 72 °C в течение 5 мин.
- После завершения программы храните пробирки для ПЦР при температуре 4 °C.
ПРИМЕЧАНИЕ: Это удобная остановка. ПЦР-продукты могут храниться в течение нескольких месяцев при температуре -20 °C - Приготовьте 1% агарозный гель, взвесив 0,6 г агарозы в колбе объемом 250 мл и добавив 60 мл 1x буфера трис-ацетат-ЭДТА (TAE) (отрегулируйте реагенты, если требуется другой размер геля). Осторожно и медленно растопите агарозу в микроволновой печи, чтобы агароза не пролилась на колбу, и дайте ей остыть примерно до 55 ° C (10-15 мин).
- Приготовьте все реагенты с использованием сверхчистой деионизированной воды и реагентов аналитического класса:
- Буфер TAE 50x (основание Tris, уксусная кислота и ЭДТА) (1 л): смешайте 121,1 г основания Tris + 372,24 г ЭДТА и добавьте 500 мл дистиллированной воды. Растворите с помощью магнитной мешалки. Добавьте 57,1 мл уксусной кислоты и добавьте дистиллированную воду до общего объема 1000 мл.
- Автоклав при давлении 15 фунтов на квадратный дюйм, 121 °C в течение 15 минут и хранить при комнатной температуре до готовности до 6 месяцев.
- Буфер TAE 1x (1 л): Смешайте 20 мл буфера TAE 50x с 980 мл дистиллированной воды и перемешайте.
- Под вытяжным шкафом добавьте 6 мкл SYBR Green в расплавленную агарозу, перемешайте и вылейте в лоток (и расческу), предварительно заклеенный клейкой лентой, чтобы избежать просыпания. Дайте гелю застыть в течение 15-25 минут до появления помутнения.
ПРИМЕЧАНИЕ: Также доступны другие альтернативные красители30,31,32,33. - Снимите клейкую ленту и поместите гель в камеру электрофореза, добавив достаточное количество 1x буфера TAE, чтобы покрыть гель.
- Смешайте 5 мкл 6-кратного ДНК-гелевого загрузочного красителя с 25 мкл каждой реакции. Аккуратно перемешайте, пипеткой вверх и вниз не менее 10 раз.
ПРИМЕЧАНИЕ: Не весь продукт ПЦР необходимо загружать в гель, чтобы визуализировать ожидаемый продукт (отрегулируйте количество красителя в соответствии с требованиями). Оставшийся образец ПЦР можно сохранить и хранить при температуре -20 °C в течение нескольких месяцев. - Загрузите смесь в лунки (избегайте образования пузырьков) и опустите крышку камеры.
ПРИМЕЧАНИЕ: Загрузите первый образец во вторую скважину (зарезервируйте первую на лестнице), начиная с отрицательного контроля. - Загрузите 4 мкл 1 кб ДНК-лестницы в первую скважину.
- Запустите электрофорез при напряжении 120 В, 400 мА и 60 минут.
- Визуализируйте гель под ультрафиолетовым светом (с помощью УФ-осветителя) и запишите изображение.
ПРИМЕЧАНИЕ: Если присутствует продукт ПЦР, окрашенные полосы ДНК можно обнаружить с помощью стандартного УФ-трансиллюминатора, трансиллюминатора видимого света или лазерного сканера.
| Реагент | Стоковое решение | Объем, добавленный к реакции 50 мкл (1x) | Последний | Пример: объем | Пример: объем | Пример: объем, добавленный в каждую пробирку Final Vol. 50 мкл | Добавлена громкость к положительному контролю | Громкость, добавленная к отрицательному контролю |
| Концентрация | Добавлено в 1x | Добавлено в 3x (пул) | ||||||
| Стерильная вода | - | 21,5 мкл (от q.s. до 50 мкл) | - | 21,5 мкл | 64,5 мкл | 49 мкл/тюбик | 49 мкл/тюбик | 49 мкл/тюбик |
| Мастер-микс | 2x | 25 мкл | 1x | 25 мкл | 75 мкл | |||
| Передний праймер | 25 мкМ | 1 мкл | 0,5 мкМ | 1 мкл | 3 мкл | |||
| Обратная грунтовка | 25 мкМ | 1 мкл | 0,5 мкМ | 1 мкл | 3 мкл | |||
| Шаблон ДНК | Переменная (100–200 нг/мкл) | Переменная (1 мкл) | Переменная | 0,5 мкл | 1,5 мкл | |||
| Полимераза | 5 единиц/мкл | 0,5 мкл | 2.5 Единицы измерения | - | - | 1 мкл (трансконъюгантный) | 1 мкл (донор) | 1 мкл (реципиент) |
| ПРИМЕЧАНИЕ: q.s. - это латинская аббревиатура от quantum satis, означающая необходимую сумму. | ||||||||
Таблица 1: ПЦР-реагенты и пул для трех реакций (пример).
| Грунтовки (последовательность указана в ориентации 5' - 3') | Программа ПЦР | Ожидаемый размер |
| (БП) См. | ||
| blaCTX-M группа 1 | 94 oC 7 мин | (864) 23 См. |
| CTX-M: GGTTAAAAAATCACTGCGYC | 94 oC 50 с (35 циклов) | |
| CTX-M: TTGGTGACGATTTTAGCCGC | 50 oC 40 с | |
| 68 oC 1 мин | ||
| 68 oC 5 мин | ||
| блаСМО-2 | 95 oC 3 мин | (1855) 24 См. |
| CMY-2-F: GATTCCTTGGACTCTTCAG | 95 °C 30 с (30 циклов) | |
| CMY-2-R: TAAAACCAGGTTCCCAGATAGC | 53 oC 30 с | |
| 72 oC 30 с | ||
| 72 oC 3 мин | ||
| aac(3')-II | 94 oC 5 мин | (237) 25 См. |
| aac(3')-ii-f: actgtgatgggatacgcgtc | 94 °C 30 с (32 цикла) | |
| aac(3')-ii-r: ctccgtcagcgtttcagcta | 60 oC 45 с | |
| 72 oC 2 мин | ||
| 72 oC 8 мин | ||
| aadA | 94 oC 5 мин | (283) 26 См. |
| aadA1: GCAGCGCAATGACATTCTTG | 94 oC 1 мин (35 циклов) | |
| aadA2: ATCCTTCGGCGCGATTTTG | 60 oC 1 мин | |
| 72 oC 1 мин | ||
| 72 oC 8 мин | ||
| СУЛ-3 | 94 oC 5 мин | (799) 27 См. |
| sul-3-F: GAGCAAGATTTTTTGGAATCG | 94 oC 1 мин (30 циклов) | |
| sul-3-R: CATCTGCAGCTAACCTAGGGCTTTGGA | 51 oC 1 мин | |
| 72 oC 1 мин | ||
| 72 oC 5 мин | ||
| тет(А) | 95 oC 5 мин | (957) 28 См. |
| TETA-1: GTAATTGAGCACTGTCGC | 95 °C 30 с (23 цикла) | |
| ТЭТА-2: CTGCCTGGACAACATTGCTT | 62 oC 30 с | |
| 72 oC 45 с | ||
| 72 oC 7 мин | ||
| DFR A | 95 oC 5 мин | (302) Эта работа |
| dfrA-F: CATACCCTGGTCCGCGAAAG | 95 oC 1 мин (30 циклов) | |
| 55 oC 1 мин | ||
| dfrA-R: CGATGTCGATCGTCGATAAGTG | 72 oC 1 мин | |
| 72 oC 7 мин | ||
| catA2 | 95 oC 5 мин | |
| catA2-F: GACCCGGTCTTTACTGTCTTTC | 95 oC 1 мин (25 циклов) | (225) Эта работа |
| catA2-R: TCCGGTGATATTCAGATTAAAT | 60 oC 1 мин | |
| 72 oC 1 мин | ||
| 72 oC 7 мин |
Таблица 2: Праймеры и программы ПЦР, используемые для амплификации генов диагностической резистентности.
| Репликон | Грунтовка (последовательность указана в ориентации 5' - 3') | Цель | Программа ПЦР | Ожидаемый размер (б..) | |||
| ИнкФИБ | F: TCTGTTTTTCTTTTACTGTCCAC | repA | 94 oC 5 мин | 683 | |||
| R: CTCCCGTCGCTTCAGGGCATT | 94 oC 1 мин (30 циклов) | ||||||
| 60 oC 30 с | |||||||
| IncFIC | F: GTGAACTGGCAGATGAGGAAGG | repA2 | 72 oC 1 мин | 262 | |||
| R: TTCTCCTCGTCGCCAAACTAGAT | 72 oC 5 мин | ||||||
| IncI1 | F: CGAAAGCCGGACGGCAGAA | РНАИ | 139 | ||||
| R: TCGTCGTTCCGCCAAGTTCGT | |||||||
Таблица 3: Праймеры и программа ПЦР, используемые для классификации плазмид p134797 и p101718 методом репликонного типирования на основе ПЦР29.
Результаты
Учитывая, что доноры SW4955 и SW7037 были секвенированы, ожидается, что эти два донорских штамма будут иметь фенотипы резистентности, соответствующие профилю гена резистентности, идентифицированному в их геномной последовательности. Плазмида p134797 (из SW4955) имеет гены, которые придают устойчивость к цефалоспоринам третьего поколения (blaCTX-M-55) и устойчивость к аминогликозидам (aac (3) -IIa и aadA1), фениколам (catA2), тетрациклинам (tet (A)), триметоприму (dfrA14) и сульфаниламидам (sul3); гены устойчивости к антибиотикам не были обнаружены в хромосоме SW4955. Плазмида p101718 (из SW7037) несет только один ген устойчивости к антибиотикам (bla CMY-2), который, как ожидается, придаст устойчивость к цефалоспоринам третьего поколения (blaCTX-M-55). Опять же, в хромосоме SW7037 не было обнаружено генов устойчивости к антибиотикам.
После спаривания ожидалось обнаружение переноса двух конъюгативных плазмид, несущих все упомянутые выше гены резистентности. Обнаружение положительной конъюгации подразумевает, что реципиенты, идентифицированные как трансконъюганты, должны были приобрести конъюгативные плазмиды. Также ожидалось наличие генов диагностической резистентности для конъюгативных плазмид в трансконъюгантах (обнаруженных с помощью ПЦР).
Чтобы проиллюстрировать описанные здесь методы, была проверена способность двух экологических изолятов E. coli переносить плазмидную ДНК путем конъюгации. Схематическое изображение экспериментальной установки показано на рисунке 1. Два донора (E. coli SW4955 и SW7037) и один реципиент (E. coli LMB100) были спарены независимо друг от друга. Карта генов конъюгативных плазмид, обнаруженных у E. coli SW4955 (p134797) и SW7037 (p101718), показана на рисунке 2.
Конъюгативные плазмиды были отобраны с карбенициллином и встречно отобраны с использованием рифампицина и стрептомицина, детерминанты резистентности которых находятся в хромосоме реципиента. Агар Макконки использовали, чтобы отличить лактозоположительных доноров (которые продуцируют большие розовые колонии) от реципиента и трансконъюгантов (которые являются лактозоотрицательными и производят меньшие бледно-желтые колонии) (рис. 3).
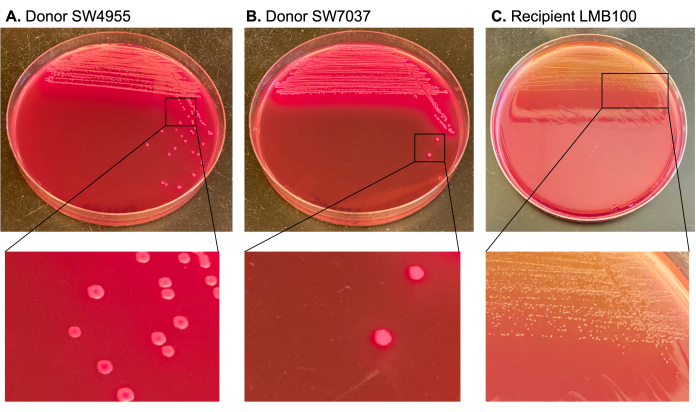
Рисунок 3: Иллюстрация дифференциальных цветовых маркеров для колоний донора и реципиента на агаре МакКонки. Колонии, соответствующие донорам, имеют розовый цвет на агаре Макконки, потому что они лактозоположительные. Это отличает колонии донора от колоний-реципиентов, которые бледно-желтые и меньше (лактозоотрицательные). Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Была обнаружена мобилизация конъюгативной плазмиды p134797, при этом каждый из пяти антибиотиков соответствовал пяти различным классам генов резистентности, обнаруженных в плазмиде.
Приведен пример расчета эффективности сопряжения (CE) для деформации SW4955. Из анализа со штаммом SW4955 в планшете от разведения 10-2 было насчитано 172 КОЕ трансконъюгантов; количество реципиентов из соответствующего разведения (10-2) составило 10 300 000 КОЕ/мл (табл. 4).
CE рассчитывается следующим образом:
CE = (174 КОЕ/мл)/(10 300 000 КОЕ/мл)
CE = 1,67 x 10-5 трансконъюгантов / реципиент
| ЛМБ100 | Трансконъюганты из штамма SW4955, отобранные с карбелициллином | Эффективность сопряжения | ||
| Разбавление | КОЕ (счетная пластина) | Приблизительно КОЕ/мл | КОЕ (счетная пластина) | |
| 100 | приток | 1.03E+09 | ||
| 10-1 | приток | 1.03E+08 | ||
| 10-2 | приток | 10300000 | 172 | 1,67 x 10-5 трансконъюгантов/реципиент |
| 10-3 | приток | 1030000 | ||
| 10-4 | приток | 103000 | ||
| 10-5 | приток | 10300 | ||
| 10-6 | приток | 1030 | ||
| 10-7 | 103 | 103 | ||
| Значения, используемые для расчета CE, выделены жирным шрифтом. | ||||
Таблица 4: Пример расчета эффективности сопряжения (CE) для штамма SW4955.
Результаты приведены в таблице 5, выраженные как эффективность сопряжения на одного реципиента. Пять показателей эффективности конъюгации, полученных с использованием штамма SW4955 в качестве донора, находились в пределах одного порядка величины. Эти результаты указывают на то, что мобилизация конъюгативной плазмиды может быть обнаружена независимо от отбора, используемого для трансконъюгантной идентификации.
Используя штамм SW7037 в качестве донора, полученная эффективность конъюгации была на три порядка ниже; Эти результаты позволяют сравнивать эффективность конъюгации разных доноров и типов плазмид с одними и теми же реципиентами.
| Эффективность сопряжения | |||||
| Напряжение | Карбенициллин (100 мг/л) | Гентамицин (2 мг/л) | Хлорамфеникол (25 мг/л) | Тетрациклин (10 мг/л) | Триметоприм (20 мг/л) |
| SW4955 | 1,67 х 10-5 | 5,67 х 10-5 | 2,17 х 10-5 | 7,62 х 10-5 | 1,36 х 10-5 |
| SW7037 | 2,14 х 10-6 | ||||
Таблица 5: Эффективность конъюгации донорских штаммов E. coli SW4955 и SW7037 в зависимости от антибиотика, используемого для отбора.
У трансконъюгантов с помощью ПЦР проверяли наличие репликонов и всех генов резистентности, кодируемых в двух тестируемых конъюгативных плазмидах, и соответствующих им репликонов. Условия, используемые для этих диагностических реакций ПЦР, показаны в таблице 3.
Диагностические гели показаны на рисунке 4. Эти гели подтверждают наличие ожидаемых репликонов в трансконъюгантах (IncFIC и IncFIB в p1347975 и IncI1 в p101718). Они также подтверждают наличие ожидаемых генов устойчивости к антибиотикам, а именно группы bla CTX-M-55 (бета-лактам), aac (3) -II и aadA (аминогликозид), catA2 (феникол), tet (A) (тетрациклин), dfrA14 (триметоприм) и sul3 (сульфонамид) для p1347975 и bla CMY-2 для p101718 (рис. 4).
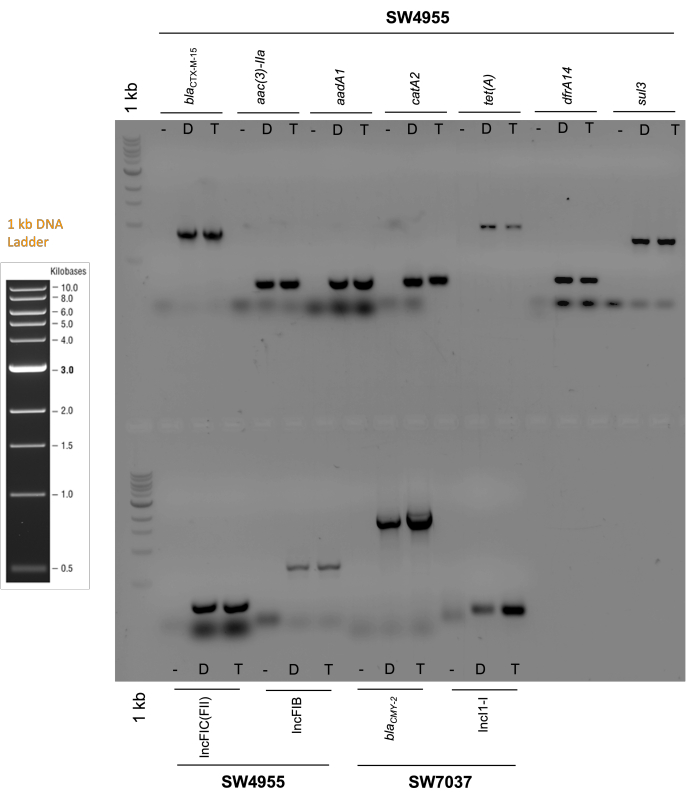
Рисунок 4: Диагностические гели для электрофореза. Гель-электрофорез ПЦР-продуктов генов антибиотикорезистентности и плазмидных репликонов, обнаруженных в конъюгативных плазмидах р134797 и р101718 в донорских клетках (штаммы SW4955 и SW7037 соответственно) и в соответствующих трансконъюгантах LMB100. Карбенициллин использовали для селекции плазмид. Сокращения. -: отрицательный контроль (в качестве отрицательного контроля использовалась ДНК штамма LMB100); D: донор; Т: трансконъюгантный. Ожидаемые размеры ампликона: blaCTX-M-55: 864 пб; aac(3)-IIa: 237.н.; aadA1: 283.н.; catA2 : 225.н.; tet(A): 957.н.; dfrA14: 302.н.; sul3: 799.н.; IncFIC(FII): 262 б..; IncFIB: 683.н.; blaCMY-2: 1,855 б..; IncI1-I: 139.н. В геле 1% агарозы. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Обсуждение
Конъюгативные плазмиды обеспечивают доступ к общему пулу генов в определенных условиях окружающей среды посредством рекомбинации и горизонтального переноса генов34. Таким образом, конъюгативные плазмиды являются эволюционными образованиями, способными приобретать и передавать функции, которые позволяют бактериям адаптироваться к множеству условий (включая устойчивость к антибиотикам, устойчивость к металлам, приобретение металлов, образование биопленки и патогенные гены, среди прочего) в течение временной шкалы часов.
В данной работе представлен протокол идентификации конъюгативных плазмид у бактерий. Для того, чтобы протокол работал, используемые маркеры должны дифференцировать донорские и реципиентные штаммы, как показано контрольной группой в средах А и В. Им также необходимо эффективно отбирать клетки, несущие плазмиду. Реакция спаривания имеет решающее значение. В этой реакции донорам и реципиентам необходимо установить длительный контакт (через пили) для конъюгации. Все, что может нарушить межклеточный контакт, например, недостаточное время инкубации или встряхивание или перемешивание культуры, таким образом, снижает эффективность конъюгации. Выбор реципиента также имеет решающее значение, так как некоторые штаммы-реципиенты рефрактерны к конъюгации35,36. В качестве реципиента предлагается LMB100, так как он способен принимать плазмиды нескольких типов несовместимости.
Скорость конъюгации специфична для каждой пары хромосом плазмиды-донора, реципиента и условий окружающей среды. Было обнаружено, что конъюгация специфических плазмид чувствительна к большому количеству переменных, включая фазу роста, плотность клеток, отношение донора к реципиенту, проводится ли конъюгация в жидких или твердых средах, углерод, кислород, соли желчных кислот, концентрации металлов, присутствие клеток млекопитающих, температуру, рН и время спаривания13,14,15 . Изучение этих взаимодействий зависит от первоначального обнаружения конъюгативной плазмиды, подлежащей углубленному изучению. Таким образом, описанный здесь протокол также может быть изменен для изучения влияния различных экспериментальных переменных, хотя это происходит за счет ограничения числа проверенных доноров. Он также может идентифицировать мобилизуемые плазмиды в хозяевах, у которых есть вспомогательные плазмиды (т.е. плазмиды, которые обеспечивают конъюгацию, обеспечивая функции, отсутствующие у мобилизуемых плазмид в транс-6).
Рекомендуется знать последовательность конъюгативной плазмиды (но не обязательно для обнаружения конъюгации, как обсуждалось выше). Когда доноры являются лактозоотрицательными (продуцируя желтые колонии на агаре Макконки), лактоз-положительный реципиент (продуцирующий розовые колонии на агаре Макконки) может быть использован для отличия истинных трансконъюгантов от донорских клеток, которые способны расти на среде для выбора трансконъюгантов. Описанный здесь протокол предназначен для обнаружения конъюгативных плазмид из экологических, комменсальных и патогенных членов семейства Enterobacteriaceae; Тем не менее, его можно использовать с любыми видами бактерий с подходящим донором, реципиентом, антибиотиком (антибиотиками) и цветовыми маркерами. Идентификация этих критических компонентов в других бактериях требует систематических исследований с использованием нескольких доноров, реципиентов и маркеров (антибиотиков и красителей). Этот протокол не был протестирован на грамположительных бактериях.
В литературе сообщалось о нескольких вариантах метода, представленных здесь, недавно рассмотренных20. Качественный результат также может быть обозначен по-разному (например, частота эксконъюганта и частота переноса генов), а безразмерные единицы могут использоваться для сообщения об эффективности конъюгации (мл/КОЕ x h)20.
Описанный здесь протокол решает несколько ограничений, которые ранее не рассматривались существующими методами 16,18,19,20. Во-первых, был определен подходящий реципиент. Во-вторых, использование двух антибиотиков (рифампицина и стрептомицина) для выбора истинных трансконъюгантов сводит к минимуму вероятность того, что у доноров развивается устойчивость к одному из антибиотиков, используемых для отбора трансконъюгантов, посредством спонтанного мутагенеза. Ложные трансконъюганты также могут быть результатом защиты свидетелей путем гидролиза антибиотика, используемого для отбора трансконъюгантов, ферментами (например, бета-лактамазами), продуцируемыми в больших количествах донором. В-третьих, включено несколько экспериментальных контролей, чтобы убедиться, что продукт спаривания является истинным трансконъюгантом (т.е. клеткой-реципиентом, которая стабильно включила конъюгативную плазмиду донора). Здесь мы представили два независимых метода проверки подлинности трансконъюгантов, а именно колориметрический маркер в агаре Мак-Конки и ПЦР-обнаружение репликонов и генов устойчивости к антибиотикам конъюгативной плазмиды у реципиента. Кроме того, описанный здесь протокол предназначен для выделения и характеристики конъюгативных плазмид из экологических, комменсальных и патогенных членов семейства Enterobacteriaceae (Escherichia, Klebsiella, Enterobacter, Citrobacter, Salmonella, Shigella и других видов).
Чтобы понять механику сопряжения, экспериментальные наблюдения были смоделированы с использованием компьютерного моделирования. Эти прогностические модели оценивают частоту переноса плазмиды при заданной плотности роста доноров, реципиентов и трансконъюгантов. Модель, известная как конечная модель, обнаружила пороговые значения, выше которых скорость переноса плазмиды в жидкой культуре, и пришла к выводу, что скорость переноса не зависит от плотности клеток, соотношения донора и реципиента и времени спаривания19. Флуоресцентная гибридизация in situ (FISH) была использована в качестве альтернативного метода обнаружения трансконъюгантной плазмиды. FISH позволяет визуализировать плазмиды с помощью флуоресцентной микроскопии путем гибридизации ДНК-зонда и ДНК-мишени. Таким образом, FISH позволяет визуально обнаруживать потоки плазмид в разных клеточных популяциях37, хотя он не имеет такого же уровня чувствительности, как представленный здесь метод, если трансконъюганты обнаруживаются с помощью визуального скрининга, а не отбора.
Существует огромная потребность в понимании биологии конъюгативных плазмид, которые распространяют гены устойчивости к антибиотикам через различные компоненты экосистемы (клиника, сельское хозяйство, канализация, дикая природа, домашние животные, почвы, реки и озера). В целом, упрощенные экспериментальные условия, представленные в описанных здесь протоколах, облегчают скрининг доноров в масштабе и, таким образом, представляют собой ключевой инструмент для изучения горизонтального переноса генов, происходящего из конъюгативных плазмид из различных источников. Они могут быть использованы для исследования распространенности генов устойчивости к антибиотикам или других клинически значимых генов в конъюгативных плазмидах из нескольких источников и бактерий. Они также могут быть адаптированы для изучения конъюгации in vivo (например, в кишечнике позвоночных) и для изучения условий, которые модулируют эффективность конъюгации. Все эти исследования в значительной степени внесут свой вклад в понимание того, как мобилизация конъюгативных плазмид с множественной лекарственной устойчивостью способствует распространению множественной лекарственной устойчивости.
Раскрытие информации
Авторам раскрывать нечего.
Благодарности
LM-B, IMG, AT и IS были поддержаны грантом NIH GM055246, присужденным LM-B. GC-C был удостоен стипендии UC MEXUS-CONACYT Postdoctoral Fellowship в течение двух лет подряд: AY 2017-18 и 2018-19. Мы очень благодарим студентов Сейджа Чавеса и Пеппер Сент-Клер из программы наставничества Academic Inspiration Network (GAIN), спонсируемой Genentech-Foundation, за их техническую поддержку в экспериментах.
Материалы
| Name | Company | Catalog Number | Comments |
| 1.5 mL tube racks | Thermo Fisher Scientific | 22-313630 | It can be replaced for another brand |
| 2.0 mL Cryogenic vials | Corning | 430659 | It can be replaced for another brand |
| 14 mL conical tubes | FALCON | 149597 | It can be replaced for another brand |
| 14 mL tube racks | Thermo Fisher Scientific | 8850 | It can be replaced for another brand |
| 1 kb DNA ladder | New England Biolabs | N0552G | |
| 250 mL sterile flasks | PYREX | 5320 | It can be replaced for another permanent marker brand |
| Acetic acid | Fisher Scientific | A38SI-212 | It can be replaced for another brand |
| Agarose (molecular biology grade, multipurpose) | Fisher Scientific | BP160-500 | It can be replaced for another brand |
| Carbenicillin | GOLD BIOTECHNOLOGY | C-103-50 | It can be replaced for another brand |
| Disposable inoculating loops: 1 µL | Fisherbrand | 22-363-595 | It can be replaced for another brand |
| DNA gel loading dye 6x | New England Biolabs | B7024S | It can be replaced for another brand |
| EDTA | Fisher Scientific | BP119-500 | It can be replaced for another brand |
| Electronic digital scale | Denver Instrument | APX-2001 | It can be replaced for another brand |
| Eppendorf conical tubes: 1.5 mL | Eppendorf | 14-282-302 | It can be replaced for another brand |
| Equipment for agarose gel electrophoresis | Fisher Scientific | FP300 | It can be replaced for another brand |
| Ethanol-resistant markers | Sharpie | 37001; 37002; 37003 | It can be replaced for another brand |
| Gel documentation systems (UVP GelSolo) | Analytakjena | SP-1108; 849-97-0936-01; 95-0612-01 | It can be replaced for another brand |
| Gloves | X-GEN | 44-100M | Any nitrile gloves brand works |
| Ice bucket | Thermo Fisher Scientific | 432128 | It can be replaced for another brand |
| MacConkey agar | BD DIFCO | 212123 | |
| Master Mix | BioLabs | M0496S | It can be replaced for another brand |
| Methanol | Fisher Scientific | A452-4 | It can be replaced for another brand |
| Microcentrifuge tubes: 2.0 mL | Fisherbrand | 05-408-138 | It can be replaced for another brand |
| Mueller Hinton agar | BD DIFCO | DF0479-17-3 | |
| Mueller Hinton broth | BD DIFCO | 275730 | |
| NucleoSpin Plasmid, Mini kit for plasmid DNA | Takara Bio USA, Inc., MACHEREY-NAGEL | 740588. 250 | |
| PCR tube racks | AXYGEN | R96PCRFSP | It can be replaced for another brand |
| PCR tubes (0.2 mL) | AXYGEN | PCR-02-C | It can be replaced for another brand |
| Rifampicin | Fisher Scientific | 50-164-7517 | |
| Set of micropipettes that dispense between 1 - 10 μL (P10), 2–20 μL (P20), 20–200 μL (P200) and 200–1000 μL (P1000) | RAININ | 17008648; 17008650; 17008652; 17008653 | Micropipettes should be calibrated; can be replaced for another brand |
| Sodium chloride | Fisher Scientific | S671-3 | It can be replaced for another brand |
| Spectrophotometer | Thermo Scientific | 335905P | It can be replaced for another brand |
| Sterilized tips for 10 μL, 200 μL and 1000 μL | Eclipse | 1011-260-000-9; 1018-260-000; 1019-260-000-9 | It can be replaced for another brand |
| Streptomycin | Fisher Scientific | BP910-50 | |
| SYBR Safe DNA gel stain | Thermo Fisher Scientific | S33102 | |
| Taq DNA Polymerase | BioLabs | M0273S | |
| Thermal cycler C1000 Touch | Bio-Rad | 1851196 | It can be replaced for another brand |
| Tris | Fisher Scientific | BP153-500 | It can be replaced for another brand |
Ссылки
- Lederberg, J., Tatum, E. Gene recombination in Escherichia coli. Nature. 158 (4016), 558 (1946).
- de la Cruz, F., Frost, L. S., Meyer, R. J., Zechner, E. L. Conjugative DNA metabolism in Gram-negative bacteria. FEMS Microbiology Reviews. 34 (1), 18-40 (2010).
- Grohmann, E., Muth, G., Espinosa, M. Conjugative plasmid transfer in gram-positive bacteria. Microbiology and Molecular Biology Reviews. 67 (2), 277-301 (2003).
- Koraimann, G., Wagner, M. A. Social behavior and decision making in bacterial conjugation. Frontiers in Cellular and Infection Microbiology. 4, 54 (2014).
- Dziewit, L., et al. Diversity and role of plasmids in adaptation of bacteria inhabiting the Lubin copper mine in Poland, an environment rich in heavy metals. Frontiers in Microbiology. 6, 152 (2015).
- Smillie, C., Garcillán-Barcia, M. P., Francia, M. V., Rocha, E. P., de la Cruz, F. Mobility of plasmids. Microbiology and Molecular Biology Reviews. 74 (3), 434-452 (2010).
- Balbuena-Alonso, M. G., et al. Genomic analysis of plasmid content in food isolates of E. coli strongly supports its role as a reservoir for the horizontal transfer of virulence and antibiotic resistance genes. Plasmid. 123-124, 102650 (2022).
- San Millan, A., MacLean, R. C. Fitness costs of plasmids: A limit to plasmid transmission. Microbiol Spectrum. 5 (5), (2017).
- Coluzzi, C., Garcillán-Barcia, M. P., de la Cruz, F., Rocha, E. P. C. Evolution of plasmid mobility: Origin and fate of conjugative and nonconjugative plasmids. Molecular Biology and Evolution. 39 (6), 1-23 (2022).
- Bevan, E. R., et al. Molecular characterization of plasmids encoding blaCTX-M from faecal Escherichia coli in travellers returning to the UK from South Asia. The Journal of Hospital Infection. 114, 134-143 (2021).
- Minja, C. A., Shirima, G., Mshana, S. E. Conjugative plasmids disseminating CTX-M-15 among human, animals and the environment in Mwanza Tanzania: a need to intensify one health approach. Antibiotics. 10 (7), 836 (2021).
- Carattoli, A. Plasmids and the spread of resistance. International Journal of Medical Microbiology. 303 (6-7), 298-304 (2013).
- Sengupta, M., Austin, S. Prevalence and significance of plasmid maintenance functions in the virulence plasmids of pathogenic bacteria. Infection and Immunity. 79 (7), 2502-2509 (2011).
- Alderliesten, J. B., et al. Effect of donor-recipient relatedness on the plasmid conjugation frequency: a meta-analysis. BMC Microbiology. 20 (1), 135 (2020).
- Neil, K., Allard, N., Rodrigue, S. Molecular mechanisms influencing bacterial conjugation in the intestinal microbiota. Frontiers in Microbiology. 12, 673260 (2021).
- Liu, G., Bogaj, K., Bortolaia, V., Olsen, J. E., Thomsen, L. E. Antibiotic-induced, increased conjugative transfer is common to diverse naturally occurring ESBL plasmids in Escherichia coli. Frontiers in Microbiology. 10, 2119 (2019).
- Suchman, E. Polymerase chain reaction protocol. American Society for Microbiology. , 1-14 (2011).
- Watanabe, T. Infective heredity of multiple drug resistance in bacteria. Bacteriological Reviews. 27 (1), 87-115 (1963).
- Simonsen, L., Gordon, D. M., Stewart, F. M., Levin, B. R. Estimating the rate of plasmid transfer: an end-point method. Journal of General Microbiology. 136 (11), 2319-2325 (1990).
- Huisman, J. S., et al. Estimating plasmid conjugation rates: A new computational tool and a critical comparison of methods. Plasmid. 121, 102627 (2022).
- Jung, B., Hoilat, G. J. MacConkey medium. StatPearls. , (2022).
- . NucleoSpin Plasmid DNA purification Available from: https://www.mn-net.com/media/pdf/45/51/02/Instruction-NucleoSpin-Plasmid.pdf (2022)
- Jiang, X., et al. Detection of extended-spectrum beta-lactamases in clinical isolates of Pseudomonas aeruginosa. Antimicrobial Agents and Chemotherapy. 50 (9), 2990-2995 (2006).
- Stapleton, P. D., Shannon, K. P., French, G. L. Carbapenem resistance in Escherichia coli associated with plasmid-determined CMY-4 beta-lactamase production and loss of an outer membrane protein. Antimicrobial Agents and Chemotherapy. 43 (5), 1206-1210 (1999).
- Ben Yahia, H., et al. Detection of CTX-M-15 harboring Escherichia coli isolated from wild birds in Tunisia. BMC Microbiology. 18 (1), 26 (2018).
- Madsen, L., Aarestrup, F. M., Olsen, J. E. Characterisation of streptomycin resistance determinants in Danish isolates of Salmonella Typhimurium. Veterinary Microbiology. 75 (1), 73-82 (2000).
- Perreten, V., Boerlin, P. A new sulfonamide resistance gene (sul3) in Escherichia coli is widespread in the pig population of Switzerland. Antimicrobial Agents and Chemotherapy. 47 (3), 1169-1172 (2003).
- Guardabassi, L., Dijkshoorn, L., Collard, J. M., Olsen, J. E., Dalsgaard, A. Distribution and in-vitro transfer of tetracycline resistance determinants in clinical and aquatic Acinetobacter strains. Journal of Medical Microbiology. 49 (10), 929-936 (2000).
- Carattoli, A., et al. Identification of plasmids by PCR-based replicon typing. Journal of Microbiological Methods. 63 (3), 219-228 (2005).
- Green, M. R., Sambrook, J. Agarose gel electrophoresis. Cold Spring Harbor protocols. 2019 (1), (2019).
- Singer, V. L., Lawlor, T. E., Yue, S. Comparison of SYBR Green I nucleic acid gel stain mutagenicity and ethidium bromide mutagenicity in the Salmonella/mammalian microsome reverse mutation assay (Ames test). Mutation Research. 439 (1), 37-47 (1999).
- Tuma, R. S., et al. Characterization of SYBR Gold nucleic acid gel stain: a dye optimized for use with 300-nm ultraviolet transilluminators. Analytical Biochemistry. 268 (2), 278-288 (1999).
- Oatey, P. Imaging fluorescently stained DNA with CCD technology How to increase sensitivity and reduce integration times. Biotechniques. 42 (3), 376-377 (2007).
- Norman, A., Hansen, L. H., Sørensen, S. J. Conjugative plasmids: vessels of the communal gene pool. Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 364 (1527), 2275-2289 (2009).
- Du, L., Liu, R. H., Ying, L., Zhao, G. R. An efficient intergeneric conjugation of DNA from Escherichia coli to mycelia of the lincomycin-producer Streptomyces lincolnensis. International Journal of Molecular Sciences. 13 (4), 4797-4806 (2012).
- Kirk, J. A., Fagan, R. P. Heat shock increases conjugation efficiency in Clostridium difficile. Anaerobe. 42, 1-5 (2016).
- Esteves, G. M., Pereira, J. A., Azevedo, N. F., Azevedo, A. S., Mendes, L. Friends with benefits: An inside look of periodontal microbes' interactions using fluorescence in situ hybridization-Scoping review. Microorganisms. 9 (7), 1504 (2021).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены