このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
HIV感染患者との経験:末梢血中の細菌叢のシーケンシング
要約
私たちの実験では、HIV陽性患者の末梢血中に転位細菌種のシークエンス解析を実行する方法を説明します。
要約
健康な消化管は、生理的体液性および細胞性粘膜免疫系の1,2の開発に影響を与える共生微生物の多種多様によって植民地化されている。
微生物叢は、強力な粘膜関門を介した免疫系から遮蔽されている。感染症と抗生物質は、通常の消化管の障壁と3つの可能な免疫異常につながることが常駐細菌の構成、両方を変更することが知られています。
HIVは、全身免疫活性化4-7を貢献する、リポ多糖と細菌のDNA断片のような細菌のバイオ製品、、の全身循環への粘膜免疫と漏れの進行性破壊と消化管バリアの侵害を引き起こします。微生物の転座は、HIV /エイズ免疫病原性と治療4,8への応答に関与している。
我々は、HIV感染患者の末梢血中に転位細菌の組成を特徴づけることを目的とした。私たちの目的を追求するために我々は、シークエンス解析に続いてpanbacteric 16S ribosomial遺伝子のPCR反応をセットアップします。
簡単に言えば、両方のHIV感染と健常人全血が使用されます。健常者が正常な腸内恒常性を提示することを考えるとフローラのは転座は、これらの患者に期待されていません。静脈穿刺および血漿分離によって全血採取に続いて、DNAは血漿から抽出し、panbacteric 16S ribosomial遺伝子9用の幅広い範囲のPCR反応を実行するために使用されます。以下のPCR産物の精製、クローニングとシークエンシング解析を実施しています。
プロトコル
HIVに感染した血液サンプルの取り扱いが重要な推奨事項が必要です。
血液のすべての標本は、堅牢な漏れ防止のコンテナで輸送する必要があります。コンテナの外装のと試料に付随する事務処理の汚染を避けるために標本を収集する際には注意が必要です。
感染した血液を処理するすべての者は、手袋を着用する必要があります。手袋が変更され、手は、検体処理の完了後に洗浄する必要があります。
HIV感染血液サンプルの処理は、クラスIIバイオハザードキャビネットのフードで行う必要があります。
機械式ピペットエイドを使用する必要があります。
針や他の鋭利(ガラスなどのピペットやキャピラリーチューブを含む)の使用は選択肢が存在しない状況に限定されている必要があります。
実験室の表面は血の流出後の適切な化学消毒剤で除染する必要があり、作業活動が完了しているとき。
使用される汚染された材料は再使用前に除染する必要がありますまたは臨床廃棄物の経路を経由して正しく廃棄する必要があります。
介入が効果的であることが速やかに開始しなければならないとして、潜在的に感染血液や体液(すなわち、それらの必要とする普遍的予防策)への職業ばく露のすべての事件は、医療上の緊急事態として扱う必要があります。
プロトコルは、その完成のための5日間が必要です。時間枠は、図1に詳述されています。
細菌種は、図2で説明した方法を用いて識別されます。
1。サンプルコレクション
- 全血9mlのは、EDTAを含む試験管に描画されます。
- チューブは、プラズマを得るために、室温で10分間2000rpmで遠心分離されています。
- 血漿は、無菌の2ミリリットルエッペンドルフチューブに回収される。
2。血漿サンプルからのDNA抽出
- 適切に無菌性を保証するために、実験に必要なフード、ピペットと材料を消毒する。
- 少なくとも30分間UVライトの下にすべての材料を合わせます。
- 消毒と手袋を拭きます。
- エタノールのいくつかの紙タオルを浸し、ボンネットの下に配置します。たびに先端がウェットペーパータオルの上でピペットを拭いて破棄されます。
DNAは、製造業者の指示(簡単DNAキット、Invitrogen社、カールスバッドカリフォルニア州、米国)以下の市販のキットを使用して抽出されます。
- 血漿350μLを滅菌した2ミリリットルエッペンドルフチューブに配置されます。
- フィルタ処理された超純水350μLを陰性コントロールとして使用されています。
- サンプルにリゾチーム(1mg/ml)を10μLを加える。
- 37℃で30分間インキュベート℃に
- のLysis Solution 500μLを追加し、サンプルに軽く混合します。
- 65℃7分間インキュベート℃に
- サンプルにクロロホルム900μLを加える。
- サンプルが均一に粘性になるまで激しくボルテックスする。
- 降水量のソリューションと激しくボルテックス200μLを加える。
- 相を分離し、インタフェースを形成するために室温で10分間、10500 rpmで試料を遠心分離します。
- エタノール1 mlの100%を含む新しい微量遠心管に上部の水相を転送します。
- 4℃で10分間、10500 rpmで試料を遠心℃に
- エタノールを削除します。
- 70%エタノールを1mlを追加。
- 4℃で10分間、最高速度で試料を遠心℃に
- エタノールを削除します。残留エタノールはpipettatorで削除する必要があります。
- 超純水50μLでペレットを再懸濁する。
- 分光光度計でDNA濃度を読み取る。
3。 16S rRNA遺伝子のPCR
PCR増幅は、前述の9として実行されます。
- 10 × PCR緩衝液の10μL、25 mMのMgCl 2の5μL、2mMの合計のdNTPs 5μL、50μMのプライマーRW01(AACTGGAGGAAGGTGGGGAT)、50μMのプライマーDG74の1μLの1μLから成る100μL反応混合物中のDNAを増幅(AGGAGGTGATCCAACCGCA)、TaqポリメラーゼのH20および0.5μL(のAmpliTaqゴールド、アプライドバイオシステム、フォスターシティー、CA、米国)34μL。
- 細菌のTaqポリメラーゼによって可能な汚染を避けるためにフィルタにPCRミックスを転送します。
- 4で500 rcfで30分間、遠心フィルター(マイクロコン、ミリポア、ビルリカ、MA、米国)℃
- アリコート(正と負のPCRコントロール、試料と抽出された水)、増幅する必要のあるサンプル数に応じてPCRミックス。
- 以下のサーマルサイクラー条件使用:94℃で10分間、94℃1分ごとに時間の40倍° C、55 ° Cおよび72 ° C、および72℃で10分
- 2%アガロースゲルでPCR産物を可視化する。 100 bpのDNAラダーを使用してください。 PCR産物のサイズは360 bpの(図3)についてです。
4。 PCR産物の精製
唯一のPCR陽性検体は精製されるべきである。精製は、使用して実行されますメーカーの指示(PureLink PCR microkit、Invitrogen社、カールスバッドカリフォルニア州、米国)以下の市販のキット。
- PCR産物の1ボリュームあたりのイソプロパノールを含む結合緩衝液の4容量を追加。
- 列への結合バッファーでPCR産物を転送する。
- RTで10000 RCFで1分間遠心します。
- エタノールを含有Wash Bufferでカラムを洗浄します。
- RTで10000 RCFで1分間遠心します。
- シリカメンブレンを乾燥し、エタノールで残存する洗浄バッファーを除去するために、室温で1分間最大速度で遠心する。
- 超純水10μLを加える。
- 室温で1分間インキュベートする。
- 精製されたDNAを回収するために室温で2分間、最高速度で遠心する。
5。クローニング
溶原性ブロス(LB)プレートの準備
- 水の約800 mlのLBミックスの25グラムを溶かす。
- 1リットルの最終容量をもたらす
- Bactoagarの15グラムを追加。
- 20分間オートクレーブ。
- オートクレーブした後、精力的にスワールフラスコ内の溶液は、溶融寒天を混合する。
- 50℃にソリューションを冷却
- アンピシリン(50μg/ mlの)と渦巻き、それが溶けるまでを追加。
- 約3mmの深さに板を注ぐ。
- 室温でプレートを残す。
- 37各LBプレートとインキュベートのスプレッドはX - Gal(40mg/ml)とIPTG(100 mM)を° Cの使用の準備ができるまで。
コンピテントセルの形質転換
変換は、市販のキット以下のメーカーの指示に従って(TOPO TAクローニングキット、Invitrogen社、カールスバッドカリフォルニア州、米国)を使用して実行されます。
- クローニング反応ミックスを(新鮮なPCR産物1-4μL、塩溶液の1μL、ベクトルと水の1μL必要に応じて)用意してください。
- 穏やかに反応を混合し、室温で5〜10分間インキュベートする。
- 氷上で反応を置きます。
- コンピテントセルのバイアルにクローニング反応の2μLを加え、穏やかに混ぜる。
- 30分間氷上でインキュベートする。
- 42℃で30秒間熱ショック細胞℃に
- 直ちに氷中にチューブを移す。
- 培地250μLを加える。
- tighlyチューブにフタをし、37℃で水平にチューブを振る℃で1時間。
- 予熱した選択プレート上の各変換から50μLを広げる。
- 37℃で一晩インキュベート℃、
インキュベーション後、白色と青色のコロニーがプレート上で開発しています。白いコロニーがPCR産物の挿入のために正であり、青色のコロニーは、PCR産物の挿入のために陰性である。
6。配列解析
シークエンシング反応
- 2,5μlのDNA、1μlのプライマー(μL/ 5pmol)1,1μlのBigDye(アプライドバイオシステム、フォスターシティー、CA、米国):ミックスは、これらの試薬を用いて行われます。
- サーマルサイクラーの条件:96℃で1分間、4分15秒と60℃で10秒、55℃に対して96℃の場合は25回。
カラム精製
- 各反応について、あるマイクロスピンカラム(キアゲン、、ミラノ、イタリア)を準備する。
- 樹脂を混合する列と渦を反転。
- カラムの底部を折ります、マイクロ遠心チューブに蓋¼回転、および位置の列を緩めます。
- 1分間3200 rpmで遠心する。
- きれいな微量遠心チューブにカラムを移し。
- 慎重にピペット列の中心に全体のPCRシークエンス反応。
- 1分間3200 rpmで遠心する。
- 精製したDNAは、チューブ(超純水20μl)にeluiteなります。
配列解析
- 96マルチウェルプレートに、精製サンプル(20μl)をロードする。
- シーケンサーにプレートをロードする。自動DNAシーケンサは、シーケンスの実行の結果を示す4つの色のクロマトグラムを生成する。
- 公共シーケンスデータベースに対してクエリとしてヌクレオチド配列入力。検索は基本的なローカル配列検索ツール(BLAST)で、NCBIのデータベースとサーバー上で実行されます。
- 98から100パーセントの相同性と細菌だけを考えてみましょう。
7。代表的な結果
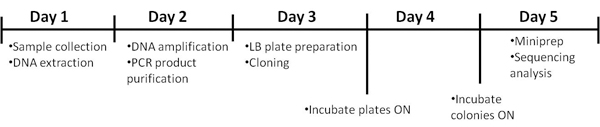
図1の手順のタイムライン。
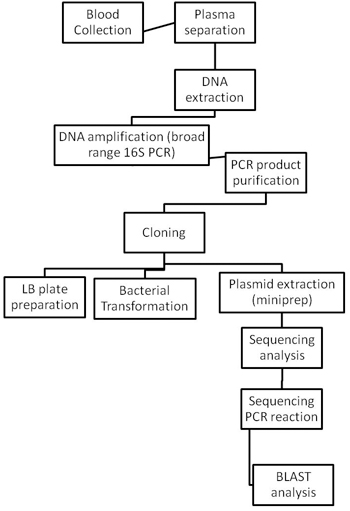
図2。全体の細菌同定の手順のフローチャート。
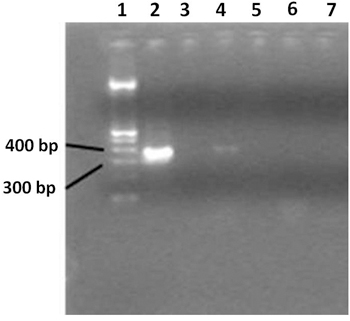
図3。幅広い範囲の16S rRNA遺伝子のPCR産物を示す、2%アガロースゲル。レーン1は100ベーシスポイントのDNAラダーを含む、レーン2はPCR陽性コントロールが含まれている、レーン3は負のPCRコントロールを示しています。レーン4は、HIV陽性の患者からサンプルを示し、レーン5は水が含まれています。レーン6 SH健康な人と否定的なPCR反応からのOWSのサンプル、レーン7は、水を含んでいます。唯一のHIV陽性患者では、肯定的なPCR増幅が表示されます。抽出工程中に、ネガティブコントロールとして使用される超純水は、コンタミネーションが発生していないことを示します。
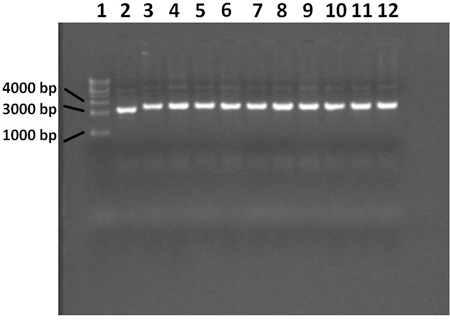
プラスミドを示す図4。0.7%アガロースゲルでは、ミニプレップの手順で抽出した。レーン1は1キロベースのDNAラダーを含む、レーン2は3〜12は、白色のコロニーを含んでいる車線、青いコントロールコロニーが含まれています。青いコロニーからのプラスミドは、PCR産物のインサートが含まれていません。すべての10個の白色コロニーが正しいインサートを持つプラスミドが含まれています。

図5は、1つHIV陽性の個体からの血漿中の細菌のシークエンス解析の例を示します。我々の結果は、HIV感染症の微生物の転座は、細菌のトランスロケーションを制御する腸管免疫の実質的な障害を示唆するHIV陰性の被験者ではない、と思われているpolimicrobic植物を、含むことを示している。
ディスカッション
我々はここにHIV感染者の末梢血中の細菌の転座を特徴づけるためにPCR /シーケンシングプロトコールを示す。
最も信頼性の高い結果が得られる。採血後、血漿が溶血し、DNA断片の劣化を避けるために、2 / 3時間以内に遠心分離によって分離されるべきである。サンプルは-80℃で、約5日間と℃、-20℃で最初に格納さ...
開示事項
謝辞
我々は、ビデオの製作と優秀な支援のためのジャンニシモーネに感謝しています。
資料
| Name | Company | Catalog Number | Comments |
| 試薬の名前 | 会社 | カタログ番号 | コメント(省略可能) |
|---|---|---|---|
| イースティ- DNAキット | インビトロジェン | K 180001 | |
| クロロホルム | シグマアルドリッチ | C2432 | |
| エタノール | シグマアルドリッチ | E7203 | |
| 超高純度Waer | インビトロジェン | 10977049 | |
| リゾチーム | フルカ | 62970 | 蒸留水で10μg/ mLの |
| のAmpliTaqゴールド | アプライドバイオシステム | 26478701 | |
| マイクロコントローラ100 | ミリポア | 42413 | |
| PCRプライマー | インビトロジェン | ||
| アガロース | エッペンドルフ | C1343 | |
| DNAラダー | インビトロジェン | 15628019 | |
| Purelink PCRマイクロキット | インビトロジェン | K310050 | |
| LB寒天、粉 | インビトロジェン | 22700025 | |
| Bactoagar | インビトロジェン | ||
| アンピシリン | インビトロジェン | 11593027 | 蒸留水に10 mg / mLの |
| X - galを | インビトロジェン | 15520034 | DMFで40mg/mL |
| IPTG | インビトロジェン | 15529019 | 蒸留水に100mMの |
| TOPO TAクローニングキット | インビトロジェン | K450002 | |
| Purelinkクイックプラスミドミニプレップキット | インビトロジェン | K210010 | |
| ビッグ染料 | アプライドバイオシステム | 4337455 | |
| DyeEx 2.0スピンキット | キアゲン | 63204 |
参考文献
- Hooper, L. V., Macpherson, A. J. Immune adaptations that maintain homeostasis with the intestinal microbiota. Nat Rev Immunol. 10, 159-169 (2010).
- Macpherson, A. J., Harris, N. L. Interactions between commensal intestinal bacteria and the immune system. Nat Rev Immunol. 4, 478-485 (2004).
- Kanauchi, O., Mitsuyama, K., Araki, Y., Andoh, A. Modification of intestinal flora in the treatment of inflammatory bowel disease. Curr Pharm Des. 9, 333-346 (2003).
- Brenchley, J. M. Microbial translocation is a cause of systemic immune activation in chronic HIV infection. Nat Med. 12, 1365-1371 (2006).
- Brenchley, J. M., Price, D. A., Douek, D. C. HIV disease: fallout from a mucosal catastrophe. Nat Immunol. 7, 235-239 (2006).
- Jiang, W. Plasma levels of bacterial DNA correlate with immune activation and the magnitude of immune restoration in persons with antiretroviral-treated HIV infection. J Infect Dis. 199, 1177-1185 (2009).
- Marchetti, G. Microbial translocation is associated with sustained failure in CD4+ T-cell reconstitution in HIV-infected patients on long-term highly active antiretroviral therapy. AIDS. 22, 2035-2038 (2008).
- Marchetti, G. Role of Microbial Translocation and Immune Hyperactivation in Disease Progression of HIV+ Patients with Preserved CD4 Count in the Absence of ART. , (2010).
- Greisen, K., Loeffelholz, M., Purohit, A., Leong, D. PCR primers and probes for the 16S rRNA gene of most species of pathogenic bacteria, including bacteria found in cerebrospinal fluid. J Clin Microbiol. 32, 335-351 (1994).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved