Method Article
Kırmızı Un Beetle Larva RNA Girişim,
* Bu yazarlar eşit katkıda bulunmuştur
Bu Makalede
Erratum Notice
Özet
RNA enterferans (RNAi) tabanlı gen demonte teknikleri Tribolium araştırma özünde vardır. Burada, biz Tribolium castaneum'ların bizim larva RNAi tekniğinin bir bakış sağlar. Larva RNAi araştırmacılar farklı bağlamlarda gen fonksiyonlarını incelemek için izin, kayıp fonksiyon-fenotiplerine hızlı erişim sağlayan basit, ama güçlü bir tekniktir.
Özet
Kırmızı un böcekleri, Tribolium castaneum, tam açıklamalı genom sekansı, transpozon bazlı genetik dönüştürme ve etkin bir RNA girişimi (RNAi) de dahil olmak üzere genetik ve geliştirme çalışmaları için, deney araçları bir repertuar sunar. Bu avantajlarının yanında, RNAi dayalı gen demonte teknikleri Tribolium araştırma özünde vardır. T. confusum mümkün basitçe böceğin vücut boşluğuna çift kollu RNA (dsRNA) enjekte edilmesiyle herhangi bir yaşam safhasında RNAi bir hale getirmektedir, sağlam bir sistemik RNAi tepki gösterir.
Bu yazıda, T. bizim larva RNAi teknik bir bakış sağlamak castaneum. Protokol T. uygun aşamasında (i) izolasyonu, Enjeksiyon için confusum larva ve enjeksiyon ayarı için, (ii) hazırlanması, ve (iii) dsRNA enjeksiyonu. Larva RNAi kaybı fonksiyon-fenotipinin hızlı erişim bize sağlayan basit, ama güçlü bir tekniktirBirden fazla gen demonte fenotiplerle yanı sıra hypomorphic fenotipleri bir dizi dahil, es. Hemen hemen tüm T. yana confusum dokuların hücre dışı dsRNA duyarlıdır, larva RNAi teknik araştırmacılar dış ortama doğru yanıtların organizma, genetik olarak dahil çeşitli bağlamlarda, dokuların ve çeşitli çalışma sağlar. Ayrıca, bu tekniğin basitliği T. yapma, araştırma daha öğrenci katılımını uyarır Bir sınıf ortamında kullanmak için ideal bir genetik sistem castaneum.
Giriş
Kırmızı un böceği, Tribolium castaneum nedeniyle RNA girişimi (RNAi) 1-3 gerçekleştirme kolaylığı kısmen biyoloji çeşitli alanlarda popülerlik kazanıyor. RNAi dayalı gen demonte teknikleri bilim adamları kayıp fonksiyon-kompleks genetik yöntemler kullanarak olmadan analizleri yapmak için izin verir. T. confusum mümkün böceğin vücut boşluğuna 4-6 olarak iki-şeritli RNA (dsRNA), basit enjeksiyon yoluyla herhangi bir aşamada RNAi bir hale getirmektedir, sağlam bir sistemik RNAi tepki gösterir. Birden fazla genin eşzamanlı devirme da T. mümkündür Aynı zamanda 7,8, iki veya daha fazla farklı dsRNA molekülleri enjekte confusum. Buna ek olarak, hypomorphic fenotiplerin bir dizi 8 dsRNA enjekte konsantrasyonunu azaltmak suretiyle oluşturulabilir. Bu özellikler T. geleneksel ileri genetik RNAi tabanlı ters genetik teknikleri cazip alternatifler yapmak castaneum. Yana neredeyseTüm T. confusum dokuların bu teknik, araştırmacılar farklı bağlamlarda dokuların çeşitli çalışma sağlar, hücre dışı bir dsRNA molekülleri 9 karşı hassastır. Ayrıca, bu rapor T. RNAi performans odaklansa da castaneum, burada açıklanan birçok prosedürler diğer böcekler için de geçerlidir. Isteyenler kaybı-fonksiyonu T. ilgi kendi bağlamlarında analizleri gerçekleştirmek için Dolayısıyla, bu protokol yararlıdır castaneum, yanı sıra diğer böcekler için bir RNAi tabanlı tekniği uygulamak isteyen araştırmacılar için.
Larva halinde dsRNA'yı enjekte larva, pupa olmak üzere böceği yaşam evrelerinde, çeşitli fonksiyonel analiz sağlar, ve yetişkin 4,5,10 sahneliyor. Biz daha önce moleküler biyoloji prosedürleri 11 olmak üzere bizim genel larva RNAi protokolü bildirdi. Mevcut raporda, biz en iyi görsel yardımcıları ile açıklanmıştır dsRNA'nın enjeksiyon prosedürleri açıklayan odaklanmak. Biz sağlayabilirayrıntılı adım-adım enjeksiyon işlemleri yanı sıra iyi ve kötü enjeksiyon örnekler. Bu görsel protokolü önceki protokol tamamlar ve kombine edildiğinde, onlar T. larva RNAi prosedürlerin daha kapsamlı bir görünüm sağlar castaneum. Buna ek olarak, RNAi, fizyolojik araştırma için RNAi bazlı deneylerde uygulama başarısını, hem de bir öğretim laboratuarda larva RNAi protokolünün uygulanabilirliğini etkileyebilecek dsRNA molekülleri için parametreleri tartışırlar.
Protokol
1. T. castaneum Stoklar ve Kültürleme
- Bir T. karar verin castaneum gerginlik deney için kullanılacak.
NOT: Birçok lab kurulan T. confusum suşlar mevcuttur. Ga-1 (Georgia-1) genom sekanslama 3 için kullanılan Ga-2 ebeveyn suşudur. Ga-1 (tek nükleotid polimorfizm, SNP) hisse senetleri çoğu DNA polimorfizmleri Ga-2, ve daha az olması nedeniyle soyluluk Ga-2 daha sağlıklı olduğundan, RNAi deneyler için idealdir. Pu-11 kullanımı uygun başka türdür Gelecek kanat primordia eşsiz gelişmiş sarı floresan protein (EYFP) ifadesi, diğer instars gelen son larva ayırt etmek bize izin verir gibi, (Clark-HACHTEL ve ark. 2013 12 Şekil S4 bakınız). Genetik arka anlamlı aff görünür gibi, deneyde kullanılan hangi böceği gerginlik belgelemek önemlidirEKT RNAi 13 fenotip. - T. hazırlayın (karıştırıldıktan sonra -20 ° C 'de kültür un saklamak) organik tam buğday ununa önceden elenmiş bira mayası (ağırlık olarak)% 5 eklenerek confusum un kültür. 6 oz plastik Drosophila hazır şişe (yaklaşık 40 g / şişe) içerisine (oda sıcaklığında) kültür un kısım.
- Kültür T. % 70 nem ile 30 ° C'de confusum. Bir nem kontrollü inkübatör mümkünse kullanın. Kültür şişe başına 30-40 yetişkin Ekle (erkek: kadın oranı 1: 1) kültürünü başlatın.
NOT: kalıp nadiren kültür un küf neden olabilir 30 ° C% 70 nem ile, düşük sıcaklıklar (örneğin 25 ° C) bir konu olmasına rağmen. Bu oluşursa nem indirin. - Alt kültür (kültür unundan yetişkin izole etmek nasıl adım 5.2-5.5 bakınız) için her iki haftada bir yeni bir kültür şişesine yetişkin aktarın.
NOT: Bu son dönem larvaları elde etmek için yaklaşık üç hafta sürer. Alternatively T. confusum kültürler daha uzun bir süre boyunca kültürleme ile de olsa, daha düşük bir sıcaklıkta (20-25 ° C) muhafaza edilebilir (25 ° C 'de gelişim süresi yaklaşık olarak iki katıdır, 30 ° C' de olan).
Larva DsRNA Enjeksiyon için Çözümler ve Araçların 2. Hazırlık
- In vitro transkripsiyon kullanılarak, hedef genin homolog dsRNA moleküllerini sentez. -80 ° C'de saklayın. Detaylı moleküler biyoloji prosedürleri için Philip ve Tomoyasu 2011 11 Bkz. Ayrıca DsRNA molekülleri tasarlarken dikkat edilmesi gereken parametrelerin bir dizi tartışma bakın.
- 1,5 ml 1 M NaH 2 PO 4, 8.5 ml 1 M Na-2 HPO 4 karıştırılarak (25 ° C'de pH 7.6), 0.1 M sodyum fosfat tampon maddesi, 10 ml olun. PH metre ile pH değeri kontrol edilir ve buna göre ayarlanır.
- 100 _ (25 ° C'de pH 7.6), 0.1 M sodyum fosfat tampon maddesi, 10 ul 10x karıştırılarak enjeksiyon tamponu 1 ml yapmak6, 0,5 M KCI, yeşil bir gıda boyası, 100 ul, iki kez damıtılmış suyun 790 ul (GKD 2 O). 2x enjeksiyon tampon (200 ul 10x enjeksiyon tampon + 800 ul GKD 2 O) yapmak için 10x enjeksiyon tampon sulandırmak. , Gerekli olana kadar, 4 ° C'de ve 2 x hem 10x tampon enjeksiyon saklayın.
- Sabit Cam Slaytlar hazırlayın.
- Larva enjeksiyonlar için repositionable tutkal formu ile bütün bir cam slayt örtün. Anahtar ya da pupa enjeksiyonlar için, sürgünün uzun bir kenar boyunca tutkal iki ince şeritler olun.
- Ayrıca enjeksiyonundan sonra bunların çıkarılmasını kolaylaştırmak için yeterince esnek kalarak tutkal, tutkal slayt böcekleri uymak için yeterli yapışkan kalmasını sağlar birkaç gün, kurumasını bekleyin.
NOT: tutkal çok yapışkan kalırsa, bir parmağınızı kullanın ve yapışkanlığını azaltacak, tutkal üzerine dokunun. Her slayt 40 veya 50 böceklerine kadar tutabilir ve güvenli hayvanları koruyamıyor kadar tekrar edilebilir. AlternBant bazen larvaları tutmak için yeterli yapışkan olmamakla birlikte rin, çift taraflı bant da kullanılabilir.
- Bir eterleştirme Sepeti olun.
- 10 ml'lik atılabilir bir şırınga pistonu çıkarın ve 6 mi doğrultusunda yaklaşık yarısında şırınga kesti.
- Şırınganın alt yarısı atın. Kısaca, bir gaz memesi ile şırınganın üst kısmı kesme yüzeyinin ısıtılması, hızlı bir şekilde ve şırınga üzerine yapıştırmak için örgü, naylon elekten bir parça üzerine erimiş plastik itin. Plastik sertleşir kez herhangi bir aşırı örgü uzak trim.
- Eter şişesi hazırlayın. Dar ağızlı bir 100 veya 250 ml'lik bir cam şişe içine 30 ml eter ekleyin. Eter buharlaşmasını geliştirmek için kağıt mendil birkaç parçaları ekleyin.
NOT: Eter yangın tehlikesi sunuyor ve aynı zamanda zararlıdır. Her bir davlumbaz altında eter anlaştım. Kullanımda sıkıca değilken kapağını kapatın.
Not: Buz sedatio rağmen (örneğin, bir sınıf ortamında olduğu gibi) daha güvenli bir alternatif olarak kullanılabilirn, daha az etkilidir.
Larva Enjeksiyon Aparatı 3. hazırlanması
- Bir mikroskop üzerine bir XY mekanik sahne yerleştirin.
NOT: XY mekanik aşamaları büyük mikroskop firmalardan temin edilebilir. Alternatif olarak, ucuz bir mikroskop aşamaları da bazı modifikasyonlar ile en kesme mikroskopları için kullanılabilir (örneğin, malzemeler tabloya bakınız). - XY mekanik sahne yakınındaki mekanik bir iğne manipülatör yerleştirin.
- Bir enjeksiyon şırınga birleştirin. Bir iğne basıncını etkilemeksizin enjeksiyon şırıngasının işleme izin veren, cam bir iğne tutucu bir 30 ml'lik atılabilir bir şırınga bağlamak için (Luer bağlantısı olan) dört yollu valf kullanarak (daha detaylı enjeksiyon şırınga için Philip, Tomoyasu 2011 11'e bakınız montaj).
4. Çekme Enjeksiyon İğneleri
- Bir borosilikat cam ile iğneler (0,5 mm, uzunluğu 15 cm: 1 mm İD B100-50-15, OD) Çekmeiğne çektirmenin.
NOT: Sutter P-87 veya P-97, ayarı kullanmak için "Isı = 70 = 45, Vel = 75, Zaman = 90 çekin" veya Pipet Cookbook Bölüm 2 izleyin: Değme Hücre, C elegans, Drosophila, ve Zebra balığı - Programlar önerilir. Optimum ayarları iğne çektirmenin modeline bağlı olarak değişebilir. Genel bir Drosophila enjeksiyon iğne ayarı iyi bir başlangıç noktasıdır. - Mağaza plastik durumda (örneğin, plastik bir CD kutusu) iğneler çekti ve çıkarılabilir montaj macun ile sabitleyin.
5. İzolasyon ve Larva Seçimi
- Bir elek alıcı üzerine 25. elek yerleştirin.
- Elek üzerinde kültür tüpüne (böcekleri ve kültür un) içeriğini yerleştirin ve hemen içeriği eleyin. Larvaları hızla elekten girecekler ve takılıyorum çalışacağız gibi, eleme olmadan elek üzerinde içeriğini bırakmayın. Agresif un düşmesine izin içeriğini elemekyoluyla ve yaşlı larvaları bırakın (genellikle 6 ve 7. larvası), elek üstünde arkasında (kendi cast-off tırnak etlerini, exuviae) ile birlikte pupa ve yetişkin.
- Tohum tavasına elek (böcekleri ve exuviae) kalan malzemeleri aktarın. Kaçan böcekleri önlemek için tavayı dokunarak tutun.
- Exuviae ve yavaşça tohum tavaniza üfleyerek böcek yüzeyi üzerinde geride kalan un partiküllerini.
- Tencerenin dibine içeriğini taşımak için tohum tava dokunun. Sonra, birkaç saniye boyunca kullanılmayan pan bırakın. Kazık çıkıp, diğer aşamalarda daha hareketli olan yetişkinler, bekleyin. Bir sanat fırça (örneğin, 1 cm genişliğinde) kullanarak yetişkin çıkarın.
- Pupa olarak, hafifçe aşağı tencerenin ağzını tutarak yavaşça tohum tava vurma ayrı pupa hızlı ağzına doğru rulo eğilimindedir. Tohum pan larvalarını bırakarak pupa kaldırmak için bir fırça kullanılır.
- Pltemiz bir Petri kabındaki izole larvaları ace. Enjeksiyon için, larvaların bir uygun seviyedeki seçip, ayrı bir Petri tabağına yerleştirin.
NOT: yetişkin morfolojileri yanı sıra başkalaşım üzerinde RNAi etkisini analiz edilirken Erken geçen larvası (son larva molt sonra 1-2 gün) genellikle uygundur. Ancak, bazen gerekli (örneğin, 3E-3H Rakamlar. Ayrıca Clark-HACHTEL ve ark. 2013 12) erken gen fonksiyonunu değerlendirmek için sondan bir önceki (veya daha erken) sahne RNAi gerçekleştirmek için olduğu. Instar larvalarının belirlemek için bir boyut referans olarak pupa kullanın. Son dönem larva biraz daha uzun pupa daha vardır. Alternatif olarak, poliüretan-11 son dönem larvaları tespit etmek yanı sıra, son dönem larvaların gelişimi (Clark HACHTEL Şekil S4 ve ark. 2013 12) zaman sürecini tespit etmek için kullanılabilir. - Eterleştirme kadar bir Petri kabındaki seçilen larva tutun. Kalanını yerleştiringeri un ile bir kültür şişeye ve inkübatör iade larva ve (örneğin pupa ve yetişkin olarak) böceklerinin diğer aşamaları.
Enjeksiyon İğneler 6. hazırlanması
- Yapışkan yapışkanlığı ya da çift taraflı bant kullanarak cam bir mikroskop lamı üzerine önceden çekilmiş cam iğne yerleştirin. Nerede ucu virajlı görmek için mikroskop bakarken forseps kullanarak, iğne çekti ucunu test edin. Forseps ve bükülme ile iğne virajlı kırmak için nerede uç tarafına doğru hafifçe alan tut.
- Iyi iğneler tutun ve diğerlerini atın. Bir ki, ne çok büyük veya çok küçük olan açma gibi iyi bir iğne düşünün (yaklaşık 0.05 mm çapında. Şekiller 1 A ve 1 B), ve larva kütikül daha kolay (Şekil 1B ve Şekil 2A-2B) nüfuz yapmak için açılıdır. Diffi iğne içine dsRNA çözelti alımı yapma ve kötü bir iğne, (i) çok küçük göz önündekült (basamak 7) (Şekil 1B ve 2B), (ii) çok büyük, enjeksiyon sonrası olası yaralanma ve larva öldürücülüğü yol (Şekil 1C ve 2F), üst deri zor ve artan yaralanma (iii) küt yapımında penetrasyon.
- İğne Tutucu içine İğne yerleştirin.
- İlk olarak, iğne tutucunun ucu sökün ve tutucu ucu içine iğnenin arka ucuna yerleştirin. Daha sonra, tutucu ucunun altına (cam iğnenin arka ucundan en az 1 cm) kauçuk bir contanın yerleştirilmesi.
- Tamamen iğne tutucusunun deliğine yerleştirilir kauçuk conta ile tutucu içine iğnenin arka, yerleştirin. Geri tutucuya ucu vida.
- İğne manipülatör üzerine monte iğne tutucu yerleştirin. Yatay yakın iğne tutucu tutun. MICR bakarak zaman manipülatör pozisyonunu ayarlayın, böylece iğnenin ucu görünümün merkezindeOscope.
İğne içine 7. önden DsRNA Çözüm
- GKD 2 O konsantrasyonunun, ve 2 x enjeksiyon tamponu (adım 2.3) eşit hacimlerde dsRNA solüsyonu karıştırılarak enjeksiyondan hemen önce dsRNA enjeksiyon çözelti hazırlayın. Buz üzerinde karışık çözelti, tutun. DsRNA'nın konsantrasyona ilişkin açıklamalara bakın.
- 20 ul atılabilir pipet ucu kesilir. Pipet kesilmiş pipet içine çözeltisinin 10 ul. Geri basınç sağlayarak ucundaki akışkan tutarken dikkatlice pipetten pipet çıkarın. Alternatif olarak, dikkatli bir ucu çıkartmak ve daha sonra, bir parmak kullanılarak basınç sağlayarak ucunun sonunda solüsyonun hareket ettirin.
- Iğne ucu yukarı bakacak şekilde açılması ile yapışkan yapışma kullanılarak mikroskop sahnede dsRNA çözeltisi ile pipet yerleştirin.
- Mikroskop bakarak, yavaş yavaş ucu kadar iğnenin doğru yüklenmiş ucu taşımakİğne sadece yüklenen pipet ucunun içine ve bu çözelti içine.
- Mikroskop bakarken, yavaşça yavaşça iğne içine dsRNA çözeltisi çekmek için enjeksiyon şırınga pistonu geri çekin.
NOT: İğneyi aşırı yüklenmeyin. DsRNA çözeltinin ucunun iğnenin ucu yaklaştıkça, çekme hızını yavaşlatır ve hava ulaşacak iğnenin ucu önce solüsyonunun durdurun. Hava ucu ulaşırsa, çözelti hızlı bir şekilde, ciddi kirlenme sorunları ile sonuçlanan iğne tutucu içine çekilecektir. İğne tutucunun ayrıntılı temizleme prosedürleri Philip ve Tomoyasu 2011 11 tarif edilmiştir. - Vananızı açarak enjeksiyon şırınga ve iğne tutucu gelen basıncı çıkarın. Daha sonra, iğne ucundan uzağa pipet hareket ettirin. Sahnede larvaları yerleştirirken yanlışlıkla iğneyi zarar görmesini önlemek için aşamasından iğne yukarı kaldırın. Aşamasından boşaltılmış pipet çıkarın.
8. dsRNA Enjeksiyon
- Eterleştirme sepet içine larva yerleştirin. Öğrenme tekniği ise en az 10 larva kullanın. Tekniği ile bir kez rahat bir tur 30-40 larva kullanın.
- Eter şişede larvaları ile sepet koyun ve kapağını kapatın.
NOT: Eter yangın tehlikesi sunuyor ve aynı zamanda zararlıdır. Davlumbaz altında bu adımı gerçekleştirin. - Yaklaşık 3 dakika boyunca eter haline larva. 3 dakika sonra bir hareket için larvaları kontrol edin. Onlar hala hareket halinde başka bir 30 saniye boyunca eter şişede onları geri yerleştirin. Letalitenin artabilir olarak en fazla 5 dakika boyunca eter haline etme.
NOT: Optimum eterleştirme süresi sıcaklık ve neme bağlı olarak değişebilir. - Yapışkan cam slayt yapışmaz kenarına sepetten Eterlenmiş larvaları aktarın. Forseps kullanma ve mikroskop aracılığıyla bakarken, biri her larva bir pick up ve slayt üzerine koyun. F vücutlarını aşağı dokunun hafifçe yanal yatırın veEğer gitmek gibi forseps ile kuyruk rom kafa, biraz onlar slayt üzerine güvenli olduğundan emin olmak için, onları germe.
- Mikroskop sahnede larvaları ile yapışkan slayt yerleştirin.
- MSS zarar görmesini önlemek için larva dorsal tarafına hafifçe dsRNA'nın yüklenen iğne takın. Larva kalbi burada yer alan olarak da, dorsal orta hat kaçının. Bu ve sonraki adımlarda, her zaman (yerine iğne taşımak için iğneli bir manipülatör kullanılarak) iğne Larvalar taşımak için sahne kullanın.
NOT: Belirli bir enjeksiyon sitesi T. RNAİ'nin kadar önemli değil confusum sistemik olarak görünmektedir. Ancak, torasik veya abdominal segmentlerin dorsal tarafına enjekte genellikle en kolay yoldur. - Larva içine iğne taktıktan sonra, dsRNA'nın larva vücut boşluğuna girmek için oda izin hafifçe arkaya iğneyi çekin.
- Larva dönüş yeşil (ya da enjeksiyon tampon rengi) kadar enjeksiyon şırınga hafifçe bastırın ve s bakmaktretched tam.
Not: tekniği öğrenme ise, belirgin olmayan bir öldürücülüğünün bir larvaya enjekte edilebilir çözelti miktarının saptanması mümkün olduğu kadar enjekte deneyin. Genellikle, yaklaşık 0.5-0.7 ul'dir. - Larvaları iğneyi çıkarın. Iğne çıkarılırken, biraz geri dsRNA'nın kaybını önlemek için enjeksiyon şırınga çekin (aynı zamanda hava çekmek için dikkatli olun).
- Slayt tüm larvaları enjekte edilir. Başarıyla enjekte değil larva kaldırmak için emin olun. Larvaları önce Komple enjeksiyon (yaklaşık 10 dk) uyanıyorum.
- Enjeksiyon mikroskop enjekte larva ile slayt çıkarın ve tüm larvalar eterleştirme kurtarmak kadar 5 dakika daha slayt bırakın.
- Forseps ile ve bir mikroskop altında, hafifçe yapışkan slayt onları serbest bırakmak için baş kuyruk larvaları kaldırın. Temiz bir Petri kabındaki yeni piyasaya larva yerleştirin. W enjeksiyon imkan vermek üzere 10-15 dakika süre ile Petri tabağına larvaları bırakpıhtılaşmaya ound.
- Uygun bir soy adı dahil olmak üzere temiz unu ve etiket ile yeni bir şişe içine yerleştirin larvaları, dsRNA türü, dsRNA konsantrasyonu enjekte edilen larva sayısı, ve tarih enjekte edilir.
- Kültür% 70 nem ile 30 ° C'de Enjeksiyon yapılmış olan larvalar. Düzenli RNAi fenotipleri için larvaları gözlemleyin.
NOT: 7 gün içinde son dönem larvalar pupa. (RNAi kaynaklanan zamanlama hiçbir anormallik varsa) Sonra, pupa 7 gün sonra yetişkinler eclose olacaktır.
Demonte ve Fenotipik Analizleri 9. Onayı
- Böyle nicel ters transkripsiyon-PCR (qRT-PCR) ve Western Blot gibi çeşitli moleküler biyoloji teknikleri ile yıkmak RNAi değerlendirmek verimliliği göz önünde bulundurun. Sırasıyla, Miller ve diğ. 2012 7 Philip ve ayrıntılı QPCR için Tomoyasu 2011 11 ve Western Blot 'daki protokole bakınız.
- RNAi ilgili fenotipleri analiz edin.
NOT: İlgili RNAifenotipler hedeflenmiş gen bağlı olarak, birkaç farklı aşamalarında ve farklı kültür koşulları altında gözlemlenebilir. RNAi böceği morfolojisi, metamorfoz, fizyoloji, ve davranışını etkileyebilir. Ne kadar sıklıkla fenotip varlığı kontrol edilir ve böcekleri yetiştirilir koşulları belirli sorulara uygun olmalıdır ne altında RNAİ'nin yoluyla araştırılmaktadır.
Sonuçlar
Başarılı enjeksiyon için önemli adımlardan biri iyi bir iğne yapmaktır. Aşama 6'da tarif edildiği gibi, iğne ucu önceki T. enjekte parçalanmasına gerek castaneum. Iyi ve kötü iğne örnekleri, Şekil 1 'de gösterilmiştir. Iyi bir iğne, yaklaşık olarak 0,05 mm çaplı bir delik (Şekil 1B) ile, keskin ve sert bir uca sahiptir.
Şekil 2, bir başarılı bir enjeksiyon (Şekil 2A ve 2B) ve başarısız enjeksiyonlar (Şekiller 2C-2F) arasında çeşitli durumları gösterir. Uygun büyüklükte bir enjeksiyon iğnesi ile, iğne ucu en az direnç (Şekil 2A) ile larva kütikül girer ve dsRNA çözeltisi (yeşil) herhangi bir sızıntı (Şekil 2B) olmadan larva akar. Aşırı enjekte gibi bile doğru boyutta bir enjeksiyon iğnesi (Şekil ile DsRNA çözümün taşmasına neden olacaktır etmeyin2C). Iğne ucu çok ince olursa, iğne ucu genellikle zor enjeksiyon (Şekil 2D), yapım larva kütikül ve virajlı nüfuz başarısız olur. Bu durumda, kırpma iğne ucu bazen yardımcı olur. Büyük iğneler larva manikür (Şekil 2E) nüfuz bazı zorluklarla da olsa, sık sık hala kullanılabilirler. Bununla birlikte, dsRNA çözeltinin büyük bir miktan, genellikle dsRNA çözeltisi (Şekil 2F) bir taşma ile sonuçlanan, hatta enjeksiyon şırınga üzerinde hafif basınçla iğne dışarı itilir.
RNAi yaparken, bu RNAi düzgün çalıştığını ve bir negatif kontrol gözlenen etki DsRNA'nın non-spesifik bir etkisi veya sebep gibi yaralanma gibi enjeksiyon prosedürleri (bir sonucu olmadığını doğrulamak için değerlendirmek için olumlu bir kontrole sahip olmak önemlidir ) eterleştirme enjeksiyonla ya da anormallik. DsRNA hedefleme EYFP enjeksiyon bir olarak hizmet verebilirpozitif kontrol iyi pu-11 suşu 5,7 kullanırken. EYFP dsRNA son larva aşamasında enjekte edildiğinde, kanat gelecek primordia içinde EYFP sinyalinde önemli bir azalma olarak bir gün önceden art enjeksiyon (Şekil 3A) olarak görülmektedir. EYFP bir yok etme iki gün EYFP dsRNA'nın (Şekil 3B) enjeksiyonundan sonra tamamlanır ve bu yok etme dsRNA konsantrasyonu yeterince (1 gibi yüksek ise pupal aşamada (Şekil 3C ve 3D) boyunca ve böceğinin yaşam boyunca devam ug / ml) 7. EYFP dsRNA'nın olmayan bir endojen gen dizisi olduğu için, aynı zamanda, bir negatif kontrol olarak kullanılabilir ve morfolojik ve fizyolojik aksaklıkları (Şekiller 3A-3D) neden olmamalıdır.
Bu ne kadar EF başka bir örnek olarak, artık (VG) için larva RNAi görüntülerini kritik kanat gen 12.Bu enjeksiyon dayalı RNAi tekniği T. olduğu etkinleştirilecek castaneum. VG dsRNA'nın sondan bir önceki aşama larvaları (son larva aşamasında önceki bir aşamada) enjekte edildiğinde, kanat yapılarının tam bir kayıp pupa aşamasına (Şekil 3E ve 3F) gözlenebilir. Oluşan yetişkin de tamamen kanat yapıları (Şekil 3G ve 3H) yoksun. VG RNAi sonucu sağlamlık ve T. RNAİ'nin sistemik doğasını hem de örnekliyor castaneum.
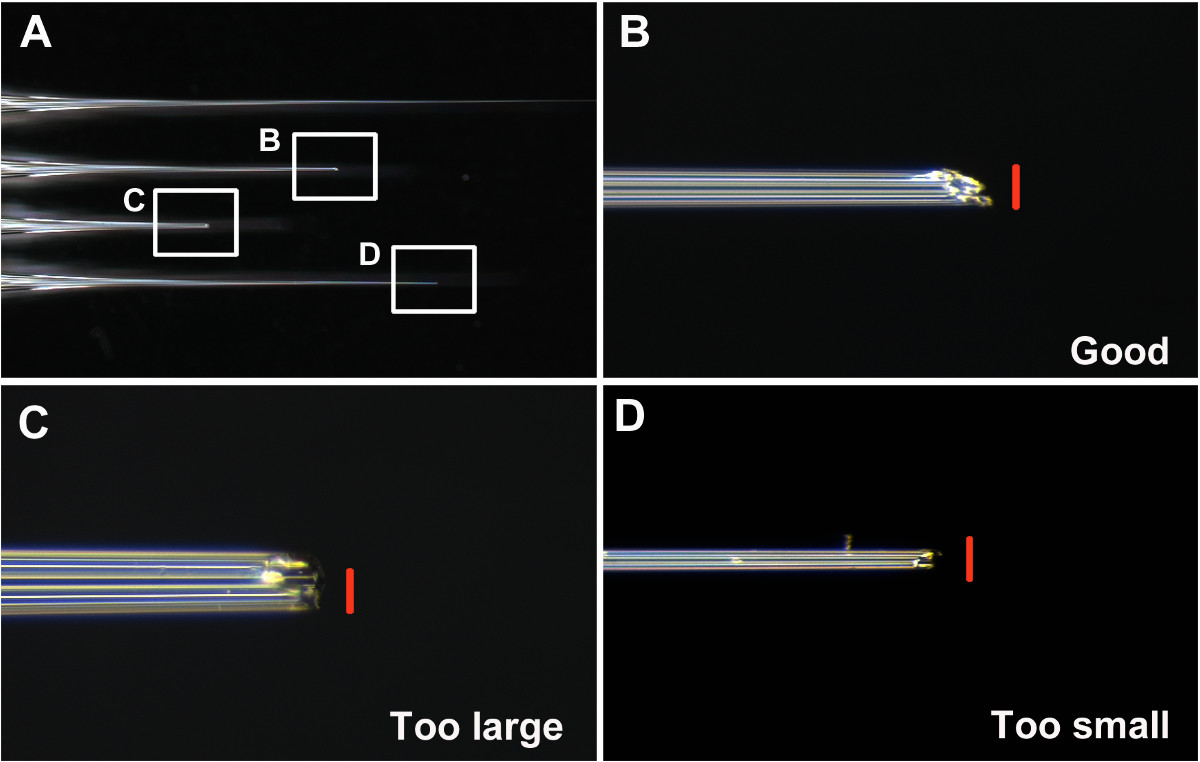
Şekil 1:, kırılmamış iyi ve kötü iğne (A) Örnekler (B) iyi-kırık iyi iğne ucu (C) çok büyük ve künt bir kırık iğne ucu (D) ucu... Bir kırdı arasında Çok ince iğne n. Ölçek çubukları (kırmızı) 0,05 mm. , bu rakamın büyük bir versiyonunu görmek için lütfen buraya tıklayınız.

Şekil 2:.. (A). Orta ölçekli bir enjeksiyon iğnesi son dönem larva yerleştirilir (B) arasındaki bir doz uygun bir şekilde, yeşil dsRNA enjekte edilen çözelti (C) aşırı enjeksiyonunun sebep olduğu enjeksiyon noktasında dsRNA çözeltinin taşması (D ) larva manikür nüfuz başarısız İnce bir iğne. (E) son dönem larva içine yerleştirilen büyük bir enjeksiyon iğnesi. (F) Larva DsRNA çözümün taşması ve sızıntılara neden büyük bir iğne ile enjekte edilir. Oklar iğneler göstermektedir.ove.com/files/ftp_upload/52059/52059fig2highres.jpg "target =" _blank "> Bu rakamın büyük bir versiyonunu görmek için lütfen buraya tıklayınız.
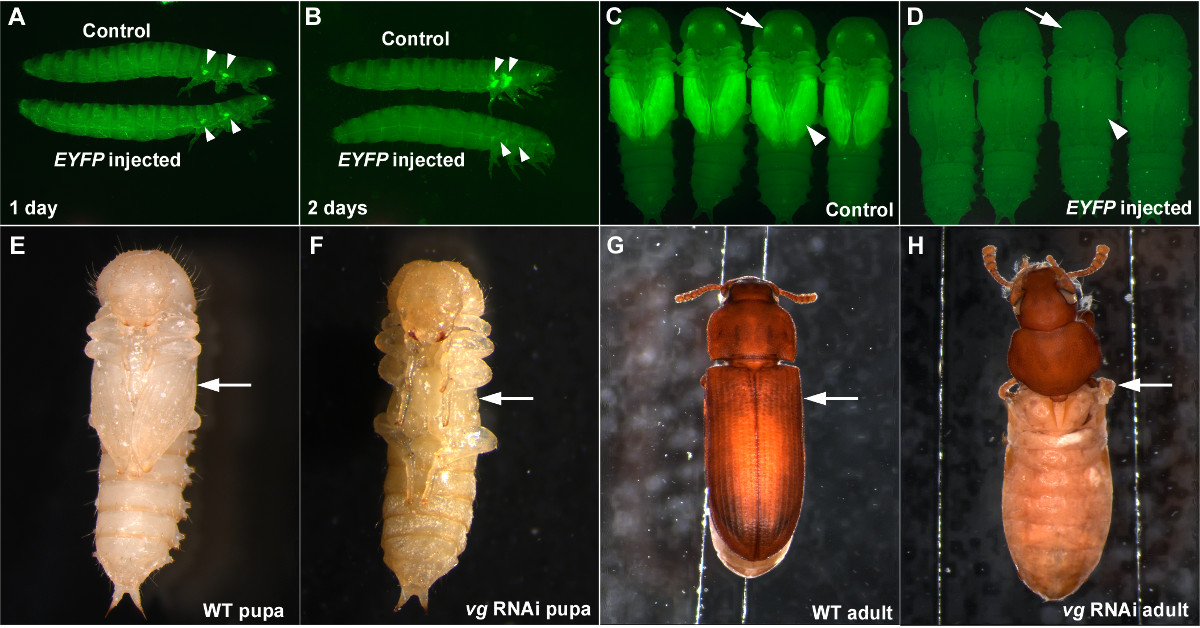
Şekil 3: T. başarılı RNAi örnekleri confusum. (AD), EYFP ekspresyonunun azaltılması EYFP dsRNA sonuç yorumlanan larva enjeksiyonu. elde edilen (A), Larva enjeksiyonundan bir gün sonra. (B) 'Larva enjeksiyondan iki gün sonra. (C) Kontrol pupa. (D) Pupa larva EYFP dsRNA enjeksiyon. Negatif kontroller, tampon enjeksiyon (A, B) ve DsRed dsRNA'nın enjeksiyon (C, D) 'dir. Ok uçları ve oklar EYFP ifadesini belirtmek veya sırasıyla kanat primordia ve gözler, bunların eksikliği. (EH) KalemVG nihai larva RNAi. (E) Yabani-tip pupa. (F) VG RNAi pupa. Kanat yapılarının yokluğu pupa aşamasına (ok). G) Yabani-tip yetişkin. (Y) VG RNAi yetişkin daha önce görülebilir. Kanat ilgili yapılar tamamen (ok) eksik. , bu rakamın büyük bir versiyonunu görmek için lütfen buraya tıklayınız.
Tartışmalar
There are a number of important issues that need to be considered to guarantee the success of RNAi, including the length and concentration of the dsRNA molecules, competition among different dsRNA molecules (when attempting multiple knock down), and the possibility of Off-Target Effects (OTE).
dsRNA Length
The length of dsRNA molecules affects the efficiency of the systemic RNAi response, with a longer dsRNA being more efficient to trigger RNAi7,14,15 (though the longer limit of dsRNA is currently unknown). The dsRNA length needs to be longer than 50 bp to induce effective RNAi in T. castaneum7. dsRNA between 150 bp and 500 bp appears to be ideal for RNAi experiments. Although longer dsRNA molecules can also be used, they will have an increased chance of OTE and the gene-cloning step will become increasingly difficult.
dsRNA Concentration
Different degrees of gene knockdown can be achieved depending on the concentration of dsRNA. 1 μg/μl appears to be a reasonable starting concentration, which often produces a near-null phenotype (may vary depending on the gene(s) of interest). RNAi can be performed with a higher concentration (e.g., 7-8 μg/μl) to obtain a stronger RNAi phenotype. RNAi with a serial dilution of dsRNA can sometimes be beneficial to produce a series of hypomorphic phenotypes (Supplemental Data of Tomoyasu et al. 20098, and Borràs-Castells unpublished data).
RNAi Competition
Multiple gene knockdown can be accomplished in T. castaneum by injecting several different dsRNA molecules simultaneously. However, it is also known that having several different dsRNA molecules present within the organism often results in competition between the dsRNAs for access to the RNAi components7,14. It is important to use the same length and the same concentration for all dsRNA when attempting multiple gene knockdown to avoid one dsRNA out-competing the others (although, further adjustments of the dsRNA length and concentration may be required when the expression levels greatly differ among the target genes). We, as well as others, have successfully performed double and triple knockdown (e.g., Tomoyasu et al. 200516, Tomoyasu et al. 200917, and Yang et al. 200918). Although feasible, quadruple RNAi (or more) might be challenging, as it would likely cause significant reduction of RNAi efficiency for all four target genes.
Off-targeting
OTE is an inherent concern for RNAi-based approaches. One way to minimize OTE is to identify regions in the target gene that share similar sequences with other genes and avoid these regions when designing dsRNA. A simple BLAST analysis against the T. castaneum predicted gene set can identify such regions. Several online tools also allow evaluation of potential OTE (e.g., E-RNAi19). Performing RNAi for two non-overlapping regions of the target gene is an easy and efficient way to eliminate the possibility that observed phenotypes are caused by OTE. The possibility of OTE is minimized if RNAi for two non-overlapping regions produce the same phenotypes (unless the two non-overlapping regions share a similar sequence).
Evaluating gene knockdown by means other than phenotypic analyses is often critical to effectively present RNAi-related data. Two major ways to evaluate gene knockdown are qRT-PCR and western blot analysis. qRT-PCR is a convenient way to measure the level of the target mRNA, and has been used in many RNAi-related studies including those in T. castaneum (see Miller et al. 20127 for example). However, caution must be taken, as we have recently seen some cases in which the target mRNA level is up-regulated by RNAi (though the protein product is down-regulated) (Borràs-Castells unpublished data). It is currently unknown if this RNAi induced mRNA up-regulation can be widespread or unique to certain genes. Western blot analysis is another way to confirm gene knockdown. This method is quite reliable as it measures the amount of the final protein product. The requirement of a specific antibody against the protein product of the target gene is a downside to this approach. Utilizing multiple independent measurements in addition to phenotypic analysis will increase the confidence of the phenotypic data obtained by RNAi-based analysis.
Since its conception in T. castaneum, RNAi has primarily been used to study gene function in development and pattern formation. These T. castaneum developmental studies have been highly successful in characterizing evolutionarily conserved and diverged functions of genes (reviewed in Denell 20081 and Klingler 20042). However, RNAi-based studies in T. castaneum are not limited to developmental biology. For example, RNAi can be utilized to study gene function in a wide range of physiological and behavioral responses, including stress tolerance, predation, aggression, mate choice, activity patterns, and defense mechanisms.
One difficulty of applying RNAi to these contexts is the likelihood of pleiotropic effects. Often, genes of interest will have a variety of roles throughout the T. castaneum life cycle, thus making the removal of genes without unintended phenotypic effects difficult. However, the ability to easily perform RNAi at a variety of stages can often be an effective strategy for avoiding these pleiotropic effects. For instance, performing RNAi in adults instead of larvae or pupae might allow us to circumvent unintended lethality caused by gene knockdown during early development. The flexibility of the RNAi response in T. castaneum thus makes this model an attractive choice for adapting RNAi to experiments of gene function in physiological and behavioral responses.
The T. castaneum system is also ideal for use in a teaching laboratory. T. castaneum can be easily cultured on a flour/yeast mixture at room temperature (25 °C) without frequent subculturing, and RNAi techniques in T. castaneum are simple enough to be adapted to a laboratory with young, learning scientists. As RNAi is becoming an essential technique in a variety of biological fields, it is crucial that students are exposed to this technique. The straight-forward nature of the larval RNAi technique in T. castaneum also encourages more students to be involved in research, making T. castaneum a prime candidate for a classroom oriented genetic system.
Açıklamalar
Yazarlar ifşa hiçbir şey yok.
Teşekkürler
We thank the Center for Bioinformatics and Functional Genomics (CBFG) at Miami University for technical support. This work was supported by Miami University start-up grant (YT), and National Science Foundation (YT: IOS 0950964).
Malzemeler
| Name | Company | Catalog Number | Comments |
| Organic whole wheat flour | Heartland Mill Inc. Kansas | G1 | |
| Brewer’s yeast | MP Biomedicals | 2903312 | Sift yeast with #35 stainless sieve before use. Wear protective mask and cover the sieve with plastic wrap, as the sifted yeast is a fine particle and respiratory hazardus. |
| 6 oz plastic Drosophila stock bottles | Fisher Scientific | 11-888 | |
| Sieve | Fisher Scientific | 04-881N | 8 in. dia. x 2 in.D. Use #25 (Nominal opening 710 µm) for larvae, pupae, and adults. |
| Sieve | Fisher Scientific | 04 881 10P | 8 in. diameter #35 (Nominal seive opening: 600 µm) Stainless Steel Sieves, 8 in. dia. x 2 in.D. This sieve is ideal to remove clumps from yeast powder. |
| Sieve receiver | Fisher Scientific | 04-866B | 8 in. diameter |
| 1.5 Quart spouted sample pan | Seedburo Equipment Co. | Model 33 | collection pan |
| Incubator | BioCold Environmental Inc | BC26-IN | Keep it 30 °C with 70% humidity. |
| Na2HPO4 | Fisher Scientific | S374500 | |
| NaH2PO4 | Fisher Scientific | S397-500 | |
| KCl | Fisher Scientific | P217-500 | |
| Food dye | Kroger | green, blue, or red preferable | |
| Microscope glass slide | Fisher Scientific | 22-038-103 | |
| Tack-It Over&Over | Aleene's | Repositionable glue for sticky slides. Double sided tape can be used as an alternative, however, we found that the adhesiveness varies. | |
| Plastic CD case | Amazon | ||
| Boroslilicate glass capillary | Sutter Instrument | BF100-50-15 | O.D. 1 mm, I.D. 0.5 mm, 15 cm. Without filament |
| Needle puller | Sutter Instrument | P-87 or P-97 | |
| Removable mounting putty | Loctite Fun-Tak | ||
| Compressed gas duster | OfficeMax | OM96091 | |
| Forceps | Fine Science Tool | 11231-30 | Dumoxel #3 (to manipulate beetles) |
| Forceps | Fine Science Tool | 11252-20 | INOX #5 (to break needle tips) |
| Ethyl ether, anhydrous | Fisher Scientific | E138-500 | |
| Nylon mesh | Flystuff/Genessee Scientific | 57-102 | 120 µm pore size/49% open area |
| Media bottle, 100 ml | VWR | 89000-926 | |
| Stereomicroscope | Zeiss | SteREO Discovery V12. Injection microscope. | |
| Stereomicroscope | Fisher/Zeiss | 12-070-513 | Stemi2000. Use to break the needle and place larvae onto the sticky slide. |
| X-Y mechanical stage | Zeiss | 4354600000000000 | |
| X-Y mechanical stage | Microscopenet.com | A512 | Inexpensive alternative |
| Manipulator | Narishige | M-152 | |
| Magnetic stand | Narishige | GJ-1 | |
| Glass capillary holder | Narishige | IM-H1 | |
| 30 ml Disposable syringe | BD syringe | 309650 | BD Luer-Lok Tip |
| Four-way stopcock | Cole-Parmer Instrument Co. | EW-30600-03 | Stopcocks with Luer connections; 4-way; male slip |
| Art paint brush | Amazon | Art Advantage Oil and Acrylic Brush Set, 24-Piece | Any general paint brush will work. |
Referanslar
- Denell, R. Establishment of Tribolium as a genetic model system and its early contributions to evo-devo. Genetics. 180, 1779-1786 (2008).
- Klingler, M. Tribolium. Curr Biol. 14, R639-R640 (2004).
- Richards, S., et al. The genome of the model beetle and pest Tribolium castaneum. Nature. 452, 949-955 (2008).
- Bucher, G., Scholten, J., Klingler, M. Parental RNAi in Tribolium (Coleoptera). Curr Biol. 12, 85-86 (2002).
- Tomoyasu, Y., Denell, R. E. Larval RNAi in Tribolium (Coleoptera) for analyzing adult development. Dev Genes Evol. 214, 575-578 (2004).
- Tomoyasu, Y., et al. Exploring systemic RNA interference in insects a genome-wide survey for RNAi genes in Tribolium. Genome biology. 9, R10 (2008).
- Miller, S. C., Miyata, K., Brown, S. J., Tomoyasu, Y. Dissecting systemic RNA interference in the red flour beetle Tribolium castaneum parameters affecting the efficiency of RNAi. PLoS ONE. 7, e47431 (2012).
- Tomoyasu, Y., Arakane, Y., Kramer, K. J., Denell, R. E. Repeated co-options of exoskeleton formation during wing-to-elytron evolution in beetles. Curr Biol. 19, 2057-2065 (2009).
- Miller, S. C., Brown, S. J., Tomoyasu, Y. Larval RNAi in Drosophila. Dev Genes Evol. 218, 505-510 (2008).
- Brown, S. J., Mahaffey, J. P., Lorenzen, M. D., Denell, R. E., Mahaffey, J. W. Using RNAi to investigate orthologous homeotic gene function during development of distantly related insects. Evolutio., & development. 1, 11-15 (1999).
- Philip, B. N., Tomoyasu, Y. Gene knockdown analysis by double-stranded RNA injection. Methods Mol Biol. 772, 471-497 (2011).
- Clark-Hachtel, C. M., Linz, D. M., Tomoyasu, Y. Insights into insect wing origin provided by functional analysis of vestigial in the red flour beetle. Tribolium castaneum, Proceedings of the National Academy of Sciences of the United States of America. 110, 16951-16956 (2013).
- Kitzmann, P., Schwirz, J., Schmitt-Engel, C., Bucher, G. RNAi phenotypes are influenced by the genetic background of the injected strain. BMC genomics. 14, 5 (2013).
- Parrish, S., Fleenor, J., Xu, S., Mello, C., Fire, A. Functional anatomy of a dsRNA trigger differential requirement for the two trigger strands in RNA interference. Molecular cell. 6, 1077-1087 (2000).
- Winston, W. M., Molodowitch, C., Hunter, C. P. . Systemic RNAi in C elegans requires the putative transmembrane protein SID-1. 295, 2456-2459 (2002).
- Tomoyasu, Y., Wheeler, S. R., Denell, R. E. Ultrabithorax is required for membranous wing identity in the beetle Tribolium castaneum. Nature. 433, 643-647 (2005).
- Trauner, J., et al. Large-scale insertional mutagenesis of a coleopteran stored grain pest, the red flour beetle Tribolium castaneum, identifies embryonic lethal mutations and enhancer traps. BMC Biol. 7, 73 (2009).
- Yang, X., et al. Probing the Drosophila retinal determination gene network in Tribolium (II) The Pax6 genes eyeless and twin of eyeless. Developmental biology. 333, 215-227 (2009).
- Horn, T., Boutros, M. E-RNAi a web application for the multi-species design of RNAi reagents--2010 update. Nucleic acids research. 38, 332-339 (2010).
Erratum
Formal Correction: Erratum: Larval RNA Interference in the Red Flour Beetle, Tribolium castaneum
Posted by JoVE Editors on 10/01/2015. Citeable Link.
An erratum was issued for Larval RNA Interference in the Red Flour Beetle, Tribolium castaneum. There was a typo in the settings for Sutter P-87 in step 4.1.
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır