Method Article
Bildgebende Merkmale der systemischen Sklerose-assoziierten interstitiellen Lungenerkrankung
In diesem Artikel
Zusammenfassung
Hier stellen wir praktische Empfehlungen zur Durchführung einer thorakalen hochauflösenden Computertomographie zur Diagnose und Bewertung systemischer Sklerose-bedingter interstitielle Rinnsanimen vor.
Zusammenfassung
Eine frühzeitige Diagnose der systemischen Sklerose-bedingten interstitiellen Lungenerkrankung (SSc-ILD) ist wichtig, um eine Behandlung mit minimaler Verzögerung zu ermöglichen. Die Diagnose von SSc-ILD ist jedoch eine Herausforderung, da die Hauptsymptome unspezifisch sind. Die hochauflösende Computertomographie (HRCT) der Brust wird als empfindliche bildgebende Methode zur Diagnose und Bewertung von SSc-ILD anerkannt. Die Exposition von Patienten gegenüber ionisierender Strahlung kann als Einschränkung betrachtet werden, obwohl methodische Schritte unternommen werden können, um dies zu mäßigen. Wir präsentieren praktische Empfehlungen für die Durchführung von HRCT-Scans und die Interpretation der Ergebnisse. Zu den Hauptmerkmalen von SSc-ILD auf HRCT gehört ein unspezifisches interstitielles Pneumonie-Muster (NSIP) mit peripheren Boden-Glas-Trübungen und umfangreicher Traktionsbronchiektasis. Trotz Ähnlichkeiten zwischen SSc-ILD und idiopathischer Lungenfibrose (IPF) kann HRCT verwendet werden, um zwischen diesen Bedingungen zu unterscheiden: Bei SSc-ILD im Vergleich zu IPF gibt es einen größeren Anteil an Bodenglas-Opazität und Fibrose ist weniger grob. Eine erweiterte, luftgefüllte Speiseröhre mit einem Durchmesser von >10 mm, die auf Ösophagusdysmotilität hindeutet, wird häufig in SSc-ILD gesehen. Lungenarteriengröße größer als die angrenzende aufsteigende Aorta deutet auf koexistente pulmonale Hypertonie hin. Knötchen müssen aufgrund des erhöhten Lungenkrebsrisikos überwacht werden. Ein großer Teil der Erkrankung auf HRCT (ca. 20%) oder ein hoher Fibrose-Score deutet auf ein erhöhtes Sterblichkeitsrisiko hin. HRCT ist für die Diagnose von SSc-ILD von zentraler Bedeutung, und serielle Bewertungen können bei der Überwachung des Krankheitsverlaufs oder des Behandlungsreaktionens hilfreich sein.
Einleitung
Systemische Sklerose (SSc) ist eine komplexe, heterogene Autoimmunerkrankung. Es kann als Vaskulopathie manifestiert werden, Raynaud-Phänomen und Fibrose der Haut und inneren Organe1. SSc wird wie folgt in Subtypen eingeteilt: begrenzte sinanöse, diffuse Kutane, Sinussklerodermie (ohne Hautbeteiligung) und SSc-Überlappungssyndrom1.
SSc wird nicht in mendelianischer Mode vererbt, aber genetische Faktoren scheinen die Anfälligkeit für die Krankheit zu beeinflussen. Die Inzidenzraten unterscheiden sich zwischen den ethnischen Gruppen und werden bei Personen mit einer Familiengeschichte der Krankheit erhöht2,3. Auch Umweltrisikofaktoren scheinen zu bestehen, wobei eine hohe Exposition gegenüber Kieselsäure oder organischen Lösungsmitteln das Auftreten von SSc4zu erhöhen scheint. Die weltweite Prävalenz von SSc ist etwa 1 von 10.0001. Mehr Frauen als Männer sind von SSc betroffen, mit gemeldeten Frauen-Männer-Verhältnissen zwischen 3:1 und 8:1, und die Altersgruppe mit der höchsten Inzidenz der Krankheit ist 45-54 Jahre5.
Die Lunge ist das zweithäufigste viszerale Organ bei Patienten mit SSc6. Es gibt zwei Hauptpulmonaden manifestationen von SSc: interstitielle Lungenerkrankung (ILD), und pulmonale Hypertonie7. ILD ist in der Regel fibrotisch; es tritt bei etwa 80% der Patienten mit SSc auf und ist häufiger bei diffusen kutanen Sklerodermie als in der begrenzten Form der Krankheit1,8. Pulmonale Hypertonie kann sich als isolierte pulmonale arterielle Hypertonie (PAH, die eine Prävalenz von 13–35% bei SSc hat) oder pulmonale Hypertonie manifestieren, die durch linksventrikuläre Beteiligung/diastolische Dysfunktion oder ILD/Hypoxämie7resultiert. Antikörperprofile unterscheiden sich zwischen Patienten mit SSc-ILD und Patienten mit SSc-PAH. Zum Beispiel ist das Vorhandensein von Anti-Scl-70-Antikörpern mit SSc-ILD8verbunden, während Antizentrom-Antikörper häufiger bei SSc-Patienten mit PAH auftreten als bei Patienten ohne PAH9.
Die Symptome von SSc-ILD sind Dyspnoe, Husten, Brustschmerzen, und Bewegung Begrenzung. ILD trägt wesentlich zur Morbidität in SSc10,11,12bei. Infolgedessen wurden die jährlichen Gesamtkosten für die Gesundheitsversorgung bei Patienten mit SSc-ILD höher als bei Patienten mit SSc und ohne ILD: 31.285–55.446 USD gegenüber 18.513–23.268 USDbzw. 13.
SSc-ILD ist die hauptursache Mortalität bei Patienten mit SSc, auf die 30–35% der Todesfälle in dieser Gruppe10,14entfallen. Das mediane Überleben bei Patienten mit SSc-ILD wurde berichtet, 5-8 Jahre10,15; zum Vergleich: Etwa 76% der Gesamtbevölkerung mit SSc überleben mehr als 10 Jahre von Krankheitsbeginn16. Signifikante Prädiktoren der Sterblichkeit in SSc-ILD sind Alter, erzwungene Vitalkapazität (FVC), Ausgangsdiffusionskapazität der Lunge für Kohlenmonoxid (DLCO), Krankheitsausmaß bei hochauflösender Computertomographie (HRCT), Vorhandensein von pulmonaler Hypertonie und Kerbs von den Lungren 6 (KL-6) Antigen17,18.
Eine frühzeitige Diagnose ist wichtig, um eine Behandlung mit minimaler Verzögerung zu ermöglichen, und bei Patienten mit einem progressiven Phänotyp kann das Fortschreiten der Erkrankung potenziell verlangsamt werden. Jedoch, Diagnose SSc-ILD ist eine Herausforderung, weil unspezifische Symptome von Husten, Dyspnoe, und Müdigkeit kann mit anderen Aspekten von SSc verwechselt werden, wie Herzerkrankungen und Muskel-Skelett-Beteiligung. Die Auswertungen für die Diagnose von ILDs umfassen: klinische Präsentation, Geschichte, Raucherstatus, Lungenfunktion, Bildgebung und in einigen Fällen Lungenbiopsie. Die Bestätigung der SSc-ILD-Diagnose erfordert mehrere Untersuchungen, die häufig in Kombination19verwendet werden. Die am häufigsten verwendeten Bewertungen umfassen Lungenfunktionstests und HRCT20,21,22,23. Andere bildgebende Verfahren, wie Brustradiographie und strahlungssparende Bildgebung (z.B. Magnetresonanztomographie [MRT], Lungenultraschall) können ebenfalls eingesetzt werden22. Lungenfunktionstests werden verwendet, um den Schweregrad der ILD zu bewerten und ihren Verlauf zu überwachen. Die Verwendung von Lungenfunktionstests allein ist jedoch für die Diagnose von SSc-ILD24,25von begrenztem Nutzen. HRCT der Brust gilt als das empfindlichste nicht-invasive Mittel zur Erleichterung der Differentialdiagnose von SSc-ILD19. Baseline HRCT Ergebnisse, sowie Veränderungen im Laufe der Zeit, können verwendet werden, um den zukünftigen Verlauf der Lungenerkrankung und mögliche Reaktion auf Therapie vorherzusagen26.
Die Exposition gegenüber Strahlung mit HRCT wird manchmal als begrenzender Faktor für regelmäßiges Screening betrachtet27,28; Die Begrenzung der Anzahl der Scheiben ist eine mögliche Methode zur Verringerung des Strahlenrisikos, und die Dosis kann auch reduziert werden, indem entweder die Spannung oder der Strom29,30,31verringert wird. Alternativ können unterschiedliche Bewertungsmethoden in Betracht gezogen werden. Beispielsweise scheint die MRT ein gewisses Potenzial für die Bewertung und Nachbeobachtung von ILD-Patienten zu haben22. In einer Studie mit T2-gewichteten MRT-Bildern mit Atemsynchronisation wurde HRCT parallel als "Gold-Standard"-Bewertung durchgeführt; 100% Empfindlichkeit und 60% Spezifität wurden mit MRT zur Bestimmung des Vorhandenseins von ILD32berichtet. Ähnliche Übereinstimmung zwischen MRT und HRCT bei der Erkennung und Kategorisierung von ILD wurde in einer anderen Studie berichtet33. Trotz der vielversprechenden Ergebnisse ist die MRT derzeit eine Forschungsmethodik und noch nicht für den allgemeinen klinischen Einsatz bereit.
Hier bieten wir einen praktischen Überblick über die Interpretation von bildgebenden Ergebnissen mit Schwerpunkt HRCT, zur Diagnose der Lungenbeteiligung am SSc, zur Bestimmung der Prognose und zur Erforschung zukünftiger Entwicklungen, die bildgebende Methoden und die Interpretation von Ergebnissen verbessern können. HRCT-Bilder aus repräsentativen Fällen sind in dem Papier enthalten.
Protokoll
1. HRCT-Scannen
- Durchführung volumetrischer HRCT-Erfassungsscans der Brust36. Kontrastmittel sind nicht erforderlich36,37.
- Erhalten Sie die folgenden Erfassungen mit Parametern, die in Tabelle 136,37dargestellt sind.
- Erwerben Sie einen supine inspiatorischen Scan (volumetrisch) von der Lunge apices zur Lungenbasis.
- Erwerben Sie einen supine expiratorischen Scan (sequenziell mit 10–20 mm Lücken) von 2 cm unterhalb der Lungenapices bis zur Lungenbasis.
- Erwerben Sie eine anfällige Inspiratorium optional (sequentiell mit 10–20 mm Lücken) von der Karina bis zur Lungenbasis.
- Geben Sie dem Patienten vor jeder Erfassung Atemanweisungen36,37. Für einen inspiratorischen Scan, sagen Sie" Nehmen Sie einen tiefen Atemzug ... und lassen Sie es aus. Nehmen Sie einen weiteren tiefen Atemzug auf ... und lassen Sie es raus. Nehmen Sie einen weiteren tiefen Atemzug auf und halten Sie den Atem an. Halten Sie den Atem an"37.
- Erhalten Sie inspiratory Scans mit voller Inspiration35,36.
- Verwenden Sie die dünnste Kollimation, kürzeste Rotationszeit und höchste Tonhöhe, um sicherzustellen, dass bewegungsfreie Bilder erhalten werden36. Vorgeschlagene Scanparameter sind in Tabelle 137aufgeführt.
- Für eine optimale Qualität der volumetrischen Scans erhalten Sie dünne Schnittbilder (<2 mm) mit hochauflösender Rekonstruktion35,36.
- Überprüfen Sie Scans unmittelbar nach der Erfassung und wiederholen Sie, ob entweder Bewegungsartefakt vorhanden ist oder unzureichende Inspiration aufgetreten ist37.
2. Berichterstattung
- Bereiten Sie einen Interpretationsbericht vor.
- Teilen Sie den Bericht und die HRCT-Bilder mit dem Pflegeteam des Patienten und fügen Sie sie den Krankenakten des Patienten hinzu.
Ergebnisse
Diagnose
Zu den Hauptmerkmalen von SSc-ILD auf HRCT gehört häufig ein unspezifisches interstitielles Pneumonie-Muster (NSIP) mit peripheren Boden-Glas-Trübungen und umfangreicher Traktionsbronchiektasis (Abbildung 1 und Abbildung 2). Boden-Glas-Trübungen haben eine breite Ätiologie und sind oft unspezifisch40,41,42. Zentrale Dominanz oder periphere Verteilung mit subpleuraler Sparsamkeit ist sehr suggestiv für NSIP (Abbildung 3).
In der Regel enthalten ILD-Muster in HRCT-Bildern Reticulationen mit architektonischer Verzerrung, die zu Traktionsbronchiektasis/Bronchiolektase führt (in Übereinstimmung mit einer fibrotischen Form von NSIP). In der Tat Traktion Bronchiektasis und Traktion Bronchiolektasis sind oft die vorherrschenden Merkmale von SSc-ILD (Abbildung 4)43. Weitere Befunde können Waben(Abbildung 5; häufiger in begrenzten Formen von SSc), interlobuläre Septalverdickung und intralobuläre Linien, und Mikronodulde40,44. Honeycombing bezieht sich auf gruppierte zystische Lufträume mit einem typisch konsistenten Durchmesser (ca. 3–10 mm) mit dicken, gut definierten Wänden31. Waben und Traktion Bronchiektasis sind Schlüsselmerkmale der üblichen interstitiellen Lungenentzündung (UIP) auf HRCT. Obwohl dieses Muster am häufigsten mit idiopathischer Lungenfibrose (IPF), dem Prototyp der Fibrosing ILD mit einem progressiven Phänotyp, assoziiert ist, kann es manchmal bei Patienten mit SSc-ILD10gesehen werden. Kürzlich wurden mehrere Anzeichen bei Patienten mit Bindegewebskrankheit ilD (einschließlich SSc-ILD) und das UIP-Muster auf HRCT identifiziert, aber nicht bei Patienten mit IPF. Dies sind das gerade Randzeichen (d.h. die Isolierung der Fibrose zu den Lungenbasen mit scharfer Abgrenzung in der Kranichadtebene ohne wesentliche Ausdehnung entlang der seitlichen Ränder der Lunge auf koronalen Bildern), das wabenhaltende vorherrschende (oder überschwängliche) Zeichen (>70% der fibrotischen Teile der Lunge) und das vordere obere Lappenzeichen (d.h., Konzentration der Fibrose im vorderen Aspekt der oberen Lappen, mit relativer Sparsamkeit der anderen Aspekte der oberen Lappen, und gleichzeitige Unterlappenbeteiligung)45. Das gerade Kantenzeichen wurde auch mit DerNSIP-Pathologie46assoziiert, das ist das wichtigste CT-Muster in SSc-ILD10.
Dilatierte luftgefüllte Speiseröhre wird häufig bei Patienten mit SSc (Abbildung 6)47,48,49 und bei Patienten mit SSc-ILD47,48beobachtet. Zwar gibt es keine akzeptierte obere Altersgrenze, bei der eine erweiterte Speiseröhre nicht mehr helfen kann, SSc-ILD und IPF zu unterscheiden, aber eine erweiterte Speiseröhre kann bei Patienten über 65 Jahren aufgrund der zunehmenden Inzidenz von Ösophagus-Motilitätsstörungen schwieriger zu interpretieren sein. Die mediadine Lymphadenopathie (in der Regel reaktiv), bei der die kurze Achse des Lymphknotens 10 mm überschreitet, wird häufig auch bei Patienten mit SSc-ILD47,50beobachtet. Lungenarteriengröße größer als die angrenzende aufsteigende Aorta deutet auf koexistierende pulmonale Hypertonie hin (Abbildung 6), auch bei Patienten ohne fibrotische Lungenerkrankung51,52,53. Konsolidierungsbereiche deuten auf überlagerte Infektionen, Aspirationen, Die Organisation von Lungenentzündungen, Blutungen oder Malignitäten hin. Knötchen müssen aufgrund des erhöhten Risikos für Lungenkrebs in SSc-ILD7überwacht werden; der häufigste primäre Krebs bei Patienten mit SSc-ILD ist Adenokarzinom7,54.
SSc-ILD hat eine Reihe klinischer, mechanistischer und pathologischer Ähnlichkeiten mit IPF15,55. Einige radiologische Merkmale erlauben jedoch die Differenzierung dieser beiden ILDs15,45. In SSc-ILD, im Vergleich zu IPF, gibt es einen größeren Anteil an Bodenglas Opazität und Fibrose ist weniger grob. In Fällen von UIP in SSc, Waben können in mehr als 70% des fibrotischen-Lungengewebes beobachtet werden - das überschwängliche Wabenzeichen56,57. Darüber hinaus ist das Vier-Ecken-Zeichen (auch bekannt als das vordere obere Lappenzeichen) bei SSc-ILD deutlich häufiger als in IPF; Dies ist ein Muster der Entzündung und/oder Fibrose fokal oder überproportional mit den bilateralen anterolateralen oberen Lappen und posterosuperior unteren Lappen58.
Bruströntgenbilder können zunächst ILD erkennen; Sie bieten jedoch nicht genügend Kontrastauflösung für eine zuverlässige Diagnose. In Bruströntgenaufnahmen von Patienten mit SSc-ILD ist das häufigste Muster die basale vorherrschende Retikulierung59. Weitere Merkmale können sichtbare Bronchiektase, Volumenverlust und Waben sein. Wie bei HRCT kann das Vorhandensein einer erweiterten luftgefüllten Speiseröhre bei der Diagnose von SSc-ILD47hilfreich sein.
Prognose
Es hat sich gezeigt, dass mehrere verschiedene bildgebende Befunde mit der Prognose bei SSc-ILD in Verbindung gebracht werden. Es wurde berichtet, dass das Mortalitätsrisiko bei Patienten mit einem Krankheitsgrad von mindestens 20 % des HRCT höher ist (das 10-Jahres-Überleben betrug 43 % gegenüber 67 % bei Patienten mit einem Krankheitsausdehnung über der Schwelle von 20 %)60. In ähnlicher Weise wurde ein hoher Fibrose-Score auf HRCT (basierend auf dem Ausmaß der Reticulation und Waben) mit einer erhöhten Sterblichkeit in Verbindung gebracht61. Große Speiseröhrendurchmesser sind mit einem erhöhten ILD-Schweregrad und einer verringerten DLCO48verbunden. Lungendichte und Lungenarteriendurchmesser können potenziell verwendet werden, um das Risiko einer pulmonalen Hypertonie zu prognostizieren62. Computergestützte, quantitative CT-Parameter könnten auch genutzt werden, um das Risiko von Lungenfunktionsverlust oder Mortalität zu identifizieren. Eine Studie legte nahe, dass das Ausmaß der ILD, quantifiziert von HRCT, verwendet werden könnte, um den Rückgang der FVC über 12 Monatevorherzusagen 63. In einer anderen Studie lieferten quantitative CT-Parameter der Brust Mortalitätsrisikoergebnisse, die mit den klinischen Vorhersagemodellen64übereinstimmten. Trotz ihres scheinbaren Potenzials werden bildgebende Biomarker derzeit am besten auf Populationsebene betrachtet, da ihr klinischer Nutzen bei einzelnen Patienten nicht nachgewiesen wurde.
Behandlungsreaktion
Cyclophosphamid und Mycophenolatmofetil bieten bei Patienten mit SSc-ILD einen bescheidenen Nutzen. In der wegweisenden Scleroderma Lung Studie I führte die Cyclophosphamid-Behandlung zu einer langsameren Progression der Fibrose im Vergleich zu Placebo65. In jüngerer Zeit berichtete die Scleroderma Lung Study II über eine ähnliche Wirksamkeit und verbesserte Verträglichkeit mit Mycophenolatmofetil im Vergleich zu Cyclophosphamid66. Es besteht jedoch nach wie vor Bedarf an verbesserten Behandlungsmöglichkeiten für Patienten mit SSc-ILD. Zu den derzeit untersuchten Therapien gehören monoklonale Antikörper (z. B. Rituximab, Abituzumab), Antifibrotika (z. B. Nintedanib, Pirfenidon), der direkte Thrombininhibitor Dabigatran, der Proteasome-Hemmer Bortezomib und die hämatopoetische Stammzelltransplantation19,67.
Serielle HRCT-Scans, die das Fortschreiten der Erkrankung bei einem Patienten mit SSc-ILD
HRCT-Bewertungen, die zu verschiedenen Zeitpunkten durchgeführt werden, können zur Untersuchung des Krankheitsverlaufs verwendet werden. Abbildung 7 zeigt zwei Sätze von hrCT-Bildern der axialen und koronalen Brust, die 10 Jahre voneinander entfernt bei einem Patienten mit SSc-ILD aufgenommen wurden. Die anfänglichen axialen und koronalen Bilder (Abbildung 7A,B) aus der Brust HRCT zeigen basilar vorherrschende Boden-Glas-Opazität und Reticulation mit leichter Traktion Bronchiektase und subpleurale Sparsamkeit im Einklang mit NSIP bei diesem Patienten mit SSc. Der letztgenannte Bildsatz (Abbildung 7C, D), aufgenommen 10 Jahre später, zeigt eine erhöhte Retikulierung und Traktionbronchiolektase an den Lungenbasen mit Abnahme der Boden-Glas-Opazität auf axialen und koronalen (Abbildung 7C,D) Bilder aus Brust-CT, die mit einer leichten Verschlechterung der Lungenfibrose übereinstimmen. Serielle HRCT-Scans können auch verwendet werden, um das Behandlungsverhalten68,69,70zuüberwachen; Dies wurde in der Scleroderma Lung Study II nachgewiesen, in der computergestützte Diagnoseergebnisse auf Basis von HRCT-Scans verwendet wurden, um die Wirksamkeit von Cyclophosphamid mit Mycophenolatmofetil bei Patienten mit SSc-ILD68zu vergleichen.
| Phase | Detektor kollimation | Spannung (kV) | Strom (mAs) | Scan Intervall | Pitch | Drehung | Rohrstrom Modulation |
| Supine inspiratory | Helical 1,2 mm | 120 (kann abgesenkt werden) | 230 (kann abgesenkt werden) | N/A | 1,0 € | 0,5 Sekunden oder schneller | Auf |
| Supine expiratory | Axial 2 x 1,0 mm | 120 | 150 | 20 mm | N/A | 1,0 Sekunden | Auf |
| Prone inspiratory | Axial 2 x 1,0 mm | 120 | 150 | 20 mm | N/A | 1,0 Sekunden | Auf |
Tabelle 1: Erfassungsparameter für Computertomographie37. N/A = nicht anwendbar.
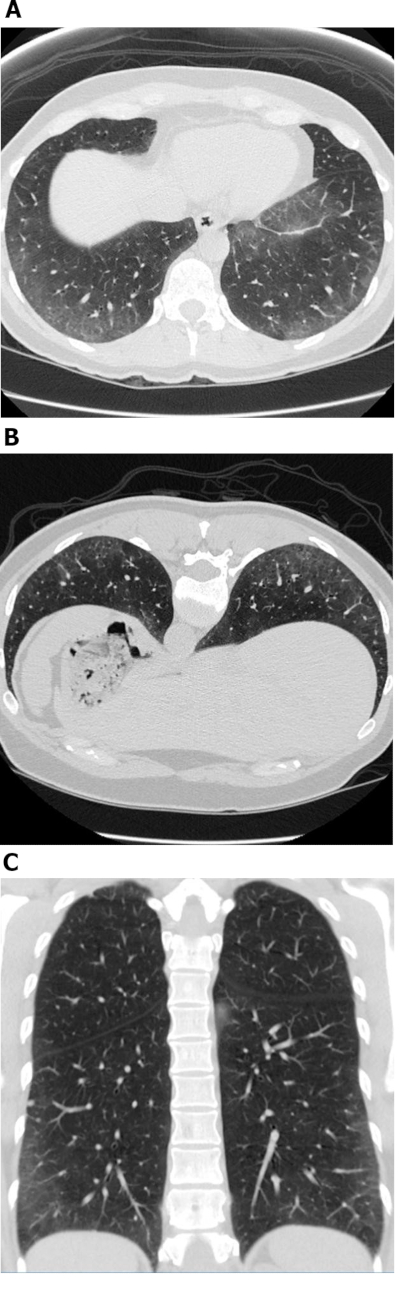
Abbildung 1:Systemische Sklerose mit einem zellulären NSIP-Muster der Krankheit. Axiale (A), anfällige (B) und koronare (C) hochauflösende Computertomographiebilder zeigen alle umfangreiche periphere und basale vorherrschende Boden-Glas-Trübungen; dies sind typische Beobachtungen mit NSIP. Der Mangel an Traktion Bronchiektasis ist ein Hinweis auf ein zelluläres NSIP-Muster der Krankheit. NSIP = unspezifische interstitielle Lungenentzündung. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
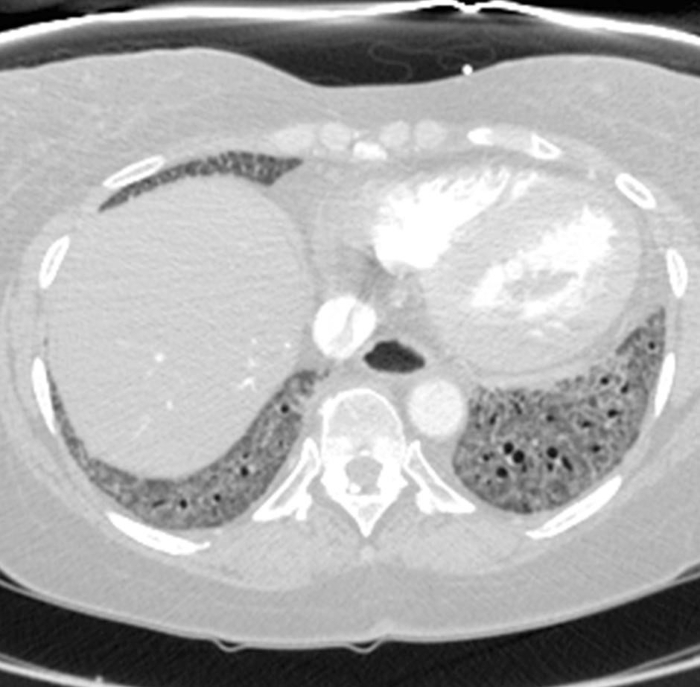
Abbildung 2:Systemische Sklerose mit einem fibrotischen nicht-spezifischen interstitiellen Lungenentzündungsmuster der Krankheit. Axiale Computertomographie zeigt umfangreiche, basal-vorherrschende Boden-Glas-Trübungen mit zugehöriger Traktionsbronchiektasis. Bemerkenswert ist, dass die Speiseröhre eine ausgeprägte Dilatation zeigt; dies ist typisch für Sklerodermie. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
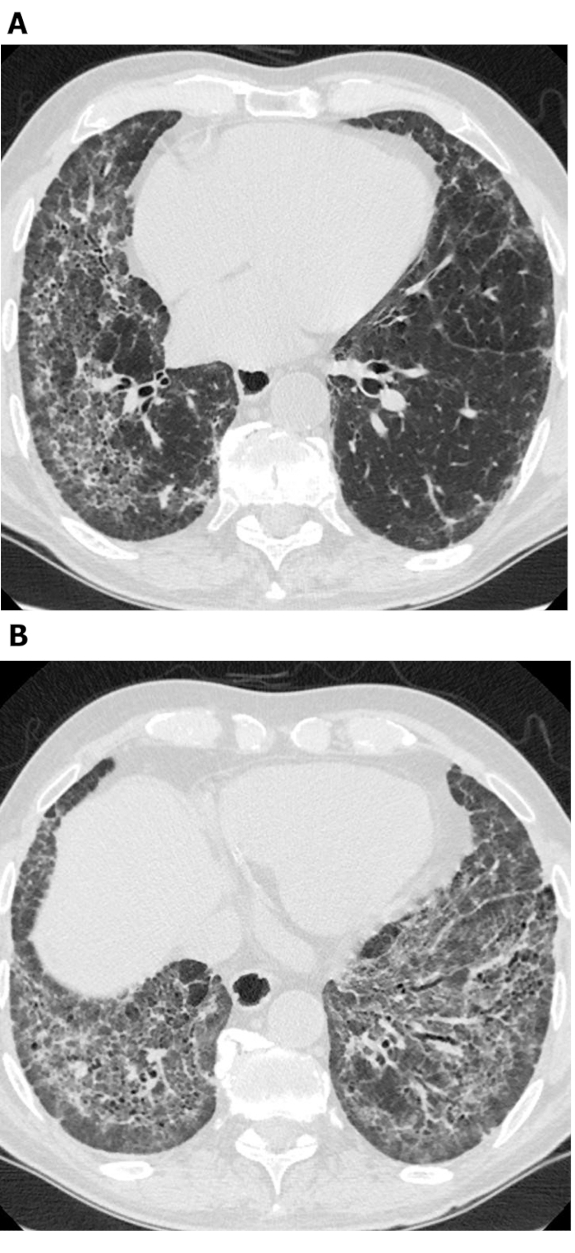
Abbildung 3:Systemische Sklerose mit einem fibrotischen NSIP-Muster. Axiale hochauflösende Computertomographiebilder (A und B) zeigen umfangreiche Boden-Glas-Trübungen, Reticulation, architektonische Verzerrung und Traktionsbronchiektasis. Bemerkenswert ist, subpleurale Sparsamung ist offensichtlich; Dies ist typisch für NSIP und wird in etwa 50% aller Fälle gesehen. NSIP = unspezifische interstitielle Lungenentzündung. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
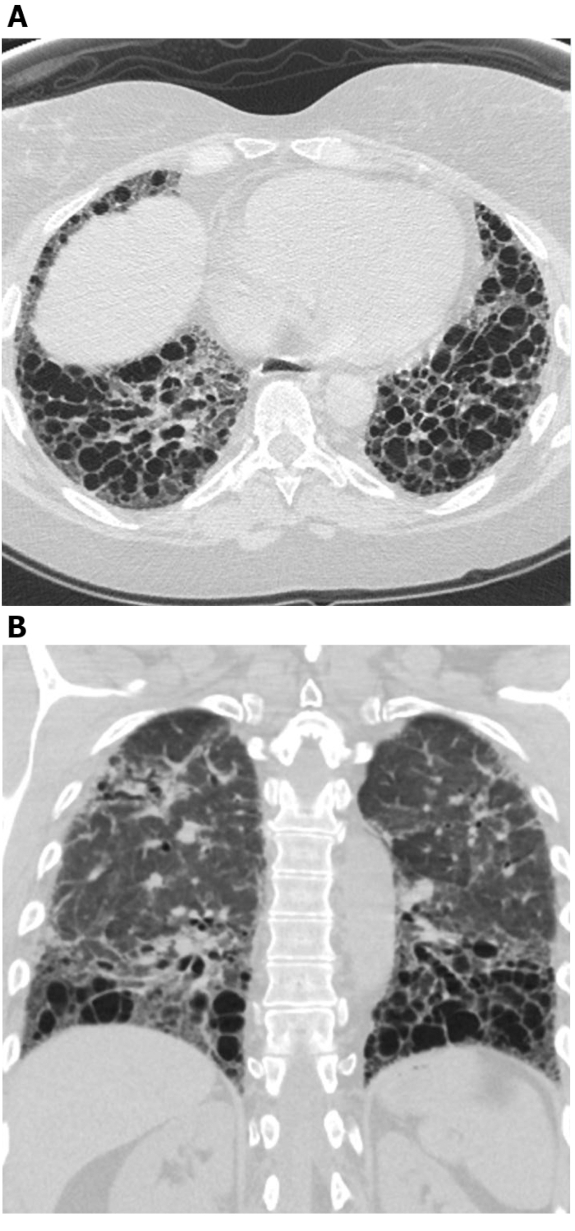
Abbildung 4: Systemische Sklerose mit überschwänglicher Traktionsbronchiektasis. Axiale (A) und koronare (B) hochauflösende Computertomographiebilder zeigen eine ausgedehnte mittlere und untere Lungenzone, die die Traktionsbronchiektasis dominiert. Während dies mit Waben verwechselt werden kann, verbinden sich die zystischen Bereiche miteinander und schonen die unmittelbare subpleurale Lunge; dies ist typisch für Bronchiektase. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
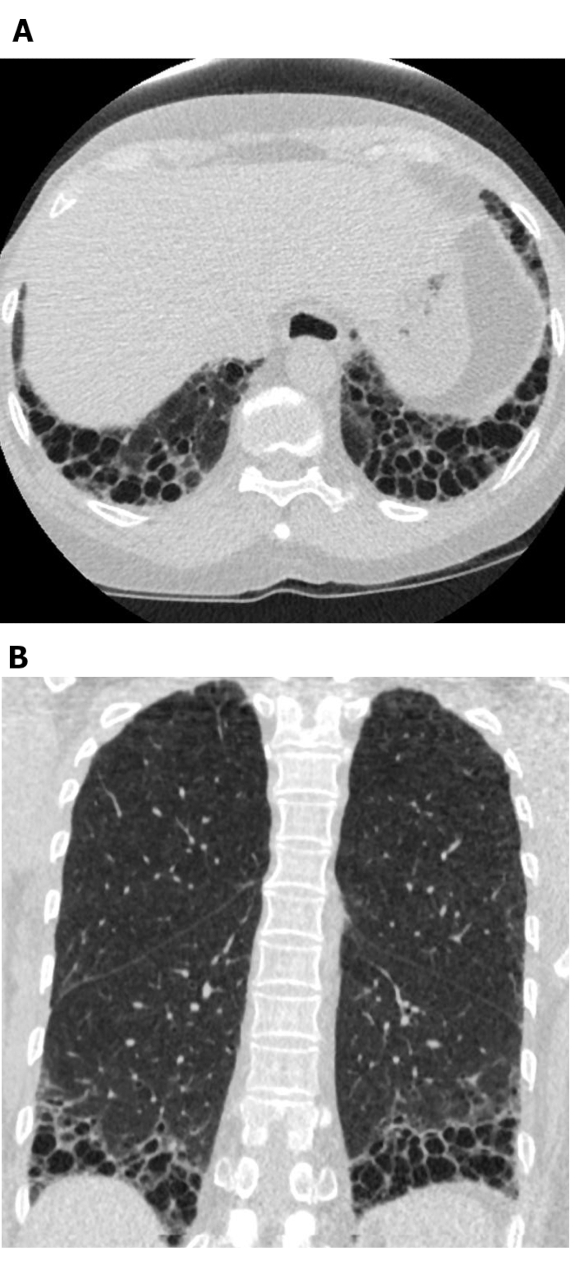
Abbildung 5: Systemische Sklerose mit einem UIP-Muster der Lungenfibrose. Axiale (A) und koronare (B) Computertomographiebilder zeigen periphere und basale vorherrschende Waben- und Traktionsbronchiektase im Einklang mit dem typischen UIP-Muster der Lungenfibrose. Beachten Sie die erweiterte Speiseröhre (zurechenbar durch Sklerodermie) und die "überschwängliche" Waben (suggestiv für ILD im Zusammenhang mit Bindegewebserkrankungen anstelle idiopathischer Lungenfibrose). UIP = übliche interstitielle Lungenentzündung. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
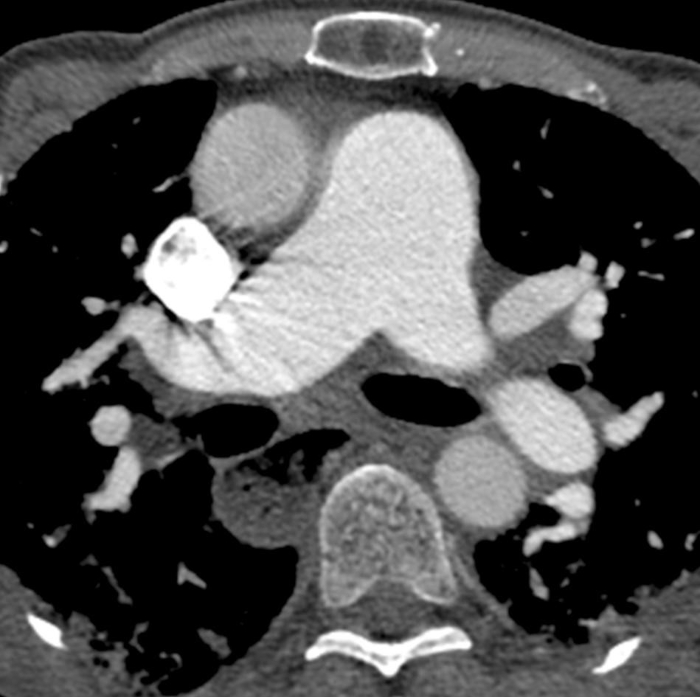
Abbildung 6: Systemische Sklerose mit pulmonaler Hypertonie und erweiterter Speiseröhre. Die kontrastreiche Brust-Computertomographie zeigt eine deutliche Vergrößerung des Lungenstammes mit einer größeren Messung als die angrenzende aufsteigende Aorta, die auf eine zugrunde liegende pulmonale Hypertonie hindeutet. Die Speiseröhre ist deutlich erweitert; dies ist auf skleroderma zurückzuführen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
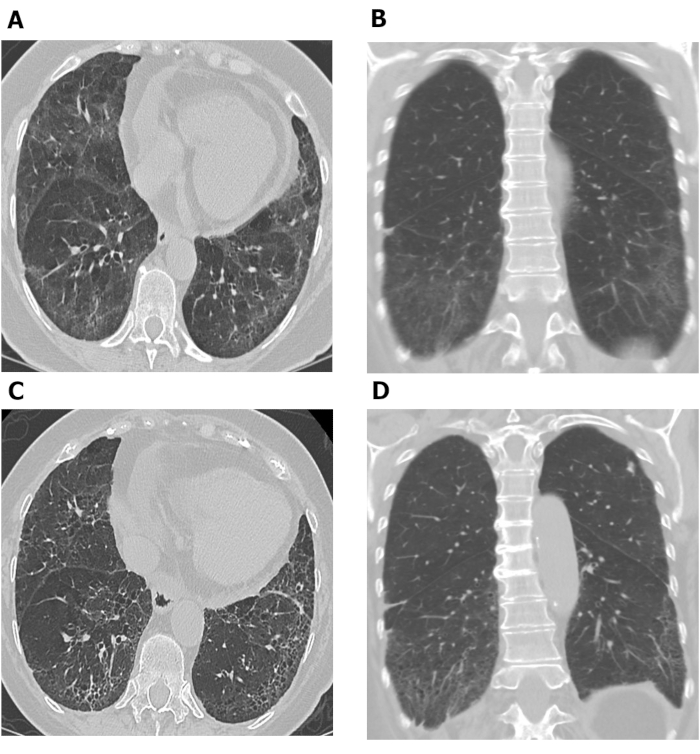
Abbildung 7: HrCT-Bilder der seriellen Brust zeigen das Fortschreiten der Lungenfibrose bei Patienten mit SSc-ILD. Axiale (A) und koronare (B) Bilder aus der Brust HRCT zeigen Basilar vorherrschende Boden-Glas-Opazität und Reticulation mit leichter Traktion Bronchiektasis und subpleurale Sparsamkeit im Einklang mit unspezifischen interstitiellen Lungenentzündung bei diesem Patienten mit SSc. Nach 10 Jahren werden erhöhte Reticulation und Traktion Bronchiolektasie an den Lungenbasen mit Abnahme der Boden-Glas-Opazität auf axialen (C) und koronalen (D) Brust HRCT-Bildern beobachtet, die mit einer leichten Verschlechterung der Lungenfibrose übereinstimmen. HRCT = hochauflösende Computertomographie; SSc-ILD = systemische Sklerodermie-assoziierte interstitielle Lungenerkrankung. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Diskussion
Während HRCT derzeit die definitive bildgebende Methode zur Diagnose und Bewertung von SSc-ILD ist, verwendet es ionisierende Strahlung und ist relativ teuer. Bruströntgenaufnahmen können stattdessen durchgeführt werden, obwohl diese die Differentialdiagnose nicht im gleichen Maße wie HRCT erleichtern, und ein normaler Bruströntgengraph schließt die Möglichkeit einer ILD nicht aus. Die vielleicht beste Verwendung von Bruströntgenbildern ist die Überwachung auf fortschreitende Krankheiten zwischen HRCT-Scans und auf den Ausschluss von erschwerenden Krankheiten, wie infektionseuchen, bei der Einstellung einer akuten Verschlechterung der Symptome.
Eine wahrgenommene Einschränkung von HRCT ist die Strahlenexposition. Wie bereits beschrieben, können neue Methoden zur Durchführung von CT-Scans eine Verringerung der Strahlenexposition31ermöglichen, und darüber hinaus bieten aktuelle CT-Scanner eine Reihe fortschrittlicher Techniken, die in Zukunft die Möglichkeit bieten, die Strahlenexposition auf fast Bruströntgenwerte zu senken. Alternativ könnten bildgebende Verfahren wie MRT oder Lungen-Ultraschall verwendet werden, um zu vermeiden, dass der Patient in Zukunft einer Strahlung aussetzt32,71,72,73. Wir glauben, dass es zwar Mitnutzenüberlegungen im Zusammenhang mit der bildgebenden Nutzung gibt, die Vorteile der CT in der Diagnose und im Patientenmanagement jedoch die potenziellen Risiken bei weitem überwiegen.
Bildgebende Daten, insbesondere HRCT, liefern die wohl wichtigsten Informationen, um die Diagnose von SSc-ILD zu ermöglichen. Eine detaillierte Betrachtung der Muster und Merkmale von HRCT-Scans reicht in der Regel aus, um SSc-ILD von anderen Lungenerkrankungen zu unterscheiden, mit dem Vorteil, dass ein invasives Biopsieverfahren vermieden werden muss.
Die visuelle Bewertung von HRCT-Scans führt zu einem gewissen Maß an Subjektivität und der Möglichkeit einer Inter-Observer-Variabilität. Computergestützte Methoden der HRCT-Scaninterpretation wurden als möglicher Ansatz zur Verbesserung der Genauigkeit63,74untersucht. Beispielsweise können quantitative Ansätze zur Beurteilung von Lungenfibrose oder des Ausmaßes der Erkrankung verwendet werden, um das Behandlungsverhalten68,70,75zu bewerten. Jedoch, Diese Methoden sind nicht weit verbreitet in der täglichen klinischen Praxis zu diesem Zeitpunkt verwendet.
Wir hoffen, dass die in diesem Manuskript vorgestellten Informationen als praktischer Leitfaden dienen werden, um Ärzte bei der Verwendung von HRCT-Scans zur Diagnose von SSc-ILD und zur Bestimmung der Prognose zu unterstützen. Verbesserte Methoden zur Bildgewinnung und zum Interpretieren von Scans haben das Potenzial, die Strahlenexposition der Patienten zu reduzieren und die diagnostische/prognostische Genauigkeit zu verbessern.
Offenlegungen
Jonathan Chung erklärt keine potenziellen Interessenkonflikte in Bezug auf die beschriebene Recherche, Urheberschaft und/oder Veröffentlichung dieses Artikels; Christopher Walker erklärt den Erhalt von Tantiemen von Amirsys (Elsevier); und Stephen Hobbs erklärt den Erhalt von Lizenzgebühren von Elsevier und Wolters Kluwer Health. Open Access Veröffentlichung dieses Artikels wird gesponsert von Boehringer Ingelheim Pharmaceuticals, Inc.
Die Autoren erfüllen die vom International Committee of Medical Journal Editors (ICMJE) empfohlenen Kriterien für die Urheberschaft. Die Autoren erhielten keine direkte Entschädigung im Zusammenhang mit der Entwicklung des Videos. Unterstützung für das Videoskript erhielt Leon Newman, PhD, von GeoMed, einer Firma aus Ashfield, die von Boehringer Ingelheim Pharmaceuticals, Inc. (BIPI) beauftragt und finanziert wurde. BIPI erhielt die Gelegenheit, das endgültige Video auf medizinische und wissenschaftliche Genauigkeit sowie Aspekte des geistigen Eigentums zu überprüfen.
Danksagungen
Die Autoren erfüllen die vom International Committee of Medical Journal Editors (ICMJE) empfohlenen Kriterien für die Urheberschaft. Die Autoren erhielten keine direkte Entschädigung im Zusammenhang mit der Entwicklung des Manuskripts. Die schriftliche Unterstützung erfolgte durch Ken Sutor, BSc, von GeoMed, einem Unternehmen aus Ashfield, das teil der UDG Healthcare plc ist und von Boehringer Ingelheim Pharmaceuticals, Inc. (BIPI) beauftragt und finanziert wurde. BIPI erhielt die Gelegenheit, das Manuskript auf medizinische und wissenschaftliche Genauigkeit sowie auf Aspekte des geistigen Eigentums zu überprüfen.
Materialien
| Name | Company | Catalog Number | Comments |
| CT scanners | Philips | NA | Multiple |
Referenzen
- Denton, C. P., Khanna, D. Systemic sclerosis. Lancet. 390 (10103), 1685-1699 (2017).
- Arnett, F. C., et al. Familial occurrence frequencies and relative risks for systemic sclerosis (scleroderma) in three United States cohorts. Arthritis & Rheumatism. 44 (6), 1359-1362 (2001).
- Barnes, J., Mayes, M. D. Epidemiology of systemic sclerosis: incidence, prevalence, survival, risk factors, malignancy, and environmental triggers. Current Opinion in Rheumatology. 24 (2), 165-170 (2012).
- Marie, I., Gehanno, J. F. Environmental risk factors of systemic sclerosis. Seminars in Immunopathology. 37 (5), 463-473 (2015).
- Silman, A. J. Epidemiology of scleroderma. Annals of the Rheumatic Diseases. 50, 846-853 (1991).
- Scholand, M. B., et al. Interstitial lung disease in systemic sclerosis: diagnosis and management. Rheumatology. 1, 008 (2012).
- Solomon, J. J., et al. Scleroderma lung disease. European Respiratory Review. 22 (127), 6-19 (2013).
- Walker, U. A., et al. Clinical risk assessment of organ manifestations in systemic sclerosis: a report from the EULAR Scleroderma Trials And Research group database. Annals of the Rheumatic Diseases. 66 (6), 754-763 (2007).
- Hinchcliff, M., Fischer, A., Schiopu, E., Steen, V. D., Investigators, P. Pulmonary hypertension assessment and recognition of outcomes in scleroderma (PHAROS): baseline characteristics and description of study population. The Journal of Rheumatology. 38 (10), 2172-2179 (2011).
- Giacomelli, R., et al. Interstitial lung disease in systemic sclerosis: current and future treatment. Rheumatology International. 37 (6), 853-863 (2017).
- Sanchez-Cano, D., et al. Interstitial lung disease in systemic sclerosis: data from the spanish scleroderma study group. Rheumatology International. 38 (3), 363-374 (2018).
- Silver, K. C., Silver, R. M. Management of systemic-sclerosis-associated interstitial lung disease. Rheumatic Diseases Clinics of North America. 41 (3), 439-457 (2015).
- Fischer, A., Kong, A. M., Swigris, J. J., Cole, A. L., Raimundo, K. All-cause healthcare costs and mortality in patients with systemic sclerosis with lung involvement. The Journal of Rheumatology. 45 (2), 235-241 (2018).
- Tyndall, A. J., et al. Causes and risk factors for death in systemic sclerosis: a study from the EULAR Scleroderma Trials and Research (EUSTAR) database. Annals of the Rheumatic Diseases. 69 (10), 1809-1815 (2010).
- Herzog, E. L., et al. Review: interstitial lung disease associated with systemic sclerosis and idiopathic pulmonary fibrosis: how similar and distinct. Arthritis & Rheumatology. 66 (8), 1967-1978 (2014).
- Rubio-Rivas, M., Royo, C., Simeon, C. P., Corbella, X., Fonollosa, V. Mortality and survival in systemic sclerosis: systematic review and meta-analysis. Seminars in Arthritis and Rheumatism. 44 (2), 208-219 (2014).
- Stock, C., et al. Serum KL-6 as a marker of disease progression in SSc-ILD. European Respiratory Journal. 52, (2018).
- Winstone, T. A., et al. Predictors of mortality and progression in scleroderma-associated interstitial lung disease: a systematic review. Chest. 146 (2), 422-436 (2014).
- Khanna, D., et al. Ongoing clinical trials and treatment options for patients with systemic sclerosis-associated interstitial lung disease. Rheumatology (Oxford). 58 (4), 567-579 (2019).
- Behr, J., Furst, D. E. Pulmonary function tests. Rheumatology (Oxford). 47, 65-67 (2008).
- Hax, V., et al. Clinical algorithms for the diagnosis and prognosis of interstitial lung disease in systemic sclerosis. Seminars in Arthritis and Rheumatism. 47 (2), 228-234 (2017).
- Molberg, O., Hoffmann-Vold, A. M. Interstitial lung disease in systemic sclerosis: progress in screening and early diagnosis. Current Opinion in Rheumatology. 28 (6), 613-618 (2016).
- Raghu, G., Goldman, L., Schafer, A. I. Interstital lung disease. Goldman-Cecil Medicine. , 575-588 (2016).
- Showalter, K., et al. Performance of forced vital capacity and lung diffusion cutpoints for associated radiographic interstitial lung disease in systemic sclerosis. The Journal of Rheumatology. 45 (11), 1572-1576 (2018).
- Suliman, Y. A., et al. Brief report: pulmonary function tests: high rate of false-negative results in the early detection and screening of scleroderma-related interstitial lung disease. Arthritis & Rheumatology. 67 (12), 3256-3261 (2015).
- Roth, M. D., et al. Predicting treatment outcomes and responder subsets in scleroderma-related interstitial lung disease. Arthritis & Rheumatology. 63 (9), 2797-2808 (2011).
- Kalra, M. K., Maher, M. M., Rizzo, S., Kanarek, D., Shepard, J. A. Radiation exposure from chest CT: issues and strategies. Journal of Korean Medical Science. 19 (2), 159-166 (2004).
- Siegel, J. A., Pennington, C. W., Sacks, B., Welsh, J. S. The birth of the illegitimate linear no-threshold model: an invalid paradigm for estimating risk following low-dose radiation exposure. American Journal of Clinical Oncology. 41 (2), 173-177 (2018).
- Frauenfelder, T., et al. Screening for interstitial lung disease in systemic sclerosis: performance of high-resolution CT with limited number of slices: a prospective study. Annals of the Rheumatic Diseases. 73 (12), 2069-2073 (2014).
- Kubo, T., et al. Radiation dose reduction in chest CT: a review. American Journal of Roentgenology. 190 (2), 335-343 (2008).
- Nguyen-Kim, T. D. L., et al. The impact of slice-reduced computed tomography on histogram-based densitometry assessment of lung fibrosis in patients with systemic sclerosis. Journal of Thoracic Disease. 10 (4), 2142-2152 (2018).
- Muller, C. S., Warszawiak, D., Paiva, E. D. S., Escuissato, D. L. Pulmonary magnetic resonance imaging is similar to chest tomography in detecting inflammation in patients with systemic sclerosis. Revista Brasileira de Reumatologia English Edition. 57 (5), 419-424 (2017).
- Pinal-Fernandez, I., et al. Fast 1.5 T chest MRI for the assessment of interstitial lung disease extent secondary to systemic sclerosis. Clinical Rheumatology. 35 (9), 2339-2345 (2016).
- Sverzellati, N. Highlights of HRCT imaging in IPF. Respiratory Research. 14, 3 (2013).
- Lynch, D. A., et al. Diagnostic criteria for idiopathic pulmonary fibrosis: a Fleischner Society White Paper. The Lancet Respiratory Medicine. 6 (2), 138-153 (2018).
- Raghu, G., et al. Diagnosis of idiopathic pulmonary fibrosis. An official ATS/ERS/JRS/ALAT clinical practice guideline. American Journal of Respiratory and Critical Care Medicine. 198 (5), 44-68 (2018).
- . Exam: CT thorax for interstitial lung disease Available from: https://www.pulmonaryfibrosis.org/docs/default-source/medical-community-documents/ct-chest-for-ild-protocol.pdf?sfvrsn=0 (2019)
- Doyle, T. J., Hunninghake, G. M., Rosas, I. O. Subclinical interstitial lung disease: why you should care. American Journal of Respiratory and Critical Care Medicine. 185 (11), 1147-1153 (2012).
- Peroni, D. G., Boner, A. L. Atelectasis: mechanisms, diagnosis and management. Paediatric Respiratory Reviews. 1 (3), 274-278 (2000).
- Branley, H. M. Pulmonary fibrosis in systemic sclerosis: diagnosis and management. Respiratory Medicine CME. 3, 10-14 (2010).
- Engeler, C. E., Tashjian, J. H., Trenkner, S. W., Walsh, J. W. Ground-glass opacity of the lung parenchyma: a guide to analysis with high-resolution CT. American Journal of Roentgenology. 160 (2), 249-251 (1993).
- Goldin, J. G., et al. High-resolution CT scan findings in patients with symptomatic scleroderma-related interstitial lung disease. Chest. 134 (2), 358-367 (2008).
- Strollo, D., Goldin, J. Imaging lung disease in systemic sclerosis. Current Rheumatology Reports. 12 (2), 156-161 (2010).
- Pandey, A. K., et al. Significance of various pulmonary and extrapulmonary abnormalities on HRCT of the chest in scleroderma lung. Indian Journal of Radiology and Imaging. 23 (4), 304-307 (2013).
- Chung, J. H., et al. CT Features of the usual interstitial pneumonia pattern: differentiating connective tissue disease-associated interstitial lung disease from idiopathic pulmonary fibrosis. American Journal of Roentgenology. 210 (2), 307-313 (2018).
- Zhan, X., et al. Differentiating usual interstitial pneumonia from nonspecific interstitial pneumonia using high-resolution computed tomography: the "Straight-edge Sign". Journal of Thoracic Imaging. 33 (4), 266-270 (2018).
- Farrokh, D., Abbasi, B., Fallah-Rastegar, Y., Mirfeizi, Z. The extrapulmonary manifestations of systemic sclerosis on chest high resolution computed tomography. Tanaffos. 14 (3), 193-200 (2015).
- Salaffi, F., et al. Relationship between interstitial lung disease and oesophageal dilatation on chest high-resolution computed tomography in patients with systemic sclerosis: a cross-sectional study. La Radiologia Medica. 123 (9), 655-663 (2018).
- Vonk, M. C., et al. Oesophageal dilatation on high-resolution computed tomography scan of the lungs as a sign of scleroderma. Annals of the Rheumatic Diseases. 67 (9), 1317-1321 (2008).
- Chowaniec, M., Skoczynska, M., Sokolik, R., Wiland, P. Interstitial lung disease in systemic sclerosis: challenges in early diagnosis and management. Reumatologia. 56 (4), 249-254 (2018).
- McCall, R. K., Ravenel, J. G., Nietert, P. J., Granath, A., Silver, R. M. Relationship of main pulmonary artery diameter to pulmonary arterial pressure in scleroderma patients with and without interstitial fibrosis. Journal of Computer Assisted Tomography. 38 (2), 163-168 (2014).
- Pandey, A. K., et al. Predictors of pulmonary hypertension on high-resolution computed tomography of the chest in systemic sclerosis: a retrospective analysis. Canadian Association of Radiologists Journal. 61 (5), 291-296 (2010).
- Raymond, T. E., Khabbaza, J. E., Yadav, R., Tonelli, A. R. Significance of main pulmonary artery dilation on imaging studies. Annals of the American Thoracic Society. 11 (10), 1623-1632 (2014).
- Colaci, M., et al. Lung cancer in scleroderma: results from an Italian rheumatologic center and review of the literature. Autoimmunity Reviews. 12 (3), 374-379 (2013).
- Distler, O., et al. Design of a randomised, placebo-controlled clinical trial of nintedanib in patients with systemic sclerosis-associated interstitial lung disease (SENSCIS). Clinical and Experimental Rheumatology. 35 (4), 75-81 (2017).
- Desai, S. R., et al. CT features of lung disease in patients with systemic sclerosis: comparison with idiopathic pulmonary fibrosis and nonspecific interstitial pneumonia. Radiology. 232 (2), 560-567 (2004).
- Mira-Avendano, I., et al. Interstitial lung disease and other pulmonary manifestations in connective tissue diseases. Mayo Clinic Proceedings. 94 (2), 309-325 (2019).
- Walkoff, L., White, D. B., Chung, J. H., Asante, D., Cox, C. W. The four corners sign: a specific imaging feature in differentiating systemic sclerosis-related interstitial lung disease from idiopathic pulmonary fibrosis. Journal of Thoracic Imaging. 33 (3), 197-203 (2018).
- Kotnur, M. R., Suresh, P., Reddy, V. S., Sharma, T., Salim, N. A. Systemic sclerosis with multiple pulmonary manifestations. Journal of Clinical & Diagnostic Research. 10 (6), 16-17 (2016).
- Goh, N. S., et al. Interstitial lung disease in systemic sclerosis: a simple staging system. American Journal of Respiratory and Critical Care Medicine. 177 (11), 1248-1254 (2008).
- Takei, R., et al. Radiographic fibrosis score predicts survival in systemic sclerosis-associated interstitial lung disease. Respirology. 23 (4), 385-391 (2018).
- Bakker, M. E., et al. Lung density and pulmonary artery diameter are predictors of pulmonary hypertension in systemic sclerosis. Journal of Thoracic Imaging. 32 (6), 391-397 (2017).
- Khanna, D., et al. Predictors of lung function decline in scleroderma-related interstitial lung disease based on high-resolution computed tomography: implications for cohort enrichment in systemic sclerosis-associated interstitial lung disease trials. Arthritis Research & Therapy. 17, 372 (2015).
- Ariani, A., et al. Quantitative chest computed tomography is associated with two prediction models of mortality in interstitial lung disease related to systemic sclerosis. Rheumatology (Oxford). 56 (6), 922-927 (2017).
- Goldin, J., et al. Treatment of scleroderma-interstitial lung disease with cyclophosphamide is associated with less progressive fibrosis on serial thoracic high-resolution CT scan than placebo: findings from the scleroderma lung study. Chest. 136 (5), 1333-1340 (2009).
- Tashkin, D. P., et al. Mycophenolate mofetil versus oral cyclophosphamide in scleroderma-related interstitial lung disease (SLS II): a randomised controlled, double-blind, parallel group trial. The Lancet Respiratory Medicine. 4 (9), 708-719 (2016).
- Distler, O., et al. Nintedanib for Systemic Sclerosis-Associated Interstitial Lung Disease. New England Journal of Medicine. 380, 2518-2528 (2019).
- Cappelli, S., et al. Interstitial lung disease in systemic sclerosis: where do we stand. European Respiratory Review. 24 (137), 411-419 (2015).
- Goldin, J. G., et al. Longitudinal changes in quantitative interstitial lung disease on CT after immunosuppression in the Scleroderma Lung Study II. Annals of the American Thoracic Society. 5 (11), 1286-1295 (2018).
- Wangkaew, S., Euathrongchit, J., Wattanawittawas, P., Kasitanon, N. Correlation of delta high-resolution computed tomography (HRCT) score with delta clinical variables in early systemic sclerosis (SSc) patients. Quantitative Imaging in Medicine and Surgery. 6 (4), 381-390 (2016).
- Kim, H. J., et al. Transitions to different patterns of interstitial lung disease in scleroderma with and without treatment. Annals of the Rheumatic Diseases. 75 (7), 1367-1371 (2016).
- Tardella, M., et al. Ultrasound B-lines in the evaluation of interstitial lung disease in patients with systemic sclerosis: cut-off point definition for the presence of significant pulmonary fibrosis. Medicine (Baltimore). 97 (18), 0566 (2018).
- Hassan, R. I., et al. Lung ultrasound as a screening method for interstitial lung disease in patients with systemic sclerosis. Journal of Clinical Rheumatology. , (2018).
- Wang, Y., Gargani, L., Barskova, T., Furst, D. E., Cerinic, M. M. Usefulness of lung ultrasound B-lines in connective tissue disease-associated interstitial lung disease: a literature review. Arthritis Research & Therapy. 19 (1), 206 (2017).
- Ariani, A., et al. Quantitative CT indexes are significantly associated with exercise oxygen desaturation in interstitial lung disease related to systemic sclerosis. The Clinical Respiratory Journal. 11 (6), 983-989 (2017).
- Kim, H. J., et al. Quantitative texture-based assessment of one-year changes in fibrotic reticular patterns on HRCT in scleroderma lung disease treated with oral cyclophosphamide. European Radiology. 21 (12), 2455-2465 (2011).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten