È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Visualizzazione e quantificazione di composti farmaceutici all'interno della pelle utilizzando l'imaging a dispersione Raman coerente
In questo articolo
Riepilogo
Viene descritta una metodologia di imaging a dispersione Raman coerente per visualizzare e quantificare i composti farmaceutici all'interno della pelle. Questo documento descrive la preparazione del tessuto cutaneo (umano e murino) e l'applicazione della formulazione topica, l'acquisizione di immagini per quantificare i profili di concentrazione spaziotemporale e l'analisi farmacocinetica preliminare per valutare la somministrazione topica di farmaci.
Abstract
La farmacocinetica cutanea (cPK) dopo l'applicazione di formulazioni topiche è stata un'area di ricerca di particolare interesse per gli scienziati regolatori e di sviluppo di farmaci per comprendere meccanicamente la biodisponibilità topica (BA). Le tecniche semi-invasive, come lo stripping del nastro, la microdialisi cutanea o la microperfusione cutanea a flusso aperto, quantificano tutte la cPK su macroscala. Mentre queste tecniche hanno fornito una vasta conoscenza di cPK, la comunità manca di una comprensione meccanicistica della penetrazione e della permeazione del principio attivo farmaceutico (API) a livello cellulare.
Un approccio non invasivo per affrontare la cPK su microscala è il Raman scattering imaging (CRI) coerente, che si rivolge selettivamente alle vibrazioni molecolari intrinseche senza la necessità di etichette estrinseche o modifiche chimiche. CRI ha due metodi principali - anti-Stokes Raman scattering (CARS) e scattering Raman stimolato (SRS) - che consentono la quantificazione sensibile e selettiva di API o ingredienti inattivi. CARS viene in genere utilizzato per ricavare informazioni strutturali sulla pelle o visualizzare il contrasto chimico. Al contrario, il segnale SRS, che è lineare con la concentrazione molecolare, viene utilizzato per quantificare le API o gli ingredienti inattivi all'interno delle stratificazioni cutanee.
Sebbene il tessuto di topo sia stato comunemente utilizzato per cPK con CRI, il BA topico e la bioequivalenza (BE) devono essere valutati nel tessuto umano prima dell'approvazione normativa. Questo documento presenta una metodologia per preparare e visualizzare la pelle ex vivo da utilizzare in studi CRI di farmacocinetica quantitativa nella valutazione di BA e BE topici. Questa metodologia consente una quantificazione API affidabile e riproducibile all'interno della pelle umana e del mouse nel tempo. Le concentrazioni all'interno dei compartimenti ricchi di lipidi e poveri di lipidi, così come la concentrazione totale di API nel tempo sono quantificate; questi sono utilizzati per stime di MICRO e macroscala BA e, potenzialmente, BE.
Introduzione
Le metodologie per valutare la cPK dopo l'applicazione di un farmaco topico si sono estese dagli studi classici di test di permeazione in vitro (IVPT) 1,2,3,4,5 e tape-stripping 6,7,8 a metodologie aggiuntive come la microperfusione a flusso aperto o la microdialisicutanea 9,10,11, 12,13,14. Esistono potenzialmente vari siti locali di azione terapeutica a seconda della malattia di interesse. Quindi, potrebbe esserci un numero corrispondente di metodologie per valutare la velocità e la misura in cui un'API arriva al sito di azione locale previsto. Mentre ciascuna delle metodologie di cui sopra ha i suoi vantaggi, il principale svantaggio è la mancanza di informazioni cPK su microscala (cioè l'incapacità di visualizzare dove va l'API e come permea).
Una metodologia non invasiva di interesse per stimare BA e BE topici è CRI, che può essere suddivisa in due modalità di imaging: CARS e microscopia SRS. Questi metodi Raman coerenti consentono l'imaging chimicamente specifico delle molecole tramite effetti Raman non lineari. In CRI, due treni di impulsi laser vengono focalizzati e scansionati all'interno di un campione; la differenza di energia tra le frequenze laser è impostata per indirizzare modalità vibrazionali specifiche per le strutture chimiche di interesse. Poiché i processi CRI non sono lineari, un segnale viene generato solo al fuoco del microscopio, consentendo l'imaging tomografico farmacocinetico tridimensionale del tessuto. Nel contesto della cPK, CARS è stato utilizzato per ottenere informazioni strutturali sui tessuti, come la posizione delle strutture cutanee ricche di lipidi15. Al contrario, SRS è stato utilizzato per quantificare la concentrazione molecolare in quanto il suo segnale è lineare con la concentrazione. Per i campioni di pelle ex vivo , è vantaggioso eseguire CARS nella direzione epi16 e SRS in modalità di trasmissione17. Pertanto, i campioni di tessuto sottili consentiranno il rilevamento e la quantificazione del segnale SRS.
Come tessuto modello, l'orecchio del topo nudo presenta diversi vantaggi con piccoli inconvenienti. Un vantaggio è che il tessuto ha già uno spessore di ~ 200-300 μm e non richiede un'ulteriore preparazione del campione. Inoltre, diverse stratificazioni cutanee sono osservate concentrandosi assialmente attraverso un campo visivo (ad esempio, strato corneo, ghiandole sebacee (SG), adipociti e grasso sottocutaneo)16,18. Ciò consente una stima preclinica preliminare delle vie di permeazione cutanea e stime topiche di BA prima di passare a campioni di pelle umana. Tuttavia, il modello di topo nudo presenta limitazioni come la difficoltà di estrapolazione a scenari in vivo a causa delle differenze nella struttura della pelle19. Mentre l'orecchio del topo nudo è un modello eccellente per ottenere risultati preliminari, il modello della pelle umana è il gold standard. Sebbene ci siano stati vari commenti sull'idoneità e l'applicabilità della pelle umana congelata per ricapitolare accuratamente la cinetica di permeazione in vivo 20,21,22, l'uso della pelle umana congelata è un metodo accettato per la valutazione della cinetica di permeazione API in vitro 23,24,25 . Questo protocollo visualizza vari strati di pelle nella pelle di topo e umana mentre quantifica le concentrazioni di API all'interno di strutture ricche di lipidi e povere di lipidi.
Mentre cri è stato utilizzato in numerosi campi per visualizzare specificamente i composti all'interno dei tessuti, ci sono stati sforzi limitati per studiare la cPK dei prodotti farmaceutici applicati localmente. Per valutare il BA/BE topico dei prodotti topici utilizzando CRI, è necessario prima disporre di un protocollo standardizzato per effettuare confronti accurati. Gli sforzi precedenti che utilizzano CRI per la somministrazione di farmaci alla pelle hanno dimostrato variabilità all'interno dei dati. Poiché si tratta di un'applicazione relativamente nuova del CRI, stabilire un protocollo è fondamentale per ottenere risultati affidabili 18,26,27. Questo approccio si rivolge solo a un numero d'onda specifico nella regione biologica silenziosa dello spettro Raman. Tuttavia, la maggior parte delle API e degli ingredienti inattivi hanno spostamenti Raman all'interno della regione delle impronte digitali. Ciò ha precedentemente posto sfide a causa del segnale intrinseco derivante dal tessuto nella regione delle impronte digitali. I recenti progressi laser e computazionali hanno rimosso questa barriera, che può anche essere utilizzata in combinazione con l'approccio presentato qui28. Questo approccio qui presentato consente la quantificazione di un'API, che ha uno spostamento Raman nella regione silenziosa (2.000-2.300 cm-1). Questo non è limitato alle proprietà fisiochimiche del farmaco, che potrebbe essere il caso di alcune metodologie di monitoraggio cPK precedentemente menzionate29.
Il protocollo deve ridurre la variabilità da campione a campione nello spessore della pelle per vari preparati, poiché i campioni di pelle umana spessa produrranno un segnale minimo dopo l'applicazione del prodotto farmaceutico a causa della diffusione della luce da parte del campione spesso. Uno degli obiettivi di questo manoscritto è quello di presentare una metodologia di preparazione dei tessuti che assicuri standard di imaging riproducibili. Inoltre, il sistema CRI è configurato come descritto per ridurre le potenziali fonti di errore e minimizzare il rapporto segnale-rumore. Tuttavia, questo documento non discuterà i principi guida e i meriti tecnici del microscopio CRI in quanto questo è stato precedentemente trattato30. Infine, viene esplorata l'ampia procedura di analisi dei dati per consentire l'interpretazione dei risultati per determinare il successo o il fallimento di un esperimento.
Protocollo
L'uso di tessuto auricolare di topo nudo è stato approvato dal Massachusetts General Hospital Institutional Animal Care and Use Committee (IACUC), mentre l'uso di tessuto cutaneo umano è stato approvato dal Massachusetts General Hospital Institutional Review Board (IRB). Secondo i protocolli IACUC, i topi appena eutanasizzati sono stati ottenuti da collaboratori con colonie di topi nudi. Il tessuto umano è stato prelevato da procedure elettive di addominoplastica presso il Massachusetts General Hospital tramite un protocollo approvato. Inoltre, specifici tipi di tessuto diversi dalla pelle addominale sono stati acquisiti tramite un'autorità di donazione del corpo, anche attraverso un protocollo approvato dall'IRB.
1. Preparazione del tessuto
- Preparazione del tessuto cutaneo dell'orecchio del topo nudo
- Dopo aver acquisito corpi di topo nudo appena raccolti, rimuovere le orecchie usando pinze e forbici microchirurgiche. Metti un orecchio in una piccola capsula di Petri (cioè 35 mm x 10 mm). Posizionare il corpo del topo nudo in una sacca a rischio biologico da smaltire in conformità con i protocolli IACUC locali.
- Risciacquare ogni orecchio di topo con soluzione salina tamponata con fosfato (PBS) e tamponarlo delicatamente con un tergicristallo. Ripetere due volte per rimuovere eventuali residui di sporco o detriti sull'orecchio che possono influire sulla qualità dell'immagine (vedere la Figura 1).
- Se l'orecchio deve essere utilizzato entro 24 ore, metterlo in una piccola capsula di Petri (cioè 35 mm x 10 mm) con PBS fresco in frigorifero (2-8 °C). Se l'orecchio verrà utilizzato dopo 24 ore dalla raccolta, metterlo in una capsula di Petri (35 mm x 10 mm) senza PBS, coprire il piatto con parafilm e metterlo in un congelatore a -20 °C.
- Preparazione del tessuto cutaneo umano
- Dopo l'approvvigionamento del tessuto umano, metterlo in una grande capsula di Petri (cioè 60 mm x 15 mm) in una cappa biologica per consentire spazio sufficiente per la preparazione del campione.
- Posizionare il lato dello strato corneo rivolto verso il basso in modo tale che il grasso sottocutaneo sia accessibile.
- Usando pinze e forbici microchirurgiche, inizia a rimuovere con cura il grasso sottocutaneo. Una volta che il grasso sottocutaneo non può più essere rimosso con le forbici, passare a un bisturi monouso a 10 lame (o equivalente) per rimuovere il grasso sottocutaneo rimanente. Utilizzare il bisturi con un angolo di 45° rispetto alla pelle tenendo la pelle ferma con una pinza (vedere Figura 1).
NOTA: per avere immagini SRS di trasmissione di alta qualità, i campioni devono essere il più sottili possibile senza essere forati.
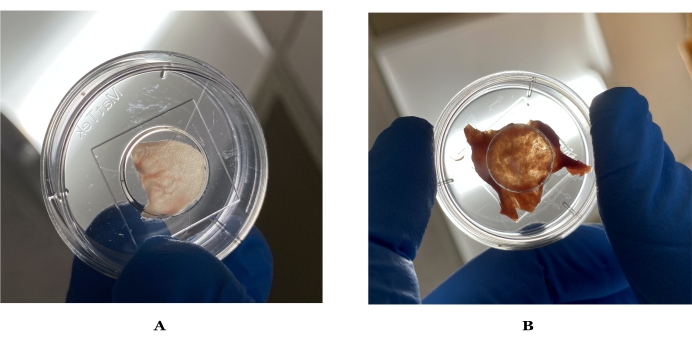
Figura 1: Immagini di spessore ideale per l'imaging della pelle di topo e umana. (A) Pelle dell'orecchio del topo tenuta alla luce, che può visibilmente far passare la luce. (B) Pelle umana ideale tenuta alla luce dopo la preparazione. Fare clic qui per visualizzare una versione più grande di questa figura.
- Sezionare la pelle umana in pezzi di 1 cm x 1 cm.
NOTA: Pelle fresca, può essere utilizzata per un massimo di 24 ore senza l'uso di un letto di gel di agarosio, come descritto in precedenza31. Tuttavia, la pelle fresca può essere utilizzata più a lungo se conservata su un letto di gel di agarosio. Se la pelle deve essere utilizzata in un secondo momento, la pelle viene posta in un sacchetto per il trasporto del campione e quindi posta in un congelatore a -20 °C. La pelle congelata deve essere scongelata utilizzando la procedura riportata di seguito per ottenere risultati ottimali (vedere il passaggio 3.1.2).
2. Configurazione laser e microscopio
- Circa 30 minuti prima dell'imaging, accendere il laser ultraveloce ampiamente sintonizzabile (di seguito denominato laser) e lasciarlo riscaldare. Abilitare il sistema di segnalazione/blocco laser per avvisare il personale al di fuori di un potenziale pericolo all'ingresso.
NOTA: gli occhiali adeguati devono essere sempre indossati quando si lavora con laser di Classe IV. Per il laser specifico utilizzato qui, l'occhiale corretto consigliato è OD ≥ 6 per il campo di lavoro del laser 800-1.300 nm. - Mentre il laser si sta riscaldando, abilitare l'hardware rimanente per il controllo del microscopio, il rilevamento CARS e il rilevamento SRS.
- Allineare correttamente il microscopio per garantire un'imaging ottimale. Nella finestra Controllo acquisizione immagini del software di controllo del microscopio (di seguito software MC), fare clic sulla lampada di trasmissione per consentire alla luce di provenire dalla lampada di transilluminazione del microscopio.
- Garantire la corretta illuminazione di Köhler per allineare il microscopio lungo l'asse verticale: chiudere l'iride verso il basso in modo che una quantità minima di luce sia visibile attraverso l'oculare32.
- Mentre guardi attraverso l'oculare, apri l'iride per vedere se il poligono tocca tutti i lati contemporaneamente. Regolare l'altezza del condensatore se non è possibile vedere una forma poligonale prima di aprire il diaframma.
- Se la forma del poligono non tocca tutti i lati contemporaneamente, regolare la posizione di allineamento dell'apertura utilizzando le manopole di regolazione.
NOTA: Vedi Sanderson et al.33 per una configurazione approfondita del microscopio. - Posizionare un vetrino per microscopio con un coperchio e un distanziatore adesivo a doppia faccia contenente un campione di olio (ad esempio, olio d'oliva, poiché ci sono molti legami -CH2- all'interno degli oli) sul supporto del palco del microscopio.
- Nella finestra Impostazioni di acquisizione del software MC, individuare il menu a discesa del microscopio e impostare l'obiettivo del microscopio su 20x.
- Verificare che il filtro di rilevamento CARS (645 nm/50 nm) sia in posizione per visualizzare e misurare il segnale epiCARS lungo il tubo fotomoltiplicatore della porta laterale del microscopio.
NOTA: Questo filtro specifico è selezionato per l'imaging dei lipidi come segnale anti-Stokes CARS generato a 652 nm per una lunghezza d'onda della pompa di 803 nm e una lunghezza d'onda di Stokes di 1.040 nm (vedi Eq. (1)).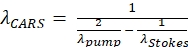 (1)
(1)
Dove le variabili λ hanno unità di nm; Lapompa λ è la lunghezza d'onda del fascio della pompa; e λStokes è la lunghezza d'onda del fascio di Stokes. - Guarda attraverso l'oculare per trovare il bordo del campione di olio, che verrà utilizzato per verificare l'allineamento del sistema.
- Assicurarsi che il bordo sia a fuoco Z utilizzando le manopole di messa a fuoco sul microscopio e regolare il controller dello stadio per ottenere la messa a fuoco XY.
- Dopo che il laser si è riscaldato, impostare il raggio della pompa a 803 nm con la messa a punto del motore impostata su 50.0 nell'interfaccia utente grafica del laser. L'esatta messa a punto del motore utilizzata può differire da configurazione a configurazione.
NOTA: Il raggio della pompa è l'unico raggio con una lunghezza d'onda regolabile su questo laser poiché la lunghezza d'onda del fascio di Stokes è fissata a 1.040 nm. Questa configurazione si rivolge alla vibrazione CH a 2850 cm-1 (vedi Eq. (2) per calcolare la lunghezza d'onda della pompa per il targeting del numero d'onda).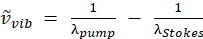 (2)
(2)
Dove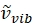 ha unità di numero d'onda relativo (cm−1) e le variabili λ hanno unità in cm.
ha unità di numero d'onda relativo (cm−1) e le variabili λ hanno unità in cm. - Controllare l'allineamento del laser al microscopio prima dell'imaging; vedere la Figura 2 per la rappresentazione del percorso laser. Durante la configurazione iniziale del microscopio, installare due iris nel percorso del fascio come guide per il corretto allineamento nel microscopio. Poiché il percorso ottico del laser può andare alla deriva nel tempo, assicurarsi che i percorsi del raggio laser attraversino il centro delle iridi in modo che entrino correttamente nel microscopio.
- Utilizzando il visualizzatore IR, chiudere completamente tutti i iris e assicurarsi che il raggio sia centrato su entrambi: prima sull'iride più vicino al laser e infine sulla porta di ingresso del microscopio.
- Per prima cosa, controlla il raggio della pompa per assicurarti che il raggio stia andando dritto nel microscopio. Una volta che la pompa è allineata, verificare che anche il raggio di Stokes entri correttamente nel microscopio.
- Se le travi non sono allineate attraverso i iris, camminare iterativamente le travi attraverso i iris usando le manopole di regolazione x e y dei due supporti a specchio per la pompa e i percorsi di stokes.
- Una volta che i punti del fascio si sovrappongono prima di entrare nel microscopio, verificare che stiano attraversando correttamente il microscopio.
- Nella finestra Controllo acquisizione immagini del software MC, fare clic sul canale TD per la trasmissione, ALG1 (canale analogico 1) per il canale Raman anti-Stokes coerente e ALG2 (canale analogico 2) per il canale di diffusione Raman stimolato. Utilizzare le seguenti impostazioni (come in questo protocollo): guadagno di 1 e offset di -1 per ALG1, guadagno di 1,25 e offset di -2 per ALG2.
NOTA: a seconda della configurazione del sistema, i canali analogici possono avere una numerazione diversa per i singoli canali di imaging. Se il rilevatore SRS è in posizione, non ci sarà alcun segnale di trasmissione in quanto nessuna luce può passare (cioè, non è possibile visualizzare le immagini con TD e ALG2 contemporaneamente in questa configurazione).
- Nella finestra Controllo acquisizione immagini del software MC, fare clic sul canale TD per la trasmissione, ALG1 (canale analogico 1) per il canale Raman anti-Stokes coerente e ALG2 (canale analogico 2) per il canale di diffusione Raman stimolato. Utilizzare le seguenti impostazioni (come in questo protocollo): guadagno di 1 e offset di -1 per ALG1, guadagno di 1,25 e offset di -2 per ALG2.
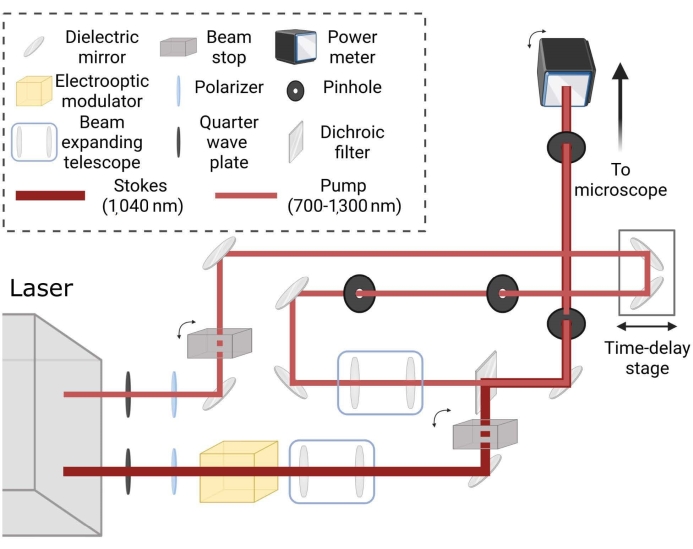
Figura 2: Layout schematico per un percorso di imaging laser Raman coerente. I fasci sono condizionati in modo indipendente per le dimensioni dello spot e abbinati tramite lo stadio di ritardo temporale per generare uno scattering Raman coerente nei campioni per la frequenza di sintonizzazione desiderata. Fare clic qui per visualizzare una versione più grande di questa figura.
- Accendere il misuratore di potenza e, utilizzando un sensore di potenza termica ad alta potenza, misurare la potenza della pompa e dei fasci di Stokes individualmente per l'esperimento.
NOTA: In questo esempio specifico, la potenza del fascio della pompa era di 80 mW, mentre la potenza del fascio di Stokes era di 180 mW prima dell'ingresso al microscopio. - Nella finestra Controllo acquisizione immagini , fare clic sul pulsante Focus x2 per visualizzare l'immagine nel software MC.
- Nella finestra Impostazioni acquisizione, assicurarsi che il rapporto pixel e il tempo di permanenza siano impostati sui parametri desiderati per l'esperimento.
NOTA: in questo protocollo sono stati utilizzati un rapporto di 1.024 x 1.024 pixel e un tempo di permanenza di 2 μs/pixel. - Confermare l'allineamento laser rispetto al microscopio sbloccando il fascio della pompa e osservando il canale TD .
NOTA: il laser è allineato correttamente se il raggio viene visto centrato nell'immagine con le impostazioni corrette del rilevatore. - In caso contrario, utilizzare le manopole di regolazione X e Y sul periscopio per riposizionare il raggio al centro dell'immagine.
- Confermare l'allineamento laser e microscopio visualizzando la stessa immagine in entrambi i canali CARS e SRS.
- Per acquisire l'immagine di allineamento, fare clic sul pulsante di scansione XY nella finestra Controllo acquisizione immagini con la modalità filtro appropriata impostata (ad esempio, Kalman Line 3).
- Salvare questo set di immagini con un nome file descrittivo da confrontare nel tempo e confermare le prestazioni/l'allineamento del sistema.
3. Imaging lipidico
- Orecchio di topo e tessuto umano
- Se si utilizza tessuto fresco, saltare il passaggio 3.1.2.
- Rimuovere la pelle dell'orecchio del topo dal congelatore a -20 °C e metterla in una camera di incubazione (32 °C) per 10 minuti. Rimuovere l'orecchio del topo dalla camera di incubazione.
NOTA: vedere il passaggio 1.1.2. per la preparazione della pelle dell'orecchio del topo. La manipolazione approssimativa o la raschiatura del tessuto può causare degradazione meccanica, distruzione o interruzione del tessuto, in particolare dello strato corneo. - Se si utilizza un orecchio di topo nudo, posizionare la parte anteriore dell'orecchio rivolta verso il fondo di vetro di un piatto di 35 mm, n. 0. Se si utilizza la pelle umana, posizionarla con lo strato corneo a faccia in giù in quanto ciò consentirà la quantificazione del farmaco dagli strati superficiali agli strati più profondi (Figura 1).
NOTA: La parte posteriore dell'orecchio del topo nudo è più soggetta a imperfezioni dall'alloggiamento. Se la pelle umana non viene posizionata con il lato dello strato corneo rivolto verso il basso sul microscopio invertito, non si sarà in grado di vedere oltre il derma poiché c'è una discreta quantità di luce diffusa e il farmaco che permea lo strato corneo non può essere visto. - Una volta che il tessuto è stato centrato sul fondo di vetro, utilizzare un applicatore con punta di cotone per assicurarsi che la pelle sia piatta e abbia un contatto completo con la superficie del coperchio del piatto con fondo di vetro.
NOTA: questo è un passaggio che può causare difficoltà durante l'imaging della pelle se non è completamente piatta. - Posizionare una rondella sulla parte superiore della pelle per impedire qualsiasi movimento durante l'imaging. Assicurarsi che il tessuto sia visibile attraverso il foro centrale della rondella per il rilevamento della trasmissione SRS.
- Rimuovere l'inserto dello stadio di scorrimento e sostituirlo con la camera di incubazione, che ha l'inserto del piatto singolo.
- Posizionare il piatto con fondo di vetro con il tessuto cutaneo nell'attacco del piatto singolo della camera di incubazione.
NOTA: in alternativa, utilizzare una piastra a 6 pozzetti per visualizzare più campioni di pelle e formulazioni contemporaneamente. - Ridurre il rapporto pixel nella finestra Impostazioni di acquisizione del software MC (ad esempio, da 1.024 x 1.024 a 512 x 512) per una maggiore velocità di scansione galvo mentre la profondità Z viene modificata per trovare lo strato corneo (vedere la Figura 3A per il mouse o la Figura 3E per l'uomo).
- Dopo che lo strato corneo è stato trovato, registra quella posizione assiale come posizione zero nella finestra Impostazioni di acquisizione e modifica il rapporto pixel per ogni esperimento specifico (ad esempio, 1.024 x 1.024).
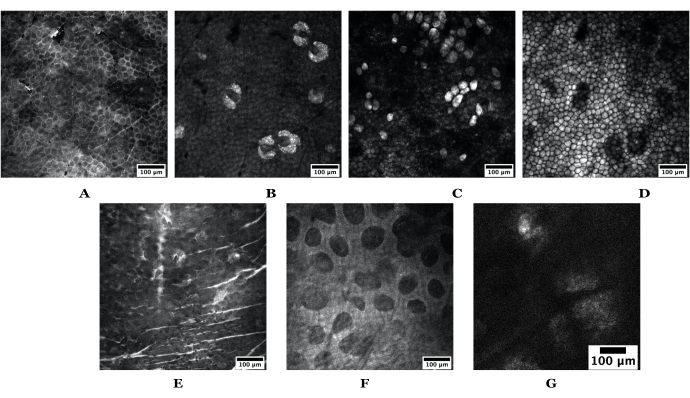
Figura 3: Esempi di profondità cutanee ottenute utilizzando SRS. La serie superiore di immagini proviene dalla pelle dell'orecchio di topo nudo che raffigura quanto segue: (A) strato corneo, (B) ghiandole sebacee, (C) adipociti, (D) grasso sottocutaneo. La serie inferiore di immagini è ottenuta dalla pelle umana che raffigura quanto segue: (E) strato corneo, (F) derma papillare e (G) una ghiandola sebacea. Barre di scala = 100 μm. Sia le immagini del mouse che quelle della pelle umana sono state acquisite utilizzando un obiettivo 20x a 1024 pixel x 1024 pixel; l'SG umano è stato preso a 512 x 512 pixel. Abbreviazioni: SRS = scattering Raman stimolato; SG = ghiandola sebacea. Fare clic qui per visualizzare una versione più grande di questa figura.
4. Applicazione della formulazione topica
- Pipettare la dose di formulazione predeterminata sulla pelle (ad esempio, 10 μL/cm2).
NOTA: la viscosità della formulazione avrà un ruolo nella scelta della pipetta. Si raccomanda l'uso di una pipetta a spostamento positivo per formulazioni viscose, come creme o gel, e di una pipetta a spostamento d'aria per soluzioni. In questo esperimento, ruxolitinib era il composto modello in una semplice soluzione di glicole propilenico (propano-1,2-diolo). - Usando la punta dello stantuffo da una siringa o un dito guantato, strofinare la formulazione in senso orario per 30 s. Si noti il momento in cui la formulazione viene applicata per un'analisi cPK successiva (vedere i passaggi 6.15-6.17 di seguito).
NOTA: la durata dell'applicazione dipende dall'esperimento; ognuno può essere diverso. - Dopo che è trascorso il tempo assegnato per la permeazione della formulazione, rimuovere la formulazione in eccesso e posizionare la pelle con il lato della formulazione rivolto verso il piatto con fondo di vetro.
NOTA: La formulazione viene rimossa utilizzando un tergicristallo delicato o un piccolo tergipavimento stampato in 3D (~ 1 pollice) in un'unica direzione (ad esempio, da nord a sud).
5. Configurazione sperimentale per la quantificazione dei farmaci
- Impostare il raggio della pompa su 803 nm. Controlla la pompa e le potenze del fascio di Stokes con il fotodiodo per assicurarti che siano le potenze desiderate per l'esperimento. Sblocca ogni raggio individualmente per misurare la potenza e ribloccare i raggi.
NOTA: in questo esempio specifico, la potenza del fascio della pompa era di 100 mW, mentre la potenza del fascio di Stokes era di 180 mW. - Posizionare il piatto con fondo di vetro in una camera di incubazione con un inserto per un piatto con fondo di vetro. Fissare il piatto con clip per impedire il movimento durante l'imaging.
- Accendere la spia di trasmissione nel software MC. Guardando attraverso l'oculare, regolare la messa a fuoco assiale con la manopola di regolazione per garantire che il tessuto sia a fuoco.
- Sblocca sia la pompa che le travi stokes. Assicurarsi che i canali ALG1 e ALG2 siano abilitati, quindi fare clic su Focus x2 sul software MC per visualizzare la pelle nei canali CARS e SRS. Assicurarsi che il fotodiodo SRS sia in posizione sopra il condensatore.
- Nel menu a discesa Dispositivo, fare clic su Multi Area Time Lapse (MATL). Cerca un avviso di fase XY da visualizzare; quando lo stage si sposta per trovare la sua origine meccanica, fate clic su OK.
- Nel modulo MATL , vai su Visualizza e quindi fai clic su Elenco punti registrati all'interno del software MC. Inizia ad aggiungere 1) profondità specifiche all'interno della pelle (ad esempio, strato corneo, SG, adipociti, grasso sottocutaneo come determinato durante l'imaging dal vivo con contrasto lipidico) o 2) posizioni XY se devono essere prese intere pile di profondità. Vedere la Figura 3 per alcuni esempi.
- Una volta identificato lo strato corneo, scorrere il fuoco assiale (o z-focus) per identificare specifiche stratificazioni tissutali sopra menzionate. Vedere la Figura 3 per esempi all'interno della pelle umana e del topo.
- Nel caso di imaging di profondità specifiche rispetto a pile di profondità Z complete, per ogni stratificazione cutanea, fare clic su Registra punto per aggiungerlo alla coda MATL. Per gli stack a profondità completa, fare clic su Registra punto per ogni posizione XY con selezione della profondità nella finestra dei parametri di acquisizione .
- Una volta che tutte le posizioni XY (full Z-depth stacks) o XYZ (specifiche stratificazioni cutanee) desiderate sono state registrate all'interno del software MATL, modificare la directory e il nome dei file in modo coerente durante gli esperimenti per le analisi di immagini e cPK (vedere i passaggi 6.15-6.17).
- Impostare il numero di ripetizioni su 1 nel modulo MATL e fare clic su Pronto. Attendi che Play passi da una freccia grigia a una freccia nera, indicando che il software è pronto. Premere Play per iniziare a visualizzare lo stack lipidico preliminare (di seguito Lipid Images).
NOTA: Questo sarà utilizzato per separare le regioni ricche di lipidi e povere di lipidi delle singole stratificazioni tissutali durante l'analisi. Il ciclo e il tempo totale sono indicati in basso a destra nell'elenco dei punti registrati. - Una volta completato il ciclo, bloccare sia la pompa che le travi Stokes. Modificare la lunghezza d'onda dell'interfaccia utente grafica laser alla lunghezza d'onda desiderata in base al numero d'onda target o alla vibrazione Raman.
NOTA: ad esempio, 843 nm per il raggio della pompa vengono utilizzati per indirizzare 2.250 cm-1 utilizzando Eq. (2) e la messa a punto del motore viene modificata in 50,1. Il farmaco di esempio presentato qui, ruxolitinib, contiene un nitrile che può essere mirato a 2.250 cm-1. Il numero d'onda mirato per la struttura della pelle sarà sempre lo stesso (2.850 cm-1); tuttavia, il numero d'onda per un'API può essere qualsiasi numero d'onda, ma deve essere noto o calcolato a priori. - Regolare lo stadio di ritardo temporale manuale (Figura 2) per garantire la sovrapposizione nel tempo per la nuova lunghezza d'onda e la potenza del fascio della pompa. Assicurarsi che le stesse potenze vengano utilizzate sia per l'imaging lipidico che api, che sono stabiliti a priori.
- Utilizzare la durata per ciclo per calcolare il numero totale di ripetizioni necessarie per esperimento. Basta dividere il tempo-corso totale desiderato dell'esperimento per quello della durata del ciclo.
NOTA: la durata del ciclo è una funzione delle dimensioni dell'immagine, del tempo di permanenza dei pixel, della media di Kalman e del numero di immagini per ciclo. L'ottimizzazione di questi parametri ridurrà il tempo di ciclo, aumentando così la risoluzione temporale. - Una volta scelto il numero totale di ripetizioni del ciclo, sbloccare il fascio della pompa, controllare la potenza utilizzando il fotodiodo e assicurarsi che corrisponda a quella della potenza desiderata. Infine, sblocca il raggio di Stokes per consentire l'imaging.
- Premere Riproduci per avviare l'imaging automatizzato dei set-point.
- Una volta completata l'imaging MATL, riportare il fascio della pompa a 803 nm e riportare la potenza alla potenza di imaging lipidico originale utilizzata nel passaggio 5.1.
- Come nei passaggi precedenti, modificare il nome del file in modo che sia coerente per le immagini post-esperimento durante lo studio.
- Impostare il numero di ripetizioni su 1.
- Fai clic su Pronto | Pulsante Play per acquisire uno stack lipidico post-time-course e assicurarsi che non ci sia stato alcun movimento tissutale durante l'imaging (Figura 4).

Figura 4: Movimento tissutale nella pelle dell'orecchio del topo nudo dimostrato visualizzando le ghiandole sebacee. Esempio di movimento limitato dei tessuti è raffigurato in A e B, mentre il movimento sostanziale dei tessuti è raffigurato in C e D. (A) mostra le ghiandole sebacee al momento dell'applicazione della formulazione e (B) la stessa profondità a 120 minuti dopo l'applicazione. (C) ghiandole sebacee di topo al momento dell'applicazione della formulazione e (D) 120 minuti dopo l'applicazione della formulazione; le ghiandole sebacee sono appena visibili, il che è un'indicazione che questo esperimento non stava misurando l'assorbimento nelle ghiandole sebacee per l'intera durata sperimentale. Barre di scala = 100 μm. Le immagini sono 1024 pixel x 1024 pixel. Fare clic qui per visualizzare una versione più grande di questa figura.
6. Analisi dei dati
- Acquisire immagini come . OIB (o . OIR a seconda del microscopio e del software MC) tipi di file con ogni posizione XYZ con una sottocartella separata.
- Compila le immagini lipidiche con le immagini del canale API rinominando le immagini lipidiche con la seguente _lipid.oib.
- Eseguire i seguenti passaggi con ogni stratificazione cutanea (dimostrata qui usando solo la stratificazione SG per semplicità; vedere figura 3B).
- Importa un'immagine lipidica SG in ImageJ (o Fiji)34 e seleziona la casella Split Channels per dividere il file nei canali CARS e SRS.
NOTA: Fiji dividerà il file nel numero di immagini acquisite durante l'esperimento attraverso il numero di canali. - Aprire il gestore della regione di interesse (ROI) facendo clic su Analizza | Strumenti | ROI Manager.
- Utilizzando il canale SRS (ad esempio, C = 1), delimitare un SG nell'immagine.
NOTA: gli SG sono le posizioni luminose a causa della vibrazione mirata -CH2-. - Aggiungilo al ROI manager facendo clic su Aggiungi [t] nel ROI manager o premendo t sulla tastiera. Ripetere questa procedura per ogni SG all'interno dell'immagine.
- Per mascherare le regioni ricche di lipidi, selezionare ciascun ROI e fare clic sulla scheda Altro | OR (Combina) | Aggiungi a ROI manager.
- Per mascherare le regioni povere di lipidi, usa lo strumento rettangolo nel menu FIGI e disegna un quadrato attorno all'intera immagine. Aggiungilo al ROI manager.
- Fai clic sul ROI quadrato appena aggiunto oltre al ROI che seleziona tutte le regioni ricche di lipidi nel ROI manager. In Altro, selezionare XOR per generare una maschera delle regioni povere di lipidi e aggiungerla al ROI manager.
- Importa un'immagine lipidica SG in ImageJ (o Fiji)34 e seleziona la casella Split Channels per dividere il file nei canali CARS e SRS.
- Carica le immagini API in Fiji.
- Concatenare le immagini in ordine numerico (ad esempio, Image0001, Image0002, Image0003, ecc.) utilizzando la seguente sequenza di menu: Image | Stack | Strumenti | Concatenare.
- In alternativa, importare queste immagini caricando una delle immagini nelle Figi e quindi selezionando un'opzione chiamata File di gruppo con nomi simili nella pagina di configurazione .
NOTA: in questo modo è possibile importare tutte le immagini con un nome file simile e concatenarle automaticamente.
- In alternativa, importare queste immagini caricando una delle immagini nelle Figi e quindi selezionando un'opzione chiamata File di gruppo con nomi simili nella pagina di configurazione .
- Mentre l'immagine concatenata è attiva, vai al gestore del ROI, seleziona le regioni ricche di lipidi (ad esempio, l'SG), fai clic su Altro e seleziona Multi-misura. Attendere la visualizzazione della finestra Risultati .
- Cercare Area, Media, Min, Max e Mediana nelle impostazioni di misurazione predefinite. Se si desiderano altre metriche per l'analisi, abilitare queste opzioni selezionando la casella di controllo pertinente nella finestra Imposta misure (Analizza | Imposta misure...).
- Esporta i dati dalla finestra Risultati in un foglio di calcolo e aggiungi una colonna intitolata Regione.
- Aggiungi ricchi di lipidi a ogni riga di dati per le regioni ricche di lipidi. Aggiungi poveri di lipidi alle regioni che erano al di fuori dei lipidi.
- Aggiungere una colonna intitolata layer e aggiungere il rispettivo layer analizzato (Tabella supplementare S1).
- Ripetere i passaggi 6.5 - 6.7 per le regioni povere di lipidi mentre viene selezionato il ROI appropriato.
- Per visualizzare i dati, salvare il foglio di calcolo e importarlo in JupyterLab (pacchetto matplotlib)35 o in R (pacchetto ggplot2)36. Traccia i dati in funzione del numero dell'immagine rispetto all'intensità media per stimare i dati concentrazione-tempo. (Figura 5).
- Importare il foglio di calcolo in RStudio per eseguire analisi non comunitarie (NCA) per l'analisi farmacocinetica dei dati CRI.
- Aggiungi una colonna intitolata ora.
- Per Image0001, calcolare la durata tra l'applicazione della formulazione e la prima immagine.
NOTA: questo è il primo timepoint. La durata del ciclo viene utilizzata per calcolare le immagini rimanenti (e quindi i punti temporali) che aumentano nel tempo. Ad esempio, se il tempo trascorso dall'applicazione è di 30 minuti, Image0001 avrà un punto temporale di 30 minuti e con una durata del ciclo di 8 minuti, Image0002 avrà un punto temporale di 38 minuti, Image0003 avrà un punto temporale di 46 minuti e così via. - Eseguire NCA in RStudio (utilizzando il pacchetto NonCompart)37 sui dati di intensità-tempo importati dal foglio di calcolo, con la seguente chiamata per un livello/regione:
sNCA(x = tempo, y = media, dose = 1, timeUnit = "s", doseUnit ="mg")
Dove x si riferisce ai punti temporali, y si riferisce all'intensità e la dose può essere lasciata come una, calcolata come la dose mM del farmaco nella formulazione o la dose del prodotto.
NOTA: l'output NCA fornirà parametri come Cmax e AUCtutti. Tuttavia, trattandosi di pelle ex vivo , questi parametri sono, di fatto, Jmax e AUCflux-all. - Confronta visivamente le metriche Jmax e AUCflux-all tracciandole (Figura 6) oltre ai confronti statistici tra le condizioni sperimentali. Si veda la Figura 6 per un esempio di analisi degli studi CRI ex vivo .
NOTA: i test statistici appropriati dipendono da ciascun set di dati specifico. È anche importante notare che tutti i parametri farmacocinetici sono normalmente distribuiti e qualsiasi confronto deve utilizzare i dati trasformati in log (log naturale o log10).
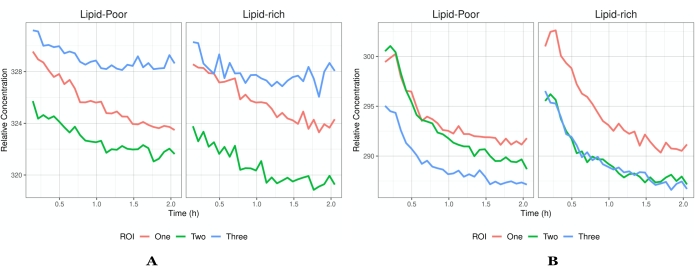
Figura 5: Intensità rispetto ai profili temporali. (A) Si vede un esempio di profili di flusso che hanno raggiunto la saturazione e quindi solo una diminuzione dell'intensità. Ogni ROI ha un profilo di flusso diverso per dimostrare l'eterogeneità dei dati che si potrebbero acquisire. (B) Un esempio di concentrazioni che aumentano dopo l'inizio dell'imaging. Ogni ROI è un diverso campo visivo (indicato dalle diverse tracce di colore) all'interno dello stesso tessuto dello stesso esperimento. Oltre alle concentrazioni globali, c'è la capacità di chiarire quale ambiente locale un API / formulazione preferisce come indicato dalle regioni ricche di lipidi e povere di lipidi. I profili presentati in A indicano che non vi è alcun assorbimento del farmaco nel tessuto poiché l'API ha già permeato e ha iniziato a lasciare il tessuto una volta iniziata l'imaging. Tuttavia, in B, il tessuto non ha raggiunto la saturazione e c'è ancora assorbimento dell'API seguito dall'eliminazione. La segmentazione delle immagini in ricche di lipidi e povere di lipidi aiuterà a chiarire la localizzazione dell'API (o inattivi) e delle vie di permeazione nella pelle (cioè lo strato corneo). Una concentrazione più elevata all'interno delle regioni ricche di lipidi indica che l'API si localizza all'interno della struttura lipidica dello strato in esame, il che aiuta nelle informazioni mirate sulla somministrazione di farmaci. Abbreviazioni: ROI = regione di interesse; API = principio attivo farmaceutico. Fare clic qui per visualizzare una versione più grande di questa figura.
Risultati
L'imaging è considerato di successo se il tessuto non si è mosso in modo significativo in direzione assiale (<10 μm) o laterale al completamento dell'esperimento (Figura 4). Questa è un'indicazione immediata se la misurazione SRS per l'API di interesse non è rappresentativa della profondità iniziale, per la quale la quantificazione è specifica del livello. Ciò è mitigato dall'imaging di z-stack per ogni posizione XY di interesse, con il compromesso che è la risoluzione temporale. S...
Discussione
La valutazione del BA/BE topico è un'area di ricerca che richiede un approccio sfaccettato in quanto nessun singolo metodo può caratterizzare completamente la cPK in vivo . Questo protocollo presenta una metodologia per la valutazione del BA/BE di un prodotto farmaceutico topico basato sull'imaging Raman coerente. Uno dei primi punti che potrebbero essere trascurati è quanto devono essere sottili i campioni di pelle, specialmente per l'imaging SRS a trasmissione quantitativa. Se la pelle è troppo spessa (
Divulgazioni
CLE è un inventore di brevetti per la microscopia CARS che sono stati concessi in licenza a più produttori di microscopi. Tutti gli altri autori non hanno conflitti di interesse da rivelare.
Riconoscimenti
Gli autori desiderano ringraziare il Dr. Fotis Iliopoulos e Daniel Greenfield del Gruppo Evans per la loro discussione e correzione di bozze di questo manoscritto. Inoltre, gli autori vorrebbero riconoscere il sostegno di LEO Pharma. La Figura 2 è stata creata con BioRender.com.
Materiali
| Name | Company | Catalog Number | Comments |
| Tissue Preparation | |||
| Autoclavable Biohazard Bags | FisherBrand | 22-044562 | As refered to in text: biohazard bags https://www.fishersci.com/shop/products/fisherbrand-polyethylene-biohazard-autoclave-bags-without-sterilization-indicator-8/22044562?searchHijack=true&searchTerm= 22044562&searchType=RAPID& matchedCatNo=22044562 |
| Cell Culture Buffers: Dulbecco's Phosphate-Buffered Salt Solution 1x | Corning | MT21030CV | As refered to in text: PBS https://www.fishersci.com/shop/products/corning-cellgro-cell-culture-buffers-dulbecco-s-phosphate-buffered-salt-solution-1x-8/MT21030CV?searchHijack=true&searchTerm= 21-030-cv&searchType= RAPID&matchedCatNo=21-030-cv |
| Disposable Scalpels | Exel International | 14-840-00 | As refered to in text: scalpel https://www.fishersci.com/shop/products/exel-international-disposable-scalpels-3/1484000?keyword=true |
| High Precision 45° Angle Broad Point Tweezers/Forceps | Fisherbrand | 12-000-132 | As refered to in text: forceps https://www.fishersci.com/shop/products/high-precision-45-angle-broad-point-tweezers-forceps/12000132#?keyword= |
| Kimwipes Delicate Task Wipers, 1-Ply | Kimberly-Clark Professional Kimtech Science | 06-666 | As refered to in text: task wiper https://www.fishersci.com/shop/products/kimberly-clark-kimtech-science-kimwipes-delicate-task-wipers-7/06666 |
| Parafilm M Laboratory Wrapping Film | Bemis | 13-374-12 | As refered to in text: parafilm https://www.fishersci.com/shop/products/curwood-parafilm-m-laboratory-wrapping-film-4/1337412 |
| Petri Dish (35 mm x 10 mm) | Fisherbrand | FB0875711YZ | As refered to in text: small petri dish https://www.fishersci.com/shop/products/fisherbrand-petri-dishes-specialty-6/FB0875711YZ?keyword=true |
| Petri Dish (60 mm x 15 mm) | Fisherbrand | FB0875713A | As refered to in text: large petri dish https://www.fishersci.com/shop/products/fisherbrand-petri-dishes-clear-lid-12/FB0875713A?keyword=true |
| Surgical Scissors | Roboz | NC9411473 | As refered to in text: scissors https://www.fishersci.com/shop/products/scissors-327/NC9411473?searchHijack=true&searchTerm= RS-5915SC&searchType=RAPID& matchedCatNo=RS-5915SC |
| Laser/microscope | |||
| 650/60 nm BrightLine single-band bandpass filter | Semrock | As refered to in text: CARS filter - CH2 vibrations (645nm/60nm filter) | |
| Control box IX2-UCB | Olympus | As refered to in text: Control Box | |
| D700/30m | Chroma | As refered to in text: CARS filter - deuterated band https://www.chroma.com/products/parts/d700-30m | |
| DeepSee Insight | Spectra-Physics | As refered to in text: Laser https://www.spectra-physics.com/f/insight-x3-tunable-laser | |
| Digital Handheld Optical Power and Energy Meter Console | ThorLabs | PM100D | As refered to in text: power meter https://www.thorlabs.com/newgrouppage9.cfm?objectgroup_id=3341 |
| Fluoview Software | Olympus | As refered to in text: Microscope Control software | |
| Frosted Microscope Slides | FisherBrand | As refered to in text: microscope slides https://www.fishersci.com/shop/products/fisherbrand-frosted-microscope-slides-4/22265446 | |
| FV1000 | Olympus | As refered to in text: Microscope | |
| Incubation Chamber | Tokai Hit | GM-800 | As refered to in text: incubation chamber |
| Integrating Sphere Photodiode Power Sensor | ThorLabs | S142C | As refered to in text: photodiode https://www.thorlabs.com/newgrouppage9.cfm?objectgroup_id=3341 |
| Power supply FV31-PSU | Olympus | As refered to in text: Power Supply | |
| Precision 4063, 80MHz Dual Channel Function Generator | BK Precision | As refered to in text: function generator | |
| ProScan – Precision Microscope Automation | Prior Scientific Instruments | As refered to in text: stage controller https://www.prior.com/microscope-automation/inverted-microscope-systems/proscan-linear-stage-highest-precision-microscope-automation | |
| SecureSeal Imaging Spacers | Grace Biolabs | 654004 | As refered to in text: spacer https://gracebio.com/product/secureseal-imaging-spacers-654004/ |
| SRS Detection Kit | APE | As refered to in text: SRS detector | |
| UPLSAPO 20X NA:0.75 | Olympus | As refered to in text: 20X Objective https://www.olympus-lifescience.com/en/objectives/uplsapo/ | |
| Lipid/Drug Imaging | |||
| 35 mm Dish, No. 0 Uncoated Coverslip, 14 mm Glass Diameter | MatTek Corporation | NC9711297 | As refered to in text: Glass bottom dish https://www.fishersci.com/shop/products/glass-bottom-mircrowell-dish/nc9711297 |
| Cotton-tipped applicators | FisherBrand | As refered to in text: Cotton-tipped applicator | |
| Distriman Postive Displacement Pipette | Gilson | As refered to in text: Postive Displacement Pipette https://www.fishersci.com/shop/products/gilson-distriman-positive-displacement-repetitive-pipette/F164001G#?keyword= | |
| Distriman Postive Displacement Pipette Tips | Gilson | As refered to in text: Tips for pipette https://www.fishersci.com/shop/products/gilson-distritip-syringes-6/f164100g?keyword=true | |
| Data Analysis | |||
| FIJI | Open-source | As refered to in text: FIJI/ImageJ https://imagej.net/software/fiji/ | |
| Jupyter-Lab | open-source | As refered to in text: JupyterLab https://jupyter.org/ | |
| Rstudio | Open-source | As refered to in text: Rstudio https://www.rstudio.com/ |
Riferimenti
- Finnin, B., Walters, K. A., Franz, T. J., Benson, H. E., Watkinson, A. C. In vitro skin permeation methodology. In Transdermal and topical drug delivery: principles and methodology. Transdermal and topical drug delivery: principles and practice. , 85-108 (2012).
- Shin, S. H., et al. On the road to development of an in vitro permeation test (IVPT) model to compare heat effects on transdermal delivery systems: exploratory studies with nicotine and fentanyl. Pharmaceutical Research. 34 (9), 1817-1830 (2017).
- Hossain, A., et al. Preparation, characterisation, and topical delivery of terbinafine. Pharmaceutics. 11 (10), 548 (2019).
- Santos, L. L., Swofford, N. J., Santiago, B. G. In vitro permeation test (IVPT) for pharmacokinetic assessment of topical dermatological formulations. Current Protocols in Pharmacology. 91 (1), 79 (2020).
- Iliopoulos, F., Caspers, P. J., Puppels, G. J., Lane, M. E. Franz cell diffusion testing andquantitative confocal Raman spectroscopy: In vitro-in vivo correlation. Pharmaceutics. 12 (9), 887 (2020).
- Cordery, S., et al. Topical bioavailability of diclofenac from locally-acting, dermatological formulations. International Journal of Pharmaceutics. 529 (1-2), 55-64 (2017).
- Pensado, A., et al. Stratum corneum sampling to assess bioequivalence between topicalacyclovir products. Pharmaceutical Research. 36 (12), 1-16 (2019).
- Zhang, Y., et al. Dermal delivery of niacinamide-in vivo studies. Pharmaceutics. 13 (5), 726 (2021).
- Bodenlenz, M., et al. Open flow microperfusion as a dermal pharmacokinetic approach to evaluate topical bioequivalence. Clinical Pharmacokinetics. 56 (1), 91-98 (2017).
- Eirefelt, S., et al. Evaluating dermal pharmacokinetics and pharmacodymanic effect of soft topical PDE4 inhibitors:Open flow microperfusion and skin biopsies. Pharmaceutical Research. 37 (12), 1-12 (2020).
- Stagni, G., O'Donnell, D., Liu, Y. J., Kellogg, J. D. L., Shepherd, A. M. Iontophoretic current and intradermal microdialysis recovery in humans. Journal of Pharmacological and Toxicological Methods. 41 (1), 49-54 (1999).
- Garcia Ortiz, P., Hansen, S. H., Shah, V. P., Menne, T., Benfeldt, E. Impact of adultatopic dermatitis on topical drug penetration: assessment by cutaneous microdialysis and tape stripping. Acta Dermato-Venereologica. 89 (1), 33-38 (2009).
- Joshi, A., Patel, H., Joshi, A., Stagni, G. Pharmacokinetic applications of cutaneous microdialysis: Continuous+intermittent vs continuous-only sampling. Journal of Pharmacological and Toxicological Methods. 83, 16-20 (2017).
- Kuzma, B. A., et al. Evaluation of local bioavailability of metronidazole from topical formulations using dermal microdialysis: Preliminary study in a Yucatan mini-pig model. European Journal of Pharmaceutical Sciences. 159, 105741 (2021).
- Begley, R., Harvey, A., Byer, R. L.Coherent anti-Stokes Raman spectroscopy. Applied Physics Letters. 25 (7), 387-390 (1974).
- Evans, C. L., et al. Chemical imaging of tissue in vivo with video-rate coherent anti-Stokes Raman scattering microscopy. Proceedings of the National Academy of Sciences of the United States of America. 102 (46), 16807-16812 (2005).
- Hill, A. H., Manifold, B., Fu, D. Tissue imaging depth limit of stimulated Raman scattering microscopy. Biomedical Optics Express. 11 (2), 762-774 (2020).
- Feizpour, A., Marstrand, T., Bastholm, L., Eirefelt, S., Evans, C. L. Label-free quantification of pharmacokinetics in skin with stimulated Raman scattering microscopy and deep learning. Journal of Investigative Dermatology. 141 (2), 395-403 (2021).
- Ghosh, B., Reddy, L. H., Kulkarni, R. V., Khanam, J. Comparison of skin permeability of drugs in mice and human cadaver skin. Indian Journal of Experimental Biology. 38 (1), 42-45 (2000).
- Nielsen, J. B., Plasencia, I., Sørensen, J. A., Bagatolli, L. Storage conditions of skin affect tissue structure and subsequent in vitro percutaneous penetration. Skin Pharmacology and Physiology. 24 (2), 93-102 (2011).
- Barbero, A. M., Frasch, H. F. Effect of frozen human epidermis storage duration and cryoprotectant on barrier function using two model compounds. Skin Pharmacology and Physiology. 29 (1), 31-40 (2016).
- Babu, R., et al. The influence of various methods of cold storage of skin on the permeation of melatonin and nimesulide. Journal of Controlled Release. 86 (1), 49-57 (2003).
- Skelly, J. P., et al. FDA and AAPS report of the workshop on principles and practices of in vitro percutaneous penetration studies: relevance to bioavailability and bioequivalence. Pharmaceutical Research. 4 (3), 265-267 (1987).
- OECD. Guidance document for the conduct of skin absorption studies. OECD. , (2004).
- OECD. Test no. 428: Skin absorption: In vitro method. OECD. , (2004).
- Saar, B. G., et al. Video-rate molecular imaging in vivo with stimulated Raman scattering. Science. 330 (6009), 1368-1370 (2010).
- Saar, B. G., Contreras-Rojas, L. R., Xie, X. S., Guy, R. H. Imaging drug delivery to skin with stimulated Raman scattering microscopy. Molecular Pharmaceutics. 8 (3), 969-975 (2011).
- Pence, I. J., Kuzma, B. A., Brinkmann, M., Hellwig, T., Evans, C. L. Multi-windowsparse spectral sampling stimulated Raman scattering microscopy. Biomedical Optics Express. 12 (10), 6095-6114 (2021).
- Herkenne, C., et al. In vivo methods for the assessment of topical drug bioavailability. Pharmaceutical Research. 25 (1), 87-103 (2008).
- Alfonso-Garcıa, A., Mittal, R., Lee, E. S., Potma, E. O. Biological imaging with coherent Raman scattering microscopy: a tutorial. Journal of Biomedical Optics. 19 (7), 071407 (2014).
- Osseiran, S., et al. Longitudinal monitoring of cancer cell subpopulations in monolayers, 3D spheroids, and xenografts using the photoconvertible dye DiR. Scientific Reports. 9 (1), 1-10 (2019).
- Evennett, P. Kohler illumination: a simple interpretation. Proceedings of the Royal Microscopical Society. 28 (4), 189-192 (1983).
- Sanderson, J. Fundamentals of microscopy. Current Protocols in Mouse Biology. 10 (2), 76 (2020).
- Schindelin, J., et al. Fiji: an open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Hunter, J. D. Matplotlib: A 2D graphics environment. Computing in Science & Engineering. 9 (3), 90-95 (2007).
- Wickham, H. . ggplot2: Elegant Graphics for Data Analysis. , (2016).
- Kim, H., Han, S., Cho, Y. S., Yoon, S. K., Bae, K. Development of R packages:'Non-Compart' and 'ncar' for noncompartmental analysis (NCA). Translational and Clinical Pharmacology. 26 (1), 10-15 (2018).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon