Method Article
Tümör türevi Exosomes ölçmek için Nanoplasmon-gelişmiş saçılma ve düşük büyütme mikroskop görüntüleme kullanma
Bu Makalede
Özet
Hastalıklı ve malign hücreler için dış türev biomarkerlerin klinik çevirisi, hızlı ve doğru ölçme yöntemlerinin olmaması ile engellenmiştir. Bu raporda, küçük hacimli serum veya plazma örneklerindeki belirli dış alt türleri ölçmek için düşük büyütme koyu alan mikroskop görüntülerinin kullanımı açıklanmaktadır.
Özet
Enfekte veya malign hücreler sıklıkla daha fazla exosomes salgılıyor, sirkülasyonda hastalık ilişkili exosomes yüksek seviyelere yol. Bu dış, hastalık tanısı için Biyomarkörler olarak hizmet ve hastalık ilerlemesi ve tedavi tepkisi izlemek için potansiyele sahiptir. Ancak, çoğu dış analiz prosedürleri, genellikle zaman alıcı ve emek yoğun olan ve böylece klinik ayarlarında sınırlı yarar eksozom yalıtım ve arıtma adımları gerektirir. Bu raporda, ayrı izolasyon ve arıtma adımlarına gerek kalmadan harici dış membranlardaki belirli biyomarkerlerin analiz edilmesi için hızlı bir prosedür açıklanmaktadır. Bu yöntemle, exosomes bir slaytın yüzeyinde exosome spesifik antikorlar tarafından yakalanır ve daha sonra bir hastalığa özgü nanopmakale-konjuçe antikor probları ile hybrioklu. Hybridization sonra, hedef eksozom nüfusun bolluğu düşük büyütme karanlık alan mikroskop analiz ederek belirlenir (lmdfm) bağlı nanopartiküller görüntüleri. Bu yaklaşım, hastalığa bağlı membran ilişkili dış biyomarkerleri analiz etmek için araştırma ve klinik kullanım için kolayca benimsenebilir.
Giriş
Exosomes çoğu hücre türlerinden serbest bırakılır ve hücre-hücre iletişimleri, çeşitli hastalıklarla ilişkili patofizyolojik süreçler de dahil olmak üzere önemli bir rol oynamaktadır, onlar belirli doku veya hücre türlerine ev olabilir, ve nükrenik asitler çeşitli içeren , proteinler ve menşe hücresini yansıtan ve kendi alıcı hücreleri1,2,3,4üzerinde düzenleyici etkileri oluşturabilir lipidler. Exosomes genellikle hastalık Devletlerinde yüksek seviyelerde salgılanan, hem bitişik hem de uzak hücreler ile etkileşime girebilir ve dolaşımda nispeten yüksek konsantrasyonda, tükürük, idrar, pankreas ve safra dahil olmak üzere en diğer vücut sıvılarının yanı sıra bulunur meyve suyu ve Bronkoalveoler Lavaj sıvısı5,6,7,8,9,10,11. Bu bolluk ve insan vücudu sıvılarında dış istikrar, onların bilgi açısından zengin doğası ile birleştiğinde, onları hastalık tanı ve tedavi izleme için ideal Biyomarkörler yapar.
Bu tümör-spesifik veya seçici faktörler, tümör ilişkili mutant allerleri de dahil olmak üzere hastalık Biyomarkörler olarak hizmet verebilir içeren tümörlerin türetildiği (TDEs), içerir. TDEs, tümör gelişimi ve metastaz kolaylaştırmak için tümör mikroortamının yeniden modelleme katılabilir ve anti-tümör tepkiler düzenleyen12. Artan TDE salgılanması çoğu kanserlerin ortak bir fenotürü ve tümör mikroortamın çeşitli özellikleri, hipoksi dahil, Asidik pH, ve inflamasyon, dış salgılanmasını teşvik bilinmektedir. Şaşırtıcı şekilde, exosomes, toplam eksozom düzeyinde bir artış, kendisi, bir kanser Biomarker olarak işlev salgılıyor hücrelerin sayısını verilen. Örneğin, son çalışmada, safra suyunda toplam EV konsantrasyonu% 100 doğruluk7olan ortak safra kanalı stenozu hastalarda malign ve nonmalign ayrımcılık bulundu. Plazma dahil olmak üzere diğer vücut sıvılarını kullanarak çalışmalar ile benzer sonuçlar bulundu. Ancak, konu varyasyonu ve diğer şok edici faktörlere tabi potansiyeli nedeniyle, hastalık biyolojik olarak exosomes araştıran çoğu çalışmalar, seçilerek toplam eksozom yerine tdes ile ilişkili biyomarker tespiti odaklı Numara.
Ancak, en çok bildirilen dış tahlil yaklaşımlarının zaman alıcı ve emek yoğun yalıtım prosedürleri gerektirdiğinden, dış biomarkerlerin klinik pratiklere çevrilmesinde zorlu kalır 13. Şu anda popüler eksozom yalıtım yöntemleri ultracent, yoğunluk degradeler, boyut-dışlama, Co-yağış, benzeşimi yakalama ve mikrofluidik yalıtım yaklaşımlar içerir. Ultracent, "altın standart" yöntemidir ve en sık eksozom izolasyonları için kullanılır, ancak bu prosedür zaman alıcı ve dış hasar ve eksozom membran kümeleme ile sonuçlanır proteinler, lipoproteinler ve sonraki analizleri etkileyebilecek diğer faktörler14. En dış izolasyon yöntemleri, ultracent, dahil olmak üzere, dış (30 – 150 Nm) mikro-veziküller (100 – 1000 Nm) ve apoptotik organları (100 – 5000 Nm), farklı mekanizmalar aracılığıyla ortaya çıkan ve farklı fonksiyonları var, boyutu nedeniyle ayrılmış Bu gruplar arasında çakışıyor, ve eksozom nüfusun çeşitliliği15. Yeni yaklaşımlar, dış hasar ve kontaminasyon azaltılması sırasında eksozom iyileşme artırarak duyarlılık ve yeniden üretilebilirliği artırmak için gerekli olan, bu tür yöntemlerle dayalı herhangi bir konuda da onları işlemek için optimize edilmesi gerekecektir rağmen klinik ayarlarında uygulamalara çeviri için uygundur.
Birkaç son çalışmalar doğrudan vücut sıvılarından exosomes yakalamak ve analiz etmek için entegre platformlar istihdam önerdi. Bu yöntemler mikrofluidik, Elektrokinetik, benzeşme yakalama ve eksozom yalıtım için çeşitli yöntemler, elektrokimya, yüzey plasmon rezonans ve diğer yöntemler yakalanan exosomes algılamak için istihdam. Karmaşıklık, gider, düşük verim veya diğer sorunlar nedeniyle bu yaklaşımların birçoğu klinik ayarlarında ne kadar uygulanabilir olduğu açık değildir.
Biz toplam exosomes ve spesifik eksozom alt türlerinin hassas ve spesifik kantifikasyon için kullanılabilir bir hızlı ve ucuz tahlil geliştirdik, gibi hastalık ilişkili exosomes, tdes gibi, hangi örnek sadece küçük bir miktar gerektirir ve hangi klinik ortamlar için uygun aerodinamik bir iş akışı kullanır. Bu testin içinde, bir slayt, doğrudan küçük hacimli plazma veya serum numuneleri mevcut hedef exosomes yakalamak için dış yüzey üzerinde ifade bir eksozom özel veya hastalığa özgü Marker bağlamak antikorlar ile kaplı üzerinde kuyuları uygulanan Slayt. Yakalanan exosomes daha sonra bir antikor ile hybri,-bu exosomes üzerinde ilgi biyomarker tanıyan konjudi nanopmadde, hangi ya genel bir eksozom marker veya bir faktör bir dış ilgi alt türü için özel olabilir. Bu örnek kuyuların görüntüleri daha sonra bir karanlık alan mikroskop (DFM) kullanılarak yakalanan ve nanopartiküller her örnek iyi6,16,17yakalanan faiz exosomes bağlı dağılmış ışık ölçmek için analiz edilmiştir. Özellikle, düşük büyütme DFM (LMDFM) tarafından iyi bir tüm örnek görüntüleme kullanıcılar doğrudan sonraki görüntü analizi için yakalamak için hangi alanları seçmeniz gerekir, yüksek büyütme DFM analizleri ile karşılaşılan bir seçim önyargı önler. LMDFM görüntü analizi, çizik ve örnek enkaz dahil olmak üzere yüzey düzensizlikleri ışık saçılma eserler tabidir, ancak bu arka plan NıH görüntü analiz programında çalıştırmak için geliştirilen basit bir gürültü azaltma algoritması kullanılarak azaltılabilir, Imagej (https://imagej.nih.gov/ij/). Bu algoritma önce sonraki çözümleme için görüntünün bölgesini tanımlamak için iyi örnek sınırlarını algılamak için kullanılan bir giriş kontur eşik uygular. Bu kontur bölgesi tarafından tanımlanan bölge, görüntünün kırmızı, mavi ve yeşil kanallarında bulunan ayrı sinyale ayrılır ve mavi kanal, yüzey yapıtlarından kaynaklanan sinyali ve Nanorod 'tan düzensiz aydınlatmayı kaldırmak için kırmızı kanaldan çıkarılır. Sinyal.
Bu makalede, plazma veya serum numunelerinde toplam veya spesifik dış seviyeleri hızla ölçmek için bu tahlil nasıl kullanılacağı açıklanır.
Protokol
1. nanopmadde problarının hazırlanması
Not: Bu deney, neutravidin polimerleri (AV) ile uyumlu bir şekilde konjuli olan ve DFM üzerine kırmızı (641 nm Peak) saçılma sinyali üreten bir yüzey plasmon rezonans zirvesine sahip olan functionalized Gold nanorods (AuNRs; 25 Nm çapı x 71 nm uzunluğunda) kullanmaktadır. Aydınlatma.
- 4 °c ' de santrifüjleme ve Aspir8.500 asyon (10 dakika için 40 x g) ve ardından aunr-av Pelet askıya alındıktan sonra son santrifüjleme ve aspirasyon adımıyla üç kez (2,56 x 10 11 partiküller), 3 7,0 200 kat 40 μL PBS içinde.
- Bu aunr-av süspansiyonu 10 μL biyotinlenmiş antikor ile karıştırın (0,5 mg/ml), dış ilgi alt türünün yüzeyinde bir antijen için özeldir ve 150 μL PBS ve sonra 4 °c ' de 2 h için bir mikser kullanarak nötravidin-biotin bağlamanın tamamlanmasına izin vermek için karıştırın.
- Ortaya çıkan antikor-konjugated AuNRs (AuNR-IgG) santrifüjleme ve aspirasyon (6.500 x g 10 dakika Için 4 °c ' de) ile üç kez yıkayın ve sonra 200 ΜL PBS onları askıya ve 4 °c kullanıma kadar saklayın.
Not: steril teknik ve kısa depolama süreleri, AuNR-IgG ' ı k i kontaminasyonu ve bozulması önlemek için kullanılmalıdır. Bu onların konjugasyon 24 saat içinde antikor-Conjugated AuNRs kullanmak en iyisidir.
2. EV yakalama slaytlarının hazırlanması
- PBS 'de 0,025 mg/mL 'Lik bir dış yakalama antikorları seçmiş ve bu seyreltinin 1 μL/kuyu 'yı çok iyi bir protein A/G kaydırağı üzerine ekleyecek ve daha sonra bu slaytı 37 °C ' de 1 saat boyunca nemlendirilmiş bir odada tutuşturarak, antikor proteini A/G 'de immobilize hale getirilmesine izin verir kaydırın.
- İlişkisiz antikorları çıkarmak için aspirate kuyuları ve 1 μL/kuyu PBS ek ve aspirasyonu ile üç kez kuyuları yıkayın, sonra her iyi yük 1 μL engelleme tampon (bkz. malzeme tablosu37) kalan protein bağlama sitelerini kilitleyin.
- Engelleyici tamponları kaldırmak için aspirate kuyuları, 1 μL/kuyu PBS 'nin eklenmesi ve aspirasyonu ile üç kez yıkama kuyuları ve hemen dış yakalama ve analiz için engellenen slaytları kullanın.
3. Standart eğrisi hazırlama
- Belirli bir dış alt türünün mutlak veya göreceli zenginliğini doğru bir şekilde ölçmek için, Kullanıcı, ilginin dış yüzey biyomarker değerini tek bir şekilde ifade eden saf bir dış nüfus ile standart bir eğri oluşturmalıdır. Bu çalışmada, pankreas kanseri aşaması ve prognoz ile bildirilen bir ilişki olan metasozun ilişkili membran proteini, ephrin a2 reseptörü ifade eden exosomların bolluğunu analiz eder6,18.
Not: insan pankreas kanseri hücre hattı panc-1 ve onun exosomes bu protein ve izole exosomes bu hücre çizgisinin ifade bilinirler karmaşık eksozom bu protein ifade exosomes sayısını ölçmek için standart bir eğri oluşturmak için kullanıldı Örnekleri. - Medya içinde dış birikimine izin vermek için, serum içermeyen kültür medyasında 37 °c ' de 48 saat için kültür hücreleri, daha sonra süspansiyon kültürlerinin santrifüjasyonu veya bağlı hücre kültürlerinden kültür medyasını doğrudan aspirasyon ile hücre kültürü süpernatanlarında izole.
- 2000 x g 'de toplanan medyayı 30 dakika boyunca Santrifüjden çıkarın ve supernatant 'i kurtarın.
- Uygun kapasitenin 0,45 μm düşük protein bağlayıcı filtre ünitesi (örn. 250 ml politersülfon vakum filtrasyon ünitesi) ile açıklık kültürü süpernatant filtre.
- 250 μL son hacmine 100.000 nominal moleküler ağırlık limit filtre sistemi kullanarak 3200 x g 'de santrifüjleme ile elde edilen süzüntü konsantre olun. Bu filtreden tutulan hacmi toplayın, sonra filtreyi 200 μL PBS ile yıkayın ve bu yıkama hacmini toplanan eksozom numune hacmine birleştirin.
- Bu numune Santrifüjü 45 dakika 21.000 x g ve dikkatle supernatant kurtarmak, herhangi bir çöktürülmüş malzeme toplamak için dikkat çekmek.
- 100.000 x g 'de kurtarılan süpernatant 'i 3 saat boyunca santrifüjler. Süpernatant uzakta aspirate ve 100 μL PBS içinde eksozom Pelet toplamak.
- Uzun süreli depolama için 24 saat içinde veya-80 °C ' de kullanıldığında, elde edilen dış süspansiyon süspansiyonları 4 °C ' de saklayın.
Not: dondurma çözme döngüleri tekrarlamak için eksozom örnekleri konu etmeyin. - Eksozom sayıların doğrudan ölçümü ile karıştırıldıktan sonra eksozom süspansiyon bir kısım ölçmek (örneğin, nanopartikül izleme analizi veya ayarlanabilir direnç nabız algılama veya mikro-bicinchoninic tarafından eksozom endoglikozidazları protein konsantrasyonu ölçme asit tahlil, ya da eşdeğer bir yöntem, bir araç olarak eksozom miktarı yaklaşık)16,19.
- Nano madde sinyalinin giriş eksozom sayı veya protein içeriğine karşılaştırılması izin vermek için eksozom süspansiyon seri dilüsyonları bir dizi oluşturun.
- Her bir dış standartın 1 μL ' sini, tahlil plakasının her bir çoğaltma kuyusundan aktarın.
Not: Standart eğrileri nanopartikül sinyal ve eksozom konsantrasyon arasındaki korelasyon çizgisinin eğimi hesaplamak için kullanılabilir (1) tahlil performansını değerlendirmek ve (2) deneysel numunelerde hedef exosomes göreli konsantrasyonu belirlemek.
4. insan plazma veya serum numuneleri işleme
- Standart yöntemlerle plazma veya serum örnekleri toplayın ve dış analiz için gerekli olana kadar-80 °C ' de saklayın. Bir oda sıcaklığında su banyosunun örneklerini hızla çözün. Homojen süspansiyonu teşvik etmek için çözülmüş numuneleri inversiyon ile tekrar tekrar karıştırın.
Not: serum ve plazma örneklerinden gelen sonuçlar eşdeğer olmayabilir, çünkü pıhtılaşma reaksiyonu sırasında önemli bir exosomes salınımı vardır. - 500 x g 'de santrifüj plazma veya serum numuneleri 15 dakika boyunca protein agregaları ve diğer enkaz çökeltir. Plazma veya serum numunesi bir kısım taze bir tüp aktarmak ve bir 1:1 seyreltme oluşturmak için PBS ekleyin. Seyreltilmiş numuneyi uygun olarak nazik voreksleme veya inversion ile karıştırın. Her bir plazma veya serum süspansiyonunun 1 μL 'i, test plakasının her bir çoğaltma kuyusundan aktarın.
5. exosome yakalama ve algılama
- 1 μL/Iyi eksozom örnek ile engellenen bir ev yakalama slaytı yük kuyuları, örnek başına 8 çoğaltır kullanarak, ve bir gece 4 °c ' de nemlendirilmiş bir odada slayt kulkayak. Tüm numune kuyularını aspirate ve ardından kuyuları yıkamak için 1 μL/kuyu PBS ekleyin ve yüklü eksozom örneğinden ilişkisiz exosomes ve diğer kirleticileri kaldırın.
- Daha önce hazırlanmış bir AuNR-IgG süspansiyonunun 1 μL/kuyu ile örnek kuyuları yükleyin (yukarıdaki Bölüm 1 ' e bakın) ve nemlendirilmiş bir odada 37 °C ' de 2 saat boyunca slaytı inküt. Nanopartikül solüsyonu Aspire ve PBS içinde slayt yıkama 0,01% Tween-20 (PBST) ile 10 dakika için bir mikser kullanarak, sonra Aspire ve 10 dakika için deiyonize su ile tüm numune kuyuları yıkama dönen bir mikser kullanarak, ve hava-kuru sonraki lmdfm görüntüleri için.
Not: varyasyon (CVs) arası tahlil katsayıları aynı numunenin sekiz çoğaltır tarafından değerlendirilir. CVs >% 20 ' si sergileyen örnekler, yeterli örnek varsa, bilgilendirici olmayan ve tekrar edilmelidir.
6. DFM görüntü yakalama
- Karanlık alan kondansatörü (1,2 < na < 1,4) ve 4X objektif bir 1/220 s pozlama süresi istihdam ile donatılmış bir mikroskop bağlı bir dijital kamera kullanarak tutarlı aydınlatma altında eksozom kantifikasyon için görüntüleri yakalayın.
- Görüntü yakalama yazılımını açın.
Not: aşağıda açıklanan protokol için NIS-Elements mikroskop görüntüleme yazılımını ( malzeme tablosunabakın) kullanıyoruz, ancak görüntü yakalama parametrelerine uyan başka bir yazılım kullanmak mümkündür. NIS-Elements Viewer görüntüleme yazılımı, analiz, görselleştirme ve arşivleme araçlarını içeren görüntü dosyalarını ve veri kümelerini görüntülemek için ücretsiz bir bağımsız programdır. Aşağıdaki parametreler de otofokus ile mikroskop ve birden fazla görüntü otomatik olarak yakalanan ve tek bir görüntü içine dikişli izin otomatik bir aşama için de vardır. - Slaytı mikroskop aşamasına ters yerleştirin, slayt konumunu ayarlayın ve kaydıranın arkasına küçük bir damla daldırma yağı uygulayın, böylece kondenser lensin slaytla bağlantı kurar.
- Yazılım arayüzündeki Live düğmesine tıklayın ve görüntü doymamış olduğundan emin olmak için yüksek konsantrasyon standardına karşı pozlama süresini ayarlayın.
- Alma sekmesinden büyük görüntü Tara penceresini açın ve yazılım arabirimi parametrelerini aşağıdaki gibi ayarlayın: makro görüntü optik conf = akım; Amaç: 2:10X, tarama optik conf = akım, Amaç: 2:10X; Dikiş çakışma = 20%; Ile dikiş = optimum yol.
- Büyük görüntü oluştur'u seçin, aşama hareketi sırasında etkin deklanşöü kapatın, her yakalamadan önce bekleyin: 20 MS, Başlangıç olarak el ile odaklanınve her 20 alanda adım adım odak kullanın. Bu ayar taranan görüntülerle kaydedilecektir.
- Hedef tarama alanının sol üst sağ alt sınırlarını tanımlamak için mikroskop aşamasını taşıyın. Odaklı görüntüde herhangi bir aydınlatma düzensizlikleri en aza indirmek için ekranda net bir görüntü elde etmek ve kondansatör ayarları ve çevresel aydınlatma ayarlamak için odağı ayarlayın.
- Yazılımda görüntü çıktı dosyasını adlandırın. Scan düğmesine tıklayın ve mikroskop tarama ve oluşturmak ve tüm slayt bir dikişli görüntü kaydetmek için izin verin.
- Kullandığınız görüntü yakalama yazılımı ile kaydedilmiş görüntüyü açın ve ımagej DSM eklentisi üzerinde sonraki analiz için 1/8 ölçekte kaydedin.
7. DFM görüntü analizi
- Imagej programını indirin (https://imagej.nih.gov/ij/). Https://imagej.net/Plugins#Installing_plugins_manually adresinde listelenen talimatları kullanarak DSM algoritması eklentisini ımagej 'ye yükleyin.
- Imagej yazılımını açın, sonra DSM algoritması içinde aşağıdaki giriş parametrelerini ayarlayın: kontur eşik (CT) = 253,020, tip = kırmızı, Merkez ölçek (ler) = 0,8, düşük (lt)/yüksek (HT) miktar limiti = 0/62.
- Imagej ile 6,8 bölümünden kaydedilmiş görüntüyü açın. Eklentiler sekmesinden DSM tarama düğmesini seçin, ardından açılan görüntüye göre sütun ve satır sayısını tanımlayın. Program algılama alanları tanıyabilir ve analiz nanopartikül Scatter yoğunluğu alanlarda otomatik olarak göre. DSM tarama penceresi içinde aşağıdaki giriş parametrelerini ayarlayın: yüzdesini yeniden boyutlandırma = 25, spot çapı (piksel cinsinden) = 190 – 200, çap aralığı = 32, artış çapı (piksel cinsinden) = 8, DSM yapılandırma-düşük limit = 0, yüksek sınır = 62, bitişik mesafe = 100, çıkarmak Bias = 0.
Not: nanopmaddenin dağılım yoğunluğunun sonuçları, slayttaki bağlı exosomların miktarını yansıtır.
Sonuçlar
Multi-Well protein A/G kaplı slaytlar (Şekil 1a) Anti-EphA2 antikor ile functionalized ve daha sonra özellikle pankreas kanseri olan ve olmayan hastaların serum örneklerinden EphA2-pozitif exosomes yakalamak için kullanılan (1 μL/Well) ve inkübe bir anti-CD9 antikor (Şekil 1B) ile conjuated altın nanoçubuklar ile. Bu nanopartiküllerden dağınık ışık DFM görüntüleri her iyi bağlı EphA-2 pozitif exosomes ölçmek için ımagej yazılım DSM eklentisi kullanılarak analiz edildi. DSM algoritması otomatik olarak bir örnek iyi sınırlarını tanımlar, yapılardan gürültü filtreler, her kuyunda dağınık sinyali hesaplar ve bu bilgileri çıkarır (Şekil 2). DSM algoritması, numunedeki çizik veya enkaz üzerindeki ışık saçılma yapılarını şiddetle zayıflatır ve nanopmakale algılamanın hassasiyetini ve yeniden üretilebilirliğini geliştirir ve yüksek verim için bir toplu Slayt görüntülerini otomatik olarak işleyebilir Kullanın. Bu algoritma, görüntü arka planını çıkarmak, her bir kuyunda saçılma sinyalini hesaplamak ve bir veri ve görüntü dosyası (Şekil 3) çıktısını almak için Kullanıcı tarafından ımagej komutlarını ve parametreleri girişini kullanır. İlgi bölgeleri, ımagej makro programının kontur eşiği işlevini kullanarak yakalama görüntüsünde yüksek yoğunluklu iyi sınırlar tarafından tanımlanır. Görüntü analizleri, her bir kuyu için nanopartikül saçılma yoğunluğunu hesaplamak için önceden tanımlanmış bir kontur eşik ve görüntü parametrelerini kullanır.
Önceki çalışmalarımız (Liang ve ark.6' nın ek bilgileri) olarak bildirilen, transmisyon elektron mikroskobu ile karakterize panc-1 hücreli kültürlerden izole exosomes ve Batı leke boyutu aralığı sergiledi, morfoloji, ve protein Marker ifade yüksek saflıkta eksozom örnek ile tutarlı. Önceki çalışmalarımız ile aynı prosedür ile hazırlanan panc-1 exosomes, eksozom quantification için bizim npes tahlil doğrulamak için burada kullanıldı. Bu tahlil bir anti-EphA2 antikor toplam eksozom nüfusu ve genel eksozom protein CD9 karşı bir antikor gelen exosomes büyük bir nüfus yakalamak için yakalanan exosomes algılamak için kullanılır. 0,24 ila 1,2 μg/μL arasında değişen protein konsantrasyonlarıyla seri seyreltilmiş PANC-1 dış numuneler kullanılarak elde edilen sonuçlar, çoğul kuyularda (Şekil 4A) iyi bir yeniden üretilebilirlik ve scatter tepkisi ile protein konsantrasyonu (Şekil 4b).
Bu yöntemin potansiyel uygulama göstermek için, pankreas kanseri olan ve olmayan hastalarda serum numuneleri kanser ilişkili biyomarker EphA2 ifade serum exosomes bolluk algılamak için analiz edildi, bir anti-EphA2 antikor kullanarak doğrudan bir anti-CD9 antikor ile konjuli serum ve nanopartiküller hedef exosomes yakalama bağlı exosomes tespit etmek. Bu analiz, pankreas kanseri hastalarından gelen serum numunelerinin EphA2 + exosomes (Şekil 5) ' in kontrollerinden daha önemli ölçüde daha yüksek olduğunu göstermiştir.
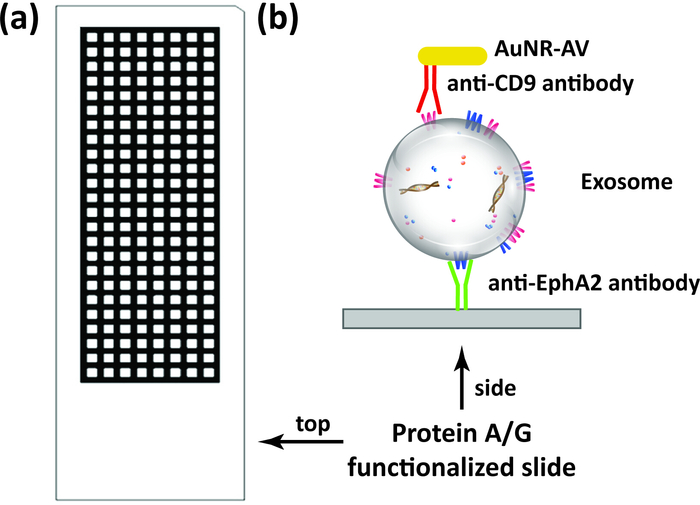
Resim 1: exosome kantifikasyon şeması. (A) bu tahlil kullanılan Multi-Iyi protein A/G slaytlar (192 kuyuları) şematik. (B) hedef exosomes doğrudan numunelerden yakalanan, serum ve plazma dahil, yakalama antikor üzerinde yüzey immobilizasyon tarafından (örneğin Anti-EphA2 antikor) slayta bağlı, ve daha sonra altın nanoçubuklar ile konjuk bir algılama ile inkübe antikor (örneğin Anti-CD9 antikor) DFM görüntü analizi tarafından analiz önce. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
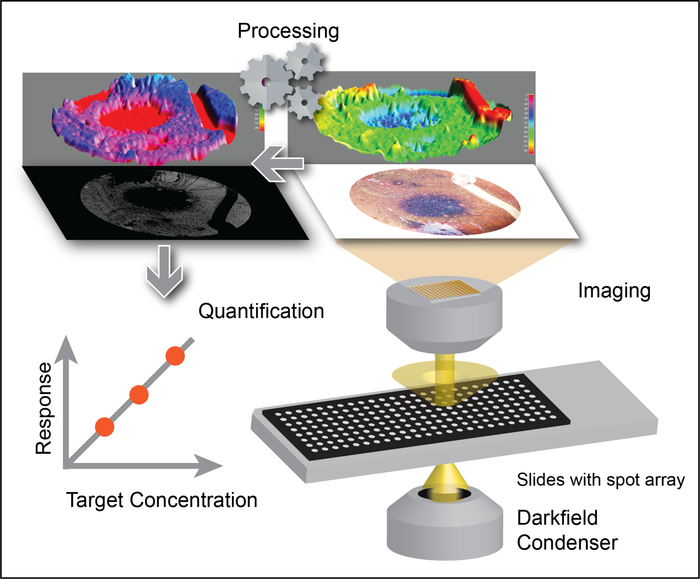
Şekil 2: DSM algoritmasını lmdfm görüntülerine uygulayarak exosome kantifikasyon. Düşük büyütme görüntüleri, arka plan sinyali ve çizik ortaya çıkabilir sinyal eserler ortadan kaldırmak için DSM algoritması ile işlenir, boşlukları karıştırma, enkaz, ve düzensiz örnek aydınlatma altın Nanorod sinyalinin sağlam tespiti için izin, hangi Dış konsantrasyon ile ilişkilendirir. Bu rakam, Sun, D. ve Al 'dan izin ile adapte edilmiştir. düşük büyütme Dark-Field mikroskop uzak alan görüntülerde Nanopmakale ışık saçılma ölçülerek için gürültü azaltma yöntemi. Analitik Kimya. 88 (24), 12001-12005 (2016). Copyright (2016) Amerikan Kimya Derneği. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
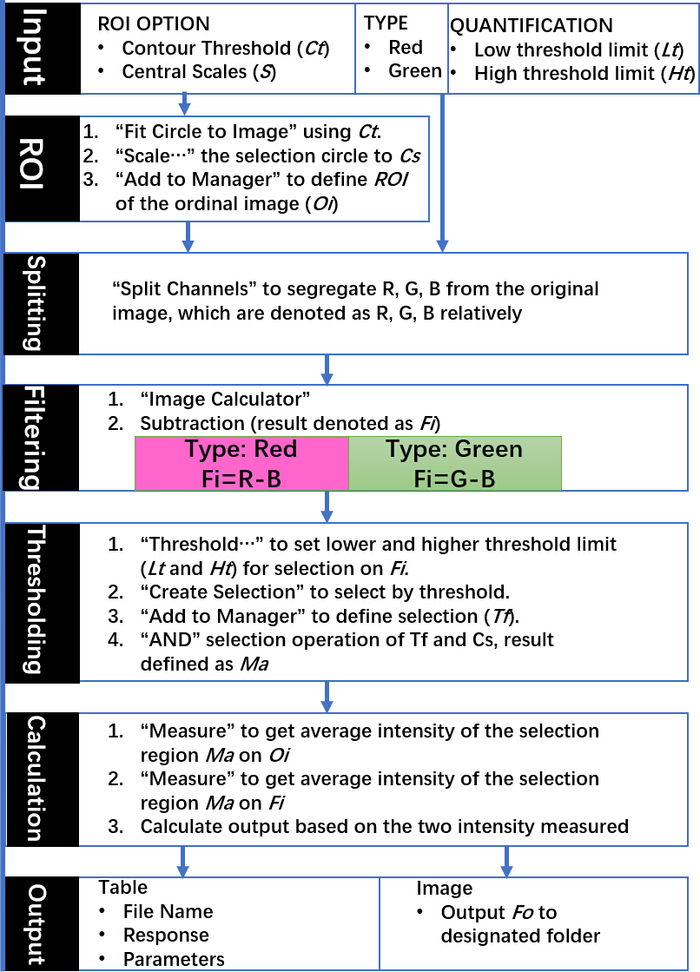
Şekil 3: DSM algoritması komutları ve çıkışları şematik. Belirtilen adımlar ımagej 'den yerel komutlar kullanır ve tüm giriş parametreleri grafik kullanıcı arabirimi aracılığıyla deneylerin gereksinimlerine göre seçilir. Bu rakam, Sun, D. ve Al 'dan izin ile adapte edilmiştir. düşük büyütme Dark-Field mikroskop uzak alan görüntülerde Nanopmakale ışık saçılma ölçülerek için gürültü azaltma yöntemi. Analitik Kimya. 88 (24), 12001-12005 (2016). Copyright (2016) Amerikan Kimya Derneği. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
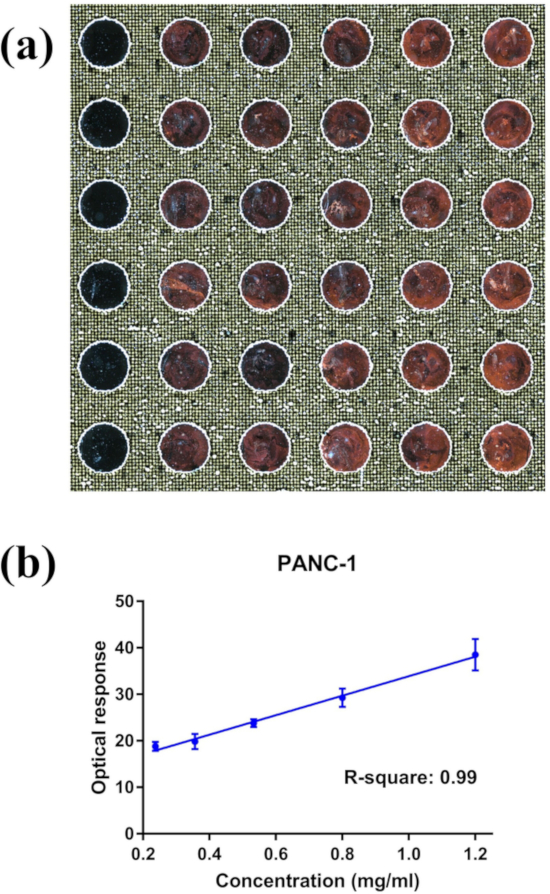
Şekil 4: temsilci nPES LMDFM görüntüleri ve DSM çıkış verileri. (A) bir npes tahlil lmdfm görüntü panc-1 exosomes bir konsantrasyon gradyan analiz ve (B) bu slayttan optik sinyal ve eksozom konsantrasyon doğrusal korelasyonu (soldan sağa: 0,24, 0,356, 0,53, 0,80, 1,20 μg/μL her sütun için sırasıyla). Veri Mean ± SE olarak sunulur, n = 6, bir Pearson korelasyon katsayısı R2 = 0,99 ve her konsantrasyon çoğaltır için varyasyon katsayısı 0,2 <. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
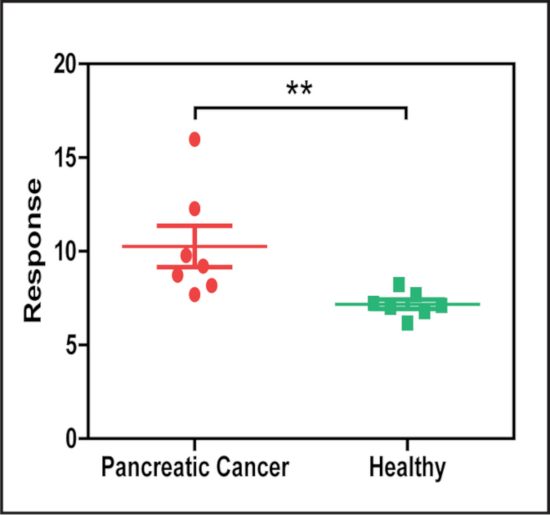
Şekil 5: EphA2+ exosomes 'ın LMDFM sinyali, pankreas kanseri olan ve olmayan hastalarda serumda farklılık gösterir. Anti-EphA2 yakalama antikor (kanser ilişkili) ve anti-CD9 algılama antikor (genel eksozom Marker) kullanarak npes tarafından analiz serum numuneleri, hastaların serum örneklerinde EphA2 + exosomes konsantrasyonunda önemli bir fark sergiledi ve pankreas kanseri olmadan (N = 7/Grup). Sonuçlar, Mann-Whitney U-test (iki taraflı) tarafından ortalama ± SE. * *p = 0,002 olarak sunulur. Bu rakam, [Sun, D. ve al. düşük büyütme Dark-Field mikroskop Far-Field görüntülerde Nanoparticle ışık saçılma ölçülerek için gürültü azaltma yöntemi. Analitik Kimya. 88 (24), 12001-12005 (2016)]. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
Tartışmalar
Exosomes multiveziküler organları üreten dış endosome membranın düzenlenmiş invaginasyonlarının ortaya, Olgun serbest bırakmak için plazma membranı ile füzyon geçmesi intraluminal veziküller çok sayıda içeren özel bir alt kümesi ekstrasellüler uzayda içine exosomes. Bu biyogenesis yolu nedeniyle, exosomes oluşturan veya endosome membran ile sigorta membran fraksiyonları ile ilişkili membranlar bağlı faktörler, yanı sıra birden fazla farklı türde sitosolik bileşenleri, ve böylece proteinler, DNA kargoları içeren taşıyabilirler ve çeşitli RNA alt türleri (mRNAs, microRNAs, uzun kodlama olmayan RNAs), Orijin hücresinin fenotipini yansıtabilir20. Exosomes çoğu değil tüm hücre türleri tarafından salgılanan beri, hastalıklı veya malign hücrelerden artan salgılanmasını gösterebilir, ve çoğu vücut sıvılarında birikir, exosomes umut verici bir minimal olarak kapsamlı ve sistematik soruşturma konusu belirli hastalık koşullarını tespit etmek ve tedavi yanıtlarını izlemek için invazif anlamına gelir21.
En güncel dış analiz için gerekli olan eksozom yalıtım, uzun ve emek yoğun bir işlemdir, potansiyel tıbbi alaka ile dış ilişkili biyomarkerlerin klinik çevirisini kısıtlayarak. Birçok yaygın izolasyon yöntemleri (ultracent, büyüklüğü-dışlama, yağış, vb) genellikle yeterince dış (30 – 100 Nm) mikro-veziküller (100 – 1000 Nm) ve apoptotik organları (100 – 5000 Nm) arasında çakışmalar nedeniyle ayırt etmez onların boyutu aralıkları veya fiziksel özellikleri veya dış bütünlük15zarar verebilir. Yeni yaklaşımlar daha hızlı dış analizlere izin verebilir geliştirme aşamasında, ancak bu platformlar nedeniyle klinik ayarları birçok uygulamak için ne kadar mümkün olabilir açık değildir.
Bu raporda, düşük büyütme karanlık alan mikroskop görüntüleri kullanarak Nanoparticle tabanlı yüksek verimlilik eksozom kantifikasyon sağlayan bir yeni yaklaşım sunuyoruz. Bu yöntem eksozom arıtma, pahalı özel ekipman veya yeni teknik uzmanlık gerektirmez ve böylece çoğu araştırma ve klinik ayarlarında hızlı çeviri için zorunlu olmalıdır. Tahlil sonuçları standart bir eğriye kıyasla belirli bir biyomarker taşıyan bir hedef dış nüfusun konsantrasyonunu tam olarak ölçmek için testimiz uygulanabilir, çünkü bizim sonuçlar sergi güçlü bir doğrusal korelasyon (R2 = 0,99) Optik yanıt ve dış konsantrasyon arasında. Bu yaklaşımın gerçek dünya potansiyelini göstermek için, bu yöntemi kullanılan ve olmayan hastalarda elde edilen serum örneklerinde pankreas kanseri ile ilişkili bir dış biyomarker konsantrasyonunun ölçülmesine yönelik veri temin ettik pankreas kanseri.
LMDFM 'de, tüm örnek iyi yüksek büyütme DFM analizlerinde bulunan seçim önyargı önlemek için görüntülenmiş, burada kullanıcıların doğrudan sonraki görüntü analizi için yakalamak için örnek alanları seçmeniz gerekir, ancak yüzeyden ışık saçılma eserler tabidir çizikler ve örnek enkaz dahil olmak üzere düzensizlikler. Bu arka plan NıH görüntü analiz programı, ımagej üzerinde çalışan DSM gürültü azaltma algoritması kullanarak hedef exosome-türetilmiş sinyal algılamak için azaltılabilir, ancak bakım hala dinamik aralığını azaltabilir gibi eserler tanıtmak önlemek için alınmalıdır tahlil.
Bu tahlil kullanılan malzemeler:
1 μL/kuyu tutan Multi-Well SuperProtein A/G slaytlar Arrayit Corporation (AGMSM192BC) satın alınmıştır. Nano maddeler Nanopartz (C12-25 -650-TN-DIH-50-1, 6,4 x 1012/ml) elde edilmiştir. DFM görüntüleri, tutarlı aydınlatma ve 1/220 s pozlama süresi ile Nikon ti-Eclipse mikroskop bağlı bir Nikon DiR2 dijital kamera ile yakalandı. Bu çalışmada kullanılan PANC-1 hücre hattı Amerikan tür kültürü koleksiyonundan satın alındı.
Açıklamalar
Yazarlar, rakip finansal çıkarların olmadığını beyan ederler.
Teşekkürler
Çalışma öncelikle NıH (U01CA214254, R01HD090927, R01AI122932, R01AI113725 ve R21Al126361-01), Arizona Biyomedikal Araştırma Komisyonu (ABRC) genç araştırmacı Ödülü tarafından sağlanan araştırma finansmanı tarafından destekleniyordu.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Eppendorf Repeater stream | Fisher Scientific | 05-401-040 | |
| Eppendorf Research plus | Eppendorf | 3120000011 | 0.1 – 2.5 µL, dark gray |
| Functionalized Gold Nanorods | Nanopartz | C12-25-650-TN-DIH-50-1 | In vitro neutravidin polymer functionalization |
| HulaMixer Sample Mixer | Thermo Fisher Scientific | 15920D | |
| Incu-shaker 10L | Benchmark Scientific | H1010 | |
| Inverted Research Microscope | Nikon | Ti-DH | With Dark field condenser, DS-Ri2 camera, and Ti-SH-U universal holder, and motorized stage |
| NIS-Elements | Nikon | Microscope imaging software | |
| Phosphate Buffered Saline (1X) | GE Healthcare Life Sciences | SH30256.02 | HyClone |
| Protein A/G Treated Glass Substrate Slides | Arrayit Corp. | AGMSM192BC | Premium microarray substrate |
| Q500 Sonicator | Qsonica, LLC | Q500-110 | With standard probe (#4220) |
| Superblock blocking buffer | Thermo Scientific | ||
| TWEEN 20 | Sigma Life Sciences | 9005-64-5 |
Referanslar
- Andaloussi S, E. L., Mager, I., Breakefield, X. O., Wood, M. J. Extracellular vesicles: biology and emerging therapeutic opportunities. Nature Reviews Drug Discovery. 12 (5), 347-357 (2013).
- Choi, D. S., Kim, D. K., Kim, Y. K., Gho, Y. S. Proteomics, transcriptomics and lipidomics of exosomes and ectosomes. Proteomics. 13 (10-11), 1554-1571 (2013).
- Schorey, J. S., Cheng, Y., Singh, P. P., Smith, V. L. Exosomes and other extracellular vesicles in host-pathogen interactions. EMBO Reports. 16 (1), 24-43 (2015).
- Hoshino, A., et al. Tumour exosome integrins determine organotropic metastasis. Nature. 527 (7578), 329-335 (2015).
- Zaborowski, M. P., Balaj, L., Breakefield, X. O., Lai, C. P. Extracellular Vesicles: Composition, Biological Relevance, and Methods of Study. Bioscience. 65 (8), 783-797 (2015).
- Liang, K., et al. Nanoplasmonic Quantification of Tumor-derived Extracellular Vesicles in Plasma Microsamples for Diagnosis and Treatment Monitoring. Nature Biomedical Engineering. 1, (2017).
- Severino, V., et al. Extracellular Vesicles in Bile as Markers of Malignant Biliary Stenoses. Gastroenterology. 153 (2), e498 495-504 (2017).
- Osteikoetxea, X., et al. Detection and proteomic characterization of extracellular vesicles in human pancreatic juice. Biochemical and Biophysical Research Communications. 499 (1), 37-43 (2018).
- Bulacio, R. P., Nosetto, E. C., Brandoni, A., Torres, A. M. Novel finding of caveolin-2 in apical membranes of proximal tubule and first detection of caveolin-2 in urine: A promising biomarker of renal disease. Journal of Cellular Biochemistry. , (2018).
- Nair, S., Tang, K. D., Kenny, L., Punyadeera, C. Salivary exosomes as potential biomarkers in cancer. Oral Oncology. 84, 31-40 (2018).
- Kim, J. E., et al. Diagnostic value of microRNAs derived from exosomes in bronchoalveolar lavage fluid of early-stage lung adenocarcinoma: A pilot study. Thoracic Cancer. 9 (8), 911-915 (2018).
- Boussadia, Z., et al. Acidic microenvironment plays a key role in human melanoma progression through a sustained exosome mediated transfer of clinically relevant metastatic molecules. Journal of Experimental & Clinical Cancer Research. 37 (1), 245(2018).
- An, M., Wu, J., Zhu, J., Lubman, D. M. Comparison of an Optimized Ultracentrifugation Method versus Size-Exclusion Chromatography for Isolation of Exosomes from Human Serum. Journal of Proteome Research. , (2018).
- Brenner, A. W., Su, G. H., Momen-Heravi, F. Isolation of Extracellular Vesicles for Cancer Diagnosis and Functional Studies. Methods in Molecular Biology. 1882, 229-237 (2019).
- Li, P., Kaslan, M., Lee, S. H., Yao, J., Gao, Z. Progress in Exosome Isolation Techniques. Theranostics. 7 (3), 789-804 (2017).
- Sun, D., et al. Noise Reduction Method for Quantifying Nanoparticle Light Scattering in Low Magnification Dark-Field Microscope Far-Field Images. Analytical Chemistry. 88 (24), 12001-12005 (2016).
- Sun, D., Hu, T. Y. A low cost mobile phone dark-field microscope for nanoparticle-based quantitative studies. Biosensors and Bioelectronics. 99, 513-518 (2018).
- Koshikawa, N., Minegishi, T., Kiyokawa, H., Seiki, M. Specific detection of soluble EphA2 fragments in blood as a new biomarker for pancreatic cancer. Cell Death & Disease. 8 (10), e3134(2017).
- Clayton, A., Turkes, A., Navabi, H., Mason, M. D., Tabi, Z. Induction of heat shock proteins in B-cell exosomes. Journal of Cell Science. 118 (Pt 16), 3631-3638 (2005).
- Henne, W. M., Buchkovich, N. J., Emr, S. D. The ESCRT pathway. Developmental Cell. 21 (1), 77-91 (2011).
- Panagiotara, A., Markou, A., Lianidou, E. S., Patrinos, G. P., Katsila, T. Exosomes: a cancer theranostics road map. Public Health Genomics. 20 (2), 116-125 (2017).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır