Method Article
Genetiği Değiştirilmiş Anopheline Sivrisinek Popülasyonlarındaki Indels Mutasyonlarını Tespit Etmek için Dijital Damlacık PCR
Bu Makalede
Özet
Bu protokol, gRNA kaynaklı Cas9 bölünmesi ve DNA onarımının ardından hedef sahalarda homolog olmayan son birleştirme (NHEJ) olaylarının tanımlanması ve nicelleştirilmesi için analiz de dahil olmak üzere DNA ekstraksiyonundan dijital damlacık PCR (ddPCR) için deneysel kuruluma kadar adımları sağlar. Bu yöntemin diğer kullanımları arasında polimorfizm tespiti ve gen düzenleme varyant doğrulaması gibi uygulamalar yer almaktadır.
Özet
Sivrisinek genomik ve genetik mühendisliği teknolojilerindeki son gelişmeler, hedeflenen DNA dizi varyasyonlarını büyük ölçekte tespit etmek için hızlı ve verimli yöntemlere duyulan ihtiyacı teşvik etti. Özellikle, CRISPR kılavuzu RNA (gRNA)/Cas9 aracılı homolog olmayan son birleştirme (NHEJ) tarafından oluşturulan gen düzenlemeli sitelerdeki eklemelerin ve silmelerin (indels) tespiti, mutajeninzin doğruluğunu ve istenmeyen değişikliklerin sıklığını değerlendirmek için önemlidir. Burada, yüksek verimli NHEJ analizi için çok uygun olan dijital damlacık PCR (ddPCR) için bir protokol açıklıyoruz. Bu yöntem, tek tek sıra varyasyonlarını tanımlayan veriler üretmese de, bir popülasyon içindeki sıra varyasyonunun nicel bir tahminini sağlar. Ayrıca, uygun kaynaklarla, bu protokol bir alan alanı laboratuvar ortamında yeni nesil veya Sanger diziliminden daha kolay uygulanabilir. ddPCR ayrıca, genetik olarak tasarlanmış organizmaların saha denemeleri sırasında vahşi popülasyonlardaki genetik varyasyonun daha hızlı ve eksiksiz bir analizini sağlayan bu yöntemlerin her ikisinden de daha hızlı bir dönüş süresine sahiptir.
Giriş
Gen tahrikleri, tıbbi ve tarımsal alaka düzeyi 1 , 2 ,3,4,5böcek popülasyonlarını kontrol etmek için muazzam birpotansiyelesahiptir. Örneğin, CRISPR Cas nükleaslarına ve kılavuz RNA'lara (gRNA'lar) dayanan gen tahrik sistemleri, daha az bulaşma ve daha az hastalığa yol açan sıtma parazitlerine refrakterlik sağlayan özellikleri getirerek vektör sivrisinek popülasyonlarını değiştirmek için kullanılabilir1,4,5. Gen tahrik sistemi kendini ve ilişkili özelliği meiotik mikrop öncesi hücrelerde bir homolog kromozomdan diğerine kopyalar ve bu, yavruların çoğunluğunun sürücüyü devralmasını ve alanda uzun süreli ve sürdürülebilir popülasyon modifikasyonu potansiyeli yaratmasını sağlar. Bununla birlikte, Cas/gRNA tabanlı yöntemlerin bir dezavantajı, homolog olmayan son birleştirici (NHEJ) DNA onarımı yoluyla ekleme ve silme (indel) mutasyonları üretme olasılığıdır, bu da popülasyonda yeterince yüksek bir frekansa biriktiğinde tahrik sistemininyayılmasını durdurabilen sürücüye dayanıklı alellerin üretilmesine neden olur. . Bu protokol, Cas/gRNA tabanlı gen güdüsü sırasında hem popülasyon hem de bireysel düzeyde indel mutasyonlarının yaygınlığını ve göreceli miktarını belirleyebilen yüksek verimli ve güvenilir bir yöntemi detaylandırıyor.
Yeni nesil sıralama (NGS) yöntemleri benzersiz sıralama çözünürlüğü sağlar. Bununla birlikte, NGS ile ilişkili maliyet ve teknik gereksinimler rutin testleri yasaklar veindels 6,7,8'ideğerlendirmek için yüksek verimli bir yöntem olarak kullanımını sınırlar. Geleneksel PCR nicelleştirme yöntemleri uzun zamandır genom indelleri için standart değerlendirme prosedürü olarak kullanılmaktadır; ancak, bu yöntemler emek yoğundur, veri temini uzun zaman alır ve yüksek derecede değişkenliğe sahiptir. Digital-Droplet PCR (ddPCR) bazı uygulamalarda Sanger diziliminden daha hassas mutasyonları tespit etme konusunda daha hassas olduğu kanıtlanmıştır ve diğerlerinde NGS'den daha düşük bir algılama sınırına sahiptir6,7,8,9. Ayrıca, bir örnek seti değerlendirmenin maliyeti ve sonuç elde etmek için dönüş süresi, ddPCR için Sanger diziliminden veya NGS9'dandaha az pahalı ve daha hızlıdır. Çift problu bir sistem kullanan Bırakma tahlili, gRNA tarafından yönlendirilen hedef Cas9 kesim yerinde vahşi tip (WT) sırasının yokluğuna bağlı olarak NHEJ alellerini tanımlar. Bu testte, Cas/gRNA tabanlı sistemin öngörülen kesim bölgesini içeren kısa bir amplicon belirli bir astar çifti ile yükseltilir. Bir floresan prob amplicon'un korunmuş bir bölgesine bağlanmak için tasarlanmıştır ve başka bir floresan prob kesim bölgesinin WT sırasını tanır. Bir NHEJ alelesinin varlığında, ikincisi amplicon'a bağlanmaz.
DdPCR kullanımı, sivrisinek popülasyon analizlerinde NHEJ profillemesine izin verecek olan silmeleri, tek baz çifti farklılıklarını ve eklemeleri hedeflemek için astarlar tasarlama yeteneği sağlar9. Bu çekici özellikler göz önüne alındığında, sivrisineklerde Cas/gRNA tabanlı gen tahrik sisteminden oluşturulan indellerin yüksek verimli tespiti için ddPCR için bir protokol oluşturduk.
Protokol
1. DNA ekstraksiyonu
- Numune başına 500 μL NLS ve 120 μL EDTA oranına sahip EDTA/Nuclei Lizis Tamponu (EDTA/NLS) hazırlayın. Birden çok örnek için ölçeklendirin. Karışımı buzda soğutun.
NOT: Çözelti, ses seviyesine bağlı olarak soğuduğunda 2-5 dakika içinde bulanıklaşır. - Sivrisinek örneğini 600 μL soğutulmuş EDTA/NLS ile doldurulmuş 1,5 mL mikrosantrifüj tüpünde 10-15 sn için mekanik bir homojenizatör kullanarak homojenize edin; iyice karıştırın.
- Tüpe 17,5 μL 20 mg/mL Proteinaz K ekleyin ve iyice karıştırın.
- 55 °C'de gece boyunca kuluçkaya yaslanın. Alternatif olarak, numuneyi 55 °C'de 3 saat boyunca her 1 saat sallama ve girdap ile kuluçkaya yatırın.
- Oda sıcaklığı örneğine 200 μL Protein Çökeltme Çözeltisi ekleyin ve 20 sn boyunca güçlü bir şekilde girdap ekleyin.
- Numuneyi buzda 5 dakika soğutun.
- Numuneyi 4 dakika boyunca 15.890 RCF'de pelet proteinlerine santrifüj edin.
- DNA'yı içeren süpernatantı dikkatlice emiş ve 600 μL izopropanol içeren temiz bir 1,5 mL mikrosantrifüj tüpüne aktarın.
- Tüpü 5-10 kez ters çevirerek çözeltiyi hafifçe karıştırın. 15.890 RCF'de 1 dakika santrifüj. DNA peletini korurken süpernatantı dikkatlice dekante edin.
- 600 μL oda sıcaklığı %70 etanol ekleyin. Peletlenmiş DNA'yı tüpü hafifçe ters çevirerek yıkayın.
- 15.890 RCF'de 1 dakika santrifüj. Cam pipet ucu kullanarak aspirasyon yaparak süpernatant dikkatlice çıkarın.
- Tüpü temiz emici kağıda ters çevirin ve peletin havayla 10-15 dakika kurulayın.
- DNA'yı PCR sınıfı suyla yeniden kullanın. Bireysel sivrisinek örneği başına 20 μL veya 10 havuzlu sivrisinek için 100 μL kullanın.
NOT: Piyasada bulunan bir kit kullanan sivrisinek örnekleri için DNA çıkarma yöntemleri (bkz. Malzeme Tablosu),üreticinin Doku Kültürü Hücrelerinden ve Hayvan Dokusu protokolünden izole edilen Genomik DNA'sından uyarlanmıştır.
2. ddPCR reaksiyonları ve damlacık üretimi hazırlığı
- Bir florometre kullanarak DNA'yı ölçün.
NOT: Bırakma tahlilleri için, reaksiyon başına 3.000-30.000 haploid genom kopyası kullanılması önerilir, bu da NHEJ olaylarını hedeflenen kesim bölgesinin WT dizisine bağlanan ve hedef bölgeye bir silme veya ekleme varsa tavlama (bırakma) yapmayan bir HEX etiketleme probu ile tespit etmek için tasarlanmıştır. bir NHEJ varyantının varlığını gösterir. - Fotokopi genom ağırlığını ve ekstrakttaki DNA konsantrasyonu kullanarak kopya numarasını hesaplayın. Bu, çıkarılan DNA'nın konsantrasyonunun toplam DNA kütlesini elde etmek için kullanılan hacimle çarparak ve daha sonra haploid genom ağırlığına bölünmesiyle yapılır. Eklenen hacmin 1-10 μL arasında olduğundan emin olun.
NOT: Bir Anopheles gambiae haploid genomun yetişkin sivrisinek başına 0.27 pg olduğu tahmin edilmektedir10. - Astarlar ve problar tasarlayin. 150-400 bp'lik bir amplicon üreten gRNA hedef bölgesinin 5've 3'uçlarını kuşatan 55-60 °C aralığında astar Erime Sıcaklığı (Tm) ile ileri ve geri oligonükleotid astarlar tasarlayın.
- NHEJ algılaması için HEX (Hexachloro-floresan) etiketli prob: Hedef bölgeye tamamlayıcı olarak ~15-20 bp uzunluğunda bir oligonükleotid tasarlayın ve HEX-probu 5'uç ve BHQ1'e (BLack Hole Quencher 1) 3' uca ekleyin. Hidroliz probunun Tm'si astarların Tm'sinden 3-10 °C daha yüksek olmalıdır.
- Referans WT için FAM (6-karboksifluorescein) etiketli prob: Hedef bölgeden uzak korunmuş bir genom alanına (yaklaşık 25 bp) tamamlayıcı bir oligonükleotid ~15-20 bp uzunluğunda bir tasarım ve FAM-prob'u 5'uç ve BHQ1'i 3' uca ekleyin. Hidroliz probunun Tm'si astarların Tm'sinden 3-10 °C daha yüksek olmalıdır.
3. PCR reaksiyon hazırlığı
- Aşağıdaki bileşenlerle 25 μL ddPCR Numune Karışımı hazırlayın: problar için ddPCR supermix (UTP yok): 12,5 μL, ileri ve ters astarlar (10 μM): Her biri 1 μL, HEX/FAM probları (10 μM): her biri 0,625 μL, DNA: 1-5 μL (3.750-37.500 haploid genom kopyası) ve su: 25 μL'ye kadar.
- Reaksiyonları girdaplama veya reflü pipetleme (yukarı ve aşağı) (20x) ile iyice karıştırın.
NOT: Reaksiyonlar 96 kuyulu bir plakadaysa, kabarcık oluşumunu önlemek için girdap yerine tüm ses seviyesini 20 kez yukarı ve aşağı pipetlayın. - Karışımı tüpün altına veya kuyuya yerleştirmek için numuneleri kısaca santrifüjleyin.
NOT: Damlacık üretimi için reaksiyonların oda sıcaklığında olduğundan emin olun. Her kartuşta ekstra/kullanılmayan kuyular için 1x ddPCR karışımı hazırlayın (her kartuşta 8 kuyu vardır).
4. Damlacık üretimi
- 50 μL çok kanallı pipet kullanarak, ddPCR numune karışımının 20 μL'lik kısmını kartuşun orta sırasına yükleyin(Şekil 1A, üst).
- Yağın 70 μL'yi alt sıraya yükleyin. Kullanılmayan kuyulara 20 μL 1x ddPCR supermix yükleyin.
NOT: Kabarcıkları tanıtmayın. - Contayı sadece kenarlara dokunarak, orta konik alandan kaçınarak yerleştirin(Şekil 1B).
- Plakayı damlacık jeneratörüne güvenli bir şekilde yerleştirin ve çalıştırmayı başlatmak için kapağı kapatın.
- Çok kanallı pipeti kullanarak, emersion karışımının 40 μL'lik kısmını kartuşun üst sırasından(Şekil 1A, altta) 96 kuyu plakasına aktarın.
- 45-30° açıyla 3-5 sn için sıvı numunesi çekin. Karışımı 3 sn'nin üzerinde yavaşça kuyunun kenarına 45° açıyla atın ve yan tarafa damlamasını sağlar. Tüm sıvıyı dışarı çıkarmak için pipetin ikinci durağına (tamamen atılma) gitmek sorun değildir.
- Folyo ısı contalarını kullanarak plakaları 180 °C'de 5 sn kapatın.
5. PCR
- Sızdırmaz plakayı termositlere yerleştirin (Şekil 1C) ve NHEJ Bırakma yönergelerini aşağıdaki gibi takip ediyorsanız önerilen PCR koşullarını ayarlayın:
- 10 dakika boyunca 95 °C'de ilk denatürasyon.
- Denatüre etmek için 30 sn için 94 °C, tavlama için 1 dakika için 55 °C ve 2 dakika uzatmak için 60 °C 40 döngü ayarlayın.
- 98 °C'de 10 dakika bekletin.
- 4 °C'de tutun.
NOT: Belirli astarlar ve prob setleri için tavlama sıcaklığı termal gradyan kullanılarak optimize edilebilir. Tüm adımlar için 2 °C/s rampa hızı kullanın. PCR koşulları her deneysel tasarıma ve kuruluma bağlı olarak ayarlanmalıdır.
6. Damlacık okuma
- Plakayı sol üstte iyi A-1 ile damlacık okuyucuya güvenli bir şekilde yerleştirin (düzleştirilmiş köşe, diğer üçü kenarlı) (Şekil 1D).
- Programdaki plakayı ayarlayın: FAM'ı bilinen referans kanalı ve HEX'i bilinmeyen kanal olarak belirleme (Şekil 2A).
- Damlacık okuma deneyini doğrudan niceleme olarak çalıştırın. Çalıştırma bittikten sonra, analiz için Deneme türünü Bırakma (DOF) olarak değiştirin (Şekil 2A).
7. Analiz
- Doğru deneysel parametreleri belirleyin (Şekil 2A): Örnek Bilgi, SuperMix, Hedef Adı (WT veya NHEJ), Hedef Türü (Ref veya Unknown), Signal Ch1 (HEX veya FAM), Signal Ch2 (HEX veya FAM) ve damlacık sayısı eşiğini manuel olarak ayarlayın (güvenilir sonuçlar için 10.000'in üzerine önerin). Yazılım, analizin çoğunu belirlenen parametreyle gerçekleştirecektir.
- Damlacık sekmesinde damlacık sayısını kontrol edin; hepsinin 10.000'in üzerinde olduğundan emin olun (Şekil 2B).
- Negatiflerden etkili sinyal ayırma için 1 D genliği kontrol edin.
- Plaka Düzenleyicisi'nde, tüm plakayı vurgulayın ve Deneme Türünü Bırak olarak ayarlayın.
- WT hedefini Başvuruolarak ayarlayın, FAM için kanal 1 ve HEX için kanal ikiyi belirleyin.
- NHEJ hedefini bilinmiyor olarak ayarlayın, FAM için kanal 1 ve kanal 2'yi yok olarak belirleyin.
- 2D genlik sekmesinde, her örnek için grafik araçlarıyla Küme Eşiklerini ayarlayın. WT kümesiyle ilişkili kuyruğu göz önünde bulundurun; Bu NHEJ tahlilleri için normaldir (Şekil 3A).
NOT: Oran sekmesinin altında, grafiğin sağ üst kısmındaki Dişli Simgesi'ne tıklayın. Kesirli Bolluk 'useçin. Grafik şimdi NHEJ olaylarının yüzdesine karşılık gelen bir nokta çizecektir (Şekil 3B).
Sonuçlar
Bu prosedürün bir uygulaması Carballar-Lejarazú ve ark.9'da görünür. DDPCR Bırakma tahlili, WT ve indel dizilerini ayırt etmek için iki floresan prob kullanır: BIR FAM probu amplicon içinde korunmuş bir diziye bağlanırken, HEX probu hedeflenen sitenin WT dizisini hedefler (Şekil 4A). Bir indel varlığında, HEX probu bağlanmaz. Temsili sonuçlar Şekil 2, Tablo 1 ve Tablo 2'de Carballar-Lejarazú veark. Bu protokolü kullanarak, ddPCR'nin çok çeşitli CRISPR-Cas9 kaynaklı NHEJ olaylarını tespit ettiği ve tek bir veya havuza alınan örnekte NHEJ frekansını ölçtği kanıtlanmıştır. Her biri çeşitli NHEJ alelleri içeren 10 sivrisinekten oluşan on beş farklı havuzlu örnek (Carballar-Lejarazú ve ark.9'unTablo 2). Bunlar burada sunulan protokol ve parametreler kullanılarak ddPCR ile analiz edildi. Tablo 19'dan elde edilen sonuçlar, 15 numunenin tümünü Drop-off testinde tanımlanan % 100 indel alelleri taşıdığını göstermektedir (Şekil 4B). Başka bir deneyde, farklı NHEJ yüzdelerine sahip 11 adet havuzlu WT sivrisinek ve NHEJ sivrisinek örneği (%0, %10, %20, %30, %40, %50, %60, %70, %80, %90 ve %100) bu ddPCR protokolü ile incelenmiştir ve sonuçlar (Şekil 2; Carballar- Lejarazú vd.9) tanımlanan yüzdenin Amplicon Analizi ile Indel Algılama tekniğine yakın olduğunu göstermiştir (Şekil 4C).

Şekil 1: Deneysel kurulum ve prosedür. (A) Damlacık üretimi için kartuş hazırlığı. (Üstte) Numuneler kartuşun orta satırına doldurulurken, yağ alt sıraya doldurulur. (Alt) Damlacık oluşturmadan sonra emülsifiye damlacıklarla dolu üst sıra. (B) Numune ile doldurulmuş ve yerinde bir conta ile kaplanmış bir kartuş ile damlacık jeneratörü. (C) Bir Termo-Cycler folyo conta ile kaplı 96 kuyu plakası. (D) 96-well plakalı damlacık okuyucu, sabitlemek için plakanın üzerine metal bir kapak tutturmuş. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
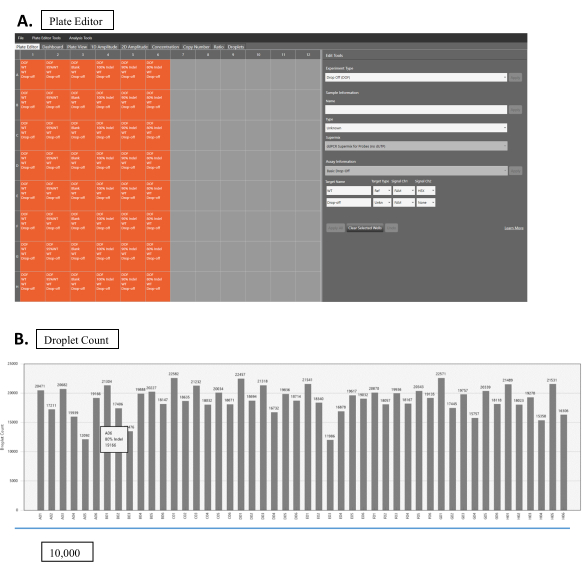
Şekil 2: Damlacık okuma. (A) Damlacık okuma için yazılım arayüzü. Turuncu kutular örneklerin olduğu kuyuları gösterir. Gri kutular boş kuyulardır. Deneysel parametreler Araçları Düzenle panelinde (sağ tarafta) ayarlanır. Her örnek, ilgili örnek kutusuna tıklayarak düzenlenebilir. Deneysel Tür için Bırakma (DOF) seçeneğini belirleyin. Örnek bilgilerde, örneğin Adı ve Türüve SuperMixiçin uygun bilgileri doldurun. Tahlil Bilgileri için Temel Bırakma 'yıseçin. WT örneği için sırasıyla Hedef Adıiçin WT , Hedef Türüiçin Ref ve Ch1 ve Ch2 Sinyali için hem FAM hem de HEX'i seçin. NHEJ örnekleri için, Hedef Adıiçin uygun adı doldurun, Hedef Türüiçin Bilinmiyor 'u seçin ve Ch1 Sinyaliiçin FAM 'ı seçin. Signal Ch2'i Yok'ta bırakın. (B) Birden fazla örnek için damlacık sayısı sonuçları. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
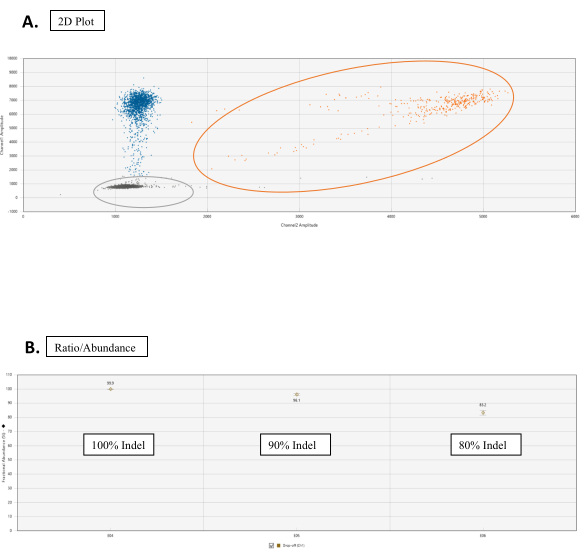
Şekil 3: Bırakma tahlil analizi. (A) WT ve NHEJ alellerinin damlacık sayısı için Küme 2D çizimi. 2D Genlik sekmesinde, tüm damlacıklar varsayılan olarak sınıflandırılmaz. Bu şekilde, renkler ayırt etmek için el ile atanır. Turuncu noktalar kümesi, sırasıyla referans sırası ve hedef site dizisinde hem FAM hem de HEX problarının bağlanmasıyla elde edilen WT alaşım sayılarıdır. Mavi noktalar, başvuru sırasına FAM bağlaması olan ancak hedef site dizisinde HEX bağlaması olmayan damlacıkların puanlarını temsil eder (bu nedenle HEX'in bırakması). Gri noktalar, FAM veya HEX bağlaması olmayan boş damlacıklardır. (B) NHEJ olaylarının oran/bolluk grafikleri. Oran sekmesinin altında, NHEJ olaylarının muhabir yüzdesine sahip bir grafik için Kesirli Bolluk'u seçin. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
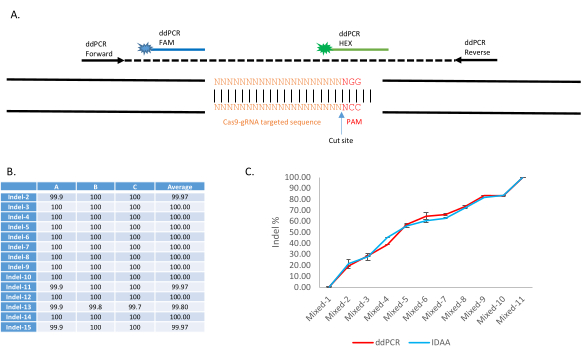
Şekil 4: Transgenik Anopheles stephensi hattında homolog olmayan son birleştirme tanımlaması ve nicelemesi için ddPCR ile Bırakma tahlilinin uygulanması, AsMCRkh1. (A) Çift prob sistemine sahip hedeflenen bir DNA yerindeki mutasyonları tespit etmek için ddPCR Bırakma testinin şematik sunumu. 150-400 bp'lik bir amplicon ileri ve ters astarlarla yükseltilir. FAM etiketli bir prob amplicon'un korunmuş bir dizisine bağlanmak için tasarlanmıştır, HEX etiketli bir prob ise WT gRNA hedeflenen bölgeye bağlanmak için tasarlanmıştır. (B) DdPCR ile çeşitli indel türlerinin tespiti. Her biri ekleme, silme ve değiştirme dahil olmak üzere çeşitli türde indel içeren 10 AsMCRkh1 sivrisinekten oluşan 15 havuz, ddPCR Drop-Off test ile analiz edildi. Mutasyonların ve dizilerin ayrıntıları Tablo 2 ve Tablo S3'te bulunabilir. 9. (C) AsMCRkh1 ve WT sivrisineklerinin çeşitli oranlarda karışık örneklerinde NHEJ'nin nicelemesi (10:0, 9:1, 8:2, 7:3, 6:4, 5:5, 4:6, 3:7, 2:8, 1:9 ve 0:10) ddPCR ve Amplicon Analysis9ile karşılaştırılan bir Indel Algılama tekniği kullanarak. Carballar-Lejarazú ve ark. Biotechniques'tenuyarlanmış görüntüler. 68(4):172-179 (2020)9. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
| Astar/Prob | Sıra (5' » 3') |
| ddPCR İleri Astar | ATGATCAAATGTCGACCG |
| ddPCR Ters Astar | ACCGTACTGGTTGAACA |
| ddPCR HEX Probu (BHQ1) | [HEX]-TTCTACGGGCAGGGC-[BHQ1] |
| ddPCR FAM Sondası (BHQ1) | [6FAM]-CCACGTGGGATCGAAGG-[BHQ1] |
| HEX: Hexachloro-floresan, FAM: 6-carboxyfluorescein, BHQ: Kara Delik Quencher | |
Tablo 1: Astar ve prob dizileri.
Tartışmalar
Dijital damlacık PCR, Cas/gRNA tabanlı bir gen tahrik sisteminde NHEJ olaylarından kaynaklanan indel alellerinin varlığını belirlemek için etkili bir yöntemdir ve bireylerde veya popülasyonlarda bu alellerin sıklığının ölçülmesini sağlar. Güvenilir sonuçlar elde etmek için protokolün bazı adımlarının özel bir dikkatle takip edilmesi gerekir. Öncelikle, genomik DNA ekstraksiyonu, yüksek kalite ve yeterli miktarda sağlamak için dikkatli bir şekilde yapılmalıdır. İyi bir ekstraksiyon, reaksiyon başına haploid genom kopyalarının doğru bir şekilde belirlenmesini sağlayacaktır. Deneyimlerimize göre, piyasada bulunan bir kit (bkz. Malzeme Tablosu)sürekli olarak yüksek kaliteli DNA ekstraksiyonları sağladı. Bununla birlikte, bireysel sivrisineklerin ekstraksiyonları, DNA peletinin görselleştirilmesi zorlaştığından ve dikkatli olmazsa süpernatant ile kolayca emilebileceğinden özellikle zor olabilir. İkincisi, astarlar ve problar dikkatlice tasarlanmalıdır. DDPCR deneyini tamamlamadan önce, tasarlanan astarların önce geleneksel bir PCR gerçekleştirerek ve jel elektroforez yoluyla tek bir ürünü görselleştirerek tek bir PCR ürünüyle sonuçlandığından emin olun. Başvuru FAM probu da yüksek oranda korunmuş bir sıranın tamamlayıcısı olacak şekilde tasarlanmalıdır. Bu, farklı bir popülasyon boyunca WT alellerinin doğru şekilde algılanmasını sağlayacaktır. Her benzersiz deney için astar/prob kombinasyonları farklı termosikleyici koşullarına sahip olacaktır ve bu koşulların bir termal degrade kullanılarak optimize edilmesiniz önerilir.
Sanger dizilimi veya NGS gibi indelleri tanımlamak için başka yöntemler de vardır. Sanger dizilimi sınırlıdır, çünkü yeni varyantları tanımlamak için daha düşük bir algılama sınırına ve düşük keşif gücüne sahiptir. Sanger dizilimi de emek yoğundur ve yüksek verim değildir. Sanger dizilimi ile karşılaştırıldığında, NGS düşük hassasiyet, keşif gücü ve aktarım hızı ile aynı sınırlamalara sahip değildir. NGS'nin bir diğer faydası da tek nükleotid polimorfizmden (SNP' ler) yeniden yapılanmalara kadar çeşitli mutasyonları tespit edebilmesidir. Bununla birlikte, NGS Cas9/gRNA ile ilişkili indellerin belirlenmesi uygulamasında daha maliyetli ve zaman alıcı bir yöntemdir, çünkü ilgi çekici tek bir hedef bölge vardır ve daha büyük genom çapında analizler için en uygun yöntemdir. Yukarıda belirtilen yöntemlerle karşılaştırıldığında, ddPCR yüksek aktarım hızına sahiptir ve hızlı bir dönüş süresine sahiptir. DdPCR malzemeleri ve aletleri şirket içinde mevcutsa, 96 numune 1-2 gün içinde işlenebilir, bu da Cas9 / gRNA modifiye organizmaların büyük denemelerinin hızlı analizi için çok uygundur.
ddPCR için birçok avantaj olsa da sınırlamalar da vardır. İlk olarak, ddPCR ekipmanı bağımsız bir laboratuvar ortamında sıkça bulunmaz. ddPCR ekipmanı daha büyük araştırma kurumlarında ortaklaşa mevcut olabilir, ancak bu, kurum dışında veri oluşturma ve analiz kolaylığına izin vermez. İkincisi, alternatiflerin aksine, ddPCR tanımlanan indel mutasyonlarının bireysel benzersiz dizilerini sağlamaz. Dijital damlacık PCR, bir popülasyondaki indel mutasyonlarının sıklığını sağlayacaktır, ancak dizi olmadan, mevcut indellerin ilgi geninin işlevini koruma veya engelleme olasılığının daha fazla olup olmadığını belirleyemez. DdPCR yöntemi, Cas9/gRNA tabanlı bir tahrik organizmasının alan serbest bırakma denemesinden sonra vahşi popülasyonları analiz etmek için belki de en uygun olanıdır, çünkü transjenin yerli popülasyona giriş sıklığını ve popülasyon içindeki indellerin neslini gerçek zamanlıya yakın bir şekilde verimli bir şekilde belirleyebilir. DdPCR hızlı dönüş süresi nedeniyle, malzemeler yerel olarak mevcutsa, bir saha deneme bölgesinde popülasyonu haftalık olarak örneklemek ve analiz etmek mümkün olacaktır. DdPCR ekipmanını satın almak, ithal etmek ve kurmak için başlangıç maliyetleri uzak laboratuvarlarda yüksek olacaktır, ancak bir tahrik sisteminden değişiklik gördüğü için vahşi bir popülasyonu titizlikle değerlendirebilmenin yararları maliyetleri haklı çıkaracaktır.
Açıklamalar
Yazarların hiçbir açıklaması yok.
Teşekkürler
Finansman Kaliforniya Üniversitesi Irvine Sıtma Girişimi tarafından sağlandı. AAJ, Irvine Kaliforniya Üniversitesi'nde Donald Bren Profesörüdür.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Reagents | |||
| ddPCR Super Mix for Probes (no dUTP) | Bio-Rad | 1863024 | |
| DNA extraction reagent (e.g. Wizard Genomic DNA Purification kit) | Promega | A1120 | |
| EDTA (pH 8.0) | Invitrogen | AM9260G | |
| Ethanol, 200 Proof | Thermo Fisher Scientific | A4094 | |
| Isopropanol (Certified ACS) | Thermo Fisher Scientific | A416-500 | |
| Nuclei Lysis Solution (NLS) (Wizard Genomic DNA Purification kit) | Promega | A1120 | |
| PCR-grade Water | Any certified PCR-grade water can be used | ||
| Protein Precipitation Solution (Wizard Genomic DNA Purification kit) | Promega | A1120 | |
| Proteinase K 20 mg/mL | Thermo Fisher Scientific | AM2546 | |
| Materials | |||
| ddPCR 96-Well Plate | Bio-Rad | 12001925 | |
| Droplet Generator DG8 Cartridge and Gaskets | Bio-Rad | 1864007 | |
| Droplet Generation Oil for probes | Bio-Rad | 1863005 | |
| Fluorescent probes (e.g. FAM/HEX probes) | Sigma-Aldrich | N/A | Probes are experiment specific and can be purchased from any certified seller available. |
| Forward and Reverse oligonucleotide primers | Sigma-Aldrich | N/A | Primers are experiment specific and can be purchased from any certified seller available. |
| Equipment | |||
| C1000 Touch Thermal Cycler | Bio-Rad | 1851148 | Can use other Thermo cycler with gradient function and deep well |
Referanslar
- Gantz, V. M., et al. Highly efficient Cas9-mediated gene drive for population modification of the malaria vector mosquito Anopheles stephensi. Proceedings of the National Academy of Sciences of the United States of America. 112 (49), 6736-6743 (2015).
- Hammond, A., et al. A CRISPR-Cas9 gene drive system targeting female reproduction in the malaria mosquito vector Anopheles gambiae. Nature Biotechnology. 34, 78-83 (2016).
- Courtier-Orgogozo, V., Morizot, B., Boëte, C. Agricultural pest control with CRISPR-based gene drive: time for public debate: Should we use gene drive for pest control. EMBO Reports. 18 (6), 878-880 (2017).
- Carballar-Lejarazú, R., et al. Next-generation gene drive for population modification of the malaria vector mosquito, Anopheles gambiae. Proceedings of the National Academy of Sciences of the United States of America. 117 (37), 22805-22814 (2020).
- Adolfi, A., et al. Efficient population modification gene-drive rescue system in the malaria mosquito Anopheles stephensi. Nature Communications. 11, 5553 (2020).
- Wang, Z., et al. Comparison of droplet digital PCR and direct Sanger sequencing for the detection of the BRAFV600E mutation in papillary thyroid carcinoma. Journal of Clinical Laboratory Analysis. 33 (6), 22902 (2019).
- Dong, L., Wang, S., Fu, B., Wang, J. Evaluation of droplet digital PCR and next generation sequencing for characterizing DNA reference material for KRAS mutation detection. Scientific Reports. 8 (1), 9650 (2018).
- Bell, C. C., Magor, G. W., Gillinder, K. R., Perkins, A. C. A high-throughput screening strategy for detecting CRISPR_Cas9 induced mutations using next-generation sequencing. BMC Genomics. 15 (1), 1002 (2014).
- Carballar-Lejarazú, R., Kelsey, A., Pham, T. B., Bennett, E. P., James, A. A. Digital droplet PCR and IDAA for the detection of CRISPR indel edits in the malaria species Anopheles stephensi. Biotechniques. 68 (4), 172-179 (2020).
- Holt, R. A., et al. The genome sequence of the malaria mosquito Anopheles gambiae. Science. 298 (5591), 129-149 (2002).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır