Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Nötralizasyon Testi Yoluyla SARS-CoV-2'ye Karşı Humoral İmmün Yanıtları İzlemek İçin Moleküler Bir Araç Olarak Psödotiplenmiş Virüsler
* Bu yazarlar eşit katkıda bulunmuştur
Bu Makalede
Özet
Psödotipli virüsler (PV'ler), otantik virüsleri işlemekten daha güvenli koşullar altında konak-virüs etkileşimlerini incelemek için kullanılan replikasyon kusurlu virionlardır. Burada, SARS-CoV-2 PV'lerin COVID-19 aşılamasından sonra hastaların serumunun nötralize edici yeteneğini test etmek için nasıl kullanılabileceğini gösteren ayrıntılı bir protokol sunulmaktadır.
Özet
Psödotipli virüsler (PV'ler), ilgilenilen bir genin verilmesi için gen terapisinde daha iyi bilinen kullanımlarına ek olarak, konak-virüs etkileşimlerini incelemek ve serum örneklerinin nötralize edici yeteneğini test etmek için kullanılabilen moleküler araçlardır. PV'ler replikasyon kusurludur çünkü viral genom, PV'lere dahil edilmeyen farklı plazmitlere bölünmüştür. Bu güvenli ve çok yönlü sistem, biyogüvenlik seviye 2 laboratuvarlarında PV'lerin kullanılmasına izin verir. Burada, burada belirtildiği gibi üç plazmide dayalı lentiviral PV'ler üretmek için genel bir metodoloji sunuyoruz: (1) enfeksiyonu izlemek için gereken raportör geni taşıyan omurga plazmidi; (2) PV'leri üretmek için gereken tüm yapısal proteinler için genleri taşıyan ambalaj plazmidi; (3) virüs tropizmini belirleyen ve konakçı hücreye viral girişe aracılık eden zarf yüzeyi glikoprotein ekspresyon plazmidi. Bu çalışmada, SARS-CoV-2 Spike, replikatif olmayan SARS-CoV-2 psödotipli lentivirüslerin üretimi için kullanılan zarf glikoproteinidir.
Kısaca, paketleme hücreleri (HEK293T) standart yöntemler kullanılarak üç farklı plazmit ile birlikte transfekte edildi. 48 saat sonra, PV'leri içeren süpernatan hasat edildi, filtrelendi ve -80 °C'de depolandı. SARS-CoV-2 PV'lerin enfektivitesi, enfeksiyondan 48 saat sonra bir hedef hücre hattında raportör genin (lusiferaz) ekspresyonu incelenerek test edildi. Bağıl lüminesans birimleri (RLU'lar) için değer ne kadar yüksek olursa, enfeksiyon/transdüksiyon oranı o kadar yüksek olur. Ayrıca, enfeksiyöz PV'ler, RLU yoğunluğundaki azalma olarak ölçülen, psödovirüslerin hedef hücrelere girişinin nötralizasyon sürecini incelemek için seri olarak seyreltilmiş serum örneklerine eklendi: yüksek nötralize edici aktiviteye karşılık gelen daha düşük değerler.
Giriş
Psödotipli virüsler (PV'ler), mikrobiyolojide konak-virüs ve patojen-patojen etkileşimlerini incelemek için kullanılan moleküler araçlardır 1,2,3,4. PV'ler, viral genomu koruyan viral çekirdek olan bir iç kısımdan ve bir dış kısımdan, tropizmi tanımlayan virüsün yüzeyindeki zarf glikoproteinlerinden oluşur5. Bir psödovirüs, yeni viral parçacıklar oluşturmak için tüm genetik bilgiyi içermediği için hedef hücrede replikasyon yetersizdir. Tuhaf özelliklerin bu kombinasyonu, PV'leri vahşi tip bir virüse güvenli bir alternatif haline getirir. Vahşi tip virüsler ise oldukça patojeniktir ve BSL 2 laboratuvarlarında analiz içinkullanılamaz 6.
PV'lerin enfektivitesi, genellikle bir floresan proteini (GFP, RFP, YFP) veya kemilüminesan ürünler (lusiferaz) üreten bir enzimi kodlayan bir raportör gen tarafından izlenebilir. Bu, PV üretimi için kullanılan plazmitlerden birinde bulunur ve psödovirüs7'nin genomuna dahil edilir.
Şu anda HIV-1 genomuna dayanan lentiviral türevli parçacıklar da dahil olmak üzere çeşitli PV çekirdek türleri mevcuttur. HIV-1 tabanlı PV'lerin diğer platformlara göre en büyük avantajı, hedef hücre genomundaki içsel entegrasyon süreçleridir8. HIV-1 oldukça bulaşıcı bir virüs olmasına ve AIDS'e neden olmasına rağmen, bu lentiviral vektörlerin yıllar boyunca kapsamlı optimizasyon adımları nedeniyle kullanımı güvenlidir. Viral genlerin transdüksiyon yeteneklerini etkilemeden tükendiği 2nd nesil lentiviral vektörün piyasaya sürülmesiyle optimal güvenlik koşulları sağlandı9. 3. ve 4. nesiller, viral genomun ayrı plazmitlere daha fazla bölünmesiyle lentiviral vektör işlemenin artan güvenliğine katkıda bulundu10,11. En yeni nesil PV'ler genellikle gen terapisi için lentiviral vektörler üretmek için kullanılır.
PV'ler, hem üretim hem de enfeksiyon aşamalarında virüsler ve konakçı hücreler arasındaki etkileşimleri incelemek için kullanılabilir. PV'ler özellikle psödovirüs nötralizasyon deneylerinde (PVNA) kullanılır. PVNA'lar, PV'nin zarfı12,13 üzerindeki viral glikoproteini hedefleyerek serum veya plazmanın nötralizasyon potansiyelini değerlendirmek için geniş çapta doğrulanmıştır. İnhibitör konsantrasyon 50 (IC50) olarak ifade edilen nötralizasyon aktivitesi, viral partikül girişinin %50'sini bloke eden serum/plazmanınseyreltilmesi olarak tanımlanır 14. Bu protokolde, bir rapel aşı dozu almadan önce ve sonra toplanan serumlarda Şiddetli Akut Solunum Sendromu - Koronavirüs 2'ye (SARS-CoV-2) karşı antikor aktivitesini test etmek için bir PVNA'nın kurulumunu tanımladık.
Protokol
Bu protokol, Verona Üniversitesi Etik Komitesi tarafından onaylanmıştır ve yönergelerini takip etmektedir (onay protokolü numarası 1538). Çalışmaya katılan insan deneklerden bilgilendirilmiş yazılı onam alınmıştır. Anti-SARS-CoV-2 aşıları alma sürecinde olan sağlık çalışanı (HCW) gönüllülerinden tam kan örnekleri toplandı. Bu örnekler, serum15'in daha sonra izolasyonu için antikoagülan içeren plastik tüplerde toplandı.
Aşağıdaki tüm işlemler, steril koşullar altında çalışan Sınıf-2 biyolojik bir başlıkta gerçekleştirilmelidir. Virüs işleme dikkatli yapılmalı ve tüm atık ürünler seyreltilmiş bir ağartma çözeltisinde nötralize edilmelidir. Protokole genel bir bakış Şekil 1'de gösterilmektedir.
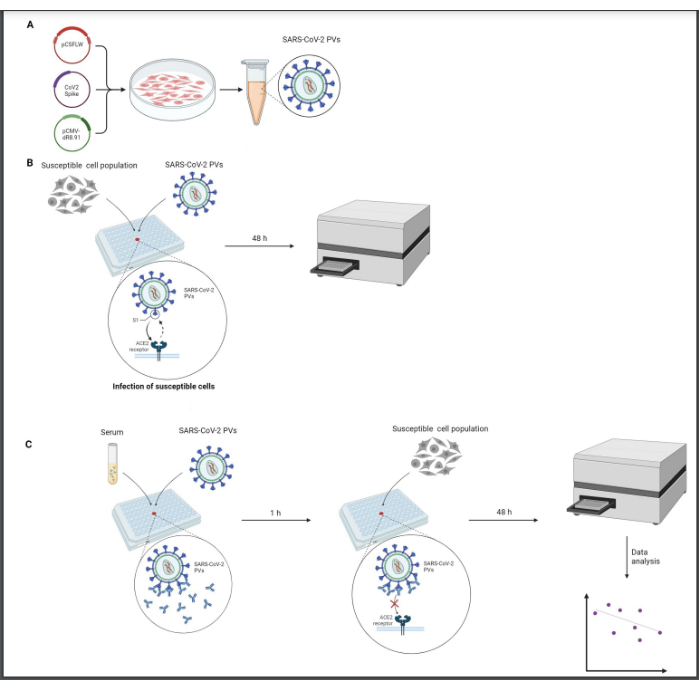
Şekil 1: Bir nötralizasyon testinin grafiksel gösterimi. (A) PV üretimi, (B) PV titrasyonu ve (C) nötralizasyon testi. Tüm işlemler steril koşullar altında sınıf-2 biyolojik başlıkta gerçekleştirilir. Nötralizasyon testinde (C) kullanılmadan önce PV'lerin enfektivite seviyelerini standartlaştırmak için titrasyon adımının (B) gerçekleştirilmesi gerekir. Bu figür BioRender ile oluşturulmuştur. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
1. SARS-CoV-2 PV üretimi ve bulaşıcılık testi
- Kullanılan transfeksiyon reaktifi ile uyumlu uygun bir hücre yoğunluğuna ulaşmak için 6 oyuklu bir plakada (6WP) Dulbecco'nun Modifiye Eagle Medium'unda (DMEM, yüksek glikoz,% 10 fetal sığır serumu (FBS),% 1 L-glutamin,% 1 penisilin / streptomisin) 5 x 105 HEK293T hücrelerini tohumlayın. Polietilenimin (PEI) ile transfeksiyon yapılması durumunda (reaktifi üretici talimatlarına göre hazırlayın), transfeksiyon gününde hücrelerin %40-60 yoğunluğa ulaştığından emin olun (adım 1.3). Hücreleri 37 °C ve %5CO2'de nemlendirilmiş bir inkübatörde tutun.
- Transfeksiyondan önce, daha yüksek transfeksiyon verimliliği elde etmek için kullanılmış hücre ortamını antibiyotiksiz taze ortamla (DMEM, yüksek glikoz,% 10 FBS,% 1 L-glutamin) değiştirin.
NOT: Tohumlamadan sonraki gün, HEK293T hücreler transfekte edilmeye hazırdır. - Yapışan HEK293T hücrelerini, üreticinin talimatlarına göre uygun bir transfeksiyon reaktifi ile transfekte edin. PEI kullanıyorsanız, iki karışım hazırlayın ve aşağıdaki adımları izleyin.
- Karışım A'yı hazırlamak için, 100 μL indirgenmiş serum ortamında 500 ng pCMV-dR8.91 ambalaj plazmidi16, 750 ng pCSFLW raportör plazmidi16 ve 450 ng SARS-CoV-2 Spike eksprese eden plazmid ekleyin.
- B karışımını hazırlamak için, indirgenmiş serum ortamının 100 μL'sine 17.5 μL PEI (konsantrasyon: 1 mg / mL) ekleyin.
- Her iki karışımın da oda sıcaklığında (RT) 5 dakika inkübe etmesine izin verin. Daha sonra, PEI karışımı B'yi DNA karışımı A'ya ekleyerek her iki tüpün içeriğini karıştırın.
- Tüpü RT'de 20-30 dakika inkübe edin. Karışımı arttırmak için tüpü her 3-4 dakikada bir hafifçe hafifçe vurun. Son olarak, karışımı HEK293T hücrelere ekleyin.
- Transfeksiyondan 16-20 saat sonra, kültür ortamını taze, tam DMEM ile değiştirin. 37 °C ve %5CO2'de inkübe edin, transfekte edilmiş hücreler tarafından PV'lerin üretilmesine izin vermek için.
- Transfeksiyondan 72 saat sonra, PV içeren süpernatanı hasat edin. Ardından, hücre kalıntılarını ve ölü hücreleri çıkarmak için oda sıcaklığında 7 dakika boyunca 1600 x g'da santrifüjleyin ve 0.45 μm selüloz asetat filtresinden süzün.
- İSTEĞE BAĞLI ADIM: PV titresinin nihai verimini artırmak için birden fazla transfeksiyon gerçekleştirin, PV'leri içeren hücre ortamını bir araya getirin ve konsantre tüpler kullanarak konsantre edin.
- Doğrudan sonraki adımlara geçin ("PV titrasyonu", bölüm 2) veya kullanıma kadar -80 °C'de saklamak için PV içeren ortamı uygun tüplerde ayırın. Titrasyon için kullanılacak ek bir alikot (400-500 μL) hazırlayın.
NOT: Birden fazla alikot yapmak, aşırı çözülme-donma döngülerinden kaçınarak deneyler arasında tekrarlanabilirliği garanti edecektir.
2. PV titrasyonu
- Sonraki adımlar için taze PV içeren ortamı kullanın veya yeni viral stoğun titrasyonunu gerçekleştirmek için test alikotunu (adım 1.7) çözün. Aynı PV stoğunun dondurulması, tekrarlanabilirliği garanti edecektir.
- PV stoğunu çoğaltmak için gerekli olan 96 kuyulu plakanın (96WP) tüm kuyucuklarına 50 μL tam DMEM (veya kullanımdaki hedef hücre hattıyla uyumlu tam ortam) ekleyin ve "A" satırını boş bırakın. "A" satırına 100 μL PV stoğu ekleyin. Test edilecek preparatların sayısına bağlı olarak, "yalnızca hücre" kontrolü olarak virüssüz bir sütun bırakın (Şekil 2).
- A satırından B satırına 50 μL pipetleyin ve ilk stoğun seri seyreltmelerini elde etmek için bu işlemi G satırına kadar tekrarlayın. Son satırdaki fazla birimi atın.
- Dulbecco'nun fosfat tamponu salin 1x'te (DPBS 1x) tripsin/etilendiamintetraasetik asit 1x (EDTA) kullanarak, harcanan ortamı çıkardıktan ve hücreleri DPBS 1x ile iki kez yıkadıktan sonra hücreleri ayırın. Hücreleri 4 x 105 hücre/mL yoğunluğa hazırlayın.
NOT: Bu protokolde, PV enfeksiyonu duyarlı hücre hattı HEK293T/ACE2 üzerinde test edilmiştir; bu tür hücreler, ACE2 reseptörünü eksprese etmek için bir lentiviral vektör kullanılarak transdüksiyon HEK293T türetilmiştir. - Oyuk başına 2 x 104 hücreli bir hücre sayısı sağlamak için her bir oyuğa 50 μL hücre süspansiyonu ekleyin.
- 37 °C ve %5CO2'de 48 saat inkübe edin.
- İnkübasyondan sonra, üreticinin talimatlarına göre okumayı elde etmek için Luciferaz testini gerçekleştirin. Kuyucuklara 100 μL lusiferaz reaktifi ekleyin ve karanlıkta RT'de 2 dakika inkübe edin. Her kuyucuğun içeriğini siyah bir 96 kuyulu plakaya (mevcut plaka okuyucu ile uyumlu) taşıyın ve plakaları 96 kuyulu bir plaka okuyucusunda okuyun.
NOT: Lusiferaz okuması için kullanılan luminometre, aşağı akış analizi için kullanılacak ham, işlenmemiş verileri içeren bir elektronik tablo dosyası üretecektir (bu durumda bir Excel dosyası). Virüsün bulaşıcılığı, bağıl lüminesans birimleri (RLU) olarak ifade edilecektir (paragraf 4.1'de açıklanmıştır).
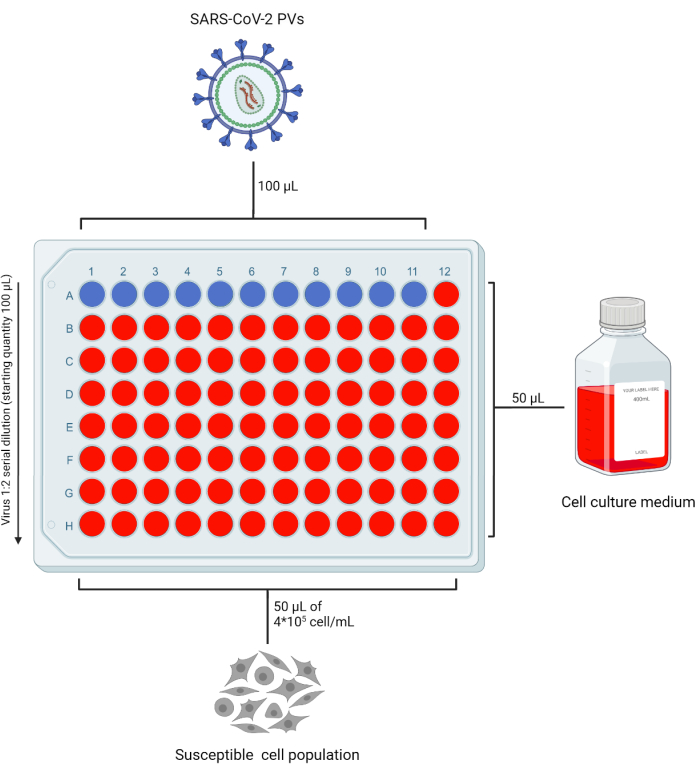
Şekil 2: PV titrasyonu için 96 kuyulu bir plakanın temsili yerleşimi. A satırına, sütun 1-11'e sabit hacimde PV içeren süpernatan eklenir ve seri olarak seyreltilir. Son sütun "yalnızca hücre" denetimi olarak bırakılır. Bu figür BioRender ile oluşturulmuştur. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
3. Nötralizasyon testi
- Hastaların serumlarını buz üzerinde çözdürün. Serum örneklerini 56 °C'de 30 dakika inkübe ederek inaktive edin.
- 96 oyuklu bir plakada, aşağıdaki oyukların her birine 50 μL taze, tam DMEM (veya kullanılan hedef hücre hattıyla uyumlu tam ortam) ekleyin: B satırından (sütun 1-10) H satırına (sütun 1-10). 95 μL taze, tam DMEM'i A satırına koyun (sütun 1-10). Sırasıyla 11 ve 12 numaralı sütunların kuyucuklarına 50 μL ve 100 μL tam DMEM ekleyin. Bunlar sırasıyla enfekte (virüs kontrolü veya VC) ve enfekte olmayan (sadece hücre veya CC) kontroller olacaktır (Şekil 3).
- A satırına 5 μL ısıyla inaktive serum/plazma numunesi ekleyin (sütun 1-10). Her örnek iki kopya olacaktır. Çok kanallı bir pipetle, numuneleri ilk sırada karıştırın ve 50 μL serum içeren ortamı A satırından B satırına taşıyın. Bu işlemi son satıra kadar tekrarlayın (Şekil 3). Kalan 50 μL'yi atın.
- Gerekli sayıda PV'nin alikotunu çözün ve ≥ 104 RLU/mL'ye seyreltin. Virüse ısıyla etkisiz hale getirilmiş serum/plazmanın 1:1 oranında seyreltilmesine ulaşmak için çok kanallı bir pipet kullanarak her bir oyuğa (kolon 1'den kolon 11'e) 50 μL seyreltilmiş PV içeren ortam ekleyin. Serum örneklerindeki antikorların PV'lerdeki SARS-CoV-2 spike proteinine bağlanmasına izin vermek için 37 °C ve %5 CO2'de 1 saat inkübe edin.
- 4 x 105 hücre / mL hücre yoğunluğunda en az 5 mL duyarlı hücre süspansiyonu (HEK293T / ACE2) hazırlayın. Her bir oyuğa 50 μL hücre süspansiyonu ekleyin ve 48 saat boyunca 37 ° C ve% 5CO2'de inkübe edin.
- İnkübasyondan sonra, lusiferaz tahlil okumasını adım 2.7'de açıklandığı gibi üreticinin talimatlarına göre gerçekleştirin.
NOT: Lusiferaz okuması için kullanılan luminometre, aşağı akış analizi için kullanılacak ham, işlenmemiş verileri içeren bir elektronik tablo dosyası (bu durumda .xlsx) üretecektir (Luciferaz tahlil dosyası).
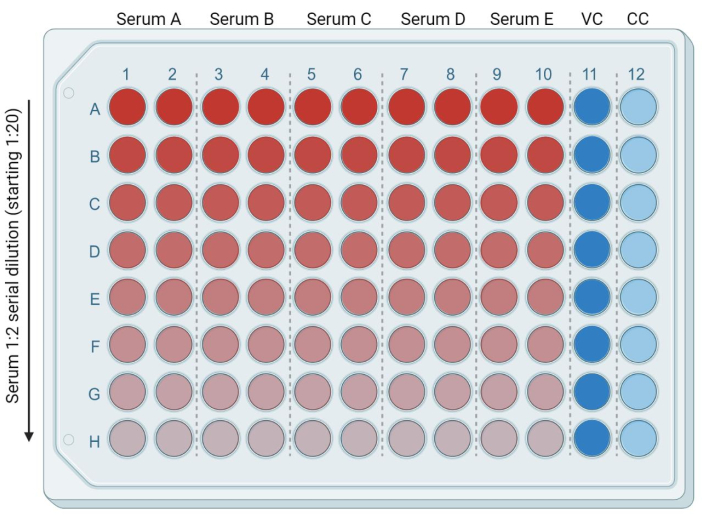
Şekil 3: Serum dilüsyonuna dayalı plaka gösterimi. Parlak kırmızı, daha yüksek miktarda seruma karşılık gelir ve parlak mavi şerit (sütun 11), enfekte hücre kontrolüne (VC, virüs kontrolü) karşılık gelir. Açık mavi şerit (sütun 12) enfekte olmamış hücrelere (CC, hücre kontrolü) karşılık gelir. Bu figür BioRender ile oluşturulmuştur. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
4. Titrasyon analizi
- Luciferaz tahlil dosyasında, adları/başlıkları ilgili örneklere atayın.
- RLU/mL elde etmek için RLU ölçümünü seyreltme faktörleriyle (ızgaranın üstünden altına: 20x, 40x, 80x, 160x, 320x, 640x, 1,280x, 2,560x) çarpın. Farklı seyreltme faktörleri kullanılıyorsa, çarpma faktörlerini buna göre değiştirin.
- Her PV preparatı için ortalama RLU/mL'yi hesaplayın.
5. PV nötralizasyon tahlil analizi
- Luciferaz tahlil elektronik tablo dosyasında (bu durumda, .xlsx), test edilen numunelere ilgili başlıkları atayın. Numunenin seyreltme faktörünü girin (40s, 80x, 160x, 320x, 640x, 1.280x, 2.560x, 5.120x). Seyreltme faktörlerinin Log10'unu hesaplayın.
- Enfekte olmamış ve enfekte kontrolün ortalama RLU'sunu hesaplayın (Şekil 3, sırasıyla sütun 11 ve 12). Bu değerler, adım 5.5'teki normalleştirme için yararlı olacaktır.
- Veri analizi için yeni bir belge açın. X/Y analizini seçin, X'i Sayılar olarak girin ve Y'yi girin 2 değerleri yan yana alt sütunlarda çoğaltın.
- Log10 (seyreltme) değerlerini X rakamı olarak girin. Örneklerin yinelenen RLU'sunu girin.
- Analiz Et > Normalleştir > Aynı sayfadaki tüm örnekleri İşaretle'ye gidin. Ortalama VC ve CC değerlerini sırasıyla %0 nasıl tanımlanır? ve %100 nasıl tanımlanır? Tamam'a tıklayın.
- Normalleştirilmiş veri sayfasında, > XY analizlerini analiz et > Doğrusal olmayan analizler (eğri uyumu) bölümüne gidin. Tüm örnekleri işaretleyin ve Tamam'a tıklayın. Doz-yanıt - İnhibisyon için, log (inhibitör) ve normalleştirilmiş yanıt - değişken eğimi seçin.
- Kısıtlama altında, HillSlope'u 0'dan küçük olmalıdır olarak değiştirin.
- Çıktı'nın altında Özet tablo ve grafik oluştur seçeneğini işaretleyin. Son analizleri almak için Tamam'a tıklayın. Analiz için bir şablon içeren bir çalışma sayfası Ek Dosya 1'de verilmiştir.
Sonuçlar
Bu protokol, anti-COVID-19 aşısı17 alan deneklerin serum/plazmasının nötralizasyon aktivitesini analiz etmek için SARS-CoV-2 PV'lerin üretimini ve bu PV'lerin aşağı akış uygulamasını açıklar. Ayrıca, bu protokol, nötralize edici yanıtın evrimini test etmek için her bir SARS-CoV-2 endişe varyantının (VOC) sözde tiplerini üretmek için uygulanabilir. COVID-19 aşılamasından sonra humoral immün yanıtın incelenmesini kolaylaştıran bu protokole rağmen, farklı serumla...
Tartışmalar
Vahşi tip bir virüs kullanmak gerçek enfeksiyonu simüle etse de, lentiviral PV'ler, patojenik virüslerle çalışmak için gerekli katı güvenlik gereksinimleri olmadan viral giriş ve enfeksiyonla ilişkili mekanizmaları incelemek için daha güvenli bir seçenektir 4,20,21. PV'ler, çalışmanın amacı olan patojenik bir virüsün yüzey zarfı glikoproteini ile çevrili replikasyon kusurlu bir viral çekirdekten oluş...
Açıklamalar
Yazarlar herhangi bir çıkar çatışması olmadığını beyan ederler.
Teşekkürler
Sağlık çalışanları gönüllülerinin katkılarını kabul ediyoruz. Bu proje, Mükemmellik Departmanı 2023/2027, MUR, İtalya tarafından desteklenmiştir. AR ve DZ, PRIN2022 (AB fonları; Yeni NesilEU)
Malzemeler
| Name | Company | Catalog Number | Comments |
| 0.45 μm filter | SARSTEDT | 83 1826 | |
| 6-well plate | SARSTEDT | 83 3920 | |
| 96-well plate | SARSTEDT | 8,33,924 | |
| Amicon Ultra-15 Centrifugal Filter Units | Merck | 10403892 | |
| Black Opaque 96-well Microplate | Perkin Elmer | 60005270 | |
| Dulbecco's Modified Eagle Medium | SIGMA-ALDRICH | D6546 - 500ML | |
| Dulbecco's phosphate buffered saline (PBS 1x) | AUROGENE | AU-L0615-500 | |
| Foetal Bovine Serum | AUROGENE | AU-S1810-500 | |
| Graphpad Prism version 7 | graphpad dotmatics | NA | In the manuscript, we replace the commercial name with 'data analysis program' |
| HEK293T cells | ATCC | CRL-3216 | |
| HEK293T/ACE2 cells | ATCC | CRL-3216 | HEK293T has been transduced to overexpress ACE2 with a lentiviral vector. |
| L-glutamine | AUROGENE | AU-X0550-100 | |
| Luminometer - Victor3 | Perkin Elmer | HH35000500 | In the manuscript, we replace the commercial name with 'luminometer' |
| Opti-MEM | Thermo Fisher Scientific | 11058021 | In the manuscript, we replace the commercial name with 'reduced serum medium' |
| p8.91 packaging plasmid | Di Genova et al., 2021 | A kind gift from Prof. Nigel Temperton (ref 16.) | |
| pCSFLW reporter plasmid | Di Genova et al., 2021 | A kind gift from Prof. Nigel Temperton (ref 16.) | |
| Penicillin/streptomycin | AUROGENE | AU-L0022-100 | |
| Polyethylenimine, branched (PEI) (25 kDa) | SIGMA-ALDRICH | 408727 | |
| RRL.sin.cPPT.SFFV/Ace2.IRES-puro.WPRE (MT126) | Addgene | 145839 | This plasmid was used to generate HEK293Tcells/ACE2 |
| SARS-CoV-2 Spike expressing plasmid | Addgene | pGBW-m4137382 | |
| steadylite plus Reporter Gene Assay System | Perkin Elmer | 6066759 | In the manuscript, we replaced the commercial name with 'luciferase reading reagent' |
| Trypsin EDTA 1x | AUROGENE | AU-L0949-100 |
Referanslar
- Ozaki, D. A., et al. International technology transfer of a GCLP-compliant HIV-1 neutralizing antibody assay for human clinical trials. Plos One. 7 (1), e30963 (2012).
- Pouget, M., et al. Generation of liposomes to study the effect of Mycobacterium tuberculosis lipids on HIV-1 cis- and trans-infections. International Journal of Molecular Sciences. 22 (4), 1945 (2021).
- McKay, L. G. A., et al. The HCV envelope glycoprotein down-modulates NF-κB signalling and associates with stimulation of the host endoplasmic reticulum stress pathway. Frontiers in Immunology. 13, 831695 (2022).
- Xiang, Q., Li, L., Wu, J., Tian, M., Fu, Y. Application of pseudovirus system in the development of vaccine, antiviral-drugs, and neutralizing antibodies. Microbiological Research. 258, 126993 (2022).
- Li, Q., Liu, Q., Huang, W., Li, X., Wang, Y. Current status on the development of pseudoviruses for enveloped viruses. Reviews in Medical Virology. 28, e1963 (2018).
- D'Apice, L., et al. Comparative analysis of the neutralizing activity against SARS-CoV-2 Wuhan-Hu-1 strain and variants of concern: Performance evaluation of a pseudovirus-based neutralization assay. Frontiers in Immunology. 13, 981693 (2022).
- Falzarano, D., Groseth, A., Hoenen, T. Development and application of reporter-expressing mononegaviruses: current challenges and perspectives. Antiviral Research. 103, 78-87 (2014).
- Gutierrez-Guerrero, A., Cosset, F. -. L., Verhoeyen, E. Lentiviral vector pseudotypes: Precious tools to improve gene modification of hematopoietic cells for research and gene therapy. Viruses. 12, 1016 (2020).
- Zufferey, R., Nagy, D., Mandel, R. J., Naldini, L., Trono, D. Multiply attenuated lentiviral vector achieves efficient gene delivery in vivo. Nature Biotechnology. 15 (9), 871-875 (1997).
- Dull, T. A third-generation lentivirus vector with a conditional packaging system. Journal of Virology. 72 (11), 8463-8471 (1998).
- Berkhout, B. A Fourth generation lentiviral Vector: Simplifying genomic gymnastics. Molecular Therapy. 25 (8), 1741-1743 (2017).
- Wu, X. Development and evaluation of a pseudovirus-luciferase assay for rapid and quantitative detection of neutralizing antibodies against Enterovirus 71. Plos One. 8 (6), e64116 (2013).
- Ferrara, F., et al. Development of lentiviral vectors pseudotyped with Influenza B hemagglutinins: application in vaccine immunogenicity, mAb potency, and sero-surveillance studies. Frontiers in Immunology. 12, 661379 (2021).
- Hu, J., et al. Development of cell-based pseudovirus entry assay to identify potential viral entry inhibitors and neutralizing antibodies against SARS-CoV-2. Genes & Diseases. 7 (4), 551-557 (2020).
- Dalle Carbonare, L., et al. Serology study after BTN162b2 vaccination in participants previously infected with SARS-CoV-2 in two different waves versus naïve. Communications Medicine. 1 (1), 38 (2021).
- Di Genova, C., et al. Production, titration, neutralisation, storage and lyophilisation of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) lentiviral pseudotypes. Bio-protocol. 11 (21), e4236 (2021).
- Chmielewska, A. M., Czarnota, A., Bieńkowska-Szewczyk, K., Grzyb, K. Immune response against SARS-CoV-2 variants: The role of neutralization assays. NPJ Vaccines. 6 (1), 1-8 (2021).
- Chen, Q., et al. Development and optimization of a sensitive pseudovirus-based assay for HIV-1 neutralizing antibodies detection using A3R5 cells. Human Vaccines & Immunotherapeutics. 14 (1), 199-208 (2018).
- Gauger, P. C., Vincent, A. L. Serum virus neutralization assay for detection and quantitation of serum neutralizing antibodies to influenza A virus in swine. Methods in Molecular Biology (Clifton, N.J). 2123, 321-333 (2020).
- Miglietta, R., Pastori, C., Venuti, A., Ochsenbauer, C., Lopalco, L. Synergy in monoclonal antibody neutralization of HIV-1 pseudoviruses and infectious molecular clones. Journal of Translational Medicine. 12 (1), 346 (2014).
- Chen, M., Zhang, X. -. E. Construction and applications of SARS-CoV-2 pseudoviruses: A mini review. International Journal of Biological Sciences. 17 (6), 1574-1580 (2021).
- Zipeto, D., et al. Induction of human immunodeficiency virus neutralizing antibodies using fusion complexes. Microbes and Infection. 8 (6), 1424-1433 (2006).
- WHO Coronavirus (COVID-19) Dashboard. Available from: https://covid19.who.int (2022)
- Zhou, P. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 579 (7798), 270-273 (2020).
- Chen, X., Huang, H., Ju, J., Sun, R., Zhang, J. Impact of vaccination on the COVID-19 pandemic in U.S. states. Scientific Reports. 12 (1), 1554 (2022).
- Stefani, C., Fantoni, T., Bissoli, M., Thomas, J., Ruggiero, A. HIV and SARS-CoV-2 Co-Infection: From Population Study Evidence to In Vitro Studies. Life. 12 (12), 2089 (2022).
- Watson, O. J., et al. Global impact of the first year of COVID-19 vaccination: a mathematical modelling study. The Lancet Infectious Diseases. 22 (9), 1293-1302 (2022).
- Cantoni, D. Analysis of antibody neutralisation activity against SARS-CoV-2 variants and seasonal human coronaviruses NL63, HKU1, and 229E induced by three different COVID-19 vaccine olatforms. Vaccines. 11 (1), 58 (2023).
- Siracusano, G., et al. Different decay of antibody response and VOC sensitivity in naïve and previously infected subjects at 15 weeks following vaccination with BNT162b2. Journal of Translational Medicine. 20 (1), 22 (2022).
- Ruggiero, A. SARS-CoV-2 vaccination elicits unconventional IgM specific responses in naïve and previously COVID-19-infected individuals. eBioMedicine. 77, (2022).
- Piubelli, C. Subjects who developed SARS-CoV-2 specific IgM after vaccination show a longer humoral immunity and a lower frequency of infection. eBioMedicine. 89, 104471 (2023).
- Zhang, G. F. Infectivity of pseudotyped SARS-CoV-2 variants of concern in different human cell types and inhibitory effects of recombinant spike protein and entry-related cellular factors. Journal of Medical Virology. 95 (1), e28437 (2023).
- da Costa, K. A. S. Influenza A (N1-N9) and Influenza B (B/Victoria and B/Yamagata) neuraminidase pseudotypes as tools for pandemic preparedness and improved influenza vaccine design. Vaccines. 10 (9), 1520 (2022).
- Condor Capcha, J. M. Generation of SARS-CoV-2 spike pseudotyped virus for viral entry and neutralization assays: a 1-week protocol. Frontiers in Cardiovascular Medicine. 7, 618651 (2021).
- Diomede, L., et al. Doxycycline inhibition of a pseudotyped virus transduction does not translate to inhibition of SARS-CoV-2 infectivity. Viruses. 13 (9), 1745 (2021).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır