A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
عن طريق الجلد كبدي الإرواء (PHP) مع ملفلان كعلاج للالغير قطوعة الانبثاث تقتصر على الكبد
In This Article
Summary
في هذا المخطوط، وصفنا عن طريق الجلد نضح الكبدي معزولة مع chemofiltration في وقت واحد لعلاج بسرطانة الكبد. يتم تنفيذ هذا الإجراء تحت التخدير العام في angiosuite من قبل فريق من ذوي الخبرة، تتكون من الأخصائي، وهو اختصاصي الإرواء السريري والتخدير.
Abstract
بسرطانة الكبد من سرطان القولون والمستقيم يمكن علاجها مع العلاج الكيميائي النظامية، والتي تهدف للحد من هذا المرض، تمديد بقاء أو إيقاف الانبثاث الغير قطوعة في تلك resectable. بعض المرضى ومع ذلك، يعانون من الآثار الجانبية أو التقدم تحت العلاج الشامل. للمرضى الذين يعانون من سرطان الجلد العنبي الجسد لا توجد خيارات العلاج النظامية القياسية. للمرضى دون مرض خارج الكبد، معزولة نضح الكبد (البرنامج الهيدرولوجي الدولي) قد تمكن من السيطرة على الأمراض المحلية مع الآثار الجانبية الجهازية محدودة. سابقا، تم تنفيذ هذا أثناء الجراحة المفتوحة مع نتائج مرضية، ولكن معدلات الاعتلال والوفيات المتعلقة بإجراءات فتح، يحظر تطبيق على نطاق واسع. لذلك، تم تطوير نضح الكبد عن طريق الجلد (PHP) مع chemofiltration في وقت واحد. وإلى جانب خفض معدلات الاعتلال والوفيات، وهذا الإجراء يمكن أن تتكرر، آملين أن يقودنا هذا إلى معدل الاستجابة العالي وتحسين البقاء على قيد الحياة (عن طريق السيطرة المحلية على المرض). خلال PHP، القطتوضع heters في الشريان الكبدي السليم، للبث وكيل العلاج الكيميائي، وفي الوريد الأجوف السفلي لنضح الدم chemosaturated عودته عبر الأوردة الكبدية. الوريد الأجوف القسطرة هي قسطرة البالون المزدوجة التي تحظر التسرب إلى الدوران الجهازي. ويستنشق الدم العائدين من الأوردة الكبدية من خلال fenestrations القسطرة ثم perfused من خلال نظام الترشيح من خارج مادية. بعد الترشيح، ويتم إرجاع الدم إلى المريض عن طريق القسطرة الثالثة في الحق حبل الوريد الداخلي. خلال PHP هي التي غرست جرعة عالية من ملفلان في الكبد، والتي هي سامة ومن شأنه أن يؤدي إلى مضاعفات تهدد الحياة عندما تدار بشكل منتظم. بسبب عدم استقرار الدورة الدموية الجسيمة الناجمة عن الجمع بين انسداد الأجوف الوريد وchemofiltration، ورصد الدورة الدموية والدورة الدموية الدعم هو من أهمية قصوى أثناء هذا الإجراء المعقد.
Introduction
استئصال أورام الكبد الخبيثة هو الخيار الأول لعلاج الأورام الخبيثة على حد سواء الكبد الأولية والثانوية. ومع ذلك، فإن نسبة كبيرة من المرضى غير المرشحين للجراحة بسبب مرض الموسعة أو موقع الانبثاث. للمرضى الذين يعانون من الانبثاث الغير قطوعة من سرطان القولون والمستقيم، والعلاج النظامية وغالبا ما يكون العلاج المفضل. الانبثاث الكبد من سرطان الجلد العنبي غالبا ما تكون صغيرة وتنتشر منتشرة في جميع أنحاء الكبد. لا العلاج المنهجي هو معيار متاح لهذه الفئة من المرضى. العلاج المحلي يمكن أن يكون بديلا للعلاج النظامية، في حال تقتصر على الانبثاث إلى الكبد.
بسبب تشريح الأوعية الدموية معين في الكبد، وهذا الجهاز يمكن عزله عن الدوران الجهازي. وهذا يسمح نضح من الكبد مع ارتفاع جرعة العلاج الكيميائي (برنامج الهيدرولوجي الدولي، معزولة نضح كبدي). الى جانب ذلك، الأورام الخبيثة في الكبد لديها امدادات الأوعية الدموية المهيمن أو حصرية من hepatiالشريان ج، مشتق بينما 70-80٪ من إمدادات من لحمة الكبد غير ورمي من الوريد البابي. 1، وضعت 2 هذه التقنية منذ أكثر من عشرين عاما، لعلاج المرضى الذين يعانون من الانبثاث الغير قطوعة من مختلف الأصول الأولية. 3، 4 خصوصا المرضى سرطان الجلد العنبي مع الانبثاث في الكبد قد يكون مرشحا للبرنامج الهيدرولوجي الدولي لأن الانبثاث غالبا ما تكون صغيرة ومنتشرة في جميع أنحاء الكبد بالكامل، وفي الوقت الحاضر لا يوجد علاج النظامية هو معيار متاح 5 و 6
مبدأ البرنامج الهيدرولوجي الدولي هو عزل مؤقتا الكبد من الدورة الدموية ويروي الجهاز مع جرعة عالية من العلاج الكيميائي، مما يؤدي إلى التعرض للمخدرات المحلية عالية مع الآثار الجانبية الجهازية محدودة. 7 هذه جرعة عالية من العلاج الكيميائي أن تكون سامة وتؤدي إلى مضاعفات عندما تدار بشكل منتظم. وقد أجريت معظم الدراسات البرنامج الهيدرولوجي الدولي مع ملفلان، ولقد حققت علاج metastasi كبديوتشير الصورة من مرضى سرطان القولون والمستقيم، وكذلك المرضى الذين يعانون من الانبثاث سرطان الجلد عنبوية 8،9 العديد من الدراسات من البرنامج الهيدرولوجي الدولي أثناء الجراحة المفتوحة أن هذا العلاج قد يكون فعالا: 50-59٪ معدلات الاستجابة الورم (استجابة جزئية وكاملة) لعلاج تم الإبلاغ عن سرطان القولون والمستقيم ومعدل استجابة الورم 68٪ للمرضى الذين يعانون من سرطان الجلد العنبي النقيلي. 8،10،11،12 وعلى الرغم من هذه النتائج العلاج، هذا الإجراء أبدا اكتسبت قبولا واسعا، بسبب تعقيد الإجراءات، ومدة المستشفى البقاء والاعتلال والوفيات المرتبطة بها.
نضح الكبد عن طريق الجلد (PHP) يقدم بديلا الغازية الحد الأدنى للبرنامج الهيدرولوجي الدولي وأظهر لأول مرة في نموذج الخنازير في عام 1993 باستخدام دوكسوروبيسين 13 والأولى من نوعها في محاكمة الإنسان كان يؤديها Ravikumar وآخرون. في عام 1994. 14 نظرا لعدم وجود أدلة على فعالية، تم التخلي عن هذه التقنية إلى حد كبير حتى في وقت مبكر 2000 عندما ثكما قيمت إعادة في المعهد الوطني للسرطان (NCI) في الولايات المتحدة. 15 خلال PHP، يتم وضع القسطرة عن طريق الجلد في الشريان الكبدي السليم عن طريق الشريان الفخذي للبث وكيل العلاج الكيميائي. يتم وضع القسطرة الثانية في الوريد الأجوف السفلي عن طريق الوريد الفخذي إلى نضح تدفق chemosaturated الكبدي (انظر الدائرة PHP في الشكل 1). القسطرة العزلة طموح وضعها في الوريد الأجوف هو قسطرة البالون مزدوجة، يحظر التسرب إلى الدوران الجهازي. يتم تصفية الدم chemosaturated يستنشق عن طريق فلتر الفحم مزدوج وعاد للمريض عن طريق القسطرة الثالثة وضعها في الوريد الوداجي الداخلي. واعترف المريض في المستشفى مع طول بقاء ~ 3 أيام. يتم تنفيذ الإجراء PHP في غرفة القسطرة تحت التخدير العام من قبل فريق متعدد التخصصات المدربين تدريبا جيدا وتتألف من مخصص التداخلية أشعة وتخدير وperfusio خارج الجسمنيست. والأورام الجراحية والاورام الطبية هم أيضا أعضاء في هذا الفريق متعدد التخصصات، والتركيز خصوصا على توعية المريض، واختيار المرضى والرعاية اللاحقة للعمليات الجراحية.
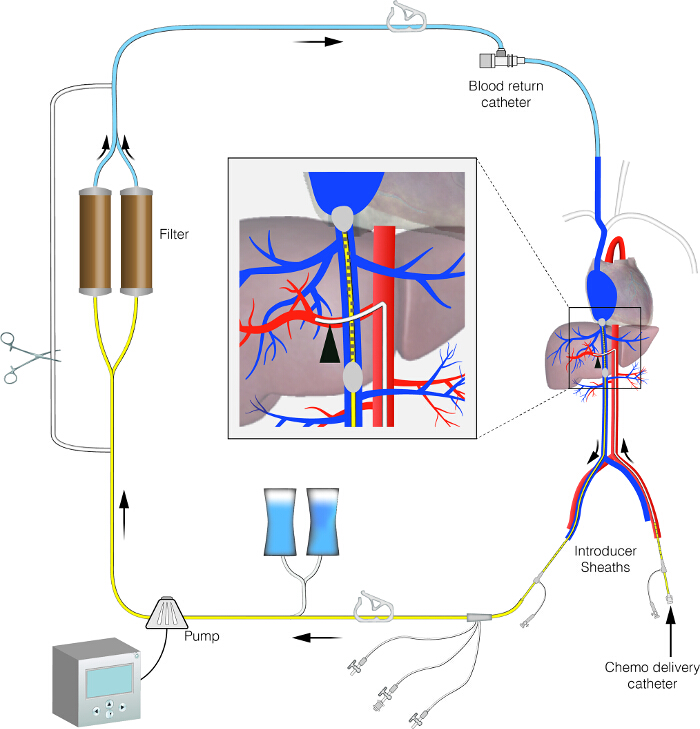
الشكل 1. صورة تخطيطية للدائرة PHP. يعرض هذا الرقم مجموعة المتابعة من الدائرة PHP. هذا يظهر دائرة نضح الكبدية المعزولة مع خط الالتفافية خارج مادية. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
ويرتبط هذا الإجراء الغازية مع الحد الأدنى من أقل معدلات الاعتلال المنطوق ويمكن أن يتكرر عدة مرات (على الأقل تصل إلى 4 مرات). الى جانب ذلك، فإنه يأخذ فقط حوالي 3-4 ساعة والانتعاش المريض بسرعة. ميزة PHP هو حقيقة أن جميع الأحجام من الانبثاث يمكن معالجته، والانبثاث الجزئي يجري تعامل بهاد كذلك. أيضا موقع الانبثاث، على مقربة من الهياكل الأوعية الدموية والقنوات الصفراوية، ليست موانع للPHP. وقد أجريت دراسات أولية مع شارع مرشح الجيل 1، مع 77٪ (يعني) كفاءة استخراج التصفية. 16 مؤخرا، ونشرت نتائج المحاكمة المرحلة الثالثة من هيوز وآخرون. مما يدل على تحسن ملحوظ في الكبد التقدم البقاء على قيد الحياة الحرة في عنبي مرضى سرطان الجلد مع نقائل كبدية تعامل مع PHP مقارنة مع أفضل رعاية بديلة. 17
منذ أبريل 2012 جيل 2 الثانية المرشح هو متاح. في دراسات ما قبل السريرية جيل مرشح 2 الثانية تستخرج 98٪ من ملفلان. وقد نشرت العديد من الدراسات وسلسلة من الحالات التحقيق PHP للمؤشرات متعددة، ولكن بصرف النظر عن محاكمة مرحلة النشر الثالثة الأخيرة، لم نطاق واسع تم تحليل البقاء على قيد الحياة. 16،18،19،20 في الدراسة الحالية، ونحن نركز على را التداخليةالإجراء diology، فضلا عن إدارة مخدر والدورة الدموية من خارج الجسم الذي يتم استخدامه أثناء هذا الإجراء من أجل تسهيل استخدام هذا العلاج في مراكز طبية أخرى.
Protocol
ملاحظة: بعد استيفاء المريض عن معايير الاشتمال وتقييمها بعناية من قبل طبيب الأورام الطبية، الجراح وطبيب التخدير، أدرج المريض في الدراسة. جميع المرضى شريطة موافقة خطية مستنيرة. تمت الموافقة على الدراسات السريرية التي كتبها لجنة الأخلاقيات الطبية المحلية من المركز الطبي لجامعة لايدن ويتم تنفيذ وفقا للمعايير الأخلاقية للإعلان هلسنكي.
1. تصوير الأوعية الدموية قبل الإجرائية التي كتبها التدخلي الأشعة
- استعدادا لإجراء PHP، إجراء القسطرة قبل الإجرائي 20 عدة أيام قبل PHP لرسم الخرائط الشرايين التشريح. خلال هذا الإجراء إجراء القسطرة من الشريان المساريقي العلوي (SMA) والجذع الاضطرابات الهضمية والشرايين الكبدية. 21
- خلال تصوير الأوعية، واستخدام عامل تباين باستخدام محقن مضخة في الشرايين الشرايين وفصي الكبد المشتركة باستخدام 2.4F أو 2.7F microcatheter. (المادةقائمة البند 7).
- ضخ 15 مل من النقيض غير المخفف (iopromide 300) (قائمة المواد، البند 14) بمعدل 5ML / ثانية لتصوير الأوعية من الشريان الكبدي و 12 مل في 3ML / ثانية لحقن فصي 21
- ترسيم تشريح الأوعية الدموية الكبدية وتوريد ورم الأوعية الدموية عن طريق حقن النقيض من ذلك كما هو موضح في الخطوة 1.1.2 21
- تحديد خطر ارتداد وكيل العلاج الكيميائي لhepatico-المعوية مفاغرة (مثل معدي إثناعشري أو شريان المعدة الأيمن). 21 تحديد المتغيرات الأوعية الدموية، مثل حق الشاذة أو اليسار الشريان الكبدي. 21
- في حالة وجود خطر محتمل من الجزر، إذا كان هناك أقل من ~ 1 سم من القاصي الشريان الكبدي السليم إلى الشريان معدي (GDA)، embolize هذا الشريان مع microcoils انفصال أو المكونات الأوعية الدموية (قائمة المواد، البند 15 و 16). embolize أيضا gastro- البعض و / أو مفاغرة معوية لمنع تدفق chemotheالمخدرات raputic إلى المنشآت الأخرى. 21
- Embolize فروع الشرايين البعيدة للموقع التسريب مع العرض الأوعية الدموية إلى المعدة والبنكرياس والأمعاء من الحجاب الحاجز. 21
2. PHP الإجراءات الأول: إعداد وإنشاء حلبة الإرواء
- إعداد من قبل اختصاصي الإرواء مادية إضافية (ECP)
- جمع tubingpack chemosaturation، chemofilters ومضخة طرد مركزي. (قائمة المواد والمواد 1B و 12) وتكتظ هذه العناصر في مربع المقدمة من قبل الشركة المصنعة.
- تدفق الدائرة خارج الجسم كاملة مع غاز ثاني أكسيد الكربون 2.
- رئيس الدائرة مع كلوريد الصوديوم 0.9٪ والهيبارين (2000 وحدة دولية / لتر) بما في ذلك المرشحات.
- شطف نظام خارج الجسم مع 6 لتر من heparinized كلوريد الصوديوم 0.9٪، في البداية بواسطة قوة الجاذبية باعتبارها primeline غير موجودة بالفعل في النظام. بعد رطب مرشحات الكربون بشكل كامل، استخدم ص الطرد المركزيالحزب الحاكم لوضع المزيد من الضغوط على المرشحات، من أجل إزالة فقاعات الغاز المتبقي.
ملاحظة: مطرقة صغيرة يمكن استخدامها لإزالة فقاعات الغاز عن طريق الاهتزاز والرنين.- رئيس مزدوجة خط بالون قسطرة وخط الالتفافية.
- chemofilter رئيس اليسار (مع 1 لتر) وإزالة فقاعة، chemofilter الحق في ذلك الحين رئيس الوزراء (مع 1 لتر) وإزالة فقاعة.
- chemofilters هيدرات (3 L في خرطوشة) بعد فتيلة الأولي لنظام ببطء. هذا يمكن أن يستغرق 10-20 دقيقة لكل chemofilter.
- فخ فقاعة رئيس (فلتر الشرياني).
- شطف نظام خارج الجسم مع 6 لتر من heparinized كلوريد الصوديوم 0.9٪، في البداية بواسطة قوة الجاذبية باعتبارها primeline غير موجودة بالفعل في النظام. بعد رطب مرشحات الكربون بشكل كامل، استخدم ص الطرد المركزيالحزب الحاكم لوضع المزيد من الضغوط على المرشحات، من أجل إزالة فقاعات الغاز المتبقي.
- فحص ومعايرة أجهزة الاستشعار تدفق وضغط المراقبين، كما كان مخططا في قائمة البرامج مضخة طرد مركزي، وفقا لتعليمات الشركة الصانعة.
- تحضير المريض في غرفة تصوير الأوعية الدموية عن طريق التخدير
- إعداد المراقبة اللازمة لإدارة التخدير:
- وضع الفرقة ضغط الدم غير الغازية ضغط الدم قياس تخطيط القلبالأقطاب الكهربائية على صدره المريض لمراقبة تخطيط القلب وكذلك ساو 2 الرصد.
- وضع Bispectral مقياس مؤشر (BIS) جهاز استشعار على جبهته المريض لقياس عمق المريض من التخدير، في هذه الحالة يتم استخدام التخدير للعمل مع هذا.
- إعداد معدات التهوية وفقا لتعليمات الشركة الصانعة، بما في ذلك ET-CO 2 عبر آلة التهوية وأنابيب القصبة الهوائية. وضع آلة التهوية على الجانب المقابل للمريض من حيث الأشعة تحت الحمراء يقف، وفقا لتعليمات الشركة المصنعة.
- وضع المريض على طاولة غرفة تصوير وتغطية مباشرة للمريض مع بطانية الهواء الدافئ ل mantain سوائية الحرارة.
- وضع على وصول وريدي الطرفية في الوريد الذراع اليمنى للإدارة الرابع التخدير والسوائل الوريدية.
- حمل التخدير (مع التخدير في تفضيل تخدير)، وإجراء التنبيب الرغامي وتبدأ كثافة العملياتermittent التهوية بالضغط الإيجابي (IPPV).
- الحفاظ على التخدير لبنك التسويات الدولية = 50 حسب ما أوردته و= 65 مم زئبق، normuria من 0.5 مل / كغ / ساعة.
- وضع البلعوم الحرارة درجة حرارة الجسم.
- وضع قطار من أربعة (TOF) أقطاب لرصد الحصار العصبية والعضلية كما هو موضح في تعليمات الشركة الصانعة (في تفضيل طبيب التخدير).
- إعداد وإعداد نظام سريع إدارة السائل / أو السوائل الدافئة (قائمة المواد، البند 2) كما هو موضح في تعليمات الشركة الصانعة.
- تشغيل شاشة العرض المتقدمة (قائمة المواد، البند 4) وتوصيل جميع الكابلات.
- إدراج G خط الشرايين 22 في الشريان الكعبري غادر لمراقبة الضغط الشرياني يعني (MAP). (قائمة المواد، البند 3).
- وضع خط وريدي مركزي لقياس الضغط الوريدي المركزي في الوريد الوداجي الداخلي الأيسر.
- ادخال قسطرة المثانة البولية.
- الحفاظ على سوائية الحرارة بذ البطانيات الهواء الدافئ والسوائل الوريدية الدافئة.
- CVP رصد وداخل الشرايين ضغط الدم باستخدام جهاز متطور (قائمة المواد، البند 4) في جميع أنحاء الداخلي.
- تحديد خط الأساس تنشيط زمن التخثر (ACT) عن طريق رسم عينة من الدم ووضعه في متر ACT.
- وبالإضافة إلى ذلك، في تحريض إدارة الوريد سيفازولين 1 غرام، بانتوبرازول 40 ملغ و 300 ملغ الهيدروكورتيزون.
- إعداد المراقبة اللازمة لإدارة التخدير:
- إعداد من قبل صيدلي
- إعادة ملفلان (3.0 ملغم / كغم من وزن الجسم (الجرعة القصوى 220 ملغ) (قائمة المواد، البند 9)) عن طريق حقن بسرعة 10 مل من مخفف الموردة مباشرة في قارورة من مسحوق مجفف بالتجميد باستخدام إبرة معقمة (20 G أو إبرة أكبر قطر ) والحقنة.
- يهز فورا قارورة بقوة حتى يتم الحصول على حل واضح. وهذا يوفر 5 ملغ / مل حل ملفلان.
- على الفور تخفيف الجرعة إلى أن تدار في كلوريد الصوديوم حقن 0.9٪، جامعة جنوب المحيط الهادئ، لتركيز لا تزيد عن 0.45 ملغ / مل.
- إدارة كاملة في غضون 60 دقيقة من إعادة.
- إعداد على غرفة تصوير الأوعية الدموية التي كتبها التدخلي الأشعة (الأشعة تحت الحمراء)
- وضع الأدوات واللوازم (العقيمة) اللازمة في الجدول. (قائمة المواد والبنود 1A، 3،5،6،7،8،11).
- تغطية المريض مع ورقة معقمة.
- موضع شوبا من الأشعة تحت الحمراء
- استخدام توجيه الموجات فوق الصوتية لوضع الأغماد في عروق الوريد الداخلية (IJV) على حد سواء الأيمن والأيسر.
- وضع 7.5F التجويف ثلاثية قسطرة وريدية، 20 سم (قائمة المواد، البند 5) في IJV نقاط. يستخدم هذا الغلاف من قبل طبيب التخدير لقياس CVP وضخ محاكي ودي.
- وضع 10F الوريدية عودة القسطرة (قائمة المواد، البند 1A) في حق IJV. يستخدم هذا الغلاف لالعائد الوريدي من الدم تصفيتها بعد chemofiltratio خارج الجسمن.
- وضع غمد 5F إلى اليسار الشريان الفخذي المشترك (CFA) (قائمة المواد، البند 6).
ملاحظة: يتم استخدام هذا غمد لmicrocatheter وضع محوري للبث وكيل العلاج الكيميائي. - وضع غمد 18F إلى اليمين الوريد الفخذي المشترك (CFV) (قائمة المواد، البند 8) بعد اتساع التسلسلي مع 8-10F و12-14F الموسعات. استخدام الموسعات لضبط افتتاح الإدراج إلى الحجم المناسب لوضع نهاية المطاف بشكل صحيح غمد 18F. ملاحظة: يتم استخدام هذا غمد لإدخال القسطرة البالونية مزدوجة (عزل الطموح القسطرة).
- عزل الكبدي الوريد وإنشاء حلبة خارج الجسم
- إدارة الهيبارين بعد أن تم وضع كل الأغماد. في جرعة أولية من 300 وحدة دولية / كغ (قائمة المواد، البند 11).
- المحافظة على الوقت تخثر المنشط (ACT) فوق 50 ثانية خلال الإجراء بأكمله مع جرعات إضافية الهيبارين البلعة كما هو مطلوب.
- ستاغ بافراز (50 مل 0.2mg / مل) 0،1-2 ميكروغرام / كغ / دقيقة وفينيليفرين (50 مل 0.1mg / مل) 0،1-2 ميكروغرام / كغ / دقيقة، وإدارة السوائل (500 مل من بلورانيات) للحفاظ على المعلمات الدورة الدموية وثيقة لضغط متوسط الشرياني (MAP) من 65 مم زئبق، وكمية البول من 0.5 مل / كغ / ساعة.
- من خلال غمد 5F في الأيسر الشريان الفخذي المشترك، ويعرض microcatheter 2.7F (قائمة المواد، البند 7) شارك في محوريا ووضعه في الشرايين الشريان أو فصي الكبد باستخدام المناسبة مراقبة الأوعية.
- من خلال غمد 18F في حق الوريد الفخذي المشترك، ويعرض 16F بالون قسطرة مزدوجة (عزل الطموح القسطرة) ووضعه مع طرف في الأذين الأيمن باستخدام الرصد الأوعية.
- مباشرة بعد وضع القسطرة، ونعلق هذه إلى النظام خارج الجسم باستخدام نقاط الاتصال الخاصة؛ خط عودة الوريدي إلى غمد في IJV وخطوط تدفق لالقسطرة العزلة.
- بدء جمضخة entrifugal كما هو موضح من قبل الشركة المصنعة:
ملاحظة: جميع خطوط مفتوحة الآن وتدفق تشغيل على خط الالتفافية. - بعد الحقن في الوريد من محلول 0.5 L الغروي (قائمة المواد، البند 13)، تضخيم بالون الجمجمة مع المياه المالحة 50٪ و 50٪ خليط سائل الإعلام التباين.
- مع البالون الذيلية لا يزال بددت، يتراجع ببطء القسطرة البالونية مزدوجة حتى البالون الجمجمة هو عند تقاطع الأذين الأيمن والوريد الأجوف السفلي (IVC)، فقط فوق الوريد الكبدي الأيمن (البالون هو الآن على شكل وتد، كما هو موضح في الشكل 2).
- تضخيم بالون الذيلية مع خليط من 90٪ المالحة وسائط تباين 10٪ حتى تبدأ الحواف الجانبية للبالون منتفخ لتصبح ممسوح من قبل IVC.
وتضخم البالونات مع خليط من مختلف وسائل الإعلام على النقيض: مذكرة. البالون الذيلية هو تضخم لعرقلة الوريد الأجوف السفلي فوق أوردة الكلى، لذلك الانعزال الذي تدفق الوريدي الكبدي و مدمج الدورة الدموية الوريدية النظامية. ويمكن حقن حجم القصوى 38 مل في كل بالون. - تحقق المواقع من البالونات ويستبعد تسرب مع الوريد
- أداء الوريد عن طريق حقن 20 مل من المقابل (أي iopromide 300) عن طريق ميناء نوفذة البالون المزدوج الوريدية قسطرة البالون المزدوج باستخدام حقن اليد.
- إذا رأيت تسرب النقيض من ذلك، إعادة البالونات أو مواصلة تضخيم بالونات وتكرار الوريد كما هو موضح في الخطوة 2.6.11.1 (انظر الشكل 2).
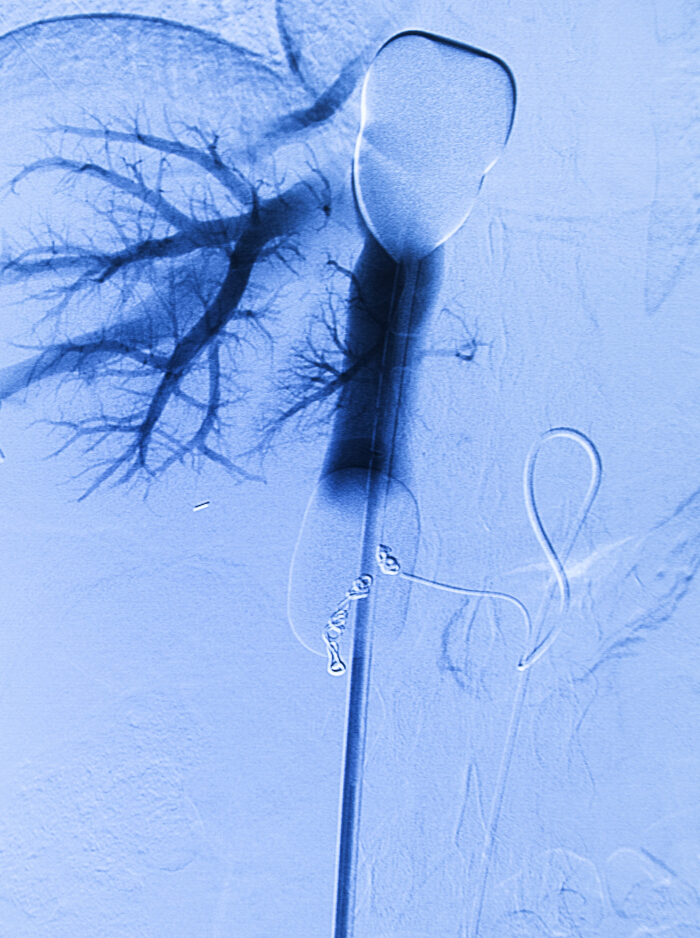
الشكل 2. لكل إجرائية وعائية. الوريدية مزدوجة قسطرة البالون في أدنى الأجوف قسطرة الوريد والشرايين ضخ في الشريان الكبدي السليم. يتم حقن النقيض إلى الوراء عن طريق القسطرة الوريدية. لفائف من تصوير ما قبل الإجرائية والانصمام في مكانها الصحيح.ww.jove.com/files/ftp_upload/53795/53795fig2large.jpg "الهدف =" _ فارغة "> الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
- إغلاق الدائرة
- ضخ 0.5 لتر آخر من حل الغروي. تأكد من أن chemofilters اثنين مغلقة في هذه اللحظة من الزمن، في حين أن تجاوز مفتوح.
- في محاولة لتحقيق تدفق كاف (س = 400-500 مل / دقيقة) مع الضغوط آمن الداني (بشكل عام <-70 مم زئبق) والبعيدة (<100 مم زئبق) من مضخة الطرد المركزي (قائمة المواد، البند 12).
- عاير بافراز 0،1-2 ميكروغرام / كغ / دقيقة وفينيليفرين 0،1-2 ميكروغرام / كغ / دقيقة، وإدارة السوائل للحفاظ على BP الانقباضي من 160 مم زئبق، وكمية البول من 0.5 مل / كغ / ساعة.
- عند الوصول إلى التدفقات والضغوط الكافية، فتح المرشحات واحد تلو الآخر.
ملاحظة: مرور الدم على الرغم من أن المرشحات سوف hemofiltrate الدم وإزالة معظم وكيل العلاج الكيميائي. يحدث ترشيح الدم في جميع أنحاء proceduإعادة وكذلك في فترة 'فشل' بعد فترة العلاج الكيميائي التسريب مباشرة. خلال هذه الفترة تبييض، وكيل العلاج الكيميائي الذي يعود من أنسجة الكبد، و"جرفت" من التداول. - عندما تم التوصل إلى BP الانقباضي بين 140-160 مم زئبق، أغلق الخط الالتفافي.
ملاحظة: التخدير يجب أن تكون على استعداد لمواجهة انخفاض في ضغط الدم الناتج عن انخفاض في التحميل المسبق بسبب انسداد الوريد الأجوف، توسع الأوعية المحيطية من مرور الدم من خلال إزالة chemofilters وكلاء فعال في الأوعية (على سبيل المثال، بافراز وفينيليفرين) من قبل chemofilters و ربما آثار vasodilative الإنتاج NO الذاتية. ضبط معدلات ضخ بافراز وفينيليفرين وفقا لذلك الحفاظ على خطة من 65 مم زئبق. - تحقق لتحديد المواقع من القسطرة البالونية مزدوجة عن طريق إجراء الوريد (كما هو موضح في الخطوة 2.6.11.1).
- إجراء عائية عن طريق حقن الكونترار (iopromide 300) من خلال microcatheter في الشريان الكبدي إلى يستبعد تشنج الشرايين. إذا رأيت تشنج، إدارة 100-200 ميكروغرام من النيتروجلسرين في الشريان الكبدي (كما هو موضح أيضا في الخطوة 1.1 و الخطوات الفرعية).
3. PHP الإجراءات الثاني: تسريب من العلاج الكيميائي وتبييض الفترة
- ضخ ملفلان
ملاحظة: بعد وضع الدائرة نظام التسليم، وبدء ضخ ملفلان في الشريان الكبدي من خلال microcatheter.- عندما يتم تأسيس معدل تدفق مستمر، أي تسرب موجود وضغط دم المريض مستقرة، وضخ ملفلان بجرعة 3 ملجم / كجم في الشريان الكبدي السليم أو بالتتابع في كل من الشرايين فصي.
- لا تبدأ العلاج الكيميائي ضخ حتى خطة عمل البحر المتوسط أعلى من 65 مم زئبق.
- حقن الدواء في جرعة من 100 مل باستخدام السيارات حاقن بمعدل 0.4 سم / ثانية، ما يقرب من 30 دقيقة، أونتيل يتم حقن الجرعة كاملة.
- خلال التسريب، على فترات منتظمة، إجراء التصوير الشرياني لمراقبة حدوث بالتشنج والموقف وكبح التضخم من القسطرة البالونية مزدوجة مع التنظيف التباين. (راجع الخطوة 2.6.11.1 (الوريد) و 1.1 و 2.7.9 (تصوير) للحصول على معلومات عن وكيل النقيض من ذلك).
- في حالة بالتشنج وإدارة نيترو-الغليسيرين (100-200 ميكروجرام).
- بعد 30 دقيقة من الحقن المعالجة الكيميائية، ومواصلة ترشيح الدم لفترة إضافية تبييض 30 دقيقة (انظر الملاحظة في خطوة 2.7.5).
- إدارة 10 ملغ من المورفين الرابع للسيطرة على الألم بعد العملية الجراحية.
- بعد إخفاق الفترة فرغ ببطء البالونات اثنين في الوريد الأجوف.
- عندما يتم تأسيس معدل تدفق مستمر، أي تسرب موجود وضغط دم المريض مستقرة، وضخ ملفلان بجرعة 3 ملجم / كجم في الشريان الكبدي السليم أو بالتتابع في كل من الشرايين فصي.
- نهاية تسريب وإزالة القسطرة
- في نهاية الفترة تبييض، تفريغ الدائرة خارج الجسم قدر الإمكان ومن ثم وقف نضح خارج الجسم.
- وقف centrifuمضخة غال وقطع الأنابيب.
- إزالة القسطرة البالونية مزدوجة وmicrocatheter التسريب، ولكن ترك الأغماد الوصول في مكان حتى يتم تطبيع تخثر. ويمكن وضع جهاز إغلاق الأوعية الدموية في الشريان الفخذي المشترك لتحقيق تخثر الدم.
- إبقاء القسطرة العودة في حق IJV في مكان حتى يتم تطبيع الشخصية التخثر.
- الحفاظ على 7.5F قسطرة وريدية التجويف ثلاثة أضعاف في IJV تترك في مكان لهذا يمكن استخدامه في وحدة العناية التخدير المشاركة (PACU).
- نهاية التخدير وتنقص
ملاحظة: نفذ الخطوات التالية في نهاية الإجراء، عند الانتهاء من نقل الدم لصناعة السيارات.- إغلاق وإزالة الدائرة الالتفافية.
- وقف ضخ بافراز وفينيليفرين فور مزدوج الانكماش البالون. وهذا ممكن بسبب عودة التحميل المسبق كافية لقلب الصحيح وإنهاء chemofiltration.
- تطبيع تخثر مع بروتامين (1: 1)، والبلازما الطازجة المجمدة و / أو الراسب القري مع أو بدون نقل من thrombocytes. تحقق ACT بعد ذلك.
- بعد استقرار الدورة الدموية وإنهاء بافراز وضخ فينيليفرين، إنهاء الدواء صيانة مخدر.
- بعد أن عاد المريض إلى التهوية العفوية وعيه، وينزع الأنبوب في القصبة الهوائية للمريض.
- نقل المريض إلى PACU لمدة 24 ساعة من مراقبة وظائف حيوية (ضغط الدم والمعلمات التخثر).
- إزالة غمد الأوعية الدموية مرة واحدة في عدد الصفائح الدموية> 50 × 10 9 / L، APTT <1.5 × العادي، وINR <1.5. تطبيق ضغط اليدوي لتحقيق تخثر الدم وتطبيق ضمادة الضغط على كل من الخاصرتين.
- العناية بعد الجراحة
- مراقبة المرضى في PACU لأول ساعة 24 بعد العملية.
- فحص الموقع الارقاء من inserti قسطرةعلى والنبض رصد وضغط الدم ودرجة الحرارة والتهوية وتوازن السوائل وعشرات الألم، فضلا عن تجلط الدم.
- نقل المريض إلى قسم ما بعد الجراحة لمدة 1-2 أيام.
- إخراج المريض في اليوم التالي للجراحة 2 من 3، بعد أمراض الدم والكيمياء اختبار الدم النهائي. تحقق لتسمم الكبد وإنشاء خط الأساس لمتابعة سمية - وقت البروثرومبين (PT) في غضون 2 ثانية من الحد الاعلى للطبيعي، المنشط الجزئي تجلط الدم الوقت (APTT) ضمن المعدل الطبيعي، والصفائح الدموية> 75000 / مم 3 دون نقل الصفائح الدموية أو> 100000 / مم 3 مع نقل، عاد الهيموغلوبين> 10 غ / دل (> 6.2 ملمول / لتر) واسبارتاتي ناقلة أمين الألانين وألانين (AST / ALT) إلى حدود 10٪ من مستويات خط الأساس.
- إدارة مستعمرة تحفيز النمو الدعم عامل (pegfilgastrim، 0.6 الحقنة مل) عند التفريغ أو خلال 48 ساعة بعد العلاج PHP.
النتائج
ويستند المعرفة حول PHP على مرحلة صغيرة أنا والمحاكمات الثاني وسلسلة القضية ومحاكمة مرحلة أكبر الأخيرة الثالث؛ وأظهرت لمحة عامة عن النتائج التي نشرت في الجدول 1. وتناقش ورقة واحدة لإجراء التخدير، الدورة الدموية والتمثيل الغذائي جوانب من الع...
Discussion
المرضى الذين يعانون من بسرطانة الكبد يمكن علاجها مع العلاج المنهجي. ومع ذلك، للمرضى الذين يعانون سرطان الجلد المنتشر العنبي، أي العلاج المنهجي هو معيار المتاحة ووالعلاج المناعي أو العلاج الموجه لم تكن حتى الآن قادرة على أن تظهر تحسين البقاء على قيد الحياة. وقد تب...
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors have no acknowledgements.
The phase II study is financially supported by Delcath Systems.
Materials
| Name | Company | Catalog Number | Comments |
| Delcath 2nd Generation Hepatic CHEMOSAT Delivery System | Delcath Systems Inc., New York, New York, USA | 602001 and 602002 | Item no. 1 |
| Isofuse Isolation Aspiration Catheter (Double Balloon Catheter) | Delcath Systems Inc., New York, New York, USA | Item no. 1a | |
| 10F Venous Return Catheter | Delcath Systems Inc., New York, New York, USA | ||
| Hemofiltration Cartridges | Delcath Systems Inc., New York, New York, USA | Item no. 1b | |
| Circuit components | Delcath Systems Inc., New York, New York, USA | ||
| Level-1 rapid fluid management system | Smiths Medical | Item no. 2 | |
| 22 G arterial line | Arrow International Inc. / Teleflex Inc.,Dublin, Ireland | Item no. 3 | |
| Vigileo, Monitor | Edwards Lifesciences Corp, Irvine, California, USA | Item no. 4 | |
| 7.5F Triple lumen intravenous catheter, 20 cm | Vygon, Valkenswaard, Nederland | Item no. 5 | |
| 5F sheath | Item no. 6 | ||
| 2.7 Progreat microcatheter | Terumo, Tokyo, Japan | MC-PP27131 | Item no. 7 |
| 18F sheath | Item no. 8 | ||
| Auto-injector Medrad Mark V ProVis | Bayer, Indianola, Pennsylvania, USA | Not available anymore, replaced by Medrad Mark 7 Arterion Injection System | Item no. 9 |
| Melphalan | Alkeran, Aspen Pharmacare, Dublin, Ireland | Item no. 10 | |
| Heparin LEO, 5,000 IE/ml | LEO Pharma AB, Denmark | Item no. 11 | |
| Centrifugal pump | Medtronic, Minneapolis, Minnesota, VS | Item no. 12 | |
| Voluven colloid solution (6% hydroxyethyl starch 130/0.4 in 0.9% sodium chloride injection) | Item no. 13 | ||
| Iopromide 300, Ultravist | Bayer, Indianola, Pennsylvania, USA | Item no. 14 | |
| Detachable coil, Interlock | Boston Scientific, Marlborough, Massachusetts, USA | Item no. 15 | |
| Vascular plug, Amplatzer 4 | St. Jude Medical, St Paul,Minnesota, USA | Item no. 16 |
References
- Jovanovic, P., et al. Ocular melanoma: an overview of the current status. Int J Clin Exp Pathol. 6 (7), 1230-1244 (2013).
- Taylor, I., Bennett, R., Sherriff, S. The blood supply of colorectal liver metastases. Br J Cancer. 38 (6), 749-756 (1978).
- van de Velde, C. J., et al. A successful technique of in vivo isolated liver perfusion in pigs. J Surg Res. 41 (6), 593-599 (1986).
- Vahrmeijer, A. L., Der Eb, M. M. V. a. n., Van Dierendonck, J. H., Kuppen, P. J., Van De Velde, C. J. Delivery of anticancer drugs via isolated hepatic perfusion: a promising strategy in the treatment of irresectable liver metastases?. Semin Surg Oncol. 14 (3), 262-268 (1998).
- Vahrmeijer, A. L., van de Velde, C. J., Hartgrink, H. H., Tollenaar, R. A. Treatment of melanoma metastases confined to the liver and future perspectives. Dig Surg. 25 (6), 467-472 (2008).
- Ben-Shabat, I., et al. Isolated hepatic perfusion as a treatment for liver metastases of uveal melanoma. J Vis Exp. (95), e52490 (2015).
- Vahrmeijer, A. L., et al. Increased local cytostatic drug exposure by isolated hepatic perfusion: a phase I clinical and pharmacologic evaluation of treatment with high dose melphalan in patients with colorectal cancer confined to the liver. Br J Cancer. 82 (9), 1539-1546 (2000).
- Rothbarth, J., et al. Isolated hepatic perfusion with high-dose melphalan for the treatment of colorectal metastasis confined to the liver. Br J Surg. 90 (11), 1391-1397 (2003).
- van Iersel, L. B., et al. Isolated hepatic perfusion with 200 mg melphalan for advanced noncolorectal liver metastases. Ann Surg Oncol. 15 (7), 1891-1898 (2008).
- van Iersel, L. B., et al. Isolated hepatic melphalan perfusion of colorectal liver metastases: outcome and prognostic factors in 154 patients. Ann Oncol. 19 (6), 1127-1134 (2008).
- Alexander, H. R., et al. A phase I-II study of isolated hepatic perfusion using melphalan with or without tumor necrosis factor for patients with ocular melanoma metastatic to liver. Clin Cancer Res. 6 (8), 3062-3070 (2000).
- Olofsson, R., et al. Isolated hepatic perfusion for ocular melanoma metastasis: registry data suggests a survival benefit. Ann Surg Oncol. 21 (2), 466-472 (2014).
- Curley, S. A., et al. Increased doxorubicin levels in hepatic tumors with reduced systemic drug exposure achieved with complete hepatic venous isolation and extracorporeal chemofiltration. Cancer Chemother Pharmacol. 33 (3), 251-257 (1993).
- Ravikumar, T. S., et al. Percutaneous hepatic vein isolation and high-dose hepatic arterial infusion chemotherapy for unresectable liver tumors. J Clin Oncol. 12 (12), 2723-2736 (1994).
- Lillemoe, H. A., Alexander, H. R. Current Status of Percutaneous Hepatic Perfusion as Regional Treatment for Patients with Unresectable Hepatic Metastases: A Review. Am Oncology and Hematology Rev. (15-23), (2014).
- Pingpank, J. F., et al. Phase I study of hepatic arterial melphalan infusion and hepatic venous hemofiltration using percutaneously placed catheters in patients with unresectable hepatic malignancies. J Clin Oncol. 23 (15), 3465-3474 (2005).
- Fitzpatrick, M., et al. Use of partial venovenous cardiopulmonary bypass in percutaneous hepatic perfusion for patients with diffuse, isolated liver metastases: a case series. J Cardiothorac Vasc Anesth. 28 (3), 647-651 (2014).
- Forster, M. R., et al. Chemosaturation with percutaneous hepatic perfusion for unresectable metastatic melanoma or sarcoma to the liver: a single institution experience. J Surg Oncol. 109 (5), 434-439 (2014).
- Deneve, J. L., et al. Chemosaturation with percutaneous hepatic perfusion for unresectable isolated hepatic metastases from sarcoma. Cardiovasc Intervent Radiol. 35 (6), 1480-1487 (2012).
- Kandarpa, K., Machan, L. . Handbook of Interventional Radiologic Procedures. , 269-270 (2011).
- Hofmann, H., et al. Unresectable isolated hepatic metastases from solid pseudopapillary neoplasm of the pancreas: a case report of chemosaturation with high-dose melphalan. Pancreatology. 14 (6), 546-549 (2014).
- Miao, N., et al. Percutaneous hepatic perfusion in patients with metastatic liver cancer: anesthetic, hemodynamic, and metabolic considerations. Ann Surg Oncol. 15 (3), 815-823 (2008).
- Vogl, T. J., et al. Chemosaturation with percutaneous hepatic perfusions of melphalan for hepatic metastases: experience from two European centers. Rofo. 186 (10), 937-944 (2014).
- Pingpank, J. F., et al. A phase III random assignment trial comparing percutaneous hepatic perfusion with melphalan (PHP-mel) to standard of care for patients with hepatic metastases from metastatic ocular or cutaneous melanoma. J Clin Oncol. 28, 18s (2010).
- Rothbarth, J., Vahrmeijer, A. L., Mulder, G. J. Modulation of cytostatic efficacy of melphalan by glutathione: mechanisms and efficacy. Chem Biol Interact. 140 (2), 93-107 (2002).
- Bartlett, D. L., Libutti, S. K., Figg, W. D., Fraker, D. L., Alexander, H. R. Isolated hepatic perfusion for unresectable hepatic metastases from colorectal cancer. Surgery. 129 (2), 176-187 (2001).
- van Iersel, L. B., et al. Isolated hepatic perfusion with oxaliplatin combined with 100 mg melphalan in patients with metastases confined to the liver: A phase I study. Eur J Surg Oncol. , (2014).
- Rothbarth, J., Tollenaar, R. A., van de Velde, C. J. Recent trends and future perspectives in isolated hepatic perfusion in the treatment of liver tumors. Expert Rev Anticancer Ther. 6 (4), 553-565 (2006).
- van Etten, B., de Wilt, J. H., Brunstein, F., Eggermont, A. M., Verhoef, C. Isolated hypoxic hepatic perfusion with melphalan in patients with irresectable ocular melanoma metastases. Eur J Surg Oncol. 35 (5), 539-545 (2009).
- van Iersel, L. B., et al. Management of isolated nonresectable liver metastases in colorectal cancer patients: a case-control study of isolated hepatic perfusion with melphalan versus systemic chemotherapy. Ann Oncol. 21 (8), 1662-1667 (2010).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved