A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
التوليف واختبار دعم بت-سو الصلبة محلول جسيمات متناهية الصغر للجسيمات البروبان ديهيدروجيناتيون
In This Article
Summary
وهناك طريقة مريحة لتجميع 2 نانومتر المدعومة متعلق بنظام المعدنين جسيمات متناهية الصغر بت-سو محفزات لالهيدروجين البروبان وذكرت هنا. وتسمح تقنيات الأشعة السينية السنكروترون في الموقع بتحديد هيكل المحفز، الذي لا يمكن الحصول عليه عادة باستخدام أدوات المختبرات.
Abstract
وهناك طريقة مريحة لتجميع المحفزات ثنائية المعدن بت-سو محفزات واختبارات الأداء لهيدروجين البروبان وتوصيف وتظهر هنا. ويشكل المحفز بنية حل صلبة بديلة، مع حجم الجسيمات الصغيرة والموحدة حوالي 2 نانومتر. ويتحقق هذا عن طريق التحكم الدقيق في التشريب، والتكلس، وخطوات الحد خلال إعداد حافزا ويتم تحديدها من قبل تقنيات السنكروترون المتقدمة في الموقع . أداء محفز البروبان الهيدروجين يحسن باستمرار مع زيادة النحاس: بت النسبة الذرية.
Introduction
هيدروجين البروبان (بد) هو خطوة تجهيز رئيسية في إنتاج البروبيلين، والاستفادة من الغاز الصخري، المصدر الأسرع نموا للغاز في البلاد 1 . هذا التفاعل يكسر اثنين من السندات تش في جزيء البروبان لتشكيل واحد البروبيلين والهيدروجين الجزيئي. وتظهر المحفزات المعدنية النبيلة، بما في ذلك الجسيمات النانوية بد، انتقائية ضعيفة ل بد، وكسر السندات سيسي لإنتاج الميثان مع ارتفاع الغلة، مع ما يصاحب ذلك من إنتاج فحم الكوك، مما يؤدي إلى تعطيل حافز. وأظهرت التقارير الأخيرة أن محفزات بد انتقائية يمكن الحصول عليها عن طريق إضافة المروجين مثل الزنك أو في إلى بد 2 ، 3 ، 4 . وتكون المحفزات المشجعة قريبة من 100٪ انتقائية ل بد، بدلا من أقل من 50٪ للجسيمات النانوية بد من أحادية المعدن من نفس الحجم. ويعزى التحسن الكبير في الانتقائية إلى تشكيل بدن أو بدين بينتاليتيك المركب(إمك) على سطح المحفز. تم عزل الصفيف المطلوب من نوعين مختلفين من الذرات في المركبات الكيميائية الحيوية (إمك) هندسيا مواقع بد النشطة مع زن غير حفاز أو في ذرات، مما أدى إلى إيقاف التفاعلات الجانبية المحفزة من قبل مجموعة (مجموعة) المواقع النشطة النشطة بد.
البلاتين لديه أعلى الانتقائية الذاتية بين المعادن النبيلة لهيدروجين البروبان، ولكنها لا تزال غير مرضية للاستخدام التجاري 1 . عادة، يتم إضافة سن أو زن أو إن أو غا كمروج ل بت 5 و 6 و 7 و 8 و 9 و 10 و 11 و 12 و 13 . واستنادا إلى فكرة أن عزل الموقع النشط الهندسي يساهم في الانتقائية العالية، فإن أي عنصر غير حفاز يشكل سبيكة sهيكل مع حزب العمال، مثل النحاس، وينبغي أيضا يحتمل أن تعزز أداء حافزا 14 . وأشارت العديد من الدراسات السابقة إلى أن إضافة النحاس في الواقع تحسين الانتقائية بد من المحفزات بت 15 ، 16 ، 17 ، 18 . ومع ذلك، لم يتم الإبلاغ عن أي دليل مباشر لتحديد ما إذا كان حزب العمال والنحاس شكل نانوية متعلق بنظام المعدنين أو هياكل أمر، وهو أمر حاسم لفهم تأثير الترويجية من النحاس. في مخطط الطور الثنائي ل بت-سو، هناك نوعان مختلفان من الهيكل يكونان ممكنين على مدى تشكيلة واسعة 16 ، 18 : مركب بين المعدن، حيث يحتل كل من بت و سو كل مواقع بلورية محددة، و حل صلب، حيث يحل النحاس بشكل عشوائي في بت شعرية. وتشكل المواد الكيميائية المتطايرة المتوسطة عند درجة حرارة منخفضة وتحول إلى محلول صلب عند حوالي 600 - 800 درجة مئوية للمواد السائبة 14. قد تكون درجة حرارة التحول هذه أقل بالنسبة للجسيمات النانوية، بالقرب من درجة حرارة تفاعل بد ( أي 550 درجة مئوية). ولذلك، فمن الضروري للتحقيق في النظام الذري من بت-سو تحت ظروف التفاعل. بالنسبة للجسيمات النانوية المعتمدة مع أحجام الجسيمات الصغيرة، فمن الصعب جدا للحصول على معلومات هيكلية ذات مغزى باستخدام أدوات المختبرات 19 . ويؤدي التكرار المحدود لخلايا الوحدة إلى قمم انعراج واسعة جدا مع شدة منخفضة جدا. بسبب الجزء المرتفع من ذرات السطح في الجسيمات النانوية 1 - 3 نانومتر في الحجم، والتي تتأكسد في الهواء، يجب جمع الحيود في الموقع باستخدام الأشعة السينية عالية التدفق، وعادة ما تتوفر مع تقنيات السنكروترون.
وكانت محفزات بت-سو بد التي تم الإبلاغ عنها سابقا أكبر من 5 نانومتر في حجم 15 ، 16 ، 17 ، 18 - ومع ذلك، بالنسبة للمحفزات النانوية المعدنية النانوية، هناك دائما رغبة قوية لتحقيق أقصى قدر من النشاط الحفاز لكل وحدة التكلفة عن طريق توليف المحفزات مع تشتت عالية (عادة حوالي أو أقل من 2 نانومتر في الحجم) 19 . على الرغم من أن إعداد الجسيمات النانوية متعلق بنظام المعدنين من هذا الحجم هو ممكن من قبل طرق التشريب القياسية، والرقابة العقلانية على الإجراءات أمر ضروري. إن السلائف المعدنية، ودرجة الحموضة من محلول التشريب، ونوع الدعم تحتاج إلى التحكم في تحسين رسو الأنواع المعدنية على دعم مساحة سطح عالية. وينبغي أيضا أن تحلل العلاجات الحرارية التكليس والحد من لاحق بعناية لقمع نمو الجسيمات النانوية المعدنية.
هذا المقال يغطي بروتوكول لتوليف دعم 2 نانومتر بت-سو محفزات متعلق بنظام المعدنين جسيمات متناهية الصغر للالاختبار من أداء البروبان نزع الهيدروجين. يتم فحص هيكل المحفزات بواسطة المسح الضوئي T(ستيم)، في الموقع سينكروترون الأشعة السينية امتصاص الطيفي (زاس)، وفي الموقع الحيود السنكروترون الأشعة السينية (زرد)، والتي تساعد على توضيح تحسن أداء حافزا عند إدخال النحاس.
Protocol
1. توليف دعم 2 نانومتر بت-سو متعلق بنظام المعدنين محفزات جسيمات متناهية الصغر
- إعداد حل السلائف المعدنية
- حل 0.125 غرام من نترات النحاس ثلاثي الهيدرات (النحاس (نو 3 ) 2 · 3H 2 O) في 1 مل من الماء لتحقيق حل أزرق السماء.
تنبيه: استخدم قفازات واقية عند التعامل مع المواد الكيميائية. - إضافة الأمونيا قطرة إلى محلول نترات النحاس، وتشكيل راسبات زرقاء داكنة من هيدروكسيد النحاس.
الحذر: استخدام غطاء الدخان للتعامل مع القواعد والمواد الكيميائية المتطايرة. - الحفاظ على إضافة الأمونيا حتى تترسب راسبات زرقاء داكنة لتشكيل حل أزرق داكن ودرجة الحموضة> 10.
- إضافة 0.198 غرام من نترات تيتراامينبلاتينوم ((نه 3 ) 4 بت (نو 3 ) 2 ) إلى حل وماء إضافي بحيث الحجم الكلي للحل هو 3.5 مل. إضافة الأمونيا إضافية إذا لزم الأمر للحفاظ على درجة الحموضة من الحل أكبر من 10.
- تسخين الحل إلى 70 درجة مئوية حتى يتم حل جميع أملاح نترات تيتراامينبلاتينوم في الحل. السماح للحل بارد ل رت.
- حل 0.125 غرام من نترات النحاس ثلاثي الهيدرات (النحاس (نو 3 ) 2 · 3H 2 O) في 1 مل من الماء لتحقيق حل أزرق السماء.
- التشريب المشترك من محلول السلائف المعدنية
- قبل إعداد المحفز، وتحديد حجم المسام تشريب من دعم السيليكا. تزن بعناية حوالي 5 غرام من السيليكا الجافة في طبق الترجيح. في حين خلط، إضافة H 2 O قطرة حتى السيليكا هو الرطب تماما، ولكن مع عدم وجود حل الزائد. ريويغ السيليكا الرطب. تقسيم غرام من الماء المضافة بواسطة غرام من العينة لحساب حجم المسام.
- إضافة حل السلائف المعدن المذاب بضع قطرات في وقت إلى 5 غرام من السيليكا عالية المسامية (شافي 2 ) في طبق تبخير السيراميك ويقلب بلطف لتفريق الجسيمات التي تلتصق معا لتحقيق توزيع متجانس للحل.
ملاحظة: السيليكا الأبيض سوف تتحول الأزرق الداكن مرة واحدة أنه يمتص كل 3.5 مل من السلائف المعدنية سولوتيون.- تأكد من أن نسيج جزيئات السيليكا يبقى مثل الرمال الجافة. تجنب تراكم الحل الزائد أثناء التشريب.
- وضع المشربة بت-0.7Cu / سيو 2 حافزا السلائف في فرن التجفيف وتجفيفه في 125 درجة كو / N.
- التكليس والحد
- كالسين المحفز في فرن في 250 درجة مئوية مع معدل منحدر 5 درجة مئوية / دقيقة في الهواء لمدة 3 ساعات.
ملاحظة: الكلسين في درجات حرارة أعلى يؤدي عموما إلى أكبر بت نانوبارتيكلس. - وضع طبقة 2 سم من الصوف الكوارتز في منتصف مفاعل أنبوب الكوارتز 1 وتحميل المكلس بت-0.7Cu / سيو 2 حافزا في أنبوب من خلال قمع البلاستيك.ضع أنبوب في الفرن صدفي المبرمج درجة الحرارة.
- بعد تطهير الأنبوب مع N 2 لمدة 5 دقائق في رت، تبدأ في التدفق H 2 (في رت) في نفس معدل التدفق كما N 2 (100 سم مكعب) للحد من بت-0.7Cu /سيو 2 حافزا.
- زيادة درجة الحرارة إلى 150 درجة مئوية مع 5 درجة مئوية / دقيقة منحدر معدل وعقد لمدة 5 دقائق.
- بدء بطيئة تسلق درجة الحرارة بمعدل 2.5 درجة مئوية / دقيقة إلى 250 درجة مئوية. عقد درجة الحرارة لمدة 15 دقيقة في كل 25 درجة مئوية.
ملاحظة: قد تتطلب المعادن الأخرى درجات حرارة أقل أو أعلى من التخفيض. ويمكن تحديد درجة الحرارة بالضبط عموما من خلال فحص التغيرات اللون من المحفز (على سبيل المثال، من الأزرق إلى الأسود) ل بت-سو. - المنحدر إلى 550 درجة مئوية (أو درجة حرارة التفاعل، إذا كان أعلى) في 10 درجة مئوية / دقيقة والبقاء لمدة 30 دقيقة لاستكمال التخفيض. تطهير مع N 2 وباردة لدرجة حرارة الغرفة.
- تفريغ المحفزات بت-0.7Cu / SiO2 وتخزينها في قارورة للاستخدام في المستقبل.
ملاحظة: تكرار إجراءات تركيب مماثلة باستخدام كمية مختلفة من النحاس (NO 3) 2 · 3H 2 O و (NH 3) 4 حزب العمال (NO 3) 2 لإعداد أخرى PT-X نحاس / شافي 2
- كالسين المحفز في فرن في 250 درجة مئوية مع معدل منحدر 5 درجة مئوية / دقيقة في الهواء لمدة 3 ساعات.
2. البروبان-- نزع الهيدروجين اختبار الأداء
- تحميل المحفز
- اتخاذ 3/8 "مفاعل أنبوب الكوارتز ووضع طبقة 1 سم من الصوف الكوارتز ضد الدمل في الوسط.
الحذر: استخدام قفازات واقية عند التعامل مع الصوف الكوارتز، منذ الإبر الدقيقة يمكن الحصول على جزءا لا يتجزأ من الجلد. - تزن 40 ملغ من بت-0.7Cu / سيو 2 محفز و 960 ملغ من السيليكا للتخفيف. مزيج الجسيمات (1 جم الوزن الكلي) في قارورة فارغة.
- استخدام قمع البلاستيك لتحميل كل خليط محفز في أنبوب التفاعل. امسح الجدار الخارجي لكلا طرفي الأنبوب مع مناديل خالية من الوبر لإزالة أي تراب للحصول على ختم جيد مع الحلقة O.
- وضع تركيبات الأنابيب على طرفي أنبوب مفاعل الكوارتز وإرفاقها إلى نظام المفاعل مجهزة فرن صدفي.
<لي> اختبار التسرب والمحفز المعالجة المسبقة - اتخاذ 3/8 "مفاعل أنبوب الكوارتز ووضع طبقة 1 سم من الصوف الكوارتز ضد الدمل في الوسط.
- بدوره على 50 سم 3 / دقيقة N 2 تدفق من خلال مفاعل الأنبوب. بعد دقيقة واحدة، أغلق صمام الكرة على مخرج المفاعل. انتظر الضغط النظام لزيادة إلى 5 رطل لكل بوصة مربعة. إغلاق صمام الكرة على مدخل N 2 خط لوقف N 2 تدفق وختم نظام المفاعل.
- انتظر لمدة دقيقة واحدة وتسجيل الضغط قراءة من المقياس. إذا انخفض الضغط، افتح صمام الكرة على مخرج المفاعل للافراج عن الضغط وأعد تركيب التجهيزات. إذا لم يكن كذلك، فتح أولا صمام الكرة على مخرج المفاعل للافراج عن الضغط قبل إعادة تشغيل تدفق N 2 عن طريق تحويل صمام الكرة على مدخل خط N 2 لتطهير النظام لمدة 1 دقيقة.
- بدء تدفق 50 سم 3 / دقيقة من 5٪ H 2 / N 2 للحد من حافزا قبل تشغيل رد فعل ووقف تدفق N 2 . بدء تسخين الأنبوب إلى درجة حرارة التفاعل من 550 درجة مئوية، مع أرأكل من 10 درجة مئوية / دقيقة. انتظر لمدة 30 دقيقة بعد وصول الفرن إلى نقطة مجموعة والسماح لدرجة حرارة النظام لتحقيق الاستقرار في درجة الحرارة المستهدفة.
- البروبان نزع الهيدروجين اختبار التفاعل
- بدء جهاز كروماتوجراف الغاز (غ) في نظام المفاعل وتحديد الطريقة المناسبة لتحليل مكونات الغاز.
- تحويل تدفق غاز المفاعل إلى خط الالتفافية. تدفق 100 سم 3 / دقيقة من 5٪ البروبان / N 2 و 100 سم 3 / دقيقة من 5٪ H 2 / N 2 . انتظر لمدة 1 دقيقة بحيث يستقر تدفق البروبان وحقن تدفق الالتفافية في غ كعينة مرجعية.
- تبديل تدفق الغاز مرة أخرى إلى خط أنبوب المفاعل لبدء التفاعل وتسجيل الوقت.
- بعد تشغيل التفاعل لمدة 4 دقائق، ضخ مفاعل تدفق الغاز مخرج (عينة غ) في غ للحصول على معلومات مكون غاز منفذ. حقن عينات كل 4 دقائق وتشغيل الاختبار حتى يصل التحويل ستا ثابت تي أو التحويل منخفض جدا.
- استخدام المقابلة تحليل ذروة البرمجيات لتحليل كل ذروة.
- انقر لتحديد نقاط البداية والنهاية من الذروة. استخدام وظيفة دمج للحصول على منطقة الذروة. كتابة منطقة الذروة للبروبان (C 3 H 8 ) متفاعلة؛ البروبيلين (C 3 H 6 ) المنتج؛ والمنتجات الجانبية، والميثان (CH 4) والإيثان (C 2 H 4)، والإيثيلين (C 2 H 6).
ملاحظة: لكل حقنة، يتم الحصول على نمط غ مع قمم متعددة التي تتعلق مساحة لعدد من الشامات من أنواع الغاز المختلفة.
- انقر لتحديد نقاط البداية والنهاية من الذروة. استخدام وظيفة دمج للحصول على منطقة الذروة. كتابة منطقة الذروة للبروبان (C 3 H 8 ) متفاعلة؛ البروبيلين (C 3 H 6 ) المنتج؛ والمنتجات الجانبية، والميثان (CH 4) والإيثان (C 2 H 4)، والإيثيلين (C 2 H 6).
- تحويل منطقة الذروة إلى عدد من الشامات لكل الأنواع باستخدام عامل الاستجابة. تحديد تحويل البروبان والانتقائية البروبيلين في الوقت لكل عينة وفقا للصيغ التالية:
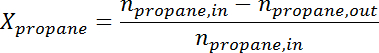
أد / 56040 / 56040eq2.jpg "/>
أين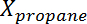 هو تحويل البروبان،
هو تحويل البروبان، 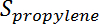 هو الانتقائية البروبيلين،
هو الانتقائية البروبيلين، 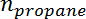 هو عدد الشامات من البروبان، و
هو عدد الشامات من البروبان، و 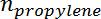 هو عدد الشامات من البروبيلين.
هو عدد الشامات من البروبيلين. - الحصول على قيمة التحويل والانتقائية الأولية عند t = 0 من خلال استقراء التحويل والانتقائية المقيسة مقابل الوقت على تيار باستخدام تناسب أسي.
- بدء جهاز كروماتوجراف الغاز (غ) في نظام المفاعل وتحديد الطريقة المناسبة لتحليل مكونات الغاز.
- بعد رد فعل
- وقف التدفئة المفاعل عن طريق إيقاف تشغيل برنامج درجة الحرارة. تبديل تدفق الغاز إلى 10 سم 3 / دقيقة N 2 .
- تبديل كروماتوغراف الغاز مرة أخرى إلى طريقة الاستعداد للحد من معدل تدفق الغاز الناقل.
- تفريغ المحفز المستخدم من مفاعل الإصلاح الكوارتز بعد التبريد إلىدرجة حرارة الغرفة. جمع وزن العامل الحفاز في منطقة معينة للتخلص من النفايات.
3. توصيف عينات محفز
- المسح الضوئي انتقال المجهر الإلكتروني 4 ، 20
- تحميل حافزا في هاون وطحنه في أقل من 100 شبكة مسحوق باستخدام مدقة.
- تفريق حوالي 30 ملغ من مسحوق حفاز إلى حوالي 5 مل من الكحول الآيزوبروبيل في قارورة صغيرة. يهز القارورة لخلط كامل ثم ترك القارورة الجلوس لمدة 5 دقائق للسماح لترسب الجزيئات الكبيرة نسبيا.
ملاحظة: يجب أن يحتوي التعليق المحصل على جزيئات صغيرة جدا من المحفزات المدعومة. - وضع الاتحاد الافريقي تيم الشبكة جاهزة على طبق تبخير. تسخين الطبق إلى 80 درجة مئوية على طبق ساخن. إضافة ثلاث قطرات من تعليق حافزا إلى الشبكة.
ملاحظة: سوف يتبخر آيزوبروبيل بسرعة وترك جزيئات محفز على ثه الشبكة. - تحميل الشبكة على حامل عينة للإلكترون المجهري عينة التصوير.
- في الموقع الأشعة السينية امتصاص الطيفي 3 ، 4 ، 19 ، 20
- تحميل المحفز في هاون وطحنه في أقل من 100 شبكة مسحوق باستخدام مدقة. تحميل مساحيق دقيقة في مجموعة يموت واضغط عليه مع الأصابع لتشكيل رقاقة ذاتية الدعم.
- تحميل عينة ~ 100 ملغ في صاحب العينة.
- وضع صاحب العينة في مفاعل أنبوب الكوارتز و بريترات العينة عن طريق الحد من ذلك في 50 سم 3 / دقيقة 3٪ H 2 / انه.
- بعد التبريد إلى رت، وختم الأنبوب ونقله إلى خط شعاعي السنكروترون لجمع البيانات زاس.
- في الحيود حيود الأشعة السينية 19 ، 20
- لوأد حافزا في هاون وطحنه إلى أقل من 100 شبكة مسحوق باستخدام مدقة.
- اضغط رقاقة رقيقة باستخدام معيار 7 مم قطرها يموت مجموعة.
ملاحظة: مجموعة يموت يحتوي على قطعة الإناث وأعلى وأسفل قطع الذكور.- إرفاق الجزء السفلي من الذكور إلى الجزء الإناث. تحميل العينة على سطح مصقول الجزء السفلي. إرفاق الجزء العلوي من الذكور ونقل مجموعة يموت إلى مرحلة عينة من الصحافة. اضغط مع القوة المناسبة.
- تفريغ الرقاقة ونقلها إلى كوب السيراميك من مرحلة العينة المتخصصة (انظر جدول المواد ). ختم المرحلة وإصلاحه على الجدول عينة على خط شعاع.
- تقليل العينة عن طريق التدفق و تسلق درجة الحرارة إلى 550 درجة مئوية. جمع بيانات الحيود الأشعة السينية في الموقع تحت 3٪ H 2 / انه تدفق الغاز عند 550 درجة مئوية وبعد التبريد إلى رت 20 .
النتائج
يتم عرض الانتقائية البروبيلين مقابل الوقت ل بت و بت-سو محفزات قياسها في تحويل البروبان الأولي من حوالي 20٪ في الشكل 1A . المحفز بت لديه انتقائية الأولية من 61٪، مما يزيد إلى حوالي 82٪ مع مرور الوقت على تيار كما حفز ينشط لمدة 1H. يظهر المحفز ...
Discussion
تحتوي المحفزات بت-سو التي تم تحضيرها في هذا العمل على جسيمات نانوية موحدة حول 2 نانومتر في الحجم، على غرار المحفزات غير المتجانسة المؤهلة للتطبيق الصناعي. وتشكل جميع السلائف بت والنحاس هياكل ثنائية المعدن، بدلا من الجسيمات أحادية المعدن المنفصلة. هذا التفاعل بين الم...
Disclosures
الكتاب ليس لديهم ما يكشف.
Acknowledgements
وأيد هذا العمل من قبل كلية الهندسة الكيميائية، جامعة بوردو. تم دعم استخدام مصدر الفوتون المتقدم من قبل وزارة الطاقة الأمريكية، مكتب علوم الطاقة الأساسية، بموجب عقد رقم. DE-AC02-06CH11357. وتدعم عمليات مركات، وخط أنابيب 10-بم من قبل وزارة الطاقة والمؤسسات الأعضاء في مركات. كما يعترف المؤلفون باستخدام الخط الحديدي 11-إد-C. نشكر إيفان فيجنر للمساعدة التجريبية مع زاس.
Materials
| Name | Company | Catalog Number | Comments |
| 1" quartz tube reactor | Quartz Scientific | Processed by glass blower | |
| drying oven | Fisher Scientific | ||
| calcination Furnace | Thermo Sciencfic | ||
| clam-shell temperature programmed furnace | Applied Test System | Custom made | |
| propane dehydorgenation performance evaluation system | Homemade | ||
| gas chromatography | Hewlett-Packard | Model 7890 | |
| TEM grid | TedPella | 01824G | |
| pellet press | International Crystal Lab | 0012-8211 | |
| die set | International Crystal Lab | 0012-189 | |
| Linkam Sample Stage | Linkam Scientific | Model TS1500 | |
| copper nitrate trihydrgate | Sigma Aldrich | 61197 | |
| tetraammineplatinum nitrate | Sigma Aldrich | 278726 | |
| ammonia | Sigma Aldrich | 294993 | |
| silica | Sigma Aldrich | 236802 | |
| isopropyl alcohol | Sigma Aldrich | ||
| balance | Denver Instrument Company | A-160 | |
| spatulas | VWR | ||
| ceramic and glass evaporating dishes, beakers | VWR | ||
| heating plate | |||
| kimwipe papers | |||
| mortar and pestle | |||
| quartz wool | |||
| Swagelok tube fittings |
References
- Sattler, J. J., Ruiz-Martinez, J., Santillan-Jimenez, E., Weckhuysen, B. M. Catalytic dehydrogenation of light alkanes on metals and metal oxides. Chem. Rev. 114 (20), 10613-10653 (2014).
- Childers, D. J., et al. Modifying structure-sensitive reactions by addition of Zn to Pd. J Catal. 318, 75-84 (2014).
- Gallagher, J. R., et al. Structural evolution of an intermetallic Pd-Zn catalyst selective for propane dehydrogenation. Phys. Chem. Chem. Phys. 17, 28144-28153 (2015).
- Wu, Z., et al. Pd-In intermetallic alloy nanoparticles: highly selective ethane dehydrogenation catalysts. Catal Sci Technol. 6 (18), 6965-6976 (2016).
- Siddiqi, G., Sun, P., Galvita, V., Bell, A. T. Catalyst performance of novel Pt/Mg (Ga)(Al) O catalysts for alkane dehydrogenation. J Catal. 274 (2), 200-206 (2010).
- Passos, F. B., Aranda, D. A., Schmal, M. Characterization and catalytic activity of bimetallic Pt-In/Al 2 O 3 and Pt-Sn/Al 2 O 3 catalysts. J Catal. 178 (2), 478-488 (1998).
- Virnovskaia, A., Morandi, S., Rytter, E., Ghiotti, G., Olsbye, U. Characterization of Pt, Sn/Mg (Al) O catalysts for light alkane dehydrogenation by FT-IR spectroscopy and catalytic measurements. J Phys Chem C. 111 (40), 14732-14742 (2007).
- Jablonski, E., Castro, A., Scelza, O., De Miguel, S. Effect of Ga addition to Pt/Al 2 O 3 on the activity, selectivity and deactivation in the propane dehydrogenation. Appl Catal A. 183 (1), 189-198 (1999).
- Galvita, V., Siddiqi, G., Sun, P., Bell, A. T. Ethane dehydrogenation on Pt/Mg (Al) O and PtSn/Mg (Al) O catalysts. J Catal. 271 (2), 209-219 (2010).
- Shen, J., Hill, J. M., Watwe, R. M., Spiewak, B. E., Dumesic, J. A. Microcalorimetric, infrared spectroscopic, and DFT studies of ethylene adsorption on Pt/SiO2 and Pt-Sn/SiO2 catalysts. J Phys Chem B. 103 (19), 3923-3934 (1999).
- Silvestre-Albero, J., et al. Microcalorimetric, reaction kinetics and DFT studies of Pt–Zn/X-zeolite for isobutane dehydrogenation. Catal Lett. 74 (1-2), 17-25 (2001).
- Sun, P., Siddiqi, G., Vining, W. C., Chi, M., Bell, A. T. Novel Pt/Mg (In)(Al) O catalysts for ethane and propane dehydrogenation. J Catal. 282 (1), 165-174 (2011).
- Sun, P., Siddiqi, G., Chi, M., Bell, A. T. Synthesis and characterization of a new catalyst Pt/Mg (Ga)(Al) O for alkane dehydrogenation. J Catal. 274 (2), 192-199 (2010).
- Okamoto, H. . Phase diagrams for binary alloys. Desk handbook. , (2000).
- Hamid, S. B. D. -. A., Lambert, D., Derouane, E. G. Dehydroisomerisation of n-butane over (Pt, Cu)/H-TON catalysts. Catal Today. 63 (2), 237-247 (2000).
- Veldurthi, S., Shin, C. -. H., Joo, O. -. S., Jung, K. -. D. Promotional effects of Cu on Pt/Al 2 O 3 and Pd/Al 2 O 3 catalysts during n-butane dehydrogenation. Catal Today. 185 (1), 88-93 (2012).
- Han, Z., et al. Propane dehydrogenation over Pt-Cu bimetallic catalysts: the nature of coke deposition and the role of copper. Nanoscale. 6 (17), 10000-10008 (2014).
- Komatsu, T., Tamura, A. Pt 3 Co and PtCu intermetallic compounds: promising catalysts for preferential oxidation of CO in excess hydrogen. J Catal. 258 (2), 306-314 (2008).
- Gallagher, J. R., et al. In situ diffraction of highly dispersed supported platinum nanoparticles. Catal Sci Technol. 4 (9), 3053-3063 (2014).
- Ma, Z., Wu, Z., Miller, J. T. Effect of Cu content on the bimetallic Pt-Cu catalysts for propane dehydrogenation. Catal Struct React. 3 (1-2), 43-53 (2017).
- Richards, R. . Surface and nanomolecular catalysis. , (2006).
- Jiao, L., Regalbuto, J. R. The synthesis of highly dispersed noble and base metals on silica via strong electrostatic adsorption: I. Amorphous silica. J Catal. 260 (2), 329-341 (2008).
- Miller, J. T., Schreier, M., Kropf, A. J., Regalbuto, J. R. A fundamental study of platinum tetraammine impregnation of silica: 2. The effect of method of preparation, loading, and calcination temperature on (reduced) particle size. J Catal. 225 (1), 203-212 (2004).
- Wei, H., et al. Selective hydrogenation of acrolein on supported silver catalysts: A kinetics study of particle size effects. J Catal. 298, 18-26 (2013).
- Ertl, G., Knözinger, H., Schüth, F., Weitkamp, J. . Handbook of heterogeneous catalysis: 8 volumes. , (2008).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved