Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Синтез и испытание поддерживаемых твердых растворов Pt-Cu Наночастицы для дегидрирования пропана
В этой статье
Резюме
Сообщается об удобном методе синтеза катализаторов Pt-Cu на основе биметаллических наночастиц для дегидрирования пропана. Синтетронные рентгеновские методы in situ позволяют определять структуру катализатора, которая обычно недоступна с использованием лабораторных приборов.
Аннотация
Здесь продемонстрирован удобный метод синтеза биметаллических катализаторов Pt-Cu и эксплуатационные испытания дегидрирования и характеризации пропана. Катализатор образует структуру твердого раствора замещения с небольшим и однородным размером частиц около 2 нм. Это достигается путем тщательного контроля за стадиями пропитки, прокаливания и восстановления при подготовке катализатора и идентифицируется передовыми методами синхротронной in situ . Производительность катализатора дегидрирования катализатора непрерывно улучшается с увеличением атомного отношения Cu: Pt.
Введение
Дегидрирование пропана (PDH) является ключевым этапом обработки в производстве пропилена, используя сланцевый газ, самый быстрорастущий источник газа в стране 1 . Эта реакция разрушает две связи СН в молекуле пропана с образованием одного пропилена и молекулярного водорода. Благородные металлические катализаторы, включая наночастицы Pd, демонстрируют слабую селективность для PDH, разрушая связь CC с получением метана с высоким выходом, при одновременном производстве кокса, что приводит к дезактивации катализатора. Недавние сообщения показали, что селективные катализаторы PDH могут быть получены добавлением промоторов, таких как Zn или In, к Pd 2 , 3 , 4 . Промодированные катализаторы почти 100% селективны к PDH, а не менее 50% для монометаллических наночастиц Pd одинакового размера. Большое улучшение селективности объяснялось образованием интерметаллического соединения PdZn или PdIn(IMC) на поверхности катализатора. Упорядоченный массив двух разных типов атомов в ИМЦ геометрически изолировал активные сайты Pd с некаталитическими атомами Zn или In, которые отключили побочные реакции, катализируемые ансамблем (группой) соседних активных центров Pd.
Платина обладает самой высокой собственной селективностью среди благородных металлов для дегидрирования пропана, но она все еще не является удовлетворительной для коммерческого использования 1 . Как правило, Sn, Zn, In или Ga добавляют в качестве промотора для Pt 5 , 6 , 7 , 8 , 9 , 10 , 11 , 12 , 13 . Основываясь на идее, что изоляция геометрического активного сайта способствует высокой селективности, любой некаталитический элемент, образующий сплав sСтруктура с Pt, такая как Cu, также должна потенциально способствовать повышению эффективности катализатора 14 . В нескольких предыдущих исследованиях было показано, что добавление Cu действительно улучшает селективность PDH для Pt-катализаторов 15 , 16 , 17 , 18 . Тем не менее, никаких прямых доказательств не было установлено, чтобы определить, образуют ли Pt и Cu биметаллические наночастицы или упорядоченные структуры, что имеет решающее значение для понимания стимулирующего эффекта Cu. В бинарной фазовой диаграмме Pt-Cu возможны два разных типа структуры в широком диапазоне составов 16 , 18 : интерметаллическое соединение, в котором Pt и Cu каждый занимают определенные участки кристалла и твердый раствор, в котором Cu случайно замещает в Pt-решетка. IMC формируются при низкой температуре и превращаются в твердый раствор при температуре около 600-800 ° C для сыпучих материалов 14. Эта температура превращения может быть ниже для наночастиц, вблизи температуры реакции PDH ( т.е. 550 ° C). Поэтому в экспериментальных условиях необходимо исследовать атомный порядок Pt-Cu. Для поддерживаемых наночастиц с малыми размерами частиц очень сложно получить значимую структурную информацию с использованием лабораторных приборов 19 . Ограниченное повторение элементарных ячеек приводит к очень широким дифракционным пикам с очень малой интенсивностью. Из-за высокой доли поверхностных атомов в наночастицах размером 1 - 3 нм, которые окисляются на воздухе, дифракция должна собираться in situ с использованием рентгеновского излучения с высоким потоком, как правило, с синхротронными методами.
Ранее сообщаемые катализаторы Pt-Cu PDH были размером больше 5 нм размером 15 , 16 , 17 , 18. Однако для катализаторов наночастиц благородного металла всегда существует сильное желание максимизировать каталитическую активность на единицу стоимости за счет синтеза катализаторов с высокими дисперсиями (обычно около или менее 2 нм) 19 . Хотя получение биметаллических наночастиц такого размера возможно с помощью стандартных методов пропитки, необходим рациональный контроль за процедурами. Предшественники металла, рН пропитывающего раствора и тип носителя необходимо контролировать, чтобы оптимизировать анкеры на металлических видах на опорах с высокой площадью поверхности. Последующую термическую обработку кальцинирования и восстановления следует также тщательно контролировать для подавления роста металлических наночастиц.
Эта статья посвящена протоколу синтеза поддерживаемых 2 нм Pt-Cu биметаллических наночастиц катализаторов и для тестирования их дегидрирования пропана. Структура катализаторов исследуется с помощью сканирования Transmission электронной микроскопии (STEM), Situ синхротронного рентгеновского абсорбционной спектроскопии в (РАС), а также на месте синхротронное дифракции рентгеновских лучей (ДРЛ), которые помогают пролить свет на улучшение эксплуатационных характеристик катализатора при введении Cu.
протокол
1. Синтез поддерживаемых 2 нм Pt-Cu биметаллических катализаторов наночастиц
- Получение раствора предшественника металла
- Растворить 0,125 г тригидрата нитрата меди (Cu (NO 3 ) 2 · 3H 2 O) в 1 мл воды для достижения голубого раствора.
Внимание! При обращении с химикатами используйте защитные перчатки. - Добавьте аммиак по каплям к раствору нитрата меди, образуя синие осадки гидроксида меди.
Внимание: используйте вытяжной шкаф для обработки оснований и летучих химических веществ. - Продолжайте добавлять аммиак до тех пор, пока синие осадки не растворятся, чтобы образовать темно-синий раствор и рН> 10.
- Добавьте 0,198 г тетрааминоплатина нитрата ((NH 3 ) 4 Pt (NO 3 ) 2 ) в раствор и дополнительную воду, чтобы общий объем раствора составлял 3,5 мл. При необходимости добавьте дополнительный аммиак, чтобы поддерживать рН раствора более 10.
- Нагреть раствор до 70 ° С до тех пор, пока все соли нитрата тетраамминовой платины не растворятся в растворе. Дайте раствору охладиться до комнатной температуры.
- Растворить 0,125 г тригидрата нитрата меди (Cu (NO 3 ) 2 · 3H 2 O) в 1 мл воды для достижения голубого раствора.
- Совместная пропитка раствора предшественника металла
- Перед приготовлением катализатора определите объем пропитывающей пор оксида кремния. Осторожно взвесьте приблизительно 5 г сухого кремнезема в весовую тарелку. При перемешивании добавьте H 2 O по каплям до тех пор, пока кремнезем не станет полностью влажным, но без избыточного раствора. Возьмите влажный кремнезем. Разделите граммы добавленной воды на граммы образца, чтобы рассчитать объем пор.
- Добавьте раствор растворенного раствора металла в несколько капель одновременно до 5 г высокопористого диоксида кремния (SiO 2 ) в керамической испарительной чашке и осторожно перемешайте, чтобы разбить частицы, которые склеиваются вместе для достижения гомогенного распределения раствора.
ПРИМЕЧАНИЕ. Белый диоксид кремния станет темно-синим, если он адсорбирует все 3,5 мл раствора предшественника металлап.- Убедитесь, что текстура частиц двуокиси кремния остается такой же, как у сухого песка. Избегайте накопления избыточного раствора во время пропитки.
- Поместите пропитанный предшественник катализатора Pt-0,7Cu / SiO 2 в сушильную печь и высушите его при 125 ° СО / N.
- Кальцинирование и сокращение
- Кальцинируйте катализатор в печи при 250 ° С со скоростью 5 ° С / мин на воздухе в течение 3 часов.
ПРИМЕЧАНИЕ. Кальцинирование при более высоких температурах обычно приводит к увеличению наночастиц Pt. - Поместите 2-сантиметровый слой кварцевой шерсти в середине 1-дюймового кварцевого трубчатого реактора и загрузите прокаленный катализатор Pt-0,7Cu / SiO 2 в трубку через пластиковую воронку. Поместите трубку в печь с температурным режимом раскладушки.
- После продувки трубки с N 2 в течение 5 минут при комнатной температуре начните поток H 2 (при комнатной температуре) при той же скорости потока, что и N 2 (100 см 3), чтобы уменьшить Pt-0,7Cu /SiO 2 .
- Увеличьте температуру до 150 ° C со скоростью 5 ° C / мин и удерживайте ее в течение 5 минут.
- Начните медленное скачкообразное изменение температуры со скоростью 2,5 ° C / мин до 250 ° C. Удерживайте температуру в течение 15 минут при каждых 25 ° C.
ПРИМЕЧАНИЕ. Другим металлам может потребоваться более низкая или более низкая температура восстановления. Точную температуру можно, как правило, определить, исследуя изменения цвета катализатора ( например, от синего до черного) для Pt-Cu. - Рампа до 550 ° C (или температура реакции, если выше) при 10 ° C / мин и пребывание в течение 30 минут для завершения восстановления. Продуйте N 2 и охладите до комнатной температуры.
- Выгрузите катализаторы Pt-0,7Cu / SiO2 и храните во флаконе для будущего использования.
ПРИМЕЧАНИЕ. Повторите аналогичные процедуры синтеза с использованием различного количества Cu (NO 3 ) 2 · 3H 2 O и (NH 3 ) 4 Pt (NO 3 ) 2 для получения другого Pt-X Cu / SiO 2 (X = 0,7, 2,3 и 7,3 и обозначает атомные отношения Cu: Pt) и катализаторы Pt / SiO2.
- Кальцинируйте катализатор в печи при 250 ° С со скоростью 5 ° С / мин на воздухе в течение 3 часов.
2. Испытание на прогиб-дегидрирование
- Загрузка катализатора
- Возьмите 3/8 "кварцевый трубчатый реактор и поместите 1 см слой кварцевой шерсти против углубления посередине.
Внимание! При работе с кварцевой шерстью используйте защитные перчатки, так как тонкие иглы могут попасть в кожу. - Взвешивают 40 мг катализатора Pt-0,7Cu / SiO 2 и 960 мг диоксида кремния для разбавления. Смешайте частицы (общий вес 1 г) в пустой флаконе.
- Используйте пластиковую воронку для загрузки всей каталитической смеси в реакционную трубку. Протрите наружную стенку обоих концов труб без ворса, чтобы удалить грязь, чтобы получить хорошее уплотнение с уплотнительным кольцом.
- Поместите трубчатые фитинги на оба конца трубки кварцевого реактора и присоедините их к реакторной системе, оборудованной раскладушкой.
- Возьмите 3/8 "кварцевый трубчатый реактор и поместите 1 см слой кварцевой шерсти против углубления посередине.
- Испытание на герметичность и предварительная обработка катализатора
- Включите 50 см 3 / мин N 2, проходя через трубчатый реактор. Через 1 мин закройте шаровой клапан на выходе из реактора. Подождите, пока давление в системе увеличится до 5 фунтов на квадратный дюйм. Закройте шаровой клапан на входе N 2, чтобы остановить поток N 2 и закройте реакторную систему.
- Подождите 1 мин и запишите давление, считываемое с датчика. Если давление падает, откройте шаровой клапан на выходе из реактора, чтобы снять давление и снова присоединить фитинги. Если нет, сначала откройте шаровой клапан на выходе из реактора, чтобы высвободить давление до перезапуска потока N 2 , включив шаровой клапан на впускной линии N 2 для продувки системы в течение 1 мин.
- Начинайте поток 50 см 3 / мин 5% H 2 / N 2 для восстановления катализатора перед проведением реакции и остановите поток N 2 . Начните нагрев трубки до температуры реакции 550 ° С, при этомСо скоростью 10 ° С / мин. Подождите 30 минут после того, как печь достигнет заданного значения и дайте температуре системы стабилизироваться при заданной температуре.
- Испытание реакции дегидрирования пропана
- Запустите газовый хроматограф (ГХ) в реакторной системе и выберите подходящий метод анализа газовых компонентов.
- Переключите поток реакторного газа в обводную линию. Поток 100 см 3 / мин 5% пропана / N 2 и 100 см 3 / мин 5% H 2 / N 2 . Подождите 1 мин, чтобы поток пропана стабилизировался и вводил байпасный поток в GC в качестве эталонного образца.
- Переключите поток газа обратно в трубку реактора, чтобы начать реакцию и записать время.
- После того, как реакция протекает в течение 4 мин, введите поток газа в реактор (образец GC) в GC, чтобы получить информацию о компоненте выходного газа. Внесите образцы каждые 4 мин и выполните тест до тех пор, пока конверсия не достигнет устойчивого значения Te или конверсия очень низкая.
- Используйте соответствующее программное обеспечение для анализа пиков для анализа каждого пика.
- Нажмите, чтобы выбрать начальную и конечную точки пика. Используйте функцию интеграции, чтобы получить область пика. Запишите площадь пика для пропана (C 3 H 8 ) реагента; Продукт пропилена (C 3 H 6 ); И побочные продукты, метан (CH 4 ), этан (C 2 H 4 ) и этилен (C 2 H 6 ).
ПРИМЕЧАНИЕ. Для каждой инъекции получается GC-образец с несколькими пиками, площадь которого относится к числу молей различных видов газа.
- Нажмите, чтобы выбрать начальную и конечную точки пика. Используйте функцию интеграции, чтобы получить область пика. Запишите площадь пика для пропана (C 3 H 8 ) реагента; Продукт пропилена (C 3 H 6 ); И побочные продукты, метан (CH 4 ), этан (C 2 H 4 ) и этилен (C 2 H 6 ).
- Преобразуйте площадь пика в число молей для каждого вида с использованием коэффициента отклика. Определите конверсию пропана и селективность пропилена в то время для каждого образца в соответствии со следующими формулами:
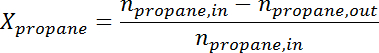
Ad / 56040 / 56040eq2.jpg "/>
где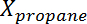 Представляет собой превращение пропана,
Представляет собой превращение пропана, 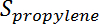 Является селективность пропилена,
Является селективность пропилена, 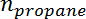 - число молей пропана и
- число молей пропана и 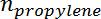 - количество молей пропилена.
- количество молей пропилена. - Получите начальное значение преобразования и селективности при t = 0, экстраполируя измеренное преобразование и селективность в зависимости от времени в потоке, используя экспоненциальное соответствие.
- Запустите газовый хроматограф (ГХ) в реакторной системе и выберите подходящий метод анализа газовых компонентов.
- После реакции
- Остановите нагрев реактора, выключив программу температуры. Переключите поток газа на 10 см 3 / мин N 2 .
- Переключите газовый хроматограф обратно в режим ожидания, чтобы уменьшить расход газа-носителя.
- Выгрузите использованный катализатор из реактора с фиксированным слоем кварца после охлаждения докомнатная температура. Соберите вес катализатора в обозначенной зоне утилизации отходов.
3. Характеристика образцов катализатора
- Сканирующая трансмиссия Электронная микроскопия 4 , 20
- Загрузите катализатор в ступке и измельчите его до порошка менее 100 меш, используя пестик.
- Диспергируют около 30 мг порошка катализатора в примерно 5 мл изопропилового спирта в небольшом флаконе. Встряхните флакон для полного смешивания, а затем дайте флакон сидеть в течение 5 минут, чтобы обеспечить осаждение относительно больших частиц.
ПРИМЕЧАНИЕ. Полученная суспензия должна содержать очень мелкие частицы нанесенных катализаторов. - Поместите готовую сетку Au TEM на испаряющееся блюдо. Нагрейте блюдо до 80 ° C на горячей плите. Добавьте три капли суспензии катализатора в сетку.
ПРИМЕЧАНИЕ. Изопропиловый спирт быстро испарится и оставит частицы катализатора наСетка. - Загрузите сетку на держатель образца для получения изображений электронной микроскопии.
- In-situ рентгеновская абсорбционная спектроскопия 3 , 4 , 19 , 20
- Загрузите катализатор в раствор и измельчите его до порошка менее 100 меш, используя пестик. Загрузите тонкие порошки в матрицу и нажмите пальцами, чтобы сформировать самонесущую пластину.
- Загрузите образец образца 100 мг в держатель образца.
- Поместите держатель образца в кварцевый трубчатый реактор и предварительно обработайте образец, уменьшив его в 50 см 3 / мин 3% H 2 / He.
- После охлаждения до RT герметизируйте трубку и перенесите ее на синхротронную лучевую линию для сбора данных XAS.
- In-situ дифракция рентгеновских лучей 19 , 20
- вотAd катализатор в ступке и измельчить его в порошок менее 100 меш, используя пестик.
- Надавите тонкую пластину, используя стандартную матрицу диаметром 7 мм.
ПРИМЕЧАНИЕ. Набор штампов содержит кусочек женской и верхней и нижней частей.- Прикрепите нижнюю охватываемую деталь к охватывающей части. Загрузите образец на полированную поверхность нижней части. Прикрепите верхнюю охватываемую деталь и перенесите штамп на ступень образца пресса. Пресс с соответствующей прочностью.
- Выгрузите пластину и перенесите ее в керамическую чашку специализированного образца (см. Таблицу материалов ). Закрепите сцену и зафиксируйте ее на таблице образцов на линии луча.
- Уменьшите образец, протекая и опустив температуру до 550 ° C. Соберите данные рентгеновской дифракции in situ при потоке газа 3% H 2 / He при 550 ° C и после охлаждения до RT 20 .
Результаты
Селективность пропилена в зависимости от времени для катализаторов Pt и Pt-Cu, измеренная при начальной конверсии пропана около 20%, представлена на фиг. 1А . Pt-катализатор имеет начальную селективность 61%, что приводит к увеличению до 82% с течением време?...
Обсуждение
Катализаторы Pt-Cu, полученные в этой работе, содержат однородные наночастицы размером около 2 нм, аналогичные гетерогенным катализаторам, пригодным для промышленного применения. Все предшественники Pt и Cu образуют биметаллические структуры, в отличие от отдельных монометаллических час...
Раскрытие информации
Авторам нечего раскрывать.
Благодарности
Эта работа была поддержана Школой химической инженерии Университета Пердью. Использование расширенного источника фотонов было поддержано Министерством энергетики США, Управлением основных энергетических наук, по контракту №. DE-AC02-06CH11357. Операции MRCAT, пучок 10-BM поддерживаются Департаментом энергетики и учреждениями-членами MRCAT. Авторы также признают использование пучка 11-ID-C. Мы благодарим Эвана Вегенера за экспериментальную помощь с XAS.
Материалы
| Name | Company | Catalog Number | Comments |
| 1" quartz tube reactor | Quartz Scientific | Processed by glass blower | |
| drying oven | Fisher Scientific | ||
| calcination Furnace | Thermo Sciencfic | ||
| clam-shell temperature programmed furnace | Applied Test System | Custom made | |
| propane dehydorgenation performance evaluation system | Homemade | ||
| gas chromatography | Hewlett-Packard | Model 7890 | |
| TEM grid | TedPella | 01824G | |
| pellet press | International Crystal Lab | 0012-8211 | |
| die set | International Crystal Lab | 0012-189 | |
| Linkam Sample Stage | Linkam Scientific | Model TS1500 | |
| copper nitrate trihydrgate | Sigma Aldrich | 61197 | |
| tetraammineplatinum nitrate | Sigma Aldrich | 278726 | |
| ammonia | Sigma Aldrich | 294993 | |
| silica | Sigma Aldrich | 236802 | |
| isopropyl alcohol | Sigma Aldrich | ||
| balance | Denver Instrument Company | A-160 | |
| spatulas | VWR | ||
| ceramic and glass evaporating dishes, beakers | VWR | ||
| heating plate | |||
| kimwipe papers | |||
| mortar and pestle | |||
| quartz wool | |||
| Swagelok tube fittings |
Ссылки
- Sattler, J. J., Ruiz-Martinez, J., Santillan-Jimenez, E., Weckhuysen, B. M. Catalytic dehydrogenation of light alkanes on metals and metal oxides. Chem. Rev. 114 (20), 10613-10653 (2014).
- Childers, D. J., et al. Modifying structure-sensitive reactions by addition of Zn to Pd. J Catal. 318, 75-84 (2014).
- Gallagher, J. R., et al. Structural evolution of an intermetallic Pd-Zn catalyst selective for propane dehydrogenation. Phys. Chem. Chem. Phys. 17, 28144-28153 (2015).
- Wu, Z., et al. Pd-In intermetallic alloy nanoparticles: highly selective ethane dehydrogenation catalysts. Catal Sci Technol. 6 (18), 6965-6976 (2016).
- Siddiqi, G., Sun, P., Galvita, V., Bell, A. T. Catalyst performance of novel Pt/Mg (Ga)(Al) O catalysts for alkane dehydrogenation. J Catal. 274 (2), 200-206 (2010).
- Passos, F. B., Aranda, D. A., Schmal, M. Characterization and catalytic activity of bimetallic Pt-In/Al 2 O 3 and Pt-Sn/Al 2 O 3 catalysts. J Catal. 178 (2), 478-488 (1998).
- Virnovskaia, A., Morandi, S., Rytter, E., Ghiotti, G., Olsbye, U. Characterization of Pt, Sn/Mg (Al) O catalysts for light alkane dehydrogenation by FT-IR spectroscopy and catalytic measurements. J Phys Chem C. 111 (40), 14732-14742 (2007).
- Jablonski, E., Castro, A., Scelza, O., De Miguel, S. Effect of Ga addition to Pt/Al 2 O 3 on the activity, selectivity and deactivation in the propane dehydrogenation. Appl Catal A. 183 (1), 189-198 (1999).
- Galvita, V., Siddiqi, G., Sun, P., Bell, A. T. Ethane dehydrogenation on Pt/Mg (Al) O and PtSn/Mg (Al) O catalysts. J Catal. 271 (2), 209-219 (2010).
- Shen, J., Hill, J. M., Watwe, R. M., Spiewak, B. E., Dumesic, J. A. Microcalorimetric, infrared spectroscopic, and DFT studies of ethylene adsorption on Pt/SiO2 and Pt-Sn/SiO2 catalysts. J Phys Chem B. 103 (19), 3923-3934 (1999).
- Silvestre-Albero, J., et al. Microcalorimetric, reaction kinetics and DFT studies of Pt–Zn/X-zeolite for isobutane dehydrogenation. Catal Lett. 74 (1-2), 17-25 (2001).
- Sun, P., Siddiqi, G., Vining, W. C., Chi, M., Bell, A. T. Novel Pt/Mg (In)(Al) O catalysts for ethane and propane dehydrogenation. J Catal. 282 (1), 165-174 (2011).
- Sun, P., Siddiqi, G., Chi, M., Bell, A. T. Synthesis and characterization of a new catalyst Pt/Mg (Ga)(Al) O for alkane dehydrogenation. J Catal. 274 (2), 192-199 (2010).
- Okamoto, H. . Phase diagrams for binary alloys. Desk handbook. , (2000).
- Hamid, S. B. D. -. A., Lambert, D., Derouane, E. G. Dehydroisomerisation of n-butane over (Pt, Cu)/H-TON catalysts. Catal Today. 63 (2), 237-247 (2000).
- Veldurthi, S., Shin, C. -. H., Joo, O. -. S., Jung, K. -. D. Promotional effects of Cu on Pt/Al 2 O 3 and Pd/Al 2 O 3 catalysts during n-butane dehydrogenation. Catal Today. 185 (1), 88-93 (2012).
- Han, Z., et al. Propane dehydrogenation over Pt-Cu bimetallic catalysts: the nature of coke deposition and the role of copper. Nanoscale. 6 (17), 10000-10008 (2014).
- Komatsu, T., Tamura, A. Pt 3 Co and PtCu intermetallic compounds: promising catalysts for preferential oxidation of CO in excess hydrogen. J Catal. 258 (2), 306-314 (2008).
- Gallagher, J. R., et al. In situ diffraction of highly dispersed supported platinum nanoparticles. Catal Sci Technol. 4 (9), 3053-3063 (2014).
- Ma, Z., Wu, Z., Miller, J. T. Effect of Cu content on the bimetallic Pt-Cu catalysts for propane dehydrogenation. Catal Struct React. 3 (1-2), 43-53 (2017).
- Richards, R. . Surface and nanomolecular catalysis. , (2006).
- Jiao, L., Regalbuto, J. R. The synthesis of highly dispersed noble and base metals on silica via strong electrostatic adsorption: I. Amorphous silica. J Catal. 260 (2), 329-341 (2008).
- Miller, J. T., Schreier, M., Kropf, A. J., Regalbuto, J. R. A fundamental study of platinum tetraammine impregnation of silica: 2. The effect of method of preparation, loading, and calcination temperature on (reduced) particle size. J Catal. 225 (1), 203-212 (2004).
- Wei, H., et al. Selective hydrogenation of acrolein on supported silver catalysts: A kinetics study of particle size effects. J Catal. 298, 18-26 (2013).
- Ertl, G., Knözinger, H., Schüth, F., Weitkamp, J. . Handbook of heterogeneous catalysis: 8 volumes. , (2008).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены