Method Article
توليد أورام البنكرياس التقويمية وتوصيف الجسم السابق للخلايا التي تتسلل إلى الخلايا T
In This Article
Summary
يصف هذا البروتوكول الجيل الجراحي لأورام البنكرياس التقويمية والهضم السريع لأورام البنكرياس المعزولة الطازجة. بعد الهضم ، يمكن استخدام الخلايا المناعية القابلة للاستمرار لمزيد من التحليل المصب ، بما في ذلك تحفيز الجسم الحيوي السابق للخلايا التائية للكشف عن الخلايا الخلوية عن طريق قياس التدفق.
Abstract
في نماذج الجسم الحيوي لسرطان البنكرياس توفير أدوات لا تقدر بثمن لدراسة ديناميات المرض, تسلل المناعي والاستراتيجيات العلاجية الجديدة. ويمكن اجراء نموذج المريدين العظام علي الأفواج الكبيرة من الفئران المناعية في وقت واحد ، غير مكلفه نسبيا ويحافظ علي البيئة المجهرية الانسجه المتشابهة. ويوفر القياس الكمي لتسلل الخلايا التائية والنشاط السام للخلايا داخل الأورام التقويمية مؤشرا مفيدا للاستجابة المضادة للفم.
يصف هذا البروتوكول منهجيه التوليد الجراحي لأورام البنكرياس التقويمية عن طريق حقن عدد قليل من الخلايا السرطانية المتزامنة التي أعيد تعليقها في غشاء الطابق السفلي 5 μL في البنكرياس مباشره. تاخذ الفئران التي تحمل الأورام التقويمية حوالي 30 يوما للوصول إلى نقطه النهاية ، وعندها يمكن حصاد الأورام ومعالجتها لتوصيف نشاط خلايا T التي تتسلل إلى الورم. الهضم الانزيمي السريع باستخدام كولاجيناز و DNase يسمح للتعليق خليه واحده ليتم استخراجها من الأورام. يتم الحفاظ علي مقومات البقاء وسطح الخلية من الخلايا المناعية المستخرجة من الورم. ولذلك ، فانه من المناسب للتطبيقات المتلقية للمعلومات متعددة ، بما في ذلك الفرز خليه بمساعده التدفق من الخلايا المناعية للثقافة أو استخراج RNA ، تحليل تدفق الخلوي لسكان الخلايا المناعية. هنا ، ونحن وصف التحفيز الجسم السابق من السكان الخلية T للقياس الكمي خلوية داخل الخلايا (Ifnγ و TNFα) والنشاط التحبيب (CD107a) كمقياس للخلايا الكلية. وقد تم تحفيز الأورام الكاملة بالورم مع خلات ميريستات الفطرية و ionomycin لمده 5 ساعات ، في وجود الأجسام المضادة لCD107a من أجل إنتاج اوبريجوليت السايسيسين والتحبيب. تم اجراء أضافه brefeldin A و مونينسين لنهائي 4 ح لمنع النقل خارج الخلية وتعظيم الكشف السايسيسين. ثم تم اجراء تلطيخ خارج وداخل الخلوية من الخلايا لتحليل التدفق الخلوي ، حيث تم تحديد نسبهifnγ +، tnfα + وCD107a + + وCD8 + T الخلايا.
توفر هذه الطريقة قاعده انطلاق لاجراء تحليل شامل لبيئة الورم المجهرية.
Introduction
هذه الطريقة التفاصيل ، من البداية إلى النهاية ، والعملية الجراحية لتوليد أورام البنكرياس العظام باستخدام كميه الحد الأدنى من المواد الخلوية والتفكك السريع اللاحقة من الأورام الراسخة لتحليل التدفق الخلوي شامله لسكان الخلايا المناعية ، بما في ذلك تحليل ex الجسم الخليوي وظيفة
سرطان الغدة السرطانية في البنكرياس (PDAC) هو سرطاني العدوانية مع 8 ٪ فقط من المرضي الذين يعيشون 5 سنوات1. بما ان اقل من 20 ٪ من المرضي مؤهلون لاستئصال الجراحية2، عينات المريض الطازجة ليست متاحه بسهوله للبحوث ، التالي في نماذج الجسم الحيوي توفير الاداات الاساسيه للتحقيق في هذا المرض. هناك نماذج متعددة murine من PDAC: العظام ، تحت الجلد ، المحورة وراثيا ، الحقن الوريدي والمرضي المشتقة (PDAC) ، وصفت علي نطاق واسع هنا3. يسمح نموذج الهجاء الموصوف هنا بحقن خلايا PDAC المتزامنة في بنكرياس الفئران المناعية. وهذا يمكن ان يؤديها في أفواج كبيره من الفئران من النوع البري أو متحولة ، التالي يوفر نموذج فعاله من حيث التكلفة ومتسقة للمقارنة بين العوامل العلاجية. والاهم من ذلك ، فان نموذج الهجاء يوفر البيئة المجهرية لنمو الخلايا السرطانية وينتشر في ايدينا والآخرين4 إلى المواقع ذات الصلة سريريا (علي سبيل المثال ، الكبد) ، مما يجعلها أكثر ملاءمة سريريا من النماذج تحت الجلد أو المستحثة كيميائيا. تعرض الأورام التقويمية الملامح الرئيسية ل PDAC ، مثل تفاعل قوي من البلاستيك مع وفره من الخلايا الليفية وترسب مصفوفة خارج الخلية5. النماذج المحورة وراثيا من PDAC هي المعيار الذهبي للنموذج murine والأكثر شيوعا هو نموذج الفيلق ، الذي يعبر عن متحولة KrasG12D/+ و Trp53R172H/+ تحت البنكرياس الخاص pdac-1-cre المروج6. وتستعرض المؤسسة الاضافيه لفيلق حماية كوسوفو وغيرها من نماذج pdac هنا7. الفئران الفيلق تطوير تلقائيا أورام البنكرياس مع تطور المرض الذي يحاكي بإخلاص ملامح الإنسان PDAC6. ومع ذلك ، النسبة لجميع النماذج المحورة وراثيا ، وبرنامج تربيه مكلفه ، وتطور الورم هو متغير ، التالي غالبا ما يتطلب أفواج كبيره من الفئران. تستخدم نماذج PDX الخلايا السرطانية المشتقة من المريض أو القطع التي يتم زراعتها بعد ذلك اما بالتنظير أو في كثير من الأحيان جلد في الفئران المناعية. نماذج الطعم الغريب توفر أدوات مفيده لفحص المركبات العلاجية وحساب تغاير المريض. ومع ذلك ، فانها لا توفر بيئة مناعية كامله ، التالي الحد من تطبيقاتها8،9.
مره واحده المنشاة ، والأورام التقويمية عاده ما يستغرق حوالي 1 شهر أو أكثر لتنمو (اعتمادا علي خط الخلية المستخدمة) وتشكل الأورام الكبيرة التي يمكن ان تكون بسهوله التصوير بالموجات فوق الصوتية أو التصوير بالرنين المغناطيسي لتتبع التقدم وتحديد فعاليه العلاج4،5،10. ومع ذلك ، مره واحده في النمو المتسارع ، والمرحلة الاخيره من نمو الورم يمكن ان تكون سريعة ، لذلك بدات معظم نظم العلاج في وقت مبكر نسبيا (علي سبيل المثال ، 14 يوما)11،12. يلعب الجهاز المناعي دورا حاسما في تطوير الورم ، بما في ذلك في PDAC ، والذي يتميز بورم المناعة التسلل مع ندره نسبيه من الخلايا T وكثرة وجود خلايا النخاع13. وجود عال من [ت] خلايا في [بداك] يمنح تكهن جيده14,15. ومع ذلك ، كعوامل واحده ، ومثبطات نقاط التفتيش المناعية التي تخفف من كبت المناعة الخلية T ، مثل مكافحه CTLA-416 ومكافحه PD-L117، لم تظهر الفائدة السريرية في المرضي pdac ، علي الأرجح لان الخلية الكلية t التفاعلية منخفضه جدا. ومع ذلك ، فان العوامل التي الاستجابات الخلية الرئيسية T ، مثل المضادة لCD40 ، يمكن التغلب علي مكافحه PD-L1/ctla-4 المقاومة18،19 والتطعيم مع جنرال موتورز-السائل النخاعي-سيكريتينغ اللقاح pdac (gvax) يمكن ان تزيد من والاستمناع الأورام pdac20، مشيرا إلى ان
الحرجة لاستجابه الخلايا T انتيتورال هو التعرف علي المستضدات المشتقة من الورم عبر مستقبلات الخلايا التائية (TCR) والإنتاج اللاحق من السايتوكينات السامة للخلايا والحبيبات. في حين يمكن تحديد التعرف علي مستضد الخلية T بواسطة تسلسل TCR ، فان هذا النهج مكلف ويستغرق وقتا طويلا. ومع ذلك ، القياس الكمي للورم التسلل الخلايا الفرعية T يوفر مؤشرا جيدا لاستجابه مضاده للتوشف. المزيد من الفحص لنشاط الخلية T ex الجسم الفيفو من حيث التحبيب ، وإنتاج السايتوكين وغيرها من العوامل السامة للخلايا يوفر تحليل وظيفي أعمق. ويمكن اجراء هذه الاختبارات علي عينات الأورام الطازجة والعديد من المعلمات من وظيفة الخلية T يمكن قياسها بسرعة عن طريق تدفق الخلوي.
CD8 + و الخلايا التائية + T تنتج السايتوكينات مثل Ifnγ و TNFα لتحفيز استجابه مناعية21. IFNɣ يحفز MHCI الحاملة علي الخلايا المستهدفة ، ويدفع التمايز وتجنيد الخلايا المناعية والإيدز موت الخلايا. Ifnγ الإنتاج بواسطة خلاياCD8 + T يتميز جيدا ليكون جزءا من استجابه انتيتورال ويرتبط مع الانحدار الورم22,23. TNFα هو السايسيسين التهابيه الأخرى التي تنتجها كل منCD8 + و الخلاياالتائية . فانه يعزز التنشيط المعتمدة علي TCR وتكاثر الخلايا T ، ومساعده الاستجابة المضادة للتوشف. عند مشاركه TCR ، يمكن للخلاياCD8 + T السامة للخلايا الخضوع لتحبيب ، حيث يتم تحرير الخلايا الشحمية التي تحتوي علي جزيئات سامه للخلايا في المشبك المناعي للتسبب في تدهور الخلايا المستهدفة21. وتشمل هذه الجزيئات تثقيب ، وهو البروتين الذي يربط إلى غشاء الخلية المستهدفة ، وتشكيل المسام التي ثم تعطيل سلامه الغشاء والسماح انتشار21 أو ندره المحببات24 من الجزيئات السامة للخلايا الأخرى ، مثل granzyme ب ، مباشره في سيتوتوبلاسما الخلية المستهدفة. غرانزيم B هو الانزيم البروتيني الذي يسن تحلل البروتينات المتعددة داخل الخلية المستهدفة ، مما يؤدي إلى وفاه الخلية21. ويتطلب الإفراج عن هذه الجزيئات كثرة التنظير الباطني علي سطح الخلية ، حيث يتم دمج علامة التنظير الباطني CD107a (المعروف أيضا باسم مصباح-1) بشكل عابر في غشاء الخلية25.
ويتطلب قياس إفراز السايسيسين بواسطة الخلايا التائية عزلها بواسطة فرز الخلايا بمساعده التدفق أو اختبارات الفصل القائمة علي الخرزة ، والتي لا يمكن تنفيذها بسهوله علي عدد كبير من العينات في وقت واحد. ومع ذلك ، فان قياس السايتوكينات داخل الخلايا لا يتطلب اي خطوات سابقه للعزل ، ويمكن تنفيذها بسهوله علي عينات متعددة في وقت واحد ، مما يسمح باتباع نهج الانتاجيه الأعلى. كما يفرز بسرعة السايتوكينات الخلايا T ، يمكن ان تكون المستويات داخل الخلايا غير قابل للكشف ، التالي فان خليه T يتطلب التحفيز لزيادة إنتاج السايتوكين القاعدية. لتقييم إنتاج السايسيسين التي يحركها مستضد ، يجب ان يتم تقديم مستضد المعترف بها من قبل TCR إلى الخلية T من قبل APC تستعد في المختبر. وفي الحالات التي لا تعرف فيها الخصوصية الخاصة بالمولد ، يلزم اتباع نهج محفز واسع النطاق. يمكن محاكاة التحفيز TCR باستخدام الخرز المضادة لCD3/28 التي توفر كلا من التنشيط TCR والتزاوج ، الذي يحفز إنتاج السايسيسين وانتشار. ومع ذلك ، فان البديل الأكثر فعاليه من حيث التكلفة هو استخدام النقد الذاتي و ionomycin ، الذي ينشط معا علي نطاق واسع مسارات الإشارات التي تؤدي إلى توليف وإطلاق السايتوكينات داخل الخلايا. علي وجه التحديد ، والنقد الخاص ينشط البروتين كيناز C (PKC) و ionomycin يثير الخلايا Ca2 + الأيونات ، مما يؤدي إلى زيادة الخلايا الإشارات. من أجل الحفاظ علي المحتوي داخل الخلايا من السايتوكينات ، يمكن ان يقترن هذا التحفيز بشكل فعال مع مثبطات البروتين والنقل brefeldin A و مونينسين ، والتي تمنع البروتينات في Golgi التالي منع الإفراج خارج الخلية. استخدام نقدا/ionomycin هو وسيله راسخة لتحفيز الخلايا T وهناك علاقة قويه بين الخلوية الصادرة وخلايا السايتوكينات26. التحفيز من الخلايا T مع نقدا و ionomycin أيضا يزيد من الاتجار يحلول إلى غشاء الخلية ، التالي CD107a يصبح بشكل عابر متكاملة علي سطح الخلية قبل أعاده تدويرها في الخلية. بما في ذلك الأجسام المضادة لCD107a اثناء التحفيز ، فمن الممكن استخدامه كعلامة من النشاط التحبيب25.
هذه الطريقة بسرعة بهضم الأورام لتوفير تعليق خليه واحده. عند هذه النقطة ، يمكن ان يكون السكان الفردية ملطخه مباشره لقياس التدفق الخلوي أو تنقيه بواسطة أساليب المصب: تدفق الخلايا بمساعده الفرز أو الفصل المغناطيسي حبه. اعداد تعليق خليه واحده لتحليل التدفق الخلوي يسمح تحليل عاليه الانتاجيه من العديد من الخلايا المناعية وعلامتاتها الظاهرية ، وتوفير كميات دقيقه من رقم الخلية المناعية والنمط الظاهري.
وأخيرا ، فان بروتوكول الهضم الموصوف هنا يمنع فقدان علامات سطح الخلية ويحافظ علي سلامه الخلايا المناعية ، مما يسمح للخلايا المناعية بالخضوع لمزيد من خطوات تنقيه الخلايا والثقافة حسب الحاجة. ومع ذلك ، لم يتم اختبار هذه الطريقة لاشتقاق الخلايا الظهاريه من هذا الهضم.
Protocol
تم إنشاء أورام البنكرياس التقويمية كما سبق وصفها10 وفقا لقانون الإجراءات الحيوانية والعلمية لوزارة الداخلية في المملكة البريطانية 1986 والتوجيه الأوروبي 2010/63/EU. تم رصد جميع الفئران بشكل غير محدد لعلامات الم أو المعاناة ، بما في ذلك ولكن ليس علي سبيل الحصر فقدان الوزن (> 15 ٪ في 72 h أو 20 ٪ في اي فتره معينه) ، والانتصاب ، وتضييق العينين ، وأثار مشيه ، مظهر منحني ، فضلا عن علامات عدوي الجرح بما في ذلك النزيف واحمرار وتقرح تم رصد نمو الورم عن طريق الجس ، ورصدت أيضا علامات سريريه اضافيه مثل التنفس الكادح ، اليرقان والأطراف الباردة من أجل تقييم ما إذا كان قد تم التوصل إلى علامات نقطه النهاية. وينبغي تنفيذ جميع الإجراءات في ظروف عقيمه. يجب اعداد جميع الكواشف المستخدمة قبل تلطيخ التدفق الخلوي في ظروف معقمه.
1. اعداد الخلايا السرطانية للحقن
- خذ الغشاء السفلي من-20 درجه مئوية ومكان علي الجليد في 4 °C بين عشيه وضحيها.
ملاحظه: قد يختلف تركيز غشاء القبو من دفعه إلى دفعه ؛ ولذلك ، يجب اختبار الكثير محدده دفعات غشاء الطابق السفلي في الجسم المجري لضمان استنساخ. يتم أذابه دفعه جديده من غشاء الطابق السفلي علي الجليد عند 4 درجه مئوية بين عشيه وضحيها ثم اقتبس في الارصفه المعرفة من قبل المستخدم ، علي الجليد ، ومن ثم مزيد من المخزنة في-20 درجه مئوية حتى المطلوبة. وهذا يقلل من الأنابيب وتجميد الذوبان عند استخدام غشاء القبو.- ضع المعقمة في 4 °C ليلا لتبرد.
- ضعي 200 μL المعقمة و 1000 μL الماصة في-20 درجه مئوية ليلا لتبرد.
- استخدام الخلايا السرطانية التي هي الميكوبلازما الحرة ، نمت لما لا يقل عن 2-10 الممرات بعد الذوبان وفي مرحله السجل من النمو قبل الحصاد. ويستخدم هذا البروتوكول خط الخلية المستخرج من الفيلق C57BL/6 ، وهو: TB32048 قدمت كهديه سخية من مختبر ديفيد توفيسان.
- عندما تكون الخلايا السرطانية مطلوبه للحصاد ، وأزاله المتوسطة من القارورة وغسل الخلايا مرتين في الاذاعه التلفزيونية (قبل تسخينها إلى 37 درجه مئوية).
- أضف 2x التريبسين (قبل التسخين إلى 37 درجه مئوية) إلى القارورة لمده 10 دقائق عند 37 درجه مئوية (إلى قارورة T175 ، أضف 5 مل).
- بعد 10 دقيقه ، أضف حجما متساويا من المتوسط الكامل (10% من العدد الكلي ، البنسلين 1x ، 1x ستربتومايسين في DMEM) إلى القارورة وفك الخلايا عن طريق التنصت برفق علي القارورة وأعاده التعليق جيدا في الوسط.
- نقل الخلايا إلى أنبوب والطرد المركزي لمده 5 دقائق في 300 x g ودرجه حرارة الغرفة (RT).
- أزاله ماده طافي وأعاده تعليق الخلايا في المتوسط الكامل لجرد الخلايا.
- خلايا الطرد المركزي مره أخرى لمده 5 دقائق في 300 x g و RT ، وأزاله supernatant.
- أعاده التعليق الخلايا في ما قبل المبردة تلفزيوني لتحقيق تركيز 1x106 خلايا/مل.
ملاحظه: يتم اعداد تركيز هذا المخزون لتحقيق تركيز الحقن النهائي للخلايا 1000 في 5 μl. وجدنا حقن لعدد اقل من الخلايا في حجم حقن منخفضه الحد من تسرب الخلايا التالي زيادة استنساخ ومع ذلك ، قد يكون نمو الورم الخلية التابعة لذلك يجب علي المستخدمين تحسين كل خط الخلية.
- إلى جانب هذا ، ضع غشاء القبو قبل النقل السفلي ، علي الجليد ، في غطاء المحرك.
- نسبه الحل النهائي لغشاء الطابق السفلي ، والخلايا السرطانية والأورام في الاذاعه التلفزيونية المعدة للحقن هو 5:3:2. لذلك إلى 500 μL ميكرولتر من غشاء الطابق السفلي أضافه 300 μL من المبردة مسبقا باستخدام المبردة مسبقا 1000 μL طرف ماصه.
- أضافه التلفزيونية مباشره إلى الطابق السفلي غشاء قسامه للتقليل من التنضيد.
- الحفاظ علي تعيين p1000 إلى 300 μL وأعاده التعليق علي الغشاء السفلي والقبو ، والتاكد من الحفاظ علي أنبوب علي الجليد للحفاظ علي غشاء الطابق السفلي في حاله السائل.
- عند الانتهاء من إخراج كل غشاء الطابق السفلي من طرف p1000 ، ترك غيض في أنبوب للسماح لأي غشاء الطابق السفلي/تلفزيوني لينزل غيض ماصه.
- بعد 5-10 دقيقه ، وإخراج المزيد من الغشاء السفلي من تلميح p1000 مره أخرى إلى الأنبوب وترك الأنبوب للجلوس علي الجليد.
- خذ 200 μL من الخلايا السرطانية المعاد تعليقها في الاذاعه التلفزيونية وأضافه مباشره إلى غشاء الطابق السفلي باستخدام طرف ماصه قبل المبردة 200 μL.
- خذ p1000 الماصة الطازجة قبل المبردة ، اضبط الماصة علي 300 μL وأعاده التعليق 30-40 مره. ومن الأفضل ان يكون الطرف الأكبر من الماصة ، الذي يتم تعيينه علي مستوي منخفض ، كما يمكن ان يصل الغشاء السفلي إلى الطرف الآخر وان يلمس فلتر طرف الماصة اثناء أعاده التعليق.
- الخلايا السرطانية جاهزه للحقن. الحفاظ علي الخلايا السرطانية/غشاء القبو علي الجليد اثناء الجراحة.
2. حقن العظام من الخلايا السرطانية
- تاقلم الفئران في منشاه الحيوانية لمده 7 أيام.
- حوالي 2 ساعة قبل الجراحة ، حلق الجانب الأيسر من البطن والظهر ، ثم أداره الجلد المسكنة قبل العملية تحت الوازع من الرقبة (Buprenorphine في 50-100 ميكروغرام/كغ).
- اعداد المجال الجراحي ، مع حصيره الحرارة لوضع الماوس علي والستائر للمعدات المحيطة بها وأكثر من الماوس. تعقيم جميع الاداات الجراحية. اعداد مجموعات كافيه من الاداات لكل ماوس.
- ضع الماوس في ايزوفلونان 5 ٪ مع الغرفة O2 حتى فاقد الوعي.
- نقل الماوس ، والكذب علي ظهره ، علي حصيره الحرارة والحفاظ علي التخدير باستخدام قناع ، وعاده في اقل 2-3 ٪ ايزوفلواني.
- تاكيد التخدير العميق. كما حددتها فقدان منعكس دواسة الانسحاب عندما يتم ضغط مخلب الخلفية ورصد معدل التنفس لا يزال ثابتا.
- غطيت الجسم في ثني, مع فقط ال يحلق جزء يعرض. تاكد من ان الماوس أمن في قناع التخدير.
- باستخدام برعم القطن المعقم ، أضافه محلول اليود في حركه دائريه علي المنطقة حليق: بدءا من المركز وتحلق خارجا إلى الحافة. كرر العملية مره أخرى مع برعم القطن الطازج واليود.
- استخدم المشرط لاجراء شق بطول 1 سم فوق موقع البنكرياس/الطحال مباشره (الربع العلوي الأيسر). ويمكن أيضا ان تستخدم مقص معقمه لجعل الشق ، إذا كان يفضل.
- سحب الجلد بعيدا باستخدام ملقط. مع ملقط جديد ، حدد موقع الجدار البريتوني واستخدام مقص لجعل آخر شق 1 سم من خلال الجدار الصفاقي.
- استخراج البنكرياس ، والتي قد تاتي مع الطحال ، من الجسم باستخدام الزوج الثاني من الملقط.
- عكس برفق قارورة من الخلايا السرطانية/غشاء الطابق السفلي عده مرات لخلط.
- اعداد حقنه زجاجيه مع 5 μL تحتوي علي خلايا الورم 1,000 في غشاء الطابق السفلي ومكان علي حصيره الحرارة لبضع ثوان للسماح لها بالدفء.
ملاحظه: سوف الاحترار وجيزة من حقنه تسمح غشاء الطابق السفلي للبدء في ترسيخ ، من أجل جعله أسهل لحقن دون تسريب. ومع ذلك ، يجب ان يبقي هذا موجزا ، إذا تركت طويلة جدا غشاء القبو سوف يصلب تماما ولن يتم حقن. استخدام حقنه زجاجيه يسمح حجم منخفض ليتم حقنها بدقه. - عقد البنكرياس في الذيل لتوسيعه وادراج الابره مباشره في وسط البنكرياس ، موازيه للبنكرينفسه مع محاولة لتجنب الاوعيه الدموية المرئية.
ملاحظه: مركز البنكرياس لديه مساحة كبيره وانه من الأسهل لحقن. ومع ذلك ، يمكن أيضا حقن راس أو ذيل البنكرياس علي وجه التحديد إذا كان يفضل. - حقن ببطء 5 μL من غشاء الطابق السفلي في البنكرياس وعقد ابره ثابته في البنكرياس لمده 30 ثانيه علي الأقل بعد الحقن للسماح لغشاء الطابق السفلي ليصلب ومنع تسرب. يجب ان يكون الغشاء السفلي مرئيا كما ستكون فقاعه واضحة صغيره شكلت; ومع ذلك ، قد لا تكون مرئية.
ملاحظه: يمكن حقن كميات أكبر من الخلايا السرطانية/غشاء الطابق السفلي ؛ ومع ذلك ، يجب اختبار وحده التخزين بالبالضبط لضمان عدم حدوث تسرب. - أزاله الابره من البنكرياس والانتظار لتاكيد عدم حدوث نزيف. ادراج البنكرياس برفق مره أخرى في تجويف البطن ، مع الحرص علي عدم لمس فقاعه غشاء الطابق السفلي.
- سحب الجدار البريتوني معا واجراء خياطه واحده ، أو اثنين من الغرز المتقطعة إذا لزم الأمر.
- سحب الجانبين من شق الجلد معا وأداء الغرز التي توقفت متعددة حسب الحاجة أو ادراج اثنين من لقطات الجراحية.
- أداره حقنه أخرى تحت الجلد من البوبرينورفين في التوفف.
- نقل الماوس في قفص 37 درجه مئوية ساخنه لمده 30 دقيقه علي الأقل بعد الجراحة للحفاظ علي درجه حرارة الجسم قبل نقل مره أخرى إلى قفص جديد.
- اعداد حمية الهريس المتاحة في القفص ، لضمان الاماهه ووزن الجسم.
- أعاده أداره تسكين بعد العملية الجراحية علي النحو الموصي به ومشاهده عن كثب لعلامات فتح الجرح ، والم أو العدوى وفقدان الوزن. إذا كان استخدام لقطات الجراحية ، ويمكن أزاله هذه 7-10 أيام في وقت لاحق باستخدام مزيل كليب.
- بعد حوالي 14 يوما سوف تلتئم الانسجه ندبه بما فيه الكفاية للبدء في خفقان البطن. رصد حجم الورم عن كثب عن طريق الجس حتى تصل الفئران نقطه النهاية.
- عند نقطه النهاية يتم إعدام الماوس عن طريق خلع عنق الرحم تليها قطع الراس. يتم فتح الجلد والتجويف الصفاقي باستخدام المقص وورم البنكرياس المثير باستخدام ملقط لعقد الورم ، ومقص لأزاله الانسجه المحيطة بها.
3. هضم أورام البنكرياس
- ضعي ورم البنكرياس الذي تم تشريحه ، أورام الموقع المنتشرة ، أو انسجه البنكرياس الصحية في الثلج البارد ، وخزنيه علي الجليد.
- استخدم الملقط لنقل الورم إلى طبق بيتري.
- أضافه 5.0 mL من الهضم المتوسطة (2 ملغ/مل كولاجيناز, 0.025 mg/mL DNase RPMI) في أنبوب 50 mL; تخزين علي الجليد لمنع النشاط انزيم البدء.
ملاحظه: يستخدم هذا البروتوكول النوع الخامس كولاجيناسي ، الذي لديه نشاط ≥ 1 وحده/ملغ FALGPA وال> 125 الكولاجين وحدات الهضم (الحزب الديمقراطي المسيحي)/mg الصلبة. كولاجيناز و dnase القسامات يمكن تخزينها في-20 درجه مئوية وأذابها علي الجليد قبل الاستخدام. عندما يتم أذابه كليهما في RPMI معقمه ، يمكن تمريرها من خلال فلتر 0.2 μm لأزاله الملوثات. كولاجيناز يجب ان يكون تماما solubilized قبل تصفيه لتجنب فقدان المواد. - خذ القليل من هذا المحلول لتغطيه الورم علي طبق بيتري.
- استخدام مشرط معقمه وملقط لقطع الورم إلى قطع صغيره ، وتقريبا اقل من 3 ملم في الطول.
- كشط قطع الورم في الأنبوب وعكس الأنبوب برفق حتى يتم غمر جميع القطع في وسائل الهضم. تخزين علي الجليد إذا عينات الورم الأخرى تحتاج إلى ان تكون مستعدة في دفعه واحده.
- نقل إلى جهاز اهتزاز لمده 20 دقيقه في 37 درجه مئوية. تاكد من غمر جميع قطع الورم وعدم التصاقها بحافه الأنبوب. إذا الاهتزاز غير ممكن ، ثم دوامه العينة كل 5 دقائق للمساعدة في الهضم.
4-اعداد تعليق الخلية الواحدة من الورم المهضوم
- مباشره بعد خطوه الهضم ، ضع الأنبوب علي الجليد لإبطاء نشاط الانزيم.
- أضافه أدتا لتحقيق تركيز نهائي من 20 ملم وعينه دوامه لفتره وجيزة لخلط. وهذا سيؤدي إلى زيادة تباطؤ نشاط الانزيم.
- فتح الأنبوب وشطف اي هضم الورم قباله غطاء الأنبوب مع المتوسطة RPMI الطازجة.
- اعداد مصفاه 70 μm (يمكن تغيير حجم ميكرومتر من مصفاه حسب الرغبة) علي أنبوب مفتوح 50 mL ، علي الجليد.
- قبل الرطب فلتر مع المتوسطة.
- أعاده تعليق الخلايا المهضومة وغسل الجانبين من الأنبوب باستخدام ستريبيتي 25 مل ، أو أكبر. الافتتاح الأوسع لستريبيتي مهم للسماح للخلاصة السميكة بالمرور بسهوله.
- نقل كل من الخلاصة ، وذلك باستخدام ستريبيتي 25 مل ، علي مصفاه.
- الهريس الورم علي راس فلتر باستخدام 1 مل حقنه الغطاس. الهريس فقط مباشره صعودا وهبوطا للحد من الإجهاد القص إلى الخلايا.
- اغسل الخلايا باستمرار من خلال المصفاة مع RPMI. تاكد من غسل بقوة كافيه لدفع الخلايا من خلال.
- إذا كان هناك ما زالت المواد للهريس ، ولكن RPMI توقف التنظيف من خلال ، سيتم المشبعة مصفاه. لذلك ، نقل العينة إلى عامل تصفيه جديد ومتابعه.
ملاحظه: في نهاية المطاف فقط مكونات مصفوفة خارج الخلية ستبقي في عامل التصفية ، يجب ان تكون كافة الخلايا المفردة مرت.
- الطرد المركزي أنبوب لمده 5 دقائق في 300 x g و 4 ° c.
- أعاده تعليق بعناية بيليه الخلية في RPMI كامله وتمر مباشره من خلال فلتر آخر لأزاله اي مصفوفة خارج الخلية أو كتل الخلايا الكبيرة التي لا يمكن أعاده تعليقها بشكل كاف.
- عند هذه النقطة ، إذا لم يكن هناك حاجه التحفيز ، وصمه عار علي الفور الخلايا المعزولة لتحليل تدفق الخلوي عن طريق تخطي إلى الخطوة 6.1. بدلا من ذلك ، أعاده تعليقها في المتوسطة تجميد (10 ٪ DMSO في المعرض) وتخزين في-80 درجه مئوية تليها التخزين علي المدى الطويل في النيتروجين السائل.
ملاحظه: يمكن ان تسمح خطوه التجميد تنقيه الخلايا المناعية في وقت لاحق. ومع ذلك ، قد يتطلب القياس الكمي للخلايا المناعية الفرعية التحسين للتاكد من ان أرقام الخلايا والنمط الظاهري لا يتاثر بعمليه التجميد/الذوبان. يتم تنفيذ التحفيز الخلية السابقة الفيفو T أفضل علي عينات الورم الطازجة. عند هذه النقطة يمكن تنقيه العينة بواسطة أزاله الخلايا الميتة المبنية علي الخرزة أو اختبارات تخصيب الخلايا المناعية إذا لزم الأمر.
5. اعداد الخلايا لتحفيز الجسم السابق
- عد الخلايا لتحقيق تركيز 2 × 106/100 μl في المتوسطة الكاملة (rpmi 10 ٪ ار ، 1x البنسلين و 1x ستربتومايسين).
ملاحظه: العدد الكبير من مجموع الخلايا مطلي يضمن انه سيكون هناك خلايا T كافيه داخل هذه العينة لتحليل. ومع ذلك ، يمكن تحجيم الرقم صعودا أو هبوطا اعتمادا علي توافر العينة والطبيعة النادرة لمجموعات فرعيه من الفائدة للخلية T.- لوحه 100 μL من الخلايا في لوحه 96-بئر القاع.
- أضافه 100 μL من المتوسطة الكاملة التي تحتوي علي اعداد 2x من نقدا/ionomycin (لتحقيق التركيز النهائي 0.081 μM و 1.34 μM ، علي التوالي ، علي النحو الموصي به من قبل الشركة المصنعة).
ملاحظه: إذا قياس التحبيب/الاكندره ، وتشمل أيضا هنا فلوريسسينتلي مترافق المضادة للماوس CD107a في وسائل الاعلام. يجب أيضا تنفيذ نموذج عنصر تحكم لا يحتوي علي CD107a. - مكان في 37 درجه مئوية حاضنه مع 5 ٪ CO2 لمده 1 ساعة.
- أضافه 20 μL من اعداد 10x من brefeldin A و مونينسين (لتحقيق تركيز النهائي 1.06 μM و 2.0 μM ، علي التوالي (علي النحو الموصي به من قبل الشركة المصنعة) في وسائل الاعلام الكاملة.
ملاحظه: Brefeldin A و مونينسين هي مثبطات نقل البروتين التالي منع الإفراج خارج الخلية من السايتوكينات ، وما إلى ذلك السماح الكشف عن طريق تدفق الخلوي. إذا كان قياس السايسيسين الإفراج في ماده طافي من قبل اليسا أو أساليب مماثله-ثم يمكن تخطي هذه الخطوة. - وضع لوحه في 37 درجه مئوية حاضنه مع 5 ٪ CO2 لمزيد من 4 ح.
6. تلطيخ خارج الخلية وداخل الخلايا لتدفق الخلوي
- أزاله لوحه وأعاده تعليق كل بئر لنقل جميع المواد إلى لوحه القاع الخامس ، وضعت علي الجليد.
ملاحظه: قد لا يتم استرداد الخلايا الظهاريه والضامة والخلايا الملتصقة الأخرى بشكل كامل عن طريق أعاده تعليق. ولكن كما تحليل المصب هو فقط علي الخلايا T ، وهذا ليس مشكله.- 6.1.1 الطرد المركزي لوحه لمده 5 دقائق في 300 x g و 4 درجه مئوية (استخدم هذه الشروط للخطوات اللاحقة ما لم يذكر).
- أزاله ماده طافي عن طريق تحريك لوحه راسا علي عقب في حركه واحده حاده.
- أعاده التعليق في 50 μL من صبغه قابله للتثبيت ، أعدت في الجليد الباردة. عند أعاده التعليق ، اضبط الماصة علي حجم اقل لتجنب صنع الفقاعات.
- احتضان لمده 20 دقيقه في 4 درجه مئوية ، في الظلام.
- غسل الخطوة: أضافه 100 μL من العازلة FACS ، الطرد المركزي وأزاله supernatant.
- أعاده التعليق كل بئر مع 50 μL من المضادة لCD16/CD32 (2.5 ميكروغرام/مل) في المخزن المؤقت FACS (0.5 ٪ جيش الصرب البوسنيين ، 2.0 mM أدتا في تلفزيوني) لمنع ملزمه غير محدده من الأجسام المضادة للكشف عن مستقبلات Fc.
- احتضان لمده 15 دقيقه في 4 درجه مئوية ، في الظلام.
- أضافه مباشره إلى كل بئر 2x ماسترميكس من الفلوروكروم-مترافق المضادة للماوس CD45 ، CD3 ، و CD8 (يمكن أضافه علامات خارج الخلية كما هو مطلوب) في المخزن المؤقت FACS.
- احتضان لمده 30 دقيقه في 4 درجه مئوية ، في الظلام.
- غسل الخطوة: أضافه 100 μL من العازلة FACS ، الطرد المركزي وأزاله supernatant.
- أضافه 100 μL من 1x داخل الخلايا (IC) تثبيت العازلة واحتضان لمده 30 دقيقه في RT ، في الظلام.
- اعداد جهاز الطرد المركزي في RT.
- أضافه 100 μL من المخزن المؤقت FACS ، الطرد المركزي لمده 5 دقائق في 300 x g و RT وأزاله supernatant. كرر مع 1x العازلة والطرد المركزي لمده 5 دقائق في 300 x g؛ ثم أزاله سوبرناتانت.
- أضافه 50 μL من 1x ماسترميكس من الفلوروكروم-مترافق المضادة للماوس IFNγ ، TNFα ، وعلامات داخل الخلايا الأخرى التي أعدت في 1x العازلة تخلل.
- احتضان لمده 1 ساعة في RT ، في الظلام.
- أضافه 100 μL من المخزن المؤقت تخلل لغسل. ثم أجهزه الطرد المركزي لمده 5 دقائق في 300 x g و RT وأزاله supernatant.
- أضافه 100 μL من المخزن المؤقت FACS لغسل ، الطرد المركزي لمده 5 دقائق في 300 x g و RT وأزاله supernatant.
- بعد هذا الطرد النهائي ، أعاده تعليق الخلايا في وحده تخزين متوافقة لمقياس التدفق الخلوي. قد تختلف تبعا لحجم أنابيب FACS.
- نقل وحده التخزين هذه إلى أنابيب FACS المناسبة للحصول عليها.
- تغطيه من الضوء وتخزينها في الثلاجة والحصول علي عينات في غضون 24 ساعة.
النتائج
بعد حقن 1000 الخلايا TB32048 في البنكرياس ، والأورام التقويمية تاخذ ما يقرب من 30 يوما لتطوير (الشكل 1ا ، ب). يمكن ان يسبب تسرب غشاء القبو اثناء الجراحة أوراما كبيره لتشكل مباشره علي الجدار الصفاقي ، والتي تظهر بشكل بارز من خلال الجلد (الشكل 1ج). سنزيل هذه الفئران من الدراسة ومع ذلك ، مع المهارات الجراحية الجيدة يتم تقليل حدوث التسرب. يمكن ان تنمو الأورام التقويمية التي تحصد عند نقطه النهاية إلى حجم كبير في C57BL/6 الفئران من النوع البري (الشكل 1د). أورام العظام المقطوعة تتطلب الهضم في كولاجيناز/DNase لمده 20 دقيقه من أجل تحقيق تعليق خليه واحده (الشكل 2). عند هذه النقطة ، يمكن ان تكون مطليه الخلايا المشتقة من الورم في لوحه U-القاع في 2 × 106 خلايا/حسنا. يمكن تغيير عدد الخلايا مطلي اعتمادا علي انتشار الخلايا T داخل العينة; يمكن خفض رقم الخلية إذا كانت الخلايا T في كثافة عاليه. السيطرة علي الطحال أو عينات العقدة الليمفاوية يمكن أيضا ان تكون مطليه في هذه المرحلة للتحفيز. يتم تحفيز كل بئر مع النقد الشخصي و ionomycin لمده 5 ساعات وبعد 1 ح الحضانة ، يتم أضافه brefeldin A و مونينسين من أجل منع الإفراج خارج الخلية من السايتوكينات (الشكل 2). بعد الحضانة ، يتم تلطيخ العينات للمرفه خارج الخلية والخلويات داخل الخلايا للتحليل عن طريق قياس التدفق الخلوي (الشكل 2).
تم تحليل عينات من الطحال والأورام من الفئران تحمل الأورام التقويمية عن طريق تدفق الخلوي. استراتيجية النابض المستخدمة في تحليل تدفق الخلوي للأورام الطحال والأورام التقويمية يستبعد الحطام باستخدام FSC-A ، SSC-a ، المشككين من قبل FSC-A/FSC-H و SSC-A/SSC-W ، ثم الخلايا الميتة أو ابوتوتيك ايجابيه لصبغ البقاء قابل للتثبيت (الشكل 3ا). ثم يتم بوابات الخلايا المناعية علي النحوCD45 +، والخلايا T بوابات اضافيه علي النحوCD3 + التي تم تعريفها منالمجموعاتالفرعية و CD8 + (الشكل 3ا). ويجري تنفيذ الفلورية ناقص واحد (FMO) لتحديد الفلورية الخلفية للنابضة و brefeldin A/مونينسين فقط يتم تنفيذ السيطرة لتحديد الإنتاج القاعدي من السايتوكينات (الشكل 3ب-د).
بالنسبة لifnγ ، ادي الاحتضان مع brefeldin A/مونينسين في اي زيادة في IFNγ فوق التحكم FMO في عينات الطحال والورم علي حد سواء. ومع ذلك ، فان أضافه النقد الذاتي و ionomycin زيادة ٪ من ifnɣ داخل الخلايا القابلة للكشف في كل من الطحال والأورام المشتقة من الخلايا التائية وCD8 + T.
الطحال و CD8 + T الخلايا ، وتستخدم كعنصر تحكم إيجابي ، لديها إنتاج ifnγ اعلي نسبيا من الأورام المتسللة الخلية T الفرعية ، مع متوسط 6.60 ± 1.5 ٪ و 12.97 ± 3.4 ٪ بالمقارنة مع 4.81 ± 1.0 ٪ و 4.13 ± 1.3 ٪ ، مما يدل علي كبت المناعة يحدث داخل الورم (الشكل 3B و 4a). باستخدام نفس الاستراتيجية ل TNFα ، ونحن تصور ان نسبه عاليه من الخلاياالطحال + t هي ايجابيه لل tnfα داخل الخلايا (65.93 ± 2.3 ٪) ، بالمقارنة مع الخلايا السرطانية التسلل الورم (22.45 ± 5.4 ٪). الطحال والورم التسلل الخلاياCD8 + T تنتج مستويات مماثله من tnfα (25.15 ± 3.7 ٪ و 19.91 ± 5.1 ٪ ، علي التوالي) (الشكل 3ج، الشكل 4ب).
وأخيرا ، CD107a هو علامة التنظير الداخلي التي يتم التعبير عنها عابرا علي سطح الخلية اثناء كثرة المحببات من الحبيبات السامة للخلايا و السايتوكينات ، علي هذا النحو ، يتم استخدامه كعلامة بديله للخلايا الخلوية. الفائدة من تلطيخ ل CD107a اثناء التنشيط ان كل [ترنسنتلي] [سل-سورفس] عبر عن CD107a سوفت كنت أمسكت بالفلوري-جسم مضاد. وتظهر المستويات القاعدية من CD107a في brefeldin A/مونينسين الخلايا المعالجة فقط. لخلاياCD8 + T الطحال ، والتحفيز مع قوه النقد الخاصة/ionomycin يزيد من مستوي CD107a الكشف ، مع اقوي الحامل فيCD8 + الخلايا التي كانت 23.95 ± 3.5 ٪CD107a +، مقارنه 5.8 ± 1.9 ٪ في الورم التسللCD8 + الخلايا ، مما يدل علي الطحالCD8 + كان معدل أكبر من التحبيب. من ناحية أخرى ، وأعرب عن الطحال والورمالتسلل + المستويات القابلة للمقارنة من CD107a 9.37 ± 1.5 ٪ و 11.50 ± 1.8 ٪ (الشكل 3د و 4c).
عموما هذه النتائج تسليط الضوء علي ان الأورام التقويمية يمكن ان تتولد من حقن عدد منخفض جدا (1,000) من الخلايا السرطانية في البنكرياس. ويمكن هضم هذه الأورام بسرعة لعزل الخلايا T لتحفيز الجسم السابق . الكشف عن السايتوكينات داخل الخلايا هو ممكن ويسلط الضوء علي المستوي القاعدي لكبت المناعة من الخلايا T التسلل ، بالمقارنة مع الخلايا T في الاجهزه اللمفاوية الثانوية.
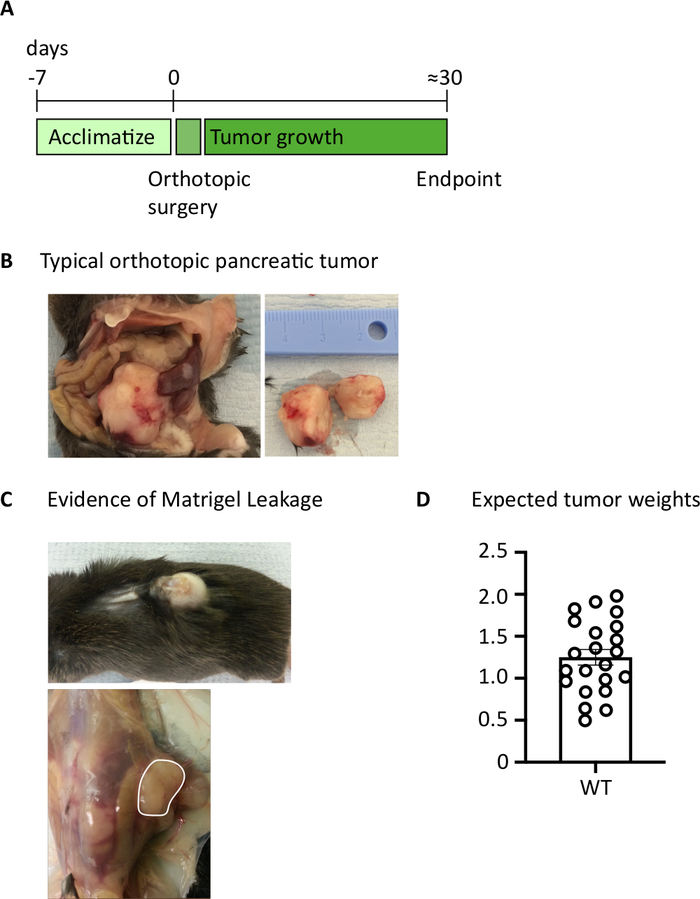
الشكل 1: توليد أورام البنكرياس التقويمية. (ا) الجدول الزمني للتجارب في الجسم المجري . (ب) المظهر المجهري للأورام التقويمية داخل تجويف البطن (يسار) وبعد الاستئصال (يمين) حيث تم قطع الورم الظاهر إلى النصف. (ج) يمكن ان يؤدي الدليل علي تسرب غشاء القبو اثناء الجراحة إلى تطور الأورام التي تظهر من خلال الجلد (الصورة العلوية) والشكل علي الجدار الصفاقي (الصورة السفلية). (د) أوزان أورام البنكرياس التي يتم حصادها من الفئران التي وصلت إلى نقطه النهاية (ن = 22). كل نقطه بيانات يمثل الماوس الفردية ، شريط يظهر الرسم البياني يعني ± SEM. تم تعديل البيانات في هذا الرقم من العمل المنشور سابقا10. يرجى النقر هنا لعرض نسخه أكبر من هذا الرقم.
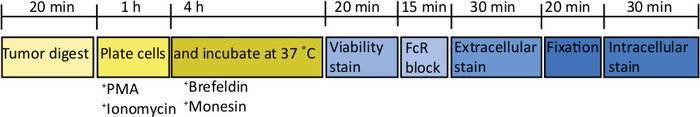
الشكل 2: التخطيطي لمعالجه الأورام التقويمية لتحفيز الخلية السابقة الفيفو T. بعد الحصاد ، يتم هضم أورام البنكرياس بسرعة في كولاجيناز (2 مغ/مل) و DNase (0.025 mg/mL) لمده 20 دقيقه عند 37 درجه مئوية. بعد ذلك ، يتم أعاده تعليق الخلايا في 2 × 106/مل في وسائل الاعلام rpmi كامله ومطلي في لوحه القاع. يتم أضافه كوكتيل التحفيز من نقدا و ionomycin ل 5 ح ، وعند هذه النقطة المضادة للماوس CD107a يمكن أيضا ان تضاف إلى الثقافة. بعد 1 h حضانة حاصرات النقل داخل الخلايا ، brefeldin A و مونينسين ، تضاف. بعد [اكس] [ فيفو ] تنشيط الخلايا [ترنسفرد] داخل [ف-فلي] لوحه ل يصبغ مع ال [رسبل] بقاء صبغ (في [ببس]) ل 20 [مين] 4 [ك.]. يتم غسل الخلايا في المخزن المؤقت FACS وحضنت في المضادة لCD16/32 (FcR كتله) لمده 15 دقيقه (في المخزن المؤقت FACS) ومن ثم حضن مع الأجسام المضادة الفلورية مترافق خارج الخلية لمده 30 دقيقه أخرى (في المخزن المؤقت FACS). يتم غسل الخلايا مره أخرى في المخزن المؤقت FACS وأعاده التعليق في المخزن المؤقت للتثبيت داخل الخلايا لمده 20 دقيقه. بعد ذلك ، يتم غسل الخلايا مره واحده في المخزن المؤقت FACS ومره واحده في 1x العازلة تخلل. يتم أعاده تعليق الخلايا لمده 1 ساعة في RT في الأجسام المضادة الفلورية المترافقة داخل الخلايا لمده 1 ساعة (في المخزن المؤقت للتخلل 1x). يتم غسل الخلايا مره واحده في 1x المخزن المؤقت تخلل ومره واحده في المخزن المؤقت FACS قبل أعاده تعليق في المخزن المؤقت FACS للحصول علي تدفق المضخم الخلوي في غضون 24 ح. الرجاء النقر هنا لعرض نسخه أكبر من هذا الرقم.
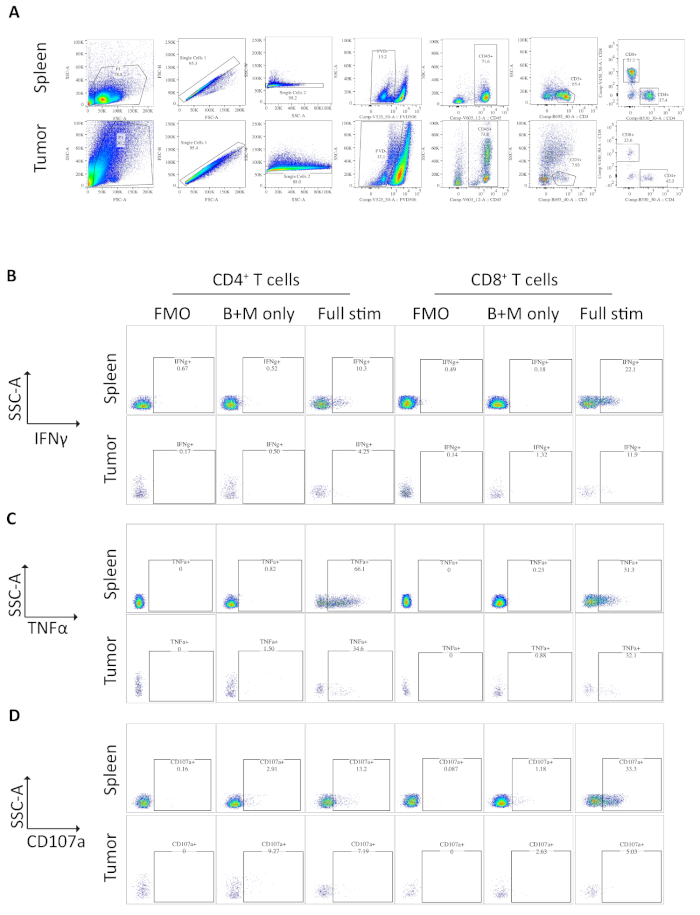
الشكل 3: تحليل التدفق الخلوي للخلايا السابقة التي تحفز الطحال وخلايا T المشتقة من الورم. (ا) التدفق الخلوي الاستراتيجية المستخدمة في الطحال (السيطرة الايجابيه) وعينات الأورام التقويمية. يتم تمييز الخلايا من الحطام باستخدام FSC-ا/SSC-A ويتم عزل الخلايا المفردة باستخدام FSC-A/FSC-H و SSC-A/SSC-W. يتم استبعاد الخلايا الميتة أو ابوتوتيك باستخدام FVD506 الحيوية القابلة للتثبيت ويتم بوابات الخلايا المناعية بواسطةCD45 +. بعد هذاCD3 + Tخلايا و [كد] و [ CD8 + ] حددت مجموعات فرعيه. وقد تم الحصول علي البيانات علي مجموعه "فورنيسا". (ب) استراتيجية الصب المستخدمة لقياس الخلاياifnγ + + + و CD8 + T. يتم استخدام الفلورسنت ناقص واحد (FMO) السيطرة علي عينات حفزت بالبالكامل (سلطه النقد الخاصة/ionomycin/brefeldin A/مونينسين) لتحديد مضان الخلفية. ويستخدم التحكم في المونينسين فقط (B + M فقط) لتحديد إنتاج السايسيسين القاعدي. ثم يتم استخدام العينة المحفزة بالبالكامل لحساب الخلايا%ifnγ + T. (ج) استراتيجية الصب المستخدمة لقياس خلايا TNFα + CD8 + T. ويستخدم عنصر تحكم FMO علي عينات محفزه بالبالكامل (سلطه النقد الخاصة/ionomycin/brefeldin A/مونينسين) لتحديد الفلورية الخلفية. ويستخدم التحكم في المونينسين فقط (B + M فقط) لتحديد إنتاج السايسيسين القاعدي. ثم يتم استخدام العينة المحفزة بالبالكامل لحساب خلايا % TNFα + T. (د) استراتيجية الصب المستخدمة لتحديدخلايا CD107a + + + و CD8 + T. ويستخدم عنصر تحكم FMO علي عينات محفزه بالبالكامل (سلطه النقد الخاصة/ionomycin/brefeldin A/مونينسين) لتحديد الفلورية الخلفية. يتم استخدام التحكم بالمونينسين فقط (B + M فقط) لتحديد التحبيب القاعدي. ثم يتم استخدام العينة المحفزة بالبالكامل لحساب الخلايا%CD107a + T. تم تحليل جميع البيانات تدفق الخلوي علي FlowJo الإصدار 10.6.1. تم تعديل البيانات في هذا الرقم من العمل المنشور سابقا10. يرجى النقر هنا لعرض نسخه أكبر من هذا الرقم.
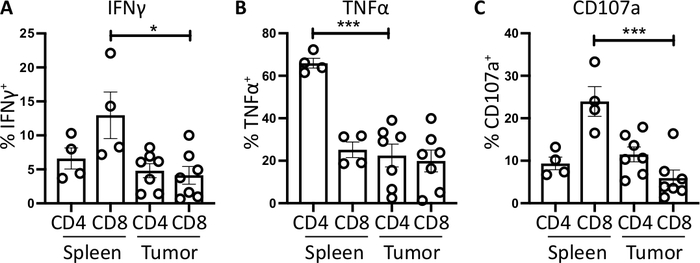
الشكل 4: القياس الكمي لنشاط الخلايا التائية المستمدة من الطحال والورم. نسبه الخلاياالموجبة لCD8 + T الايجابيه ل (ا)ifnγ + (ب) tnfα + و (ج)CD107a + تم تحديدها كميا في الطحال (n = 4) والورم (ن = 7) من الفئران التي تحمل الورم. يمثل كل نقطه بيانات الماوس الفردية وأشرطه الخطا عرض يعني ± SEM. تم اختبار الاهميه الاحصائيه باستخدام اختبار t غير المقترن حيث * = p < 0.05 و * * * = p < 0.001. تم تحليل جميع البيانات باستخدام بريزم 8. تم تعديل البيانات في هذا الرقم من العمل المنشور سابقا10. يرجى النقر هنا لعرض نسخه أكبر من هذا الرقم.
Discussion
في نماذج الجسم الفيفو من سرطان البنكرياس توفير أدوات لا تقدر بثمن لفهم تطور المرض وتقييم المداواة الجديدة الأهداف3. نموذج المجسم علي وجه الخصوص هو نموذج فعاله من حيث التكلفة واستنساخه التي يمكن تطبيقها في أفواج كبيره من الفئران في وقت واحد4,27. كما يوفر نموذج المجسم البيئة المجهرية والنظام المناعي السليم لنمو الورم ، مما يجعله أكثر ملاءمة من النماذج تحت الجلد والطراز PDX. ومع ذلك ، وجدنا ان بعض عناصر التسلل المناعي يمكن ان تختلف بين نموذج الجهاز التقويمي والفئران الفيلق ، ونموذج murine الذهب القياسية10. أحد الأسباب لهذا يمكن ان يكون نمو الورم المتسارع ينظر في نموذج الهجاء. وقد تم وصف المزيد من الاختلافات في كثافة الخلايا المناعية الفرعية بين المجسمات والنماذج تحت الجلد3,28. ولذلك ، وعلي الرغم من ان نموذج الفيلق المحور وراثيا أكثر تكلفه ومتغير6، ينبغي التحقق من النتائج الرئيسية في مجموعه صغيره من فئران فيلق حماية كوسوفو حيثما أمكن ذلك.
يعد اعداد الخلايا السرطانية للجراحة التقويمية خطوه حاسمه في البروتوكول. يجب ان تكون الخلايا دائما في مرحله السجل من النمو والميكوبلازما-وخاليه من العدوى. يجب تاجيل الجراحة التقويمية إذا كان هناك اي مخاوف بشان نمو الخلايا السرطانية. استخدام غشاء الطابق السفلي يحسن معدل حدوث الورم علي الخلايا بالحقن دون ذلك29 ويقلل من تسرب الخلايا التالي انتشار البريتوني27. ومع ذلك ، مره واحده معلقه في غشاء الطابق السفلي ، يجب حقن الخلايا السرطانية بسرعة (في غضون 2 ساعة) لتجنب اي فقدان الخلايا. من المرجح ان يكون عدد الخلايا السرطانية المطلوبة لتوليد الأورام معتمدا علي الخلايا ، وينبغي اختبار مجموعه من أرقام الخلايا (علي سبيل المثال ، من 100 – 100,000) والتي قد تحدد أيضا الوقت اللازم للوصول إلى نقطه النهاية. فمن المرجح ان يكون هناك هامش خطا عند اعداد 1,000 خلايا لكل ماوس للحقن. لذلك ، إذا كانت هناك حاجه لعده أيام من الجراحة ، يجب ان ينتشر علاج المجموعات علي قدم المساواة عبر الأيام للسيطرة علي الآثار الدفعيه. يمكن تعديل معظم الخطوات الجراحية اعتمادا علي تفضيلات; ومع ذلك ، يجب الحرص علي عدم إزعاج غشاء الطابق السفلي عند استبدال البنكرياس في تجويف البطن أو إغلاق الجدار الصفاقي. يمكن ان يسبب تسرب غشاء القبو نمو الخلايا السرطانية علي الجدار الصفاقي ، والتي تشكل بسرعة ويمكن ان يؤدي إلى الاضطرار إلى التضحية الحيوانية في وقت سابق.
ومن الناحية المثالية ، ينبغي هضم أورام البنكرياس بسرعة بعد الحصاد واعدادها لتحفيز الجسم السابق علي الفور. ومع ذلك ، قد لا يكون هذا ممكنا إذا كان هناك دفعه كبيره من الأورام للحصاد ، في هذه الحالة يجب ان تبقي الأورام علي الجليد وهضمها علي دفعات. وقد تبين ان نوع وتركيز وطول التعرض لانزيمات الجهاز الهضمي تؤثر علي عدد كبير من جزيئات السطح علي الخلايا المناعية30،31،32. ال [هضم تيم] أيضا عمدا قصيرة ان يحد خليه موت33. يمكن تجميد الخلايا المهضومة في وسط التجميد للتخزين علي المدى الطويل. ومع ذلك ، فان بعض فقدان الخلايا تحدث عند الذوبان. عمليه الهضم يمكن ان تكون اقل من الأمثل إذا قطع الورم ليست مكعبات بما فيه الكفاية قبل حضانة كولاجيناز وهذا سيكون واضحا كما ستبقي قطع الورم الثابت في تصفيه بعد الهضم. يمكن خفض تركيز كولاجيناز إذا كان يعمل مع البنكرياس الصحي أو الأورام في مرحله مبكرة. تقارير عن استخراج خلايا الاقنيه البنكرياس صحية استخدام تركيزات اقل بكثير34. وهناك درجه عاليه من الموت الخلايا الظهاريه المتوقع خلال الهضم; ومع ذلك ، يجب ان تتسامح الخلايا المناعية العملية جيدا. توجد طرق بديله لعزل الخلايا الظهاريه القابلة للحياة للنمو العضوي35 أو للحفاظ علي الانسجه المعمارية36.
ويمكن اجراء تعديلات علي بروتوكول التحفيز بسهوله ، اعتمادا علي القراءة المطلوبة والخلية المناعية تحليلها (علي سبيل المثال ، الضامة أو الخلايا B). استخدام الكواشف عموم التحفيز نقدا/ionomycin لا يميز لتحديد TCR-antigen ، مما يجعلها مفيده عندما لا يعرف مستضد. ومع ذلك ، يرتبط إنتاج ifnɣ بشكل وثيق مع المشاركة TCR37 وكل ifnɣ وإنتاج tnfα حاسمه في الاستجابات روبوطيه pdac38. يعكس التحفيز الكهربي الكهربي/ionomycin القدرة القصوى للخلايا التائية لإنتاج السايتوكينات ، والتي قد تنتجها خلايا T داخل البيئة المجهرية للورم. ويمكن قياس الإنتاج الذاتي دون الحاجة إلى التحفيز ؛ ومع ذلك ، قد تكون مستويات اقل بكثير أو غير قابل للكشف. هناك طرق بديله لتحفيز الخلايا T: المضادة لCD3/28-الخرز المغلفة ، والتي لا تتطلب أيضا مستضد أو في الواقع غيرها من الخلايا المناعية السكان. والفائدة من هذه الطريقة هي السماح بالقياس الكمي لإنتاج السايسيسين بواسطة مجموعات فرعيه معينه من خلايا T دون الحاجة إلى أساليب الفصل. علامات أخرى من السمية الخلوية (granzyme ب و تثقيب A) ، والنشاط (IL-2) أو كبت المناعة (آيل-10) يمكن أيضا ان تضاف21. ومع ذلك ، لا تتوفر الأجسام المضادة عاليه الجودة لقياس التدفق الخلوي للكشف عن جميع السايتوكينات والعوامل ذات الاهميه. ولذلك ، إذا كانت هناك تطبيقات أخرى مثل اليسا المطلوبة التحفيز يمكن ان يؤديها دون ادراج brefeldin A/مونينسين ، مما يسمح بإطلاق السايسيسين في supernatant. ومع ذلك ، من الجدير بالذكر ان هذا سيسمح بالإفراج عن الخلية الكلية ولن يكون من الممكن تحديد اي من الخلايا المساهمة.
Ifnγ الإنتاج هو السمة المهيمنة لاستجابه الخلية T انتيتورال ، وغالبا ما تستخدم كبديل للاعتراف الاعتراف مستضد37،38. الأخرى في الكائنات المجرية التي تحدد بدقه أكثر الاستجابات الخاصة antigen استخدام الخلايا السرطانية التعبير عن مستضد معروفه ، مثل اوفالبومين أو SV40. يمكن بعد ذلك استخدام مستضد العالمية السابقة المجرية لاختبار التعرف علي الخلايا T أو في تركيبه مع الماوس المضيف المقيدة TCR. بدلا من ذلك ، حيث مستضد غير معروف ، يمكن اجراء القياس الكمي من التوسع الخلوية T بواسطة التسلسل tcr السائبة ، أو أكثر مؤخرا أحاديه الخلية التسلسل tcr39،40. لفهم تماما حاله استجابه الخلية T داخل الفم, علامات تدل علي الإرهاق أو مستقبلات المثبطة وينبغي أيضا ان تقاس بما في ذلك: CTLA-4, PD-1, تاخر-3, TIM3, 2B4. فضلا عن علامات الخلايا T المستجيب (CD44hi, CD62lo) والنشاط التكاثري, Ki67 + أو csfe التخفيف41,42,43,44. وعموما ، فان نموذج الهجاء يوفر منصة مفيده لاختبار الاستراتيجيات العلاجية بسرعة ، ولا سيما التي قد تعدل استجابه الخلايا التائية المضادة للفم ، والتي يمكن التحقق منها بعد ذلك علي مجموعه أصغر من المعدلة وراثيا ، الفيلق ، الفئران.
Disclosures
وليس لدي المؤلفين ما يفصحون عنه.
Acknowledgements
ونود ان نشكر دائره الفنيين الحيوانيين والدكتور الزبيتا تالاروفيتشي (معهد بارتس للسرطان ، جامعه الملكة ماري في لندن ، لندن ، المملكة المتحدة) علي مساعدتهم خلال جراحه العظام. ونود أيضا ان نشكر الدكتورة جنيفر مورتون (معهد بيرسون لبحوث السرطان ، غلاسكو ، المملكة المتحدة) لتوجيهها في التقنية الجراحية ، الدكتورة كريستينا غيللي (معهد بارتس للسرطان ، جامعه الملكة ماري في لندن ، لندن ، المملكة المتحدة) لنصيحها بشان هضم الأورام والدكتور فأبيان ماككلاهان (معهد بارتس للسرطان ، جامعه الملكة ماري في لندن ، لندن ، المملكة ونود أيضا ان نشكر مجلس البحوث الطبية ، وصندوق بحوث سرطان البنكرياس (PCFR) والعمل سرطان المبيض الذين مولوا هذا البحث.
Materials
| Name | Company | Catalog Number | Comments |
| 6/0 gauge coated vicryl absorbable sutures | Ethicon | W9500T | |
| 70 μm pore-size cell strainer | Fisher Scientific | 11597522 | |
| 9 mm Clay Adams clips | VetTech Solutions | IN015A | |
| anti-CD107a PE (clone 1D4B) | Biolegend | 121612 | 1:100 to culture media |
| anti-CD16/CD32 | BD Biosciences | 553142 | Use at final dilution 1:200 |
| anti-CD3 PerCP eFluor710 (clone 17A2) | Biolegend | 46-0032 | Use at final dilution 1:50 |
| anti-CD4 FITC (clone GK1.5) | eBioscience | 11-0041 | Use at final dilution 1:100 |
| anti-CD45 Brilliant Violet 605 (clone 30-F11) | Biolegend | 103140 | Use at final dilution 1:200 |
| anti-CD8 Brilliant Violet 421 (clone 53-6.7) | Biolegend | 100738 | Use at final dilution 1:100 |
| anti-IFN-gamma PE/Cy7 (clone XMG1.2) | Biolegend | 505826 | Use at final dilution 1:50 |
| anti-TNF-alpha Alexa Fluor 647 (clone MP6-X) | Biolegend | 506314 | Use at final dilution 1:50 |
| BD Matrigel Basement Membrane Matrix High Concentration | BD Biosciences | 354248 | Aliquot on ice and store in -20 °C |
| Bovine Serum Albumin (BSA) | Sigma-Aldrich | A4503 | |
| Cell Stimulation Cocktail (500x) (phorbol 12-myristate 13-acetate (PMA) and ionomycin) | eBioscience | 00-4970-03 | 1x Final concentration PMA 0.081 μM, ionomycin 1.34 μM |
| Clay Adams Autoclip Applier | VetTech Solutions | IN015B | |
| Clay Adams Autoclip remover | VetTech Solutions | IN015B | |
| Collagenase Type V from Clostridium histolyticum | Sigma-Aldrich | C9263 | 2 mg/mL in media |
| Dimethyl sulphoxide (DMSO) | Sigma-Aldrich | D2650-100mL | |
| DMEM High glucose (4.5 g/L) with L-Glutamine | PAA | E15-810 | |
| DNase (Deoxyribonuclease I from bovine pancreas Type II-S) stock 10 mg/mL in 0.15 M NaCl | Sigma-Aldrich | D4513 | Final concentration in digestion media 0.025 mg/mL |
| Fixable Viability Dye 506 (FVD506) | eBioscience | 65-0866 | Use at 1:200 in PBS |
| Foetal calf-serum (FCS) | GE Healthcare | A15-104 | 10% in RPMI |
| Hamilton syringe 700 series, 25 μL volume, 22s gauge needle bevel tip | Fisher Scientific | 10100332 | |
| Intracellular Fixation buffer and Intracellular Permeabilisation Buffer | eBioscience | 88-8824-00 | Dilute permeabilisation buffer to 1x in H2O |
| Penicillin/streptomycin | PAA | 15140122 | 100 units/mL Penicillin, 100 μg/mL Streptomycin |
| Protein transport inhibitor cocktail (500x) (brefeldin A and monesin) | eBioscience | 00-4980-03 | 1x Final concentration Brefeldin A 10.6 μM, monensin 2 μM |
| RPMI-1640 (containing 0.3 g/L Glutamine) | Sigma-Aldrich | R8758 | |
| Surgical Scalpel Blade No.10 | Swann-Morton | 0501 | |
| Trypsin-EDTA Solution 10x | Sigma-Aldrich | 594-18C | Trypsin (0.1%) EDTA (0.4%) final concentration |
| U-bottomed 96 microwell plate | VWR | 734-2080 | |
| Universal Cotton Tipped Applicators - 6 inch x 100 | Medisave | UN982 | |
| V-bottomed 96 microwell plate | VWR | 735-0184 |
References
- Siegel, R. L., Miller, K. D., Jemal, A. Cancer statistics. CA: A Cancer Journal for Clinicians. 68 (1), 7-30 (2018).
- Conroy, T., et al. Current standards and new innovative approaches for treatment of pancreatic cancer. European Journal of Cancer. 57, 10-22 (2016).
- Lee, J. W., Komar, C. A., Bengsch, F., Graham, K., Beatty, G. L. Genetically engineered mouse models of pancreatic cancer: The KPC model (LSL-KrasG12D/+;LSL-Trp53R172H/+;Pdx-1-Cre), its variants, and their application in immuno-oncology drug discovery. Current Protocols in Pharmacology. 2016, (2016).
- Tseng, W. W., et al. Development of an Orthotopic Model of Invasive Pancreatic Cancer in an Immunocompetent Murine Host. Clinical Cancer Research. 16 (14), 3684-3695 (2010).
- Majumder, K., et al. A Novel Immunocompetent Mouse Model of Pancreatic Cancer with Robust Stroma: a Valuable Tool for Preclinical Evaluation of New Therapies. Journal of Gastrointestinal Surgery. 20 (1), 53-65 (2016).
- Hingorani, S. R., et al. Trp53R172H and KrasG12D cooperate to promote chromosomal instability and widely metastatic pancreatic ductal adenocarcinoma in mice. Cancer Cell. 7 (5), 469-483 (2005).
- Herreros-Villanueva, M., Hijona, E., Cosme, A., Bujanda, L. Mouse models of pancreatic cancer. World Journal of Gastroenterology. 18 (12), 1286-1294 (2012).
- Witkiewicz, A. K., et al. Integrated Patient-Derived Models Delineate Individualized Therapeutic Vulnerabilities of Pancreatic Cancer. Cell Reports. , (2016).
- Nicolle, R., et al. Pancreatic Adenocarcinoma Therapeutic Targets Revealed by Tumor-Stroma Cross-Talk Analyses in Patient-Derived Xenografts. Cell Reports. , (2017).
- Spear, S., et al. Discrepancies in the Tumor Microenvironment of Spontaneous and Orthotopic Murine Models of Pancreatic Cancer Uncover a New Immunostimulatory Phenotype for B Cells. Frontiers in Immunology. 10, 542(2019).
- Zhu, Y., et al. CSF1/CSF1R blockade reprograms tumor-infiltrating macrophages and improves response to T-cell checkpoint immunotherapy in pancreatic cancer models. Cancer Research. , (2014).
- Lee, J. J., Huang, J., England, C. G., McNally, L. R., Frieboes, H. B. Predictive Modeling of In vivo Response to Gemcitabine in Pancreatic Cancer. PLoS Computational Biology. , (2013).
- Clark, C. E., et al. Dynamics of the Immune Reaction to Pancreatic Cancer from Inception to Invasion. Cancer Research. 67 (19), 9518-9527 (2007).
- Fukunaga, A., et al. CD8+ tumor-infiltrating lymphocytes together with CD4+ tumor-infiltrating lymphocytes and dendritic cells improve the prognosis of patients with pancreatic adenocarcinoma. Pancreas. 28 (1), 26-31 (2004).
- Tewari, N., et al. The presence of tumor-associated lymphocytes confers a good prognosis in pancreatic ductal adenocarcinoma: an immunohistochemical study of tissue microarrays. BMC Cancer. 13 (1), 436(2013).
- Royal, R. E., et al. Phase 2 Trial of Single Agent Ipilimumab (Anti-CTLA-4) for Locally Advanced or Metastatic Pancreatic Adenocarcinoma. Journal of Immunotherapy. 33 (8), 828-833 (2010).
- Brahmer, J. R., et al. Safety and Activity of Anti–PD-L1 Antibody in Patients with Advanced Cancer. New England Journal of Medicine. 366 (26), 2455-2465 (2012).
- Winograd, R., et al. Induction of T-cell Immunity Overcomes Complete Resistance to PD-1 and CTLA-4 Blockade and Improves Survival in Pancreatic Carcinoma. Cancer Immunology Research. 3 (4), 399-411 (2015).
- Beatty, G. L., et al. CD40 Agonists Alter Tumor Stroma and Show Efficacy Against Pancreatic Carcinoma in Mice and Humans. Science. 331 (6024), 1612-1616 (2011).
- Lutz, E. R., et al. Immunotherapy converts nonimmunogenic pancreatic tumors into immunogenic foci of immune regulation. Cancer Immunology Research. 2 (7), 616-631 (2014).
- Barry, M., Bleackley, R. C. Cytotoxic T lymphocytes: all roads lead to death. Nature Reviews. Immunology. 2 (6), 401-409 (2002).
- Mojic, M., Takeda, K., Hayakawa, Y. The dark side of IFN-γ: Its role in promoting cancer immunoevasion. International Journal of Molecular Sciences. , (2018).
- Castro, F., Cardoso, A. P., Gonçalves, R. M., Serre, K., Oliveira, M. J. Interferon-gamma at the crossroads of tumor immune surveillance or evasion. Frontiers in Immunology. , (2018).
- Thiery, J., et al. Perforin pores in the endosomal membrane trigger the release of endocytosed granzyme B into the cytosol of target cells. Nature Immunology. , (2011).
- Betts, M. R., et al. Sensitive and viable identification of antigen-specific CD8+ T cells by a flow cytometric assay for degranulation. Journal of Immunological Methods. 281 (1-2), 65-78 (2003).
- Schuerwegh, A. J., De Clerck, L. S., Bridts, C. H., Stevens, W. J. Comparison of intracellular cytokine production with extracellular cytokine levels using two flow cytometric techniques. Cytometry. 55 (1), 52-58 (2003).
- Partecke, L. I., et al. A syngeneic orthotopic murine model of pancreatic adenocarcinoma in the C57/BL6 mouse using the panc02 and 6606PDA cell lines. European Surgical Research. , (2011).
- An, X., et al. Immunophenotyping of Orthotopic Homograft (Syngeneic) of Murine Primary KPC Pancreatic Ductal Adenocarcinoma by Flow Cytometry. Journal of Visualized Experiments. (140), (2018).
- Jiang, Y. J., et al. Establishment of an orthotopic pancreatic cancer mouse model: Cells suspended and injected in Matrigel. World Journal of Gastroenterology. , (2014).
- Autengruber, A., Gereke, M., Hansen, G., Hennig, C., Bruder, D. Impact of enzymatic tissue disintegration on the level of surface molecule expression and immune cell function. European Journal of Microbiology & Immunology. 2 (2), 112-120 (2012).
- Trapecar, M., et al. An Optimized and Validated Method for Isolation and Characterization of Lymphocytes from HIV+ Human Gut Biopsies. AIDS Research and Human Retroviruses. , (2017).
- Liu, Q., et al. Effects of enzymatic digestion, cell culture and preservation conditions on surface CD62L expression of primary murine CD3+CD4+T cells. Biomedical Research (India). 29 (10), 2153-2159 (2018).
- Seaman, S. A., Tannan, S. C., Cao, Y., Peirce, S. M., Lin, K. Y. Differential effects of processing time and duration of collagenase digestion on human and murine fat grafts. Plastic and Reconstructive Surgery. , (2015).
- Huch, M., et al. Unlimited in vitro expansion of adult bi-potent pancreas progenitors through the Lgr5/R-spondin axis. EMBO Journal. , (2013).
- Boj, S. F., et al. Organoid models of human and mouse ductal pancreatic cancer. Cell. , (2015).
- Misra, S., et al. Ex vivo organotypic culture system of precision-cut slices of human pancreatic ductal adenocarcinoma. Scientific Reports. , (2019).
- Moran, A. E., Polesso, F., Weinberg, A. D. Immunotherapy Expands and Maintains the Function of High-Affinity Tumor-Infiltrating CD8 T Cells In Situ. The Journal of Immunology. , (2016).
- Stromnes, I. M., et al. T Cells Engineered against a Native Antigen Can Surmount Immunologic and Physical Barriers to Treat Pancreatic Ductal Adenocarcinoma. Cancer Cell. , (2015).
- Singh, M., et al. High-throughput targeted long-read single cell sequencing reveals the clonal and transcriptional landscape of lymphocytes. Nature Communications. 10 (1), 3120(2019).
- Jiang, N., Schonnesen, A. A., Ma, K. Y. Opinion Ushering in Integrated T Cell Repertoire Profiling in Cancer. Trends in Cancer. 5, 85-94 (2019).
- Schietinger, A., et al. Tumor-Specific T Cell Dysfunction Is a Dynamic Antigen-Driven Differentiation Program Initiated Early during Tumorigenesis. Immunity. 45 (2), 389-401 (2016).
- Raghav, S. K., et al. Exhaustion of tumor-specific CD8+ T cells in metastases from melanoma patients. Journal of Clinical Investigation. , (2011).
- Gros, A., et al. PD-1 identifies the patient-specific in filtrating human tumors. The Journal of Clinical Investigation. , (2014).
- Miller, B. C., et al. Subsets of exhausted CD8 + T cells differentially mediate tumor control and respond to checkpoint blockade. Nature Immunology. , (2019).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved