Method Article
可筛选的
摘要
A protocol is described for in vivo detection of effects of mitochondrial inhibitors in the model organism Caenorhabditis elegans and for identification of potential enhancing compounds. This protocol can be used to screen drug libraries for compounds modulating mitochondrial function.
摘要
The multicellular model organism Caenorhabditis elegans is a small nematode of approximately 1 mm in size in adulthood that is genetically and experimentally tractable. It is economical and easy to culture and dispense in liquid medium which makes it well suited for medium-throughput screening. We have previously validated the use of transgenic luciferase expressing C. elegans strains to provide rapid in vivo assessment of the nematode’s ATP levels.1-3 Here we present the required materials and procedure to carry out bioassays with the bioluminescent C. elegans strains PE254 or PE255 (or any of their derivative strains). The protocol allows for in vivo detection of sublethal effects of drugs that may identify mitochondrial toxicity, as well as for in vivo detection of potential beneficial drug effects. Representative results are provided for the chemicals paraquat, rotenone, oxaloacetate and for four firefly luciferase inhibitory compounds. The methodology can be scaled up to provide a platform for screening drug libraries for compounds capable of modulating mitochondrial function. Pre-clinical evaluation of drug toxicity is often carried out on immortalized cancerous human cell lines which derive ATP mostly from glycolysis and are often tolerant of mitochondrial toxicants.4,5 In contrast, C. elegans depends on oxidative phosphorylation to sustain development into adulthood, drawing a parallel with humans and providing a unique opportunity for compound evaluation in the physiological context of a whole live multicellular organism.
引言
此过程的总体目的是C的能量状态的快速定量线虫体内 ,以便将其用作在化合物筛选的端点。 该原理是基于萤火虫荧光素酶的线虫C的转基因表达通过质粒pSLGCV(1 线虫 1-3 https://www.addgene.org/49862)。萤光素酶融合到绿色荧光蛋白GFP和组成性和广泛表达在细胞质(除去荧光素酶的过氧化物酶体靶向信号)。这导致发光时所述底物萤光素是外源提供。作为蜗杆是透明的,光可在光度计的相对光单位(RLU)测量。细胞内ATP燃料的生物发光反应及其可用性决定产生的光的水平。因此,发光法提供了一个convenient表示评估相对ATP水平,并推而广之线粒体功能,因为ATP的产生主要发生在线粒体。线粒体功能和生物发光水平之间的联系之前已证实通过线粒体电子传递链的基因和随之而来的降低光输出的沉默。1
产生被指定为PE254(feIs4)的生物发光菌和 PE255(feIs5)1(见材料清单),并且可以互换使用。3许多研究已经利用这些传感器株对细胞ATP水平在体内暴露于各种生物外源性化学品如叠氮化钠1,镉2,污水以报告泥状提取物3,5'-氟-2-脱氧尿苷6,和一烟草特异性亚硝胺7。该菌株还可以用来监控风险的影响紫外线C辐射 8,破坏线粒体呼吸链功能的影响。1,9表达的荧光素酶基因没有GFP融合(PE39)发光传感器的早期版本也已在一个呼吸的重金属影响的调查和使用。解耦联10株 PE254和PE255携带荧光素酶:GFP融合和GFP荧光显示与线虫的质量比例增加,提供了一个方便的手段发光值正常化6,9每孔虫的差量的效果也可以。通过包括在测定中(至少每条件5个孔)的多个技术重复考虑。3
该协议提供在体内监测能级的可能性(而不是技术上更费力体外 ATP的测定)使化合物筛选和重新定位在一整亩的生理上下文lticellular有机体。该过程可以扩展到多种遗传背景由横过染色体整合转基因导入可用的突变株和/或通过基因沉默RNA干扰的;因此,充分利用C的线虫作为模式生物。该方法将有助于减少候选药物的后期衰竭的线粒体毒性,并朝着更高的减少动物试验的贡献。
研究方案
注:执行无菌条件下(层流柜),并与预消毒材料的所有步骤(高压灭菌126℃,11分钟)。的LB板划线E.大肠杆菌 OP50保持在4℃下每月是必需的,条纹出到新鲜LB平板和restreak。
1.细菌性食物( 大肠杆菌 OP50)准备
- 每日1接种2×5毫升的LB在两个万向瓶与 E的单个菌落大肠杆菌 OP50和发生在8小时振荡培养箱在37℃(220转)。
- 经过8小时培养,使用2毫升E的大肠杆菌 OP50 LB培养基接种每个3×200毫升LB。在振荡培养箱代替烧瓶(220转)O / N(17小时)在37℃下。
- 重20×50毫升离心管中,在管写重量。
- 第2天使用血清吸管,分装将30ml O / N E.大肠杆菌 OP50文化到预称重的离心管中。离心机在7741 x克,10℃,8分钟。
- 小心地倒出上清液,跟上盖子倒筒,并留下静置几分钟。使用移液管除去可能聚集在盖任何过量上清液。称重该管和计算粒料的重量。
- 计算需要提供30克/升的悬浮液,并标记在管本音量。日期,标签和地点管在-20℃下用1-3个月内或在 - 80℃下,如果存储用于超过3个月。
- 准备菌悬液种植线虫;允许细菌沉淀解冻出并添加的S所需的体积完全培养基11,12到每个管中,涡流轻轻重悬沉淀,不同管的池内容以获得所需的体积。在无菌条件下工作。
在96孔板2.准备药品标准
注意:如果使用的是药品库,药板在一个单一的提供在DMSO化合物的浓度。初级筛选将在单一浓度测试化合物。说明如下准备药物板确证化合物测试的范围0-160微米之间的浓度,在10μM之后统计学意义选择。下面的步骤可以适于测试其他浓度。
注意!按照必要的预防措施来处理药物(一般口罩,护目镜,手套是必需的)。
- 准备药板工作确证筛选标准:称取所需化合物的量到无菌1.7毫升离心管中,在DMSO准备16毫米化合物( 即 100倍浓缩相对于所需的最高浓度曝光)。
- 串联稀释16 1mM储备1:2于DMSO中,得到8,4,2,1,0.5和0.25毫标准(在无菌条件)。这是100倍浓缩,将稀释到终浓度为0(仅适用于车辆),2.5,5,10,20,40,80和160微米(在1%DMSO中)的药物暴露期间。
- 在层流柜,放置每化合物的标准以及20-50微升96孔板的一柱内,例如板位置A1:16毫米,B1:8毫米,C1:4毫米,D1:2毫米, E1:1mM的,F1:0.5mM的,G1:0.25mM的药和H1:DMSO中。使用不同的列稀释系列不同的药物。
- 分装到车辆中的药物板12列的孔中。
注意:这将有助于车辆控制下来除了沿H行的测试柱测试,确保车辆在整个板的位置代表测试。
注意:每种药物板确证筛选保持稀释系列,最多11种不同的药物进行测试加上车辆控制。 - 标签和密封板,盖上箔和地点在-20℃直到需要。
3.线虫实验
注:执行所有步骤ü升气管无菌条件下,在无菌条件下,用预先灭菌的材料和试剂。维护C.线虫菌株通常对NGM板与 E. 在表1中提供的大肠杆菌 OP50。12按建议定时的不同的协议的步骤。
- 第1天的任务:建立生物传感器应变液体培养后续同步。
- 拿起从一个6厘米NGM板线虫(用大量低龄幼虫的食物的地方刚刚用完)在2毫升氏完全并转移到瓶中,30g / L的E.大肠杆菌 OP50 S中完成(总体积30 ml,在250毫升容量的锥形玻璃烧瓶中)。孵育3天20℃,160转。
- 第4天的任务(允许大约30-35分钟):漂白文化丰年虫卵和同步蠕虫人口。进行所有离心步骤1分钟,600×g的。
- 准备漂白剂溶液使用前:每个加入16毫升0.156中号KOH / NaOH的加入4毫升漂白剂。
- 倒入2×14毫升蠕虫文化分为15毫升锥形离心管中。让蠕虫通过重力(3分钟)来解决。卸下并丢弃液体上方落户线虫。添加5毫升漂白溶液至每个管并启动计时器。合并卷进一管。
- 反转管轻轻地,持续2分钟,检查下立视蠕虫的破坏和卵子的释放到悬挂。当大多数蛋被释放或以2分钟,在漂白溶液,离心机的最大时间。
- 小心取出上清液。与14毫升氏完全离心洗涤沉淀1倍。
- 弃去上清液,加入10 mL的漂白粉溶液,并开始计时(本次漂白步骤确保大部分的蠕虫尸体分解,并在体视不再可见)。后在2分钟,离心漂白溶液的最大时间。
- 洗颗粒3X S中完成,轻轻倒出上清液,重悬沉淀于14ml■每个离心后完成。最后一次洗涤后,重悬卵沉淀于14ml小号Çomplete。
- 卷转移到锥形玻璃烧瓶。孵育18-24小时,在20℃,160转。
注:收获卵孵化O / N和逮捕发展的第一龄幼虫(L1),由于缺少食物,因此他们都将在相同的增长阶段。
- 第5天的任务:建立同步虫文化进行药物试验。
注:蠕虫悬浮在饥饿培养基倾向于粘附到疏水塑料表面如枪头和管。 0.01%吐温20是这里用于呈现塑料表面更具亲水性,并允许在数量更大的准确性(0.01%的Triton-X100,也可以使用)的表面活性剂。当线虫是细菌补充的培养基,他们不倾向于坚持塑料。- 确定的阴影L1的号码烧瓶,烧瓶保持在抖动的平台(160 RPM)。
- 以3倍的100微升样本瓶(使用干净的尖端每次)为单独1.7毫升小管与900微升液态间edium 0.01%吐温-20。
注:卓望100微升样品放入干净的尖端只有一次。然后配药时,吸管上下几次到吐温补充的培养基释放秉承尖端的任何蠕虫。 - 从各一式三份稀释管数的4倍的10微升液滴的线虫。计算平均值和估算存在于锥形玻璃烧瓶蠕虫数目。
- 以3倍的100微升样本瓶(使用干净的尖端每次)为单独1.7毫升小管与900微升液态间edium 0.01%吐温-20。
- 计算设置一个2×20毫升培养,每10微升10线虫所需孵出线虫悬浮液的体积。增加计算的体积减少10%,占在离心步骤一些后续线虫损失。
- 需要倒出体积为2×15 ml的离心管(预称重)。称取管,以获得实际体积分配,涡轻轻地调整以去除多余的量与5毫升吸管(只有无菌尖端应该进入管)到目标卷。
- 化妆量14毫升新鲜氏完全到了^ h线虫。离心(1分钟,600个克)。取出并弃上清小心不要打扰线虫沉淀。
- 加入5 ml的小号完整的用30g / L的大肠杆菌大肠杆菌 OP50来沉淀线虫。在每个管转移5 ml至含有15 ml的小号完全用30克/升大肠杆菌的锥形玻璃烧瓶大肠杆菌 OP50。记下时间线虫首次提供食物。
- 摇瓶轻轻(160转),取9×10微升液滴到显微镜载玻片(使用新的提示,每次)来计算线虫并确认平均约10(±2)每10微升。
- 放置线虫烧瓶中在20℃,160转42-44小时振荡培养箱。
- 确定的阴影L1的号码烧瓶,烧瓶保持在抖动的平台(160 RPM)。
- 第7天的任务:传输线虫到96孔板,并开始药物暴露。
- 结合线虫培养成单个烧瓶,保持轻轻摇动烧瓶,并放置在一个60毫升无菌槽3×4 ml的线虫培养物。将槽用颤抖的平台(160转)上。
- 使用8瓒道移液器分装每96孔黑色微量滴定板以及25微升悬浮线虫有一台透明底(于同时发光,荧光读数;或白酒板块的发光只)。盖上盒盖板并预留。
- 设置每2板后起来,放置另一个2×2.5毫升线虫低谷,以取代失去的体积(保持一个"死区"在大约7毫升槽)。
- 设置13/14板的线虫。 11线虫板将要求测试两个96孔药物板。 第 12届线虫板将专门用车辆作为控制加载。 第 13板将被用于建立在第8天的背景荧光(见下文)。一个额外的板可以使用过程中建立了应该出现的失误有所准备。
- 等分试样74微升的S完整到各孔并置于板在潮湿室(见材料清单)在振荡培养箱(20℃,160转)UNT金正日准备等分测试化合物在预选发育时间( 例如,45小时30分钟的食物提供后)。 [每孔音量现在是99微升。
- 解冻药板(县)的测试。
- 使用多道移液器设置线虫板的药物,每次更换提示。允许每个96孔板5分钟为等分的药物。
- 取1微升毒品板的1列,并加入到列1-5含有线虫板;从在药板2次列重复成列含有线虫的板8-12。加入1μl车辆的向列6和线虫板7。
注:在线虫板每孔的总体积为100微升产生了1:100的稀释化合物/车辆。 - 加入1微升药物板的列的第三 / 第四列的重复处理中的第二线虫板的1-5 / 8-12;加车辆的列6和线虫板7。
- 继续测试剩下的药板列。从药板12列采样设置最少一个线虫板与车辆的所有井。代替板背部在振荡培养箱(20℃,160 rpm)离心20-22小时潮湿室(见注8天)。
- 取1微升毒品板的1列,并加入到列1-5含有线虫板;从在药板2次列重复成列含有线虫的板8-12。加入1μl车辆的向列6和线虫板7。
- 部分准备次日发光缓冲液:添加的DMSO和10%的Triton-X-100至S的所需体积完整,得到1%DMSO和0.15%的Triton X-100。允许每盘读取5毫升的发光,加1毫升吸光度计喷油器。
- 第8天的任务:阅读实验终点 - 荧光和生物发光。 (GFP荧光读数推荐为正常化生物发光数据的装置。)
注意:目的由66-67小时后提供给线虫,以防止所述的实验条件下,显著后代生产食品读端点。- 设置板作为背景对照的GFP读数使用。 Combine孔内容从13日板入15ml管中。允许线虫定居(2-3分钟)。使用上清液加载微孔板(黑色透明底)用100μl细菌悬浮液,每孔。
- 观察镜记下油井中的线虫可以看到在后台控制板。从随后的数据分析中使用的背景估计排除这些。
- 读荧光每个96孔板的,包括背景对照。 (设置:光学的盘底;过滤器485/20激发;二十〇分之五百二十八发射。)
- 准备缓冲器为发光读数:添加荧光素(20毫米)到部分制备缓冲液(来自前一天),以获得发光缓冲用1%的DMSO(1×),0.15%的Triton-X100(3×)和0.3mM的荧光素(3× )。素光度计注射器6倍与150微升缓冲发光。
- 上一步假定药物暴露中的1%DMSO作为溶媒。当载体是水,调节共的DMSO ncentration在发光缓冲至3%(即,3×)。
- 有一个板块在同一时间的工作。每孔分配50微升的发光缓冲区。 (井150微升最终体积的3倍稀释的发光缓冲液:1%DMSO,0.05%的Triton-X100和0.1毫米荧光素终浓度)将立即在抖动的平台,并开始计时。
- 经过对抖动的平台(160 RPM)3分钟,阅读发光(每测量1秒)。
- 设置板作为背景对照的GFP读数使用。 Combine孔内容从13日板入15ml管中。允许线虫定居(2-3分钟)。使用上清液加载微孔板(黑色透明底)用100μl细菌悬浮液,每孔。
4.数据分析
- 减去平均GFP的背景荧光从结果看。由各自的GFP阅读鸿沟生物发光。
- 当检测到用于暴露于化合物线虫高GFP值,测量其自身的化合物的荧光以考虑任何化合物荧光。如果高于平均水平,以此为背景来代替。
- 快递生物发光,GFP生物发光归一第二GFP荧光数据如在各板的车辆控制的平均值的百分比。
- 画出的平均值和错误酒吧的每个浓度。
- 试验使用2-单向方差分析(ANOVA)分析与"浓度","实验"和它们的相互作用的效果显着性(每个数据点是指一种单一的孔),并使用Dunnett检验作为事后测试(与。车辆控制)。
注意:如果"试验"或"互动"的条件是显著,进一步的实验可能需要确认的响应。其中,实验之间没有可变性是从观测数据图的明显看出,一个单向ANOVA可以从独立的实验汇总的数据来执行。- 对于板(S),只有车辆的统计分析,选择在列6-7的所有井和行H作为对照组,所有的孔(这是复合测试期间定期分配给车辆的位置)。
结果
代表性的结果说明了该方法,得到为鱼藤酮(图1),百草枯(图2),草酰乙酸(图3),和4的化合物的药物库13(图4)的筛选过程中被拾起如萤火虫荧光素酶抑制剂。该药物暴露开始的L4期在所有情况下,但百草枯曝光实验开始在41小时后的食品,首先提供给线虫相比45-46小时为其它化合物。该协议允许一定程度的灵活性的时间的选择对药物暴露的开始和曝光的长度。然而,对于筛选目的,设置时间应粘合到经选定,用于实验的重复性。端点应该由66-67小时发育时间,以防止大量的产蛋和在井孵化后代来测量。 T中提供了指导方针计时能够1。
鱼藤酮,线粒体复合物I抑制剂,都相对较短的(2小时)和更长时间的曝光(24小时),浓度范围内(图1)后降低生物发光。在这种情况下,没有GFP测量是,但所用的技术重复数(n = 6)足以拉平在小井 3之间蠕虫数目的任何差异。 24小时的曝光时间窗口在其线虫生长,发展较慢的复合物I抑制的结果预计将有助于生物发光的下降。这通过肉眼观察下与体视看到的,特别是在20μM和上述浓度延迟发展确定;除了一些杀伤力从40微米注意到(没有量化定性观察)。没有杀伤力后2小时暴露观察到,但在蜗杆的运动效果进行观察。急剧下降的相对生物发光来控制通讯中断时间rred在鱼藤酮的最低测试浓度为2.5μM,对此影响进行了不容易被快速目视观察在2小时曝光检测。这种下降的生物发光是降低细胞内ATP是一致的。最大抑制,用鱼藤酮的使用的最低浓度(2.5μM),表明特异性靶向鱼藤酮的任何随后的实验,应进行0和5μM〔浓度范围0-160微米之间达到被选定为与其它药物的比较部初步确定为具有10微米显著的影响(在其他地方出版)。
除草剂百草枯影响通过活性氧增加线粒体功能。在这里,我们展示了对C 的生物发光的影响暴露于浓度范围内进行24小时(图2)的后线虫菌株PE254。由于该菌株携带吕克:: GFP融合 ,绿色荧光是ALSø测量为正常化的手段。6,9-百草枯显著降低生物发光,GFP荧光和生物发光规格化。在邓尼特事后检验表明,百草枯与相对于车辆控制显著差异的浓度分别为4和8毫米的生物发光和生物发光标准化,以及2mM的用于归一化的生物发光。唯一的浓度显著降低GFP荧光是8mM,浓度使得增长效应和偶尔的死虫,看到(定性观察)。生物发光(和规范化的生物发光)的下降幅度大于荧光,符合降低线粒体功能和ATP的产生的影响。
柠檬酸循环中间体草酰乙酸对C.测试线虫应变PE254在8mM的单一浓度,导致增加在生物发光(图3)。没有GFP发出荧光NCE测量得到的或额外的视觉观察进行;然而这种响应于单一浓度值得进一步确证暴露在浓度范围,和效果更详细的观察。生物发光的由该化合物的增强并不奇怪,因为它可以被假定为导致三羧酸循环的更大的活性,以最终更大产生ATP(然而这将是可取通过评估GFP荧光来控制对荧光素酶水平的任何影响在随后的实验)。所示的草酰乙酸的数据集揭示响应见于萤光素酶基于实验变异性的程度。在我们的经验,这是变性测试系统的特别是用于较少有害的曝光条件的特征。
萤火虫荧光素酶抑制化合物DDD00001434,DDD0001477,DDD00000635和DDD00023047被看的PU作用的体外测试了rified酶和体内使用C.线虫吕克:GFP表达株。没有证据,任何测试的化合物的曝光条件下造成线虫死亡。所有4种化合物影响体外荧光素酶活性在2浓度下测试25和100微米(图4A)。 DDD00001434杀纯化荧光素酶的活性几乎完全,它提供了一个可信的理由的大幅下降在体内生物发光( 图4B)。虽然, 在体外和体内试验不可直接比较,响应于DDD00023047在两个测定相似。 DDD0001477和DDD00000635造成体内比体外有较大下降。这些化合物提供给活虫萤光素衬底22小时之前和结果可能反映它们不容易从荧光素酶的活性位点置换时萤光素成为阿瓦伊吊牌。或者,DDD0001477和DDD00000635可能对细胞ATP水平的附加效果。这必须由不涉及萤火虫萤光素酶的手段来评估。值得注意的是绿色荧光蛋白信号在暴露于复合DDD00000635活虫体的强烈增强。这将在下面讨论。
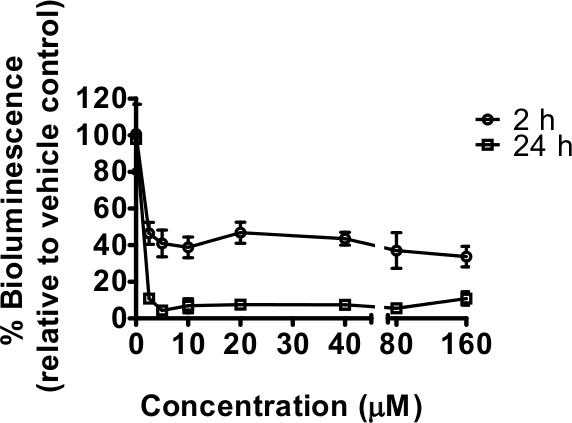
图1.线粒体复合物I抑制剂鱼藤酮降低C的能量状态线虫通过应变PE254的生物发光测定。同步L4期蠕虫暴露于0,2.5,5,10,20,40,80和160微米鱼藤酮在1%DMSO中进行2(提供给L1幼虫食物后45-46小时)小时(短)或24小时(长时间曝光)生物发光事先指数分别为48和69小时蠕虫的发展提供了食物之后。生物发光(单元相对光单位,RLU)表示为所述车辆(1%DMS的百分比O)值。误差线描绘的技术重复的SEM在各鱼藤酮浓度(N = 6)。所有测试浓度产生了相对于媒介物对照(P <0.001)一个高度统计学显著差异。
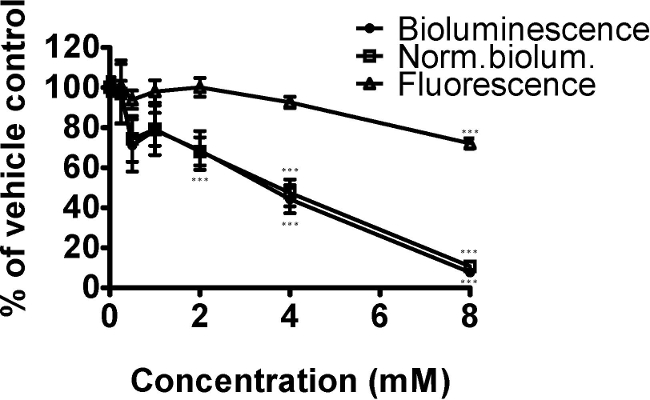
图2.氧化应激百草枯降低C的能量状态以浓度依赖性的方式线虫菌株PE254(由生物发光测定)。同步L4期蠕虫(为方便起见在此实例在提供到L1幼虫食物后41小时)暴露于0,0.25,0.5,1,2,4或8毫百草枯24小时。 GFP荧光(单位相对荧光单位,RFU)用于标准化生物发光数据(单位RLU),在65小时的发展得到两个端点。数据表示为对照的百分比(1%DMSO)中。误差线描绘的技术复制SEM(5例不同浓度; N = 18,用于控制)。单向ANOVA:*** P <0.001相对于车辆控制。
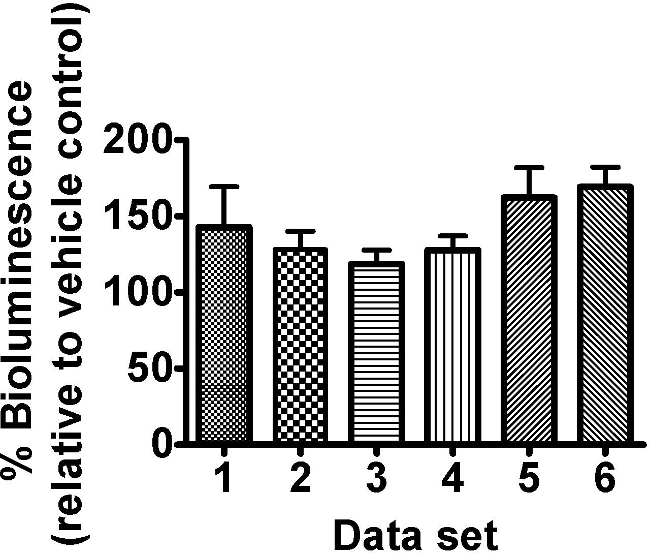
图3.三羧酸循环中间体草酰乙酸(8毫米)增强C的生物发光线虫株PE254。同步L4阶段蠕虫(提供给L1幼虫食后45-46小时)暴露于新鲜配制的8毫米草酰乙酸18小时±30分钟。生物发光(单位RLU)读取在63.5小时±1小时的发育时间,并表示为车辆控制的百分比(DDH 2 O的)。不同列代表的相同实验内分配给不同的96孔板8技术重复不同的数据集。误差线描绘的技术复制SEM(N = 8)。 2路方差分析与'设置'和'集中'的因素:̵6,设置'P> 0.05,'集中'P <0.001和交互项P> 0.05。
一个 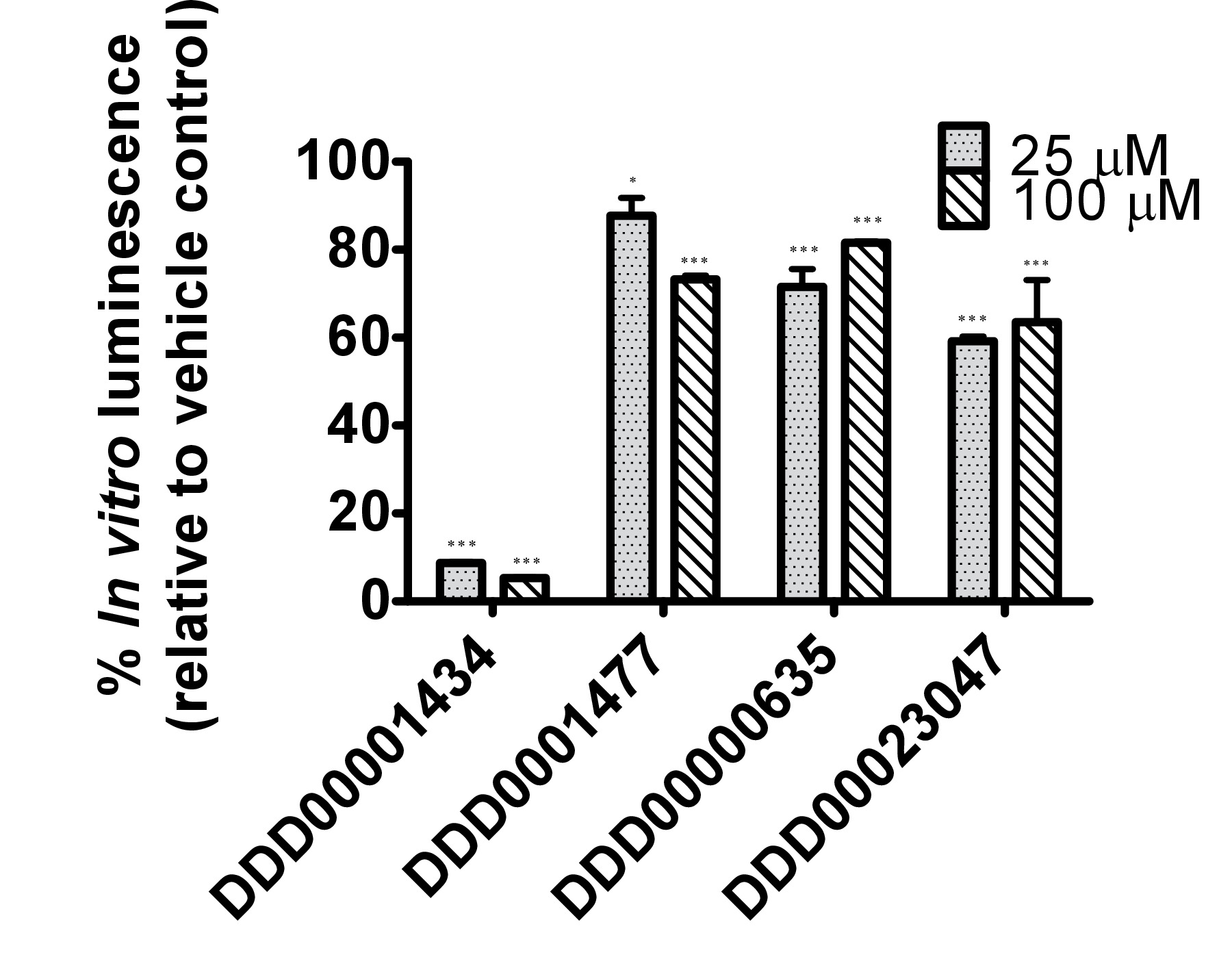
乙 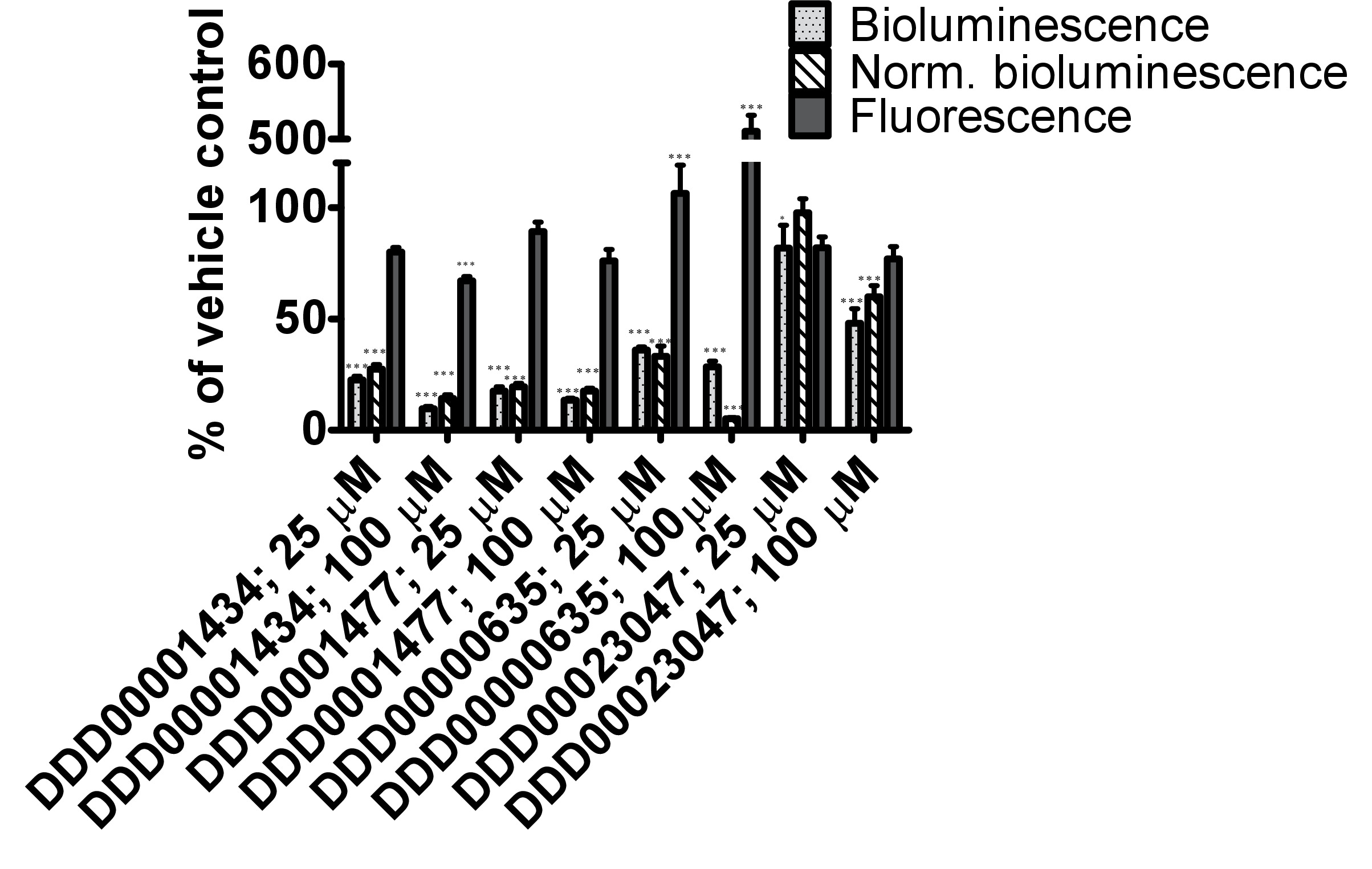
图4.测试从邓迪药物发现化合物库13反应4化合物(C1:DDD00001434,C2:DDD0001477,C3:DDD00000635和C4:DDD00023047)与萤火虫荧光素酶发光的已知抑制活性。上纯化的萤火虫萤光素酶的活性的化合物的(A)的效果(测量为光单位,RLU),表示为溶媒对照的百分比。 ATP的生物发光CLSII试剂盒(Roche,曼海姆,德国)根据与萤光素酶的等分至孔中(白色96-瓦特相同量指令中使用ELL酶标板)。 ATP的混合物在10微米和1μl化合物的最终浓度提供(最终浓度表示)或DMSO(1%)的溶液。发光信号进行了整合,持续10秒。误差线描绘的技术重复的SEM(N = 4)。分析:单向ANOVA; * P <0.05或*** P <0.001相对于车辆控制。 25和100微米之间的差异为C1(DDD00001434; P <0.001)高度显著,以及用于C2和C3显著(分别DDD0001477和DDD00000635; P <0.05)。(B)的生物发光的体内测量,生物发光归GFP荧光和C.对GFP荧光线虫应变PE254在67小时发育时间暴露于试验化合物22小时。误差线描绘的技术复制SEM(N = 8)。统计分析(单程-ANOVA)从3数据集(3 XN = 8)上进行汇集的数据。 * P <0.05或*** P <0.001相对于各自的载体对照。 Differen暴露于C4(DDD00023047)归一化的生物发光25至100μm只统计显著(P <0.05)之间的国际消费电子展。
| 一天中的时间 | 第1天 | 第2天 | 第3天 | 第4天 | 第5天 | 6天 | 7天 | 8天 |
| 9-10 | 第5步 | |||||||
| 10-11 | 第5步 | |||||||
| 11-12 | 第4步 | 第5步 | ||||||
| 12-13 | 第4步 | |||||||
| 13-14 | ||||||||
| 14-15 | ||||||||
| 15-16 | ||||||||
| 16-17 | 步骤1 | 第3步 | ||||||
| 17-18 | ||||||||
| 18-19 | 第2步 |
表1的协议步骤概述要进行对线虫实验每天(第3节),并建议定时。
讨论
该模式生物C.线虫提供了强大的实验系统。这是很容易文化(通过对L4通过少年幼体阶段L1)会产生大量基因完全相同的后代有3.5一天的生活周期,从卵到成虫复制。由于其尺寸小,它可以方便地生长在96孔板中,促进化合物的筛选。我们提出了基于C的菌株表型筛选协议线虫充当能量水平的体内传感器14的协议适用于任何实验室,尽管96-孔平板光度计和无菌柜是必需的。重要的是要防止污染的试验用良好的实验室技术是非常重要的。如果手动工作,线虫板的可实现的最大数量为13%的实验允许2×96孔药物平板上测试和其中包括两个车辆板。代表性结果呈现为线粒体复合物I抑制剂鱼藤酮即,超氧发生器百草枯,三羧酸循环中间体草酰乙酸和四种化合物与已知的萤火虫荧光素酶抑制活性。前两个化合物导致了生物发光的减少所预测,而草酰乙酸导致的增强,有可能从更大代的ATP引起的。草酰乙酸数据集还表明基于萤火虫荧光素酶作为记者在实验中的内在变化。至少三次独立实验是可取的确定的响应鲁棒性未知的化合物。
萤火虫萤光素酶活性的抑制是可识别的与使用商业试剂盒体外测定3化合物之一导致与抑制剂增加的水平相一致的大量增加的GFP荧光GFP标记萤火虫萤光素酶通过结合到荧光素酶的活性站点,并使其更稳定。15在某些情况下(未在这个特定的情况下),这可能导致生物发光的增加的水平时,抑制剂是通过过量的底物移动。15据,因此,重要的是不要错误地从与萤火虫酶相互作用的化合物解释结果减少或增加ATP水平/线粒体功能。变化的发光信号往往关联与健康的额外测量,如运动,发展,壮大。作为一个例子,一个化合物是一种可疑的萤光素酶抑制剂,如果检测在生物发光信号的大幅下降,但蠕虫是从通过显微镜观察对照没有区别。增加GFP荧光,而不是由生长或化合物自发荧光解释的,也可能指向的抑制剂。许多荧光素酶抑制剂15是已知的,并已进入PubChem数据库。因此,在一审中,这是很好的做法,以协商由PubChem数据库持有荧光素酶抑制剂的信息;接着吨与对由附加装置线粒体功能的影响纯化的酶3和/或确认中的体外测定该化合物的效果十分有趣的。16,17
GFP荧光测量使萤火虫荧光素酶水平的检测(和如上所述的一些荧光素酶抑制剂电位检测)作出强烈的情况下,用于测量该端点生物发光一起在可能的情况。生物发光读数的GFP正常化也占变化蠕虫数井之间(尽管这也可以通过包含多种技术重复实现)的一种手段。对于更高的灵敏度,重要的是从读数减去背景荧光是重要的。该协议评估菌悬液的背景荧光,但线虫自发荧光不占当前测定(限制,对于任何衰老STU特别重要的贡献,鉴于模具随着年龄的线虫的自体荧光增加)。试验化合物的自发荧光也应在平行评估。 GFP的正常化似乎是必须那里的研究人员希望适应协议来在不同的遗传突变体或沉默不同基因的后比较细胞ATP池,以控制在所述生物发光转基因的表达水平的任何应变差异。
在协议中的关键参数包括发育阶段在该曝光被启动,曝光的长度,并获得相同的数字在不同的井的线虫。曝光可以然而起始于线虫发育的任何阶段,L3阶段或以上是优选的。从这个阶段上,线虫依靠氧化磷酸化发展到成年,就证明了线粒体DNA含量,耗氧量和ATP水平非常显著增加。18,19,20本协议启动博览会URE在L4阶段。其原因仅在此阶段等分线虫到96孔板(而不是当它们首次提供食物在L1阶段),就是虽然板被放置在潮湿的腔室,以使蒸发最小化,在一定程度的蒸发仍然出现在我们的摇床,看作是非常小的液滴上的盖子形成(这可能不是一个问题与其他摇动孵化器)。通过等分线虫板只是加入药品标准之前,实际的药物浓度不会由于蒸发受任何体积变化小。装载线虫板与车辆仅是有用的检查线虫井之间均匀分布。发现车辆唯一板的任何显著差异将指示差技术在分配线虫井。
曝光的长度是一个重要的考虑因素。如果自主增长的能源状况的影响感兴趣,亲母育酚可以被修改,以适应较短的曝光(从几乎立即响应,例如,2小时)。另一方面,条目化合物为C.线虫的组织可能需要一些时间。例如12-24小时便可实现白藜芦醇和5-氟-2'-脱氧尿苷(FUDR)的最大内部的浓度。21因此,更长的曝光时间(18到24小时)可以是合理的以最大化暴露水平。曝光时间应限制在次不允许显著再现水平发生在井中。我们建议,线虫的总发育时间保持在66-67小时。虽然方便,线虫是通过再妊娠,并已开始egglaying。然而,我们发现从鸡蛋制备的生物发光读数是微不足道的(未示出)。的河畔5启动子驱动的转基因表达在最初检测只有两个两个,受精在100细胞阶段22和 ℃后一个半小时hitinous蛋壳是可能限制荧光素的条目。其他人已经发现,含胚卵不显著到妊娠成年人的代谢作出贡献。23然而,条件允许显著后代生产要避免。如果愿意,实验时间尺度可以移回:我们先前已经开始暴露在后期L3幼虫阶段(36小时)的环境毒素,并进行了生物发光和GFP测量,在55 小时 2另外,遗传背景是条件不育。可以用来防止后代生产,如例如所述FER-15(B16)二 ; FEM-1(hc17)四双它可以保持在15℃的突变体,但是无菌的,在25℃。24,使用FUDR以诱发无菌性不推荐,因为这可以在本身影响线虫的代谢。25的测定法,可以也可以在菌株更具渗透性表皮如失FUNCT部分进行离子总线8突变体是多药敏感,由于增加药物的渗透性。26这将有利于缩短接触时间和较低的化合物浓度。添加荧光素对这些线虫的条件也需要调整,即,1%DMSO和0.05%的Triton-X100中的发光缓冲器可以不需要以增强荧光素可用性。
该协议使用1%DMSO作为溶媒为化合物递送。虽然不是致命的,二甲基亚砜该浓度有一定的生物效应,因为我们在以前的出版物已经讨论了3许多可用的药物库的在100%DMSO制备,在浓度稀释车辆后,就可以适用于基于细胞的测定到0.1%。更高的化合物浓度,需要以引发反应中C.线虫当与人体细胞,例如,它常常是不可能的,在低于1%的DMSO进行分析比较。再次,使用菌株与更渗透角质层会导致较低的车辆浓度测试。不建议DMSO高于1%的浓度。
前读数一套培养时间与荧光素应遵守。如前所示,发光到达其 第二分钟内最大的水平加入萤光素,保持相对稳定的前5分钟后,随后缓慢逐渐减少发光,在未来30分钟1。动力学响应于特定的化学物质可以在30分钟的荧光素的初始分配后的初始阶段中进行。
该协议涉及饥饿步骤之后收集卵来达到线虫群体的同步。我们建议线虫测试种群同步,因为不同的发育阶段的不同之处细胞ATP水平,并且可以在测试化合物不同的反应。通过进行S中完整的饥饿介质相对于M9,孵化率线虫设置有碳源(乙醇),使幼虫不发展,但并没有完全饿死。27,28还已经表明,被捕L1的被引为食物快速响应和普通的L1生长速率在3小时的食物变得可用之后实现的。29然而,它的可能性,即饥饿步骤可以改变C的代谢线虫不能排除。30为此饥饿的长度应不超过24小时(18小时是足够的同步)。某些实验室可具有使用COPAS Biosorter年龄同步完全绕过饥饿步骤的可能性。其他实验室可能偏爱(与OP50 NGM板)在固体培养基上扩大线虫群体之前,漂白(步骤3.1),这将很好地工作过。我们接触化合物作为一个标准的媒介线虫培养,在使用培养基however其他媒体可以选择,例如ķ介质或EPA适度硬水常常用于生态毒理学研究。31,32
该协议提供筛选,并确定在对线粒体功能的影响方面的候选人进行进一步测试的装置。在初步筛选的阶段很可能一些化合物将已经错过了由于只有一个浓度被测试,因此药物屏幕不应被视为穷举的。命中可通过使用技术评估线粒体功能的不同方面例如氧消耗,C被验证线虫菌株的表达GFP的线粒体,污渍对于线粒体膜电位和/或活性氧的测量。16,33,34的方法的最大意义是有一个装置,用于筛选大量的化合物和/或条件中的多细胞有机体水平,而且重要的是要能够采取的第优点C.电子商务基因可追踪性线虫来研究作用机制。这项技术可能有助于加速和寻找新的途径,以有趣的化合物和目标的发现。据设想,与人类疾病的化合物库中的疾病相关的上下文相关联的筛选遗传背景的传感器的组合将可提供许多好处。
披露声明
作者什么都没有透露
致谢
The authors would like to thank David Gray from the Dundee Drug discovery unit for kindly donating firefly luciferase inhibitory compounds DDD00001434, DDD0001477, DDD00000635 and DDD00023047; Tibor Harkani (Medical University of Vienna) for the suggestion of oxaloacetate as a test compound; and Charlie Dear (University of Aberdeen) for illustrations. This work was funded by a BBSRC Pathfinder award (BB/FOF/PF/4/11) and the University of Aberdeen.
材料
| Name | Company | Catalog Number | Comments |
| Orion II Microplate Luminometer | Berthold Detection Systems | with injector and the Simplicity 4.2 Software; transfer data to Excel at the end of plate measurement | |
| FLx800 fluorimeter | Biotek | with Gen5 Software; transfer data to Excel at the end of plate measurement | |
| Ks 130 basic shaking platform | Ika | #0002980000 | |
| Innova 4349 | New Brunswick Scientific | Refrigerated incubator shaker | |
| Eppendorf centrifuge 5804R | Eppendorf | with eppendorf rotor A-4-44 (for 50/15 ml tubes) | |
| Stripette, Costar | Corning | #4489 | Serological pipette |
| Cellstar 50 ml tubes | Greiner bio-one | #227661 | |
| Cellstar 15 ml tubes | Greiner bio-one | #188261 | |
| Cellstar 60 mm tissue culture plates | Greiner bio-one | #628160 | |
| Superfrost Microscope slides | VWR | #631-0909 | |
| Sterile spatula | Corning | #3007; #3004 | for weighing out chemicals |
| 0.22 mM Millex GP filters | Millipore | #SLGP033RS | |
| Axygen eppendorf tubes 1.5 ml | Fisher Scientific | #MCT-150-R | |
| Corning 96 well assay plate | VWR | #3603 | Black plate clear bottom with lid |
| Nunc 96 well assay plate | Fisher Scientific | #236105 | White plate with lid |
| Reservoir reagent 60 ml | Thermo Scientific Finnpipette | #9510027 | used as trough for nematodes in protocol section 4.4.1 |
| Storage box/damp chamber | Roche Diagnostics | #10 800 058 001 | 174 x 101 x 56.6 mm, used as a damp chamber with wet paper towels; 2x 96-well plates with lids can fit into one, the lower sitting on top of a microplate lid |
| Bleach: Sodium hypochlorite solution 4-4.99% Chlorine content | Sigma Aldrich | #239305 | Store in aliquots at 4 °C, seal with Parafilm to prevent loss of chlorine and cover in foil |
| D-Luciferin, potassium salt | Biotium Inc | # 10101-2 | Molecular Probes can also be used as supplier; prepare a 20 mM stock in ddH2O, keep at -20 °C in aliquots |
| [header] | |||
| Tween 20 | Sigma Aldrich | # P9416 | |
| DMSO | CalBiochem | #317275 | Purity 99.99% |
| Triton X100 | Alfa Aesar | #A16046 | Diltute to 10% in ddH2O |
| Nystatin | CalBiochem | #475914 | |
| C. elegans bioluminescent strains | Author's own laboratory | PE254, PE255 | contain integrated arrays feIs4 and feIs5 [Psur-5::luc+::gfp; rol-6(su1006)] respectively on chromossome V and X; select for homogeneous and strong expression of luc::GFP by fluorescence microscopy (e.g. pick 15 worms) every now and then. |
| E. coli OP50 | CGC | ||
| General chemicals | Sigma Aldrich/Fisher Scientific | ||
参考文献
- Lagido, C., Pettitt, J., Flett, A., Glover, L. A. Bridging the phenotypic gap: real-time assessment of mitochondrial function and metabolism of the nematode Caenorhabditis elegans. BMC Physiol. 8, 7 (2008).
- Lagido, C., McLaggan, D., Flett, A., Pettitt, J., Glover, L. A. Rapid sublethal toxicity assessment using bioluminescent Caenorhabditis elegans, a novel whole-animal metabolic biosensor. Toxicol Sci. 109, 88-95 (2009).
- McLaggan, D., et al. Impact of sublethal levels of environmental pollutants found in sewage sludge on a novel Caenorhabditis elegans model biosensor. PloS one. 7, e46503 (2012).
- Rodriguez-Enriquez, S., Juarez, O., Rodriguez-Zavala, J. S., Moreno-Sanchez, R. Multisite control of the Crabtree effect in ascites hepatoma cells. Eur J Biochem. 268, 2512-2519 (2001).
- Marroquin, L. D., Hynes, J., Dykens, J. A., Jamieson, J. D., Will, Y. Circumventing the Crabtree effect: replacing media glucose with galactose increases susceptibility of HepG2 cells to mitochondrial toxicants. Toxicol Sci. 97, 539-547 (2007).
- Rooney, J. P., et al. Effects of 5'-fluoro-2-deoxyuridine on mitochondrial biology in Caenorhabditis elegans. Exp Gerontol. 56, 69-76 (2014).
- Bodhicharla, R., Ryde, I. T., Prasad, G. L., Meyer, J. N. The tobacco-specific nitrosamine 4-(methylnitrosamino)-1-(3-pyridyl)-1-butanone (NNK) induces mitochondrial and nuclear DNA damage in Caenorhabditis elegans. Environ Mol Mutagen. 55, 43-50 (2014).
- Leung, M. C., et al. Effects of early life exposure to ultraviolet C radiation on mitochondrial DNA content, transcription, ATP production, and oxygen consumption in developing Caenorhabditis elegans. BMC Pharmacol Toxicol. 14, 9 (2013).
- Kuang, J. J., Ebert, P. R. The failure to extend lifespan via disruption of complex II is linked to preservation of dynamic control of energy metabolism. Mitochondrion. 12, 280-287 (2012).
- Lagido, C., Pettitt, J., Porter, A. J., Paton, G. I., Glover, L. A. Development and application of bioluminescent Caenorhabditis elegans as multicellular eukaryotic biosensors. FEBS Lett. 493, 36-39 (2001).
- Lewis, J. A., Fleming, J. T. Basic culture methods. Methods Cell Biol. 48, 3-29 (1995).
- Stiernagle, T. Maintenance of C. elegans. WormBook. , 1-11 (2006).
- Brenk, R., et al. Lessons learnt from assembling screening libraries for drug discovery for neglected diseases. ChemMedChem. 3, 435-444 (2008).
- Lagido, C., Wilson, M. J., Kakouli-Duarte, T. . Nematodes as environmental indicators. , 225-251 (2009).
- Thorne, N., et al. Firefly luciferase in chemical biology: a compendium of inhibitors, mechanistic evaluation of chemotypes, and suggested use as a reporter. Chem Biol. 19, 1060-1072 (2012).
- Houtkooper, R. H., et al. Mitonuclear protein imbalance as a conserved longevity mechanism. Nature. 497, 451-457 (2013).
- Andreux, P. A., Houtkooper, R. H., Auwerx, J. Pharmacological approaches to restore mitochondrial function. Nat Rev Drug Discov. 12, 465-483 (2013).
- Tsang, W. Y., Lemire, B. D. Mitochondrial genome content is regulated during nematode development. Biochem Bioph Res Co. 291, 8-16 (2002).
- Decuyper, C., Vanfleteren, J. R. Oxygen-Consumption during Development and Aging of the Nematode Caenorhabditis-Elegans. Comp Biochem Phys A. 73, 283-289 (1982).
- Dillin, A., et al. Rates of behavior and aging specified by mitochondrial function during development. Science. 298, 2398-2401 (2002).
- Zheng, S. Q., Ding, A. J., Li, G. P., Wu, G. S., Luo, H. R. Drug absorption efficiency in Caenorhbditis elegans delivered by different methods. PloS one. 8, e56877 (2013).
- Yochem, J., Gu, T., Han, M. A new marker for mosaic analysis in Caenorhabditis elegans indicates a fusion between hyp6 and hyp7, two major components of the hypodermis. Genetics. 149, 1323-1334 (1998).
- Vanfleteren, J. R., DeVreese, A. Rate of aerobic metabolism and superoxide production rate potential in the nematode Caenorhabditis elegans. J Exp Zool. 274, 93-100 (1996).
- Garigan, D., et al. Genetic analysis of tissue aging in Caenorhabditis elegans: a role for heat-shock factor and bacterial proliferation. Genetics. 161, 1101-1112 (2002).
- Davies, S. K., Leroi, A. M., Bundy, J. G. Fluorodeoxyuridine affects the identification of metabolic responses to daf-2 status in Caenorhabditis elegans. Mech Ageing Dev. 133, 46-49 (2012).
- Partridge, F. A., Tearle, A. W., Gravato-Nobre, M. J., Schafer, W. R., Hodgkin, J. The C. elegans glycosyltransferase BUS-8 has two distinct and essential roles in epidermal morphogenesis. Dev Biol. 317, 549-559 (2008).
- Castro, P. V., Khare, S., Young, B. D., Clarke, S. G. Caenorhabditis elegans Battling Starvation Stress: Low Levels of Ethanol Prolong Lifespan in L1 Larvae. PloS one. 7, (2012).
- Baugh, L. R. To Grow or Not to Grow: Nutritional Control of Development During Caenorhabditis elegans L1 Arrest. Genetics. 194, 539-555 (2013).
- Baugh, L. R., DeModena, J., Sternberg, P. W. RNA Pol II Accumulates at Promoters of Growth Genes During Developmental Arrest. Science. 324, 92-94 (2009).
- Maxwell, C. S., Antoshechkin, I., Kurhanewicz, N., Belsky, J. A., Baugh, L. R. Nutritional control of mRNA isoform expression during developmental arrest and recovery in C. elegans. Genome Res. 22, 1920-1929 (2012).
- Cressman, C. P., Williams, P. L. Reference toxicants for toxicity testing using Caenorhabditis elegans in aquatic media. Am Soc Test Mater. 131, 518-532 (1997).
- Khanna, N., Cressman, C. P., Tatara, C. P., Williams, P. L. Tolerance of the nematode Caenorhabditis elegans to pH, salinity, and hardness in aquatic media. Arch Environ Con Tox. 32, 110-114 (1997).
- Benedetti, C., Haynes, C. M., Yang, Y., Harding, H. P., Ron, D. Ubiquitin-like protein 5 positively regulates chaperone gene expression in the mitochondrial unfolded protein response. Genetics. 174, 229-239 (2006).
- Yang, W., Hekimi, S. A Mitochondrial Superoxide Signal Triggers Increased Longevity in Caenorhabditis elegans. Plos Biol. 8, (2010).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。