需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
腔内药物输送到鼠标动静脉瘘内皮
摘要
After puncturing the aorta through the inferior vena cava (IVC) to create an aorto-caval fistula in the mouse, solution containing a drug is infused into the IVC via the same needle, followed by incubation. This method enables more robust drug delivery to the venous endothelium compared to the external route.
摘要
治疗剂的递送,以提高动静脉瘘(AVF)成熟可以通过腔内或外部途径给药。简单的鼠AVF模型用的药物溶液至静脉内皮同时作为瘘创建腔内施用相结合。这个模型的技术问题进行了讨论。在全身麻醉下腹部切口由和主动脉和下腔静脉(IVC)被曝光。在肾下主动脉和下腔静脉解剖夹紧。近端和远端夹紧后,穿刺部位进行曝光,将25g针头被用来穿刺主动脉并进入下腔静脉两壁。穿刺后,立即报告基因表达的病毒载体在IVC通过相同的针注入,随后温育15分钟。相比由外部给药途径腔内给药方法使能更健壮的病毒基因递送到静脉内皮。这诺夫递送l的方法将有利于研究,探索在AVF成熟内皮的作用,并能在外科手术的时间腔内给药。
引言
鼠aortovenous瘘(AVF)的主动脉和下腔静脉(IVC)之间穿刺模型现在是一个既定的技术。1在该模型中,红外肾主动脉的两壁与地下25针被刺破,退出进毗邻肾下腔静脉;前主动脉入口孔被修复以简单的压缩,并且不需要缝合修复。串行随访检查采用高分辨率多普勒超声和病理分析表明,AVF有一个成熟阶段,再一个失败的阶段,扼要重述人类AVF的已知病理生理学2
探索了调节AVF成熟机制,需要用于输送治疗剂来熟化AVF内皮改进的方法。治疗剂递送至血管可以是通过血管内递送至内腔,或通过外部传递到外膜。外部递送的一个实例是玉米常用的聚醚凝胶的外膜应用。当加热到体温这种共聚物是热可逆的,并从液体到固体凝胶转化。当在体内局部施用药物在普卢兰尼克凝胶混合5,6-实现先前的研究已经表明持续的药物递送。3,4-病毒载体或siRNA与的Pluronic凝胶的外膜应用已报道是有效的血管周围递送系统,我们有还报告说,治疗由肽刺激外膜人外植隐静脉的导致内皮细胞受体蛋白的磷酸化。7
在另一方面,调查也同时使用病毒和非病毒载体腔内交付8-10犬和兔11,12车型静脉移植的。在这些报告中,静脉收获后进行基因转移体外 。伊斯拉米等报道的血管内的病毒基因递送y以颈动脉原位脉,而无需创建一个旁路13 Gloverman等。在大鼠股动脉,腹壁浅静脉瘘裸DNA的报道腔内和外膜交付14梅奥组报道在小鼠颈总动脉,颈内静脉瘘外膜的药物输送15,16然而,这些先前报告的模型需要缝合吻合创造在AVF。在这份报告中,腔内给药并同时创造AVF在小鼠中的描述,使用AVF创作的缝合线少的模型。通过使用本变形鼠AVF模型可以执行用于腔内药物输送到瘘管的静脉肢的简单方法。
研究方案
获得批准相应的机构动物护理和使用委员会。
1.麻醉和手术前的程序
- 麻醉雄性C57BL / 6冰,8周龄,用汽化3%异氟醚和0.8升/分钟的氧气给予到丙烯酸感应腔室。
- 确认缺乏反应脚趾捏足够的麻醉。通过连续吸入3%异氟烷 - 定位在动作表鼠标仰卧和定位硅氧烷掩模递送汽化2。
- 腹部用化学脱毛霜去除颈部腹侧头发更低。
- 之前AVF手术进行多普勒超声检查在感兴趣的领域,以记录动脉和静脉流动和血管直径的基线特征。1,2
- 附加1ml注射器向地下25针和与所需药物加载注射器。弯针60度角约4从需要毫米乐一角。抓住一个弯针架在地下25针。
2.手术过程
- 准备切口部位有局部消毒剂和应用手术单。使用无菌手套和工具,以在整个手术保持无菌操作。
- 使一个中线腹部切口用解剖刀从下肝脏边缘水平延伸到刚好耻骨之上。
- 插入的牵开器以及从向右侧腹腔剔骨所有肠子。裹肠纱布用盐水浸湿。解剖连接复古腹膜和较低的结肠获得主动脉和下腔静脉的全视角膜。
- 从周围组织解剖肾下主动脉和下腔静脉,对近端和远端夹紧准备。
- 放置在这两个近端主动脉和在刚刚左肾静脉水平以下近端IVC单个显微剪辑。将第二显微剪辑跨两个为Distal主动脉和远侧IVC。
- 把握结缔组织围绕主动脉和内侧旋转,使得主动脉的背表面稍微露出的动脉穿刺,如先前所述。1
- 很快暴露穿刺部位。穿刺部位将在血管,从左肾静脉到主动脉分叉的距离的大约四分之三的尾方面。保持主动脉在一个旋转位置用左手,解剖主动脉的左侧缘,以便有充足的曝光,以允许用右手穿刺。要小心,不要主动脉和下腔静脉之间的解剖。
- 保持在一个旋转位置的主动脉,并使用地下25针带有附加1ml注射器含有药物溶液通过刺穿主动脉进入下腔静脉。 ( 图1A)
- 注入药液 - 利用左手(100 200微升)。针可以通过扩张和薄可见下腔静脉壁当透明药液置换静脉血出下腔静脉( 图1B,C)的。保持静止并保持在适当的位置的针15分钟。
- 移除远侧显微剪辑脱夹具仅远端主动脉和远侧IVC。
- 取出针再涂向上拉相邻复古腹膜组织主动脉的穿刺部位。
- 取出近端显微剪辑去夹紧近端主动脉和近端IVC。在去夹紧,动脉血观察流入下腔静脉,而不是深静脉血流。保持覆盖所述穿刺孔进行1分钟。
- 止血确认通过观察30秒,而没有压缩后,返回肠子到其自然的位置,并根据您批准的动物协议的连续缝合关闭的腹部。
3.手术后的程序
- 腹部闭合后,停止ANESThesia。应用术后护理包括镇痛和伤口护理按照机构动物护理和使用委员会建议的说明。镇痛我们使用丁丙诺啡在0.1毫克/千克intrasmuscularly以下的外科手术24小时,每12小时。
- 在手术后的第一天,进行多普勒超声检查,以确认AVF通畅。此外,衡量其他船只和串行流量特性,比较从术前基线值的变化。1,2
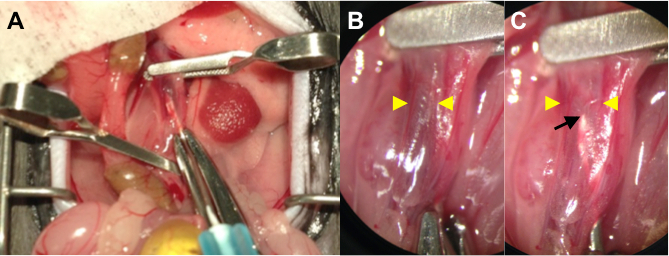
图1(a)执行照片AVF手术中显示管腔内交货。夹紧近端和远端主动脉,以及通过施加显微剪辑IVC。利用地下25针含附加注射器药液通过穿刺进入主动脉下腔静脉。(B)几点措施她电源图像输液前刺破下腔静脉(放大4倍)。针尖通过深色静脉血遮蔽。黄色箭头表示输液后刺破下腔静脉的墙到墙直径IVC。(C)更高的功率图(放大4倍)的。针尖(黑色箭头),可通过轻轻扩张和薄墙下腔静脉(黄色箭头)作为透明药材溶液中可以看出置换静脉血。
结果
在一系列33小鼠,在第一术后天存活率为97.0%; AVF通畅,如通过超声波来确定,为84.9%。
与传统的外部路由本血管内输送路线的基因转导效率进行比较。对于管腔内输送(ILD),在穿刺后,立即加入200μl腺病毒的GFP(广告-GFP)载体溶液(1×10 9 PFU / ml)的经穿刺针注入IVC,随后孵育15分钟时间。对照组小鼠用聚醚凝胶?...
讨论
鼠AVF模型的这种修改包含在AVF创建时腔内药物递送到静脉内皮。一个AVF通过穿刺用地下25针的红外肾主动脉和延伸穿过相对的主动脉壁进入下腔静脉穿刺,随后的药物溶液注射通过同一针创建。该解决方案是维持内静脉, 即 ,在AVF的静脉肢体,直到去夹紧。什么区别于其他鼠类AVF模型17-19这种模式是缺乏缝合或胶水可能导致管腔狭窄,急性血栓形成,并与分子分析可能的干扰。使?...
披露声明
The authors have nothing to disclose.
致谢
This work was supported in part by the United States Department of Veterans Affairs Biomedical Laboratory Research and Development Program Merit Review Award I01-BX002336, the National Institute of Health grant R56-HL095498, as well as with the resources and the use of facilities at the VA Connecticut Healthcare System, West Haven, CT.
材料
| Name | Company | Catalog Number | Comments |
| Pluronic F-127 | Sigma-Aldrich | P2443-250G | Used as 30% solution in d-water |
| GFP antibody | NOVUS BIOLOGICALS INC | NB100-1770 | |
| Ad-CMV-GFP | VECTOR BIOLABS | 1060 | |
| 0.9% Sodium Chloride Irrigation, USP | Baxter | 2F7122 | |
| BD PrecisionGlide Needle 25 G x 5/8 | BD | 305122 | |
| BD 1 ml Syringe Tuberculin Slip Tip | BD | 309659 | |
| Scalpel | Surgical Design Inc | 22079707 | |
| 6-0 ETHILON P-1 11 mm 3/8c Reverse Cutting | ETHICON INC | 697G | |
| Vevo 770 ultrasound machine | Visualsonics | 20 - 60 Mhz scan head; RMV-704 | |
| Vascular clamp | Roboz Surgical Instrument Co. | RS-5424 | |
| Clamp applying forceps | Roboz Surgical Instrument Co. | RS-5410 |
参考文献
- Yamamoto, K., Li, X., Shu, C., Miyata, T., Dardik, A. Technical Aspects of the Mouse Aortocaval Fistula. J. Vis. Exp. (77), e50449 (2013).
- Yamamoto, K., et al. The mouse aortocaval fistula recapitulates human arteriovenous fistula maturation. Am. J. Physiol.: Heart Circ. Physiol. 305 (12), H1718-H1725 (2013).
- Escobar-Chávez, J. J., Lòpez-Cervantes, M., Naïk, A., Kalia, Y. N., Quintanar-Guerrero, D., Ganem-Quintanar, A. Applications of thermo-reversible pluronic F-127 gels in pharmaceutical formulations. J. Pharm. Pharm. Sci. 9 (3), 339-358 (2006).
- Almeida, H., Amaral, M. H., Lobão, P., Lobo, J. M. S. Pluronic® F-127 and Pluronic Lecithin Organogel (PLO): main features and their applications in topical and transdermal administration of drugs. J. Pharm. Pharm. Sci. 15 (4), 592-605 (2012).
- Karper, J. C., et al. Toll-like receptor 4 is involved in human and mouse vein graft remodeling, and local gene silencing reduces vein graft disease in hypercholesterolemic APOE*3Leiden mice. Arterioscler., Thromb., Vasc. Biol. 31 (5), 1033-1040 (2011).
- Redmond, E. M., Hamm, K., Cullen, J. P., Hatch, E., Cahill, P. A., Morrow, D. Inhibition of patched-1 prevents injury-induced neointimal hyperplasia. Arterioscler., Thromb., Vasc. Biol. 33 (8), 1960-1964 (2013).
- Wong, D. J., et al. Ephrin type-B receptor 4 activation reduces neointimal hyperplasia in human saphenous vein in vitro. J. Vasc. Surg. , (2014).
- Matsumoto, T., et al. Hemagglutinating virus of Japan-liposome-mediated gene transfer of endothelial cell nitric oxide synthase inhibits intimal hyperplasia of canine vein grafts under conditions of poor runoff. J. Vasc. Surg. 27 (1), 135-144 (1998).
- Petrofski, J. A., et al. Gene delivery to aortocoronary saphenous vein grafts in a large animal model of intimal hyperplasia. J. Thorac. Cardiovasc. Surg. 127 (1), 27-33 (2004).
- Hata, J. A., et al. Modulation of phosphatidylinositol 3-kinase signaling reduces intimal hyperplasia in aortocoronary saphenous vein grafts. J. Thorac. Cardiovasc. Surg. 129 (6), 1405-1413 (2005).
- Ohta, S., et al. Intraluminal gene transfer of endothelial cell-nitric oxide synthase suppresses intimal hyperplasia of vein grafts in cholesterol-fed rabbit: a limited biological effect as a result of the loss of medial smooth muscle cells. Surg. 131 (6), 644-653 (2002).
- Baldwin, Z. K., et al. Modulation of vascular remodeling induced by a brief intraluminal exposure to the recombinant R7020 strain of Herpes simplex-1. J. Vasc. Surg. 41 (1), 115-121 (2005).
- Eslami, M. H., et al. Gene delivery to in situ veins: differential effects of adenovirus and adeno-associated viral vectors. J. Vasc. Surg. 31 (6), 1149-1159 (2000).
- Globerman, A. S., et al. Efficient transgene expression from naked DNA delivered into an arterio-venous fistula model for kidney dialysis. J. Gene Med. 13 (11), 611-621 (2011).
- Yang, B., et al. Adventitial transduction of lentivirus-shRNA-VEGF-A in arteriovenous fistula reduces venous stenosis formation. Kidney Int. 85 (2), 289-306 (2014).
- Brahmbhatt, A., et al. The role of Iex-1 in the pathogenesis of venous neointimal hyperplasia associated with hemodialysis arteriovenous fistula. PLoS ONE. 9 (7), e102542 (2014).
- Karram, T., et al. Induction of cardiac hypertrophy by a controlled reproducible sutureless aortocaval shunt in the mouse. J. Investig. Surg. 18 (6), 325-334 (2005).
- Perry, G. J., et al. Genetic variation in angiotensin-converting enzyme does not prevent development of cardiac hypertrophy or upregulation of angiotensin II in response to aortocaval fistula. Circ. 103 (7), 1012-1016 (2001).
- Guzman, R. J., Krystkowiak, A., Zarins, C. K. Early and sustained medial cell activation after aortocaval fistula creation in mice. J. Surg. Res. 108 (1), 112-121 (2002).
- Alexander, J. H., et al. Efficacy and safety of edifoligide, an E2F transcription factor decoy, for prevention of vein graft failure following coronary artery bypass graft surgery: PREVENT IV: a randomized controlled trial. JAMA. 294 (19), 2446-2454 (2005).
- Khaleel, M. S., et al. High-pressure distention of the saphenous vein during preparation results in increased markers of inflammation: a potential mechanism for graft failure. Ann. thorac. surg. 93 (2), 552-558 (2012).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。