Method Article
荧光活化细胞分选分离人皮肤状和网状成纤维细胞
摘要
这份手稿描述了一种基于 fac 的从人的皮肤中分离状和网状成纤维细胞的协议。它规避了体外培养, 这是不可避免的与常用的隔离协议通过外植体培养。所产生的成纤维细胞亚群功能不同, 在真皮内显示出不同的基因表达和定位。
摘要
成纤维细胞是一种高度异质性的细胞群, 与许多人类疾病的发病机制有关。在人类皮肤真皮 , 成纤维细胞传统上归因于浅状或下网状真皮根据其组织学定位。在小鼠真皮中 , 状和网状成纤维细胞起源于两个不同的谱系 , 在生理和病理过程中具有分化的功能 , 并有一个独特的细胞表面标记表达谱 , 通过这些特征可以区分它们。
重要的是, 来自浅层和低真皮层的外植体培养的证据表明, 人类皮肤真皮中至少存在两种功能不同的真皮成纤维细胞谱系。然而, 与小鼠皮肤不同的是, 能够识别不同成纤维细胞亚群的细胞表面标记尚未为人体皮肤建立。我们开发了一种新的方案 , 通过荧光激活细胞分选 ( FACS ) 分离人类状和网状成纤维细胞群的方法 , 使用两个细胞表面标记成纤维细胞激活蛋白 ( FAP ) 和胸腺细胞抗原 ( Thy1 ) / CD90 。这种方法可以在没有体外操作的情况下分离纯成纤维细胞亚群, 从而影响基因表达, 从而能够准确地分析人真皮成纤维细胞亚群在组织稳态或疾病方面的功能分析病理。
引言
成纤维细胞作为结缔组织的主要细胞成分, 主要负责胶原蛋白和弹性纤维的沉积, 最终形成细胞外基质1, 因此, 它们在组织稳态、再生和疾病长期以来一直被低估。然而, 成纤维细胞最近成为研究人员关注的焦点, 这不仅是因为它们是诱导多能干细胞2的重要细胞来源,还因为它们在其发病机制中具有很高的可塑性和意义。多种疾病, 如器官纤维化3,4,5或癌症6,7。
人的皮肤是由多层上皮 , 表皮 , 其底层结缔组织 , 真皮 , 这可以组织学细分为上状和下网状真皮 , 主要由成纤维细胞和细胞外基质8和皮下组织。根据皮肤成纤维细胞在组织中的位置 , 皮肤成纤维细胞大致分为状和网状成纤维细胞1。
重要的是, 最近的数据表明, 这些真皮成纤维细胞亚群不仅在组织学上是可区分的, 而且其功能也有相当大的差异。在小鼠皮肤中 , 状和网状成纤维细胞在胚胎发生过程中产生于两个不同的谱系9。一些证据表明, 这两种血统不仅在组织稳态、毛囊形态发生、伤口修复和纤维化方面发挥着不同的作用, 而且对不同的疾病也有反应来自肿瘤表皮干细胞的信号 11, 表明不同的作用在癌症的发病机制。方便的是, 这两个血统在成年小鼠皮肤中表达了一套独特的相互排斥的细胞标记物, 从而能够分离出纯真皮成纤维细胞群, 并随后对其在体外的具体功能进行广泛分析9,11个。
相应地, 至少有两个不同的成纤维细胞亚群具有不同的形态和功能, 包括分化的增殖率, 组织重塑能力12,13, 以及支持生长的能力表皮干细胞体外, 已描述为人类皮肤真皮14,15。然而 , 已发表的关于人真皮成纤维细胞的研究大多是使用从皮肤外植体培养物中分离出的混合成纤维细胞群体进行的 , 因为特定的细胞表面标记集能够分离出纯人类状体或网状成纤维细胞亚群类似于小鼠真皮尚未建立。
我们最近已经证明 , 人类皮肤状和网状成纤维细胞的特点是特定的细胞表面标记 , 使分离各自的亚群通过荧光激活细胞分选 ( 流式细胞组织 )16 : fap+CD90成纤维细胞代表状成纤维细胞主要位于上真皮 , 表现出较高的增殖率 , 独特的基因特征 , 但没有脂原体的潜力。FAP+cd90+和 fa-cd90+成纤维细胞属于下真皮隔间的网状谱系, 这些隔间增殖较少, 但容易发生脂肪生成--网状成纤维细胞的标志.这种方法使广泛研究这些明显的成纤维细胞亚群, 不仅在生理条件下的特定功能, 而且在包括皮肤癌的皮肤病的发病机制的背景下。
然而, 由于成纤维细胞改变了其细胞表面标记在二维体外培养中的表达 16, 17, 19, 我们的协议的应用仅限于分离原代生细胞与人真皮 , 不允许在混合细胞培养群体中识别状或网状成纤维细胞。重要的是, 尽管细胞表面标记的表达在体外发生了变化, 但我们已经证明, 根据下面描述的协议分离的成纤维细胞子集在培养16时保留了其特定的功能, 从而能够生理或病理条件下亚基特异性特性的体外研究。
总之, 我们开发了一种通过流式细胞仪分离明显成纤维细胞亚群的方案, 首次允许将纯成纤维细胞群与处于幼稚状态的人皮肤真皮分离。
研究方案
人的皮肤是从26至61岁的白人男子和妇女身上获得的 (防晒皮肤; 腹部矫正、乳房减少)。根据《赫尔辛基宣言》, 并经维也纳医科大学机构审查委员会批准, 在收集组织之前获得书面知情病人同意。
请注意:我们提供了一种从全厚度真皮 (请参阅第1节) 或将人体皮肤真皮切片到不同层后 (跳过第1节, 直接参考第2节) 的功能不同的成纤维细胞亚群的分离协议。.
1. 全厚度真皮的制备
- 放置一个10厘米 x 10 厘米的人体皮肤片 (例如, 从腹部矫正或乳房缩小) 与表皮朝下在厚厚的滤纸。
- 用钳子紧紧地抓住表皮的边缘, 用手术刀刮掉皮下脂肪层。然后将组织切成5毫米宽的条状, 然后放入培养皿中。
请注意:这促进了 Dispase II (称为离解酶从今以后, 见第3节), 如果表皮需要从整个真皮分离, 则使用。对于此跳过第2节, 直接参考第3节。为避免污染, 手术切除后保持组织无菌, 或使用乙醇或碘溶液彻底清洁。如果有的话, 对皮肤表面的乙醇治疗只会导致轻微的细胞死亡。在无菌条件下组织培养流罩中工作。
2 . 将人皮肤真皮分割成带皮肤的状层和网状层
- 将10厘米 x 10 厘米的皮肤片 (例如, 腹部矫正或乳房缩小) 放在厚厚的滤纸上, 表皮朝上。用钳子将皮肤紧紧地固定在边缘上。
- 用电皮肤切割, 调整到切割厚度的厚度-深度 300μm, 通过滑动皮肤科的头部远离自己, 刀片是在90°角相对于皮肤的表面。
- 取由表皮和状真皮组成的第一层 ( 300μm厚 , 真皮层 1 ,图 1和图 2) , 并将其放入培养皿中。立即进入第3部分或添加 1x PBS, 以防止组织干燥。
请注意:为避免污染, 手术切除后保持组织无菌, 或使用乙醇或碘溶液彻底清洁。在无菌条件下组织培养流罩中工作。
注意事项:小心处理皮肤, 因为刀片是非常锋利的。 - 重复步骤2.2 将皮肤科调整为切割厚度为 700μm, 并将剩余的真皮切割成薄片。将被定义为上网状真皮的上一片 ("真皮层 2",图 2) 放入一个单独的培养皿中。立即进入第4节或添加 1x PBS, 以防止组织干燥。
- 用手术刀从残留的下网状真皮层 (& gt;1,000 微米) 中刮掉皮下脂肪层并丢弃。收集下网状真皮 ("真皮层 3",图 2) 在另一个培养皿。立即进入第4节或添加 1x PBS, 以防止组织干燥。
请注意:或者, 不要用手术刀刮掉脂肪, 用剪刀去除脂肪层。这可能有助于把网状真皮在冰上之前刮掉脂肪。
3. 表皮和真皮的分离
-
在无菌 1x PBS 中制备 3 uml 离解酶 (即 Dispase II) 溶液。将 5 毫米皮肤条纹 ( 从第 1 节 ) 或表皮 / 状真皮 ( 从步骤 2 . 2 ) , 表皮朝上在 10 厘米的培养皿中 , 10 毫升为 3 ml 离解酶溶液。在37°c 下将培养皿培养1小时。
- 协议可能会在此处暂停。在4°c的温度下 , 将表皮 / 状真皮在4°c的冰箱中 , 隔夜产入蛋白酶中。根据需要储存其他层 (真皮层 1, 2 和 3) 隔夜浸泡在 1x PBS 在 50 mL 管在4°c。
注意事项:小心使用蛋白酶, 它可能会刺激皮肤和眼睛接触。
- 协议可能会在此处暂停。在4°c的温度下 , 将表皮 / 状真皮在4°c的冰箱中 , 隔夜产入蛋白酶中。根据需要储存其他层 (真皮层 1, 2 和 3) 隔夜浸泡在 1x PBS 在 50 mL 管在4°c。
- 孵育后 , 将表皮 / 状真皮转移到培养皿的干盖 , 并将表皮与上真皮 ( 真皮层 1 ) 分开 , 每个钳子保持表皮或真皮边缘。
4. 皮肤组织的酶消化
- 用剪刀刀 (真皮层1、2和 3) 分别用剪刀刀, 尽量彻底地将每个真皮层 (真皮层1、2和 3) 磨碎;片断越小, 组织消化越好。
请注意:真皮的韧性可能因其发源的身体部位而异 (例如, 腹部或上臂皮肤)。 - 结合 1.25 mg/mL 胶原酶 I, 制备消化混合物, dulbecco 的改良鹰培养基 (dmem) 中含有 l-谷氨酰胺的改良鹰培养基中的 0.5 mgml 胶原酶 II、0.5 mgml 胶原酶 IV 和 0.1 mgml hyaluronidase (见材料表), 10% 胎小牛血清 (FCS) 和1% 青霉素/链霉素 (P/s)。
注意事项:小心地使用胶原酶, 因为这些酶可能会刺激皮肤和眼睛接触。 - 将每个有10毫升的碎组织混合到一个50毫升的管中, 在永久搅拌下在37°c 的温水浴中孵育1小时。在消化过程中, 将管子倒置几次。
请注意:应考虑根据碎皮肤片的大小调整消化量。不要将10ml 消化与过多的组织混合, 否则细胞产量将是最小的。建议在总体积内不到三分之一的组织 (1:2wv)。
5. 单细胞悬浮液和红细胞裂解的制备
- 在消化组织中加入10毫升成纤维细胞培养基 (含 l-谷氨酰胺、10% FCS 和 1% pcs), 停止酶组织消化。从现在开始在冰上工作。
- 通过常规无菌不锈钢滤网将每个管的内容物倒入, 并在干净的培养皿中收集细胞悬浮液。用注射器柱塞边缘的培养基和饲料清洗未消化的组织件清洗过滤器。
- 随后, 移液器通过70μm 的细胞过滤器将细胞悬浮液收集到50毫升管中。用培养基冲洗细胞过滤器, 并收集流经同一管的流动。
- 在4°C 下以 500 x g的速度离心管 10分钟, 去除和丢弃上清液和用5毫升成纤维细胞介质清洗细胞颗粒。重复离心步骤。
- 取出并丢弃上清液, 并在1毫升自制的 ACK 红细胞裂解缓冲液中重新悬浮颗粒(0.15 MM nh 4 cl, 10Mm khco 3, 0.1 mm na 2 edta;ph 7.2 \ u20127.4)。在环境温度 (20\u201222) 下, 将细胞留在裂解缓冲液中大约1分钟。
- 停止裂解, 加入9毫升的 1x PBS 与10% 的 FCS 和离心后, 在 500xg在4°c 下再次管5分钟。
注意事项:如果裂解似乎不完整 (红色颗粒), 红细胞裂解的孵化时间可能会被调整。然而, 不要将细胞留在红细胞裂解缓冲液中太久, 以避免成纤维细胞和免疫细胞的裂解。
6. 流式细胞仪成纤维细胞的阻塞和染色
- 在100μl 的 1X PBS 中制备5Μl 的人 fc 受体阻滞溶液, 其中10% 为 fcs, 并在100μl 的人 Fc 阻滞剂中重新悬浮细胞。在冰上孵化10分钟。
- 设计一个流式细胞仪染色面板来染色人皮肤成纤维细胞。混合反人类 FAP APC (1:20), 反人类 CD90 af700 (1:30), 反人类 E-cstherin PE (1:20)、反人类 CD31 FITC (1:20)、反人类 CD45 太平洋蓝 (1:20)、反人类 ITGA6 pe (1:20)、反人类 CD235ab 太平洋蓝 (1:1000) 和反人类 CD106 太平洋蓝色 (1: 100) 在 1个 PBS 与10% 的 FCS。
-
在 Fc 受体阻断后, 在4°c 下将细胞在 500 x g下降到 3分钟, 在100μl 抗体混合物中去除并丢弃上清液并重新悬浮细胞。在4°C 的黑暗中孵化细胞20分钟。
- 染色前, 取出具有高细胞数的样品 20Μl, 以进行未染色和单染色流式细胞仪控制。
- 用 500μl 1x PBS 用10% 的 FCS 和在4°C 时在500Xg 的温度下清洗染色细胞和流式细胞仪控制3分钟。同时, 在具有 10% fcs 的 1x PBS 中加入 4 '、6-二胺-2-苯基 (DAPI), 使最终浓度达到 1μg/ml。
- 取出并丢弃上清液, 在 200μl DAPI 溶液中重新悬浮细胞, 并通过70μm 电池过滤器将每个细胞悬浮液过滤成 5 mL 的流式细胞仪管。
请注意:如果要延迟执行 FACS, 请在录制前不久添加 DAPI 和筛选器。
7. 人皮肤成纤维细胞亚群分离及流式细胞仪的起动策略
- 记录流式细胞仪控制, 设置正确的电压设置并执行适当的补偿。门为单个细胞和活 (DAPI-), 太平洋蓝色, PE 和FITC 负细胞 (cd45-,cd31-, cd235ab-, cd106- , itga6-和 e-cadherin-), 以获得三个成纤维细胞群: fap+ CD90-, fap+cd90+和fa-cd90+细胞。请参见图 3。
- 将三个成纤维细胞亚群分类为单独的 1.5 mL 螺帽微离心管, 其中含有350μl 裂解缓冲液进行 RNA 分离, 或填充350μl 成纤维细胞生长介质 (见材料表) 进行细胞培养。在分类后立即反转管, 并将裂解缓冲管放入液氮中进行快速冻结或将介质管放在冰上。
注意事项:在烟罩中用0.1% 的 b-硫醇制备裂解缓冲液, 避免吸入。
8. 成纤维细胞的培养和脂肪生成法
- 在流式细胞系统 (FACS) 之后, 在4°C 下, 以 500 x g 的速度将细胞旋转至 3分钟, 并在48井细胞培养皿中在成纤维细胞生长培养基 (见材料表) 中将细胞数 (5, 000\ u201210, 000 细胞) 的平板数 (5, 000\ u201210, 000细胞)。让细胞生长, 直到它们达到70% 的融合。
- 在成纤维细胞生长培养基中加入5μgml 胰岛素、5μm troglitazone、0.5 mM 3-异丁基-1-甲基黄嘌呤 (IBMX) 和 1μm dexametasone, 制备脂肪细胞分化培养基。
- 用脂肪细胞分化培养基取代培养细胞的培养基, 让细胞分化14天。第二天后与含有5μgml 胰岛素和 5μm trolititazone 的还原脂肪发生培养基交换。每第3天或第4天补充介质.
- 在分化第14天, 将 4% PFA 的细胞固定在环境温度 (20\ u201222°c) 下20分钟。用60% 异丙醇清洗井, 让它完全蒸发。用 5 mM 油红色 O (使用前过滤器) 染色细胞 20分钟, 用蒸馏水清洗染色细胞4次。继续进行显微镜检查。
注意事项:PFA 有毒和有害。小心处理。
请注意:协议可以在这里暂停。固定单元可在4°c 下存储在 1x PBS 中, 直到进行油红色 O 染色。储存前用石蜡膜覆盖盘, 以避免蒸发。 - 图像细胞以10倍放大倍率与透射光的 x 倍的放大倍率与倒置显微镜浸入水中。
结果
图 1显示了处理皮肤组织以获得单个细胞悬浮液的主要步骤, 显示了皮肤的皮肤病 (图 1 a)、不同的真皮层 (图 1 b)、皮下脂肪的去除层 (图 1c) 和表皮和状真皮的分离 (图 1C) , 以及人工和酶组织分离的不同步骤 (图 1C, f) 。图 2提供了三个真皮层的方案。
图 3显示了流式细胞仪染色面板的浇注策略, 用于分析人体皮肤中不同的成纤维细胞亚群。没有在成纤维细胞上表达的其他细胞表面标记物允许排除皮肤中存在的各种其他细胞, 如免疫细胞、表皮细胞、间充质干细胞 (MSCs)、红血球或内皮细胞, 以达到最大纯度在孤立的人口。使用图 2中使用的相同的 facs 面板来识别这些成纤维细胞亚群并不重要, 但这是我们的建议。人们可以使用贴有不同荧光染料标签的抗体, 也可以改变排除标记的组合。
值得注意的是, 该协议能够识别人体皮肤中的三个成纤维细胞群体, 这些细胞成纤维细胞群体具有不同的皮内定位、基因表达谱和功能 (图 4)。FAP+cd90-在状真皮中富集 , 而 fap+cd90+和 fap - cd90+在网状真皮中更为丰富 (图 4 a) .这三个亚群在细胞培养中分类后都表现出典型的成纤维细胞形态 (图 4b)。有趣的是, 他们在分化为脂肪细胞的能力方面存在差异, 脂肪细胞是网状成纤维细胞的标志。将这些结果与通过实时聚合酶链反应 (RT-PCR) 16 (图 4c)进行基因表达谱相结合, 显示 fap+cd90细胞表达了高水平的标记, 通常归因于状成纤维细胞如 CD26 、 NTN 和 PDPN而cd90 + 细胞在高水平表达已知的网状标记 , 如 CD36 、 ACTA2 和pparγ,我们得出结论 , fap+cd90 - 细胞属于状细胞和 cd90+细胞属于网状谱系。

图 1: 从完整的人皮肤中分离皮肤单细胞悬浮液.(A) 皮肤用电皮肤切割成状和网状真皮。(B) 与相邻表皮的状真皮为300μm ( 上 ) , 而上网状真皮为 700 微米厚 ( 底部 ) 。(C) 皮下脂肪层用手术刀刮掉下网状真皮。(D) 在37°c 的离解酶溶液中孵育后 1小时, 可以很容易地用钳子去除表皮。(E) 不同的真皮层被剪刀粉碎, 并转移到由胶原酶 i、II 和 iv 以及透明质酸酶组成的酶消化混合物中。(F) 在37°c 下分离1小时后, 组织消化停止, 并通过茶过滤器浇注悬浮液, 以去除未消化的皮肤碎片。(G) 细胞悬浮液通过70μm 电池过滤器再次过滤, 并在4°c 时在 500 x x g下离心 10分钟 (h), 细胞颗粒用 1x PBS 清洗, 采用 10% FCS, 并可进行 facs 染色。请点击这里查看此图的较大版本.
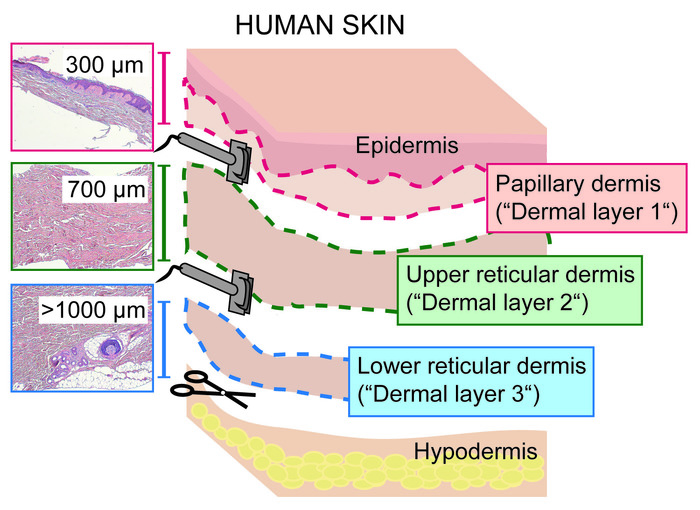
图 2 : 将人的皮肤真皮与皮肤科分离成状和网状层 .显示通过将全厚度皮肤切割成状真皮 ( 包括表皮 ; 0 \ u2012300 ; 真皮层 1 ) 、上网状 ( 3002201 千μm ; 真皮层 2 ) 和下网状真皮 ( & gt ; 1 , 000 μm ; 真皮层 3 ) 而获得的三个真皮层的方案 , 其带皮肤科。请点击这里查看此图的较大版本.
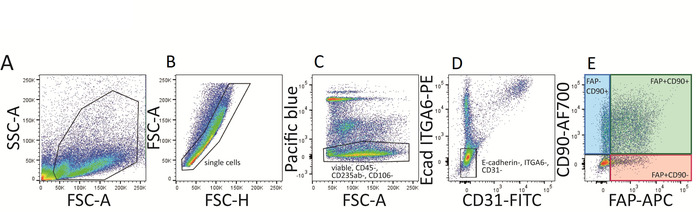
图 3: 人真皮成纤维细胞亚群的流式细胞仪门控策略.(A\ u2012e)首先, 细胞在单个 (b) 和活 (dapi-)细胞 (c) 上被门控。免疫细胞 (CD45+)、间充质干细胞 (cd106+)、红细胞 (cd235ab+) 被排除 (c) 和太平洋蓝色阴性细胞进一步被门控在 E-CADHERIN (ecad) 和 itga6 双阴性细胞 (pe 通道, d).E-钙粘蛋白和 ITGA6 是表皮细胞上表达的标记物。接下来, CD31-FITC 阳性细胞 (内皮细胞和淋巴细胞) 被排除在外 (d), 导致三个成纤维细胞群表达两个细胞表面成纤维细胞标记 FAP 和 cd90:fap+ cd90-,Fap+cd90+和 fa-cd90+ (e).请点击这里查看此图的较大版本.
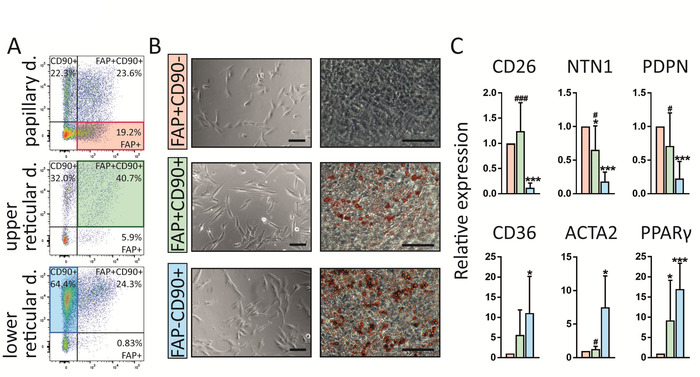
图 4: FAP+cd90-、fap+cd90+和 fa-cd90+成纤维细胞在皮肤定位、基因表达和功能方面存在差异.(A) 从状、上网状和下网状真皮中分离的门控成纤维细胞的代表性流式细胞仪图。列分策略在图 3中进行了说明。脂肪+cd90 -成纤维细胞在状真皮富集 ( 19 . 2% )与下网状真皮相比 (0.83)。FAP+cd90+细胞可以在整个真皮中找到, 但它们的最高丰度是在上网状真皮 (40.7)。FAP-CD90+在下网状真皮中富集 (64.4%).(B) 值得注意的是, 所有三个分类的亚群在培养 7天 (左) 时都会显示典型的成纤维细胞形态。有趣的是, 它们在脂肪生成试验中的行为不同。培养14天后, FAP+cd90-不分化为脂肪细胞, 而 fap+cd90 +和 fap-cd90+容易发生脂肪生成 (右;油红色 O 污渍含脂细胞红色)。标度条 = 1 , 000μm(c) 直接排序的 fap+ cd90 - 成纤维细胞表示状成纤维细胞标记 CD26 、 NTN1 和 PDPN , 而 FAP - CD90+细胞表示 Cd36 、 acta2 和pparγ , 已知为由网状血统表示。* p ≤0.05;与 FAP+/cd90 细胞相比, p≤0.0005;# p ≤0.05;# # p≤0.0005 与 Fap-/cd90+细胞相比.请点击这里查看此图的较大版本.
讨论
在这篇文章中 , 我们描述了一种方法 , 从人的皮肤上分离状和网状成纤维细胞。Cd90 已广泛用于皮肤成纤维细胞 18、20、21 的鉴定或分离。然而, 我们已经证明, 除了 CD90+ 成纤维细胞, 人类真皮还含有 CD90 -成纤维细胞群, 表示 fap16, 这已被确立为活化成纤维细胞和与肿瘤相关的成纤维细胞的标记 (Caf)22,23,24,25。重要的是, 我们能够识别三个成纤维细胞亚群 FAP+ cd90-, fap+cd90+和 fap-cd90+在皮肤活检从所有健康的人类捐献者。因此, 我们得出结论, FAP 不仅是活化成纤维细胞或 Caf 的标记, 也是正常的组织成纤维细胞。
值得注意的是, 在应用上述排除和门控策略后, fap-cd90-细胞群不包含成纤维细胞, 因为这些细胞在体外不会在成纤维细胞培养介质中增殖, 但大多数可能是一个混合细胞群, 包括淋巴细胞和周周细胞等 16.
通过使用上述协议获得的细胞产量可能因用于隔离的皮肤部位的身体部位而有所不同。不同身体部位的真皮因其结构、厚度以及胶原蛋白成分而异。例如, 面部或上臂的皮肤比腹部或大腿的皮肤薄很多, 腹部或大腿的皮肤也经常显示较厚的皮下脂肪层。此外, 皮肤捐献者的年龄和性别不仅可能进一步影响组织离解效率, 而且可能影响三个成纤维细胞亚群的分布 (图 3), 当从全厚度的皮肤中分离。这是由于状真皮缩小 , 成纤维细胞总数随着年龄的 11,26, 27,28而减少。此外 , 状真皮的细胞颗粒可能会比网状真皮大 , 因为上真皮比网状真皮更密集地由成纤维细胞填充。此外, 较低的真皮也是更硬的, 更密集的胶原蛋白, 使它更难分离的组织和释放成纤维细胞。值得注意的是, 细胞颗粒可能会出现非常红, 这也是建议红血球裂解的原因。
除了识别完整的人的皮肤中的三个亚群外 , 我们还表明 , 在皮肤皮肤上 , 每个成纤维细胞子集在状或网状真皮16中都是丰富的。用皮肤切割皮肤是至关重要的, 以获得适当的丰富每个亚群从不同的皮肤层。由于状真皮非常薄 , 代表它的皮肤切片厚度不应超过300μm . 上网状和下网状成纤维细胞都代表网状血统 , 并显示相似的功能和基因签名 ,因此, 人们也可以考虑不将它们分开。
重要的是 , 所有三个成纤维细胞种群在真皮中都有发现 , 并不完全存在于一层 , 这就是为什么状或网状真皮的外植体培养物导致混合成纤维细胞培养。然而 , FAP+cd90-状成纤维细胞在状真皮中最丰富 , 从浅层到下真皮层呈梯度 , 而 fap+cd90 + 和 fap - cd90 +成纤维细胞则遵循从较低的层到浅层的逆梯度16。此外 , 状真皮的 CD90+成纤维细胞几乎完全存在于血管周围 , 并表达血管周围成纤维细胞标记 cd146 29 ,因此可能表现出不同的功能。剩余 CD146-网状成纤维细胞16。CD146 可作为门控战略中的另一个标记, 以排除这一人群。
在真皮层分离后, 分离细胞被染色一种专门设计的抗体鸡尾酒, 其中含有各种抗体, 用于排除免疫细胞、内皮细胞和淋巴细胞、表皮细胞、红细胞和骨髓间充质干细胞。获得纯成纤维细胞的数量。值得注意的是, 选择一个标记来识别和排除骨髓间充质干细胞可能会很棘手, 因为已发布的 msc 标记 30、31的数量很多。由于骨髓间充质干细胞像成纤维细胞一样表达 CD90, 因此额外的 MSC 标记 (如 CD105 或 CD271) 可被证明对其鉴定有用。然而, 骨髓间充质干细胞只占所有真皮细胞的比例很低, 而且由于 CD90+成纤维细胞在分类时显示出典型的成纤维细胞形态特征, 人们可能会认为, 使用不同的细胞表面标记排除骨髓间充质干细胞可能会是不必要的。
重要的是, 我们分析了 FAP 和 CD90 基因表达后, 保持细胞在培养7-14 后排序 (未显示的数据), 并发现这两个标记的表达是在各自的排序单阳性 (FAP+cd90-或FAP-cd90+) 细胞16。因此, 我们强调, 上述标记集和协议允许直接从组织中分离原生成纤维细胞亚群, 但不允许从以前培养的混合成纤维细胞群体中分离。
然而 , 我们证明 , 所有三个亚群的功能保留在细胞培养中 , 而不考虑细胞表面标记表达的变化 , 因为成纤维细胞排序为 fap + cd90-状成纤维细胞不在较长的培养期后获得接受脂肪生成的能力, 而将成纤维细胞排序为 fap + cd90+或fap- cd90 + 网状成纤维细胞保持其分化为脂肪细胞的能力16.重要的是 , 我们还发现 , 状和网状特异性基因在 FAP+cd90- 和cd90+中的表达程度仍然较高。
总之, 我们建立了一个通过流式细胞仪分离功能不同的成纤维细胞亚群的协议, 该方案首次允许从人体皮肤真皮中分离和分析纯和天真的成纤维细胞亚群。该方法确立了从上、下真皮对常用的成纤维细胞外植体培养分离方案的重大推进 , 因为 ( i ) 从皮肤表面到真皮下存在状和网状成纤维细胞的相反梯度 , 以及 ( ii )成纤维细胞在体外改变基因特征。
披露声明
作者没有什么可透露的。
致谢
我们感谢 Bärbel Reininger 和 Wolfgang Bauer 在 fns 分拣方面提供的协助。这项工作得到了奥地利科学基金 (FWF:V 525-B28) 和欧洲生化协会联合会 (FEBS, 后续研究基金) 向 b. m. l. 提供的赠款的支持。S. F. 是奥地利科学院 (OeAW) doc 研究金的获得者。我们感谢维也纳医科大学核心设施的大力支持。我们感谢 Bernhard Gesslbauer、Christine Radtke 和 Martin Vierhapper 提供的人体皮肤材料。
材料
| Name | Company | Catalog Number | Comments |
| Material: | |||
| 3-isobutyl-1-methylxanthine | Sigma | I5879 | |
| Ammonium chloride | Sigma | 9718 | used for selfmade ACK Lysis Buffer |
| Amniomax-C100 (1x) Basal Medium | Gibco | 17001-074 | used for fibroblast growth medium |
| β-Mercaptoethanol | Scharlau | ME0095 | ! CAUTION |
| C100 Supplement | Thermo Scientific | 12556015 | used for fibroblast growth medium |
| Collagenase I | Thermo Scientific | 17100017 | ! CAUTION |
| Collagenase II | Gibco | 17101015 | ! CAUTION |
| Collagenase IV | Sigma | C5138 | ! CAUTION |
| DAPI | Thermo Scientific | 62248 | |
| Dexamethasone | Sigma | D8893 | |
| Dispase II | Roche | 4942078001 | ! CAUTION |
| Dulbecco‘s Modified Eagle Medium + GlutaMAX | Gibco | 31966-021 | |
| EDTA disodium salt | Sigma | E1644 | used for selfmade ACK Lysis Buffer |
| Fetal bovine serum (heat inactivated) | Gibco | 10500-064 | |
| Hyaluronidase | Sigma | H4272 | ! CAUTION |
| Insulin | Sigma | I5500 | |
| Isopropanol | Merck | 1,096,341,011 | |
| OilRed O | Sigma | O-0625 | |
| Paraformaldehyd | Sigma | 158127 | ! CAUTION Cancerogenic. Skin and eye irritant. Handle with care. |
| Penicillin/Streptomycin | Gibco | 15070-063 | |
| Phosphate-buffered saline without Ca++ & Mg++ | Lonza | BE17-512F | |
| Potassium bicarbonate | Sigma | 237205 | used for selfmade ACK Lysis Buffer |
| PureLink RNA MicroKit | Invitrogen | 12183-016 | |
| SuperScript III First-Strand Synthesis SuperMix for qRT-PCR | Invitrogen | 11752 | |
| Taqman 2xUniversal PCR Master Mix | Applied Biosystems | 4324018 | ! CAUTION Skin and eye irritant. |
| Troglitazone | Sigma | T2573 | |
| Name | Company | Catalog Number | Comments |
| Flow cytometry Antibodies: | |||
| anti human CD31-AF488 | Biolegend | 303109 | Dilution: 1:30, Lot: B213986, RRID: AB_493075 |
| anti human CD45-Pacific blue | Biolegend | 304029 | Dilution: 1:20, Lot: B218608, RRID: AB_2174123 |
| anit human CD49f/ITGA6-PE | Serotec | MCA699PE | Dilution: 1:20, Lot: 0109, RRID: AB_566833 |
| anti human CD90/Thy-1-AF700 | Biolegend | 328120 | Dilution: 1:30, Lot: B217250, RRID: AB_2203302 |
| anti human CD106-AF421 | BD | 744309 | Dilution: 1:100, Lot: 7170537, RRID: x |
| anti human CD235ab-Pacific blue | Biolegend | 306611 | Dilution: 1:1000, Lot: B224563, RRID: AB_2248153 |
| anti-human E-cadherin-PE | Biolegend | 147304 | Dilution: 1:20, Lot: B197481, RRID: AB_2563040 |
| anti human FAP-APC | R&D | FAB3715A | Dilution: 1:20, Lot: AEHI0117111, RRID: x |
| Human TruStain FcX | Biolegend | 422302 | Dilution: 1:20, Lot: B235080, RRID: x |
| Name | Company | Catalog Number | Comments |
| Equipment: | |||
| 1.4 mL micronic tubes | Thermo Scientific | 4140 | |
| 1.5 mL screw cap micro tube | Sarstedt | 72,692,405 | |
| 5 mL Polystyrene Round Bottom Tube with cell strainer cap | Falcon | 352235 | |
| 48-well cell culture cluster | Costar | 3548 | |
| 50 mL polypropylene canonical tubes | Falcon | 352070 | |
| 70 µm cell strainer nylon | Falcon | 352350 | |
| Aesculap Acculan 3Ti Dermatome | VWR | AESCGA670 | |
| Aesculap Dermatome blades | VWR | AESCGB228R | |
| MicroAmp Fast Optical 96well | Applied Biosystems | 4346906 | |
| Primary cell culture dish | Corning | 353803 | |
| Scalpel blades | F.S.T | 10022-00 | |
| Tea strainer | x | x | |
| Name | Company | Catalog Number | Comments |
| Fibroblast growth medium: | |||
| AmnioMAX basal medium with AmnioMAX C-100 Supplement, 10 % FCS and 1 % P/S |
参考文献
- Sorrell, J. M., Caplan, A. I. Fibroblast heterogeneity: more than skin deep. Journal of Cell Science. 117 (Pt 5), 667-675 (2004).
- Lowry, W. E., et al. Generation of human induced pluripotent stem cells from dermal fibroblasts. Proceedings of the National Academy of Sciences of the United States of America. 105 (8), 2883-2888 (2008).
- Kisseleva, T. The origin of fibrogenic myofibroblasts in fibrotic liver. Hepatology. 65 (3), 1039-1043 (2017).
- LeBleu, V. S., et al. Origin and function of myofibroblasts in kidney fibrosis. Nature Medicine. 19 (8), 1047-1053 (2013).
- Travers, J. G., Kamal, F. A., Robbins, J., Yutzey, K. E., Blaxall, B. C. Cardiac Fibrosis: The Fibroblast Awakens. Circulation Research. 118 (6), 1021-1040 (2016).
- Kalluri, R., Zeisberg, M. Fibroblasts in cancer. Nat Rev Cancer. 6 (5), 392-401 (2006).
- Rinkevich, Y., et al. Skin fibrosis. Identification and isolation of a dermal lineage with intrinsic fibrogenic potential. Science. 348 (6232), (2015).
- Abhishek, S., Palamadai Krishnan, S. Epidermal Differentiation Complex: A Review on Its Epigenetic Regulation and Potential Drug Targets. Cell Journal. 18 (1), 1-6 (2016).
- Driskell, R. R., et al. Distinct fibroblast lineages determine dermal architecture in skin development and repair. Nature. 504 (7479), 277-281 (2013).
- Mastrogiannaki, M., et al. beta-Catenin Stabilization in Skin Fibroblasts Causes Fibrotic Lesions by Preventing Adipocyte Differentiation of the Reticular Dermis. Journal of Investigative Dermatology. 136 (6), 1130-1142 (2016).
- Lichtenberger, B. M., Mastrogiannaki, M., Watt, F. M. Epidermal beta-catenin activation remodels the dermis via paracrine signalling to distinct fibroblast lineages. Nature Communications. 7, 10537 (2016).
- Harper, R. A., Grove, G. Human skin fibroblasts derived from papillary and reticular dermis: differences in growth potential in vitro. Science. 204 (4392), 526-527 (1979).
- Hiraoka, C., et al. Two clonal types of human skin fibroblasts with different potentials for proliferation and tissue remodeling ability. Journal of Dermatological Science. 82 (2), 84-94 (2016).
- Higgins, C. A., et al. Multifaceted role of hair follicle dermal cells in bioengineered skins. Br Journal of Dermatology. 176 (5), 1259-1269 (2017).
- Korosec, A., Lichtenberger, B. M., Marques, A. P., Pirraco, R. P., Cerqueira, M., Reis, R. L. Ch. 12. Skin Tissue Models. , 279-301 (2017).
- Korosec, A., et al. Lineage identity and location within the dermis determine the function of papillary and reticular fibroblasts in human skin. Journal of Investigative Dermatology. , (2018).
- Higgins, C. A., Chen, J. C., Cerise, J. E., Jahoda, C. A., Christiano, A. M. Microenvironmental reprogramming by three-dimensional culture enables dermal papilla cells to induce de novo human hair-follicle growth. Proceedings of the National Academy of Sciences of the United States of America. 110 (49), 19679-19688 (2013).
- Philippeos, C., et al. Spatial and Single-Cell Transcriptional Profiling Identifies Functionally Distinct Human Dermal Fibroblast Subpopulations. Journal of Investigative Dermatology. 138 (4), 811-825 (2018).
- Walmsley, G. G., et al. Live fibroblast harvest reveals surface marker shift in vitro. Tissue Engineering Part C: Methods. 21 (3), 314-321 (2015).
- Jiang, D., Rinkevich, Y. Defining Skin Fibroblastic Cell Types Beyond CD90. Frontiers in Cell and Developmental Biology. 6, 133 (2018).
- Sorrell, J. M., Caplan, A. I. Fibroblasts-a diverse population at the center of it all. International Review of Cell and Molecular Biology. , 161-214 (2009).
- Huang, Y., et al. Isolation of Fibroblast-Activation Protein-Specific Cancer-Associated Fibroblasts. BioMed Research International. 2017, 4825108 (2017).
- Jiang, G. M., et al. The application of the fibroblast activation protein alpha-targeted immunotherapy strategy. Oncotarget. 7 (22), 33472-33482 (2016).
- Pure, E., Blomberg, R. Pro-tumorigenic roles of fibroblast activation protein in cancer: back to the basics. Oncogene. 37 (32), 4343-4357 (2018).
- Hamson, E. J., Keane, F. M., Tholen, S., Schilling, O., Gorrell, M. D. Understanding fibroblast activation protein (FAP): substrates, activities, expression and targeting for cancer therapy. PROTEOMICS – Clinical Applications. 8 (5-6), 454-463 (2014).
- Gilchrest, B. A. A review of skin ageing and its medical therapy. Br Journal of Dermatology. 135 (6), 867-875 (1996).
- Gilchrest, B. A., Krutmann, J. . Skin Aging. , 198 (2006).
- Makrantonaki, E., Zouboulis, C. C. Molecular mechanisms of skin aging: state of the art. Annals of the New York Academy of Sciences. 1119, 40-50 (2007).
- Crisan, M., et al. A perivascular origin for mesenchymal stem cells in multiple human organs. Cell Stem Cell. 3 (3), 301-313 (2008).
- Kundrotas, G. Surface markers distinguishing mesenchymal stem cells from fibroblasts. Acta Medica Lituanica. 19 (2), 75-79 (2012).
- Lupatov, A. Y., Vdovin, A. S., Vakhrushev, I. V., Poltavtseva, R. A., Yarygin, K. N. Comparative analysis of the expression of surface markers on fibroblasts and fibroblast-like cells isolated from different human tissues. Bulletin of Experimental Biology and Medicine. 158 (4), 537-543 (2015).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。