Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Grüne und Low-Cost-Produktion von thermisch stabil und carboxylierte Cellulose-Nanokristalle und Nanofibrillen Mit Recycelbares Dicarbonsäuren
In diesem Artikel
Zusammenfassung
Hier zeigen wir ein neues Verfahren für grüne und nachhaltige Produktion von thermisch hochstabile und carboxylierte Cellulose-Nanokristalle (CNC) und Nanofibrillen (CNF) sehr gut recyclebar feste Dicarbonsäuren mit.
Zusammenfassung
Hier zeigen wir potenziell niedrigen Kosten und grüne Produktionen von hoher thermisch stabil und carboxylierte Cellulose-Nanokristalle (CNCs) und Nanofibrillen (CNF) aus gebleichtem Eukalyptus-Zellstoff (BEP) und rohen gemischten Hartholz-Kraftzellstoff (UMHP) Fasern sehr gut recyclebar Dicarbons festen Säuren. Typische Betriebsbedingungen waren Säurekonzentrationen von 50 bis 70 wt% bei 100 ° C für 60 min und 120 ° C (kein Sieden bei Atmosphärendruck) für 120 min, für BEP und UMHP, respectively. Die resultierenden CNCs haben eine höhere thermische Zersetzungstemperatur als die entsprechenden Zuleitungsfasern und Carbonsäuregruppengehalt von 0,2 bis 0,4 mmol / g. Die geringe Festigkeit (hohe pKa von 1,0 bis 3,0) von organischen Säuren führte auch in CNC-Steuerungen mit den beiden längeren Längen von etwa 239 bis 336 nm und eine höhere Kristallinität als CNCs Mineralsäuren hergestellt werden. Cellulose Verlust an Zucker war minimal. Faserige Cellulose-feste Rückstand (FCSR) aus der Dicarbonsäure Hydrolyse wurde verwendet, umcarboxylierten CNF durch nachfolgende mechanische Flimmern mit geringem Energieaufwand herzustellen.
Einleitung
Eine nachhaltige wirtschaftliche Entwicklung erfordert Einsatzmaterialien, die erneuerbare und biologisch abbaubar, sondern auch verwendet, grüne und umweltfreundliche Produktionstechnologien verwenden, um eine Vielzahl von Bioprodukten und Biochemikalien aus diesen nachwachsenden Rohstoffen produzieren nicht nur. Cellulose Nanomaterialien, wie Cellulose - Nanokristalle (CNC) und Cellulose - Nanofibrillen (CNF), hergestellt aus nachwachsenden Lignocellulosen sind biologisch abbaubar und haben einzigartige mechanische und optische Eigenschaften , die für die Entwicklung einer Reihe von Bioproducts 1, 2. Leider bestehende Technologien zur Herstellung von Cellulose - Nanomaterialien sind entweder energieintensiv als rein mechanische Fibrillation oder ökologisch nicht vertretbar wegen Nicht Recycling oder unzureichende Recycling von Prozesschemikalien verwendet, wie zum Beispiel , wenn die konzentrierte Mineralsäure Hydrolyse 3-8 oder Oxidationsverfahren unter Verwendung von 9- 11. Darüber hinaus können Methoden Oxidation produzieren auch umwelt toxische Kompounds durch mit Lignocellulose zu reagieren. Daher zur Herstellung von Cellulose-Nanomaterialien grün Fertigungstechnologien zu entwickeln, ist von entscheidender Bedeutung, die volle Nutzung der reichlich vorhandenen und nachwachsenden Rohstoffen zu machen - Lignocellulose.
Mit saure Hydrolyse Hemicellulose zu lösen und depolymerisieren Cellulose ist ein wirksamer Ansatz für Cellulose-Nanomaterialien zu erzeugen. Feste Säuren wurden für die Zuckerproduktion aus Zellulose mit dem Vorteil der Lockerung Säurerückgewinnung 12, 13 verwendet. Frühere Studien konzentrierten Mineralsäuren verwendet wurden, zeigten , dass eine niedrigere Säurekonzentration verbessert CNC - Ausbeute und Kristallinität 3, 5. Dies deutet darauf hin , dass eine starke Säure Cellulosekristalle beschädigen können , während ein milder Säurehydrolyse könnten die Eigenschaften und die Ausbeute an Cellulose Nanomaterialien durch den Ansatz der integrierten Produktion und CNC mit CNF 3, 14 zu verbessern. Hier dokumentieren wir ein Verfahren konzentrierten festen Dicarbonsäuren Hydrolyse unter Verwendung von zu produce CNC zusammen mit CNF 15. Diese Dicarbonsäuren haben eine geringe Löslichkeit bei niedrigen oder Umgebungstemperaturen, und daher können sie leicht durch die mature Kristallisationstechnologie gewonnen werden. Sie haben auch eine gute Löslichkeit bei erhöhten Temperaturen, die ohne zu kochen oder mit Druckbehältern konzentrierte saure Hydrolyse erleichtert. Da diese Säuren haben auch einen höheren pKa als typische Mineralsäuren für die CNC-Fertigung verwendet werden, ihre Verwendung führt zu einer guten CNC Kristallinität und trotz geringerer CNC Erträge, mit einer erheblichen Menge von zellulosehaltigen Faser festen Rückstand (FCSR oder teilweise hydrolysierten Fasern) verbleibenden aufgrund unvollständige Cellulose Depolymerisation. Die FCSR kann verwendet werden, CNF durch nachfolgende mechanische Fibrillation zu erzeugen, geringer Energieeingänge. Deshalb, um Zucker Cellulose Verlust ist minimal im Vergleich zu den Mineralsäuren.
Es ist gut bekannt , dass Carbonsäuren mit 16 Cellulose durch Fisher-Speier Veresterungsverfahren verestern kann. Dicarbonsäuren Anwendung zu Cellulose in semi-Säure unvernetzten Ester 17 (oder Carboxylierung) zur Folge haben kann, carboxylierten CNC und CNF zu produzieren , wie wir 15 zuvor gezeigt. Die Methode, die hier dokumentiert können carboxylierte und thermisch stabil CNF und CNC produzieren, die auch entweder aus gebleichtem oder ungebleichtem Breie hochkristallin ist, während relativ einfach und hohe Chemikalienrückgewinnung und mit geringem Energieeingänge.
Protokoll
HINWEIS: gebleichtem Eukalyptus-Kraft-Zellstoff (BEP) und rohen gemischten Hartholz-Kraftzellstoff (UMHP) Fasern, die aus kommerziellen Quellen wurden als Rohstoff verwendet für CNC und CNF produzieren. Kommerzielle Maleinsäuren erworben wurden für die Hydrolyse verwendet. Hydrolysebedingungen waren Säurekonzentrationen von 60 Gew% bei 100 ° C für 60 min und 120 ° C (kein Sieden bei Atmosphärendruck) für 120 min, für BEP und UMHP, respectively.
1. Herstellung von Concentrated Dicarbonsäurelösung
- Wärme 40 ml entionisiertes (DI) Wasser in einem Kolben mit mehreren Hals in einem flüssigen Glycerinbad auf einer Heizplatte auf etwa 85 ° C.
- In 60 g wasserfreie Maleinsäure in den Kolben eine 60% ige Lösung unter magnetischem Rühren zu machen. Verwendung der Dichten der Säurelösungen zuvor 15 gemeldet, die Berechnung der erforderlichen Menge an Wasser und Säure für die Herstellung der Säurelösung bei der angegebenen Massenkonzentration.
- Die Lösung wird auf die degezeugt Hydrolysetemperatur von 100 oder 120 ° C (kein Sieden aufgrund hoher Konzentrationen dicarbonsäure).
2. Hydrolysereaktion
- Sobald die Säurelösung bei einer Temperatur ist, mit 10 g ofengetrockneten (OD) von BEP oder UMHP Fasern in 80 ml Dicarbonsäurelösung (1.1) unter kontinuierlichem Rühren.
- Nehmen eines Aliquots der Säurehydrolysat (ca. 2 mL) am Ende der vorbestimmten Reaktionszeit von 60 min vor der Hydrolyse beendet durch Zugabe von 160 ml 80 ° C DI-Wasser.
- Verdünne 0,5 mL des abgetasteten Hydrolysat für Zucker und Säurekonzentration analysiert. 15 Beachten Sie die verbleibende Hydrolysat Probe für die Kristallisation stattfindet , während gurren auf Raumtemperatur.
- Trennung des Hydrolysats aus dem hydrolysierten Pulpe durch Vakuumfiltration ein Filterpapier in einem Büchner-Trichter.
ANMERKUNG: Diese Trennung muss sehr schnell erfolgen, bevor die Temperatur sinkt und die Säureginnt aus der Lösung zu kristallisieren. Aufgrund der hohen Ionenstärke aus der Säurelösung, das Agglomerat in Hydrolyse erzeugt der CNC und mit den FCSR Residuen bleiben. Ungefähr 80-90% der Säure wird mit dem Filtrat entfernt werden.
3. CNC-Trennung
- Waschen Sie die gefilterten Feststoffe aus dem Abschnitt 2 DI Wasser und verdünnt mit VE-Wasser auf etwa 1% Gesamtfeststoffe. Zentrifuge das Filtrat bei 11.960 × g für 10 min.
- Dekantieren aus den Überstand. Wiederholen Sie den Wasch- und Filtrationsverfahren unter Verwendung von frischem DI-Wasser, bis der Überstand trüb ist. Die Trübung zeigt an, dass die Ionenstärke der Lösung genug gefallen ist, damit die CNC zu zerstreuen und kolloidalem zu werden beginnen.
- Mischen Sie die trübe Überstand mit der gefestigten hydrolysierte Zellstoff (2.3). Dialysieren der Mischung in einem Dialyseschlauch (MWCO 14 kDa) unter Verwendung von entionisiertem Wasser, bis die Leitfähigkeit der Flüssigkeit deionisiertes Wasser nähert sich das. Messen Sie die Leitfähigkeit mit einem Leitfähigkeitsmessgerät.
- Zentrifuge die dialysierte Probe bei 3.500 xg für 10 min eine CNC-Dispersion in der wässrigen Phase zu erhalten. Behalten Sie den Niederschlag Phase, dh FCSR, für CNF - Produktion.
- Bestimmen Sie CNC - Ausbeute aus der gemessenen Menge der CNC in der Dispersion einen CSB - Verfahren unter Verwendung von zuvor beschriebenen 3, 18.
4. CNF Produktion
- Bestimmen Sie die Ausbeute an gefälltem FCSR durch gravimetrische Messungen nach der CNC-Dispersion zu trennen. Trocknen Sie die FCSR bei 105 ° C und messen Sie den Ofen Trockengewicht des FCSR bezogen auf die anfängliche Ofentrockengewicht von BEP oder UMHP Fasern verwendet.
- fibrillate Mechanisch die FCSR bei Fasersuspension von 0,5% durch nacheinander die Suspension 3 mal durch ein 200 & mgr; m Öffnung Kammer, die durch 2 mal durch eine 87 & mgr; m Öffnung Kammer, die alle bei 100 MPa gefolgt vorbei.
5. Rasterkraftmikroskopie (AFM) Imaging
- Beschallen etwa 0,01 Gew% CNC oder CNF suspensions für 2 min. Abzuscheiden einen Tropfen der dispergierten Suspension auf einem Glimmersubstrat. Der Luft trocknen die abgeschiedene Suspension bei Umgebungstemperatur.
- Nehmen Sie AFM-Aufnahmen der luftgetrockneten CNCs und CNF in vibrierenden Tapping Mode Protokoll des Herstellers verwendet wird. Analysieren Sie die AFM-Aufnahmen von ca. 100 einzelnen CNC-Steuerungen oder CNF kommerzielle Software mit Durchmesser und Längenverteilungen zu erhalten.
6. Fourier-Transformation Inferred (FTIR) Messungen
- Verwenden Sie einen kommerziellen FTIR-Spektrophotometer mit einem universellen abgeschwächte-Totalreflexion (ATR) Sonde die resultierenden CNC und CNF Proben zusammen mit dem Original BEP und UMHP Fasern zu analysieren Estergruppen zu identifizieren.
- Notieren Sie sich die Absorptionsspektren der Proben in einem Wellenlängenbereich zwischen 450 - 4000 cm -1 mit einer Auflösung von 4 cm -1 und 4 Scans für jede Probe.
7. konduktometrische Titration
- Verwenden Sie konduktometrische Titration quantify der Carboxylgruppe Inhalt von Proben aus der Veresterung von Dicarbonsäure geführt.
- In CNC oder CNF Suspension mit 50 mg (OD) von CNC-Steuerungen oder CNF in 120 ml 1 mM NaCl-Lösung. Daraufhin wird die Mischung von etwa 0,2 ml Zugabe von 2 mM NaOH-Lösung bei 30 s-Intervallen.
- Messen Sie die Leitfähigkeit mit einem Leitfähigkeitsmessgerät. Finden Sie den Wendepunkt (der tiefste Punkt) auf der Leitfähigkeitskurve im Verlauf NaOH hinzuzufügen.
- Berechne die Menge der Carboxylgruppen (mmol / L) auf der Basis der verbrauchten NaOH relativ zu dem Wendepunkt die folgende Gleichung verwendet , in der c die Konzentration der NaOH - Lösung (mol / L), V das Volumen an zugegebenem NaOH - Lösung (ml ), m die Masse von CNC - Steuerungen oder CNF in OD Gewicht (g).
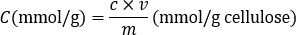
8. CNC und CNF Thermische Stabilitätsbestimmung
- thermischer Abbau Messungen von t Verhaltener CNC und CNF Proben durch thermogravimetrische Analyse (TGA).
- Spülen des Ofens einen hochreinen Stickstoffstrom bei 20 ml / min zu verhindern unerwünschte oxidative Zersetzung verwendet wird. Trocknen der Proben bei 50 ° C für 4 h vor dem Test. Verwenden Sie eine Probengröße von 5 mg in Trockengewicht.
- Das Gewicht der Probe als die Ofentemperatur von Raumtemperatur bis 600 ° C bei einer Erwärmungsrate von 10 ° C / min erhöht wird.
- Normalisieren der gemessenen Gewichtsverlust durch das Anfangsgewicht.
- Führen Sie getrennte thermische Stabilitätstests von CNC und CNF-Proben in einem Ofen bei 105 ° C. Notieren Sie sich die Farbveränderung der Proben nach 4 und 24 h nach der konventionellen Fotografie.
9. X-ray Diffraction
- Press gefriergetrocknetem CNC oder CNF Proben bei 180 MPa Pellets zu machen, wie zuvor beschrieben. 5 Durchführung Weitwinkel-Röntgenbeugungsmessungen des Pellets unter Verwendung von Cu-Ka - Strahlung auf einem Röntgendiffraktometer im 2θ Bereich von 10-38° in Schritten von 0,02 °.
- Berechnen Sie die Kristallinität Index (CRI) von einem Pellet die Segal Verfahren unter Verwendung von 19 (ohne Grundlinie Subtraktion).
Ergebnisse
Typische AFM - Bilder der CNC und CNF von BEP und UMHP zusammen mit entsprechenden SEM - Bilder der Speisesäure hydrolysiert Fasern sind in den 1 und 2 dargestellt. Die Bilder zeigen deutlich die erhebliche Reduzierung der Faserlänge durch saure Hydrolyse mit einer minimalen Änderung in Faserdurchmesser (Abbildung 1a mit 1b verglichen und 2a mit 2b). Die verkürzte Faserlänge wurde durch den gemessenen Cellulose Pol...
Diskussion
Die dickeren CNC Durchmesser der CNC Proben aus Maleinsäure Hydrolyse führte zu einer moderaten mittleren Aspektverhältnis 7,24 und 8,53 für die CNCs von BEP und UMHP bzw. trotz ihrer langen Längen wie oben diskutiert. Die CNFs hatte eine größere Länge und einen dünneren Durchmesser, die in einem großen Aspektverhältnis von 13,9 und 19,0 resultiert, für die CNCs von BEP und UMHP jeweils beide größer als ihre jeweiligen CNCs. Es ist möglich, starke mechanische Fibrillation zu verwenden CNF Durchmesser zu r...
Offenlegungen
Chen und Zhu sind Miterfinder einer Patentanmeldung US Dicarbonsäuren für CNC und CNF Produktion verwendet wird.
Danksagungen
Diese Arbeit wurde durchgeführt, während Bian, Chen und Wang Ph.D. waren zu Besuch Studenten an der US Forest Service, Forest Products Laboratory (FPL), Madison, WI, und auf offiziellen Regierungszeit von Zhu. Diese Arbeit wurde teilweise durch die USDA Landwirtschaft und Ernährung Research Initiative (AFRI) Competitive Grant (Nr 2011-67009-20056), der chinesischen Staatlichen Forstverwaltung (Projekt Nr 2015-4-54), der National Natural Science Foundation unterstützt von China (Projekt-Nr 31470599), Guangzhou Elite Project of China und China Scholarship Fund. Die Finanzierung aus diesen Programmen die Besuchstermine von Bian, Chen und Wang bei FPL möglich.
Materialien
| Name | Company | Catalog Number | Comments |
| Bleached eucalypus pulp | Aracruz Cellulose | ||
| Unbleached mixed hardwood kraft pulp | International Paper | ||
| Maleic acid | Sigma-Aldrich | M0375-1KG/CAS110-16-7 | Powder; assay: 99.0% (HPLC) |
| Glycerol | Sigma-Aldrich | G5516-4L/CAS56-81-5 | |
| Sodium hydroxide | Fisher Scientific | S318-500/CAS1310-73-2, 497-19-8 | Certified ACS |
| Sodium chloride | Mallinckrodt | 7581-12/CAS7647-14-5 | Crystal,AR |
| Cupriethylenediamine solution | GFS Chemicals | E32103-1L/CAS14552-35-3 | 1 M, for determination of solution viscosity of pulps |
| Acetone | Fisher Scientific | A18-500/CAS67-64-1 | Certified ACS |
| Accu-TestTM Vials for COD Testing | Bioscience,Inc. | 01-215-28 | COD testing for 20 to 900 mg/L standard range concentration |
| Heating plate | IKA | Mode: C-MAD HS7 digital | |
| Magnetic stir bar | ACE Glass | ||
| Pyrex three-neck round-bottom flask | Sigma-Aldrich | CLS4965B500-1EA | |
| Dialysis tubing cellulose membrane | Sigma-Aldrich | D9402-100FT | Typical molecular weight cut-off = 14,000 kDa |
| Disposable aluminum dishes | Sigma-Aldrich | Z154857-1PAK | Circles, 60 mm |
| Disintegrator | Testing Machines Inc.(TMI) | ||
| Microfluidizer | Microfluidics Corporation | ||
| Sonicator | Qsonica LLC. | Mode: 3510R-MT, 50-60 Hz, 180 W | |
| Zeta potential analyzer | Brookhaven Instruments Corporation | ||
| FTIR | PerkinElmer | ||
| Conductometric titrator | Yellow Springs Instrument (YSI) | ||
| TGA analyzer | PerkinElmer | ||
| X-ray diffractometer | Bruker Corporation | ||
| AFM imging | AFM Workshop | ||
| SEM imaging | Carl Zeiss |
Referenzen
- Giese, M., Blusch, L. K., Khan, M. K., MacLachlan, M. J. Functional Materials from Cellulose-Derived Liquid-Crystal Templates. Angew Chem Int Ed. 54 (10), 2888-2910 (2015).
- Zhu, H., et al. Wood-Derived Materials for Green Electronics, Biological Devices, and Energy Applications . Chem. Rev. , (2016).
- Wang, Q. Q., et al. Approaching zero cellulose loss in cellulose nanocrystal (CNC) production: recovery and characterization of cellulosic solid residues (CSR) and CND. Cellulose. 19 (6), 2033-2047 (2012).
- Hamad, W. Y., Hu, T. Q. Structure-process-yield interrelations in nanocrystalline cellulose extraction. Can J Chem Eng. 88 (3), 392-402 (2010).
- Chen, L. H., et al. Tailoring the yield and characteristics of wood cellulose nanocrystals (CNC) using concentrated acid hydrolysis. Cellulose. 22 (3), 1753-1762 (2015).
- Mukherjee, S. M., Woods, H. J. X-ray and electron microscope studies of the degradation of cellulose by sulphuric acid. Biochim Biophys Acta. 10 (4), 499-511 (1953).
- Camarero Espinosa, S., Kuhnt, T., Foster, E. J., Weder, C. Isolation of thermally stable cellulose nanocrystals by phosphoric acid hydrolysis. Biomacromolecules. 14 (4), 1223-1230 (2013).
- Yu, H. Y., et al. Facile extraction of thermally stable cellulose nanocrystals with a high yield of 93% through hydrochloric acid hydrolysis under hydrothermal conditions. J Mater Chem, A. 1 (12), 3938-3944 (2013).
- Leung, A. C. W., et al. Characteristics and properties of carboxylated cellulose nanocrystals prepared from a novel one-step procedure. Small. 7 (3), 302-305 (2011).
- Saito, T., Isogai, A. TEMPO-mediated oxidation of native cellulose. The effect of oxidation conditions on chemical and crystal structures of the water-insoluble fractions. Biomacromolecules. 5 (5), 1983-1989 (2004).
- Yang, H., Chen, D. Z., van de Ven, T. G. M. Preparation and characterization of sterically stabilized nanocrystalline cellulose obtained by periodate oxidation of cellulose fibers. Cellulose. 22 (3), 1743-1752 (2015).
- Huang, Y. B., Fu, Y. Hydrolysis of cellulose to glucose by solid acid catalysts. Green Chem. 15 (5), 1095-1111 (2013).
- Shimizu, K. I., Satsuma, A. Toward a rational control of solid acid catalysis for green synthesis and biomass conversion. Energy & Environ Sci. 4 (9), 3140-3153 (2011).
- Wang, Q. Q., Zhu, J. Y., Considine, J. M. Strong and optically transparent films prepared using cellulosic solid residue (CSR) recovered from cellulose nanocrystals (CNC) production waste stream. ACS Appl Mater Interfaces. 5 (7), 2527-2534 (2013).
- Chen, L. H., Zhu, J. Y., Baez, C., Kitin, P., Elder, T. Highly thermal-stable and functional cellulose nanocrystals and nanofibrils produced using fully recyclable organic acids. Green Chem. 18, 3835-3843 (2016).
- Fischer, E., Speier, A. Darstellungder der Ester. Chemische Berichte. 28 (3), 3252-3258 (1895).
- Allen, T. C., Cuculo, J. A. Cellulose derivatives containing carboxylic acid groups. J Polym Sci: Macromol Rev. 7 (1), 189-262 (1973).
- Wang, Q. Q., Zhao, X. B., Zhu, J. Y. Kinetics of strong acid hydrolysis of a bleached kraft pulp for producing cellulose nanocrystals (CNCs). Ind Eng Chem Res. 53 (27), 11007-11014 (2014).
- Segal, L., Creely, J. J., Martin, A. E., Conrad, C. M. An empirical method for estimating the degree of crystallinity of native cellulose using the X-ray diffractometer. Text Res J. 29 (10), 786-794 (1959).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten