È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Produzione Verde e basso costo di termicamente stabile e carbossilati cellulosa nanocristalli e Nanofibrils Utilizzando altamente riciclabile bicarbossilici Acidi
In questo articolo
Riepilogo
Qui mostriamo un nuovo metodo per produzioni verdi e sostenibili di nanocristalli altamente termicamente stabili e carbossilati di cellulosa (CNC) e nanofibrils (CNF) utilizzando acidi dicarbossilici solidi altamente riciclabili.
Abstract
Qui mostriamo potenzialmente a basso costo e produzioni verdi di nanocristalli alti termicamente stabili e carbossilati di cellulosa (CNC Strumenti) e nanofibrils (CNF) da sbiancanti di eucalipto (BEP) e fibre grezze di legno duro misto polpa kraft (UMHP) utilizzando acidi solidi dicarbossilici altamente riciclabile. Condizioni operative tipiche erano le concentrazioni di acido di 50 - 70% in peso a 100 ° C per 60 min a 120 ° C (senza ebollizione a pressione atmosferica) per 120 min, per BEP e UMHP rispettivamente. I CNC risultanti hanno una temperatura di degradazione termica superiore loro fibre mangimi corrispondenti e contenuto di gruppi di acido carbossilico 0,2-0,4 mmol / g. La resistenza bassa (alta pKa di 1,0-3,0) di acidi organici ha portato anche in CNC con entrambe le lunghezze di circa 239-336 nm e superiori cristallinità di CNC prodotta con acidi minerali. perdita di cellulosa in zuccheri è stato minimo. Fibroso cellulosico residuo solido (FCSR) dall'idrolisi acido bicarbossilico è stato usato perprodurre CNFs carbossilati attraverso successive fibrillazione meccanica con l'input di energia a basso.
Introduzione
Lo sviluppo economico sostenibile richiede non solo con materie prime che sono rinnovabile e biodegradabile, ma utilizza anche tecnologie di produzione rispettosi verdi ed ambientali per produrre una varietà di prodotti biologici e biochimici di queste materie prime rinnovabili. Nanomateriali di cellulosa, come nanocristalli di cellulosa (CNC) e nanofibrils cellulosa (CNF), prodotto da lignocellulosa rinnovabili sono biodegradabili e hanno proprietà meccaniche e ottiche uniche adatte per lo sviluppo di una gamma di bioprodotti 1, 2. Purtroppo, le tecnologie esistenti per la produzione di nanomateriali di cellulosa sono sia ad alta intensità energetica quando si utilizza la fibrillazione meccanica pura o insostenibili per l'ambiente a causa della non-riciclaggio o insufficiente riciclaggio di prodotti chimici di lavorazione, come ad esempio quando si utilizza il processo di idrolisi acido minerale concentrato 3-8 o ossidazione metodi 9- 11. Inoltre, i metodi di ossidazione possono anche produrre compo tossici per l'ambienteunds reagendo con lignocellulosa. Pertanto, lo sviluppo di tecnologie di produzione verdi per la produzione di nanomateriali di cellulosa è di fondamentale importanza per fare pieno uso del materiale abbondante e rinnovabile - lignocellulosa.
Utilizzando idrolisi acida per sciogliere emicellulosa e depolimerizzano cellulosa è un approccio efficace per la produzione di nanomateriali di cellulosa. Acidi solidi sono stati utilizzati per la produzione di zucchero cellulosa con il vantaggio di facilitare il recupero acido 12, 13. Studi precedenti che utilizzano acidi minerali concentrati indicato che una concentrazione di acido inferiore migliorato rendimento CNC e cristallinità 3, 5. Questo suggerisce che un acido forte può danneggiare i cristalli di cellulosa, mentre una idrolisi acida più mite potrebbe migliorare le proprietà e la resa dei nanomateriali di cellulosa attraverso l'approccio della produzione integrata e CNC con CNF 3, 14. Qui documentiamo un metodo che utilizza concentrato solido acidi dicarbossilici idrolisi di produe CNC con CNF 15. Questi acidi dicarbossilici hanno una bassa solubilità a temperature basse o ambientali, e quindi possono essere facilmente recuperate attraverso la tecnologia di cristallizzazione matura. Hanno anche buona solubilità a temperature elevate che facilita idrolisi acido concentrato senza bollire o utilizzando contenitori a pressione. Poiché questi acidi hanno una maggiore pKa di acidi minerali tipici utilizzati per la produzione CNC, loro uso comporta in buono cristallinità CNC, e nonostante rese inferiori CNC, con una notevole quantità di fibrose residuo solido cellulosiche (FCSR o fibre parzialmente idrolizzate) rimanenti causa depolimerizzazione della cellulosa incompleta. La FCSR può essere usato per produrre CNF attraverso successive fibrillazione meccanica utilizzando gli ingressi a basso consumo energetico. Pertanto, la perdita di cellulosa in zuccheri è minima rispetto all'utilizzo acidi minerali.
È noto che gli acidi carbossilici possono esterificare cellulosa attraverso Fisher-Speier esterificazione 16. Applicando acidi dicarbossilici di cellulosa può risultare in semi-acido esteri non-reticolati 17 (o carbossilazione), per produrre carbossilato CNC e CNF come abbiamo dimostrato 15 precedenza. Il metodo documentato qui può produrre carbossilato e termicamente stabile CNF e CNC che è anche altamente cristallino da polpe o sbiancato o greggi, pur avendo il recupero chimico relativamente semplice e alta e l'utilizzo di ingressi a basso consumo energetico.
Protocollo
NOTA: sbiancato eucalyptus kraft pulp (BEP) e non sbiancata di legno duro misto polpa kraft (UMHP) fibre provenienti da fonti commerciali sono stati utilizzati come materia prima per la produzione CNC e CNF. maleico commerciali acquistati sono stati utilizzati per l'idrolisi. condizioni di idrolisi erano concentrazioni di acido di 60% in peso a 100 ° C per 60 min a 120 ° C (senza ebollizione a pressione atmosferica) per 120 min, per BEP e UMHP rispettivamente.
1. Preparazione della soluzione concentrata di acidi dicarbossilici
- Calore 40 mL di acqua deionizzata (DI) in un pallone a più collo in un bagno di glicerolo liquido su una piastra di riscaldamento a circa 85 ° C.
- Aggiungere 60 g anidro acido maleico nel pallone per fare una soluzione al 60% in peso di agitazione magnetica. Utilizzando le densità delle soluzioni acide segnalati in precedenza 15, calcolare la quantità necessaria di acqua e acido per rendere la soluzione di acido alla concentrazione massa specificata.
- Riscaldare la soluzione al detemperatura di idrolisi desiderata di 100 o 120 ° C (senza ebollizione dovuta a concentrazioni elevate di acidi dicarbossilici).
2. L'idrolisi di reazione
- Una volta che la soluzione acida è a temperatura, si aggiungono 10 g forno essiccati (OD) di fibre BEP o UMHP in 80 mL di soluzione di acido dicarbossilico (1.1) con agitazione continua.
- Prendere una aliquota della idrolizzato acido (circa 2 ml) al termine del tempo di reazione predeterminata di 60 min prima di terminare idrolisi aggiungendo 160 ml di 80 ° C acqua deionizzata.
- Diluire 0,5 ml di idrolizzato campionata zucchero e analizza concentrazione dell'acido. 15 Osservare il campione idrolizzato rimanente per la cristallizzazione che si svolgono durante tubare fino a temperatura ambiente.
- Separare l'idrolizzato dalla polpa idrolizzato mediante filtrazione sotto vuoto usando una carta da filtro in un imbuto Buchner.
NOTA: Questa separazione deve avvenire piuttosto rapidamente prima scende la temperatura e l'acido siagin a cristallizzare dalla soluzione. Grazie alla elevata forza ionica della soluzione acida, generato idrolisi agglomerato e del CNC stare con i residui FCSR. Circa 80-90% di acido viene rimosso con il filtrato.
3. Separazione CNC
- Lavare i solidi filtrati dalla sezione 2 con acqua deionizzata e diluire a circa l'1% di solidi totali con acqua deionizzata. Centrifugare il filtrato a 11.960 xg per 10 min.
- Decantare il surnatante. Ripetere il processo di lavaggio e filtrazione con acqua DI fresca fino a quando il surnatante è torbida. La torbidità indica che la forza ionica della soluzione è caduto abbastanza per il CNC disperdere e inizia a diventare colloidale.
- Mescolare il surnatante torbido con la polpa idrolizzato costante (2.3). Dializzare la miscela in un sacchetto di dialisi (MWCO 14 kDa) con acqua deionizzata fino alla conducibilità del liquido si avvicina a quella di acqua deionizzata. Misurare la conduttività utilizzando un misuratore di conduttanza.
- Centrifugare il campione dializzato a 3.500 xg per 10 minuti per ottenere una dispersione CNC nella fase acquosa. Conservare la fase precipitato, vale a dire, FCSR, per la produzione di CNF.
- Determinare resa CNC dalla quantità misurata di CNC nella dispersione utilizzando un metodo COD descritto precedentemente 3, 18.
4. CNF Produzione
- Determinare la resa di FCSR precipitato da misure gravimetriche dopo la separazione della dispersione CNC. Essiccare il FCSR a 105 ° C e misurare il peso secco del forno del FCSR rispetto al peso secco del forno iniziale di BEP o fibre UMHP utilizzato.
- Meccanicamente fibrillazione il FCSR alla sospensione di fibre di 0,5% in consecutivamente passando sospensione 3 volte attraverso una camera di orifizio 200 micron seguita da 2 volte attraverso una camera orifizio di 87 micron, il tutto a 100 MPa.
5. microscopia a forza atomica (AFM) Imaging
- Sonicare circa il 0,01% in peso CNC o CNF suspensions per 2 min. Deposita una goccia di sospensione dispersa su un substrato di mica. Far asciugare la sospensione depositato a temperatura ambiente.
- Prendere immagini AFM dei CNC con aria secca e CNFs in vibrazione modalità tapping utilizzando il protocollo del produttore. Analizzare le immagini AFM di circa 100 singoli CNC o CNFs utilizzando il software commerciale per ottenere diametro e lunghezza distribuzioni.
6. Fourier Transform dedurre (FTIR) Misure
- Utilizzare uno spettrofotometro FTIR commerciale con una sonda universale attenuato-totale-riflessione (ATR) per analizzare i campioni CNC e CNF risultanti insieme con il BEP originale e fibre UMHP per identificare gruppi estere.
- Registra gli spettri di assorbimento dei campioni in un intervallo di lunghezza d'onda tra 450 - 4.000 centimetri -1 con una risoluzione di 4 cm -1 e 4 scansioni per ogni campione.
7. titolazione conduttimetrica
- Utilizzare titolazione conduttimetrica a QUAntify carbossile contenuto del gruppo di campioni risultato di esterificazione dall'acido dicarbossilico.
- Aggiungere sospensione CNC o CNF con 50 mg (OD) del CNC o CNFs in 120 ml di soluzione 1 mM NaCl. Titolare l'impasto con l'aggiunta di circa 0,2 ml di soluzione 2 mM di NaOH ad intervalli di 30 s.
- Misurare la conduttività utilizzando un misuratore di conduttanza. Trovare il punto di flesso (il punto più basso) sulla curva conduttività nel corso di aggiunta di NaOH.
- Calcolare la quantità di gruppi carbossilici (mmol / L) in base al consumo di NaOH in relazione al punto di flesso utilizzando la seguente equazione in cui c è la concentrazione della soluzione di NaOH (mol / L), v è il volume di soluzione di NaOH (mL ), m è la massa del CNC o CNFs peso OD (g).
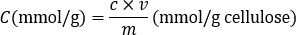
8. CNC e CNF termica Determinazione di stabilità
- Condurre le misure di degradazione termica di tegli CNC e CNF campioni per analisi termogravimetrica (TGA).
- Eliminare il forno con un flusso di azoto ad alta purezza a 20 mL / min per impedire ogni decomposizione ossidativa indesiderato. Essiccare i campioni a 50 ° C per 4 ore prima del test. Utilizzare un campione di 5 mg di peso secco.
- Registrare il peso del campione come la temperatura del forno viene aumentata da ambiente a 600 ° C ad una velocità di riscaldamento di 10 ° C / min.
- Normalizzare la perdita di peso misurato dal peso iniziale.
- Eseguire separati prove di stabilità termica di campioni CNC e CNF in stufa a 105 ° C. Registrare il cambiamento di colore dei campioni dopo 4 e 24 ore di fotografia convenzionale.
Diffrazione a raggi X 9.
- Premere liofilizzato campioni CNC o CNF a 180 MPa per rendere pellets come descritto in precedenza. 5 condotta grandangolo misurazioni diffrazione dei raggi X del pellet usando radiazione Cu-Kα su un diffrattometro a raggi X nel campo 2θ di 10 - 38° a passi di 0,02 °.
- Calcolare l'indice di cristallinità (CRI) di un pellet con il metodo Segal 19 (senza base linea di sottrazione).
Risultati
Immagini AFM tipici del CNC e CNF da BEP e UMHP insieme con corrispondenti immagini SEM delle fibre idrolizzato acido mangimi sono illustrati nelle figure 1 e 2. Le immagini mostrano chiaramente le sostanziali riduzioni di lunghezza della fibra per idrolisi acida con minime modificazioni della diametri delle fibre (a confronto con la Figura 1a 1b e 2a con 2b). La lunghezza della fibra abbreviato si riflette anche dal gr...
Discussione
I diametri CNC spessore dei campioni CNC da idrolisi acido maleico determinato una moderata rapporto medio 7.24 e 8.53, per i CNC rispettivamente da BEP e UMHP, nonostante le loro lunghezze come discusso sopra. Il CNFs aveva una lunghezza e un diametro più sottile, che ha provocato una grande aspect ratio di 13,9 e 19,0, per il CNC rispettivamente da BEP e UMHP, sia superiore alla loro rispettiva CNC. È possibile utilizzare grave fibrillazione meccanica per ridurre il diametro CNF per migliorare il rapporto di aspetto...
Divulgazioni
Chen Zhu e sono co-inventori di una domanda di brevetto statunitense usando acidi dicarbossilici per la produzione CNC e CNF.
Riconoscimenti
Questo lavoro è stato condotto mentre Bian, Chen, e Wang sono stati in visita Ph.D. studenti presso l'US Forest Service, Forest Products Laboratory (FPL), Madison, WI, e sul tempo ufficiale del governo di Zhu. Questo lavoro è stato parzialmente supportato dal USDA Agriculture and Food Research Initiative (AFRI) Sovvenzione competitivo (n ° 2011-67009-20056), i cinesi Amministrazione Forestale di Stato (Progetto n ° 2015-4-54), la National Science Foundation Naturale La Cina (Progetto n ° 31.470.599), Guangzhou Elite Progetto della Cina, e la Cina Scholarship Fund. Il finanziamento di questi programmi ha reso gli appuntamenti di visita di Bian, Chen, e Wang a FPL possibile.
Materiali
| Name | Company | Catalog Number | Comments |
| Bleached eucalypus pulp | Aracruz Cellulose | ||
| Unbleached mixed hardwood kraft pulp | International Paper | ||
| Maleic acid | Sigma-Aldrich | M0375-1KG/CAS110-16-7 | Powder; assay: 99.0% (HPLC) |
| Glycerol | Sigma-Aldrich | G5516-4L/CAS56-81-5 | |
| Sodium hydroxide | Fisher Scientific | S318-500/CAS1310-73-2, 497-19-8 | Certified ACS |
| Sodium chloride | Mallinckrodt | 7581-12/CAS7647-14-5 | Crystal,AR |
| Cupriethylenediamine solution | GFS Chemicals | E32103-1L/CAS14552-35-3 | 1 M, for determination of solution viscosity of pulps |
| Acetone | Fisher Scientific | A18-500/CAS67-64-1 | Certified ACS |
| Accu-TestTM Vials for COD Testing | Bioscience,Inc. | 01-215-28 | COD testing for 20 to 900 mg/L standard range concentration |
| Heating plate | IKA | Mode: C-MAD HS7 digital | |
| Magnetic stir bar | ACE Glass | ||
| Pyrex three-neck round-bottom flask | Sigma-Aldrich | CLS4965B500-1EA | |
| Dialysis tubing cellulose membrane | Sigma-Aldrich | D9402-100FT | Typical molecular weight cut-off = 14,000 kDa |
| Disposable aluminum dishes | Sigma-Aldrich | Z154857-1PAK | Circles, 60 mm |
| Disintegrator | Testing Machines Inc.(TMI) | ||
| Microfluidizer | Microfluidics Corporation | ||
| Sonicator | Qsonica LLC. | Mode: 3510R-MT, 50-60 Hz, 180 W | |
| Zeta potential analyzer | Brookhaven Instruments Corporation | ||
| FTIR | PerkinElmer | ||
| Conductometric titrator | Yellow Springs Instrument (YSI) | ||
| TGA analyzer | PerkinElmer | ||
| X-ray diffractometer | Bruker Corporation | ||
| AFM imging | AFM Workshop | ||
| SEM imaging | Carl Zeiss |
Riferimenti
- Giese, M., Blusch, L. K., Khan, M. K., MacLachlan, M. J. Functional Materials from Cellulose-Derived Liquid-Crystal Templates. Angew Chem Int Ed. 54 (10), 2888-2910 (2015).
- Zhu, H., et al. Wood-Derived Materials for Green Electronics, Biological Devices, and Energy Applications . Chem. Rev. , (2016).
- Wang, Q. Q., et al. Approaching zero cellulose loss in cellulose nanocrystal (CNC) production: recovery and characterization of cellulosic solid residues (CSR) and CND. Cellulose. 19 (6), 2033-2047 (2012).
- Hamad, W. Y., Hu, T. Q. Structure-process-yield interrelations in nanocrystalline cellulose extraction. Can J Chem Eng. 88 (3), 392-402 (2010).
- Chen, L. H., et al. Tailoring the yield and characteristics of wood cellulose nanocrystals (CNC) using concentrated acid hydrolysis. Cellulose. 22 (3), 1753-1762 (2015).
- Mukherjee, S. M., Woods, H. J. X-ray and electron microscope studies of the degradation of cellulose by sulphuric acid. Biochim Biophys Acta. 10 (4), 499-511 (1953).
- Camarero Espinosa, S., Kuhnt, T., Foster, E. J., Weder, C. Isolation of thermally stable cellulose nanocrystals by phosphoric acid hydrolysis. Biomacromolecules. 14 (4), 1223-1230 (2013).
- Yu, H. Y., et al. Facile extraction of thermally stable cellulose nanocrystals with a high yield of 93% through hydrochloric acid hydrolysis under hydrothermal conditions. J Mater Chem, A. 1 (12), 3938-3944 (2013).
- Leung, A. C. W., et al. Characteristics and properties of carboxylated cellulose nanocrystals prepared from a novel one-step procedure. Small. 7 (3), 302-305 (2011).
- Saito, T., Isogai, A. TEMPO-mediated oxidation of native cellulose. The effect of oxidation conditions on chemical and crystal structures of the water-insoluble fractions. Biomacromolecules. 5 (5), 1983-1989 (2004).
- Yang, H., Chen, D. Z., van de Ven, T. G. M. Preparation and characterization of sterically stabilized nanocrystalline cellulose obtained by periodate oxidation of cellulose fibers. Cellulose. 22 (3), 1743-1752 (2015).
- Huang, Y. B., Fu, Y. Hydrolysis of cellulose to glucose by solid acid catalysts. Green Chem. 15 (5), 1095-1111 (2013).
- Shimizu, K. I., Satsuma, A. Toward a rational control of solid acid catalysis for green synthesis and biomass conversion. Energy & Environ Sci. 4 (9), 3140-3153 (2011).
- Wang, Q. Q., Zhu, J. Y., Considine, J. M. Strong and optically transparent films prepared using cellulosic solid residue (CSR) recovered from cellulose nanocrystals (CNC) production waste stream. ACS Appl Mater Interfaces. 5 (7), 2527-2534 (2013).
- Chen, L. H., Zhu, J. Y., Baez, C., Kitin, P., Elder, T. Highly thermal-stable and functional cellulose nanocrystals and nanofibrils produced using fully recyclable organic acids. Green Chem. 18, 3835-3843 (2016).
- Fischer, E., Speier, A. Darstellungder der Ester. Chemische Berichte. 28 (3), 3252-3258 (1895).
- Allen, T. C., Cuculo, J. A. Cellulose derivatives containing carboxylic acid groups. J Polym Sci: Macromol Rev. 7 (1), 189-262 (1973).
- Wang, Q. Q., Zhao, X. B., Zhu, J. Y. Kinetics of strong acid hydrolysis of a bleached kraft pulp for producing cellulose nanocrystals (CNCs). Ind Eng Chem Res. 53 (27), 11007-11014 (2014).
- Segal, L., Creely, J. J., Martin, A. E., Conrad, C. M. An empirical method for estimating the degree of crystallinity of native cellulose using the X-ray diffractometer. Text Res J. 29 (10), 786-794 (1959).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon