Method Article
Aktivierung und Konjugation löslicher Polysaccharide unter Verwendung von 1-Cyano-4-Dimethylaminopyridintetrafluoroborat (CDAP)
In diesem Artikel
Erratum Notice
Zusammenfassung
Proteine und aminhaltige Liganden können kovalent mit Polysacchariden verknüpft werden, die durch das Cyanylierungsreagenz 1-Cyano-4-dimethylaminopyridintetrafluoroborat (CDAP) aktiviert werden, um kovalente Protein-(Liganden)-Polysaccharid-Konjugate zu bilden. Dieser Artikel beschreibt ein verbessertes Protokoll für die Durchführung einer kontrollierten CDAP-Aktivierung bei 0 °C und variierendem pH-Wert und die anschließende Konjugation der aktivierten Polysaccharide.
Zusammenfassung
Konjugierte Impfstoffe sind bemerkenswerte Fortschritte in der Vakzinologie. Für die Herstellung von Polysaccharid-Konjugat-Impfstoffen können die Polysaccharide mit 1-Cyano-4-Dimethylaminopyridintetrafluoroborat (CDAP), einem einfach zu handhabenden cyylierenden Reagenz, bequem funktionalisiert und mit Impfstoffträgerproteinen verknüpft werden. CDAP aktiviert Polysaccharide, indem es mit Kohlenhydrathydroxylgruppen bei pH 7-9 reagiert. Die Stabilität und Reaktivität von CDAP sind stark pH-abhängig. Der pH-Wert der Reaktion sinkt auch während der Aktivierung aufgrund der Hydrolyse von CDAP, was eine gute pH-Kontrolle zum Schlüssel für eine reproduzierbare Aktivierung macht. Das ursprüngliche CDAP-Aktivierungsprotokoll wurde bei Raumtemperatur in ungepufferten pH-9-Lösungen durchgeführt.
Aufgrund der schnellen Reaktion unter dieser Bedingung (<3 min) und des damit einhergehenden schnellen pH-Abfalls aus der schnellen CDAP-Hydrolyse war es schwierig, den Zielreaktions-pH-Wert in kurzer Zeit schnell anzupassen und aufrechtzuerhalten. Das hier beschriebene verbesserte Protokoll wird bei 0 °C durchgeführt, was die CDAP-Hydrolyse verlangsamt und die Aktivierungszeit von 3 min auf ~15 min verlängert. Dimethylaminopyridin (DMAP) wurde auch als Puffer verwendet, um die Polysaccharidlösung vor der Zugabe des CDAP-Reagens an den pH-Wert der Zielaktivierung anzupassen. Die längere Reaktionszeit, gepaart mit der langsameren CDAP-Hydrolyse und der Verwendung von DMAP-Puffer, erleichtert die Aufrechterhaltung des Aktivierungs-pH-Werts für die gesamte Dauer des Aktivierungsprozesses. Das verbesserte Protokoll macht den Aktivierungsprozess weniger hektisch, reproduzierbarer und skalierbarer.
Einleitung
Konjugierte Impfstoffe, wie sie aus Polysacchariden bestehen, die kovalent mit einem Trägerprotein verbunden sind, gehören zu den bemerkenswerten Fortschritten in der Vakzinologie1,2. Polysaccharide sind als T-Zell-unabhängige Antigene bei Säuglingen schlecht immunogen und induzieren kein Gedächtnis, Klassenwechsel oder Affinitätsreifung von Antikörpern3. Diese Mängel werden in Polysaccharid-Konjugat-Impfstoffen überwunden4. Da die meisten Polysaccharide keinen geeigneten chemischen Griff für die Konjugation haben, müssen sie zuerst reaktiv oder "aktiviert" werden. Das aktivierte Polysaccharid wird dann entweder direkt mit dem Protein (oder modifizierten Protein) verknüpft oder vor der Konjugation zur zusätzlichen Derivatisierung funktionalisiert4. Die meisten zugelassenen Polysaccharid-Konjugat-Impfstoffe verwenden entweder reduktive Aminierung oder Cyanylierung, um Polysaccharidhydroxyle zu aktivieren. Cyanogenbromid (CNBr), ein Reagenz, das zuvor zur Aktivierung von Chromatographieharzen verwendet wurde, wurde zunächst zur Polysaccharidderivatisierung verwendet. CNBr erfordert jedoch einen hohen pH-Wert, typischerweise ~ pH 10,5 oder mehr, um Polysaccharidhydroxyle teilweise zu deprotonieren, so dass sie ausreichend nukleophil sind, um die Cyanogruppe anzugreifen. Der hohe pH-Wert kann sich nachteilig auf baselabile Polysaccharide auswirken, und weder CNBr noch der ursprünglich gebildete aktive Cyanoester sind bei einem so hohen pH-Wert ausreichend stabil.
CDAP (1-Cyano-4-dimethylaminopyridintetrafluoroborat; Abbildung 1) wurde von Lees et al. zur Verwendung als Cyylierungsmittel zur Aktivierung von Polysaccharideneingeführt 5,6. Es wurde festgestellt, dass CDAP, das kristallin und einfach zu handhaben ist, Polysaccharide bei einem niedrigeren pH-Wert als CNBr und mit weniger Nebenreaktionen aktiviert. Im Gegensatz zu CNBr können CDAP-aktivierte Polysaccharide direkt mit Proteinen konjugiert werden, was den Syntheseprozess vereinfacht. CDAP-aktivierte Polysaccharide können mit einem Diamin (z. B. Hexandiamin) oder einem Dihydrazid (z. B. adipinisches Dihydrazid, ADH) funktionalisiert werden, um amino- oder hydrazidderivatisierte Polysaccharide herzustellen. Eine hohe Konzentration des homobifunktionellen Reagenzes wird verwendet, um die Vernetzung von Polysacchariden zu unterdrücken. Aminopolysaccharide können dann mit einer der unzähligen Techniken zur Proteinkonjugation konjugiert werden. Hydrazid-derivatisierte Polysaccharide werden häufig mit einem Carbodiimid-Reagenz (z. B. 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimid (EDAC)) an Proteine gekoppelt7. Eine weitere Optimierung der CDAP-Polysaccharidaktivierung wurde von Lees et al.8 beschrieben und ist in das hier beschriebene Protokoll integriert.
Übersicht über die CDAP-Konjugation
Das CDAP-Protokoll kann als zwei Phasen konzipiert werden: (1) die Aktivierung des Polysaccharids und (2) die Konjugation des aktivierten Polysaccharids mit einem Protein oder Liganden (Abbildung 2). Ziel des ersten Schritts ist es, das Polysaccharid effizient zu aktivieren, während das Ziel des zweiten Schritts darin besteht, effizient an das aktivierte Polysaccharid zu konjugieren. Das aktivierte Polysaccharid bindet die beiden Schritte zusammen. Diese Konzeptualisierung hilft, sich auf die kritischen Elemente jedes Schritts zu konzentrieren. Abbildung 2 erweitert diese Konzeptualisierung und zeigt die gewünschten Aktivierungs- und Kopplungsreaktionen sowie die Hydrolysereaktionen und Nebenreaktionen.
Während der Aktivierungsphase sind die drei Hauptanliegen die CDAP-Stabilität, die CDAP-Reaktion mit den Polysaccharidhydroxylen und die Stabilität des aktivierten Polysaccharids (Abbildung 3). Die CDAP-Hydrolyse nimmt mit dem pH-Wert zu, ebenso wie die Hydrolyse des aktivierten Polysaccharids und die Nebenreaktionen. Die CDAP-Reaktion mit dem Polysaccharid wird jedoch durch Erhöhung des pH-Werts erleichtert. Die effiziente Aktivierung von Polysacchariden mit CDAP erfordert ein Gleichgewicht zwischen 1) der Reaktivität des Polysaccharids und CDAP und 2) der Hydrolyse und nebenreaktionen sowohl des Reagenzes als auch des aktivierten Polysaccharids.
Im ursprünglichen CDAP-Aktivierungsprotokoll, das von Lees et al.5beschrieben wurde, wurde die CDAP-Aktivierung von Polysacchariden bei Raumtemperatur in ungepufferter pH-9-Lösung durchgeführt. Die Aktivierungsrate erwies sich unter dieser Bedingung als schnell und die Aktivierung wäre innerhalb von 3 Minuten abgeschlossen. Die Reaktion wurde auch von einer schnellen Hydrolyse von CDAP begleitet, was zu einem schnellen pH-Abfall der ungepufferten Reaktionslösung führte. Es war eine Herausforderung, den Reaktions-pH-Wert in so kurzer Zeit schnell anzuheben und am Zielwert zu halten. Im beschriebenen Protokoll wurde die Aktivierung durch Zugabe von CDAP aus einer 100 mg/ml Stammlösung zur ungepufferten Polysaccharidlösung durchgeführt. Der pH-Wert wurde 30 s später mit "einem gleichen Volumen von 0,2 M Triethylamin" erhöht. Das zu konjugierte Protein wurde dann nach 2,5 min zur Aktivierungsreaktion hinzugefügt. Bemerkenswerterweise war der pH-Wert des Aktivierungsschritts nicht gut kontrolliert und überschritt höchstwahrscheinlich zunächst den Ziel-pH-Wert. Die schnelle Reaktion, die eine sofortige pH-Anpassung erforderte, machte den Aktivierungsprozess schwer zu kontrollieren und schwierig zu skalieren.
Im Gegensatz zum ursprünglichen Protokoll weist das hier beschriebene modifizierte Protokoll zwei wesentliche Verbesserungen auf. Zuerst wird der pH-Wert der Polysaccharidlösung vor der Zugabe von CDAP auf den pH-Wert der Zielaktivierung unter Verwendung von DMAP als Puffer vorjustiert. DMAP hat eine pKa von 9,5 und hat somit eine gute Pufferleistung um pH 9, und im Gegensatz zu vielen anderen Puffern wurde nicht festgestellt, dass DMAP die CDAP-Hydrolysefördert 8. Darüber hinaus ist DMAP bereits ein Prozesszwischenprodukt und fügt dem Reaktionsgemisch daher keine neue Komponente hinzu. Die Voreinstellung des pH-Werts vor der Zugabe von CDAP eliminiert den großen pH-Schwung zu Beginn der Reaktion und ermöglicht eine effizientere Aufrechterhaltung des Ziel-pH-Werts während der Reaktion. Die zweite Verbesserung besteht darin, die Aktivierungsreaktion bei 0 °C durchzuführen, wobei die CDAP-Hydrolyserate deutlich langsamer ist als bei Raumtemperatur. Mit der längeren Reagenzhalbwertszeit bei 0 °C wird die Aktivierungszeit von 3 min auf 15 min erhöht, um die langsamere Aktivierungsrate bei der niedrigeren Temperatur auszugleichen. Die längere Reaktionszeit wiederum erleichtert die Aufrechterhaltung des Reaktions-pH-Werts. Die Verwendung von 0 °C verlangsamt auch den Abbau von pH-empfindlichen Polysacchariden, so dass Konjugate dieser Art von Polysacchariden vorbereitet werden können. Die Verbesserungen im Protokoll machen den Aktivierungsprozess weniger hektisch, einfacher zu kontrollieren, reproduzierbarer und zugänglicher für die Skalierung.
Dieser Artikel beschreibt das verbesserte Protokoll zur Durchführung einer kontrollierten CDAP-Aktivierung von Polysaccharid bei 0 °C und bei einem bestimmten Ziel-pH-Wert und zur anschließenden Derivatisierung der aktivierten Polysaccharide mit ADH. Ebenfalls beschrieben ist ein Trinitrobenzolsulfonsäure (TNBS) Assay, basierend auf der Methode von Qi et al.9,zur Bestimmung des Hydrazidgehalts an dem modifizierten Polysaccharid. Ein modifizierter Assay für Hexosen auf Basis von Resorcin und Schwefelsäure10 wird ebenfalls beschrieben, der zur Bestimmung eines breiteren Spektrums von Polysacchariden verwendet werden kann. Für weitere Informationen zur CDAP-Aktivierung und -Konjugation wird der Leser auf frühere Publikationen5,6,8 von Lees et al. verwiesen.
Protokoll
HINWEIS: Bereiten Sie die Polysaccharidlösung, die ADH-Lösung, die DMAP-Lösung und die CDAP-Lagerlösung im Voraus vor, bevor Sie die Polysaccharidaktivierungs- und -funktionalisierungsverfahren ausführen. Platzieren Sie die Lösungen und Geräte an einem organisierten, bequemen und logischen Ort. Die beschriebene Reaktion besteht aus 10 mg Polysaccharid und kann nach oben oder unten skaliert werden. Es wird empfohlen, das Protokoll vor der Skalierung in kleinem Maßstab zu evaluieren.
1. Bereiten Sie 5 mg / ml Polysaccharidlösung, 2 ml vor.
- Für lyophilisiertes Polysaccharid
- Lassen Sie den Polysaccharidbehälter vor dem Öffnen auf Raumtemperatur kommen. Wiegen Sie 10 mg Polysaccharid in einem Schraubverschlussrohr mit einer Analysenwaage ab. Verwenden Sie einen statischen Eliminator für eine einfachere Probenahme und ein genaueres Wiegen des Pulvers.
- 2 ml 0,15 M Natriumchlorid (NaCl) in das Röhrchen geben, um das Polysaccharid aufzulösen. Kappe und Wirbel das Rohr.
HINWEIS: Natriumchlorid beeinflusst die CDAP-Reaktion nicht, kann jedoch die Polysaccharid-Sekundärstruktur beeinflussen. Einige Polysaccharide sind bei unterschiedlichen Salzkonzentrationen besser löslich. - Mischen Sie das Röhrchen durch End-over-End-Rotation für 12-24 h, abhängig vom Molekulargewicht des Polysaccharids, damit das Polysaccharid vollständig hydratisieren kann. Erwärmen Sie bei Bedarf vorsichtig die Tube, um die Solubilisierung zu fördern.
- Für solubilisiertes Polysaccharid in gepufferter Lösung
HINWEIS: Für eine effiziente CDAP-Aktivierung sollte die Polysaccharidlösung keinen Puffer, insbesondere kein Phosphation, enthalten. Gehen Sie wie folgt vor, um den Puffer durch Wasser oder eine Kochsalzlösung zu ersetzen und die Polysaccharidkonzentration auf 5 mg/ml einzustellen.- Erhalten Sie eine 4 mL oder 15 mL Zentrifugal-Spin-Filtervorrichtung der entsprechenden Molekulargewichts-Cutoff (MWCO).
HINWEIS: Der MWCO ist idealerweise 5-10 mal kleiner als das Molekulargewicht des Polysaccharids. - Fügen Sie ein Volumen der gepufferten Polysaccharidlösung mit ~ 20 mg des Polysaccharids in den Filtereinsatz hinzu. Füllen Sie bis zur vollen Markierung mit Wasser oder einer Kochsalzlösung. Verschließen Sie den Filter fest. Mischen Sie ein paar Mal durch Ende-über-Ende.
- Zentrifugieren Sie die Filtervorrichtung mit der vom Hersteller vorgeschlagenen Zentrifugalkraft. Stellen Sie sicher, dass die Zentrifugationszeit lang genug ist, um nach jedem Spin eine mindestens 5-fache Volumenreduzierung zu erreichen. Verwerfen Sie den Durchfluss. Stellen Sie das Filtergerät wieder zusammen.
- Füllen Sie den Filtereinsatz bis zur vollen Markierung mit Frischwasser oder Kochsalzlösung auf. Verschließen Sie den Filter fest. Mischen Sie den Inhalt im Filter durch End-over-End-Rotation ~ 10-mal oder durch sanftes Vortexing; Wiederholen Sie den Spin.
HINWEIS: Polysaccharid kann sich am Boden des Filtereinsatzes der Zentrifugalvorrichtung ansammeln und ein Gel bilden. Es wird empfohlen, das Retentant im Filtereinsatz vor dem nächsten Spin erneut mit dem frischen Refill zu mischen. - Wiederholen Sie den Nachfüll- und Schleuderzyklus mindestens 3 Mal.
- Befolgen Sie die folgende Übung, um das Polysaccharid-Retentant aus dem Filtereinsatz wiederherzustellen.
- Fügen Sie dem Filtereinsatz Frisches Wasser oder Kochsalzlösung hinzu, so dass das Volumen ~ 1 ml beträgt. Mischen Sie durch Pipettieren auf und ab oder durch sanftes Vortexing.
- Geben Sie das gesamte gemischte Retentant in ein 5-ml-Röhrchen. Fügen Sie 1 ml Frischwasser oder Kochsalzlösung in den Filtereinsatz hinzu. Spülen Sie den Filter durch Pipettieren auf und ab oder durch sanftes Vortexing. Übertragen und kombinieren Sie alle Spülungen mit dem zurückgewonnenen Polysaccharid.
- Bestimmen Sie die Polysaccharidkonzentration (siehe Polysaccharid-Assay in Abschnitt 7.3). Verdünnen Sie das Polysaccharid mit zusätzlichem Wasser oder Kochsalzlösung auf 5 mg/ ml.
- Erhalten Sie eine 4 mL oder 15 mL Zentrifugal-Spin-Filtervorrichtung der entsprechenden Molekulargewichts-Cutoff (MWCO).
- Wenn die Polysaccharidlösung hergestellt ist, kühlen Sie das Röhrchen mit der Polysaccharidlösung in einem Eiskübel.
2. Bereiten Sie 0,5 M Adipinsäuredihydrazid (ADH) Lösung, 10 ml vor.
- Wiegen Sie 0,87 g ADH in einer Analysenwaage und solubilisieren Sie in 8 mL 0,1 M HEPES (4-(2-Hydroxyethyl)-1-piperazinethansulfonsäure), pH 8.
- Passen Sie den Ziel-pH-Wert mit 1 M Natriumhydroxid (NaOH) an, der von einem pH-Messgerät überwacht wird. Mit zusätzlichem Puffer auf 10 ml bringen und den pH-Wert erneut bestätigen.
3. Bereiten Sie 2,5 M DMAP-Lösung, 10 ml vor.
HINWEIS: DMAP ist giftig und dringt in die Haut ein. Tragen Sie bei der Durchführung des Verfahrens Nitrilhandschuhe.
- Wiegen Sie vorsichtig 3 g DMAP in ein 50 mL konisches Rohr. Fügen Sie 5 ml Wasser zu DMAP hinzu und mischen Sie durch Wirbeln für 5 min, um eine trübe Lösung (~ 7 ml) zu erhalten.
- Fügen Sie während des Mischens 50 μL-Schritte von 10 N Salzsäure (HCl) zur DMAP-Lösung hinzu. Mischen Sie zwischen den einzelnen Zusätzen. Beenden Sie das Hinzufügen, wenn die Lösung klar wird.
- Fügen Sie 10 N NaOH in 25 μL-Schritten hinzu, um die DMAP-Lösung auf ~pH 8 zu bringen.
- Bringen Sie die DMAP-Lösung mit Wasser auf 10 ml, um eine 2,5-m-Lösung zu erhalten.
- Optimieren Sie den pH-Wert der 2,5 M DMAP-Lösung.
HINWEIS: Der pH-Wert der DMAP-Lösung ändert sich mit der Konzentration und der Ionenstärke. Diese Übung besteht darin, den 2,5 M DMAP-Bestand auf einen bestimmten pH-Wert zu verfeinern, so dass, wenn er mit 10 Volumina Polysaccharid gemischt wird, die resultierende Lösung nahe am Ziel-pH-Wert für die Aktivierung liegt.- Bereiten Sie eine Reihe von 1,5-ml-Röhrchen vor, die 1 ml Wasser oder die NaCl-Lösung enthalten, je nachdem, was zur Herstellung der Polysaccharidlösung verwendet wurde. Kühlen Sie die Schläuche auf Eis.
- 100 μL DMAP in ein gekühltes Rohr geben. Wirbel und messen Sie den pH-Wert mit einem pH-Meter. Entsorgen Sie dann das gemessene Rohr.
- Wenn der gemessene pH-Wert nicht nahe am Zielwert liegt, passen Sie den pH-Wert des DMAP-Bestands mit 1 M NaOH oder HCl an. Wiederholen Sie die Schritte 3.5.2 und 3.5.3, bis der gemessene pH-Wert nahe am Ziel-pH-Wert liegt.
4. Bereiten Sie 100 mg / ml CDAP-Stammlösung vor
HINWEIS: CDAP-Pulver sollte fest verschlossen und bei -20 °C gelagert und vor dem Öffnen auf Raumtemperatur kommen gelassen werden. Tragen Sie bei der Durchführung des Verfahrens Nitrilhandschuhe.
- Taren Sie ein 1,5 ml Schnappkappen-Mikrozentrifugenröhrchen auf einer Analysenwaage. Mit einem kleinen Spatel 10-140 mg CDAP in die Tube wiegen. Beachten Sie das tatsächliche Gewicht von CDAP.
- Bestimmen Sie das Volumen an Acetonitril, das zur Herstellung von 100 mg / ml CDAP benötigt wird. Öffnen Sie Acetonitril in einem Abzug.
- Ziehen und lösen Sie mit einem geeigneten Volumenpipet das Acetonitril, um seinen Dampf in der Pipettspitze auszugleichen. Warten Sie, bis das Lösungsmittel nach einigen Sekunden aus der Pipettspitze tropft, und bereiten Sie sich darauf vor, es direkt in das CDAP-Röhrchen zu übertragen. Ziehen Sie das berechnete Volumen von Acetonitril und übertragen Sie es direkt in die CDAP-Röhre. Schnappen Sie die Kappe zu.
HINWEIS: Acetonitril kann auch mit einer Hamilton-Spritze oder einem Äquivalent geeigneter Größe in das CDAP-Röhrchen übertragen werden. - Vortex zur vollständigen Lösung des CDAP. Legen Sie das CDAP-Rohr in einen Eiskübel.
HINWEIS: CDAP ist in Acetonitril in der Kälte stabil. Lösliche Bestände können >1 Woche bei -20 °C gehalten werden. Es ist jedoch vorzuziehen, frische CDAP-Lösungen zuzubereiten.
5. Polysaccharidaktivierung und Hydrazidfunktionalisierung
- Stellen Sie sicher, dass alle folgenden Elemente bereit sind und die Lösungen auf Eis gekühlt werden, bevor Sie mit der Aktivierung beginnen: 2 ml einer 5 mg / ml Polysaccharidlösung in einem Flachbodenbehälter mit breitem Mund, der einen Rührstab enthält, der auf einen Magnetrührer gelegt wird; 100 mg/ml CDAP-Stammlösung; 2,5 M DMAP-Lagerlösung; ein pH-Messgerät mit einer Semimikro-pH-Sonde, wie die Sonde mit einem Durchmesser von 6 mm, die gemäß den Anweisungen des Herstellers für 0 °C kalibriert ist; eine gebrauchsfertige 100 μL-Pipett; ein Timer geräumt und einsatzbereit; ein autotitrator-Spenderkopf positioniert oder 10 μL Pipett gebrauchsfertig; 0,5 M ADH-Lösung.
- Stellen Sie den pH-Wert des Polysaccharids mit DMAP auf den Ziel-pH-Wert ein.
- Legen Sie die pH-Sonde in die Polysaccharidlösung und lassen Sie sie während des gesamten Aktivierungsvorgangs in der Lösung.
- 200 μL der DMAP-Stammlösung durch tropfenweise Zugabe unter Rühren in die Polysaccharidlösung überführen. Passen Sie den pH-Wert der Lösung an den pH-Wert der Zielaktivierung an. Fügen Sie 0,1 M HCl hinzu, um den pH-Wert zu senken, und 0,1 M NaOH, um den pH-Wert zu erhöhen. Vermeiden Sie es, den Ziel-pH-Wert um mehr als 0,1 pH-Wert zu überschreiten, und halten Sie die Reaktion für die Dauer der Aktivierung in einem Eiswasserbad gekühlt.
- CDAP-Aktivierung
- Pipeten Sie 100 μL CDAP nach oben und unten, um den Dampf in der Pipettspitze auszugleichen. 100 μL CDAP unter Rühren in die Polysaccharidlösung überführen.
HINWEIS: Bei dieser Aktivierung wird 1 mg CDAP für 1 mg Polysaccharid als Startverhältnis verwendet. Das Verhältnis kann bei der Optimierung der Aktivierung erhöht oder verringert werden. - Starten Sie den Timer und überwachen Sie die pH-Änderung während der gesamten Aktivierung. Halten Sie die Reaktion auf dem Ziel-pH-Wert, indem Sie der Reaktion mit Hilfe eines Autotitratorspenders (oder einer Pipett) umgehend 10 μL-Inkremente von 0,1 M NaOH hinzufügen.
HINWEIS: Es kann helfen, die pH-Reaktionszeit zu reduzieren, um mit einer pH-Sonde sanft zu rühren. Der pH-Wert sinkt zu Beginn schneller und es kann notwendig sein, die 0,1 M NaOH häufiger hinzuzufügen. Wenn die Reaktion fortschreitet, wird der pH-Wert langsamer und die Zugabe wird seltener. Der pH-Wert sollte im Wesentlichen unverändert bleiben, wenn man sich der optimalen Aktivierungszeit nähert, die 10-15 minuten für die Aktivierung von pH 9 beträgt.
- Pipeten Sie 100 μL CDAP nach oben und unten, um den Dampf in der Pipettspitze auszugleichen. 100 μL CDAP unter Rühren in die Polysaccharidlösung überführen.
- ADH-Funktionalisierung
- Wenn die optimale Aktivierungszeit erreicht ist, fügen Sie dem aktivierten Polysaccharid unter Rühren 2 ml 0,5 M ADH auf einmal hinzu. Überprüfen Sie, ob der pH-Wert im Zielbereich liegt (pH 8-9 für ADH).
HINWEIS: Eine Zugabe mit schnellem Mischen minimiert die Wahrscheinlichkeit, dass beide Enden des Dihydrazids mit dem aktivierten Polysaccharid reagieren, wodurch eine Polysaccharidvernetzung verhindert wird. - Rühren Sie das Reaktionsgemisch mindestens 1 h weiter. Übertragen Sie das Reaktionsgemisch auf 4 °C, aber 0-20 °C ist akzeptabel.
HINWEIS: Die ADH-Funktionalisierungsreaktion ist nicht stark temperaturabhängig. Da der große Überschuss an Dihydrazid als Abschreckreagenz wirkt, ist es nicht notwendig, das aktivierte Polysaccharid weiter abzuschrecken. Bei der direkten Konjugation von Proteinen sollte die Reaktion jedoch abgeschreckt werden, typischerweise mit 1 M Glycin, pH 8-9.
- Wenn die optimale Aktivierungszeit erreicht ist, fügen Sie dem aktivierten Polysaccharid unter Rühren 2 ml 0,5 M ADH auf einmal hinzu. Überprüfen Sie, ob der pH-Wert im Zielbereich liegt (pH 8-9 für ADH).
6. Reinigung von ADH-funktionalisiertem Polysaccharid durch Dialyse
HINWEIS: Das Rohprodukt aus der ADH-Funktionalisierungsreaktion enthält eine hohe Konzentration von ADH (0,5 M), die am effizientesten durch umfangreiche Dialyse entfernt werden kann. Die Gelfiltration, entweder mit einer Säule oder einer Spin-Entsalzungsvorrichtung, ist nicht so effizient, insbesondere wenn die verbleibende ADH-Verunreinigung entfernt werden muss.
- Bestimmen Sie den MWCO der Dialysemembran. Verwenden Sie einen 3 kDa- Cutoff für kleinere Polysaccharide.
HINWEIS: Der MWCO der Dialysemembran ist idealerweise 5-10 mal kleiner als der MW von Polysaccharid. - Wählen Sie das gewünschte Dialyseformat (Kassetten oder Schläuche) und die richtige Gerätekapazität. Stellen Sie sicher, dass die Gerätekapazität 2-mal größer ist als das Probenvolumen. Konsultieren Sie die Anweisungen der Hersteller für die Verwendung des Geräts.
- Hydratisieren Sie die Dialysemembran vor Gebrauch in Wasser. Die rohe derivatisierte Polysaccharidlösung wird gemäß den Anweisungen des Herstellers in das Dialysegerät überführen.
HINWEIS: Tragen Sie Nitrilhandschuhe, um den Kontakt mit DMAP zu vermeiden. - Dialysieren In einem Behälter gefüllt mit 2-4 L 1 M NaCl und einem Rührstab. Stellen Sie den Behälter auf eine Rührplatte in einem Kühlraum oder in einen Kühlschrank. Rühren Sie das Dialysat während der Dialyse sanft und kontinuierlich um.
- Nach dem Dialysieren für mindestens 4 h wechseln Sie zu frischem 1 M NaCl und dialysieren Sie für mindestens 12 h. Dialysieren Sie gegen 2 Veränderungen von 0,15 M Kochsalzlösung, jeweils für mindestens 12 h. Falls gewünscht, dialysieren Sie gegen 2 Wasserwechsel.
- Überprüfen Sie, ob das gesamte ADH entfernt wird, indem Sie das Dialysat über Nacht mit einem TNBS-Schnelltest testen.
- Erhalten Sie 3 Borosilikatröhrchen, kennzeichnen Sie sie als Negativkontrolle (Strg), Positiv-Strg und Probe.
- Zum negativen Strgrohr werden 975 μL 0,1 M Borat, pH 9, hinzugefügt.
- Zum positiven Strgrohr werden 100 μL 0,05 mM ADH (0,1 mM Hydrazid) und 875 μL 0,1 M Borat, pH 9, hinzugefügt.
- In das Probenröhrchen werden 500 μL des Dialysats über Nacht und 475 μL 0,1 M Borat, pH 9, gegeben.
- Fügen Sie 25 μL 1% TNBS zu allen drei Röhrchen hinzu. Gut mischen. Für 1 h in die Dunkelheit stellen.
- Vergleichen Sie die Farbintensität der 3 Röhren in 1 h. Stellen Sie sicher, dass die Farbintensität des Probenröhrchens zwischen der der positiven Strg und der negativen Strg liegt, was darauf hinweist, dass die ADH-Verunreinigung auf 0,01 mM oder darunter gesunken ist. Dialyze noch einmal.
HINWEIS: Es ist ratsam, den Gehalt der ADH-Verunreinigung so weit wie möglich zu reduzieren, so dass das ADH-Hydrazid weniger als 1% des Gesamthydroxids im gereinigten Hydrazid-Polysaccharid ausmacht. - Rückgewinnung des derivatisierten Polysaccharids aus der Dialyse. Bestimmen Sie die Konzentration der Polysaccharide und Hydrazid. Berechnen Sie das Hydratizid/Polysaccharid-Verhältnis (siehe Abschnitt 7). Wenn das dialysierte Polysaccharid auf 5-10 mg/ml konzentriert werden muss, konsultieren Sie Abschnitt 1.2.
7. Analyse von Hydrazid-derivatisierten Polysacchariden
HINWEIS: Der Zweck der hier beschriebenen Analyse besteht darin, die Polysaccharidkonzentration, die Hydrazidkonzentration und den Grad der Hydrazidderivatisierung in Bezug auf das Hydrazid/Polysaccharid-Verhältnis zu bestimmen.
- Probenvorbereitung
HINWEIS: Polysaccharide, die untersucht werden sollen, müssen frei von niedermolekularen Kohlenhydrat-, Amin- oder Hydrazidverunreinigungen sein. Lyophilisierte Proben sollten trocken und salzfrei sein, um eine genaue Gewichtsmessung zu gewährleisten. Normalerweise ist ~ 1 ml einer 1-2 mg / ml Lösung für Assays ausreichend.- Wiegen Sie mindestens 10 mg der lyophilisierten Polysaccharidprobe auf einer Analysenwaage mit einem nichtstatischen Spatel oder einem statischen Eliminator. Lösen Sie das Polysaccharid in Wasser oder Kochsalzlösung in einer Konzentration (z. B. 2 mg/ml) auf, so dass die Assay-Signale in den linearen Bereich der Standardkurve fallen.
- Mischen Sie Ende-über-Ende und lassen Sie genügend Zeit, damit sich die Probe vollständig auflöst. Führen Sie die Hydratation über Nacht in Abhängigkeit vom Molekulargewicht des Polysaccharids durch.
- Polysaccharid-Assay: Resorcin/Schwefelsäure-Methode
HINWEIS: Der geeignete Assay für Polysaccharide hängt von der Kohlenhydratzusammensetzung der Polymere ab. Der ursprüngliche Resorcin/Schwefelsäure-Assay war für Hexosezucker bestimmt10. Der Assay wurde hier modifiziert, indem die Temperatur des Heizschritts von 90 °C auf 140 °C angehoben wurde. Bei dieser höheren Temperatur verliert der Assay etwas an Spezifität, kann aber verwendet werden, um viele Zucker zu bestimmen. Es ist jedoch immer noch notwendig, die Eignung des Assays für ein bestimmtes Polysaccharid zu bestimmen. Triplikate werden für jeden Punkt empfohlen, aber einige Unterkünfte können aufgrund der Kapazität des Heizblocks erforderlich sein.- Bereiten Sie 75% Schwefelsäure vor
HINWEIS: Konzentrierte Schwefelsäure ist extrem korrosiv und kann schwere Verbrennungen verursachen. Führen Sie dieses Verfahren in einem chemischen Abzug durch. Gießen Sie immer konzentrierte Säure in Wasser, nicht umgekehrt!- Fügen Sie 50 ml Wasser zu einer 200 ml Glasflasche hinzu. Stellen Sie die Flasche in ein kaltes Wasserbad. Fügen Sie langsam 150 ml Schwefelsäure hinzu. Verschließen Sie die Flasche so, dass sie entlüftet wird.
- Lassen Sie die Lösung auf Raumtemperatur ausgleichen. Verwenden Sie die Lösung innerhalb von 3 Monaten.
- Kohlenhydratstandards vorbereiten
- Bereiten Sie die unveränderte Polysaccharidlösung bei 1 mg/ml vor, um sie standardmäßig zu verwenden. Alternativ können Sie eine Mischung einzelner Zucker in dem Verhältnis verwenden, das in der Wiederholungseinheit des Polysaccharids bei 1 mg / ml der Gesamtzuckerkonzentration als Standard gefunden wird.
HINWEIS: Obwohl die Zuckermischung normalerweise das gleiche Ergebnis wie das Kohlenhydratpolymer mit identischer Zuckerzusammensetzung liefert, sollte dies experimentell bestätigt werden.
- Bereiten Sie die unveränderte Polysaccharidlösung bei 1 mg/ml vor, um sie standardmäßig zu verwenden. Alternativ können Sie eine Mischung einzelner Zucker in dem Verhältnis verwenden, das in der Wiederholungseinheit des Polysaccharids bei 1 mg / ml der Gesamtzuckerkonzentration als Standard gefunden wird.
- Stellen Sie sicher, dass der Heizblock mit Rohrhaltern für 13 x 100 Borosilikat-Reagenzgläser funktioniert. Verwenden Sie ein Schutzpad unter und um den Heizblock herum, falls Säure verschüttet wird. Heizen Sie den Heizblock für mindestens 1 h auf 140 °C vor, um eine stabile, gleichmäßige Temperatur durch alle verwendeten Blöcke zu erreichen.
- Etikett 13 x 100 Borosilikat-Reagenzgläser, dreifach für jeden Standard und jede Probe. 0, 2,5, 5, 7,5, 10 μg (oder μL) des 1 mg/ml Kohlenhydratstandards in die entsprechend gekennzeichneten Standardröhrchen geben. Fügen Sie jedem Rohr Wasser hinzu, um das Volumen auf 100 μL zu bringen.
HINWEIS: Die erzeugte Farbe hängt von bestimmten Zuckern ab. Da einige Zucker mehr Masse benötigen, um den vollen Absorptionsbereich zu erzeugen, können die tatsächlichen Mengen, die für die Standardkurve verwendet werden, variieren. - Richten Sie Probenassays ein, indem Sie ein Volumen mit ~ 5 μg des derivatisierten Polysaccharids in drei Probenröhrchen geben und das Gesamtvolumen mit Wasser auf 100 μL bringen. Alternativ, wenn die Polysaccharidkonzentration in der Probe unbekannt ist, führen Sie eine Reihe von 4-fachen Verdünnungen durch. Testen Sie 100 μL jeder Verdünnung in dreifacher Ausfertigung.
- Bereiten Sie frisches Resorcin bei 6 mg / ml in entionisiertem (dI) Wasser unmittelbar vor dem Gebrauch vor. Wirbel, bis das Resorcin in Lösung ist. 100 μL 6 mg/ml Resorcin in jedes Röhrchen geben.
- Gießen Sie vorsichtig die geschätzte Menge an 75% Schwefelsäure in ein kleines Becherglas.
HINWEIS: Tragen Sie einen Laborkittel, Nitrilhandschuhe und eine Schutzbrille. Seien Sie vorsichtig mit Tropfen, Verschüttungen und Spritzern. Halten Sie nasse Papierhandtücher griffbereit, um Tropfen abzuwischen. Da sich die Aktivität der Schwefelsäure bei längerer Lufteinwirkung ändert, verwenden Sie eine gleichmäßige Mischung aus Schwefelsäure für den gesamten Assay. - Mit einem Wiederholungspipettor werden gleichmäßig 300 μL 75% Schwefelsäure in jedes Röhrchen gegeben. Wirbeln Sie die Rohre kräftig ein, um sich gut zu mischen, und richten Sie das Rohr beim Wirbeln weg. Legen Sie die Rohre in einem gleichmäßigen Tempo in sequenzieller Reihenfolge in einen Heizblock. Sobald alle Röhren eingesät sind, stellen Sie den Timer sofort auf 3 Minuten ein.
- Entfernen Sie nach 3 Minuten die Schläuche in einem gleichmäßigen Tempo in der gleichen Reihenfolge und legen Sie sie direkt in ein Gestell in einem Eiswasserbad. Lassen Sie die Schläuche stehen, bis sie eiskalt sind. Entfernen Sie die Röhren und lassen Sie sie für ~ 5 minuten auf Raumtemperatur ausgleichen, um Kondensation auf der Küvette während des Lesens zu verhindern.
- Stellen Sie ein UV/VIS-Spektralphotometer ein, um die Absorption bei 430 nm mit einer 10 mm Pfadlängenküvette abzulesen. Rohling mit einem Null-Standardrohr. Lesen Sie die Absorption aller Röhrchen bei 430 nm ab.
HINWEIS: Einweg-Kunststoffküvetten sind bequem zu verwenden. - Konstruieren Sie eine Standardkurve, indem Sie μg kohlenhydratstandard vs. A430 aufzeigen. In Abbildung 4 finden Sie eine typische Standardkurve, die Glukose als Referenzstandard verwendet.
- Verwenden Sie die Probenassayröhrchen mit A430-Werten, die in den linearen Bereich der Standardkurve fallen, berechnen Sie die μg-Menge des unbekannten Polysaccharids in den Probenassayröhrchen aus der Standardkurvengleichung. Bestimmen Sie die Konzentration des unbekannten Polysaccharids aus dem Volumen des unbekannten zugesetzten Polysaccharids unter Berücksichtigung von Verdünnungen. Wandeln Sie die Konzentration je nach Bedarf in mg/ml- oder μM-Wiederholungseinheiten um.
- Bereiten Sie 75% Schwefelsäure vor
- Hydrazid-Assay mit Trinitrobenzolsulfonsäure (TNBS)
- 0,9% NaCl mit 0,02% Natriumazid (Probenpuffer) durch Lösen von 9 g NaCl und 200 mg Natriumazid in dIH2Oauf ein Endvolumen von 1 L vorbereiten.
- 0,1 M Natriumborat, pH 9 (Assaypuffer), durch Mischen von 100 ml 0,5 M Natriumborat, pH 9, mit 400 ml dIH2O. Bestätigen, dass der pH-Wert der Lösung 9 ± 0,1 beträgt; bei Bedarf anpassen.
- 1% TNBS durch Verdünnen von 200 μL 5% 2,4,6-Trinitrobenzolsulfonsäurelösung auf 1 ml mit dIH2O. Das Röhrchen als 1% TNBS markieren und bei 4 °C im Dunkeln eine Woche lagern.
- Bereiten Sie 50 mM ADH-Schaft vor (entspricht 100 mM Hydrazid).
- Wiegen Sie 871 mg adipinisches Dihyrazid (ADH) Pulver mit einer Analysenwaage ab. Lösen Sie das Pulver in einer Reagenzflasche auf, indem Sie mit Hilfe einer Toploader-Waage einen Probenpuffer auf 100 ml geben.
- Kennzeichnen Sie die Flasche mit 100 mM Hydrazid/50 mM ADH. Die Flasche fest verschließen und bei 4 °C 1 Jahr lagern.
- Bereiten Sie Hydrazidstandards (0,1, 0,2, 0,3, 0,4, 0,5 und 0,6 mM Hydrazid) vor.
- Bereiten Sie die 6 Hydrazidstandards vor, indem Sie den 100 mM Hydrazidbestand mit Hilfe einer Totladerwaage mit Probenpuffer verdünnen. Bereiten Sie 100 ml jedes Standards vor, um Konzentrationsfehler zu minimieren. Die Flaschen fest verschließen und 1 Jahr bei 4 °C lagern.
- Einrichten von Assay-Reaktionen
HINWEIS: Der TNBS-Assay wird mit einem Reaktionsvolumen von 1 ml durchgeführt. Jedes Assay-Röhrchen besteht aus 100 μL einer Probe (oder einem Standard), 875 μL Assay-Puffer und 25 μL 1%igen TNBS-Lösung. Alle Assay-Reaktionen (sowohl für Proben als auch für Standards) sind in dreifacher Ausfertigung aufgebaut.- Etikett 3 Borosilikatglasröhren (12 x 75 mm) für jeden Standard, einschließlich des Nullstandards. Sortieren und ordnen Sie die Standardrohre im Rohrgestell in der Reihenfolge der zunehmenden Konzentration an. Verwenden Sie eine kalibrierte 100 μL oder 200 μL Mikropipette, um 100 μL der Standards genau in jedes entsprechende Röhrchen zu geben. Verwenden Sie für den Nullstandard 100 μL Probenpuffer.
- Etikett 3 Borosilikatglasröhrchen (12 x 75 mm) für jede zu untersuchenden verdünnten Probe. Sortieren und ordnen Sie die Probenröhrchen im Tubengestell entsprechend an. Verwenden Sie eine kalibrierte 100 μL oder 200 μL Mikropipette, um 100 μL der Probe genau in jedes entsprechende Probenröhrchen zu geben.
- Verwenden Sie eine kalibrierte 1000 μL Mikropipette, um 875 μL Assay-Puffer genau zu allen Assay-Röhrchen hinzuzufügen: den Standards und den Proben.
- Um die Assay-Reaktion zu starten, verwenden Sie eine kalibrierte 100 μL-Mikropipette, um jedem Assay-Röhrchen genau 25 μL 1% TNBS hinzuzufügen. Beginnen Sie mit den Null-Standardröhrchen, gehen Sie zu den Standardröhrchen in der Reihenfolge der steigenden Konzentration und dann zu den Probenröhrchen gemäß der vorgegebenen Reihenfolge. Ändern Sie die Tipps, wenn Sie einen neuen Standard oder eine neue Probe starten, und halten Sie die Zeit, die Sie mit dem Hinzufügen von TNBS zu allen Röhrchen verbringen, innerhalb von 5 Minuten.
- Wirbeln Sie alle Assay-Röhrchen für 2 s bei hoher Geschwindigkeit oder bei einer Geschwindigkeitseinstellung, die es der Flüssigkeit im Assay-Röhrchen ermöglicht, nach oben zu wirbeln, um eine Höhe von 1/2 Zoll von der Rohröffnung zu erreichen.
- Notieren Sie die Startzeit des Assays und stellen Sie den Timer auf 2 h ein. Stellen Sie das Assay-Tube-Rack für 2 h bei Raumtemperatur in die Dunkelheit. Wenn die Zeit vorbei ist, wirbeln Sie alle Röhren noch einmal und fahren Sie mit der Datenerfassung fort.
- Datensammlung
- Lassen Sie das UV/VIS-Spektralphotometer aufwärmen und die Grundlinie stabilisieren. Stellen Sie die Nachweiswellenlänge für den Hydrazid-Assay auf 500 nm ein. Verwenden Sie eine 1 mL Quarzküvette von 1 cm Pfadlänge für alle Absorptionsmessungen für den gesamten Assay.
- Starten Sie die Datenerfassung, indem Sie einen Null-Standard-Assay auf die Küvette übertragen. das Gerät ausblenden (Saugfähigkeit auf Null setzen).
- Führen Sie einen einzigen Lesewert für jedes Rohr durch und notieren Sie die Absorptionswerte in einer Datentabelle. Entfernen Sie alle Restflüssigkeiten aus der Küvette, bevor Sie eine neue Probe lesen. Beginnen Sie mit den Nullstandards, gehen Sie zu den Standards der Erhöhung der Konzentration und dann zu den Proben über. Führen Sie nach dem Start alle Schritte effizient ohne Unterbrechung aus und lesen Sie alle Röhren innerhalb von 10 Minuten.
- Analysieren von Beispieldaten
- Erstellen Sie eine Standardkurve, indem Sie den mM-Hydrazidstandard im Vergleich zu A500 auftäten. Finden Sie die Standardkurvengleichung in Form von y = ax + b, wobei y für mM-Hydrazid und x für A500 steht. Eine typische Standardkurve finden Sie in Abbildung 4.
- Berechnen Sie mM-Hydrazid in den Proben mit der Standardkurvengleichung und passen Sie die Verdünnungsfaktoren an. Wählen Sie für die Berechnung nur die Probenassayröhrchen mit A500-Werten, die innerhalb des linearen Bereichs der Standardkurve liegen.
- Berechnen Sie das molare Verhältnis von Hydrazid/Polysaccharid mit Hilfe der Gleichung (1).
Hydrazid/Polysaccharid = h/c × MW ( 1)
Dabei ist h das mM-Hydrazid, c die mg/ml-Konzentration des Polysaccharids und MW das Polysaccharid-Molekulargewicht in kDa. - Berechnen Sie die Hydrazid-Markierungsdichte pro 100 kDa Polysaccharid mit Gleichung (2).
Markierungsdichte pro 100 kDa Polysaccharid = h/c × 100 (2)
Dabei ist h das mM-Hydrazid und c die mg/ml-Konzentration des Polysaccharids.
HINWEIS: Der Einfachheit halber kann davon ausgegangen werden, dass die Polysaccharide ein Molekulargewicht von 100.000 Dalton haben. Dies ermöglicht es, eine "Markierungsdichte" beim Vergleich des Derivatisierungsgrades verschiedener Polysaccharide zu berücksichtigen. - Berechnen Sie die Hydrazid-Markierungsdichte als Gewichtsprozent ADH.
- Bestimmen Sie die effektive mg/ml-Konzentration von ADH mit Hilfe der Gleichung (3).
mg/ml ADH = (mM Hydrazid / 1000) × 174 (3)
wobei 174 die MW von ADH ist. - Berechnen Sie das Gewicht % ADH mit Hilfe der Gleichung (4).
Gewicht % ADH = (mg/ml ADH) / (mg/ml Polysaccharid) × 100 (4)
- Bestimmen Sie die effektive mg/ml-Konzentration von ADH mit Hilfe der Gleichung (3).
Ergebnisse
Um die Aktivierung und Derivatisierung eines Polysaccharids mittels CDAP-Chemie zu veranschaulichen, wurde Dextran bei 0,25 und 0,5 mg CDAP/mg Dextran aktiviert. Für jede Reaktion wurde eine 10 mg/ml Dextranlösung in Wasser auf Eis gekühlt und 1/10 Volumen eines 2,5 M DMAP-Vorrats (hergestellt wie in Abschnitt 3 beschrieben) zugegeben. Die endgültige Lösung wurde durch Zugabe von 0,1 M NaOH in 10 μL Aliquoten auf pH 9 gebracht. Die Lösung wurde gekühlt und gerührt, CDAP hinzugefügt und der pH-Wert bei pH 9 gehalten, indem 10 μL Aliquoten von 0,1 M NaOH für 15 min hinzugefügt wurden. Nur 0,25 ml 0,5 M ADH bei pH 9 wurden zugegeben (weniger als die übliche Menge) und die Reaktion konnte über Nacht bei 4 °C fortgesetzt werden.
Das markierte Dextran wurde dann sequenziell gegen 1 M NaCl, 0,15 M NaCl und Wasser dialysiert, wie in Abschnitt 6 beschrieben. Das ADH-Dextran wurde dann mit dem Resorcin/Schwefelsäure-Assay auf Dextran untersucht (Abschnitt 7.2). Eine typische Standardkurve, die Glukose als Zuckerstandard verwendet, ist in Abbildung 4A dargestellt. Der Hydrazidgehalt wurde mit dem in Abschnitt 7.3 beschriebenen TNBS-Assay bestimmt. Eine typische Hydrazid-Standardkurve mit ADH als Standard ist in Abbildung 4Bdargestellt.
Repräsentative Berechnungen aus der Aktivierung von Dextran auf den beiden Aktivierungsebenen sind in Abbildung 4A,B dargestellt. Die Daten werden sowohl als Hydrazide pro 100 kDa Dextranpolymer als auch als Gewichtsprozent ADH zu Dextran dargestellt, wie in den Abschnitten 7.9.3.4 bzw. 7.9.3.5 in Abbildung 4Cbeschrieben. Der Derivatisierungsgrad verdoppelte sich in etwa, als sich das CDAP-Verhältnis verdoppelte.
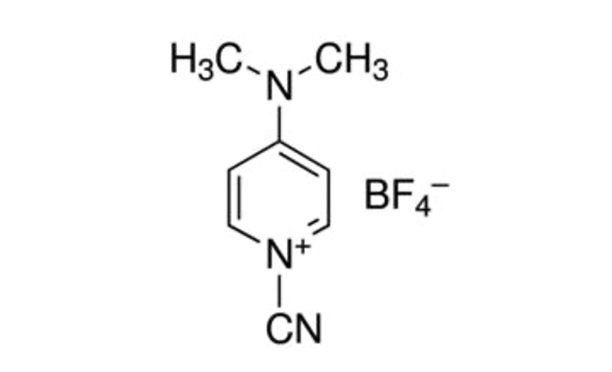
Abbildung 1: Chemische Struktur von CDAP. CDAP = 1-Cyano-4-dimethylaminopyridintetrafluoroborat. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
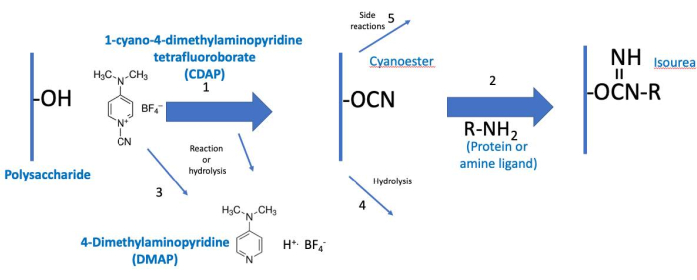
Abbildung 2: Prozess der CDAP-Aktivierung und -Konjugation. Der Prozess ist konzeptionell in zwei Phasen unterteilt, wobei das aktivierte Polysaccharid beiden gemeinsam ist. Unter grundlegenden Bedingungen aktiviert CDAP Polysaccharidhydroxyle und setzt DMAP frei (Reaktion 1). Die CDAP-Hydrolyse setzt auch DMAP frei (Reaktion 3). Obwohl ein Cyanoester gezeigt wird, ist dies möglicherweise nicht das eigentliche Zwischenprodukt. Das Zwischenprodukt wird daher als (CDAP) "aktiviertes" Polysaccharid bezeichnet. Während der ersten Aktivierungsphase kann das aktivierte Polysaccharid hydrolysieren (Reaktion 4) oder Nebenreaktionen (Reaktion 5) durchlaufen. In der zweiten Konjugationsphase (Reaktion 2) reagiert das aktivierte Polysaccharid mit einem Amin, um neben den Reaktionen 4 und 5 eine stabile Isoureabindung zu bilden. Abkürzungen: CDAP = 1-Cyano-4-dimethylaminopyridintetrafluoroborat; DMAP = 4-Dimethylaminopyridin; R-NH2 = Amin. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
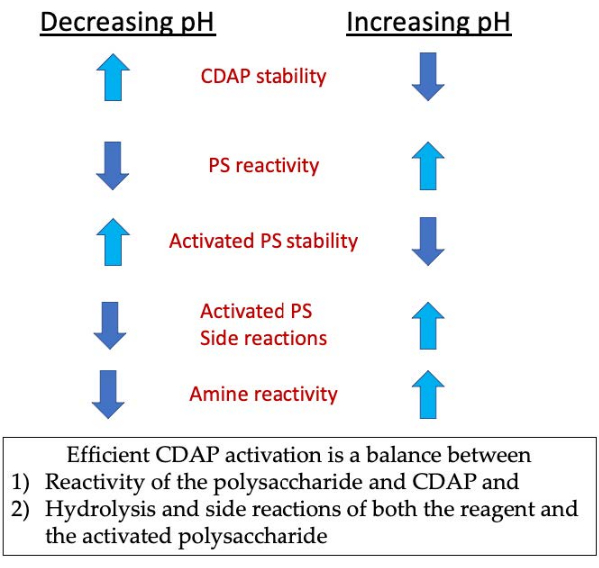
Abbildung 3:CDAP-Aktivierung und -Konjugation. Der Prozess erfordert ein Gleichgewicht zwischen der CDAP-Reaktivität mit dem Polysaccharid, der Stabilität des CDAP und des aktivierten Polysaccharids sowie der Reaktivität des aktivierten Polysaccharids mit der des Amins. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
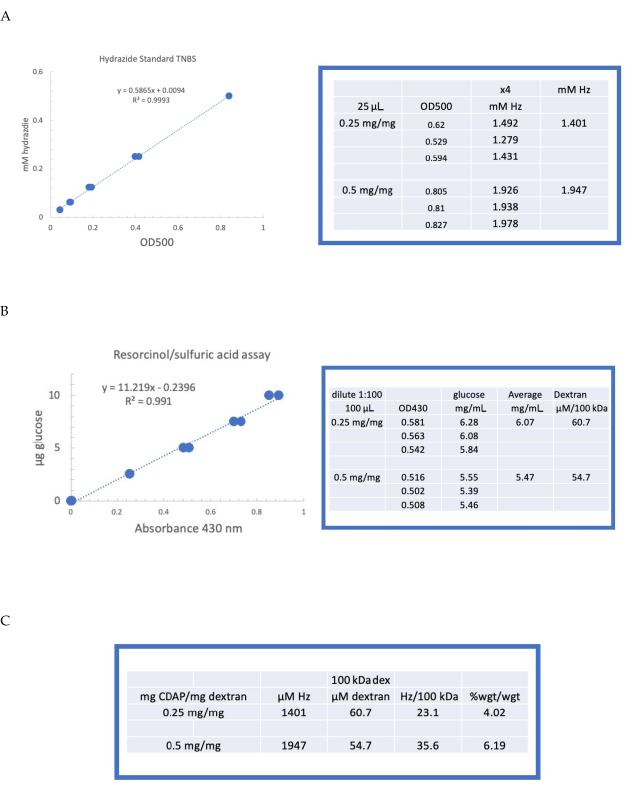
Abbildung 4: Repräsentative Ergebnisse für die CDAP-Aktivierung von Dextran. Typische Standardkurven für die (A) Resorcin/Schwefelsäure und (B) TNBS Assays. Die Assay-Ergebnisse für Dextran, das mit 0,25 und 0,5 mg CDAP/mg Dextran aktiviert wurde, werden gezeigt. Glukose wurde als Standard für den Resorcin-Assay verwendet. Dextran, in mg / ml, wird durch 100 kDa geteilt, um eine molare Konzentration zu erhalten. Die Hydrazidkonzentration wird unter Verwendung von ADH als Standard bestimmt und die Ergebnisse als μM Hz ausgedrückt. (C) Berechnung von Hydrazid: Dextranverhältnissen. Der Grad der Derivatisierung wurde als Hydrazide pro 100 kDa Dextran berechnet, um den Vergleich zwischen Polymeren unterschiedlicher mittlerer Molekulargewichte zu erleichtern. Das Prozentgewicht von g ADH/g Dextran wurde mit einem MW von 174 g/Mol für ADH berechnet. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Diskussion
CDAP ist ein praktisches Reagenz zur Derivatisierung und Konjugierung von Polysacchariden. Dieser Artikel beschreibt die allgemeine Methode zur Verwendung von CDAP zur Derivatisierung von Polysacchariden mit Hydraziden (PS-ADH) und enthält kürzlich veröffentlichte Verbesserungen8. Erstens betont die Technik, wie wichtig es ist, den Ziel-pH-Wert aufrechtzuerhalten, um den Aktivierungsprozess zu kontrollieren. Wir fanden heraus, dass, während viele gängige Puffer die CDAP-Aktivierungsreaktion stören, DMAP erfolgreich als Puffer zur Verwaltung despH-Werts 8verwendet werden könnte. Darüber hinaus ist DMAP bereits ein Reaktionsnebenprodukt der CDAP-Aktivierung. Schließlich ermöglicht die Pufferung der Polysaccharidlösung mit DMAP vor der Zugabe des CDAP eine präzise Ausrichtung und Aufrechterhaltung des pH-Werts der Reaktion. Wie wir beschreiben, ist es nützlich, den pH-Wert der konzentrierten DMAP-Stammlösung so einzustellen, dass sie, wenn sie verdünnt wird, den angestrebten pH-Wert erreicht. Zweitens verlangsamte die Durchführung des Prozesses in der Kälte die Reaktionszeit, wodurch der Aktivierungsprozess weniger hektisch und verzeihender wurde. Eine niedrigere Temperatur verringerte die CDAP-Hydrolyserate, und die optimale Aktivierungszeit bei pH 9 steigt von ~ 3 min auf ~ 15 min. Darüber hinaus ist weniger CDAP erforderlich, um das gleiche Aktivierungsniveau zu erreichen, als bei Raumtemperatur.
ADH-derivatisierte Polysaccharide können mit Carbodiimiden (z.B. EDAC)7zu Proteinen konjugiert werden. Zum Beispiel verwenden mehrere zugelassene Haemophilus influenzae b (Hib) -Impfstoffe das polyribosylribitolphosphat (PRP), das mit ADH derivatisiert wurde, um mit EDAC zu Tetanustoxoid zu konjugieren. CNBr wurde ursprünglich verwendet, aber CDAP ist ein viel einfacheres Reagenz für diesen Zweck. Nach unserer Erfahrung liegt ein guter Zielbereich für die ADH-Derivatisierung bei 10-30 Hydraziden pro 100 kDa Polysaccharid oder ~1-3 Gewachsprozent.
Das gleiche Verfahren kann verwendet werden, um Polysaccharide mit primären Aminen zu derivatisieren, indem die ADH durch ein Diamin ersetzt wird. Es wird empfohlen, Hexandiamin zu verwenden, um Polysaccharide mit Aminen8 zuderivatisieren. Das aminierte Polysaccharid(PS-NH2)kann mit Reagenzien konjugiert werden, die für die Proteinkonjugation entwickelt wurden11. Typischerweise wird das PS-NH2 mit einem Maleimid (z. B. Succinimidyl-4-[N-Maleimidomethyl]cyclohexan-1-carboxylat (SMCC) oder N-γ-Maleimidobutyryl-oxysuccinimid-Ester (GMBS)) derivatisiert und das Protein thioliert (z. B. mit Succinimidyl-3-(2-pyridyldithio)propionat (SPDP)). Die Thiol-Maleimid-Chemie ist sehr effizient.
Proteine können auch direkt an CDAP-aktivierte Polysaccharide über das ɛ-Amin an Lysine gekoppelt werden. Während das verwendete Aktivierungsprotokoll im Allgemeinen dem hier beschriebenen ähnlich ist, ist es notwendig, das Aktivierungsniveau, die Polysaccharid- und Proteinkonzentration sowie das Protein:Polysaccharid-Verhältnis5,6,8zu optimieren.
Dextran ist eines der am einfachsten zu aktivierenden Polysaccharide mit CDAP aufgrund seiner relativ hohen Dichte an Hydroxylgruppen, aber einige Polysaccharide, wie das Vi-Antigen, können eine Herausforderung darstellen. Folglich gibt es kein einziges "bestes" Protokoll für die CDAP-Konjugation direkt mit Proteinen. Wir schlagen vor, zunächst ein Protokoll zu entwickeln, um geeignete Aktivierungsniveaus zu erreichen, die durch das Ausmaß der Hydrazidderivatisierung bestimmt werden, und dann mit der direkten Proteinkonjugation zu CDAP-aktiviertem Polysaccharid fortzufahren.
Offenlegungen
Andrew Lees ist Gründer und Inhaber von Fina Biosolutions. Er hält mehrere Patente in Bezug auf cdAP-Chemie und profitiert von der Lizenzierung des Chemie- und CDAP-Konjugations-Know-hows.
Danksagungen
Die hier beschriebene Arbeit wurde von Fina Biosolutions LLC finanziert.
Materialien
| Name | Company | Catalog Number | Comments |
| Acetonitrile | Sigma | 34851 | |
| Adipic acid dihydrazide | Sigma | A0638 | MW 174 |
| Amicon Ultra 15 10 kDa | Millipore | UFC901008 | MW cutoff can be 30 kDa for 200 kDa PS |
| Analytical balance | |||
| Autotitrator or electronic pipet | |||
| Beaker 2-4 L | |||
| CDAP | SAFC | RES1458C | Sigma |
| DMAP | Sigma | 107700 | MW 122.2 |
| Flake ice | |||
| HCl 1 M | VWR | BDH7202-1 | |
| Micro stir bar | VWR | 76001-878 | |
| Microfuge tube (for CDAP) | VWR | 87003-294 | |
| NaCl | VWR | BDH9286 | |
| NaOH 1 M | Sigma | 1099130001 | |
| NaOH 10 M | Sigma | SX0607N-6 | |
| pH meter | |||
| pH probe | Cole Parmer | 55510-22 | 6 mm x 110 mm Epoxy single junction |
| pH temperature probe | |||
| Pipets & tips | |||
| Saline or PBS | |||
| Small beaker 5-20 mL | VWR | 10754-696 | A 10 mL beaker allows room for pH probe & pipet |
| Small ice bucket | |||
| Small spatula | |||
| Stir plate | |||
| Resorcinol assay | |||
| Combitip | Eppendorf | 10 ml | |
| DI water | |||
| Dialysis tubing | Repligen | 132650T | Spectra/Por 6-8kDa |
| Dialysis tubing clips | Repligen | 142150 | |
| Heating block | |||
| Nitrile gloves | VWR | ||
| Repeat pipettor | Eppendorf | M4 | |
| Resorcinol | Sigma | 398047 | |
| Sugar standard | As appropriate | ||
| Sulfuric acid 75% | VWR | BT126355-1L | |
| Timer | |||
| TNBS assay | |||
| Adipic dihydrazide | Sigma | A0638 | MW 174 |
| Borosilcate test tubes 12 x 75 | VWR | 47729-570 | |
| Sodium borate, 0.5 M pH 9 | Boston Biologicals | BB-160 | |
| TNBS 5% w/v | Sigma | P2297 | MW 293.17 |
Referenzen
- Ellis, R. W., Granoff, D. M. . Development and clinical uses of Haemophilus B conjugate vaccines. , (1994).
- Goebel, W. F., Avery, O. T. Chemo-immunological studies on conjugated carbohydrate-proteins. Journal of Experimental Medicine. 50 (4), 533-550 (1929).
- Mond, J. J., Vos, Q., Lees, A., Snapper, C. M. T cell independent antigens. Current Opinion in Immunology. 7 (3), 349-354 (1995).
- Cruse, J. M., Lewis, R. E. . Conjugate Vaccines. 10, (1989).
- Lees, A., Nelson, B. L., Mond, J. J. Activation of soluble polysaccharides with 1-cyano-4-dimethylaminopyridinium tetrafluoroborate for use in protein-polysaccharide conjugate vaccines and immunological reagents. Vaccine. 14 (3), 190-198 (1996).
- Shafer, D. E., et al. Activation of soluble polysaccharides with 1-cyano-4-dimethylaminopyridinium tetrafluoroborate (CDAP) for use in protein-polysaccharide conjugate vaccines and immunological reagents. II. Selective crosslinking of proteins to CDAP-activated polysaccharides. Vaccine. 18 (13), 1273-1281 (2000).
- Schneerson, R., Barrera, O., Sutton, A., Robbins, J. B. Preparation, characterization, and immunogenicity of Haemophilus influenzae type b polysaccharide-protein conjugates. Journal of Experimental Medicine. 152 (2), 361-376 (1980).
- Lees, A., Barr, J. F., Gebretnsae, S. Activation of soluble polysaccharides with 1-cyano- 4-dimethylaminopyridine tetrafluoroborate (CDAP) for use in protein-polysaccharide conjugate vaccines and immunological reagents. III Optimization of CDAP activation. Vaccines. 8 (4), 777 (2020).
- Qi, X. -. Y., Keyhani, N. O., Lee, Y. C. Spectrophotometric determination of hydrazine, hydrazides, and their mixtures with trinitrobenzenesulfonic acid. Analytical biochemistry. 175 (1), 139-144 (1988).
- Monsigny, M., Petit, C., Roche, A. C. Colorimetric determination of neutral sugars by a resorcinol sulfuric acid micromethod. Analytical biochemistry. 175 (2), 525-530 (1988).
- Hermanson, G. . Bioconjugate Techniques. 3rd ed. , (2013).
Erratum
Formal Correction: Erratum: Activation and Conjugation of Soluble Polysaccharides using 1-Cyano-4-Dimethylaminopyridine Tetrafluoroborate (CDAP)
Posted by JoVE Editors on 7/09/2021. Citeable Link.
An erratum was issued for: Activation and Conjugation of Soluble Polysaccharides using 1-Cyano-4-Dimethylaminopyridine Tetrafluoroborate (CDAP). A figure was updated.
Figure 4 was updated from:

Figure 4: Representative results for CDAP activation of dextran. Typical standard curves for the (A) resorcinol/sulfuric acid and (B) TNBS assays. The assay results for dextran activated with 0.25 and 0.5 mg CDAP/mg dextran are shown. Glucose was used as the standard for the resorcinol assay. Dextran, in mg/mL, is divided by 100 kDa to give a molar concentration. The hydrazide concentration is determined using ADH as the standard and the results expressed as µM Hz. (C) Calculation of hydrazide: dextran ratios.The level of derivatization was calculated as hydrazides per 100 kDa of dextran to facilitate the comparison between polymers of different average molecular weights. The % weight ratio of g ADH/g dextran was calculated using a MW of 174 g/mole for ADH. Please click here to view a larger version of this figure.
to:
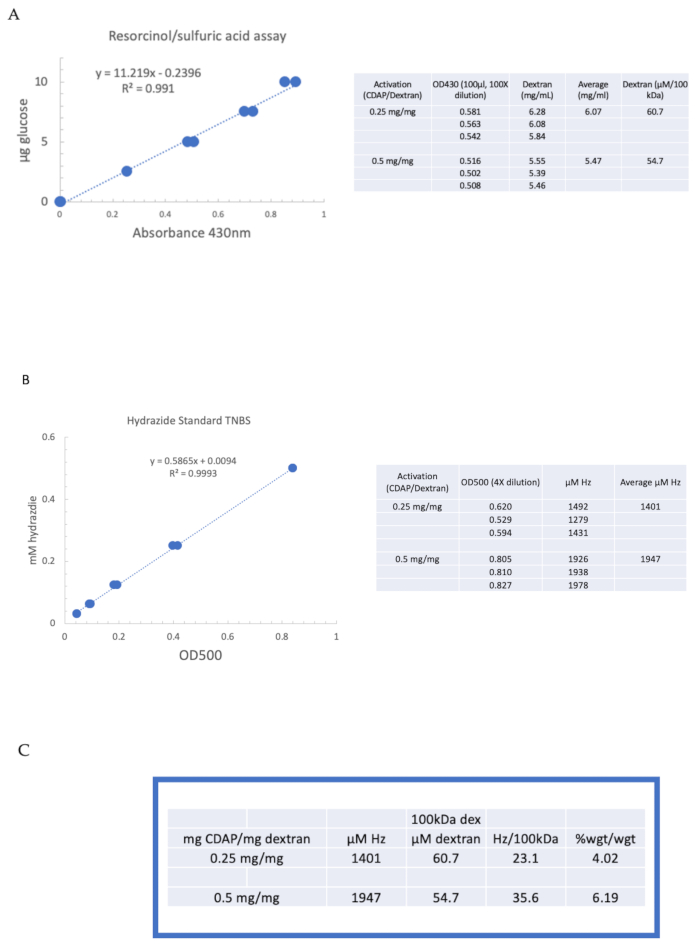
Figure 4: Representative results for CDAP activation of dextran. Typical standard curves for the (A) resorcinol/sulfuric acid and (B) TNBS assays. The assay results for dextran activated with 0.25 and 0.5 mg CDAP/mg dextran are shown. Glucose was used as the standard for the resorcinol assay. Dextran, in mg/mL, is divided by 100 kDa to give a molar concentration. The hydrazide concentration is determined using ADH as the standard and the results expressed as µM Hz. (C) Calculation of hydrazide: dextran ratios.The level of derivatization was calculated as hydrazides per 100 kDa of dextran to facilitate the comparison between polymers of different average molecular weights. The % weight ratio of g ADH/g dextran was calculated using a MW of 174 g/mole for ADH. Please click here to view a larger version of this figure.
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten