Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Caracterización fenotípica y funcional de las células endoteliales Formadoras de Colonias derivados de la sangre del cordón umbilical
En este artículo
Resumen
Las células endoteliales formadoras de colonias (ECFCs) son las células endoteliales circulantes con un robusto potencial de proliferación clonal que deben mostrarse intrínseca En vivo capacidad de formación. Caracterización fenotípica y funcional de las células endoteliales derivadas de la excrecencia CB son importantes para identificar y aislar Buena fe ECFCs de potencial aplicación clínica en la reparación de tejidos dañados.
Resumen
Puntos de vista de muchos años de la formación de nuevos vasos sanguíneos a través de la angiogénesis, vasculogénesis, y arteriogénesis se han revisado recientemente 1. La presencia de células progenitoras endoteliales circulantes (EPC) se identificaron por primera vez en adultos sangre periférica humana por Asahara et al. En 1997 2, trayendo una infusión de nuevas hipótesis y estrategias para la regeneración vascular y reparación. EPC son componentes poco comunes, pero normal de la sangre circulante de que el hogar de los sitios de formación de vasos sanguíneos o el remodelado vascular, y facilitar tanto la vasculogénesis postnatal, la angiogénesis, o en gran medida a través de arteriogénesis estimulación paracrina de la pared de los vasos existentes derivan las células 3. No hay un marcador específico para identificar un EPC ha sido identificado, y en la actualidad el estado del campo es comprender que numerosos tipos de células madre, incluyendo proangiogénico hematopoyéticas y las células progenitoras, las células circulantes angiogénicos, Tie2 + monocitos, cel progenitor mieloideLS, tumorales macrófagos asociados, y M2 macrófagos activados participar en la estimulación del proceso angiogénico en una variedad de sistemas de modelos animales preclínicos y en los sujetos humanos en numerosos estados de enfermedad 4, 5. Las células endoteliales formadoras de colonias (ECFCs) son raras que circulan células viables endoteliales caracterizados por robusto potencial clonal proliferativa, colonia secundaria y terciaria capacidad de formación sobre replating, y capacidad para formar intrínseca en los vasos in vivo sobre el trasplante a ratones inmunodeficientes 6-8. Mientras ECFCs se han aislado con éxito de la sangre periférica de adultos sanos, la sangre del cordón umbilical (CB) de recién nacidos sanos, y paredes de los vasos de numerosos vasos arteriales y venosos humanos 6-9, CB cuenta con la mayor frecuencia de ECFCs 7 que la pantalla el más robusto potencial proliferativo clonal y forma los vasos sanguíneos duraderos y funcionales in vivo 8, 10-13. Mientras que la derivación deECFC de la sangre periférica de adultos se han presentado 14, 15, aquí se describen las metodologías para la derivación, la clonación, la expansión, e in vitro, así como en la caracterización in vivo de ECFCs del CB umbilical humana.
Protocolo
Reactivos y Soluciones
EMG-2 los medios de comunicación (Lonza, cat. N º CC-3162-2 que contiene la MBE medio basal y el EGM-2 Complementos kit SingleQuot, y los factores de crecimiento)
MBE-2 (Lonza, cat. N ° CC-3156) suplementado con los suplementos kit completo SingleQuot y factores de crecimiento (Lonza, cat. N ° CC-4176), 10% (v / v) de suero fetal bovino (FBS) y 1% (v / v) penicilina (10.000 U / ml) / estreptomicina (10.000 g / ml) / anfotericina (25 g / ml). Almacena hasta 1 mes a 4 ° C. Recomendados EGM-2 volúmenes a utilizar para la cultura ECFC son 500 l / pocillo de placas de 24 pocillos, 2 ml / pocillo para placas de 6 pocillos, frascos 5ml/25-cm 2, y 10 frascos ml/75-cm 2, a menos que se especifique lo contrario en el protocolo.
Solución de colágeno I
Diluir 0,575 ml de ácido acético glacial (17.4N) en 495 ml de agua destilada estéril (0,02 N concentración final). Estéril filtro el ácido acético diluido con una aspiradora de 0,22 micrasuum sistema de filtración. Añadir 25 mg de colágeno de rata cola I del ácido acético diluido a una concentración final de 50 g / ml. La cantidad de colágeno añadido variará dependiendo de la concentración de stock de colágeno. Almacene hasta por un mes a 4 ° C.
Preparación de colágeno I-recubiertos con superficies de cultivo de tejidos
Colocar 1 ml de solución de colágeno I en cada pocillo de una placa de tejido de 6 pocillos de cultivo (uso de 300 l / pocillo de placas de 24 pocillos, frascos 3ml/25-cm 2, y 8 frascos ml/75-cm 2). Incubar 1 hora a la noche a 37 ° C. Retire la solución de colágeno I y lavar la superficie dos veces, cada vez con PBS (utilizar 500 l / pocillo de placas de 24 pocillos, ml 2 / y para las placas de 6 pocillos, frascos 5ml/25-cm 2 y 10 ml/75 -cm2). Use platos de inmediato para los cultivos celulares.
FACS tampón de tinción
Salina tamponada con fosfato (PBS) suplementado con 2% (v / v) de suero fetal bovino (FBS). Tienda up para 2 semanas a 4 ° C.
A. TRANSFORMACIONES ECFC, clonación y de expansión
- Recoger CB con heparina (10 U de heparina / ml de sangre) o EDTA como anticoagulante y el transporte al laboratorio a temperatura ambiente y de inmediato (dentro de 2 horas después del parto del bebé) proceso de la muestra de células mononucleares (MNC) de aislamiento.
- Alícuota de 15 ml de CB en cada tubo de centrífuga de 50 ml cónico y añadir 20 ml de PBS a cada tubo de veces CB y la pipeta para mezclar varios. Elaboración de 15 ml de Ficoll-Paque en una jeringa de 20 ml y conecte una aguja 20G o cánula de mezcla. Colocar la punta de la cánula de mezcla en la parte inferior del tubo de sangre diluida y cuidadosamente subyacía 15 ml de Ficoll-Pague. Centrifugar los tubos 30 minutos a 740 xg, a temperatura ambiente, sin el ajuste del freno de deceleración.
- Utilizando una pipeta de transferencia, eliminar la capa brumosa de baja densidad CMN situado en la interfase entre el plasma de Ficoll-Paque y diluida. Distribuir las multinacionales en un cont tubo de 50 ml cónicoaining 10 ml EGM-2 medio. Centrifugar las multinacionales 10 minutos a 515 xg, a temperatura ambiente, con un ajuste de la desaceleración de frenos de alto.
- Con cuidado aspirar y descartar el sobrenadante. Lavar las células sedimentadas con EGM-2 dos veces (10 min a 515 xg) y volver a suspender las multinacionales en el EGM-2 a 1.25 x 10 7 células / ml. Preparar colágeno I recubiertos 6-y placas de cultivo tisular mediante la adición de 1 ml de cola de rata colágeno de tipo I (50 g / ml) por pocillo y se incubó la placa durante la noche. Pipetear 4 ml de esta suspensión MNC en cada pocillo y colocar las células en 37 ° C, 5% de CO 2 incubadora humidificada. A.1.5) Después de 24 horas (día 1), retire lentamente el medio gastado (no molestar a las células débilmente adherentes) desde el pozo con una pipeta, añadir lentamente 4 ml EGM-2 a la fuente, y devolver la placa a la incubadora . En el día 2, refrescar el medio por lentamente eliminando el medio (no molestar las células débilmente adherentes) desde el pozo con una pipeta y la adición de 4 ml de EGM-2 a cada pocillo. Repita el medio de cambio diario de las Naciones Unidashasta que el día 7 y cada dos días a partir de entonces hasta que las colonias ECFC aparecen para la clonación. Típicamente aparecen colonias entre el día 5 y el día 14 días 7 (fig. 1).
- Visualice típicas colonias con morfología ECFC adoquines con microscopio invertido (10 aumentos) y marcar los límites de la colonia con un marcador en la parte inferior del pozo para indicar la posición de cada colonia.
- En el día 14, lavar estas colonias primarias 2 veces con PBS y las colonias de cosecha individuales utilizando cilindros de clonación y sólo lo suficiente para cubrir TrypLE expresa las células dentro de los cilindros. Después de aspirar el lavado final de PBS, coloque un cilindro recubierto de gel estéril en torno a la clonación de cada colonia y presione firmemente contra la placa utilizando pinzas estériles. Añadir 2-3 gotas de cálida TrypLE expresa en cada cilindro de clonación e incubar durante 3-5 minutos hasta que las células dentro del cilindro empieza a desprenderse. Añadir aproximadamente 250 l medio EGM-2 en el centro del cilindro y pipetear arriba y hacia abajo a generate suspensión de células individuales. Transferir la suspensión de células individuales de cada cilindro clonación por separado en un individuo de micro-centrífuga tubo.
- Lavar la zona dentro de los cilindros 2-3 veces con aproximadamente 250 l EGM-2 medio para recoger todas las células restantes y transferir el lavado de cada cilindro en el respectivo tubo de microcentrífuga. Centrifugar las células a alta velocidad (≤ 300 xg) en centrífuga de mesa durante 5 min.
- Separar el sobrenadante y resuspender el pellet de células en 1,5 ml fresca EGM-2 medio. Transferir la suspensión de células (que contiene todas las células de colonias individuales) de cada tubo en un pocillo de una placa de tejido 24-pocillos pre-recubiertas con 500 l colágeno I de cola de rata (50 g / ml).
- Coloque dentro de la incubadora para la expansión de los medios de comunicación con el cambio realizado en días alternos.
- Cuando las células acercarse 80-90% de confluencia, se elimina el medio gastado luego lavar las células 2 veces con PBS y se añaden 500 l TrypLE medio expresa a cada pocillode 24-pocillos de cultivo de tejidos. Introducir la placa en la incubadora por 3-5 min hasta que las células comienzan a reunir y separar. Añadir 1 ml de EGM-2 (con 10% FBS definido) a cada pocillo para recoger las células por lavado y transferirlas a un tubo de 15 ml. Lavar el pozo con 1 ml de EGM-2 medio para recoger todas las células restantes y transferir el lavado de cada pocillo en el tubo respectivo 15 ml. Centrifugar las células a 300 xg durante 5 min.
- Retire el medio y volver a suspender el pellet de células en 1 ml fresca EGM-2 medianas (con FBS al 10% se define). Obtener el recuento de células viables de una alícuota utilizando un hemacitómetro y exclusión con azul tripán.
- Ampliar las células por la siembra de cerca de 5000 células / cm 2 en un colágeno I antes de superficies recubiertas de cultivo de tejidos en el EGM-2 medios de comunicación con los medios de comunicación cambian cada dos días hasta que las células se acercan 80-90% de confluencia antes de sub-cultivo nuevo.
B. Caracterización fenotípica in vitro de ECFCs: superficie endotelial expresión del antígeno de unEnsayo d Single Cell para el potencial de proliferación clonal
- Para la expresión del antígeno de superficie de células endoteliales, separar las células con TrypLE expresa para recoger las células mediante métodos descritos para la clonación ECFC y expansión.
- Vuelva a suspender las células en el tampón de tinción FACS (10 x 10 6 células por FACS 1ml buffer de tinción) a continuación, añadir el reactivo FcR bloqueo (20 l / 10 x 10 6 células), mezclar suavemente y colocar en hielo durante 10 minutos.
- Alícuota de 100 l de esta suspensión de células en un tubo de microcentrífuga para cada antígeno de superficie endotelial y controles de isotipo. Añadir la cantidad apropiada de fluorocromo etiquetados anticuerpos humanos monoclonales que reconocen antígenos endoteliales (CD31, CD144, CD146, y CD105) o antígenos hematopoyéticas (CD45, y CD14) y se deja en hielo durante 30 minutos protegido de la luz. Atención: 1 x 10 6 células no se requieren para cada prueba. Los autores suelen preparar 0,5 a 1 x 10 5 células / tubo para obtener 2 X 10 4 analizard eventos. Además, seguir la recomendación del fabricante para la cantidad de anticuerpo que se utilizará para cada prueba. Algunos anticuerpos pueden requerir titulación para determinar la concentración óptima de anticuerpos. Todas las manchas que los autores han realizado son la tinción de un solo color.
- Después de 30 minutos de incubación en hielo, centrifugar cada tubo a alta velocidad en una centrífuga de mesa para 5 minutos ya continuación separar el sobrenadante y resuspender el sedimento celular en tampón FACS.
- Analizar las muestras en un citómetro de flujo para determinar el porcentaje de células que mancha positiva o negativamente para cada antígeno. ECFCs mancha uniformemente positivos para CD31, CD144, y CD146, pero negativo para CD45 y CD14 en comparación con los controles de isotipo correspondiente.
- Para el ensayo de célula única para examinar el potencial de proliferación clonal, separar la pronta aprobación (2-3) con las células TrypLE expresa para recoger las células usando métodos similares a los que se ha descrito para la clonación ECFC y expansión.
- Infectar a estas célulascon el aumento de la proteína verde fluorescente (EGFP) que expresa los lentivirus 16 y recoger las células que expresan EGFP por citometría de fluorescencia. Atención: El trabajo con los lentivirus se considera un riesgo biológico y todas las precauciones de bioseguridad debe ser obedecido.
- Cultura que se ha descrito para ECFC cultivo en la sección de expansión ECFC.
- Preparar colágeno I recubiertos placas de 96 pocillos añadiendo 50 l de cola de rata colágeno tipo I (50 mg / ml) por pocillo y se incuba la placa durante la noche. Recoge los EGFP + ECFCs mediante el uso de TrypLE expresa y resuspender en medio EGM-2 con una concentración final de aproximadamente 10 6 células / ml.
- Utilizar FACS Vantage (Becton Dickinson) o clasificador comparable con el caudal bajo de 20 células / segundo para ordenar una sola EGFP + ECFC por pocillo de una placa de 96 pocillos y ajustar el volumen final a 200 l por pocillo con EGM-2. Utilizar un microscopio de fluorescencia invertida para asegurar que cada pocillo recibió sólo una célula. AlternativEly, las células individuales se pueden clasificar sobre la base de FSC y SSC y Sytox colorante nuclear tinción de las colonias se puede utilizar para la puntuación de células y cuantificación.
- Se incuba la placa durante un período de dos semanas, con dos cambios de los medios de comunicación (200 l EGM-2 con pipeta multicanal) realizadas en el día 5 y el día 10. En el día 14 de cultivo, lavar cada pocillo con 100 l de PBS antes de que se fijan las células con 100 l de paraformaldehído al 4% durante 30 min. Para ECFCs que no se expresan EGFP, añadir reactivo Sytox, un tinte verde fluorescente nuclear, tras la fijación de paraformaldehído y se incuba a 4 ° C durante la noche.
- Utilizar un microscopio de fluorescencia para examinar cada pocillo para cuantificar el número de células endoteliales que se expandieron a partir de una única célula cultivaron durante 14 días. Para el análisis cuantitativo, los pozos de puntuación de 2 o más células endoteliales como positivo (para la proliferación) y examinar a más de recuento total de células endoteliales por conteo visual con el microscopio de fluorescencia.
- Para mostrar tobtuvo los datos, los pozos con un número de células endoteliales de: 2 a 50, 51-2000, y 2001 o más, son considerados como: grupos de células endoteliales, de bajo potencial proliferativo (LPP)-ECFCs y alto potencial proliferativo (HPP) - ECFCs respectivamente. ECFCs exhiben jerarquía completa del potencial proliferativo clonal dando lugar a grupos endoteliales, LPP y HPPS cuando se cultivan en un nivel de células individuales durante 14 días. 7
C. En la caracterización in vivo de funcionamiento de ECFCs: Ensayo de Formación in vivo del barco para examinar el potencial de la ECFC para vasculogénesis
- Preparar los implantes de gel cellularized mediante el cálculo del volumen total (ml) de cada uno de los materiales de gel siguientes (con la concentración final en el paréntesis) necesaria para emitir 1-ml de gel (que será posteriormente dividida para generar 2 implantes): FBS (10 %), EBM-2 10:01 (ajustar el volumen final a 1 ml), bicarbonato de sodio (1,5 mg / ml), NaOH (ajustar el pH a 7,4), HEPES (25 mM), fibronectin (100 ug / ml), y colágeno I (1,5 mg / ml).
- Después de cálculo gel de tela, separar las células con TrypLE expresa para recoger las células utilizando métodos similares a que se ha descrito para la clonación ECFC y expansión. Obtener un recuento de células viables de una alícuota utilizando un hemocitómetro y azul de tripano. Transferir 2,4 millones de células viables en un 50 ml-cónica del tubo y precipitar las células por centrifugación a 515 xg, a temperatura ambiente. Al mismo tiempo, preparar la solución de gel de matriz mediante la adición de volúmenes calculados de HEPES, bicarbonato sódico, 10:1 MBE-2, FBS, fibronectina y de colágeno a un helado de 50-ml tubo cónico (en el mismo orden en que aparecen). Mezclar bien y ajustar el pH a 7,4 con NaOH manteniendo solución en hielo.
- Desechar el sobrenadante de las células después de la centrifugación y volver a suspender el sedimento en 360 l caliente EGM-2 y, para añadir pH ajustado 840 l de gel de disolución de la matriz, haciendo que el volumen final de implante de gel de 1 ml. Mezclar las células en una solución matriz de gel lentamente hastaLas células están completamente suspendidas en la solución de gel.
- Transferir este 1 ml de suspensión de gel cellularized a un pocillo de una placa de tejido 12-pocillos y se incuba durante 20-30 minutos hasta que el gel se polimeriza. Suavemente cubrir el gel con 2 ml de tibia EGM-2 e incubar durante la noche.
- Inmediatamente antes de la implantación, dividir en dos el gel incubaron durante la noche en dos partes iguales con unas tijeras iris y devolver las piezas de gel a la misma cultura y que contiene EGM-2 medio.
- Utilice el centro de cirugía de animales para sedar al animal (5-6 semanas de edad ratones NOD / SCID) mediante la administración de la anestesia con isoflurano. Afeitarse la parte inferior del abdomen y limpie la zona quirúrgica con toallitas impregnadas en alcohol y betadine o de otro antiséptico. A continuación, aislar el área con cortinas según las directrices del IACUC e institucional.
- Usando estériles afiladas tijeras iris para hacer una incisión de aproximadamente 5 mm en el cuadrante inferior del abdomen, dejando al descubierto el espacio subcutáneo entre la piel y los músculos abdominales. Lleve a cabo una disección roma a través de la capa dérmica de la musculatura abdominal para crear un bolsillo de 15-20 mm de ancho que conduce superiores en el cuadrante superior del abdomen. Repita el procedimiento similar para crear el bolsillo similares abierto en otro lado del abdomen mismo ratón.
- Inserte una pieza de la mitad de gel en un lado de su bolsillo abdominal y otra pieza de la mitad de gel en el otro lado de la bolsa abdominal, mediante el levantamiento de la capa dérmica acaba de caudal a la incisión.
- Después de la inserción de los geles, cerrar cada incisión con puntos de sutura de 2-3 con sutura de polipropileno 5-0 en una aguja de corte. Coloque una etiqueta a las cartas de la jaula y realizar el seguimiento post-quirúrgico y la analgesia según las necesidades institucionales y de protocolo y de 14 días para las células de estos geles implantadas para generar vasos de novo.
- Por último, la recolección de los implantes de gel se realiza normalmente 14 días después de la implantación después de la eutanasia con el ratón.
- Limpie el área abdominal con toallitas impregnadas en alcohol ycortar la piel del abdomen caudal a la línea de la incisión original. Con cuidado, diseccionar el implante mediante la eliminación de un colgajo de piel de caudales a la probable ubicación del gel. Impuestos Especiales del implante mediante la reducción de circunferencia alrededor del gel fijador, luego colóquelo en zinc (BD Biosciences, siga las recomendaciones del fabricante para obtener resultados óptimos) y les permite fijar durante 1-2 horas a temperatura ambiente.
- Preparar los geles embebidos en parafina utilizando los protocolos estándar de histoquímicas y preparar 5 de grosor, a portaobjetos de vidrio para realizar la tinción con hematoxilina y eosina, anti-humano CD31 o anti-CD31 de ratón para visualizar los vasos dentro del gel. ECFCs sufren de vasculogénesis novo para generar vasos humanizados en los implantes de gel de cellularized inserta en ratones inmunodeficientes durante 14 días 4,8,11.
D. Representante Resultados
Usando esta técnica de derivación ECFC hemos observado un crecimiento fuera de la forma de la colonia principalación tan pronto como el día 5 (fig. 1). Las colonias de crecimiento fuera ECFC exhibió aspecto en empedrado típico y dio lugar a duplicaciones> 40 la población sobre la expansión a largo plazo después de la recogida de colonias por clonación. Colonias expandidas expresaron antígenos endoteliales, pero no expresan antígenos hematopoyéticos (fig. 2). Es importante destacar que se muestra una jerarquía completa de potencial proliferativo clonal en un nivel de células individuales (fig. 3). Además, ECFCs formado vasos sanguíneos que están humanizados perfundidos con eritrocitos huésped cuando se implantan en ratones inmunodeficientes 4, 6, 8, 11 (Fig. 4).
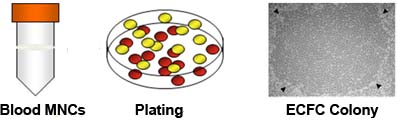
Figura 1. Aislamiento de células mononucleares (MNC) de sangre del cordón umbilical y la consecuencia de la colonia de células endoteliales que forman (ECFCs) de las empresas multinacionales culta. Capa de forma multinacionales capa leucocitaria durante Ficoll-Pague la separación en gradiente de densidad de las células de sangre de cordón. El aislamiento de la capa de la capa leucocitaria a la cultura las empresas multinacionales sobre el colágeno de cola de rata que los resultados de las placas de revestimiento en consecuencia de la colonia ECFC de 5 a 14 días. La colonia ECFC consecuencia (indicado por las cabezas de flecha) muestra la morfología de adoquines 7.
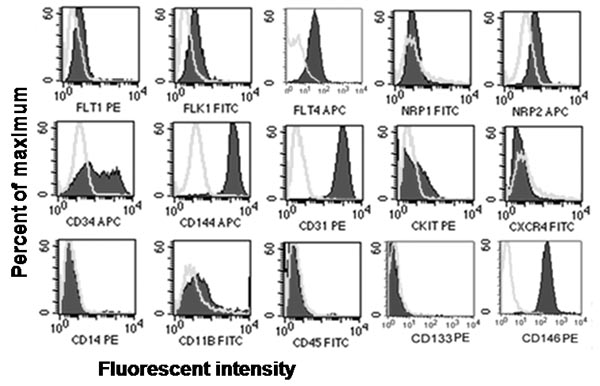
Figura 2. Representante in vitro de evaluación fenotípica de la expresión del antígeno de las células endoteliales y hematopoyéticas superficie. Inmune de la médula derivados de la sangre ECFCs reveló que ECFCs expresaron antígenos endoteliales CD31, CD34, CD144, CD146, FLT-1, Flk-1, Flt-4, y NRP2, pero no expresan antígenos hematopoyéticos CD45, CD14, CD11b, cKit, CXCR4 o AC133 7, 8.
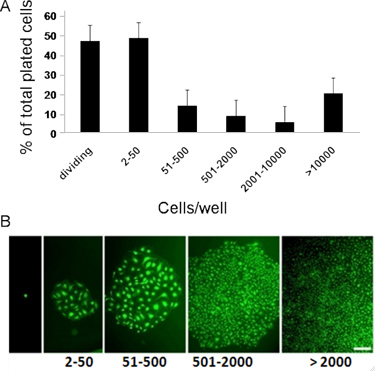
Figura 3. Representante en la cuantificación in vitro de la clonogénico y el potencial de proliferación de CB ECFCs derivados. (A) de sangre de cordónLos derivados ECFCs mostrar el potencial de proliferación clonal, con una jerarquía de las colonias que van desde grupos de 2-50 células hasta las colonias de> 2001. (B) Las micrografías de la jerarquía de las colonias (las colonias teñidas con, Sytox, un colorante fluorescente verde nucleares a que tomen imágenes de mejor calidad) obtenido después de la sangre del cordón derivados ECFCs se cultivaron en un nivel de células individuales durante 14 días. Barra de escala representa 100 micras 7, 8.
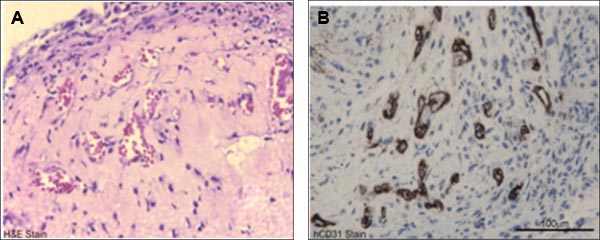
Figura 4. Representante en la caracterización in vivo funcional de sangre de cordón umbilical derivados ECFCs. A) H & E tinción de sangre del cordón umbilical derivado ECFC que contiene los implantes de gel de cellularized indicó microvasos (llena de glóbulos rojos de acogida), en la formación de gel de colágeno, fibronectina, después de 14 días a partir de la implantación. B) anti-CD31 humano coloración (manchas marrones) confirma una vez más el origen humano de estas embarcaciones.
Discusión
Caracterización fenotípica y funcional de las supuestas células progenitoras endoteliales es importante identificar los ECFCs de buena fe que son capaces de clonación y la serie de re-siembra en la cultura y dar lugar a los vasos sanguíneos duraderos y funcionales implantables in vivo. La sangre de cordón umbilical humano se enriquece con ECFCs y la concentración de estos descensos que circulan células con el envejecimiento o la enfermedad 10. Estudios recientes sugieren que ECFC pue...
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Dr. Yoder es consultor de Tecnologías de la EndGenitor, Inc. y miembro de la junta directiva de las Tecnologías de Rimedion, Inc.
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre del reactivo | Empresa | Número de catálogo | |
| Heparina sódica inyectable, USP | APP Pharmaceuticals | 504031 | |
| Ficoll-Pague | Amersham Biosciences | 17-1440-03 | |
| Mezcla cánula | Maersk Medical | 500.11.012 | |
| EGM-2 | Lonza | CC-3162 | |
| SFB se define | Hyclone | SH30070.03 | |
| TrypLE expresa | Gibco | 12605 | |
| Rata de colágeno tipo I | BD Biosciences | 354236 | |
| Matrigel | BD Biosciences | 356234 | |
| Bloquear FcR | Miltenyi Biotech | 130-059-901 | |
| hCD31, FITC conjugaciónTed | BD Pharmingen | 555445 | |
| hCD45, conjugado con FITC | BD Pharmingen | 555482 | |
| hCD14, conjugado con FITC | BD Pharmingen | 555397 | |
| hCD144, conjugado PE | eBioscience | 12-1449-80 | |
| hCD146, conjugado PE | BD Pharmingen | 550315 | |
| hCD105, conjugado PE | Invitrogen | MHCD10504 | |
| Sra. IgG1, k del anticuerpo, conjugado con FITC | BD Pharmingen | 555748 | |
| D. IgG 1, anticuerpo k, conjugado PE | BD Pharmingen | 559320 | |
| Sra. IgG2a, anticuerpo k, conjugado con FITC | BD Pharmingen | 555573 | |
| Anti-CD31 humano | Dako | clon de JC70 / A | |
| Anti-mousCD31 e | BD Pharmingen | 553370 | |
| 0,22-micras vacío sistema de filtración | Millipore | SCGPU05RE | |
| Ácido acético glacial, 17.4N | Pescador | A38-500 | |
| Antibiótico-antimicótico | Invitrogen | 15240-062 | |
| Suero fetal bovino (SFB) | Hyclone | SH30070.03 | |
| IHC zinc Fijador | BD Biosciences | 550523 | |
| Sytox verde reactivo | Invitrogen | S33025 | |
| Cilindros de clonación y estériles | Fisher Scientific | 07-907-10 |
Referencias
- Carmeliet, P., Jain, R. K. Molecular mechanisms and clinical applications of angiogenesis. Nature. 473, 298-307 (2011).
- Asahara, T. Isolation of putative progenitor endothelial cells for angiogenesis. Science. 275, 964-967 (1997).
- Urbich, C., Dimmeler, S. Endothelial progenitor cells: characterization and role in vascular biology. Circ. Res. 95, 343-353 (2004).
- Critser, P. J., Voytik-Harbin, S. L., Yoder, M. C. Isolating and defining cells to engineer human blood vessels. Cell. Prolif. 44, 15-21 (2011).
- Matthias, M., David, N., Josef, N. From bench to bedside: what physicians need to know about endothelial progenitor cells. Am. J. Med. 124, 489-4897 (2011).
- Ingram, D. A. Vessel wall-derived endothelial cells rapidly proliferate because they contain a complete hierarchy of endothelial progenitor cells. Blood. 105, 2783-276 (2005).
- Ingram, D. A. Identification of a novel hierarchy of endothelial progenitor cells using human peripheral and umbilical cord blood. Blood. 104, 2752-2760 (2004).
- Yoder, M. C. Redefining endothelial progenitor cells via clonal analysis and hematopoietic stem/progenitor cell principals. Blood. 109, 1801-1809 (2007).
- Reinisch, A., Strunk, D. Isolation and Animal Serum Free Expansion of Human Umbilical Cord Derived Mesenchymal Stromal Cells (MSCs) and Endothelial Colony Forming Progenitor Cells (ECFCs. J. Vis. Exp. (32), e1525 (2009).
- Au, P. Differential in vivo potential of endothelial progenitor cells from human umbilical cord blood and adult peripheral blood to form functional long-lasting vessels. Blood. 111, 1302-135 (2008).
- Critser, P. J., Kreger, S. T., Voytik-Harbin, S. L., Yoder, M. C. Collagen matrix physical properties modulate endothelial colony forming cell-derived vessels in vivo. Microvasc. Res. 80, 23-30 (2010).
- Melero-Martin, J. M. Engineering robust and functional vascular networks in vivo with human adult and cord blood-derived progenitor cells. Circ. Res. 103, 194-202 (2008).
- Melero-Martin, J. M. In vivo vasculogenic potential of human blood-derived endothelial progenitor cells. Blood. 109, 4761-4768 (2007).
- Hofmann, N. A., Reinisch, A., Strunk, D. Isolation and Large Scale Expansion of Adult Human Endothelial Colony Forming Progenitor Cells. J. Vis. Exp. (32), e1524 (2009).
- Lin, Y., Weisdorf, D. J., Solovey, A., Hebbel, R. P. Origins of circulating endothelial cells and endothelial outgrowth from blood. J. Clin. Invest. 105, 71-77 (2000).
- Witting, S. R. Efficient Large Volume Lentiviral Vector Production Using Flow Electroporation. Hum. Gene. Ther. , (2011).
- Yoon, C. H. Synergistic neovascularization by mixed transplantation of early endothelial progenitor cells and late outgrowth endothelial cells: the role of angiogenic cytokines and matrix metalloproteinases. Circulation. , 112-1618 (2005).
- Dubois, C. Differential effects of progenitor cell populations on left ventricular remodeling and myocardial neovascularization after myocardial infarction. J. Am. Coll. Cardiol. 55, 2232-2243 (2010).
- Medina, R. J., O'Neill, C. L., Humphreys, M. W., Gardiner, T. A., Stitt, A. W. Outgrowth endothelial cells: characterization and their potential for reversing ischemic retinopathy. Invest. Ophthalmol. Vis. Sci. 51, 5906-5913 (2010).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados