Method Article
Implantación del Corazón Artificial Total SynCardia
En este artículo
Resumen
El objetivo de este manuscrito es revisar brevemente las indicaciones, la gestión y los resultados para el corazón artificial total. Se presentan las técnicas quirúrgicas para la implantación del dispositivo de vídeo.
Resumen
Con los avances en la tecnología, el uso de dispositivos de asistencia circulatoria mecánica por insuficiencia cardiaca en etapa terminal se ha incrementado rápidamente. La gran mayoría de estos pacientes son en general un buen servicio de los dispositivos de asistencia ventricular izquierda (LVADs). Sin embargo, un subgrupo de pacientes con insuficiencia biventricular etapa tardía o otras lesiones anatómicas importantes no son tratados adecuadamente por el soporte mecánico ventricular izquierda aislada. Ejemplos de patología cardiaca concomitante que puede ser mejor tratado por resección y TAH reemplazo incluye: Poste de miocardio defecto septal ventricular, aneurisma de aorta root / disección, el fracaso del injerto cardíaco, trombo ventricular masiva, arritmias malignas refractarios (independientes de las presiones de llenado), hipertrófica / restrictiva cardiomiopatía, y la cardiopatía congénita compleja. Los pacientes a menudo presentan con shock cardiogénico y la disfunción de órganos y sistemas múltiples. La escisión de ambos ventrículos y sustitución ortotópica con un total de Artificcorazón IAL (TAH) es un eficaz, aunque extrema, la terapia para una rápida restauración del flujo sanguíneo y reanimación. Manejo perioperatorio se centra en la reanimación del órgano blanco y la rehabilitación física. Además de las preocupaciones habituales de infección, sangrado y tromboembolismo común a todos los pacientes admitidos mecánicamente, los pacientes TAH enfrentan riesgos particulares en relación con la insuficiencia renal y la anemia. La suplementación de la disminución abrupta de péptido natriurético cerebral después ventriculectomía parece tener efectos renales de protección. Anemia después de la implantación TAH puede ser profundo y persistente. Sin embargo, la anemia es generalmente bien tolerado y la transfusión se limitan a evitar la sensibilización HLA. Hasta hace poco, los pacientes TAH fueron confinados como pacientes atados a un controlador de consola 500 libras neumática. Reciente introducción de una mochila de tamaño controlador portátil (actualmente en ensayo clínico), ha permitido que los pacientes recibieron el alta domiciliaria e incluso volver al trabajo. A pesar de la profunda presenteación de estos pacientes enfermos, hay un éxito 79-87% en puente para el trasplante.
Introducción
El primer implante humano de un corazón artificial total (TAH) en el año 1969 se realizó por Denton Cooley en un varón de 47 años que fue incapaz de desconexión de un bypass cardiopulmonar después de la reparación de aneurisma ventricular izquierdo. El dispositivo experimental proporcionado soporte hemodinámico durante 64 horas hasta que un corazón donado se pudo encontrar. Aunque, soporte de dispositivos técnicamente exitosa se complicó por hemólisis e insuficiencia renal. El paciente pasaría a morir a causa de la abrumadora sepsis 32 horas después del trasplante 1. Un segundo intento de Cooley en 1981 tuvo resultados desafortunados similares 2. En 1982, William DeVries realizó el primer implante permanente ampliamente publicitado de la TAH Jarvik-7 en un dentista de 61 años de edad. El paciente tuvo un curso postoperatorio difícil marcado por insuficiencia respiratoria recurrente, fractura del puntal de la válvula mitral protésica requiere un reemplazo del dispositivo, sepsis, accidente cerebrovascular, insuficiencia renal intermitente, y el sangrado relacionado con anticoagulaciónción. Él finalmente sucumbió después de 112 días para la colitis pseudomembranosa 3.
A pesar de estos resultados desalentadores iniciales, el refinamiento progresivo en el diseño del dispositivo, la selección de pacientes, y el tratamiento del paciente han dado lugar a una marcada mejoría en los resultados. El Jarvik-7, ha desarrollado desde entonces en la SynCardia TAH, que sigue siendo el único aprobado por la FDA TAH en uso clínico actual. Hasta la fecha, más de 1.000 implantes se han realizado en todo el mundo 4.
Presentamos nuestras técnicas operatorias institucionales en el contexto de un caso clínico de vídeo.
Protocolo
Presentación del caso:
El paciente es un varón de 60 años con miocardiopatía hipertrófica. Ha desarrollado síntomas progresivos de insuficiencia cardiaca en los últimos 10 años, con las últimas múltiples reingresos por insuficiencia cardíaca descompensada. Él se inició el milrinona crónica IV, y se anunciaba para el trasplante de corazón. Su PMH se caracteriza por arritmias auriculares s / p ablación, la embolia pulmonar recurrente, hipertensión pulmonar, el trombo de la aurícula izquierda, y el accidente cerebrovascular previo. Prueba de esfuerzo cardiopulmonar demostró un consumo máximo de oxígeno bajo (VO 2 máx 10.6 ml / kg min). Imaging se destacó por severa hipertrofia LV con moderada a severamente reducida función sistólica, y ninguna obstrucción del tracto de salida del VI (FEVI 25-30%, LVIDd 5,0 cm, 1,5 cm IVSD, LVPWd 1,5 cm). Él tenía un gran trombo de la aurícula izquierda en el apéndice y un posible trombo LV también. Hemodinámica (en milrinona 0,5 mcg / kg / min) fueron notables por: RA 17 mmHg, PCWP 37 mmHg, PA 74/35 mmHg y Fick CI 1,4 l/min/m2. Debido a su miopatía restrictiva y pequeña cavidad del ventrículo izquierdo, que fue considerado como un mal candidato para aislado asistencia ventricular.
1. El dispositivo
- El total de corazón artificial SynCardia es el único aprobado por la FDA TAH en uso clínico. Fue introducido por primera vez en 1982 como el corazón Jarvik-7.
- El dispositivo consta de 2 cámaras del ventrículo de poliuretano. Cada cámara tiene un volumen de carrera máxima de ~ 70 ml. Cada cámara tiene 2 válvulas de disco basculante (Medtronic Pasillo, 27 mm de flujo de entrada, de salida 25 mm) para dirigir flujo de sangre y la salida. Cada cámara es accionado neumáticamente por una línea de transmisión separada conectada a un controlador en forma externa (Figura 1).
2. Indicaciones
- El dispositivo de desplaza un volumen total de ~ 400 ml. Recomendación general mínimo receptor incluye una BSA> 1,7 m 2 y un diámetro torácico (AP columna dimensión al esternón a nivel del 10 ª vértebra torácica)> 10 cm (Figura 2). La colocación en pacientes más pequeños es posible mediante el desplazamiento del dispositivo en la parte izquierda del pecho aunque esto aumenta el riesgo de la vena pulmonar del lado izquierdo y la compresión de los bronquios. Un dispositivo de tamaño pequeño para uso en pacientes menores está en desarrollo y se espera que en un futuro próximo.
- TAH soporte está indicado en pacientes con la fase crónica insuficiencia biventricular severa u otra anormalidad anatómica que no se trata de manera óptima con aisladas del ventrículo izquierdo soporte mecánico. Estos pacientes a menudo presente in extremis con complicaciones relacionadas con su mala perfusión. Generalmente los pacientes se clasifican como INTERMACS (Registro Interinstitucional de asistencia mecánica circulatoria Soporte) Perfil 1 (shock cardiogénico crítico) o 2 (disminución progresiva de soporte inotrópico).
- Los pacientes con patología cardiaca significativa concomitante. Pacientes críticamente enfermos con insuficiencia cardiaca en etapa terminal que requieren Suppo mecánicaRT no se puede tratar de manera óptima mediante la adición de otros procedimientos de reparación extensas. Esto puede aumentar el riesgo para la implantación posterior fracaso LVAD del ventrículo derecho, lo que aumenta el riesgo de morbilidad y mortalidad perioperatoria. Esto incluye: infarto agudo de miocardio con defecto septal ventricular; aneurisma de la raíz aórtica / disección, insuficiencia cardiaca aloinjerto, trombo ventricular masiva, arritmias malignas refractarios (independientes de las presiones de llenado), la miocardiopatía hipertrófica / restrictiva y cardiopatías congénitas complejas.
3. Preparación del dispositivo
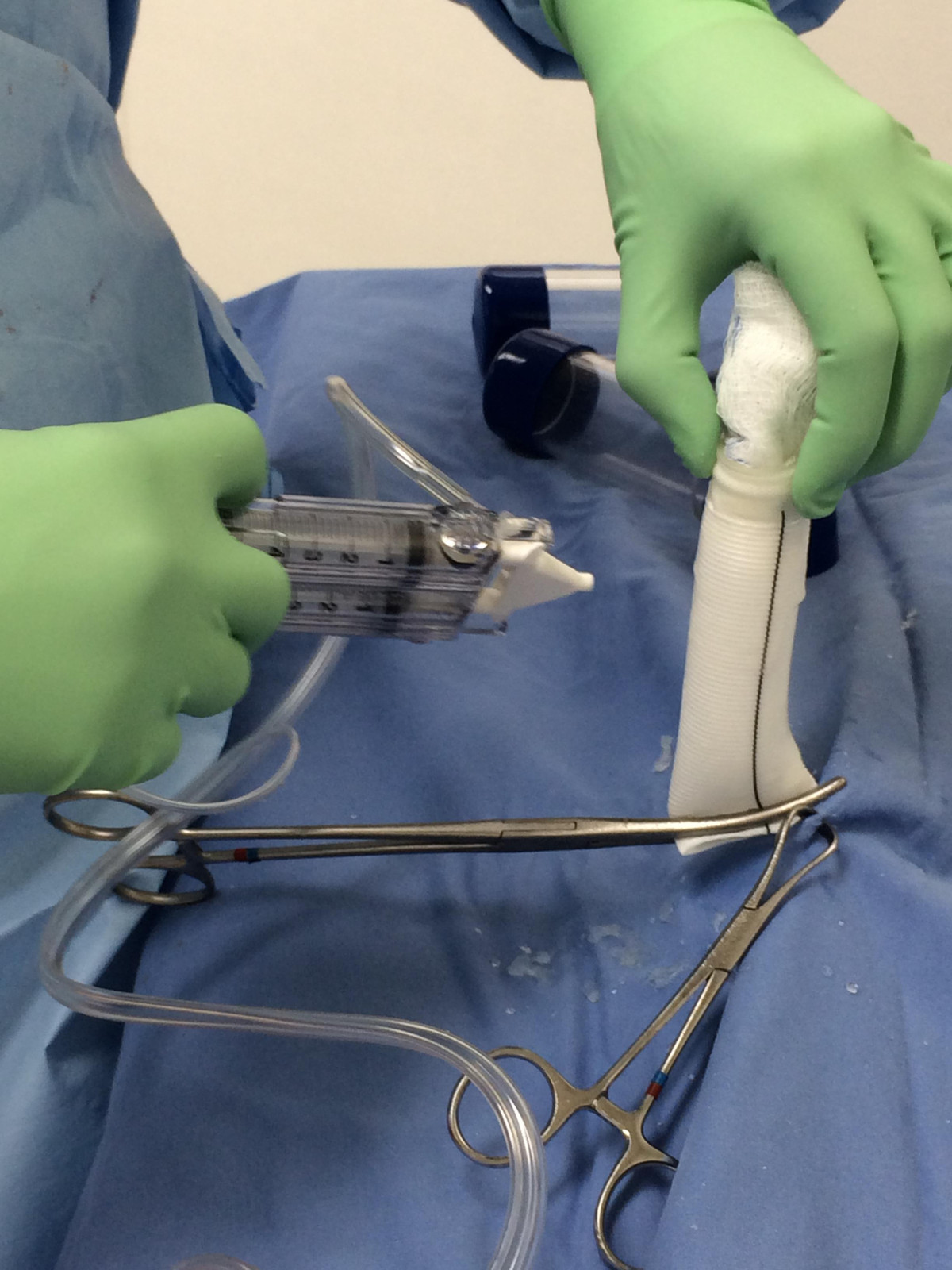
- El aórtica de Dacron y los injertos pulmonares están sellados con sellador quirúrgico CoSeal (Figura 3).
- Los injertos y los dispositivos se sumergen en la rifampicina.
4. Implantación
- Preparación de rutina y esternotomía media. El pecho y el abdomen son prepped a la manera de rutina para la cirugía cardiaca y una sternot medianamía se lleva a cabo.
- División del diafragma izquierdo y la creación de un bolsillo preperitoneal superior izquierda del abdomen. De manera similar a la del implante de un LVAD, el diafragma izquierda se divide medialmente y se crea un bolsillo preperitoneal abdominal superior izquierda de las líneas de conducción neumática. Dos incisiones ~ 5-10 cm por debajo del reborde costal izquierdo se hacen y se llevan a través de la fascia del recto. Túneles intramusculares para las transmisiones neumáticas son creados y mantenidos con dos drenajes de Penrose 1 ".
- La canulación y el inicio de la circulación extracorpórea. La aorta, SVC y IVC se canulan. Canulación bicava se realiza a través de las aurículas (vs canulación directa de la SVC / IVC) para preservar los sitios para su uso durante el posterior trasplante. Disección innecesaria dentro del pericardio se reduce al mínimo para conservar los planos tisulares.
- La aorta es sujetada cruz. La raíz de la aorta y la arteria pulmonar se dividen en el nivel de las comisuras valvulares. La escisión del ventrículo derecho escomenzó a lo largo del margen agudo, de 1-2 cm distal a y paralela a la ranura auriculoventricular derecha. El tabique interventricular se realiza una incisión de abrir el ventrículo izquierdo. La incisión del ventrículo derecho se continúa superiormente en el tracto de salida del VD. Del mismo modo, la incisión ventrículo izquierdo se extiende lateralmente paralela a la ranura auriculoventricular izquierdo. El tracto de salida del VI se abre lateralmente. El tabique interventricular restante se divide y la muestra se retira (Figura 4).
- El seno coronario se cose. Si se identifica un FOP se cose de manera similar. El apéndice de la aurícula izquierda se ligó con una grapadora endoscópica no de corte para eliminar una fuente potencial de trombo (Figuras 5 y 6).
- Las valvas de la válvula mitral y tricúspide se cortan dejando un manguito de varios milímetros al anillo. Los puños ventriculares se recortan dejando un borde de 1 cm de tejido. Los puños son luego cose con Prolene 2-0 (MH) para la hemostasiaSIS y para reducir el tamaño del orificio para el tamaño de las conexiones rápidas auriculares TAH. Algunos centros optan por usar una tira de refuerzo de fieltro.
- Los puños de las conexiones rápidas auriculares TAH se recortan a 0,5 a 1 cm. Los puños se invierte entonces y se cosen a sus respectivas esposas ventriculares izquierdo y derecho.
- En una manera similar, el injerto de la arteria conexiones rápidas aórtica y pulmonar se recortan. El injerto pulmonar se deja varios centímetros más largo que el injerto aórtico para dejar espacio para el injerto aórtico para pasar a continuación. Los injertos se cosen a sus respectivos orificios (Figura 7).
- En el momento de la posterior re-entrada para el trasplante, una intensa respuesta inflamatoria del pericardio se ve a menudo. La disección a través de este tejido en el momento del trasplante puede estar asociada con la pérdida de sangre significativa. Esto parece ser mayor que lo que se ve típicamente durante la esternotomía rehacer. Membrana pericárdica excluye se utiliza para alinear el pericardio y mantenerplanos de tejido avascular. Esta se inicia a lo largo del pericardio inferolateral izquierdo como el acceso a este espacio se vea afectada una vez que el dispositivo está en su lugar. Tiras de excluye también se colocan alrededor de la anastomosis aórtica y pulmonar. Algunos centros utilizan torniquetes de goma esterilizados para envolver las anastomosis.
- Las transmisiones son pasados a través de los túneles creados previamente. Un 13-15 mm dilatador Hegar se utiliza para guiar la línea de transmisión a través del drenaje de Penrose colocado previamente. Una hoja de membrana se oponen a se envuelve alrededor de las líneas de transmisión también. Los conectores metálicos originales de la línea de conducción de la consola externa se reemplazan con conectores de plástico que también se van a conectar con el controlador de descarga portátil.
- De-sintonizadas en los pezones en el TAH izquierda y ventrículos derecho están ligadas. La izquierda y los ventrículos artificiales adecuadas se vacían y luego conectados a sus respectivos orificios. Las conexiones rápidas plegables son atrapados por 2 conductores de agujas pesados y estirados por encima del plástico duro connectors de los ventrículos artificiales, lo que garantiza una conexión estanca (Figura 8).
- Un respiradero de la raíz aórtica se coloca. Baja tasa, se inicia el bombeo de baja presión (presión de accionamiento izquierdo 40, la presión del volante a la derecha 0,% sístole 40, la tasa de 40, de vacío 0) y los pulmones son ventilados para desaireación. El flujo a través del lado derecho es un principio pasivo.
- Se retira la abrazadera cruzada. Una vez adecuada de desaireado es confirmada por ETE, la circulación extracorpórea se puede suspender de forma relativamente rápida. Se incrementa TAH apoyo. Parámetros TAH inmediatas iniciales típicos son: la presión de accionamiento Izquierda 180-200 mmHg, presión volante a la derecha 30-60 mmHg, HR 100-120 latidos por minuto, y 50% la sístole de vacío se deja generalmente a 0 hasta que el pecho se cierra (o se sella) a. evitar el arrastre de aire. Una vez sellados, los aumentos en el vacío (en general, a 15 mm de Hg) se traducirá en un aumento de volumen de llenado y aumento del gasto cardíaco. Los parámetros se ajustaron a continuación para el llenado ventricular parcial y la expulsión completa.
- Protamine se da y se quitan las cánulas CPB. Los pacientes que requieren un TAH menudo se presentan con disfunción del órgano afectado significativa incluyendo congestión hepática crónica y pueden tener la coagulopatía subyacente asociada significativa. La complicación más común después de la implantación TAH está sangrando. Se recomienda un umbral bajo para el embalaje del mediastino y el cierre esternal retrasado.
- Una vez que el pecho está listo para ser cerrado, el resto del pericardio a lo largo de la derecha y superiormente se alinea con Impedir. La configuración de la TAH no mantiene la forma oblonga normal. La contracción del pericardio sobre el dispositivo será limitar el espacio disponible para posterior trasplante. Un implante mamario de solución salina se utiliza para mantener el espacio pericárdico apical para su posterior trasplante. Un implante mamario de solución salina suave se coloca en el vértice y se llena con 200-250 ml de solución salina (Figura 9).
- El pecho se cierra de la manera habitual. Aunque imgagin por intraoperatoria TEE es limitada, sigue siendo una herramienta útil al final de la cirugía para evaluar para la compresión de la derecha y el retorno venoso de la aurícula izquierda por el dispositivo durante el cierre. Esto es más común a la derecha (tanto la cava y las venas pulmonares del lado derecho) y en general se puede tratar con el desplazamiento del dispositivo hacia abajo y hacia la izquierda. Esto puede ser efectuada con una sutura fuerte colocado alrededor del reborde costal y se ata al ventrículo artificial derecho. Una banda de silastic se deja debajo del esternón para proteger la bomba durante el reingreso para el trasplante.
Resultados
Entre abril de 2006 y julio de 2012, 66 pacientes fueron implantados con un TAH en Virginia Commonwealth University Medical Center. Los pacientes estaban en estado crítico: 18% llegó en otro soporte mecánico (ECMO, LVAD o BIVAD), el 58% era en un balón de contrapulsación intra-aórtica, el 58% llegó en medicamentos inotrópicos, el 17% fueron ventilados mecánicamente, y el 17% llegó en hemodiálisis. Los pacientes fueron apoyados por un total de 7.863 días. La mediana de duración de la asistencia fue de 87,5 días (rango 1-602 días). 10 pacientes fueron dados de alta en un controlador de descarga portátil (como parte de un ensayo clínico, no aprobado por la FDA). 50 (76%) pacientes fueron puenteados con éxito para el trasplante, 7 (11%) se mantuvo en el dispositivo espera de trasplante, y 9 (14%) murieron, mientras que en el dispositivo (Figura 10). 3 de las muertes ocurrieron en la semana 1 de continuación de la implantación y estaban relacionados con la insuficiencia orgánica multisistémica progresiva. Las otras 6 muertes ocurrieron 32-169 días después del implante (3 sEPSIS / MSOF, 1 hemorragia mediastinal, 1 hemorragia intracraneal y 1 crisis hipertensiva). El efecto adverso más frecuente perioperatoria sangraba requiriendo mediastinal re-exploración en el 30%.
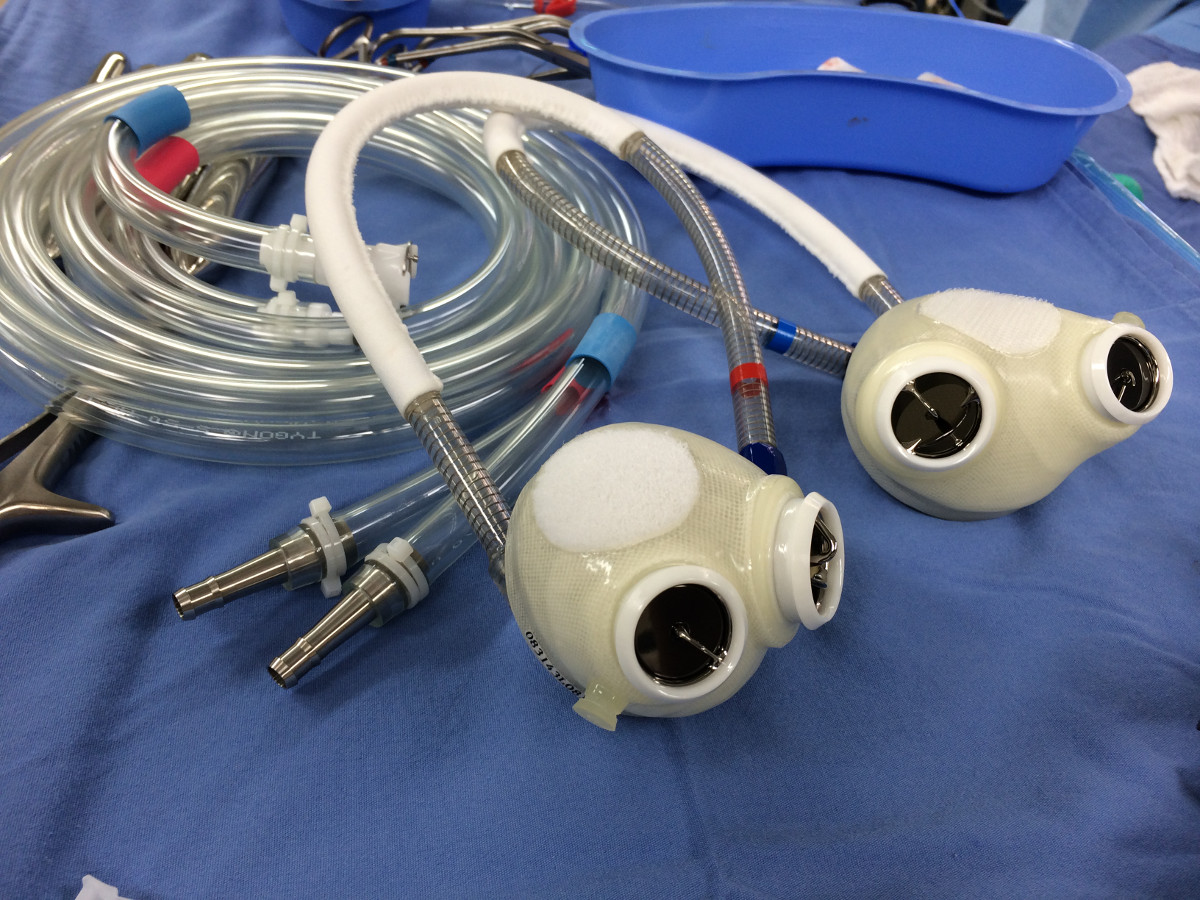
Figura 1. El corazón artificial SynCardia total.
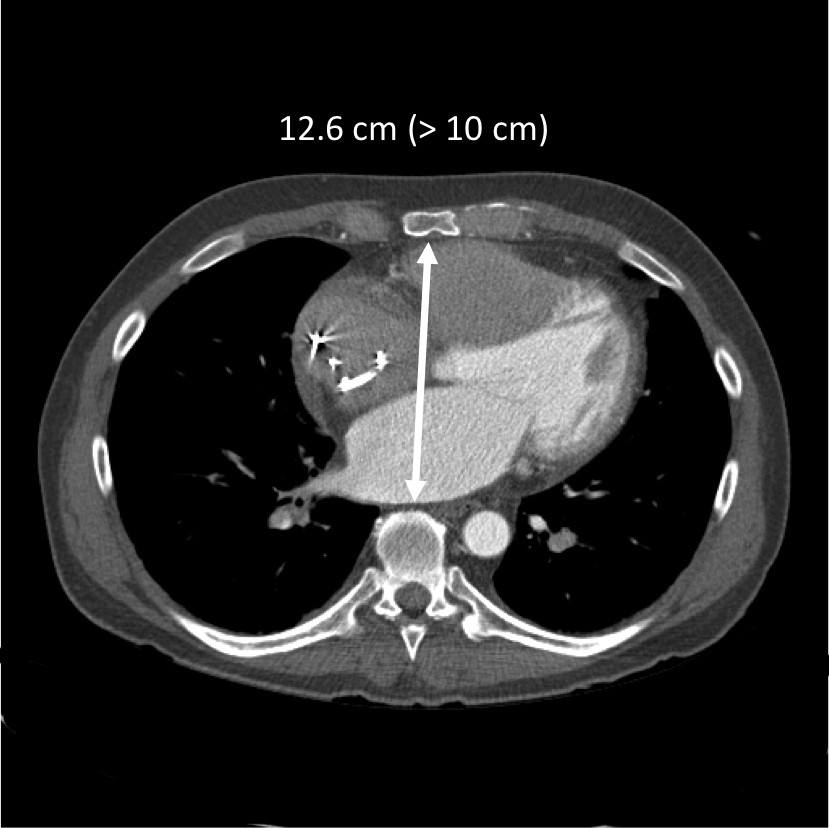
Figura 2. Medir la dimensión AP por CT. Un espacio> 10 cm entre el esternón y el borde anterior del cuerpo vertebral 10 ª se requiere generalmente para el dispositivo a la medida.
 />
/>
Figura 3. El pretratamiento de los injertos arteriales de flujo de salida. Los injertos de arteria aórtica y pulmonar están previamente sellados con sellador quirúrgico Coseal, un hidrogel sintético usado como un sellador adyuvante para injertos vasculares. Anteriormente los injertos fueron preclotted con la propia sangre del paciente antes de la heparinización.
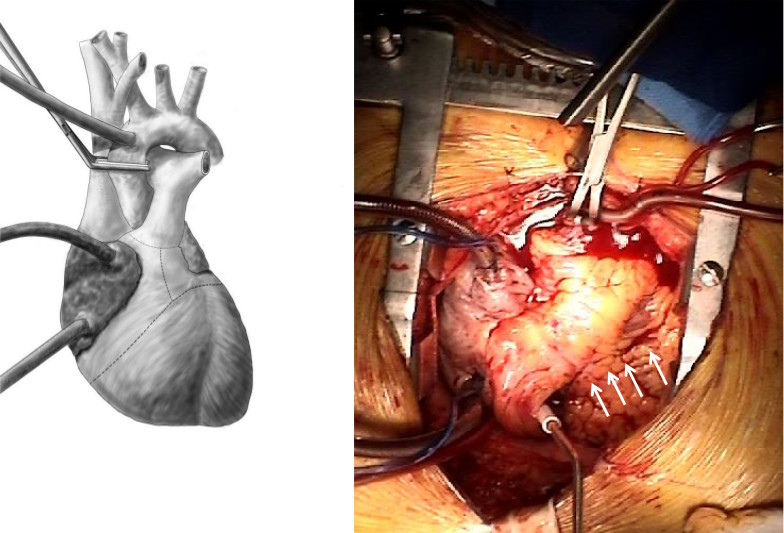
Figura 4. Escisión de la derecha y el ventrículo izquierdo. El VD y VI se cortan dejando un manguito ventricular 1 cm más allá de las válvulas mitral y tricúspide. Las flechas apuntan a la incisión a lo largo de la pared anterior de la RV. Las incisiones se extienden a través de los tractos de salida ventricular izquierdo y derecho y por medio de las válvulas aórtica y pulmonar.
oad/50377/50377fig5highres.jpg "width =" 500 "/>
Figura 5. Oversewing el seno coronario. El seno coronario (flecha) se cose a través del manguito de RV (los folletos tricúspide han sido extirpados) para la hemostasia.
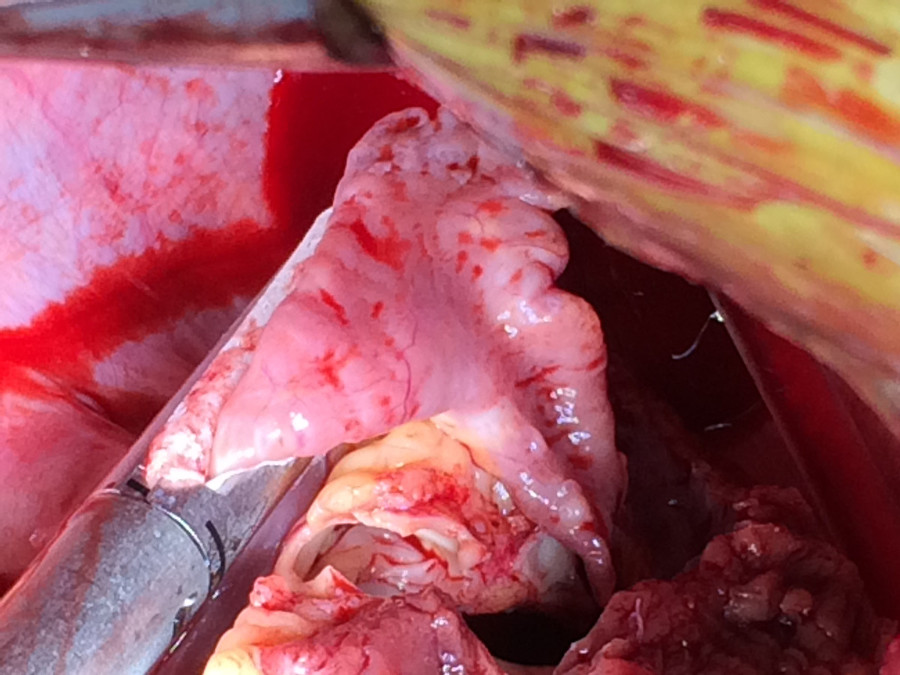
Figura 6. Ligadura apéndice auricular. El apéndice de la aurícula izquierda se ligó con una grapadora GIA endo reforzado con Seamguard para minimizar una fuente potencial de embolia sistémica.
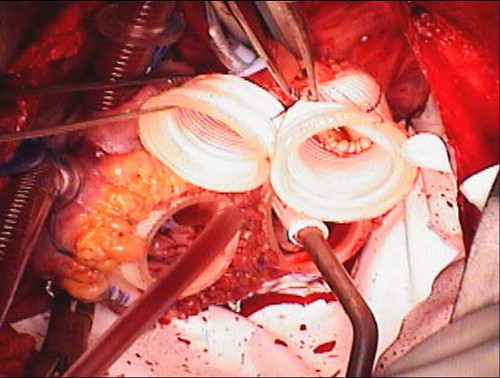
Figura 7. Conexiones rápidas y excluye Goretex implantado. Las conexiones rápidas auriculares y los injertos vasculares están cosidas a sus respectivos orificios. El pericardio se alinea con membrana Goretex para facilitar la posterior reingreso para el trasplante.
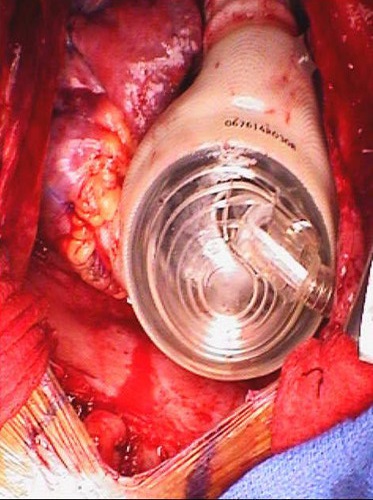
Figura 8. Dispositivo implantado. El dispositivo implantado justo antes de cierre de pecho.
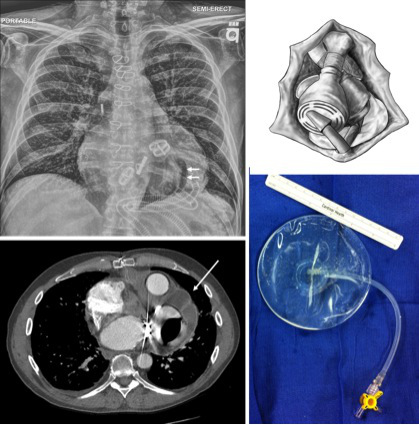
La Figura 9. Pericárdico implante de solución salina apical como se demuestra en las imágenes de TC y radiografía de tórax. Un implante de solución salina (flechas simples) se utiliza para mantener el espacio apical pericárdico para el trasplante. En la radiografía de tórax, el borde de la TAH (donde el pericardio de otro modo contrato) está delineada por la burbuja de aire central (flechas dobles).
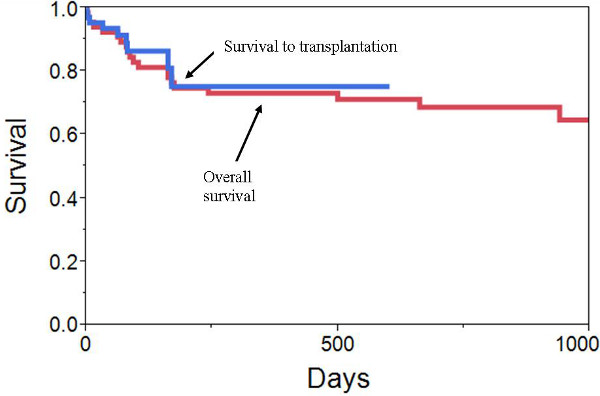
Figura 10 curvas. VCU resultados. Supervivencia de Kaplan-Meier demostrando sursupervivencia al trasplante y la supervivencia global después del implante TAH.
Discusión
Reemplazo artificial del corazón humano ha capturado la imaginación del público. Las primeras experiencias con el corazón artificial total se caracterizó por resultados subóptimos 1-3. El diseño y las técnicas de implantación de la TAH utiliza hoy en día no han cambiado significativamente desde que el Dr. DeVries 'Descripción original 6. Sin embargo, las mejoras en la selección de pacientes (como un puente al trasplante) y la comprensión de manejo perioperatorio han dado lugar a una mejora significativa en los resultados. En 2004, se publicó un estudio de referencia de 81 implantes TAH. El juicio estableció la eficacia de la TAH como puente al trasplante y la llevó a la aprobación de la FDA de la SynCardia TAH. En este estudio no aleatorizado, 79% era un puente con éxito para el trasplante. La supervivencia global a 1 año fue del 70%. En una cohorte emparejado de 35 pacientes que cumplían los criterios del estudio, pero no se sometieron a la implantación TAH, 46% sobrevivieron al trasplante y la supervivencia a 1 año fue del 31% 7.
La selección del paciente es fundamental para el buen resultado 8,9. Es importante identificar a los pacientes que aún no han desarrollado insuficiencia orgánica irreversible final u otras complicaciones que limitaría sus posibilidades de reanimación o candidatura trasplante. En nuestra institución, los resultados de la cirrosis por biopsia hepática, la dependencia de la diálisis crónica, u otros factores psicosociales que impedirían candidatura trasplante también impedirían candidatura para un TAH. Por el contrario, los pacientes con descompensación aguda u otras pruebas para una posible recuperación del órgano blanco se consideran.Es igualmente importante identificar a los pacientes con insuficiencia biventricular cuyo derecho ventricular (RV) La disfunción mejorará con aisladas LV descarga y por lo tanto no necesitan soporte circulatorio biventricular. Insuficiencia del VD después de la implantación del DAVI se asocia con una mayor morbilidad y mortalidad 10. El uso temprano de asistencia biventricular en comparación con el retraso del rescatepor la insuficiencia del VD tras LVAD también se asocia con mejores resultados 11. Un número de factores de riesgo para la insuficiencia del VD han sido identificados y varios sistemas de puntuación de riesgo se han desarrollado. La necesidad de inotrópicos / apoyo con balón intra-aórtica, la evidencia de disfunción renal y hepática (elevación de creatinina, aspartato aminotransferasa, bilirrubina), la evidencia hemodinámica de la disfunción del VD (disminución de la RV índice de trabajo sistólico, aumento de la aurícula derecha / presiones de cuña) y ecocardiográfica evidencia de disfunción ventricular derecha (dilatación del VD, disminución de la fracción de eyección del VD / motion anular tricúspide, aumentó insuficiencia tricúspide) han sido identificados como factores de riesgo 12-15. No obstante, la determinación del riesgo de insuficiencia del VD después de la colocación LVAD sigue siendo difícil. Una reciente serie pequeña no mostró valor predictivo de varios de los sistemas de puntuación para predecir la necesidad de apoyo RV 16.
Momento de la cirugía es una importante consición. Una vez que la decisión ha sido tomada de que el soporte mecánico biventricular es necesario, la implantación temprana ofrece la forma más eficaz para restablecer el flujo sanguíneo y resucitar a un paciente. Sin embargo, los pacientes pueden presentar abruptamente con profunda conmoción aguda cardiogénico, mala perfusión graves, y la evaluación previa mínima. El uso liberal de opciones de apoyo temporales (tales como ECMO / BIA) durante 24-48 horas se puede comenzar el proceso de reanimación mientras que las cuestiones relativas a la situación neurológica u otras cuestiones de la candidatura de trasplante ha sido respondido. El uso prolongado de soporte inotrópico alta dosis puede aumentar el riesgo de insuficiencia orgánica irreversible final u otras complicaciones.
Las técnicas generales de la implantación no han cambiado dramáticamente desde que el dispositivo fue introducido por primera vez 6,17. Sin embargo, los beneficios de tomar el tiempo para proteger y mantener el espacio pericárdico hay que destacar 18. El dispositivo parece incitar a una intensa inflamación de espesormiento del pericardio. Forro el pericardio con Goretex y mantener el espacio apical con un implante de solución salina facilita en gran medida la re-entrada para el trasplante. Sangrado perioperatorio sigue siendo la complicación perioperatoria más frecuente. Embalaje del pecho con cierre esternal retardada es una estrategia eficaz para limitar la cantidad de productos de la sangre perioperatorias necesarias para revertir la coagulopatía subyacente y reducir al mínimo el riesgo de taponamiento. A pesar de la carcasa relativamente rígida de los ventrículos artificiales es posible que el líquido suficiente para acumular mediastínica o dificultan flujo venoso causando el taponamiento. Ecocardiografía de superficie después de la implantación TAH tiene una utilidad limitada. Las imágenes por TAC si a menudo limitada por la disfunción renal subyacente y la necesidad de evitar el contraste IV. Se recomienda volver a las primeras exploraciones del mediastino en cualquier paciente TAH que está haciendo lo contrario mal por razones desconocidas.
Tras la implantación, el dispositivo se ajusta para maximizar el gasto cardíaco.Es capaz de generar una salida de LPM> 9. Para reducir al mínimo la inmovilización, los parámetros del dispositivo se ajustan para "llenado parcial y expulsión completa." Parámetros TAH postoperatorias precoces típicos son: la presión de accionamiento Izquierda 180-200 mmHg, presión volante a la derecha 30-60 mmHg, HR 100-120 latidos por minuto, 50% sístole, y el vacío a 15 mmHg. En los pacientes con hipertensión pulmonar de larga data, las presiones de accionamiento RV más altas requeridas para la expulsión unilateral completa derecha pueden ser perjudiciales. Es posible "sobremarcha" la salida del lado derecho. En 2 pacientes, esto dio lugar a un edema pulmonar profunda que requiere un apoyo ECMO veno-venosa temporal. Un paciente presentó insuficiencia orgánica multisistémica progresiva y expiró. El otro fue apoyado hasta que el edema disminuyó y fue destetado con éxito fuera de ECMO.
La anticoagulación se inicia generalmente 24 horas después del cierre de pecho. Los pacientes se les empiezan a bivalirudina (0,005 mg / kg / h), aspirina (81 mg diarios) y el dipiridamol (50 mg tres veces al día). Fuera de la ophabitación erating, la heparina se evita para minimizar el riesgo de trombocitopenia inducida por heparina. Bivalirudin generalmente no se valora y una vez estable transición a warfarina oral. Objetivos de la terapia son un 2-3 INR y la función plaquetaria 20-40% normal agregometría óptica. Los pacientes con evidencia de aumento de la hemólisis (LDH> 1000) pueden beneficiarse de la adición de pentoxifilina (400 mg TID) 19,20.
La insuficiencia renal en pacientes con enfermedad aguda es claramente multifactorial. Sin embargo, hemos notado una tendencia desproporcionada hacia la insuficiencia renal después de la implantación TAH. Nuestra hipótesis es que esto está en parte relacionado con la disminución brusca de la producción del péptido natriurético nativa asociada con escisión ventricular. Suplementación perioperatoria con una infusión nesiritida baja dosis (0,005 mcg / kg / min) parece reducir la incidencia de la insuficiencia renal 21. Por otra parte, la infusión de nesiritide tiene un efecto profundo en el aumento de la diuresis después de impl TAHantation 22. Una vez que los pacientes han recuperado hemos sido capaces de interrumpir la infusión en la mayoría de los pacientes. Sin embargo, hemos tenido algunos pacientes que no pudieron ser destetados de la infusión hasta que fueron trasplantadas.
Pacientes TAH menudo demuestran anemia crónica severa. Las causas incluyen la hemólisis de bajo grado y erthryopoesis ineficaz. A pesar de la anemia, los pacientes TAH demuestran una buena tolerancia de esfuerzo y síntomas mínimos, incluso con concentraciones de hemoglobina de 5-6 g / dl. Con el fin de evitar la sensibilización de HLA y otras complicaciones asociadas, las transfusiones se evitan menos que el paciente es sintomático o hay otros lados de mala perfusión del órgano de extremo 23.
Más allá del período postoperatorio temprano, la atención se centra en la rehabilitación física agresiva. A pesar de la presentación grave, la mayoría de los pacientes fueron capaces de iniciar la terapia física en la primera semana postoperatoria y la mayoría eran capaces de empezar treadmiejercicio ll en la segunda semana. Sin embargo, hemos encontrado que los pacientes TAH demuestran un embotamiento anormal de la respuesta de la presión arterial para hacer ejercicio. Esto es en parte relacionado con el uso de vasodilatadores para limitar la poscarga 24. Si bien esto podría limitar la cantidad de recuperación física, la mayoría de los pacientes van a trasplante antes de que esto se alcanza.
Hasta hace poco, los pacientes del hospital TAH fueron atados y atados a una consola de 418 libras. Como los tiempos de espera para órganos de donantes siguen aumentando, esto fue acompañado por la reducción de manera significativa la calidad de vida, así como el aumento de los costes financieros. La introducción de un dispositivo que permita la descarga portátil para el hogar e incluso el regreso al trabajo ha sido un gran avance en la utilidad práctica de la TAH. El conductor SynCardia Libertad (bajo ensayo clínico y no aprobado por la FDA) es un 14 libras, conductor de tamaño mochila con un pistón neumático accionado eléctricamente 25. Las primeras experiencias con el conductor ha demostrado que es sensitive a poscarga condiciones y que un régimen de medicamentos anti hipertensiva agresivo es necesario 26.
En resumen, los resultados actuales han establecido la TAH como un dispositivo eficaz para la reanimación y el puente posterior al trasplante. Esta cohorte de pacientes representa un extremo del espectro de pacientes con insuficiencia cardíaca en fase terminal. A menudo no hay otra opción terapéutica duradero adecuado.
Divulgaciones
La producción de este video-artículo fue patrocinado por SynCardia. MH y VK han servido como consultores para SynCardia Systems Inc. Los otros autores no tienen nada que revelar.
Materiales
| Name | Company | Catalog Number | Comments |
| Total artificial heart (implant kit) |  Syncardia Syncardia | 500101 | |
| PRECLUDE pericardial membrane |  Gore Medical Gore Medical | 1PCM101 | |
| Smooth Round Saline Implant |  Mentor Mentor | 350-1645 | |
| CoSeal Surgical Sealant |  Baxter Baxter | 93407 |
Referencias
- Cooley, D. A., Liotta, D., Hallman, G. L., Bloodwell, R. D., Leachman, R. D., Milam, J. D. Orthotopic cardiac prosthesis for two-staged cardiac replacement. American Journal of Cardiology. 24 (5), 723-730 (1969).
- Cooley, D. A. The total artificial heart. Nat. Med. 9 (1), 108-111 (2003).
- DeVries, W. C., Anderson, J. L., Joyce, L. D., Anderson, F. L., Hammond, E. H., Jarvik, R. K., Kolff, W. J. . Clinical use of the total artificial. 310 (5), 273-278 (1984).
- . Syncardia Systems. 1000th Implant of the World's Only Approved Total Artificial Heart Performed. [Press release]. , (2012).
- Joyce, L. D., et al. Nine year experience with the clinical use of total artificial hearts as cardiac support devices. ASAIO Transactions. 34, 703-707 (1988).
- DeVries, W. C. Surgical Technique for Implantation of the Jarvik-7-100. Total Artificial Heart. JAMA. 259 (6), 875-880 (1988).
- Copeland, J. G., et al. Cardiac replacement with a total artificial heart as a bridge to transplantation. N. Engl. J. Med. 351, 859-867 (2004).
- Kasirajan, V., Tang, D. G., Katlaps, G. J., Shah, K. B. The total artificial heart for biventricular failure and beyond. Curr Opin Cardiol. 27, (2012).
- Copeland, J. G., et al. Risk factor analysis for bridge to transplantation with the CardioWest total artificial heart. Ann Thorac Surg. 85, 1639-1644 (2008).
- Kormos, R. L., et al. Right ventricular failure in patients with the HeartMate II continuous-flow left ventricular assist device: incidence, risk factors, and effect on outcomes. J Thorac Cardiovasc Surg. 139, 1316-1324 (2010).
- Fitzpatrick, J. R., et al. Early planned institution of biventricular mechanical circulatory support results in improved outcomes compared with delayed conversion of a left ventricular assist device to a biventricular assist device. J Thorac Cardiovasc Surg. 137, 971-977 (2009).
- Matthews, J. C., Koelling, T. M., Pagani, F. D., Aaronson, K. D. The right ventricular failure risk score a pre-operative tool for assessing the risk of right ventricular failure in left ventricular assist device candidates. J Am Coll Cardiol. 51, 2163-2172 (2008).
- Ochiai, Y., et al. Predictors of Severe Right Ventricular Failure After Implantable Left Ventricular Assist Device Insertion: Analysis of 245 Patients. Circulation. 106 (suppl I), (2002).
- Drakos, S. G., et al. Risk factors predictive of right ventricular failure after left ventricular assist device implantation. Am J Cardiol. 105, 1030-1035 (2010).
- Fitzpatrick, J. R., et al. Risk score derived from pre-operative data analysis predicts the need for biventricular mechanical circulatory support. J Heart Lung Transplant. 27, 1286-1292 (2008).
- Pettinari, M., et al. Are right ventricular risk scores useful. Eur J Cardiothorac Surg. 42 (4), 1-6 (2012).
- Arabia, F. A., Copeland, J. G., Pavie, A., Smith, R. G. Implantation Technique for the CardioWest Total Artificial Heart. Ann Thorac Surg. 68, 698-704 (1999).
- Copeland, J. G., Arabia, F. A., Smith, R. G., Covington, D. Synthetic membrane neopericardium facilitates total artificial heart explantation. J Heart Lung Transplant. 20, 654-656 (2001).
- Crouch, M. A., et al. Successful use and dosing of bivalirudin after temporary total artificial heart implantation: a case series. Pharmacotherapy. 28, 1413-1420 (2008).
- Ensor, C. R., et al. Antithrombotic therapy for the CardioWest temporary total artificial heart. Tex Heart Inst J. 37, 149-158 (2010).
- Stribling, W. K., et al. Use of nesiritide and renal function following total artificial heart implantation. J Heart Lung Transplant. 30, 96 (2011).
- Shah, K. B., et al. Impact of low dose B-type natriuretic peptide infusion on urine output after total artificial heart implantation. J Heart Lung Transplant. 31 (6), 670-672 (2012).
- Mankad, A. K., et al. Persistent anemia in patients supported with the total artificial heart: hemolysis and ineffective erythropoiesis. J Card Fail. 17, 42-42 (2011).
- Kohli, H. S., et al. Exercise blood pressure response during assisted circulatory support: comparison of the total artificial heart with a leftventricular assist device during rehabilitation. J Heart Lung Transplant. 30, 1207-1213 (2011).
- Jaroszewski, D. E., Anderson, E. M., Pierce, C. N., Arabia, F. A. The SynCardia freedom driver: a portable driver for discharge home with the total artificial heart. J Heart Lung Transplant. 30, 844-845 (2011).
- Yankah, L., Shah, K. B., Hess, M. L., Kasirajan, V., Tang, D. G. Response of the Syncardia TAH Pneumatic Drivers to Afterload Challenge on a Mock Loop. ASAIO Journal. 58 (7), (2012).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados