Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Protocolo para la medición de las propiedades térmicas de un hidrato muestra sintética de arena-agua-gas metano a sobrefusión
En este artículo
Resumen
We present a protocol for measuring the thermal properties of synthetic hydrate-bearing sediment samples comprising sand, water, methane, and methane hydrate.
Resumen
Methane hydrates (MHs) are present in large amounts in the ocean floor and permafrost regions. Methane and hydrogen hydrates are being studied as future energy resources and energy storage media. To develop a method for gas production from natural MH-bearing sediments and hydrate-based technologies, it is imperative to understand the thermal properties of gas hydrates.
The thermal properties' measurements of samples comprising sand, water, methane, and MH are difficult because the melting heat of MH may affect the measurements. To solve this problem, we performed thermal properties' measurements at supercooled conditions during MH formation. The measurement protocol, calculation method of the saturation change, and tips for thermal constants' analysis of the sample using transient plane source techniques are described here.
The effect of the formation heat of MH on measurement is very small because the gas hydrate formation rate is very slow. This measurement method can be applied to the thermal properties of the gas hydrate-water-guest gas system, which contains hydrogen, CO2, and ozone hydrates, because the characteristic low formation rate of gas hydrate is not unique to MH. The key point of this method is the low rate of phase transition of the target material. Hence, this method may be applied to other materials having low phase-transition rates.
Introducción
Los hidratos de gas son compuestos cristalinos que comprenden estructuras de jaula de moléculas de agua con enlaces de hidrógeno que contienen moléculas huésped en la jaula 1. Grandes cantidades de hidratos de metano (MHS) en las regiones de permafrost y suelo marino son los recursos energéticos futuros interesantes, pero pueden afectar a las condiciones del clima mundial 2.
En marzo de 2013, el Japan Oil, Gas y Metales de la Corporación Nacional llevaron a cabo la primera prueba de producción en alta mar del mundo para extraer gas de los sedimentos naturales que devengan MH en el este de Nankai Trough utilizando el "método de despresurización" 3,4.
Los hidratos de gas pueden almacenar gases como el metano 1, hidrógeno 5, CO 2 1,6, y el ozono 7. Por lo tanto, los hidratos de metano e hidrógeno se estudian como potencial de almacenamiento de energía y medios de transporte. Para reducir las emisiones de CO2 a la atmósfera, CO 2 sequestración utilizando CO 2 hidratos en los sedimentos de las profundidades oceánicas se han estudiado 6. El ozono se utiliza actualmente en la purificación del agua y la esterilización de los alimentos. Estudios de la tecnología de preservación de ozono han llevado a cabo, ya que es químicamente inestable 7. La concentración de ozono en hidratos es mucho mayor que en agua ozonizada o hielo 7.
Para desarrollar la producción de gas a partir de sedimentos que devengan MH naturales y las tecnologías basadas en hidratos, es imprescindible para entender las propiedades térmicas de los hidratos de gas. Sin embargo, los datos de propiedades térmicas y estudios de modelos de sedimentos de hidratos de gas que soportan son escasos 8.
El "método de despresurización" se puede utilizar para disociar MH en el espacio de los poros de sedimentos por la disminución de la presión de poro por debajo de la estabilidad de los hidratos. En este proceso, los componentes espaciales de sedimentos de poro cambian de agua y de MH a agua, MH, y el gas. medición de las propiedades térmicas 'de esta última condición es difícil ya que el calor de fusión de MH puede afectar a las mediciones. Para resolver este problema, Muraoka et al. Cabo la medición de las propiedades térmicas 'en condiciones super-enfriadas durante la formación MH 9.
Con este protocolo de vídeo, se explica el método de medición de la muestra de arena-agua-gas-MH-enfriada sintética.
La Figura 1 muestra la configuración experimental para medir las propiedades térmicas del metano artificial sedimento hidrato-cojinete. La configuración es la misma que se muestra en la referencia 9. El sistema comprende principalmente un recipiente de alta presión, presión y control de la temperatura, y las propiedades térmicas del sistema de medición. El recipiente de alta presión se compone de acero inoxidable cilíndrico con un diámetro interno de 140 mm y una altura de 140 mm; su volumen interior con el volumen muerto es eliminado 2.110 cm3, y su límite de presión es de 15 MPa. el transie fuente plana nt técnica (TPS) se utiliza para medir las propiedades térmicas 10. Nueve sondas de TPS con radios individual de 2.001 mm se colocan dentro del recipiente. La disposición de los nueve sondas 9 se muestra en la figura 2 en la referencia 9. Las sondas están conectadas a TPS analizador de las propiedades térmicas 'con un cable y conmutar manualmente durante el experimento. Los detalles del sensor de TPS, diagrama de conexión y configuración de la embarcación se muestran en las figuras S1, 2, y 3 de la información de apoyo en referencia 9.
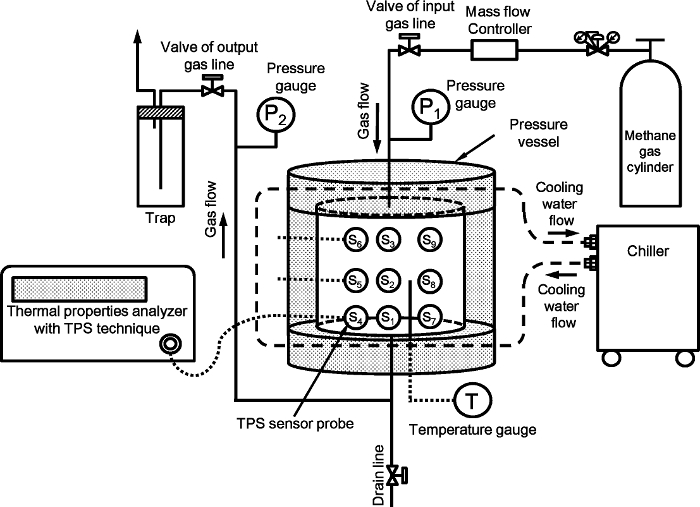
Figura 1:. La configuración experimental para la medición de las propiedades térmicas de los sedimentos de hidrato de metano-cojinete artificial La figura se modificó a partir de la referencia 9.3956fig1large.jpg "target =" _ blank "> Haga clic aquí para ver una versión más grande de esta figura.
El método TPS se utilizó para medir las propiedades térmicas de cada muestra. Los principios del método se describen en la referencia 10. En este método, el aumento de la temperatura en función del tiempo,? T ave, es
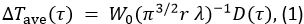
dónde
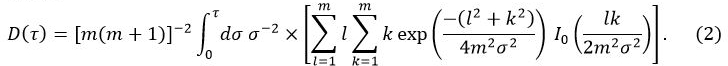
En la Ecuación 1, W 0 es la potencia de salida del sensor, r es el radio de la sonda de sensor, λ es la conductividad térmica de la muestra, α es la difusividad térmica, y t es el tiempo desde el inicio de la fuente de alimentación a la sonda de sensor. D (τ) es un tiempo adimensional función dependiente. τ está dada por (αt / r) 1/2. En la Ecuación 2, m es el número de anillos concéntricos de la sonda TPS y 0 es una función de Bessel modificada. La conductividad térmica, difusividad térmica y calor específico de la muestra se determinan simultáneamente por análisis de inversión aplicado al aumento de la temperatura como se suministra energía a la sonda de sensor.
Access restricted. Please log in or start a trial to view this content.
Protocolo
Nota: Por favor, consulte a todas las hojas de datos de seguridad de materiales relevantes ya que este estudio utiliza gas metano inflamable de alta presión y un recipiente de alta presión grande. Use un casco, gafas de seguridad y botas de seguridad. Si el sistema de control de la temperatura se detiene, la presión en el recipiente aumenta con MH disociación. Para evitar accidentes, el uso de un sistema de válvula de seguridad se recomienda para liberar automáticamente el gas metano a la atmósfera. El sistema de válvula de seguridad puede funcionar sin fuente de alimentación eléctrica.
1. Preparación de las muestras de gases de arena-agua-metano 9
- Coloque el recipiente de alta presión sobre la mesa vibratoria.
- Verter 1,5 L de agua pura en una botella de agua y 4000 g de arena de sílice en una botella de arena. Se pesan exactamente las masas de arena y agua en las botellas de arena y agua, respectivamente.
- Verter 1 L de agua pura en el recipiente de alta presión con un volumen interno de 2.110 cm 3 de una botella de aguahasta que el agua llena la mitad del recipiente interior.
- Encienda la mesa vibratoria a vibrar todo el recipiente. Ajuste la velocidad de la vibración y la fuente de alimentación a 50 Hz y 220 W, respectivamente. Aplicar la vibración hasta la finalización de la etapa 1.5. Eliminar el aire residual en la línea de drenaje y el filtro metálico sinterizado en la parte inferior del recipiente por la vibración de la embarcación.
- Verter 3.300 g de arena de sílice de una botella de arena en el recipiente a una velocidad constante de aproximadamente 1 g seg -1 usando un embudo se mantenía cerca de la superficie del agua mientras que todo el recipiente se hace vibrar para asegurar embalaje uniforme.
- Detener la vibración cuando el agua alcanza el borde de la vasija.
- Colocar un anillo como una pared temporal en el borde de la vasija para evitar que el agua se derrame.
- Vibrar el recipiente de nuevo en 50 Hz y 220 W.
- Cuando la arena alcanza el borde de la vasija (altura 140 mm), desactivar la vibración.
- Retire la pared temporal y el exceso de agua de los poros usando THlínea de drenaje e. Verter la parte de atrás el exceso de agua de los poros en la botella de agua.
- Empacar la arena por la vibración de la embarcación una vez o dos veces a 50 Hz y 300 W durante 1 segundo y añadir más arena si es necesario.
- Pesar las masas de arena y agua en las botellas de arena y agua. Calcular las masas de arena y agua en el recipiente de las diferencias de masa en las botellas de agua y arena. En este experimento, las masas de arena y agua en el buque fueron 3.385 gy 823,6 g, respectivamente. La masa de agua en el recipiente se denota como w total.
- Cubrir el recipiente de alta presión con una tapa de acero inoxidable y apriete los pernos de pares diagonalmente opuestos en secuencia.
- Mueva el recipiente de alta presión de la mesa vibratoria a la mesa destinada para el experimento.
- Cubrir el recipiente de alta presión con el aislador de calor para controlar la temperatura.
- Conectar las tuberías de alta presión y las líneas de flujo del agua de refrigeración en el recipiente de alta presión.
- Abrir las válvulas de las tuberías de entrada y de salida de gases. Ventilar 10 L de metano a una velocidad de 800 ml min -1 hasta que no haya exceso de descargas de agua en la trampa a la presión atmosférica. La descarga de la arena es impedido por un filtro metálico sinterizado fija en el fondo del recipiente. El agua residual permanece en la superficie de la arena debido a que la arena de sílice hidrófila adsorbe las moléculas de agua.
- Pesar la masa de agua en la trampa, w trampa, para determinar el volumen de gas en el recipiente. Determinar la masa de agua residual, res w, en el recipiente usando la ecuación w = w total de res - w trampa. En este caso, res w y w trampa fue 360,6 g y 463,0 g, respectivamente.
- Determinar la porosidad de la muestra utilizando la fórmula Ѱ = 1 - V de células de arena / V, donde la arena V es el volumen de tél arena determinado por la relación de masa de arena a la densidad de la arena (es decir, ρ s = 2630 kg m -3), y de células V es el volumen interior del recipiente. El Ѱ porosidad de la muestra fue de 0,39.
- Cierre la válvula de la tubería de gas de salida. Inyectar metano para aumentar la presión de poro de metano en el recipiente a aproximadamente 12,1 MPa a temperatura ambiente (es decir, 31,6 ° C).
- Cierre la válvula de la tubería de gas de entrada.
- Iniciar la grabación de la presión y la temperatura en el recipiente durante el experimento utilizando el registrador de datos. El intervalo de muestreo de datos es 5 seg. El tiempo de experimentación total es de aproximadamente 3,000 min.
2. Síntesis MH y medición de la muestra a sobrefusión 9 Propiedades Térmicas '
- Encender el refrigerador para enfriar el recipiente de temperatura ambiente a 2,0 ° C por circulación del líquido refrigerante. Permitir la circulación del refrigerante del enfriador to el fondo del recipiente, de allí a la tapa del recipiente, y finalmente de vuelta a la enfriadora. La velocidad de cambio de temperatura en el recipiente era de aproximadamente 0.001 ° C sec -1.
- Establecer los parámetros de medición utilizando el software analizador de TPS. Establecer el tipo de sensor a otro diseño # 7577. Ajustar la potencia de salida W 0 a 30 mW y el tiempo de medición de 5 seg. Tenga en cuenta que los parámetros apropiados deben ser cambiados si el tipo de sensor o condiciones de la muestra cambian. Establecer los parámetros para aumentar la temperatura de 1 ° C a 1,5 ° C.
- Calcule el grado de sobreenfriamiento,? T sup, con la siguiente ecuación:
Delta T = T eq sup (P) - T. (3)
T eq (P) es la temperatura de equilibrio de MH como una función de la presión P. T eq (P) se calcula utilizando el software CSMGem 1.0; P y T son la presión y la temperatura en el recipiente se mide mediante el uso de indicadores de presión y temperatura, respectivamente. - Al mismo tiempo medir la conductividad térmica, difusividad térmica y calor específico volumétrico utilizando el analizador de TPS después de? T sup es mayor que 2 ° C.
- Cambiar la sonda TPS conectado al analizador de propiedades térmicas después de cada medición. Cambiar los cables entre las sondas de TPS y el analizador de forma manual durante el experimento 9. El esquema de conexión se muestra en la Figura S2 en referencia 9. La secuencia de conmutación para cada sensor es no. 6 → 2 → 7 → 5 → 1 → 9 → 4 → 3 → → 8 6 .... La secuencia se basa en la distancia entre los sensores, que se establece en la medida de lo posible para evitar que el calor residual de afectar a las mediciones. Recopilar datos cada 3-5 minutos.
- Repetir las mediciones hasta que & #916; T sup llegan a 2 ° C nuevamente. En este experimento, Δ T sup inicialmente aumenta con el tiempo. Después de? T sup alcanza el valor máximo,? T sup disminuye gradualmente a 0 ° C debido a que la presión disminuye con la formación de MH. Compruebe si sup? T es mayor que 2 ° C antes de las mediciones TPS utilizando la ecuación 3.
- Asegúrese de que el perfil de temperatura no se ve afectada por MH fusión. Si MH funde durante las mediciones, la temperatura no aumentará debido a la fusión de MH es una reacción endotérmica. Compruebe el perfil de temperatura durante las medidas, y se discute en la sección de resultados.
- Realizar un análisis de las propiedades térmicas 'para todos los datos del perfil de temperatura utilizando la técnica de TPS.
3. Cálculo del cambio de saturación de la muestra 9,11
Nota:El grado de saturación para MH, agua, y gas en la muestra como una función del tiempo t se calcula utilizando la ecuación de estado del gas. Los detalles de cálculo y ecuaciones utilizadas se describen previamente 11.
- Calcular el gas V volumen de gas metano, t en el tiempo t
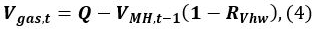
donde Q es el volumen inicial de gas en el recipiente, V MH, t - 1 es el volumen de MH en el tiempo t - 1, y R VHW es la relación en volumen de agua y MH.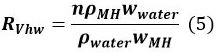
En la ecuación 5, n es el número de hidratación de MH (~ 6), ρ MH y ρ agua corresponden a la densidad de MH y el agua, respectivamente, y w MH y agua w denotan la masa molecular de MH y agua, respectively. - Calcular la cantidad Delta M t (mol) de MH formado a partir de t - 1 a t
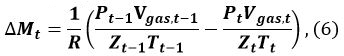
donde R es la constante de los gases, P es la presión del gas metano, y Z t (T gas, t, gas P, t) es el coeficiente de compresión de metano en el tiempo t. Nos 9 y Sakamoto et al. 11 hemos utilizado la ecuación de Benedict-Webb-Rubin (BWR), modificado por Lee y Kesler, para el cálculo de Z t 12, 13. Para este cálculo, las fórmulas (3-7.1) - (3-7.4) de la ecuación BWR 13 y las constantes de Lee-Kesler se utilizan en las Tablas 3 - 7 de referencia 13. - Calcular el cambio de volumen V Δ MH, t de MH desde t - 1 at
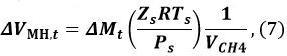
donde P s es la presión de referencia de 101.325 Pa, T s es la temperatura de referencia de 273,15 K, Z s es el coeficiente de compresión a P s y T s (Z s ~ 1), y V CH4 es la relación del volumen de gas metano en la unidad de volumen de MH [Nm 3 m -3]. Utilice un valor V de CH4 165.99 [Nm 3 m -3]. - Calcular el volumen V MH, t de la HM en el tiempo t
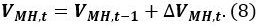
- Calcular el volumen de agua de agua V, t en el recipiente de presión en el tiempo t
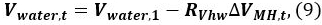
donde el agua V, 1 es el volumen inicial de agua. - Repetir los cálculos usando las ecuaciones. 4-9 en el tiempo t = 2, 3, ... para determinar el cambio en la saturación de agua, metano, y MH 11. La condición inicial es t = 1, es decir, gas V, 1 = Q. El P y T en el tiempo t se toman de los registros de datos 9. Los resultados del cálculo se muestran en la siguiente sección.
Access restricted. Please log in or start a trial to view this content.
Resultados
La figura 2a muestra el perfil de temperatura que no está afectada por MH fusión.? T c es el cambio de temperatura debido a la medida constantes térmicas. La Figura 2B muestra el perfil de temperatura que está afectada por MH fusión. El perfil en la Figura 2b no se puede analizar a través de las ecuaciones 1 y 2 debido a que estas ecuaciones se derivan asumiendo condiciones de la muestra estables.
Access restricted. Please log in or start a trial to view this content.
Discusión
Se estimó el efecto del calor formación de MH en la medición. El calor de formación MH se estimó a partir de productos de la tasa de cambio de S h como se muestra en la Figura 3b y la entalpía de formación de H = 52,9 kJ mol -1 para MH 14. En consecuencia, el cambio de temperatura máxima era de 0,00081 ° C sec -1. Esto fue mucho menor que el aumento de temperatura? T c del sensor TPS entre 1 ° C y 1,5 ° C durant...
Access restricted. Please log in or start a trial to view this content.
Divulgaciones
The authors have nothing to disclose.
Agradecimientos
Este estudio fue apoyado financieramente por el Consorcio de Investigación de Recursos MH21 hidrato de metano en Japón y el Programa Nacional de hidratos de metano por el Ministerio de Economía, Comercio e Industria. Los autores desean agradecer a T. Maekawa y S. Goto por su ayuda con los experimentos.
cifras Reproducido con permiso del (Muraoka, M., Susuki, N., Yamaguchi, H., Tsuji, T., Yamamoto, Y., Energy Fuels, 29 (3), 2015, 1345-1351, 2015, DOI.: 10.1021 / ef502350n). Derechos de autor (2015) American Chemical Society.
Access restricted. Please log in or start a trial to view this content.
Materiales
| Name | Company | Catalog Number | Comments |
| TPS thermal probe, Hot disk sensor | Hot Disk AB Co., Sweden | #7577 | Kapton sensor type, sensor radius 2.001 mm |
| Hot disk thermal properties analyzer | Hot Disk AB Co., Sweden | TPS 2500 | |
| Toyoura standard silica sand | Toyoura Keiseki Kogyo Co., Ltd., Japan | N/A | |
| Methane gas, 99.9999% | Tokyo Gas Chemicals Co., Ltd., Japan | N/A | Grade 6 N, Volume 47 L, Charging pressure 14.7 MPa |
| Water Purification System, Elix Advantage 3 | Merck Millipore., U.S. | N/A | 5 MΩ cm (at 25 °C) resistivity |
| Vibrating table, Vivratory packer | Sinfonia Technology Co. Ltd., Japan | VGP-60 | |
| Chiller, Thermostatic Bath Circulator | THOMAS KAGAKU Co., Ltd., Japan | TRL-40SP | |
| Coorant, Aurora brine | Tokyo Fine Chemical Co.,Ltd., Japan | N/A | ethylene glycol 71 wt% |
| Temparature gage | Nitto Kouatsu., Japan | N/A | Pt 100, sheath-type platinum resistance temperature detector |
| Pressure gage | Kyowa Electronic Instruments., Japan | PG-200 KU | |
| Data logger | KEYENCE., Japan | NR-500 | |
| Mass flow controller | OVAL Co., Japan | F-221S-A-11-11A | Maximum flow 2,000 N ml/M, maximum design pressure 19.6 MPa |
Referencias
- Sloan, E. D., Koh, C. A. Clathrate Hydrates of Natural Gases, 3rd ed. , 3rd ed, CRC Press. Boca Raton, FL. (2007).
- Hatzikiriakos, S. G., Englezos, P. The relationship between global warming and methane gas hydrates in the earth. Chem. Eng. Sci. 48 (23), 3963-3969 (1993).
- Yamamoto, K. Overview and introduction: pressure core-sampling and analyses in the 2012-2013 MH21 offshore test of gas production from methane hydrates in the eastern Nankai Trough. Mar. Petrol. Geol. 66 (Pt 2), 296(2015).
- Fujii, T., et al. Geological setting and characterization of a methane hydrate reservoir distributed at the first offshore production test site on the Daini-Atsumi Knoll in the eastern Nankai Trough, Japan. Mar. Petrol. Geol. 66 (Pt 2), 310(2015).
- Mao, W. L., et al. Hydrogen clusters in clathrate hydrate. Science. 297 (5590), 2247-2249 (2002).
- Lee, S., Liang, L., Riestenberg, D., West, O. R., Tsouris, C., Adams, E. CO2 hydrate composite for ocean carbon sequestration. Environ. Sci. Technol. 37 (16), 3701-3708 (2003).
- Muromachi, S., Ohmura, R., Takeya, S., Mori, H. Y. Clathrate Hydrates for Ozone Preservation. J. Phys. Chem. B. 114, 11430-11435 (2010).
- Waite, W. F., et al. Physical properties of hydrate-bearing sediments. Rev. Geophys. 47 (4), (2009).
- Muraoka, M., Susuki, N., Yamaguchi, H., Tsuji, T., Yamamoto, Y. Thermal properties of a supercooled synthetic sand-water-gas-methane hydrate sample. Energy Fuels. 29 (3), 1345-1351 (2015).
- Gustafsson, S. E. Transient plane source techniques for thermal conductivity and thermal diffusivity measurements of solid materials. Rev. Sci. Instrum. 62 (3), 797-804 (1991).
- Sakamoto, Y., Haneda, H., Kawamura, T., Aoki, K., Komai, T., Yamaguchi, T. Experimental Study on a New Enhanced Gas Recovery Method by Nitrogen Injection from a Methane Hydrate Reservoir. J. MMIJ. 123 (8), 386-393 (2007).
- Lee, B. I., Kesler, M. G. A generalized thermodynamic correlation based on three-parameter corresponding states. AIChE J. 21 (3), 510-527 (1975).
- Reid, R. C., Prausnitz, J. M., Poling, B. E. Chapter 3, Unit 3, 7. The properties of gases and liquids. , 4th ed, 47-49 (1987).
- Anderson, G. K. Enthalpy of dissociation and hydration number of methane hydrate from the Clapeyron equation. J. Chem. Thermodyn. 36 (12), 1119-1127 (2004).
- Waite, W. F., deMartin, B. J., Kirby, S. H., Pinkston, J., Ruppel, C. D. Thermal conductivity measurements in porous mixtures of methane hydrate and quartz sand. Geophys. Res. Lett. 29 (24), 82-1-82-4 (2002).
- Kumar, P., Turner, D., Sloan, E. D. Thermal diffusivity measurements of porous methane hydrate and hydrate-sediment mixtures. J. Geophys. Res. 109 (B1), (2004).
- Huang, D., Fan, S. Measuring and modeling thermal conductivity of gas hydrate-bearing sand. J. Geophys. Res. 110 (B1), (2005).
Access restricted. Please log in or start a trial to view this content.
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados