Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
La comprensión de materia orgánica disuelta Biogeoquímica través
En este artículo
Resumen
materia orgánica disuelta proporciona una fuente importante de energía y nutrientes de flujo de los ecosistemas. Aquí se demuestra un método basado en el campo de manipular la piscina ambiente de la materia orgánica disuelta en situ a través de impulsos de nutrientes fácilmente reproducibles.
Resumen
Dissolved organic matter (DOM) is a highly diverse mixture of molecules providing one of the largest sources of energy and nutrients to stream ecosystems. Yet the in situ study of DOM is difficult as the molecular complexity of the DOM pool cannot be easily reproduced for experimental purposes. Nutrient additions to streams however, have been shown to repeatedly alter the in situ and ambient DOM pool. Here we demonstrate an easily replicable field-based method for manipulating the ambient pool of DOM at the ecosystem scale. During nutrient pulse experiments changes in the concentration of both dissolved organic carbon and dissolved organic nitrogen can be examined across a wide-range of nutrient concentrations. This method allows researchers to examine the controls on the DOM pool and make inferences regarding the role and function that certain fractions of the DOM pool play within ecosystems. We advocate the use of this method as a technique to help develop a deeper understanding of DOM biogeochemistry and how it interacts with nutrients. With further development this method may help elucidate the dynamics of DOM in other ecosystems.
Introducción
materia orgánica disuelta (DOM) proporciona una fuente importante de energía y nutrientes a los ecosistemas de agua dulce y se define como la materia orgánica que pasa a través de un filtro de 0,7 micras. Dentro de los ecosistemas acuáticos, DOM también puede influir en la atenuación de la luz y la formación de complejos de metal. DOM es una mezcla altamente diversa y heterogénea de compuestos orgánicos con diversos grupos funcionales, así como nutrientes esenciales tales como el nitrógeno (N) y fósforo (P). Mientras que el término "DOM" describe toda la piscina incluyendo su C, N y P componentes, su concentración se mide como carbono orgánico disuelto (DOC). La complejidad molecular inherente de la piscina DOM sin embargo, crea retos para su estudio. Por ejemplo, no hay manera directa para medir la fracción de la reserva total de DOM compuesto de nutrientes orgánicos tales como nitrógeno orgánico disuelto (DON) y el fósforo orgánico disuelto (DOP). En lugar de ello, la concentración de nutrientes orgánicos debe ser determinada por la diferencia ( ejemplo, [DON] = [nitrógeno total disuelto] - [nitrógeno inorgánico disuelto]).
Adición de una modificación de DOM realista para una corriente es difícil debido a la diversidad de la piscina DOM ambiente. Estudios previos han añadido fuentes de carbono simples (por ejemplo, glucosa, urea 1) o una fuente concreta, como la hojarasca lixiviado 2 para manipular concentraciones en el campo. Sin embargo, estas fuentes no son particularmente representativo de la piscina DOM ambiente. Tratando de perfeccionar o concentrarse DOM ambiente para la experimentación posterior también se forja con dificultades, como la pérdida de ciertas fracciones (por ejemplo, componentes altamente lábiles) durante el procesamiento. Como resultado, es difícil de entender los controles de la piscina DOM ambiente, ya que actualmente no poseemos ningún método para manipular directamente el depósito de DOM ambiente. Sin embargo, dado que la biogeoquímica de DOM está vinculada a los nutrientes que se encuentran comúnmente en el medio ambiente (por ejemplo nittasa [NO3 -] 3), podemos añadir otros solutos de flujo de los ecosistemas y medir la respuesta de la piscina DOM para estas manipulaciones. Mediante el examen de la forma en la piscina DOM responde a una amplia gama de concentraciones de nutrientes experimentalmente impuestas que esperamos obtener una mejor idea de cómo DOM responde a las fluctuaciones de las condiciones ambientales.
Un método usado comúnmente en la biogeoquímica corriente es el método de adición de nutrientes. Experimentos de adición de nutrientes se han utilizado tradicionalmente para entender la cinética de absorción o el destino de la 4,5,6,7 soluto añadido. La adición de nutrientes pueden ser a corto plazo en la escala de 6 horas los días 4, o manipulaciones a más largo plazo en el transcurso de varios años 8. La adición de nutrientes también puede incluir nutrientes marcado con isótopos (por ejemplo, 15 N-NO 3 -) para rastrear nutriente añadido a través de reacciones biogeoquímicos. Sin embargo, los estudios basados en isótopos son a menudo EXPEnsive y requieren análisis difíciles (por ejemplo) de las digestiones múltiples compartimentos bentónicos donde los nutrientes marcados con isótopos pueden ser retenidos. La experimentación reciente ha puesto de manifiesto la utilidad de los pulsos de nutrientes a corto plazo para dilucidar los controles de solutos no añadidas y ambientales tales como DOM 9,10, revelando un nuevo camino por el cual examinar en tiempo real en las reacciones in situ biogeoquímicos. Aquí describimos y demostrar los pasos metodológicos clave para la realización de los pulsos de nutrientes a corto plazo con el objetivo de comprender la biogeoquímica acoplada de C y N y en concreto los controles de la gran diversidad depósito de DOM. Este método fácilmente reproducible implica la adición de un pulso de nutrientes a un tramo de río experimental y la medición de los cambios en la concentración de soluto tanto el manipulado y la variable de respuesta de interés (por ejemplo, DOC, DON, DOP). Mediante la manipulación de las concentraciones de nutrientes directamente in situ que son capaces de alterar indirectamente el DOMpiscina y examinar cómo los cambios de DOM concentración a través de un rango dinámico de las concentraciones de nutrientes 10.
Protocolo
1. Identificación y Caracterización de la corriente Ideal Experimental Alcance
- Asegúrese de que los alcances de transmisión experimentales son lo suficientemente largos para promover la mezcla completa de los solutos 11 y lo suficientemente largas en las que se puede producir absorción biológica. longitudes de alcance pueden variar entre los arroyos y experimentos. En las corrientes de cabecera de primer orden pequeños, llegar longitud puede variar de 20-150 m (o más si el sistema lo requiere) dependiendo de descarga y otras propiedades físicas de la corriente.
- Excluir grandes piscinas de tramos experimentales, ya que retardan el movimiento aguas abajo de solutos, secciones de flujo mínimas, y los tributarios que diluyen la solución añadido. Los tiempos de descarga de baja pueden requerir acortar la longitud del alcance de descarga más alta, mientras que puede requerir un mayor alcance.
- Identificar una ubicación en la parte superior del alcance corriente experimental por encima de un rifle para facilitar la mezcla de los solutos añadidos. Este será el sitio de adición. En la parte inferior de la corriente experimentalalcanzar, identificar una ubicación en la que está restringido el flujo y representativa de alrededor de 90% del flujo total (Figura 1). Este será el sitio de toma de muestras.

Figura 1:. Ejemplo de aguas abajo del sitio de muestreo Un sitio de muestreo ideal es que la mayor parte del flujo se estrecha y de fácil acceso y sin alteración del curso de agua y el bentos. Aquí un trozo caído de los desechos de madera ha creado este punto de muestreo en una pequeña corriente de cabecera de primer orden. Haga clic aquí para ver una versión más grande de esta figura.
- Obtener concentraciones de medida de descargas y el fondo de nutrientes de los solutos de interés antes de los experimentos con el fin de calcular la masa de solutos necesarios para la manipulations. Por favor, vea los cálculos en el paso 2.2.1.
- Obtener datos de concentración de referencia para el soluto objetivo de la manipulación (por ejemplo, NO 3 -) y cloruro (Cl -) que se utiliza a menudo como el trazador conservativo. Utilice el trazador conservativo en el contexto de estos experimentos, para seguir los cambios en la conductividad, que indican la llegada del impulso de nutrientes en la estación de muestreo y la velocidad a la que el pulso está pasando a través. Conductividad, o conductancia específica, es un sustituto para los cambios en-situ en la concentración del trazador conservador.
- Caracterizar las propiedades físico-químicas del alcance experimental mediante la recopilación de datos auxiliares tales como el ancho del alcance y profundidad, temperatura, pH y oxígeno disuelto.
- Realizar mediciones que no se pueden realizar con el uso de una sonda de medio ambiente (por ejemplo, anchura y profundidad), el día antes o inmediatamente después del experimento con el fin de minimizar cualquier bentónica or alteración química dentro del canal de flujo. Divida el alcance experimental en transectos equidistantes (por ejemplo, cada 10 m), con una anchura y al menos 3 mediciones de profundidad se pueden evaluar (por ejemplo, banco, vaguada, y la orilla derecha de la izquierda). Estos datos son valiosos para conectar las propiedades físicas de una corriente de mediciones biogeoquímicos y si los investigadores también están interesados en el cálculo de la cinética de absorción de nutrientes y parámetros 6.
2. Preparación para el Experimento
- Determinar la masa (kg) de soluto requerida para la manipulación utilizando las ecuaciones describen a continuación.
Nota: El siguiente ejemplo se aplica a un experimento a base de nitrato de NO 3 - en forma de nitrato de sodio (NaNO3) y asume un incremento específico del 3x por encima del fondo (ecuaciones se basan en las de Kilpatrick y Cobb 12). En este ejemplo los siguientes supuestos se han hecho con respecto a las condiciones de fondo: la descarga = 10 L / seg; [Cl] = 10 mg / L; [NO3 -] = 50 mg N / L. Debido a la variación entre los experimentos, ajustar los datos de entrada requeridos.- Calcular el incremento específico (Ecuación 1):
Targeted [NO3 - N mg / L] = aumento esperado de fondo [NO3 - N mg / L] * aumento apuntado
150 mg N / L = 50 g N / L * 3 - Calcular el flujo total de masa atómica (ecuación 2):
Flujo total de masa atómica (NO 3 - g de N) = 30 min 60 seg * * Q (l / s) * apuntado [NO3 - N mg / L] aumento
Donde 30 minutos es la duración supuesta de pico de soluto 12 y Q es la descarga
2 700 000 mg N = 30 min 60 seg * * 10 l / s * 150 mg N / L - Calcular el flujo de masa molecular total (Ecuación 3):
Flujo total de masa molecular (NO 3 - g de N) = flujo total de masa atómica (NO 3 - g de N) / masa atómica (14) * nos molecularvuelo (85)
Donde la masa atómica se refiere a N y el peso molecular se refiere a NaNO3.
16,392,857.14 mg N = 2.700.000 g N / (14 * 85) - Calcular la masa añadir (ecuación 4):
Masa para agregar (g) = flujo total de masa molecular (NO 3 - g de N) / 1.000.000 g / g
16.39 g de NaNO3 = 16,392,857.14 mg N / 1.000.000 g / g
Nota: Siga los cálculos anteriores para otros solutos incluyendo el trazador conservadora (por ejemplo, cloruro de sodio). Asegúrese de ajustar las masas atómicas y moleculares para el soluto de interés.
- Calcular el incremento específico (Ecuación 1):
- Preparar todos los solutos un día antes de los experimentos de campo. Pesar suficientes solutos para elevar la concentración ambiental de tanto el trazador biológica y el trazador conservador tres veces (o cantidad deseada) por encima del fondo. Es importante que la cantidad de solutos añadidos provoca un cambio medible por encima de la concentración de fondo que es suficiente para crear awide rango dinámico en la concentración de nutrientes añadido.
- Pesar solutos utilizando una balanza analítica y posteriormente almacenar en frascos de polietileno de alta densidad lavado con ácido limpias con etiquetas apropiadas. Los ejemplos de marcadores biológicos incluyen: NO 3 -: nitrato de sodio (NaNO3); NH4 +: cloruro de amonio (NH4Cl); PO 4 -3: fosfato de potasio (K 2 HPO 4). Sin embargo, la elección de trazador biológica será una función de la cuestión biogeoquímicos le está pidiendo. Las opciones para trazadores conservativos incluyen cloruro de sodio (NaCl) y bromuro de sodio (NaBr).
- Recoger los materiales restantes: el libro de campo, cinta etiquetado y la pluma, cinta de medición de campo, fresco, medidor de conductividad, ~ 20 l cubo y la varilla de gran tamaño (por ejemplo, paddle cerveza, barras de refuerzo, palo grande), aproximadamente 50 limpios y lavados de ácido 125 ml alta botellas de polietileno -Densidad. Etiquetar las botellas de 125 ml # 1-50.
Nota: Less de 50 muestras se pueden tomar por experimento y muestras de referencia están incluidos en las 50 botellas totales. - Opcional: Dependiendo de la cantidad de personal de campo, realizar el filtrado de la muestra en el lugar (ver sección # 5). Si se elige esta opción, llevar 50 botellas limpias, pre-etiquetados y se lavó con ácido 60 ml de polietileno de alta densidad en el campo. Etiquetar las botellas de 60 ml # 1-50 para que coincida con los 125 ml frascos de recolección.
3. Día de Configuración
- Desplegar el medidor de conductividad de campo en el lugar de recogida. Colocar el aparato de aguas arriba (aproximadamente 0,5-1,0 m), de donde se tomaron muestras de recolección de modo muestra no interferir con las lecturas del instrumento. El medidor permanecerá en su lugar durante todo el experimento. Un medidor de campo conductividad es mejor, ya que proporciona lecturas de conductividad en tiempo real, que son necesarios para determinar la frecuencia de muestreo (véase el paso 5.2) y filtración y el orden de análisis (pasos 5.3 y 6.1).
- Recoger 125 ml de fondo samples, por triplicado, en el sitio de adición y en el lugar de recogida del alcance experimental antes de la adición de la solución. Estos datos serán utilizados para verificar el día de la concentración ambiental y para determinar la variación en la concentración de soluto a lo largo del tramo de río. Estos datos también son valiosos para conectar la química ambiental corriente: - a las mediciones biogeoquímicos de interés (por ejemplo, Número de Documento 3 proporciones. 13).
- Registre el tiempo y la conductividad de las muestras de fondo recogidas.
- Registrar la conductividad de fondo de la corriente antes de la adición de las soluciones.
4. Los solutos Agregando
- Verter todos los reactivos (16.39 g de NaNO3 y 1,483 g de NaCl) en un recipiente grande (por ejemplo, 20 L de cubo) y añadir agua suficiente corriente para disolver completamente los solutos. Enjuagar recipientes de reactivos tres veces con agua corriente adicional y se vierte en el recipiente de enjuague solución. Realizar un seguimiento de la cantidad de agua añadida.
- Por ejemplo, utilizar una botella de 500 ml para verter el agua corriente en el recipiente. Se agita la solución hasta que todos los reactivos se han disuelto completamente.
- Recoger 60 ml de alícuota de la solución de adición. Mantener esta muestra altamente concentrada (por ejemplo bolsa zip-lock) separada de todas las demás muestras para reducir al mínimo la contaminación cruzada. Tales muestras son importantes si la cinética de absorción de nutrientes cálculo 6 es un objetivo adicional del proyecto de investigación como estas muestras se pueden usar para determinar la masa exacta de solutos añadió.
- Verter la solución en sitio de adición. Para ello, vertiendo la solución en un movimiento suave y rápido para minimizar el tiempo de retraso de los viajes y las salpicaduras que podrían reducir la cantidad de reactivos añadidos. Enjuagar el recipiente y el revuelo se pegan tres veces en la corriente inmediatamente después de la adición de garantizar que todos los reactivos se han añadido a la corriente.
- Registre el tiempo se añadió la solución: hr: min: seg.
- Grabar las masas de trazadores añadidos(Por ejemplo NaNO3 y NaCl).
- Después de que la solución se ha añadido, no perturbe la corriente. Asegúrese de que todos los viajes a lo largo de la corriente se produce en los bancos para asegurar que el flujo de bentos y la solución en sí no son perturbados.
5. El campo de muestreo
- Ordenar botellas de muestreo en orden ascendente a la espera de una solución para llegar al lugar de muestreo. El tiempo de viaje será una función de la descarga y llegar longitud y puede determinarse antes de tiempo (un día antes), ya sea con un sólo NaCl inyección o colorante rodamina (que puede ser utilizado para establecer el tiempo de viaje 14).
Nota: Si está trabajando en un proyecto con temas de DON, evitar el uso de tinte de rodamina, ya que es un tipo de DON y, por tanto, va a alterar la piscina DON ambiente si queda en el tramo de estudio.

Figura 2:Ejemplo esquemático de la curva de ruptura de solutos (BTC). Un BTC representa los cambios en la concentración de soluto en el tiempo y se puede utilizar para explicar el tránsito y los ciclos biogeoquímicos de un trazador en una corriente. Las muestras individuales se deben tomar a través de la BTC con una frecuencia que da una representación igual tanto a los ascendientes y descendientes extremidades de la BTC. Por favor, haga clic aquí para ver una versión más grande de esta figura.
- Coleccion de muestra
Nota: La sobre-objetivo global de toma de muestras, es representar adecuadamente los cambios en la concentración de soluto a ambos las extremidades de subida y bajada de la ruptura a través de la curva (BTC) (Figura 2).- A la llegada de la solución (detectado a través de un aumento de la conductividad), recoger muestras en botellas de 125 ml durante todo el BTC mediante la celebración de una botella de 125 ml en el flujo principal de agua en el punto de muestreo. RápidoLy enjuagar la botella con agua corriente y desechar enjuague aguas abajo y luego tomar la muestra. muestra de Cap y el lugar en el enfriador.
- Registre el tiempo (hr: min: seg) y la conductividad de cada muestra tomada a lo largo de la BTC en un libro de campo (Tabla 1).
- Recoger muestras basadas en el tiempo (por ejemplo, intervalos de 1 min) o en función de la velocidad a la que cambia la conductividad. Por ejemplo, si la conductividad está cambiando rápidamente, muestra cada 30-60 segundos hasta que los cambios en la conductividad lenta, en la que muestras de tiempo se pueden tomar cada 5-10 minutos. Para intervalos basados en conductividad, tomar muestras cada 15-30 unidades dependiendo de la velocidad a la que la conductividad está cambiando.
- Muestra hasta que vuelve a la conductividad de fondo o dentro de los 5 S / cm de condiciones de fondo. Intervalos de recogida de muestras se pueden ajustar durante el experimento, siempre y cuando la BTC está bien representada en las muestras al azar.
| botella # | La conductancia específica | Hora | notas |
| 1 | hr: min: seg | por ejemplo, el fondo (aguas abajo) | |
| 2 | por ejemplo, el fondo (aguas abajo) | ||
| 3 | |||
| 4 | |||
| 5 | por ejemplo, muestra a la conductancia de pico | ||
| . | |||
| . | |||
| . | |||
| Más alto de la botella # |
Tabla 1PFieldlibro: Ejemplo página del libro de laboratorio e información requerida
- Muestra de Filtrado
Nota: El filtrado de las muestras puede ocurrir ya sea en el campo o al regresar al laboratorio.- muestras de filtro de la rama ascendente en orden ascendente de la conductividad específica hasta que el pico de la conductividad específica. Espere a que el experimento sea una y muestras de filtro de la rama que cae en orden ascendente de la conductividad específica (es decir, empezar con la última muestra y trabajar hacia atrás hacia la conductividad específica pico).
Nota: Esta orden de muestras minimiza la contaminación cruzada entre las muestras y permite el mismo filtro, la jeringa y soporte del filtro para ser utilizado siempre y cuando el filtro, la jeringa y el soporte de filtro se enjuagan adecuadamente entre cada muestra (ver pasos 5.3.2- 5.3.4). - Retire el émbolo de una jeringa de 60 ml y cierre la llave de paso. Verter ~ 10 ml de la muestra en la jeringa y el émbolo volver a jeringa. Agitar la jeringa de manera que la muestraenjuagues paredes internas de la jeringa. jeringa unida al porta-filtro y abrir la llave de paso. Empuje muestra a través de porta-filtro y deseche enjuague.
- Retire el émbolo y cierre la llave de paso. Verter ~ 30 ml de la muestra en la jeringa y el émbolo volver a jeringa. Abierto stock-martillo y expulsar a ~ 10 ml a través porta-filtro y en 60 ml botella de muestreo. Tape el frasco, agitar con el filtrado y desechar. Repita este paso para un total de 3 aclarados. Esto asegurará todas las impurezas se han retirado de la botella de la muestra 60 ml y que las paredes están recubiertas con muestra.
- Retire el émbolo y cierre la llave de paso. Verter ~ 60 ml de la muestra en la jeringa y el émbolo volver a jeringa. Empuje la muestra a través del soporte del filtro y en la botella de muestra de 60 ml. Llenar las botellas hasta el hombro para evitar el agrietamiento de las botellas cuando se congela. la cápsula y el lugar en el enfriador.
- Repita los pasos 5.3.2-5.3.4 para todas las muestras restantes. Cambiar el filtro entre ascendente y descendente de las extremidades muestras para minimizar la contaminación.
- Transportar las muestras al laboratorio el mismo día y en el hielo.
- muestras de filtro de la rama ascendente en orden ascendente de la conductividad específica hasta que el pico de la conductividad específica. Espere a que el experimento sea una y muestras de filtro de la rama que cae en orden ascendente de la conductividad específica (es decir, empezar con la última muestra y trabajar hacia atrás hacia la conductividad específica pico).
6. Preparación para análisis de laboratorio
- Si el filtrado de las muestras se va a producir en el laboratorio, seguir el protocolo como se describe en la sección 5.3.1. muestras de filtros, tanto del ascenso y descenso de las extremidades del BTC con el fin de aumentar la conductividad. Cambiar el filtro entre el aumento de las extremidades y la caída de las muestras de las extremidades.
- Congelación de muestras filtradas a -20 ° C hasta su análisis.
- Asegúrese de que las instalaciones de análisis están equipados para manejar muestras altamente concentradas.
Nota: Algunos laboratorios no están equipados para analizar muestras muy concentradas y por lo tanto se debe tener cuidado. Incorporar estándares preparados que capturan ese fin más alto de las concentraciones de soluto esperados. Los altos estándares de concentración ayudarán a asegurar una curva estándar que captura el rango esperado de concentraciones de soluto manipuladas. - analizar muestrasde menor a mayor conductividad en todos los instrumentos analíticos. Ordenar muestras de baja a alta conductancia específica evita la contaminación de las muestras de bajo sal / nutrientes por las altas muestras de sal / nutrientes. Esto significa muestras de las extremidades de subida y bajada se mezclarán con respecto a la secuencia.
- Analizar las muestras para el total de carbono orgánico disuelto, nitrógeno total disuelto, nitrato y amonio, aunque la combinación exacta de análisis de soluto será una función de la pregunta de investigación (ver Wymore et al. 10 por ejemplo).
Análisis 7. Datos
- Analizar los datos mediante regresión lineal simple. La variable independiente es la concentración del nutriente añadido y la variable dependiente es la concentración de DOM, ya sea como DOC o DON. Cada punto de la figura representa una muestra al azar de la curva de ruptura y de nutrientes de que la muestra y DOC concentración / DON.
Resultados
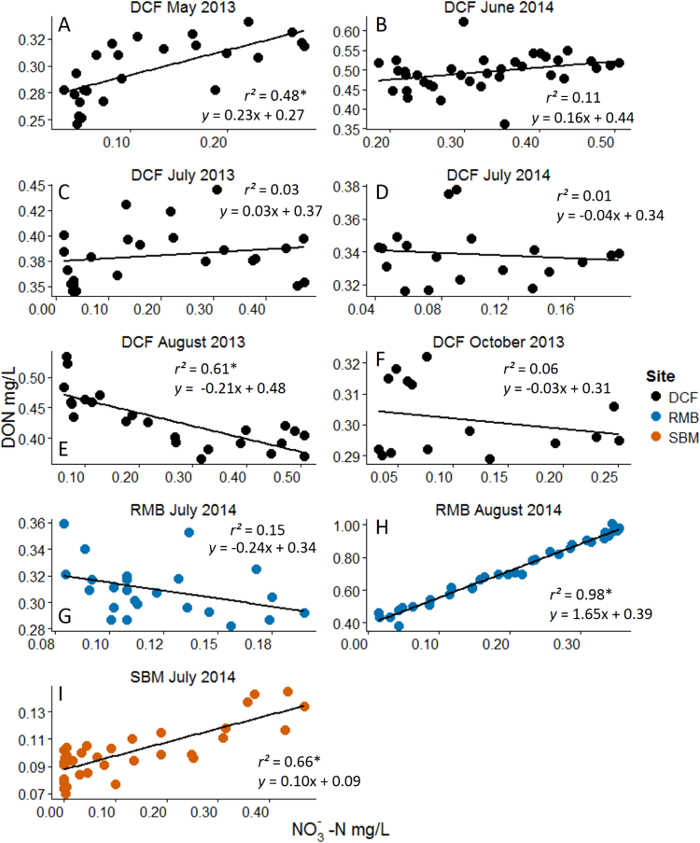
Figura 3: Ejemplo. Los resultados de nitrato (NO 3 -) Adiciones con nitrógeno orgánico disuelto (DON) como variable de respuesta Los análisis son regresiones lineales. Los asteriscos representan significación estadística a α = 0,05. Tenga en cuenta el rango dinámico de NO 3 - concentración que se consigue con el mé...
Discusión
El objetivo del método de pulso de nutrientes, tal como se presenta aquí, es caracterizar y cuantificar la respuesta de la piscina muy diverso del ambiente DOM agua de la corriente a través de un rango dinámico de un nutriente inorgánico añadido. Si el soluto añadido suficientemente aumenta la concentración del soluto reactiva, un gran espacio inferencial puede ser creado para entender cómo el ciclo biogeoquímico de DOM está ligada a la concentración de nutrientes. Este enfoque pulso de nutrientes es ideal, ...
Divulgaciones
The authors have nothing to disclose.
Agradecimientos
The authors acknowledge the Water Quality Analysis Laboratory at the University of New Hampshire for assistance with sample analysis. The authors also thank two anonymous reviewers whose comments have helped to improve the manuscript. This work is funded by the National Science Foundation (DEB-1556603). Partial funding was also provided by the EPSCoR Ecosystems and Society Project (NSF EPS-1101245), New Hampshire Agricultural Experiment Station (Scientific Contribution #2662, USDA National Institute of Food and Agriculture (McIntire-Stennis) Project (1006760), the University of New Hampshire Graduate School, and the New Hampshire Water Resources Research Center.
Materiales
| Name | Company | Catalog Number | Comments |
| Sodium Nitrate | Any | Any | |
| Sodium Chloride | Any | Any | Store purchased table salt can be used as well, however, it does contain trace levels of impurities |
| Whatman GFF glass-fiber filters | Any | Any | |
| BD Filtering Syringe | Any | Any | |
| EMD Millipore Swinnex Filter Holders | Any | Any | |
| Syringe stop-cock | Any | Any | |
| YSI Multi-parameter probe | Yellow Springs International | 556-01 | |
| Wide mouth HDPE 125 ml bottles | Any | Any | |
| 60 ml HDPE bottles | Any | Any | |
| 20 L bucket | Any | Any | |
| Field measuring tape | Any | Any | |
| Lab labeling tape | Any | Any | |
| Stir stick | Any | Any | |
| Cooler | Any | Any | |
| Sharpie pen | Any | Any | |
| Field notebook | Any | Any | |
| Tweezers | Any | Any | |
| Zip-lock bags | Any | Any |
Referencias
- Brookshire, E. N. J., Valett, H. M., Thomas, S. A., Webster, J. R. Atmospheric N deposition increases organic N loss from temperate forests. Ecosystems. 10 (2), 252-262 (2007).
- Bernhardt, E. S., McDowell, W. H. Twenty years apart: Comparisons of DOM uptake during leaf leachate releases to Hubbard Brook Valley streams in 1979 and 2000. J Geophys Res. 113, G03032 (2008).
- Taylor, P. G., Townsend, A. R. Stoichiometric control of organic carbon-nitrate relationships from soils to sea. Nature. 464, 1178-1181 (2010).
- Mulholland, P. J., et al. Stream denitrification across biomes and its response to anthropogenic nitrate loading. Nature. 452, 202-205 (2008).
- Tank, J. L., Rosi-Marshall, E. J., Baker, M. A., Hall, R. O. Are rivers just big streams? A pulse method to quantify nitrogen demand in a large river. Ecology. 89 (10), 2935-2945 (2008).
- Covino, T. P., McGlynn, B. L., McNamara, R. A. Tracer additions for spiraling curve characterization (TASCC): quantifying stream nutrient uptake kinetics from ambient to saturation. Limnol Oceanogr. 8, 484-498 (2010).
- Johnson, L. T., et al. Quantifying the production of dissolved organic nitrogen in headwater streams using 15 N tracer additions. Limnol Oceanogr. 58 (4), 1271-1285 (2013).
- Rosemond, A. D., et al. Experimental nutrient additions accelerate terrestrial carbon loss from stream ecosystems. Science. 347 (6226), 1142-1145 (2015).
- Diemer, L. A., McDowell, W. H., Wymore, A. S., Prokushkin, A. S. Nutrient uptake along a fire gradient in boreal streams of Central Siberia. Freshwater Sci. 34 (4), 1443-1456 (2015).
- Wymore, A. S., Rodríguez-Cardona, B., McDowell, W. H. Direct response of dissolved organic nitrogen to nitrate availability in headwater streams. Biogeochemistry. 126 (1), 1-10 (2015).
- Stream Solute Workshop. Concepts and methods for assessing solute dynamics in stream ecosystems. J N Am Benthol Soc. 9 (2), 95-119 (1990).
- Kilpatrick, F. A., Cobb, E. D. . Measurement of discharge using tracers: U.S Geological Survey Techniques of Water-Resources Investigations. , (1985).
- Rodríguez-Cardona, B., Wymore, A. S., McDowell, W. H. DOC: NO3- and NO3- uptake in forested headwater streams. J Geophys Res - Biogeo. 121, (2016).
- Kilpatrick, F. A., Wilson, J. F. Book 3 Chapter A9, Measurement of time of travel in streams by dye tracing. Techniques of Water-Resources Investigations of the United States Geological Survey. , (1989).
- Lutz, B. D., Bernhardt, E. S., Roberts, B. J., Mulholland, P. J. Examining the coupling of carbon and nitrogen cycles in Appalachian streams: the role of dissolved organic nitrogen. Ecology. 92 (3), 720-732 (2011).
- Michalzik, B., Matzner, E. Dynamics of dissolved organic nitrogen and carbon in a Central European Norway spruce ecosystem. Eur J Soil Sci. 50 (4), 579-590 (1990).
- Solinger, S., Kalbitz, K., Matzner, E. Controls on the dynamics of dissolved organic carbon and nitrogen in a Central European deciduous forest. Biogeochemistry. 55 (3), 327-349 (2001).
- Kaushal, S. S., Lewis, W. M. Patterns in chemical fractionation of organic nitrogen in Rocky Mountain streams. Ecosystems. 6 (5), 483-492 (2003).
- Kaushal, S. S., Lewis, W. M. Fate and transport of organic nitrogen in minimally disturbed montane streams of Colorado, USA. Biogeochemistry. 74 (3), 303-321 (2005).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados