Method Article
Protocolo de estudio observacional para el examen clínico repetido y la ecografía de cuidados intensivos dentro de los estudios de cuidados intensivos simples
En este artículo
Resumen
Los protocolos estructurados son necesarios para proporcionar respuestas a las preguntas de investigación en pacientes críticos. Los Estudios Simples de Cuidados Intensivos (SICS, por sus siglas en inglés) proporcionan una infraestructura para mediciones repetidas en pacientes críticamente enfermos, incluido el examen clínico, el análisis bioquímico y la ecografía. Los proyectos SICS tienen un enfoque específico, pero la estructura es flexible a otras investigaciones.
Resumen
Las evaluaciones longitudinales de los pacientes en estado crítico mediante combinaciones de examen clínico, análisis bioquímico y ecografía de cuidados intensivos (CCUS) pueden detectar eventos adversos de intervenciones como la sobrecarga de líquidos en una etapa temprana. Los Estudios Simples de Cuidados Intensivos (SICS) son una línea de investigación que se centra en el valor pronóstico y diagnóstico de combinaciones de variables clínicas.
El SICS-I se centró específicamente en el uso de variables clínicas obtenidas dentro de las 24 h del ingreso agudo para la predicción del gasto cardíaco (GC) y la mortalidad. Su secuela, SICS-II, se centra en las evaluaciones repetidas durante el ingreso en la UCI. El primer examen clínico por parte de investigadores capacitados se realiza dentro de las 3 horas posteriores al ingreso, que consiste en un examen físico y una conjetura informada. El segundo examen clínico se realiza dentro de las 24 horas posteriores al ingreso e incluye examen físico y conjeturas informadas, análisis bioquímicos y evaluaciones de CCUS del corazón, los pulmones, la vena cava inferior (VCI) y el riñón. Esta evaluación se repite a los días 3 y 5 después del ingreso. Las imágenes de CCUS son validadas por un experto independiente y todos los datos se registran en una base de datos segura en línea. El seguimiento a los 90 días incluye el registro de las complicaciones y el estado de supervivencia según las historias clínicas del paciente y el registro municipal de personas. El enfoque principal de SICS-II es la asociación entre la congestión venosa y la disfunción orgánica.
El propósito de publicar este protocolo es proporcionar detalles sobre la estructura y los métodos de este estudio de cohorte observacional prospectivo en curso que permite responder a múltiples preguntas de investigación. Se explica el diseño de la recolección de datos de la exploración clínica combinada y las evaluaciones de CCUS en pacientes críticos. El SICS-II está abierto a la participación de otros centros y está abierto a otras preguntas de investigación que puedan ser respondidas con nuestros datos.
Introducción
Los pacientes ingresados en la Unidad de Cuidados Intensivos (UCI) son los más críticos, con altas tasas de comorbilidades y multimorbilidades, independientemente de su diagnóstico de ingreso. Por lo tanto, la UCI es el lugar para investigar la comorbilidad y la multimorbilidad, su impacto negativo en los resultados de los pacientes y cómo la enfermedad crítica puede provocar complicaciones que contribuyan a multimorbilidades adicionales. Para obtener información sobre este grupo heterogéneo de pacientes, es de suma interés un examen detallado de cada paciente individual.
La línea de investigación de Estudios Simples de Cuidados Intensivos (SICS) está diseñada con el objetivo de evaluar el valor pronóstico y diagnóstico de una selección integral de variables clínicas, hemodinámicas y bioquímicas en pacientes de UCI recopiladas por un equipo dedicado de estudiantes-investigadores coordinados por expertos médicos. Uno de los objetivos principales del SICS-I es investigar la combinación de los hallazgos del examen clínico mejor asociados con el shock definido por el gasto cardíaco (GC) medido por ecografía de cuidados críticos (CCUS)1. El SICS-II utiliza la estructura del SICS-I, pero añade exámenes clínicos repetidos, análisis bioquímicos y CCUS. El objetivo principal del SICS-II es cuantificar la congestión venosa e identificar las variables que pueden contribuir a su desarrollo. Las mediciones repetidas proporcionan información dinámica sobre el curso de la enfermedad de un paciente. Los estudios demuestran que la sobrecarga de líquidos está presente en pacientes críticos y la sobrecarga de líquidos se asocia con nuevas morbilidades. Por lo tanto, nos centramos en la congestión venosa en estos pacientes. Además, varios estudios han sugerido los posibles efectos negativos de la administración excesiva de líquidos 2,3,4,5,6. La sobrecarga de líquidos puede percibirse como congestión venosa o sobrecarga de líquido venoso, que puede observarse por un aumento de la presión venosa central (PVC) o edema periférico. La presión elevada en el sistema venoso central puede contribuir a la reducción de la perfusión orgánica seguida de insuficiencia orgánica, pero no existe una definición exacta de congestión venosa.
Los estudios previos que sugirieron efectos negativos asociados con la administración excesiva de líquidos utilizaron mediciones sustitutivas únicas de la congestión venosa, como CVP, colapsabilidad de la VCI, equilibrio de líquidos y/o edema periférico 7,8,9,10. Hasta donde sabemos, el SICS-II es el primer estudio que realiza CCUS repetidas de múltiples órganos combinadas con los hallazgos del examen clínico para evaluar el estado hemodinámico de los pacientes de la UCI. El enfoque en esta técnica de ecografía multiorgánica es importante, ya que la insuficiencia orgánica o la disminución de la función orgánica siempre influyen en todo el sistema hemodinámico. Esperamos que los datos de los exámenes repetidos en SICS-II ayuden a desentrañar la fisiopatología y las consecuencias de la congestión venosa. En consecuencia, esto puede ayudar a mejorar la identificación temprana de pacientes críticos con riesgo de congestión venosa y guiar la optimización de la administración de líquidos. Además, se puede explorar la asociación entre la congestión venosa y la insuficiencia orgánica a corto y largo plazo. Finalmente, la implementación exitosa del protocolo SICS-II pondría en evidencia que la realización de un gran estudio prospectivo con un equipo dedicado de estudiantes-investigadores es factible y puede proporcionar datos de calidad para investigar problemas clínicos.
Aquí, se demuestra el procedimiento para realizar un examen clínico completo de los pacientes de la UCI con el objetivo de medir la congestión venosa. El11 de clinicaltrials.gov se publicó un protocolo conciso del SICS-II. Después del primer examen clínico inicial, se realizan un máximo de tres exámenes clínicos adicionales, análisis bioquímicos y CCUS. El examen físico se compone de variables que reflejan la perfusión/microcirculación periférica, como el tiempo de llenado capilar (TRC) o el moteado, así como variables de la macrocirculación, como la presión arterial, la frecuencia cardíaca y la diuresis. Además, se registran los valores de laboratorio de atención estándar (p. ej., lactato, pH). Posteriormente, se realiza CCUS del corazón, pulmones, VCI y riñón para obtener información sobre la perfusión. Se elaborarán otros métodos dentro de nuestro plan de análisis estadístico, como se hizo en el SICS-I12.
Sobre la base de 138 pacientes incluidos entre el 14-05-2018 y el 15-08-2018, las mediciones repetidas de una amplia gama de variables clínicas dentro de esta estructura parecen factibles. También demostramos que la validación independiente es factible. El SICS-II ejemplifica una metodología valiosa para permitir a los investigadores registrar con precisión los cambios en las variables de interés y, por lo tanto, puede actuar como una guía para realizar investigaciones que reflejen la progresión de la condición de los pacientes tal como se ve en la práctica diaria. El estudio SICS-II es llevado a cabo diariamente por un equipo de 2-3 estudiantes-investigadores en todo momento, con un supervisor senior disponible de guardia. Estos estudiantes-investigadores están capacitados para realizar el examen físico y la CCUS. Ejecutan todos los pasos del siguiente protocolo y se encargan de la inclusión de los pacientes tanto en horario laboral como en los fines de semana. Además, un equipo más grande de estudiantes de la UCI, de alrededor de 30 estudiantes, participa en turnos de tarde y noche, para realizar el examen clínico inicial (dentro de las 3 horas posteriores al ingreso) de los nuevos pacientes. En la Figura 1 se presenta un resumen esquemático del protocolo del estudio, y en las Figuras 2 y 3 se muestran los Formularios de Reporte de Casos (CRF) utilizados para registrar los datos en el momento de la recopilación.
Protocolo
Este estudio se lleva a cabo de acuerdo con los principios de la Declaración de Helsinki (64ª versión, Brasil 2013) y de acuerdo con la Ley de Investigación Médica con Seres Humanos (OMM), las directrices de Buenas Prácticas Clínicas y la junta de revisión institucional local (Medisch Ethische Toetsingscommissie; M18.228393).
1. Ingreso del paciente en la UCI y cribado
NOTA: Para el cribado, a lo largo del día se actualiza una lista digital con los datos mínimos del paciente, y se registran las inclusiones y exclusiones. La lista de cribado se almacena en el sistema electrónico seguro del hospital con acceso exclusivo para los investigadores. Para proteger la privacidad del paciente, todas las copias físicas de las listas se destruyen al final del día. Los criterios de inclusión son: ingreso agudo y no programado; y pacientes mayores de 18 años.
- Revise el sistema de gestión de pacientes para todas las nuevas admisiones y verifique si los pacientes cumplen con los criterios de inclusión.
- Excluir inmediatamente las readmisiones, las admisiones electivas, los pacientes menores de 18 años y aquellos que no podrán dar su consentimiento informado.
NOTA: También excluimos a los pacientes con un motivo de ingreso neurológico no traumático, ya que hemos establecido múltiples grupos de pacientes en el SICS-I, en los que este grupo estaba hemodinámicamente estable y el ingreso en UCI se refería principalmente al tratamiento neurológico1. - Agregue las posibles inclusiones a una lista de pacientes que se actualiza continuamente. Utilice esta lista para planificar mediciones nuevas y repetidas diariamente en función del momento de admisión/inclusión.
2. Examen clínico 1
NOTA: El primer examen clínico se realiza en todos los pacientes que cumplen los criterios de inclusión dentro de las 3 h posteriores al ingreso. Este examen es realizado por los estudiantes-investigadores si el paciente ingresa durante el turno diurno. Para los pacientes ingresados durante los turnos de tarde o noche, este primer examen clínico es realizado por un miembro del equipo de estudiantes de la UCI y los datos son procesados y finalizados al día siguiente por los estudiantes-investigadores. Para una descripción completa del protocolo del primer examen clínico, véase el clinicaltrials.gov13. Al lado de la cama, si es posible, se pregunta a los pacientes si dan su consentimiento para el examen clínico en ese momento. El consentimiento informado por escrito se obtiene más adelante: consulte el Paso 1.2 para obtener instrucciones y el Paso 7 .
- Examen físico
- Comience por garantizar las reglas de seguridad/aislamiento requeridas para el paciente: desinfecte las manos y las muñecas siguiendo los procedimientos hospitalarios estándar con alcohol al 70% y use guantes no estériles y un delantal de plástico o precauciones adicionales como una bata de aislamiento durante el contacto con el paciente.
- Preséntese y pida permiso al paciente para realizar el examen si no está sedado, consciente y adecuado. Explique al paciente lo que se está haciendo.
NOTA: El consentimiento informado formal se solicita en una etapa posterior durante el ingreso en la UCI o después del alta a la sala, ya sea del propio paciente o de los familiares más cercanos si el paciente no puede hacerlo. Esto se describe con más detalle en el paso 7. - Registre las variables hemodinámicas frecuencia cardíaca, frecuencia respiratoria, presión arterial sistólica (PAS), presión arterial diastólica (PAD), presión arterial media (PAM) y presión venosa central (PVC) desde el monitor de cabecera.
- Registrar la saturación de oxígeno (SpO2) y si el paciente recibe soporte respiratorio no invasivo o está ventilado mecánicamente. Si es así, registre la presión positiva al final de la espiración (PEEP) y la fracción de O2 inspirada (FiO2).
- Determine la reperfusión de la rodilla y el esternón presionando 10 s sobre la piel y soltándola, luego contando el número de segundos hasta la reperfusión completa.
- Determine la temperatura subjetiva de la piel palpando las extremidades con las manos y estime si están frías o calientes.
- Registre la temperatura de la vejiga desde el monitor, que muestra la temperatura medida por un sensor conectado a un catéter urinario permanente.
- Determine la temperatura de la piel en el dorso del pie colocando un sensor de temperatura adicional en el centro del dorso y conectándolo al monitor. Vuelva a conectar el sensor de temperatura de la vejiga al monitor después de esta medición.
- Puntúe el grado de moteado, si se puede observar, utilizando la escala de rodilla de Ait-Oufella14.
- Registre si el paciente recibe sedación y, en caso afirmativo, qué fármaco, a qué velocidad de bombeo y en qué dosis.
- Determinar y registrar la Escala de Coma de Glasgow (GCS) del paciente15.
- Estimar la supervivencia del paciente en el hospital, la supervivencia a los 6 meses y la capacidad de regresar a su residencia original a partir de una conjetura fundamentada y de los resultados de este examen clínico16,17. Pida también a la enfermera y al médico sus estimaciones y registre todas las estimaciones en el CRF.
3. Examen clínico 2
NOTA: El segundo examen clínico se realiza dentro de las 24 horas posteriores al ingreso e incluye mediciones de CCUS. Este examen siempre es realizado por estudiantes-investigadores formados en CCUS, y no por miembros del equipo estudiantil de la UCI. Además, en los pacientes que cumplen con los criterios de inclusión y se sometieron a un examen clínico 1, pero que posteriormente se demostró que padecían exclusivamente una afección neurológica (p. ej., hemorragia subaracnoidea no traumática), no se realizan mediciones repetidas, incluida la CCUS, y finalmente se excluyen.
- Obtener el consentimiento informado.
NOTA: Según lasregulaciones del Centro Médico Universitario de Groningen (UMCG) para mediciones observacionales, a partir del 1 de enero de 2016, las imágenes de ultrasonido recopiladas durante el examen clínico se pueden utilizar sin consentimiento expreso. Sin embargo, la política del estudio SICS-II es buscar el consentimiento informado de los pacientes lo antes posible y, al mismo tiempo, mantener los principios de minimizar el "estrés" para el paciente, aumentar la toma de decisiones compartida y dar al paciente el tiempo suficiente para considerar la participación. Dado que la mayoría de los pacientes no pueden dar su consentimiento al principio de su estancia en la UCI, generalmente se obtiene el consentimiento "retrasado". Si, por el contrario, pueden dar o denegar el consentimiento antes o después de los exámenes, estos no se llevarán a cabo o se eliminarán todos los datos ya obtenidos, respectivamente.- Antes de comenzar el examen, determine si el paciente está alerta/consciente y si es capaz de interactuar con los estudiantes-investigadores determinando su puntuación en el GCS. Proporcionar a los pacientes capaces una explicación sobre el examen que se va a realizar y dejar una carta escrita estandarizada que deben firmar.
- En caso de que el paciente no pueda ser consultado para obtener su consentimiento (debido a una alteración de la conciencia, capacidad mental limitada, etc.), controle su puntuación de GCS diariamente y considere obtener el consentimiento de la familia si los miembros de la familia están disponibles (como se describe en el Paso 7.1).
- Realizar el examen físico siguiendo los pasos descritos para el Examen Clínico 1.
- Realizar CCUS del corazón y los pulmones.
NOTA: Este protocolo es válido cuando se utiliza un ecógrafo en el Tabla de materiales, el transductor cardíaco para la vista de eje largo paraesternal (PLAX) y el transductor cardíaco de matriz en fase para las vistas apicales de cuatro y cinco cámaras (AP4CH, AP5CH). Para otros sistemas de ultrasonido, los usuarios deben consultar los manuales de operación de su dispositivo específico.- Encienda la máquina. Registre el ID de estudio anónimo del paciente, inicie un nuevo examen y espere a que se muestre el modo automático de imágenes 2D en la pantalla.
- Si el paciente está vestido, desabróchele la bata para exponer el pecho. Coloque nuevas pegatinas de electrocardiograma (ECG) y conéctelas a la máquina de ultrasonido si es necesario.
- Conecte el cable de ECG de la máquina al monitor de cabecera del paciente. Espere a que se estabilice y registre la frecuencia cardíaca medida por ECG en el CRF.
- Cuando sea posible, coloque al paciente ligeramente girado sobre su lado izquierdo. Esto mejora la calidad de las imágenes cardíacas y renales.
NOTA: Consideraciones técnicas: Antes de comenzar el examen, haga clic en el botón Configurar y establezca la configuración de la imagen en cinco ciclos cardíacos, una profundidad de 10 a 15 cm, un ancho de imagen de 65° y una frecuencia de 1,7/3,4 MHz. Compruebe si se ha seleccionado la sonda correcta haciendo clic en el botón Sonda . - Coloque una cantidad suficiente de gel de ultrasonido en el transductor de ultrasonido y coloque el transductor en el lateral izquierdo del esternón, entre el 3º y el 5º espacio intercostal, para obtener la vista PLAX en el modo 2D. Ajuste la profundidad según sea necesario para registrar imágenes para las mediciones del tracto de salida del ventrículo izquierdo y guardar la imagen.
NOTA: La anchura máxima del ventrículo izquierdo debe ser visible con una apertura máxima de la válvula mitral. No debe verse ningún músculo de la válvula. Antes de colocar el transductor en el pecho del paciente, adviértale que el gel está frío y puede resultar incómodo, y que sentirá algo de presión (especialmente alrededor del esternón cuando registre imágenes del tracto de salida del ventrículo izquierdo (TSVI). Tenga en cuenta que en los pacientes que tienen fracturas costales, se deben evitar algunos lugares, ya que esto puede ser incómodo para el paciente). - En el modo 2D, ajuste la profundidad a 15-20 cm y coloque el transductor sobre el vértice del corazón, caudal a la areola izquierda. Se obtiene la vista AP4CH, con las cuatro cámaras claramente visualizadas. Guarde la imagen.
- Gire la bola de seguimiento de modo que el cursor esté en el límite entre la válvula tricúspide y la pared del ventrículo derecho para obtener la excursión sistólica del plano anular tricuspídeo (TAPSE). Presione el botón M-Mode para obtener la imagen correcta y guardarla cuando se vean ondas sinusales definidas. Guarde la imagen.
- Coloque el cursor sobre la válvula tricúspide con la bola de seguimiento. Disminuya el ancho de la imagen para aumentar el número de fotogramas por segundo, necesario para la calidad del RV S. Presione primero el botón TVI y luego el botón PW para obtener la imagen correcta para el RV S y guardarla.
- Desde la vista AP4CH, incline el transductor hacia arriba (es decir, aplánelo) para obtener la vista AP5CH y obtener la raíz aórtica en la pantalla. Guarde la imagen.
- Coloque el cursor justo encima de la válvula aórtica y presione el botón PW para obtener el Doppler de onda de pulso del TSVI. Coloque el cursor exactamente en el mismo lugar donde se midió el diámetro del TSVI. Guarde la imagen con la máxima calidad (límites de onda Doppler nítidos, huecos en el interior y bien distinguibles del flujo retrógrado o mitral). Estos se utilizarán posteriormente para calcular la integral de velocidad en el tiempo (VTI) y, posteriormente, el CO.
NOTA: Trate siempre de obtener al menos tres ondas de flujo para cada medición. En caso de un ritmo irregular, se deben guardar al menos cinco ondas. - Proceda a la ecografía pulmonar utilizando el mismo transductor cardíaco phased array y cambiando la configuración a una frecuencia de 3,7 MHz, profundidad a 15 cm, y grabe las imágenes solo durante 2 ciclos cardíacos. Coloque el transductor en 6 ubicaciones diferentes, con la luz del transductor a las 12 en punto, de acuerdo con el protocolo AZUL18. Asegúrese de obtener siempre la imagen en la misma secuencia, para evitar confusiones al ver las imágenes más tarde.
- Obtener una vista superior de la clavicular media anterior de los pulmones colocando el transductor en el espacio intercostal de la2ª y3ª costilla en ambos lados. Guarde las imágenes para cada lado.
- Obtener una vista de la clavicular media anterior inferior de los pulmones colocando el transductor de 2 a 3 costillas más abajo. Guarde las imágenes para cada lado.
- Obtenga una vista axial media de los pulmones colocando el transductor debajo de las axilas del paciente. Guarde las imágenes para cada lado.
- Una vez que se completen las imágenes cardíacas y pulmonares, limpie el exceso de gel del pecho del paciente.
- Realizar CCUS de la VCI y el riñón.
- Haga clic en el botón Sonda y utilice la bola de seguimiento para cambiar la sonda activa al transductor de matriz convexa/curvilínea (abdominal) para el examen de la VCI y del riñón. La luz del transductor, que puede utilizarse para orientarse, debe estar a las 12 en punto para ambas mediciones.
- Utilizando el modo 2D y con los ajustes establecidos en una profundidad de 10-20 cm, y una frecuencia de 2,5/5,0 MHz, coloque el transductor justo debajo de la apófisis xifoides y desplácelo aproximadamente 2 cm a la derecha del paciente. La VCI debe hacerse visible. Guarde la imagen.
- Coloque el cursor justo encima de la pared superior del IVC y fuera del lumen usando la bola de seguimiento y presione el botón M-Mode . Guarde la imagen.
- Para la ecografía renal, comience con el modo 2D y ajuste la configuración a una profundidad de 10-15 cm y una frecuencia de 2,2/4,4 MHz. Coloque el transductor dorsal y caudal de la caja torácica. Obtenga el riñón elegido en el centro de la imagen y guárdelo.
NOTA: Asegúrese de colocar el transductor lo más dorsal posible para filtrar el tejido hepático y las asas intestinales. Para obtener mediciones fiables de la longitud del riñón, los bordes del riñón deben ser claramente visibles, y la distancia entre el complejo del seno central (el centro más ecogénico del riñón) y la corteza debe ser similar en toda la imagen. - Presione el botón Color para obtener una imagen Doppler en color del riñón y determinar el flujo en la vasculatura renal. Coloque el cursor sobre cualquier arteria en la unión corticomedular en el centro del riñón donde el flujo Doppler es claramente visible usando la bola de seguimiento.
- Ajuste el ángulo del cursor y pulse el botón PW . Ajuste la amplitud de la señal y el contraste en el modo activo si es necesario. Guarde la imagen.
- Determine si también hay suficiente señal venosa (es decir, flujo visible en la mitad negativa del eje y), que es necesaria para mediciones posteriores. De lo contrario, repita el paso 3.4.5 y coloque el cursor sobre una vena en la unión corticomedular en el medio donde el flujo venoso es visible. Guarde la imagen.
- Una vez que se hayan completado todas las imágenes, desconecte todos los cables, limpie el exceso de gel del paciente y del transductor, vuelva a vestir o cubrir al paciente y limpie el transductor con toallitas desinfectantes aprobadas por ultrasonido.
4. Exámenes clínicos 3 y 4
NOTA: El tercer y cuarto examen clínico se realizan los días 3 y 5 después del ingreso si el paciente todavía está en la UCI (es decir, si no se produjo ninguna muerte ni traslado a la sala).
- Examen físico
- Realizar el examen físico siguiendo los pasos descritos para el Examen Clínico 1.
- CCUS del corazón y los pulmones
- Realice el examen ultrasonográfico del corazón y los pulmones de acuerdo con el paso 3.3. Obtener el TSVI una sola vez, ya que es una medición estática y, por lo tanto, no tiene que registrarse en el Examen Clínico 3 y 4.
- CCUS de la VCI y el riñón
- Realice el examen ultrasonográfico de la VCI y el riñón de acuerdo con el paso 3.4. Obtener la longitud del riñón una sola vez, ya que es una medición estática y, por lo tanto, no tiene que registrarse en el Examen Clínico 3 y 4.
5. Mediciones y análisis de los exámenes ecográficos
NOTA: Las imágenes guardadas durante el examen clínico se utilizan después de cada examen para medir las variables deseadas. Los valores medidos se registran en el CRF y se transcriben a un sistema de gestión de datos clínicos de pacientes en línea. También se deben guardar las imágenes en las que se realizan mediciones y son visibles, además de las imágenes originales que se utilizarán posteriormente para la validación.
- Medición del TSVI
- Haga clic en el botón Sonda para seleccionar el transductor cardíaco con el fin de iniciar las mediciones.
- Usando la imagen guardada en el paso 3.3.5, detenga la imagen cuando las válvulas estén completamente abiertas.
- Haga clic en el botón Medir y, a continuación, seleccione las opciones Cardiac-Dimension-LVOT en el menú de la derecha para iniciar la medición.
- Una vez que aparezca el cursor, elija dos puntos en la base de la válvula aórtica, uno a cada lado del lumen, de borde interno a interno, durante el final de la diástole. Guarde la imagen.
NOTA: La medición del TSVI debe realizarse y guardarse antes de la medición del CO, para que la máquina pueda determinarla automáticamente.
- Medición de CO
- Usando la imagen guardada en el paso 3.3.10, trace la salida del ventrículo izquierdo. Ajuste el barrido horizontal a 100 cm/s.
- Seleccione tres ondas huecas bien formadas con bordes claros que se alineen con el ECG. Haga clic en el botón Medir y utilice la bola de seguimiento para seleccionar las opciones de Trazado de TSVI cardíaco-aórtico .
- Traza la línea de la forma de onda, comenzando y terminando en la línea de base, y la máquina de ultrasonido calculará automáticamente el CO. Repita esto durante tres ondas y guarde esta imagen.
NOTA: En caso de ritmo irregular, registre el valor medio de CO obtenido para cinco ondas.
- TAPSE
- Usando la imagen del modo M guardada en el paso 3.3.7, haga clic en el botón Medir y use la bola de seguimiento para seleccionar las opciones Cardiac-Dimension-TAPSE en el menú del lado derecho.
- Coloque el cursor primero en el punto más bajo de una onda sinusal bien definida y luego en el punto más alto. La diferencia entre los dos (el TAPSE) debería aparecer en la esquina superior izquierda de la pantalla. Haga esto en tres ondas sinusales y tome el promedio de las tres mediciones TAPSE. Guarde la imagen.
- Excursión sistólica del ventrículo derecho (RV S')
- Usando la imagen guardada en el paso 3.3.8, haga clic en el botón Calibrador y coloque el cursor en el pico más alto de una curva bien definida. Haga esto en tres curvas y tome el promedio. Guarde la imagen.
- Evaluación de artefactos de la línea B de Kerley
NOTA: Las líneas A horizontales que representan una superficie pulmonar normal se pueden utilizar como referencia en la detección de líneas B. Estos surgen de la pleura y son hiperecogénicos en comparación con las líneas A.- Ajusta el contraste de la imagen y/o la ganancia. Las líneas B no siempre son visibles inmediatamente en las imágenes guardadas.
- Determine y registre el número de líneas B de Kerley para cada una de las seis imágenes obtenidas. Dado que el número de líneas B no se guarda en la máquina, debe registrarse inmediatamente en el CRF (entre 0 y 5).
- Diámetro de la VCI y colapsabilidad
- Haga clic en el botón Sonda para seleccionar el transductor abdominal y comenzar las mediciones.
- Usando la imagen 2D guardada en el Paso 3.4.2, haga clic en el botón Calibrador y mida la distancia entre las dos paredes de la VCI a 2 cm desde el punto en que ingresa a la aurícula derecha. Este es el diámetro de la IVC, guarde esta imagen.
- Usando la imagen del modo M guardada en el paso 3.4.3, haga clic en el botón Calibrador y mida los diámetros espiratorio e inspiratorio de la VCI. Guarde esta imagen.
NOTA: Los diámetros espiratorio e inspiratorio de la VCI son los diámetros máximo y mínimo que se observan en la imagen en modo M, respectivamente.
- Longitud del riñón y flujo sanguíneo
- Usando la imagen 2D guardada en el paso 3.4.4, haga clic en el botón Calibrador y dibuje la línea más larga que se extiende desde los extremos caudales hasta los extremos craneales de la corteza renal. Esta es la longitud del riñón en cm, registre este hallazgo en el CRF. Guarde esta imagen.
- Usando la imagen Doppler guardada en el Paso 3.4.6, analice la línea de flujo venoso que se ve por debajo de la línea de base como continua, monofásica o bifásica. Registre los hallazgos en el FCI.
- Usando la imagen guardada en el paso 3.4.6, haga clic en el botón Medir y use la bola de seguimiento para seleccionar las opciones Abdominal-Renal-PS/ED/RI en el menú del lado derecho.
- Coloque el cursor en el pico y en el punto más bajo de la onda de flujo pulsátil en la mitad positiva del eje y.
NOTA: La máquina G6 puede calcular el índice resistivo renal Doppler (RRI) automáticamente si se almacena una onda de flujo pulsátil continuo, utilizando la fórmula: RRI = (velocidad sistólica máxima — velocidad diastólica final)/velocidad sistólica máxima. Guarde la imagen con la medición del ecógrafo en la pantalla. - Usando la imagen guardada en el paso 3.4.6 o 3.4.7, haga clic en el botón Calibrador y coloque el cursor, primero, sobre la velocidad máxima de flujo máxima y luego sobre la velocidad máxima de flujo en el nadir (es decir, al final de la diastólica)19. Guarde la imagen después de la medición.
NOTA: El índice de impedancia venosa (VII) se calcula a partir de: VII = (velocidad sistólica máxima — velocidad diastólica final) / velocidad sistólica máxima20,21. El VII no se registra en caso de flujo monofásico, ya que entonces solo se ve un pico y no se distinguen fases diastólica y sistólica.
6. Registro, almacenamiento y validación de datos de imágenes de ultrasonido
NOTA: Como se muestra en la Figura 1 , el registro de datos se realiza después de cada examen clínico. A continuación, se describe el procedimiento de introducción de los datos obtenidos de las mediciones, el examen clínico y la información bioquímica (Tabla 2) recuperados de la historia clínica electrónica en el archivo online anonimizado del sujeto del estudio.
- Acceda al sistema de gestión de pacientes seguro en línea y abra el expediente del paciente recién incluido. Registre los valores de gasometría, las variables séricas generales, las variables renales séricas y el análisis de orina de 24 h. La lista de todas las variables que se obtienen y las instrucciones para hacerlo se presentan en la Tabla 2.
- Validar las imágenes de CCUS cardíacas.
NOTA: Esta validación es realizada por expertos independientes de un Laboratorio Central de Imágenes Cardiovasculares de acuerdo con las directrices22 de la EACVI. Se evalúa la calidad de las imágenes obtenidas por los estudiantes-investigadores y se repiten las mediciones realizadas para garantizar la calidad requerida de las mediciones dimensionales y los trazados de los perfiles de velocidad.- Realice las mediciones del TSVI al final de la diástole, como se ve en la señal del ECG, justo debajo de la válvula aórtica.
- Trace la señal PW tomada del TSVI en una vista AP5CH para obtener el volumen sistólico del ventrículo izquierdo y el CO del ventrículo izquierdo.
- Validar todas las imágenes y mediciones de la VCI y los riñones. Esto debe ser realizado por un radiólogo abdominal independiente con experiencia. En caso de que haya problemas con la obtención de las imágenes deseadas durante el examen clínico, se puede llamar al radiólogo abdominal independiente para que realice la CCUS, en cuyo caso no se lleva a cabo ninguna validación adicional.
7. Seguimiento del paciente
- Registro del consentimiento informado
- Si se obtiene el consentimiento del paciente o de la familia durante cualquiera de los exámenes clínicos o después de que se haya finalizado el protocolo de exámenes clínicos, pero el paciente aún está ingresado en el hospital, regístrelo en el sistema de gestión de datos del paciente y cargue el formulario de consentimiento firmado a mano.
- Si se ha denegado el consentimiento, regístrelo en el sistema de gestión de datos del paciente junto con el motivo por el que no se ha obtenido el consentimiento y se lo notifique al coordinador del estudio, que eliminará todos los datos del paciente.
- Datos de mortalidad
- En el caso de los pacientes que fallecen durante el ingreso, se debe registrar la mortalidad directamente desde la historia clínica electrónica y la causa de muerte asociada.
- Para los pacientes sin mortalidad hospitalaria, se pueden obtener los datos de mortalidad del registro municipal de los Países Bajos, que se actualiza cada 90 días.
Resultados
El propósito de estos resultados representativos es ilustrar la viabilidad del protocolo.
Pacientes
En total, 663 pacientes ingresaron en la UCI entre el 14-05-2018 y el 15-08-2018. De estos, 208 pacientes fueron elegibles para la inclusión (los motivos de exclusión se muestran en la Figura 4). Se excluyeron 49 pacientes porque no había posibilidad de realizar la CCUS debido a los esfuerzos de reanimación en curso. Siete pacientes se negaron a participar (sin consentimiento informado) y en cuatro pacientes la CCUS fue imposible, por ejemplo, debido a la posición prona para la ventilación mecánica o el cierre asistido por ventosa de heridas grandes, lo que resultó en 138 pacientes incluidos con datos para el análisis.
Validación CCUS y calidad de imagen
Se planea una validación exhaustiva de las imágenes cardíacas. Se ha iniciado la validación ecográfica renal. Hasta el momento, se validaron las imágenes de 21 pacientes (15%). En 18 pacientes (86%) las imágenes parecían de calidad suficiente. Se enumeraron todas las razones de desaprobación de las imágenes y se devolvieron al investigador que realizó la ecografía para su retroalimentación. Se registra el nombre del investigador que realizó la ecografía para poder evaluar la variabilidad inter e intraobservador utilizando el Coeficiente de Correlación Intraclase (ICC). Los métodos estadísticos exactos se describirán en nuestro plan de análisis estadístico, tal como se hizo en el SICS-I12.
Caso de ejemplo: Paciente X, mujer de mediana edad
La paciente X fue admitida después de que se la encontrara con deterioro de la conciencia y presión arterial baja. Todas las mediciones obtenidas se muestran en la Tabla 1. Todas las variables se obtuvieron dentro del tiempo requerido sin datos faltantes, lo que ilustra la posible viabilidad de este protocolo. A las 3 horas del ingreso se realizó el primer examen clínico. Durante este examen, el paciente fue sedado, intubado y necesitó tratamiento vasopresor. El segundo examen clínico se realizó diez horas después y mostró signos vitales estables después de 700 mL de infusión de líquido. Se redujeron los vasopresores. La CCUS y el análisis bioquímico mostraron una función cardíaca, IVC y renal normales (Figura 5, Figura 6 y Figura 7). En T3, dos días después, se suspendieron los vasopresores, pero el balance hídrico positivo acumulado había aumentado a 6 litros, acompañado de un aumento del GC, una VCI más ancha y una disminución de la perfusión renal y de la función reflejada por el aumento de la creatinina sérica. En la T4, 5 días después del ingreso, el equilibrio hídrico y la creatinina sérica habían aumentado aún más, donde el paciente desarrolló LRA en estadio 3. El paciente falleció 2 días después por fallo multiorgánico de origen incierto, a los 7 días del ingreso.
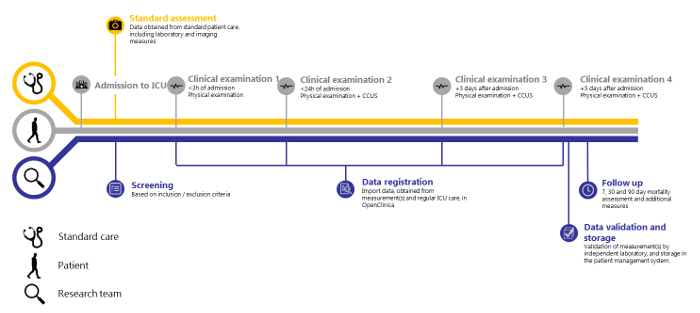
Figura 1: Resumen del estudio SICS-II. Cronología del estudio SICS-II desde el ingreso del paciente en Cuidados Intensivos hasta la etapa final del registro de datos. Haga clic aquí para ver una versión más grande de esta figura.

Figura 2: Formulario de Reporte de Caso (CRF) para examen clínico 1. CRF a ser llenado por el equipo de la UCI, los estudiantes o los estudiantes-investigadores al realizar el primer examen clínico. Haga clic aquí para ver una versión más grande de esta figura.

Figura 3: Formulario de Reporte de Caso (CRF) para los exámenes clínicos 2, 3 y 4. CRF a ser llenado por los estudiantes del equipo de la UCI o los estudiantes-investigadores al realizar el segundo, tercer y cuarto examen clínico. Haga clic aquí para ver una versión más grande de esta figura.
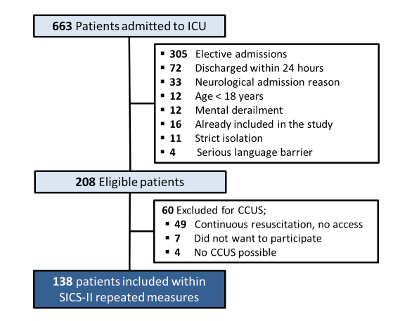
Figura 4: Cuadro de inclusión y exclusión de pacientes del SICS-II. Diagrama de flujo que describe los criterios de inclusión y exclusión de pacientes en el estudio SICS-II hasta el 15-08-2018. Haga clic aquí para ver una versión más grande de esta figura.
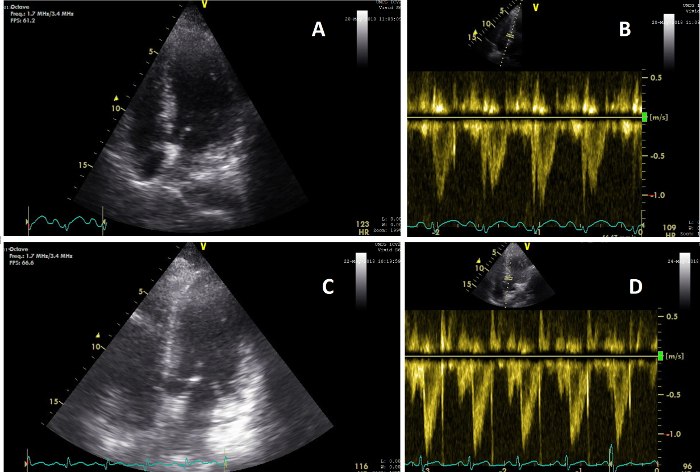
Figura 5: Vistas apicales que muestran cambios en la función cardíaca. (A) Imagen del corazón en una vista AP4CH durante la CCUS realizada durante el examen clínico 2 (T = 2); (B) Imagen de la señal de onda de pulso VTI del corazón en T = 2, que muestra un CO de 5,6 L/min; (C) Imagen del corazón en una vista AP5CH durante la CCUS realizada durante el examen clínico 3 (T = 3); (D) Imagen de la señal de onda de pulso VTI del corazón en T = 3, que muestra un CO de 8,3 L/min. Haga clic aquí para ver una versión más grande de esta figura.
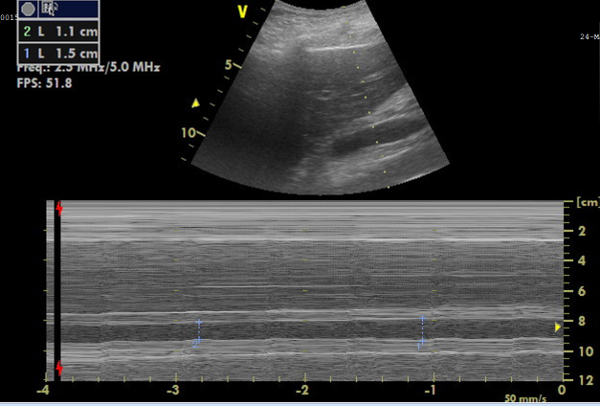
Figura 6: Imagen en modo M de la vena cava inferior (IVC) para mediciones de diámetro. Imagen que muestra, en la parte superior, la IVC en tiempo real y, debajo, la imagen en modo M que representa los cambios en el diámetro de la IVC, a partir de la cual se puede calcular la colapsabilidad. Haga clic aquí para ver una versión más grande de esta figura.
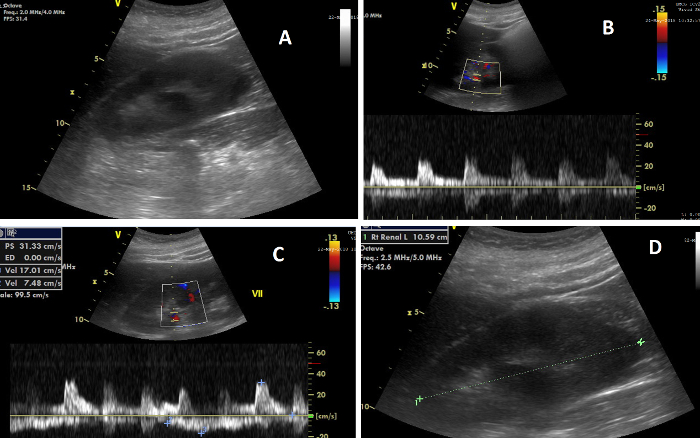
Figura 7: Los distintos elementos de la ecografía renal. (A) Imagen del riñón derecho durante la CCUS; (B) Imagen que muestra, en la parte superior, el flujo Doppler en las arterias renales y, debajo, la onda de flujo a partir de la cual se calcula el índice resistivo renal; (C) Imagen que muestra, en la parte superior, el flujo Doppler en las venas renales y, abajo, la onda de flujo a partir de la cual se calcula el índice de impedancia venosa; (D) Imagen que ilustra la medición de la longitud renal. Haga clic aquí para ver una versión más grande de esta figura.
| Variable | T1 Día 1, a las 00:38 | T2 Día 1, a las 10:53 | T3 Día 3, a las 10:14 | T4 Día 5, a las 10:20 |
| Frecuencia cardíaca (lpm) | 110 | 124 | 122 | 98 |
| Frecuencia respiratoria (respiraciones por minuto) | 24 | 15 | 26 | 12 |
| Presión arterial sistólica (mmhg) | 100 | 115 | 130 | 118 |
| Presión arterial diastólica (mmhg) | 61 | 69 | 66 | 65 |
| Presión arterial media (mmhg) | 73 | 80 | 84 | 81 |
| Balance acumulado de líquidos (mL) | 0 | 704 | 7272 | 12338 |
| Ventilación mecánica | PEEP 5, FiO2 40% | PEEP 5, FiO2 40% | PEEP 5, FiO2 30% | PEEP 5, FiO2 30% |
| Esternón CRT (segundos) | 1.5 | 2 | 4 | 3 |
| Temperatura central (◦ C) | 37.6 | 37.5 | 38.0 | 37.4 |
| Gasto urinario en la hora anterior (mL) | 117 | 60 | 0 | 10 |
| Agentes inotrópicos administrados | Noradrenalina 0,1 mg/ml 3,0 ml/h | Noradrenalina 0,1 mg/ml 1,0 ml/h | ninguno | ninguno |
| Agentes sedantes administrados | Propofol 20 mg/ml 5,0 ml/h | ninguno | ninguno | ninguno |
| Puntuación APACHE IV | 92 | 88 | 87 | 90 |
| Puntuación SOFA | 8 | 8 | 5 | 8 |
| TSVI (cm) | N.D. | 2.4 | 2.4 | 2.4 |
| Gasto cardíaco (L/min) | N.D. | 5.6 | 8.34 | 9.89 |
| CINTA (mm) | N.D. | 25 | 26 | 21 |
| RV S' (cm/s) | N.D. | 14 | 15 | 12 |
| Diámetro inspiratorio de la VCI (cm) | N.D. | 1.14 | 1.24 | 1.10 |
| Diámetro espiratorio de la VCI (cm) | N.D. | 1.27 | 1.38 | 1.50 |
| Líneas B de Kerley (total) | N.D. | 6 | 2 | 4 |
| Longitud renal (cm) | N.D. | 10.59 | N.D. | N.D. |
| Patrón de flujo venoso intrarrenal | N.D. | Continuo | Continuo | Continuo |
| IR renal Doppler | N.D. | 0.61 | 0.75 | 0.70 |
| VII | N.D. | 0.33 | 0.56 | 0.68 |
Tabla 1: Un paciente aleatorio de SICS-II. Paciente X, mujer de mediana edad ingresada en la UCI tras ser encontrada con alteración de la conciencia. Abreviaturas: lpm = latidos por minuto, CRT = tiempo de llenado capilar, TSVI = tracto de salida del ventrículo izquierdo, TAPSE = excursión sistólica del plano anular tricuspídeo, RV S' = excursión sistólica del ventrículo derecho, IVC = vena cava inferior, RRI = índice de resistencia renal, VII = índice de impedancia venosa, N.A. = no aplicable.
| Variable | Unidad | Fuente | Obtenido en |
| Lactato | mmol/L | Gasometría arterial | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| Cloruro | mmol/L | Gasometría arterial | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| pH | Gasometría arterial | Desde la atención estándar, lo más cerca posible también de cada examen clínico, máx. 12 ho de diferencia | |
| PCO2 | kPa | Gasometría arterial | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| PaO2 | kPa | Gasometría arterial | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| HCO3- | mmol/L | Gasometría arterial | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| Hemoglobina | mmol/L | Gasometría arterial | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| Leucocitos | 10 x 10-9/L | Análisis de suero | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| Trombocitos | 10 x 10-9/L | Análisis de suero | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| HS troponina | ng/L | Análisis de suero | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| ASAT | U/L | Análisis de suero | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| ALAT | U/L | Análisis de suero | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| Bilirrubina total | uoml/L | Análisis de suero | Desde la atención estándar, lo más cerca posible también de cada examen clínico, diferencia máxima de 12 h |
| Creatinina | umol/L | Análisis de suero | Todas las mediciones desde el inicio del ingreso en la UCI |
| Volumen de orina | Ml | Recogida de orina de 24 h | Todas las mediciones desde el inicio del ingreso en la UCI |
| Creatinina | mmol/24 h | Análisis de orina | Todas las mediciones desde el inicio del ingreso en la UCI |
Tabla 2: Listado de variables bioquímicas obtenidas. Aquí se enumeran todas las variables bioquímicas del paciente recopiladas durante el estudio.
Discusión
Todos los exámenes deben realizarse de acuerdo con el protocolo. El examen físico solo tiene valor si se realiza de acuerdo con definiciones preestablecidas23. Los valores de laboratorio deben recogerse de acuerdo con el protocolo para obtener todos los valores. Las imágenes claras e interpretables de CCUS son clave para responder a la pregunta de investigación de este estudio, como se describe en el Paso 3.3. Si se obtienen imágenes de mala calidad, no se pueden realizar las mediciones y análisis descritos en el paso 5 y el propósito de las mediciones repetidas caduca. Se toman tres medidas importantes para minimizar el riesgo de obtener imágenes de baja calidad. En primer lugar, los estudiantes-investigadores que realizan CCUS en nuestro estudio son entrenados por un cardiólogo-intensivista experimentado. La literatura muestra que un programa de formación corto es muy adecuado para obtener la competencia básica en CCUS24. En segundo lugar, los estudiantes investigadores son supervisados por un estudiante-investigador senior durante sus primeros 20 exámenes para que puedan recibir retroalimentación práctica. Por último, todas las imágenes cardíacas y renales adquiridas serán reevaluadas y validadas por un experto independiente de un Laboratorio Central de Imágenes Cardíacas y un radiólogo abdominal experimentado, respectivamente, para garantizar que los datos sean fiables.
Para garantizar la calidad de la imagen, los investigadores también deben prestar atención a otros aspectos. A veces es necesario volver a aplicar el gel de ultrasonido o reposicionar la sonda para que tenga un mejor contacto con la piel del paciente para garantizar una calidad de imagen óptima. También es importante tomarse el tiempo suficiente para adquirir la imagen más óptima y, en caso de duda, se debe consultar a un investigador senior, es decir, un cardiólogo-intensivista supervisor o un técnico de laboratorio central, antes de completar el examen clínico. La evaluación y validación continuas de todas las imágenes ultrasonográficas se garantiza mediante la aplicación de los pasos protocolizados que se muestran en la Figura 1. Además, los estudiantes-investigadores y los expertos intercambian comentarios con frecuencia, lo que facilita la implementación rápida de cambios en el protocolo para aumentar aún más la calidad de las imágenes y las mediciones. Esta verificación frecuente hace que los errores sistemáticos sean fáciles de detectar, de modo que la formación en CCUS para futuros estudiantes-investigadores pueda adaptarse en consecuencia. Además, las reuniones mensuales abiertas a todos los miembros del equipo permiten una evaluación exhaustiva y (si es necesario) modificaciones del protocolo.
La disponibilidad permanente para el cribado y la inclusión de pacientes es otro elemento clave para el éxito de la implementación de este estudio. Esto solo se puede lograr teniendo un equipo dedicado de estudiantes-investigadores, un gran equipo de estudiantes para brindar apoyo y una buena coordinación con los cuidadores de la UCI. Esta coordinación se lleva a cabo mediante un contacto regular y de bajo riesgo entre los cuidadores y los investigadores sobre posibles mejoras para optimizar la colaboración con la atención estándar.
Una limitación de este protocolo es que la realización exitosa de CCUS depende de la accesibilidad de las posiciones preespecificadas donde se coloca la sonda. Durante el SICS-I, ya se demostró que la CCUS cardíaca no puede realizarse cuando los pacientes requieren drenajes, gasas o apósitos para heridas que obstruyen la ventana ecocardiográfica teóricamente óptima1. Además, la posibilidad de obtener una ventana subcostal adecuada a través de la ecocardiografía transtorácica, necesaria para las mediciones de la VCI, ha demostrado previamente ser potencialmente limitada en una población general de UCI25. La disponibilidad 24/7 que requiere este protocolo para realizar los diferentes exámenes en diferentes momentos también es una posible limitación, ya que algunos centros pueden carecer de la capacidad para hacerlo. Incluso en un gran hospital académico como el UMCG, garantizar esto ha provocado retrasos en el inicio del estudio. Otra limitación intrínseca a las mediciones ultrasonográficas es la variabilidad interobservador de las mediciones. Para que la inclusión de los pacientes esté garantizada las 24 horas del día, los 7 días de la semana, es imposible que un investigador realice todos los exámenes clínicos en todos los pacientes incluidos. Este estudio tiene como objetivo que el mismo investigador lleve a cabo todas las mediciones ecográficas en un mismo paciente para minimizar la variabilidad a nivel individual, pero para toda la cohorte, la variabilidad entre observadores sigue siendo un problema.
Las imágenes ultrasonográficas de múltiples órganos pueden ser una estructura rápida, segura y eficaz para visualizar la perfusión y la función de los órganos. Es una herramienta conveniente que todos los profesionales médicos deberían poder usar, y para la cual pocas mediciones basadas en un protocolo simple y estandarizado generalmente deberían proporcionar mediciones confiables.
Además, la mayoría de los estudios observacionales que evalúan el uso de la ecografía, y en particular de la ecocardiografía, son de naturaleza retrospectiva o incluyen solo un pequeño número de pacientes. 26 Este protocolo permite un cribado estructural 24/7 de una cohorte no seleccionada de pacientes críticos, de los cuales se pueden definir subpoblaciones de interés, permitiendo así la investigación simultánea de múltiples preguntas de investigación.
Además, a pesar de que se sabe que las variables clínicas en cuidados críticos son altamente dinámicas y se influyen recíprocamente entre sí, la mayoría de los estudios solo han investigado el valor aditivo de las mediciones ecográficas singulares de órganos específicos27,28. Este es el primer protocolo que se centra en medidas repetidas, ecografía de cuerpo entero y congestión venosa. Esperamos que el SICS-II proporcione un reflejo más preciso del estado hemodinámico de los pacientes durante el ingreso en la UCI.
La estructura actual utilizada en SICS se puede aplicar a un gran número de entornos, y actualmente se está estudiando la adición de otros elementos. Su fortaleza radica en la combinación de una línea de investigación básica y una línea adaptativa en la que se pueden agregar fácilmente nuevas variables a los CRF para que se puedan investigar nuevas preguntas de investigación. Un ejemplo de esta adaptabilidad es la adición de una evaluación extensa de la pared ventricular mediante imágenes de deformación, es decir, deformación a corto plazo, al protocolo regular en un subconjunto específico de pacientes.
Además, la inclusión de los pacientes se está llevando a cabo actualmente exclusivamente en la UCI y se echa de menos parte de la trayectoria asistencial de los pacientes. Los pacientes de la UCI suelen ser admitidos primero en el servicio de urgencias (SU) y permanecen en la sala habitual del hospital después del alta de la UCI. Por lo tanto, el SICS tiene como objetivo incluir a los pacientes en una etapa más temprana mediante la inclusión de los pacientes a la llegada a la sala de emergencias y registrar las intervenciones y la función hemodinámica desde el ingreso hospitalario inicial en adelante. Además, también están en curso los planes para llevar la CCUS después del alta de la UCI a las salas regulares para que todos los pacientes puedan ser medidos en cada momento de estudio predefinido. Otro aspecto importante es la capacidad de expansión del protocolo a otros centros: su simplicidad permite una fácil adaptación por parte de los centros, que pueden iniciar la inclusión por sí mismos.
Por último, el desarrollo y la implementación exitosa de un protocolo estructurado de CCUS también pueden tener ramificaciones clínicas. A pesar de que solo se utiliza con fines de investigación, los médicos podrían implementarlo para la CCUS clínica después del corto período de capacitación propuesto. Sería interesante entonces evaluar si facilitar la formación en CCUS a los médicos (inexpertos) disminuiría las pruebas diagnósticas adicionales.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Nos gustaría agradecer a todos los miembros del grupo de estudio SICS que han estado involucrados en el SICS-I y han participado en sesiones de lluvia de ideas sobre el protocolo actual. También nos gustaría agradecer a la oficina de investigación de nuestro departamento de Cuidados Intensivos y a sus coordinadores por su apoyo; Dr. W. Dieperink y M. Onrust. Además, nos gustaría agradecer al equipo de estudiantes de la UCI y a los estudiantes-investigadores que han incluido estructuralmente a los pacientes en SICS-II hasta ahora; J. A. de Bruin, B. E. Keuning, drs. K. Selles.
Materiales
| Name | Company | Catalog Number | Comments |
| Ultrasound machine | GE Healthcare | 0144VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 3507VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 0630VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound gel | Parker | 01-08 | Aquasonic 100 ultrasound transmission gel |
| Temperature probe | DeRoyal | 81-010400EU | Skin Temperature Sensor |
Referencias
- Hiemstra, B., et al. Clinical examination, critical care ultrasonography and outcomes in the critically ill: cohort profile of the Simple Intensive Care Studies-I. BMJ open. 7 (9), 017170 (2017).
- Lee, J., et al. Association between fluid balance and survival in critically ill patients. Journal of Internal Medicine. 277 (4), 468-477 (2015).
- Perner, A., et al. Fluid management in acute kidney injury. Intensive Care Medicine. 43 (6), 807-815 (2017).
- Balakumar, V., et al. Both Positive and Negative Fluid Balance May Be Associated With Reduced Long-Term Survival in the Critically Ill. Critical care medicine. 45 (8), 749-757 (2017).
- Hjortrup, P. B., et al. Restricting volumes of resuscitation fluid in adults with septic shock after initial management: the CLASSIC randomised, parallel-group, multicentre feasibility trial. Intensive Care Medicine. 42 (11), 1695-1705 (2016).
- Prowle, J. R., Kirwan, C. J., Bellomo, R. Fluid management for the prevention and attenuation of acute kidney injury. Nature reviews. Nephrology. 10 (1), 37-47 (2014).
- Gambardella, I., et al. Congestive kidney failure in cardiac surgery: the relationship between central venous pressure and acute kidney injury. Interactive CardioVascular and Thoracic Surgery. 23 (5), 800-805 (2016).
- Chen, K. P., et al. Peripheral Edema, Central Venous Pressure, and Risk of AKI in Critical Illness. Clinical journal of the American Society of Nephrology : CJASN. 11 (4), 602-608 (2016).
- Song, J., et al. Value of the combination of renal resistance index and central venous pressure in the early prediction of sepsis-induced acute kidney injury. Journal of critical care. 45, 204-208 (2018).
- Zhang, L., Chen, Z., Diao, Y., Yang, Y., Fu, P. Associations of fluid overload with mortality and kidney recovery in patients with acute kidney injury: A systematic review and meta-analysis. Journal of Critical Care. 30 (4), (2015).
- Simple Intensive Care Studies II - Full Text View. ClinicalTrials.gov Available from: https://clinicaltrials.gov/ct2/show/NCT03577405 (2018)
- Statistical analysis plan Simple Intensive Care Studies-I DETAILED STATISTICAL ANALYSIS PLAN (SAP) 1. Administrative information 1.1. Title, registration, versions and revisions. ClinicalTrials.gov Available from: https://clinicaltrials.gov/ProvidedDocs/24/NCT02912624/SAP_000.pdf (2018)
- Simple Observational Critical Care Studies - Full Text View - ClinicalTrials.gov. ClinicalTrials.gov Available from: https://clinicaltrials.gov/ct2/show/NCT03553069 (2018)
- Ait-Oufella, H., et al. Alteration of skin perfusion in mottling area during septic shock. Annals of Intensive Care. 3 (1), 31 (2013).
- Teasdale, G., Jennett, B. Assessment of Coma and Impaired Consciousness: A Practical Scale. The Lancet. 304 (7872), 81-84 (1974).
- Detsky, M. E., et al. Discriminative Accuracy of Physician and Nurse Predictions for Survival and Functional Outcomes 6 Months After an ICU Admission. JAMA. 317 (21), 2187 (2017).
- Lipson, A. R., Miano, S. J., Daly, B. J., Douglas, S. L. The Accuracy of Nurses' Predictions for Clinical Outcomes in the Chronically Critically Ill. Research & reviews. Journal of nursing and health sciences. 3 (2), 35-38 (2017).
- Lichtenstein, D. A. BLUE-protocol and FALLS-protocol: two applications of lung ultrasound in the critically ill. Chest. 147 (6), 1659-1670 (2015).
- Tang, W. H. W., Kitai, T. Intrarenal Venous Flow: A Window Into the Congestive Kidney Failure Phenotype of Heart Failure. JACC: Heart Failure. 4 (8), 683-686 (2016).
- Jeong, S. H., Jung, D. C., Kim, S. H., Kim, S. H. Renal venous doppler ultrasonography in normal subjects and patients with diabetic nephropathy: Value of venous impedance index measurements. Journal of Clinical Ultrasound. 39 (9), 512-518 (2011).
- Iida, N., et al. Clinical Implications of Intrarenal Hemodynamic Evaluation by Doppler Ultrasonography in Heart Failure. JACC: Heart Failure. 4 (8), 674-682 (2016).
- Lang, R. M., et al. Recommendations for Cardiac Chamber Quantification by Echocardiography in Adults: An Update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. European Heart Journal - Cardiovascular Imaging. 16 (3), 233-271 (2015).
- Hiemstra, B., Eck, R. J., Keus, F., van der Horst, I. C. C. Clinical examination for diagnosing circulatory shock. Current opinion in critical care. 23 (4), 293-301 (2017).
- Vignon, P., et al. Basic critical care echocardiography: validation of a curriculum dedicated to noncardiologist residents. Critical care medicine. 39 (4), 636-642 (2011).
- Jensen, M. B., Sloth, E., Larsen, K. M., Schmidt, M. B. Transthoracic echocardiography for cardiopulmonary monitoring in intensive care. European journal of anaesthesiology. 21 (9), 700-707 (2004).
- Koster, G., van der Horst, I. C. C. Critical care ultrasonography in circulatory shock. Current opinion in critical care. 23 (4), 326-333 (2017).
- Haitsma Mulier, J. L. G., et al. Renal resistive index as an early predictor and discriminator of acute kidney injury in critically ill patients; A prospective observational cohort study. PloS one. 13 (6), 0197967 (2018).
- Micek, S. T., et al. Fluid balance and cardiac function in septic shock as predictors of hospital mortality. Critical care. 17 (5), 246 (2013).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados