Method Article
단순 집중 치료 연구 내에서 반복 임상 검사 및 중환자 치료 초음파 검사를 위한 관찰 연구 프로토콜
요약
중증 환자의 연구 질문에 대한 답변을 제공하기 위해서는 구조화된 프로토콜이 필요합니다. SICS(Simple Intensive Care Studies)는 임상 검사, 생화학 분석 및 초음파 검사를 포함하여 중증 환자의 반복 측정을 위한 인프라를 제공합니다. SICS 프로젝트는 특정 초점이 있지만 구조는 다른 조사에 유연하게 적용됩니다.
초록
임상 검사, 생화학 분석 및 중환자 치료 초음파(CCUS)를 조합하여 중증 환자에 대한 종단 평가를 통해 체액 과부하와 같은 중재의 부작용을 조기에 감지할 수 있습니다. SICS(Simple Intensive Care Studies)는 임상 변수 조합의 예후 및 진단 가치에 중점을 둔 연구 라인입니다.
SICS-I는 특히 심박출량(CO) 및 사망률을 예측하기 위해 급성 입원 후 24시간 이내에 얻은 임상 변수를 사용하는 데 중점을 두었습니다. 속편인 SICS-II는 ICU 입원 중 반복적인 평가에 중점을 둡니다. 훈련된 연구원에 의한 첫 번째 임상 검사는 입원 후 3시간 이내에 수행되며 신체 검사와 교육된 추측으로 구성됩니다. 두 번째 임상 검사는 입원 후 24시간 이내에 수행되며 심장, 폐, 하대정맥(IVC) 및 신장에 대한 신체 검사 및 교육적 추측, 생화학 분석 및 CCUS 평가가 포함됩니다. 이 평가는 입원 후 3일차와 5일차에 반복됩니다. CCUS 이미지는 독립적인 전문가에 의해 검증되며, 모든 데이터는 온라인 보안 데이터베이스에 등록됩니다. 90일 후의 후속 조치에는 환자의 의료 차트와 시 개인 등록부에 따른 합병증 및 생존 상태 등록이 포함됩니다. SICS-II의 주요 초점은 정맥 울혈과 장기 기능 장애 사이의 연관성입니다.
이 프로토콜을 발표하는 목적은 이 진행 중인 전향적 관찰 코호트 연구의 구조와 방법에 대한 세부 정보를 제공하여 여러 연구 질문에 답할 수 있도록 하는 것입니다. 중증 환자에 대한 결합된 임상 검사 및 CCUS 평가의 데이터 수집 설계가 설명됩니다. SICS-II는 다른 센터도 참여할 수 있도록 열려 있으며 당사 데이터로 답변할 수 있는 다른 연구 질문에도 열려 있습니다.
서문
중환자실(ICU)에 입원한 환자는 입원 진단과 관계없이 공동 및 다중 질환 비율이 높은 가장 위중한 환자입니다. 따라서 ICU는 동시 질환 및 다중 질환, 환자 결과에 대한 부정적인 영향, 심각한 질병이 어떻게 추가적인 다중 질환에 기여하는 합병증으로 이어질 수 있는지 조사할 수 있는 환경입니다. 이 이질적인 환자 그룹에 대한 통찰력을 얻기 위해서는 각 개별 환자에 대한 상세한 검사가 가장 중요합니다.
SICS(Simple Intensive Care Studies) 연구 라인은 의료 전문가로 구성된 전담 학생 연구원 팀이 수집한 ICU 환자의 임상적, 혈역학적 및 생화학적 변수의 포괄적인 선택의 예후 및 진단 가치를 평가하는 것을 목표로 설계되었습니다. SICS-I의 주요 목표 중 하나는 중환자 치료 초음파(CCUS)로 측정한 심박출량(CO)으로 정의되는 쇼크와 가장 관련이 있는 임상 검사 결과의 조합을 조사하는 것입니다1. SICS-II는 SICS-I의 구조를 사용하지만 반복적인 임상 검사, 생화학 분석 및 CCUS가 추가되었습니다. SICS-II의 주요 초점은 정맥 울혈을 정량화하고 정맥 울혈에 기여할 수 있는 변수를 식별하는 것입니다. 반복적인 측정은 환자의 질병 경과에 대한 동적 정보를 제공합니다. 연구에 따르면 체액 과부하는 중환자에게 존재하며 체액 과부하는 새로운 질병과 관련이 있습니다. 따라서 우리는 이러한 환자의 정맥 울혈에 초점을 맞춥니다. 또한, 여러 연구에서 과도한 체액 투여가 미칠 수 있는 부정적인 영향 2,3,4,5,6을 시사하고 있습니다. 체액 과부하는 정맥 울혈 또는 정맥액 과부하로 인식될 수 있으며, 이는 중심 정맥압(CVP) 증가 또는 말초 부종으로 관찰될 수 있습니다. 중심 정맥계의 압력 상승은 장기 관류 감소에 이은 장기 부전의 원인이 될 수 있지만 정맥 울혈에 대한 정확한 정의는 없습니다.
과도한 수액 투여와 관련된 부정적인 영향을 시사하는 이전 연구에서는 CVP, IVC 접힘, 체액 균형 및/또는 말초 부종과 같은 정맥 울혈에 대한 단일 대리 측정을 사용했습니다 7,8,9,10. 우리가 아는 한, SICS-II는 ICU 환자의 혈역학적 상태를 평가하기 위해 임상 검사 결과와 결합하여 여러 장기에 대한 반복 CCUS를 수행한 최초의 연구입니다. 장기 부전 또는 장기 기능 감소는 항상 전체 혈역학 시스템에 영향을 미치기 때문에 이 다기관 초음파 기술에 초점을 맞추는 것이 중요합니다. 우리는 SICS-II의 반복적인 검사에서 얻은 데이터가 정맥 울혈의 병태 생리학과 결과를 밝히는 데 도움이 될 것으로 기대합니다. 결과적으로, 이는 정맥 울혈의 위험이 있는 중증 환자를 조기에 식별하는 데 도움이 될 수 있으며 수액 투여의 최적화를 안내하는 데 도움이 될 수 있습니다. 또한 정맥 울혈과 단기 및 장기 장기 부전 사이의 연관성을 조사할 수 있습니다. 마지막으로, SICS-II 프로토콜의 성공적인 구현은 전담 학생 연구자 팀과 함께 대규모 전향적 연구를 수행하는 것이 실현 가능하고 임상 문제를 조사하기 위한 양질의 데이터를 얻을 수 있음을 분명하게 할 것입니다.
여기에서는 정맥 울혈을 측정하기 위해 ICU 환자에 대한 포괄적인 임상 검사를 수행하는 절차를 보여줍니다. SICS-II의 간결한 프로토콜이clinicaltrials.gov 11일에 발표되었습니다. 첫 번째 초기 임상 검사 후 최대 3회의 추가 임상 검사, 생화학 분석 및 CCUS가 수행됩니다. 신체 검사는 모세혈관 보충 시간(CRT) 또는 얼룩과 같은 말초 관류/미세순환을 반영하는 변수와 혈압, 심박수 및 소변량과 같은 거시순환 변수로 구성됩니다. 또한 표준 치료 실험실 값(예: 젖산, pH)이 등록되어 있습니다. 그 후, 관류에 대한 정보를 얻기 위해 심장, 폐, IVC 및 신장의 CCUS를 수행합니다. 추가 방법은 SICS-I12에서 수행된 것처럼 통계 분석 계획 내에서 자세히 설명될 것입니다.
2018년 5월 14일부터 2018년 8월 15일 사이에 포함된 138명의 환자를 기반으로 이 구조 내에서 광범위한 임상 변수를 반복적으로 측정하는 것이 가능한 것으로 보입니다. 또한 독립적인 검증이 가능하다는 것을 보여줍니다. SICS-II는 연구자가 관심 변수의 변화를 정확하게 등록할 수 있도록 하는 귀중한 방법론을 예시하며, 따라서 일상 진료에서 볼 수 있는 환자 상태의 진행 상황을 반영하는 연구 수행을 위한 가이드 역할을 할 수 있습니다. SICS-II 연구는 항상 2-3명의 학생 연구원으로 구성된 팀에 의해 매일 수행되며, 선임 감독자가 대기할 수 있습니다. 이 학생 연구원은 신체 검사 및 CCUS를 수행하는 교육을 받았습니다. 그들은 다음 프로토콜의 모든 단계를 실행하고 근무 시간과 주말 모두에 환자를 포함할 책임이 있습니다. 또한 약 30명의 학생으로 구성된 대규모 ICU 학생 팀이 저녁 및 야간 근무에 참여하여 새로운 환자에 대한 초기 임상 검사(입원 후 3시간 이내)를 수행합니다. 그림 1 은 연구 프로토콜의 개략적인 요약을 나타내고, 그림 2 와 3 은 수집 시 데이터를 등록하는 데 사용되는 사례 보고서 양식(CRF)을 표시합니다.
프로토콜
본 연구는 헬싱키 선언(64th version, Brazil 2013)의 원칙과 인간피험자법(WMO)과 관련된 의학연구법(WMO), 우수임상관리기준(Good Clinical Practice) 및 지역 기관심사위원회(Medisch Ethische Toetsingscommissie; M18.228393).
1. 환자의 ICU 입원 및 선별 검사
메모: 스크리닝을 위해 최소 환자 데이터가 포함된 디지털 목록이 하루 종일 업데이트되고 포함 및 제외가 등록됩니다. 선별 검사 목록은 연구자만 액세스할 수 있는 보안 병원 전자 시스템에 저장됩니다. 환자의 개인 정보를 보호하기 위해 목록의 모든 물리적 사본은 하루가 끝나면 파기됩니다. 포함 기준은 다음과 같습니다 : 급성 및 계획되지 않은 입학; 18세 이상의 환자.
- 모든 신규 입원에 대해 환자 관리 시스템을 스크리닝하고 환자가 포함 기준을 충족하는지 확인합니다.
- 재입원, 선택적 입원, 18세 미만의 환자 및 정보에 입각한 동의를 제공할 수 없는 환자는 즉시 제외합니다.
메모: 또한 SICS-I에 여러 환자 그룹을 설정했기 때문에 외상이 아닌 신경학적 입원 사유가 있는 환자는 제외하며, 이 그룹은 혈역학적으로 안정적이었고 ICU 입원은 주로 신경학적 치료와 관련이 있었습니다1. - 지속적으로 업데이트되는 환자 목록에 가능한 포함을 추가합니다. 이 목록을 사용하여 입원/포함 시간에 따라 매일 새롭고 반복되는 측정을 계획하십시오.
2. 임상시험 1
메모: 첫 번째 임상 검사는 입원 후 3시간 이내에 포함 기준을 충족하는 모든 환자를 대상으로 실시합니다. 이 검사는 환자가 주간 교대 근무 중에 입원한 경우 학생-연구원이 수행합니다. 야간 또는 야간 근무 중에 입원한 환자의 경우, 이 첫 번째 임상 검사는 ICU 학생 팀의 구성원이 수행하며 학생 연구원이 데이터를 처리하고 다음 날 마무리합니다. 첫 번째 임상 검사의 프로토콜에 대한 자세한 설명은 clinicaltrials.gov13을 참조하십시오. 가능하다면 침대 곁에서 환자에게 그 순간에 임상 검사에 동의하는지 묻습니다. 서면 동의는 나중에 얻습니다: 지침은 1.2단계를 참조하고 7단계를 참조하십시오.
- 신체 검사
- 환자에게 필요한 안전/격리 규칙을 확인하는 것부터 시작하십시오: 표준 병원 절차에 따라 70% 알코올로 손과 손목을 소독하고 비멸균 장갑과 플라스틱 앞치마 또는 환자 접촉 시 격리 가운과 같은 추가 예방 조치를 사용합니다.
- 자신을 소개하고 환자가 진정 상태이고 의식이 없으며 적절하지 않은 경우 검사를 수행할 수 있도록 허락을 구합니다. 환자에게 무슨 일이 일어나고 있는지 설명하십시오.
메모: 중환자실에 입원하거나 병동으로 퇴원한 후 환자 본인 또는 환자가 할 수 없는 경우 가장 가까운 친척에게 공식적인 사전 동의가 요청됩니다. 이 내용은 7단계에 자세히 설명되어 있습니다. - 병상 모니터에서 혈류역학적 변수 심박수, 호흡수, 수축기 혈압(SBP), 이완기 혈압(DBP), 평균 동맥압(MAP) 및 중심 정맥압(CVP)을 등록합니다.
- 산소포화도(SpO2)와 환자가 비침습적 호흡 보조를 받는지 또는 기계적 인공호흡을 받는지 여부를 등록합니다. 그렇다면 양의 호기 압력(PEEP)과 흡기 O2 (FiO2)의 분율을 등록합니다.
- 무릎과 흉골의 재관류를 확인하려면 피부를 10초 동안 누르고 손을 뗀 다음 완전히 재관류될 때까지 시간(초)을 세어 확인합니다.
- 손으로 팔다리를 촉진하여 주관적인 피부 온도를 확인하고 차가운지 따뜻한지 추정합니다.
- 모니터에서 방광 온도를 기록하면 체내 요로 카테터에 부착된 센서로 측정한 온도가 표시됩니다.
- 등쪽 중앙에 추가 온도 센서를 배치하고 모니터에 연결하여 발 등쪽의 피부 온도를 확인합니다. 이 측정 후 방광 온도 센서를 모니터에 다시 연결하십시오.
- Ait-Oufella 무릎 척도14를 사용하여 관찰 가능한 경우 얼룩 정도를 점수화합니다.
- 환자가 진정제를 투여받는지, 그렇다면 어떤 약물을 투여받을지, 어떤 펌프 속도로, 어떤 투여량을 투여받는지 등록합니다.
- 환자의 글래스고 혼수 척도(GCS)를 결정하고 등록합니다.15.
- 교육받은 추측과 본 임상검사의 결과를 바탕으로 환자의 병원 입원 생존율, 6개월 생존율 및 원래 거주지로 돌아갈 수 있는 능력을 추정한다16,17. 간호사와 의사에게도 견적을 요청하고 CRF에 모든 견적을 등록하십시오.
3. 임상검사 2
메모: 두 번째 임상 검사는 입원 후 24시간 이내에 실시되며 CCUS 측정이 포함됩니다. 이 검사는 항상 ICU 학생 팀의 구성원이 아닌 CCUS에서 교육을 받은 학생-연구원이 수행합니다. 또한, 선정 기준을 충족하고 임상검사 1을 받았으나 나중에 신경학적 상태(예: 비외상성 지주막하 출혈)만을 앓고 있는 것으로 밝혀진 환자의 경우, CCUS를 포함한 반복 측정을 수행하지 않으며, 이는 궁극적으로 제외됩니다.
- 정보에 입각한 동의를 얻습니다.
참고: 관찰 측정에 대한 UMCG(University Medical Center Groningen) 규정에 따라 2016년 1월 1일부터 임상 검사 중에 수집된 초음파 이미지는 명시적 동의 없이 사용할 수 있습니다. 그러나 SICS-II 연구의 정책은 환자에 대한 "스트레스"를 최소화하고, 공유된 의사 결정을 늘리며, 환자에게 참여를 고려할 수 있는 충분한 시간을 제공한다는 원칙을 동시에 유지하는 동시에 가능한 한 빠른 시일 내에 환자로부터 정보에 입각한 동의를 구하는 것입니다. 대부분의 환자는 중환자실 입원 초기에 동의를 제공할 수 없기 때문에 일반적으로 "지연된" 동의를 얻습니다. 반대로, 검사 전후에 동의를 제공하거나 거부할 수 있는 경우, 이는 수행되지 않거나 이미 획득한 모든 데이터가 각각 삭제됩니다.- 검사를 시작하기 전에 환자가 의식이 있고 GCS 점수를 결정하여 학생-연구원과 소통할 수 있는지 확인합니다. 유능한 환자에게 수행할 검사에 대한 설명을 제공하고 환자가 서명해야 하는 표준화된 서면 서신을 남겨둡니다.
- 환자가 동의를 구하기 위해 상담할 수 없는 경우(의식 장애, 제한된 정신 능력 등으로 인해), 매일 GCS 점수를 모니터링하고 가족 구성원과 연락할 수 있는 경우 가족의 동의를 구하는 것을 고려하십시오(7.1단계 설명 참조).
- 임상 검사 1에 설명된 단계에 따라 신체 검사를 수행합니다.
- 심장과 폐의 CCUS를 수행합니다.
메모: 이 프로토콜은 초음파 기계를 사용할 때 유효합니다. 재료 표, PLAX(parasternal long axis view)를 위한 심장 변환기, 정점 4개 및 5개의 챔버 보기(AP4CH, AP5CH)를 위한 심장 위상 배열 변환기. 다른 초음파 시스템의 경우 사용자는 해당 장치의 사용 설명서를 참조해야 합니다.- 기계를 켭니다. 환자의 익명 연구 ID를 등록하고 새 검사를 시작한 다음 자동 2D 이미징 모드가 화면에 표시될 때까지 기다립니다.
- 환자가 옷을 입고 있는 경우 가운의 단추를 풀어 가슴이 드러나도록 합니다. 새 심전도(ECG) 스티커를 부착하고 필요한 경우 초음파 기계에 연결합니다.
- 기계의 ECG 케이블을 환자의 침대 옆 모니터에 연결합니다. 안정화될 때까지 기다렸다가 ECG로 측정한 심박수를 CRF에 등록합니다.
- 가능하면 환자를 왼쪽으로 약간 회전시켜 배치합니다. 이를 통해 심장 및 신장 영상의 품질이 향상됩니다.
메모: 기술적 고려 사항: 검사를 시작하기 전에 구성 버튼을 클릭하고 이미지 설정을 5개의 심장 주기, 10–15cm의 깊이, 65°의 이미지 너비 및 1.7/3.4MHz의 주파수로 설정합니다. 프로브 버튼을 클릭하여 올바른 프로브가 선택되었는지 확인하십시오. - 초음파 변환기에 충분한 양의 초음파 젤을 바르고 변환기를 흉골의 왼쪽 측면, 3번째와 5번째 늑간 공간 사이에 배치하여 2D 모드에서 PLAX 보기를 얻습니다. 필요에 따라 깊이를 조정하여 좌심실 유출로 측정을 위한 이미지를 기록하고 이미지를 저장합니다.
메모: 좌심실의 최대 너비는 승모판막이 최대한 열릴 때 볼 수 있어야 합니다. 판막의 근육이 보이지 않아야 합니다. 트랜스듀서를 환자의 가슴에 놓기 전에 젤이 차갑고 불편함을 느낄 수 있으며 약간의 압력(특히 좌심실 유출로(LVOT)에 대한 이미지를 기록할 때 흉골 주변)을 느낄 수 있음을 경고합니다. 늑골 골절이 있는 환자의 경우 환자에게 불편할 수 있으므로 일부 부위를 피해야 합니다. - 2D 모드에서 깊이를 15-20cm로 조정하고 트랜스듀서를 심장 정점, 왼쪽 유륜 꼬리 위에 놓습니다. 4개의 챔버가 모두 명확하게 시각화된 AP4CH 보기를 얻을 수 있습니다. 이미지를 저장합니다.
- 커서가 삼첨판 판막과 우심실 벽 사이의 경계에 있도록 트랙볼을 굴려 TAPSE(Tricuspid Annular Plane Systolic Excursion)를 얻습니다. M-Mode 버튼을 눌러 올바른 이미지를 얻고 정의된 부비동파가 보일 때 저장합니다. 이미지를 저장합니다.
- 트랙볼이 있는 삼첨판 위에 커서를 놓습니다. 이미지의 너비를 줄여 RV S의 품질에 필요한 초당 프레임 수를 늘립니다. TVI 버튼을 먼저 누른 다음 PW 버튼을 눌러 RV S'에 대한 올바른 이미지를 얻고 저장합니다.
- AP4CH 보기에서 변환기를 위쪽으로 기울이면(즉, 평평하게) AP5CH 보기를 얻고 대동맥근이 화면에 표시됩니다. 이미지를 저장합니다.
- 대동맥 판막 바로 위에 커서를 놓고 PW 버튼을 눌러 LVOT 맥파 도플러를 얻습니다. LVOT 직경이 측정된 정확히 동일한 위치에 커서를 놓습니다. 최고 품질(선명한 도플러파 경계, 내부가 비어 있고 역행 또는 승모판과 잘 구별됨)으로 이미지를 저장합니다. 이는 나중에 VTI(Velocity Time Integral)를 계산하는 데 사용되며 이후에 CO를 계산하는 데 사용됩니다.
메모: 항상 모든 측정에 대해 최소 3개의 유파를 얻으십시오. 불규칙한 리듬의 경우 최소 5개의 파동을 저장해야 합니다. - 동일한 위상 배열 심장 변환기를 사용하여 폐 초음파를 진행하고 설정을 3.7MHz의 주파수, 15cm의 깊이로 변경하고 2번의 심장 주기 동안에만 이미지를 기록합니다. BLUE 프로토콜 6에 따라 12시 방향에 변환기 표시등이 있는18개의 다른 위치에 변환기를 배치합니다. 나중에 이미지를 볼 때 혼동을 피하기 위해 항상 동일한 순서로 이미지를 가져와야 합니다.
- 양쪽의 2번째 및 3 번째 늑골의 늑간 공간에 변환기를 배치하여 폐의 우수한 전방 중간 쇄골 보기를 얻습니다. 각 면에 대한 이미지를 저장합니다.
- 변환기를 갈비뼈 2-3개 더 낮게 배치하여 폐의 하전방 중간 쇄골 시야를 얻습니다. 각 면에 대한 이미지를 저장합니다.
- 환자의 겨드랑이 아래에 변환기를 배치하여 폐의 중간 축 보기를 얻습니다. 각 면에 대한 이미지를 저장합니다.
- 심장 및 폐 영상 촬영이 완료되면 환자의 가슴에서 여분의 젤을 닦아냅니다.
- IVC와 신장의 CCUS를 수행합니다.
- 프로브 버튼을 클릭하고 트랙볼을 사용하여 IVC 및 신장 검사를 위해 활성 프로브를 볼록/곡선 배열(복부) 변환기로 변경합니다. 방향에 사용할 수 있는 변환기의 조명은 두 측정 모두에 대해 12시 방향에 있어야 합니다.
- 2D 모드를 사용하고 10–20cm 깊이로 설정하고 2.5/5.0MHz의 주파수로 설정한 상태에서 변환기를 xiphoid 프로세스 바로 아래에 놓고 환자의 오른쪽으로 약 2cm 이동합니다. IVC가 가시화되어야 합니다. 이미지를 저장합니다.
- 트랙볼을 사용하여 IVC의 상부 벽 바로 위와 루멘 외부에 커서를 놓고 M-Mode 버튼을 누릅니다. 이미지를 저장합니다.
- 신장 초음파의 경우 2D 모드로 시작하여 10-15cm 깊이와 2.2/4.4MHz의 주파수로 설정을 조정합니다. 변환기를 흉곽의 등쪽과 꼬리쪽에 놓습니다. 이미지에서 선택한 신장 중심을 가져와 저장합니다.
메모: 간 조직과 장 루프를 걸러낼 수 있도록 변환기를 가능한 한 등쪽에 배치하십시오. 신장 길이를 신뢰할 수 있게 측정하려면 신장의 경계가 명확하게 보여야 하며, 중앙 부비동 복합체(신장의 반향 중심)와 피질 사이의 거리가 이미지 전체에서 비슷해야 합니다. - Color 버튼을 눌러 신장의 컬러 도플러 이미지를 얻고 신장 혈관 구조의 흐름을 확인합니다. 트랙볼을 사용하여 도플러 흐름을 명확하게 볼 수 있는 신장 중앙의 피질 수질 접합부에 있는 동맥 위에 커서를 놓습니다.
- 커서 각도를 조정하고 PW 버튼을 누릅니다. 필요한 경우 활성 모드에서 신호 진폭과 대비를 조정합니다. 이미지를 저장합니다.
- 이후 측정에 필요한 충분한 정맥 신호(즉, y축의 음의 절반에서 볼 수 있는 흐름)가 있는지 확인합니다. 그렇지 않은 경우 3.4.5단계를 반복하고 정맥류가 보이는 중간의 피질 골수 접합부의 정맥 위에 커서를 놓습니다. 이미지를 저장합니다.
- 모든 이미징이 완료되면 모든 케이블을 분리하고, 환자와 트랜스듀서에서 여분의 젤을 닦아내고, 환자를 치료하거나 덮고, 초음파 승인 소독 물티슈로 트랜스듀서를 청소합니다.
4. 임상검사 3, 4
메모: 3차 및 4차 임상 검사는 환자가 아직 ICU에 있는 경우(즉, 사망 또는 병동으로의 이송이 발생하지 않은 경우) 입원 후 3일과 5일에 실시합니다.
- 신체 검사
- 임상 검사 1에 설명된 단계에 따라 신체 검사를 수행합니다.
- 심장과 폐의 CCUS
- 3.3단계에 따라 심장과 폐의 초음파 검사를 실시합니다. LVOT는 정적 측정이므로 한 번만 획득하므로 임상 검사 3 및 4에 기록할 필요가 없습니다.
- IVC와 신장의 CCUS
- 3.4단계에 따라 IVC와 신장의 초음파 검사를 실시합니다. 신장 길이는 정적 측정이므로 한 번만 구해야 하므로 임상 검사 3 및 4에 기록할 필요가 없습니다.
5. 초음파 검사의 측정 및 분석
메모: 임상 검사 중에 저장된 이미지는 각 검사 후 원하는 변수를 측정하는 데 사용됩니다. 측정된 값은 CRF에 등록되고 온라인 임상 환자 데이터 관리 시스템에 전사됩니다. 측정이 수행되고 표시되는 이미지도 나중에 검증에 사용될 원본 이미지와 함께 저장해야 합니다.
- LVOT 측정
- Probe 버튼을 클릭하여 심장 변환기를 선택하여 측정을 시작합니다.
- 3.3.5단계에서 저장한 이미지를 사용하여 밸브가 완전히 열렸을 때 이미지를 일시 중지합니다.
- 측정 버튼을 클릭한 다음 오른쪽 메뉴에서 Cardiac-Dimension-LVOT 옵션을 선택하여 측정을 시작합니다.
- 커서가 나타나면 대동맥 판막 기저부에 있는 두 지점을 선택하는데, 이완말기 동안 내강에서 내강 가장자리까지 내강의 각 측면에 하나씩 있습니다. 이미지를 저장합니다.
알림: LVOT 측정은 CO 측정 전에 수행하고 저장해야 기계가 자동으로 결정할 수 있습니다.
- CO 측정
- 3.3.10단계에서 저장한 이미지를 사용하여 좌심실 출력량을 추적합니다. 수평 스윕을 100cm/s로 조정합니다.
- ECG와 정렬되는 명확한 경계가 있는 잘 형성된 속이 빈 세 개의 파를 선택합니다. 측정 버튼을 클릭하고 트랙볼을 사용하여 Cardiac-Aortic-LVOT Trace 옵션을 선택합니다.
- 기준선에서 시작하고 끝나는 파형 라인을 추적하면 초음파 기계가 자동으로 CO를 계산합니다. 세 개의 파동에 대해 이 작업을 반복하고 이 이미지를 저장합니다.
메모: 불규칙한 리듬의 경우 5개의 파동에 대해 얻은 평균 CO 값을 기록하십시오.
- 탭스
- 3.3.7단계에서 저장한 M-mode 이미지를 이용하여 Measure 버튼을 클릭하고, 트랙볼을 이용하여 우측 메뉴에서 Cardiac-Dimension-TAPSE 옵션을 선택합니다.
- 커서를 먼저 잘 정의된 부비동 파동의 가장 낮은 지점에 놓은 다음 가장 높은 지점에 놓습니다. 둘(TAPSE)의 차이점이 화면 왼쪽 상단 모서리에 나타나야 합니다. 세 번의 부비동 파동에서 이 작업을 수행하고 세 번의 TAPSE 측정의 평균을 취합니다. 이미지를 저장합니다.
- 우심실 수축기 이탈(RV S')
- 3.3.8단계에서 저장한 이미지를 사용하여 캘리퍼 버튼을 클릭하고 잘 정의된 곡선의 가장 높은 봉우리에 커서를 놓습니다. 세 개의 곡선으로 이 작업을 수행하고 평균을 취합니다. 이미지를 저장합니다.
- Kerley B-line 아티팩트 평가
참고: 정상적인 폐 표면을 나타내는 수평 A-라인은 B-라인 감지에 참조로 사용할 수 있습니다. 이들은 흉막에서 발생하며 A-라인에 비해 과반향입니다.- 이미지 및/또는 게인의 대비를 조정합니다. B-라인이 저장된 이미지에서 항상 즉시 표시되는 것은 아닙니다.
- 얻은 6개의 이미지 각각에 대한 Kerley B-lines의 수를 결정하고 등록합니다. B-라인의 수는 기계에 저장되지 않기 때문에 즉시 CRF에 등록해야 합니다(0에서 5 사이).
- IVC 직경 및 접이식
- Probe 버튼을 클릭하여 복부 변환기를 선택하여 측정을 시작합니다.
- 3.4.2단계에서 저장한 2D 이미지를 사용하여 캘리퍼 버튼을 클릭하고 IVC가 우심방으로 들어가는 위치에서 2cm 떨어진 곳에서 IVC의 두 벽 사이의 거리를 측정합니다. 이것이 IVC 직경입니다. 이 이미지를 저장하십시오.
- 3.4.3단계에서 저장한 M-모드 이미지를 사용하여 캘리퍼 버튼을 클릭하고 IVC 호기 직경과 흡기 직경을 측정합니다. 이 이미지를 저장합니다.
메모: IVC의 호기 직경과 흡기 직경은 각각 M 모드 이미지에서 볼 수 있는 최대 및 최소 직경입니다.
- 신장 길이와 혈류
- 3.4.4.4단계에서 저장한 2D 이미지를 이용하여 Caliper 버튼을 클릭하여 신장 피질의 꼬리에서 두개골 끝까지 가장 긴 선을 그립니다. 이것은 신장 길이(cm)이며, 이 결과를 CRF에 등록하십시오. 이 이미지를 저장합니다.
- 3.4.6단계에서 저장한 도플러 이미지를 사용하여 기준선 아래에서 보이는 정맥 유동선을 연속, 단상 또는 이위상으로 분석합니다. CRF에 결과를 등록합니다.
- 3.4.6단계에서 저장한 이미지를 이용하여 측정 버튼을 클릭하고 트랙볼을 이용하여 우측 메뉴에서 Abdominal-Renal-PS/ED/RI 옵션을 선택합니다.
- 커서를 y축의 양의 절반에 있는 pulsatile flow wave의 가장 낮은 지점과 최고점에 놓습니다.
메모: G6 기계는 연속 박동 유동이 저장된 경우 다음 공식을 사용하여 도플러 신장 저항 지수(RRI)를 자동으로 계산할 수 있습니다: RRI = (최대 수축기 속도 - 끝 이완기 속도)/최대 수축기 속도. 초음파 기계에서 측정한 내용과 함께 이미지를 화면에 저장합니다. - 3.4.6단계 또는 3.4.7단계에서 저장한 이미지를 사용하여 캘리퍼 버튼을 클릭하고 커서를 먼저 최대 유속 위에 놓은 다음 천저(즉, 끝 이완기)19에서 최대 유속 위에 놓습니다. 측정 후 이미지를 저장하십시오.
메모: 정맥 임피던스 지수(VII)는 VII = (최대 수축기 속도 - 끝 이완기 속도) / 최대 수축기 속도20,21로 계산됩니다. VII는 단상 흐름의 경우 하나의 피크만 보이고 이완기 및 수축기 위상을 구별할 수 없기 때문에 등록되지 않습니다.
6. 초음파 이미지의 데이터 등록, 저장 및 검증
메모: 그림 1 에서 볼 수 있듯이 데이터 등록은 각 임상 검사 후에 수행됩니다. 아래에서는 전자 건강 기록에서 검색된 측정, 임상 검사 및 생화학 정보(표 2)에서 얻은 데이터를 연구 대상자의 익명화된 온라인 파일에 입력하는 절차를 설명합니다.
- 온라인 보안 환자 관리 시스템에 액세스하고 최근에 포함된 환자의 서류를 엽니다. 혈액 가스 분석 값, 일반 혈청 변수, 혈청 신장 변수 및 24시간 소변 분석을 등록합니다. 얻은 모든 변수의 목록과 이를 수행하기 위한 지침은 표 2에 나와 있습니다.
- 심장 CCUS 이미지를 검증합니다.
참고: 이 검증은 EACVI 지침22에 따라 심혈관 영상 코어 실험실의 독립적인 전문가가 수행합니다. 학생-연구원이 얻은 이미지의 품질을 평가하고 수행된 측정을 반복하여 필요한 치수 측정 및 속도 프로파일 추적을 보장합니다.- 대동맥 판막 바로 아래의 ECG 신호에서 볼 수 있듯이 이완말부에서 LVOT 측정을 수행합니다.
- AP5CH 보기에서 LVOT에서 가져온 PW 신호를 추적하여 좌심실 뇌졸중 용적과 좌심실 CO를 얻습니다.
- IVC 및 신장의 모든 이미지와 측정값을 검증합니다. 이 검사는 경험이 풍부한 독립적인 복부 방사선 전문의가 수행해야 합니다. 임상 검사 중 원하는 이미지를 얻는 데 문제가 있는 경우 독립적인 복부 방사선 전문의를 불러 CCUS를 수행할 수 있으며, 이 경우 추가 검증은 수행되지 않습니다.
7. 환자 후속 조치
- 정보에 입각한 동의 등록
- 임상 검사 중 또는 임상 검사 프로토콜이 완료된 후 환자 또는 가족의 동의를 얻었지만 환자가 여전히 병원에 입원한 경우 환자 데이터 관리 시스템에 이를 등록하고 직접 서명한 동의서를 업로드하십시오.
- 동의가 거부된 경우, 동의를 얻지 못한 이유와 함께 환자 데이터 관리 시스템에 이를 등록하고 연구 코디네이터에게 알리면 코디네이터는 모든 환자 데이터를 삭제할 것입니다.
- 사망률 데이터
- 입원 중 사망한 환자의 경우 전자 환자 기록에서 직접 사망률 및 관련 사망 원인을 등록합니다.
- 병원 내 사망률이 없는 환자의 경우, 90일마다 업데이트되는 네덜란드 시 등록부에서 사망률 데이터를 얻습니다.
결과
이러한 대표적인 결과의 목적은 프로토콜의 타당성을 설명하는 것입니다.
환자
2018년 5월 14일부터 2018년 8월 15일까지 총 663명의 환자가 중환자실에 입원했습니다. 이 중 208명의 환자가 포함 대상이었습니다(제외 이유는 그림 4에 나와 있음). 49명의 환자는 지속적인 소생술 노력으로 인해 CCUS를 수행할 가능성이 없어 제외되었습니다. 7명의 환자가 참여를 거부했고(사전 동의 없음) 4명의 환자에서는 기계 환기를 위한 엎드린 자세 또는 큰 상처의 진공 보조 봉합으로 인해 CCUS가 불가능하여 138명의 환자가 분석을 위한 데이터를 포함했습니다.
CCUS 검증 및 이미지 품질
심장 영상에 대한 광범위한 검증이 계획되어 있습니다. 신장 초음파 검사가 시작되었습니다. 지금까지 21명(15%)의 환자의 이미지가 검증되었습니다. 18명의 환자(86%)에서 영상은 충분한 품질로 나타났습니다. 이미지에 대한 모든 불승인 사유를 나열하고 초음파를 수행한 연구자에게 피드백을 주기 위해 반환했습니다. 초음파 검사를 수행한 연구자의 이름은 ICC(Intraclass Correlation Coefficient)를 사용하여 관찰자 간 및 관찰자 내 변동성을 평가할 수 있도록 기록됩니다. 정확한 통계적 방법은 SICS-I12에서 수행된 것처럼 통계 분석 계획에 설명되어 있습니다.
예시 사례: 환자 X, 중년 여성
환자 X는 의식 장애와 저혈압으로 발견된 후 입원했습니다. 얻어진 모든 측정값은 표 1에 나와 있습니다. 모든 변수는 데이터 누락 없이 필요한 시간 세트 내에서 얻어졌으며, 이는 이 프로토콜의 가능한 타당성을 보여줍니다. 입원 후 3시간 이내에 첫 번째 임상 검사가 수행되었습니다. 이 검사에서 환자는 진정제와 삽관을 하고 승압제 치료가 필요했습니다. 두 번째 임상 검사는 10시간 후에 수행되었으며 700mL의 수액 주입 후 안정적인 활력을 보여주었습니다. 승압제가 감소했다. CCUS 및 생화학 분석은 정상적인 심장, IVC 및 신장 기능을 보여주었습니다(그림 5, 그림 6 및 그림 7). 이틀 후 T3에서 승압제는 중단되었지만 누적 양성 유체 균형은 6리터로 증가했으며, CO 증가, IVC 확대, 혈청 크레아티닌 증가에 따른 신장 관류 및 기능 감소가 동반되었습니다. 입원 5일 후인 T4에서는 체액 균형과 혈청 크레아티닌이 훨씬 더 증가하여 환자는 3기 AKI로 발전했습니다. 환자는 출처가 불분명한 다발장기 부전으로 인해 입원 후 7일 만에 2일 후 사망했습니다.
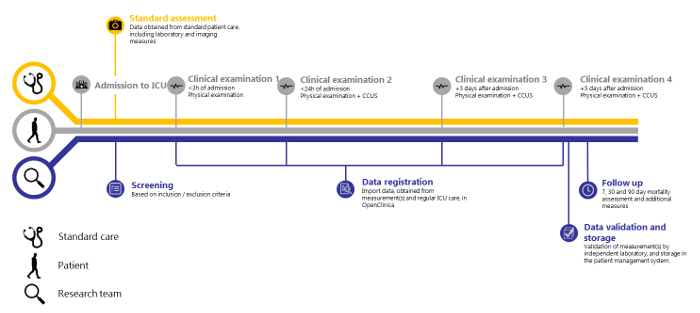
그림 1: SICS-II 연구 개요. 환자 입원부터 집중 치료실, 데이터 등록의 최종 단계까지 SICS-II 연구의 타임라인. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 2: 임상 검사를 위한 사례 보고서 양식(CRF) 1. CRF는 첫 번째 임상 검사를 수행할 때 ICU 팀 학생 또는 학생 연구원이 채웁니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 3: 임상 검사 2, 3 및 4에 대한 사례 보고서 양식(CRF). CRF는 2차, 3차 및 4차 임상 검사를 수행할 때 ICU 팀 학생 또는 학생 연구원이 채웁니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
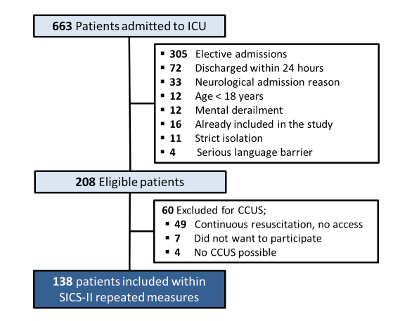
그림 4: SICS-II 환자 포함 및 제외 차트. 2018년 8월 15일까지 SICS-II 연구에서 환자 포함 및 제외 기준을 설명하는 순서도. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
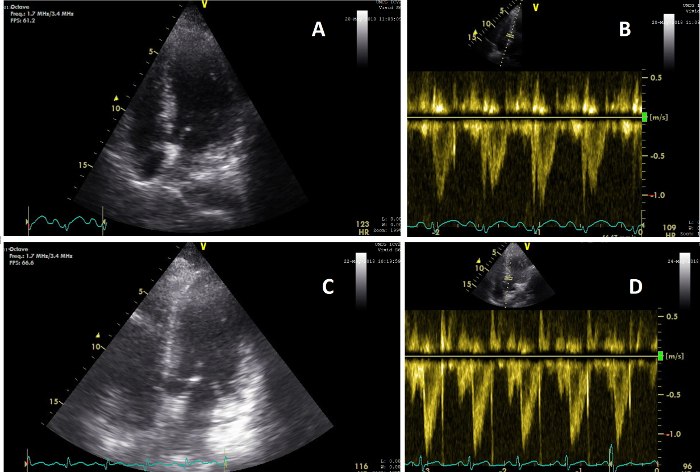
그림 5: 심장 기능의 변화를 보여주는 정점 모습. (A) 임상 검사 2 중 수행된 CCUS 중 AP4CH 뷰의 심장 이미지(T=2); (B) 5.6 L/min의 CO를 보여주는 T=2의 심장 VTI 맥파 신호 이미지; (C) 임상 검사 3 중 수행된 CCUS 중 AP5CH 보기에서 심장 이미지(T=3); (D) 8.3 L/min의 CO를 보여주는 T=3의 심장 VTI 맥파 신호 이미지. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
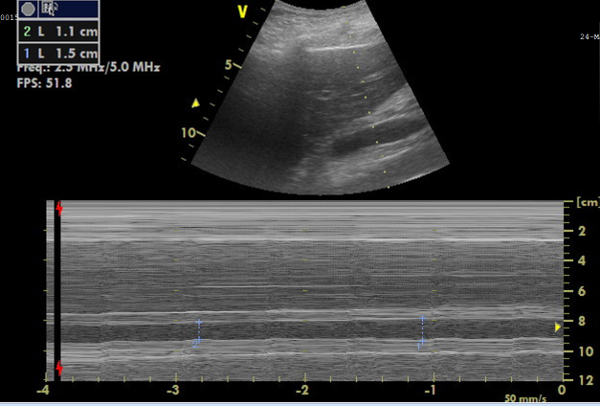
그림 6: 직경 측정을 위한 하대정맥(IVC)의 M 모드 이미지. 위에는 IVC를 실시간으로 보여주고, 아래에는 IVC 직경 변화를 나타내는 M-모드 이미지로, 접힘을 계산할 수 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
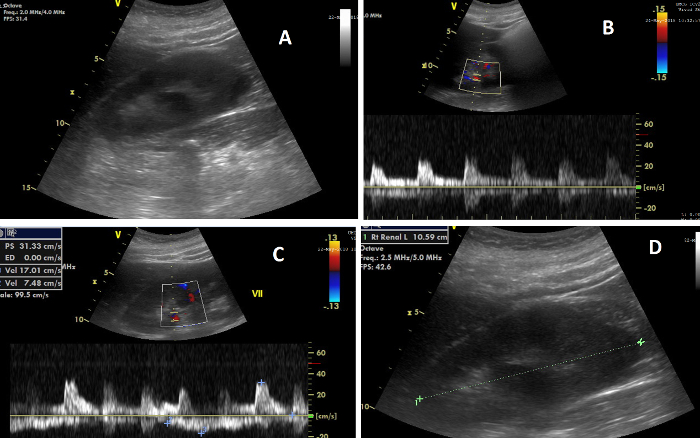
그림 7: 신장 초음파검사의 다양한 요소. (A) CCUS 중 오른쪽 신장의 이미지; (B) 위에는 신장 동맥의 도플러 흐름을 보여주고, 아래에는 신장 저항 지수가 계산되는 유동파를 보여주는 이미지; (C) 위에는 신장 정맥의 도플러 흐름을 보여주고, 아래에는 정맥 임피던스 지수가 계산되는 유동파를 보여주는 이미지; (D) 신장 길이의 측정을 보여주는 이미지. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
| 변수 | 티1 1일차 00:38 | 티2 1일차 10:53 | 티3 3일차 10:14 | 티4 5일차 10:20 |
| 심박수(bpm) | 110 | 124 | 122 | 98 |
| 호흡수(분당 호흡수) | 24 | 15 | 26 | 12 |
| 수축기 혈압(mmhg) | 100 | 115 | 130 | 118 |
| 이완기 혈압(mmhg) | 61 | 69 | 66 | 65 |
| 평균 동맥압(mmhg) | 73 | 80 | 84 | 81 |
| 누적 유체 균형 (mL) | 0 | 704 | 7272 | 12338 |
| 기계적 환기 | 핍 5, FiO2 40% | 핍 5, FiO2 40% | 핍 5, FiO2 30% | 핍 5, FiO2 30% |
| CRT 흉골 (초) | 1.5 | 2 | 4 | 3 |
| 중심 온도(◦ C) | 37.6 | 37.5 | 38.0 | 37.4 |
| 비뇨기 배출 이전 시간(mL) | 117 | 60 | 0 | 10 |
| 투여된 수축성 제제 | 노르아드레날린 0.1 밀리그램 / 밀리람베르트 3.0 ml/h | 노르아드레날린 0.1 밀리그램 / 밀리람베르트 1.0 ml/h | 없음 | 없음 |
| 진정제 투여 | 프로포폴 20 밀리그램 / 밀리람베르트 5.0 ml/h | 없음 | 없음 | 없음 |
| APACHE IV 점수 | 92 | 88 | 87 | 90 |
| SOFA 스코어 | 8 | 8 | 5 | 8 |
| LVOT (cm) | 해당 없음 | 2.4 | 2.4 | 2.4 |
| 심박출량(L/min) | 해당 없음 | 5.6 | 8.34 | 9.89 |
| 탭스(mm) | 해당 없음 | 25 | 26 | 21 |
| RV S'(cm/s) | 해당 없음 | 14 | 15 | 12 |
| IVC 흡기 직경(cm) | 해당 없음 | 1.14 | 1.24 | 1.10 |
| IVC 호기 직경(cm) | 해당 없음 | 1.27 | 1.38 | 1.50 |
| Kerley B 라인(총) | 해당 없음 | 6 | 2 | 4 |
| 신장 길이 (cm) | 해당 없음 | 10.59 | 해당 없음 | 해당 없음 |
| 신장 내 정맥 흐름 패턴 | 해당 없음 | 지속적 | 지속적 | 지속적 |
| 도플러 신장 RI | 해당 없음 | 0.61 | 0.75 | 0.70 |
| 제7장 | 해당 없음 | 0.33 | 0.56 | 0.68 |
표 1: 무작위 SICS-II 환자. 환자 X는 중년 여성으로, 의식 장애가 있는 상태로 발견되어 중환자실에 입원했습니다. 약어: bpm = 분당 박동수, CRT = 모세혈관 리필 시간, LVOT = 좌심실 유출로, TAPSE = 삼첨판 환상 수축기 이탈, RV S' = 우심실 수축기 이탈, IVC = 하대정맥 이탈, RRI = 신장 저항 지수, VII = 정맥 임피던스 지수, N.A. = 해당 없음.
| 변수 | 단위 | 근원 | 에서 획득 |
| 젖산염 | mmol/L | 동맥혈 가스 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 염화물 | mmol/L | 동맥혈 가스 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 산도 | 동맥혈 가스 분석 | 표준 치료에서 각 임상 검사도 가능한 한 가깝게 최대 12 호 차이 | |
| PCO2 | 킬로파(kPa) | 동맥혈 가스 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 파오2 | 킬로파(kPa) | 동맥혈 가스 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| HCO3- | mmol/L | 동맥혈 가스 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 헤모글로빈 | mmol/L | 동맥혈 가스 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 백혈구 | 10 x 10-9/L | 혈청 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 트롬보사이트 | 10 x 10-9/L | 혈청 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| HS 트로포닌 | NG/L | 혈청 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 아사트 | U/L | 혈청 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 알라트 | U/L | 혈청 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 총 빌리루빈 | uoml/L | 혈청 분석 | 표준 진료에서 각 임상 검사마다 가능한 한 가깝게 최대 12 시간 차이 |
| 크레아티닌 | 우몰/L | 혈청 분석 | ICU 입원 시작부터 모든 측정 |
| 소변량 | 밀리리터 | 24 시간의 소변 수집 | ICU 입원 시작부터 모든 측정 |
| 크레아티닌 | mmol/24시간 | 소변 분석 | ICU 입원 시작부터 모든 측정 |
표 2: 얻은 생화학적 변수 목록. 연구 중에 수집된 모든 환자 생화학적 변수가 여기에 나열되어 있습니다.
토론
모든 검사는 프로토콜에 따라 수행되어야 합니다. 신체 검사는 미리 지정된 정의에 따라 수행되는 경우에만 가치가 있습니다23. 모든 값을 얻기 위해 프로토콜에 따라 실험실 값을 수집해야 합니다. 명확하고 해석 가능한 CCUS 이미지는 3.3단계에서 설명한 바와 같이 이 연구의 연구 질문에 답하는 데 중요합니다. 품질이 낮은 이미지를 얻으면 5단계에서 설명한 측정 및 분석을 수행할 수 없으며 반복 측정의 목적이 만료됩니다. 저화질 이미지를 얻을 위험을 최소화하기 위해 세 가지 중요한 조치가 취해집니다. 첫째, 본 연구에서 CCUS를 수행하는 학생-연구원은 경험이 풍부한 심장 전문의-집중 전문의의 교육을 받습니다. 문헌에 따르면 단기 교육 프로그램은 CCUS24의 기본 역량을 습득하는 데 매우 적합하다. 둘째, 학생 연구자는 처음 20개의 시험 동안 선임 학생 연구원의 감독을 받아 직접 피드백을 받을 수 있습니다. 마지막으로, 획득한 모든 심장 및 신장 이미지는 데이터의 신뢰성을 보장하기 위해 각각 Cardiac Imaging Core Laboratory의 독립적인 전문가와 숙련된 복부 방사선 전문의에 의해 재평가 및 검증됩니다.
이미지 품질을 보장하기 위해 연구자들은 다른 측면에도 주의를 기울여야 합니다. 최적의 이미지 품질을 보장하기 위해 초음파 젤을 다시 바르거나 프로브의 위치를 변경하여 환자의 피부에 더 잘 닿도록 해야 하는 경우가 있습니다. 또한 최적의 이미지를 얻기 위해 충분한 시간을 할애하는 것이 중요하며, 의심이 가는 경우 임상 검사가 완료되기 전에 선임 연구원, 즉 감독 심장 전문의-집중 치료사 또는 핵심 실험실 기술자와 상담해야 합니다. 모든 초음파 이미지의 지속적인 평가 및 검증은 그림 1에 표시된 프로토콜화된 단계를 적용하여 보장됩니다. 또한 학생-연구원 및 전문가가 자주 피드백을 교환하여 프로토콜 변경을 신속하게 구현하여 이미지 및 측정의 품질을 더욱 높일 수 있습니다. 이러한 잦은 검증을 통해 체계적인 오류를 쉽게 감지할 수 있으므로 미래의 학생-연구자를 위한 CCUS 교육이 그에 따라 조정될 수 있습니다. 또한 모든 팀 구성원에게 공개되는 월간 회의를 통해 프로토콜의 철저한 평가와 (필요한 경우) 수정이 가능합니다.
환자 선별 검사 및 포함을 위한 연중무휴 가용성은 이 연구의 성공적인 구현을 위한 또 다른 핵심 요소입니다. 이는 학생 연구자로 구성된 전담 팀, 지원을 제공할 대규모 학생 팀, ICU 간병인과의 긴밀한 협력을 통해서만 달성할 수 있습니다. 이러한 조정은 표준 치료와의 협업을 최적화하기 위해 가능한 개선 사항에 대해 간병인과 연구자 간의 정기적인 저위험 접촉을 통해 이루어집니다.
이 프로토콜의 한계는 CCUS를 성공적으로 수행하는 것이 프로브가 배치되는 사전 지정된 위치의 접근성에 달려 있다는 것입니다. SICS-I 검사 기간 동안, 이론적으로 최적의 심초음파창을 막는 배액관, 거즈 또는 상처 드레싱이 필요한 환자의 경우 심장 CCUS를 수행할 수 없다는 것이 이미 밝혀졌습니다1. 또한, IVC 측정에 필요한 경흉부 심장초음파를 통해 적절한 늑골하 창을 얻을 수 있는 가능성은 이전에 일반 중환자실 인구에서 잠재적으로 제한적인 것으로 나타났습니다25. 이 프로토콜이 서로 다른 시점에서 다른 검사를 수행하는 데 필요한 24/7 가용성은 일부 센터가 그렇게 할 수 있는 능력이 부족할 수 있기 때문에 잠재적인 제한 사항이기도 합니다. UMCG와 같은 대형 학술 병원에서조차도 이를 보장함으로써 연구 시작이 지연되었습니다. 초음파 측정에 내재된 또 다른 한계는 측정의 관찰자 간 변동성입니다. 환자 포함이 연중무휴(24/7)로 보장되기 위해서는 한 명의 연구자가 포함된 모든 환자에 대해 모든 임상 검사를 수행하는 것은 불가능합니다. 본 연구는 개별 수준의 변동성을 최소화하기 위해 동일한 연구자가 한 명의 환자에서 모든 초음파 측정을 수행하는 것을 목표로 하지만, 전체 코호트에서 관찰자 간 변동성이 여전히 문제로 남아 있습니다.
여러 장기의 초음파 영상은 장기 관류 및 기능을 시각화하기 위한 빠르고 안전하며 효과적인 구조가 될 수 있습니다. 이는 모든 의료 전문가가 사용할 수 있어야 하는 편리한 도구이며, 일반적으로 간단하고 표준화된 프로토콜을 기반으로 하는 소수의 측정이 신뢰할 수 있는 측정을 제공해야 합니다.
또한, 초음파, 특히 심장초음파의 사용을 평가하는 대부분의 관찰 연구는 본질적으로 후향적이거나 소수의 환자만 포함합니다. 26 이 프로토콜은 선택되지 않은 중증 환자 코호트에 대한 구조적 24/7 스크리닝을 허용하며, 그 중 관심 하위 모집단을 정의할 수 있으므로 여러 연구 질문을 동시에 조사할 수 있습니다.
더욱이, 중환자 치료의 임상적 변수들이 매우 역동적이고 상호 영향을 미친다는 것이 알려져 있음에도 불구하고, 대부분의 연구는 특정 장기에 대한 단일 초음파 측정의 부가적 가치만을 조사했다27,28. 이것은 반복적인 측정, 전신 초음파 및 정맥 울혈에 초점을 맞춘 첫 번째 프로토콜입니다. 우리는 SICS-II가 ICU 입원 중 환자의 혈류역학적 상태를 보다 정확하게 반영할 것으로 기대합니다.
SICS에서 현재 사용되는 구조는 많은 설정에 적용될 수 있으며, 다른 요소의 추가는 현재 연구되고 있습니다. 그 강점은 새로운 연구 질문을 조사할 수 있도록 새로운 변수를 CRF에 쉽게 추가할 수 있는 기본 연구 라인과 적응형 라인의 조합에 있습니다. 이러한 적응성의 예로는 변형 영상, 즉 단기간에 대한 부담 을 통한 광범위한 심실 벽 평가를 특정 환자 하위 집합의 일반 프로토콜에 추가하는 것이 있습니다.
더욱이, 환자 참여는 현재 중환자실에서만 독점적으로 이루어지고 있으며 환자 치료 궤적의 일부는 이제 누락되었습니다. ICU 환자는 종종 응급실(ED)에 먼저 입원하고 ICU 퇴원 후 일반 병동에 머뭅니다. 따라서 SONICS는 응급실 도착 시 환자를 포함시켜 초기 입원부터 중재 및 혈류역학적 기능을 등록함으로써 초기 단계에 환자를 포함하는 것을 목표로 합니다. 또한, 중환자실 퇴원 후 일반 병동에서 CCUS를 실시하여 사전 정의된 각 연구 시간에 모든 환자를 측정할 수 있도록 하는 계획도 진행 중입니다. 또 다른 중요한 측면은 프로토콜이 다른 센터로 확장될 수 있다는 것입니다: 그 단순성으로 인해 스스로 포함을 시작할 수 있는 센터가 쉽게 적응할 수 있습니다.
마지막으로, 구조화된 CCUS 프로토콜의 개발 및 성공적인 구현은 임상적 영향을 미칠 수도 있습니다. 연구 목적으로만 사용되기는 하지만, 제안된 짧은 교육 기간 후에 의사에 의해 임상 CCUS에 구현될 수 있습니다. 그런 다음 (경험이 부족한) 의사에게 CCUS 교육을 촉진하는 것이 추가 진단 검사를 줄일 수 있는지 평가하는 것이 흥미로울 것입니다.
공개
저자는 공개할 것이 없습니다.
감사의 말
SICS-I에 참여하고 현재 프로토콜에 대한 브레인스토밍 세션에 참여한 SICS-Study 그룹의 모든 구성원에게 감사드립니다. 또한 중환자 치료과 연구실과 코디네이터의 지원에 감사드립니다. W. Dieperink 박사와 M. Onrust. 또한, 지금까지 환자를 SICS-II에 구조적으로 포함시켜 주신 ICU 학생팀과 학생 연구자들에게 감사드립니다. J. A. 드 브루인, B. E. Keuning, 박사 K. Selles.
자료
| Name | Company | Catalog Number | Comments |
| Ultrasound machine | GE Healthcare | 0144VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 3507VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 0630VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound gel | Parker | 01-08 | Aquasonic 100 ultrasound transmission gel |
| Temperature probe | DeRoyal | 81-010400EU | Skin Temperature Sensor |
참고문헌
- Hiemstra, B., et al. Clinical examination, critical care ultrasonography and outcomes in the critically ill: cohort profile of the Simple Intensive Care Studies-I. BMJ open. 7 (9), 017170 (2017).
- Lee, J., et al. Association between fluid balance and survival in critically ill patients. Journal of Internal Medicine. 277 (4), 468-477 (2015).
- Perner, A., et al. Fluid management in acute kidney injury. Intensive Care Medicine. 43 (6), 807-815 (2017).
- Balakumar, V., et al. Both Positive and Negative Fluid Balance May Be Associated With Reduced Long-Term Survival in the Critically Ill. Critical care medicine. 45 (8), 749-757 (2017).
- Hjortrup, P. B., et al. Restricting volumes of resuscitation fluid in adults with septic shock after initial management: the CLASSIC randomised, parallel-group, multicentre feasibility trial. Intensive Care Medicine. 42 (11), 1695-1705 (2016).
- Prowle, J. R., Kirwan, C. J., Bellomo, R. Fluid management for the prevention and attenuation of acute kidney injury. Nature reviews. Nephrology. 10 (1), 37-47 (2014).
- Gambardella, I., et al. Congestive kidney failure in cardiac surgery: the relationship between central venous pressure and acute kidney injury. Interactive CardioVascular and Thoracic Surgery. 23 (5), 800-805 (2016).
- Chen, K. P., et al. Peripheral Edema, Central Venous Pressure, and Risk of AKI in Critical Illness. Clinical journal of the American Society of Nephrology : CJASN. 11 (4), 602-608 (2016).
- Song, J., et al. Value of the combination of renal resistance index and central venous pressure in the early prediction of sepsis-induced acute kidney injury. Journal of critical care. 45, 204-208 (2018).
- Zhang, L., Chen, Z., Diao, Y., Yang, Y., Fu, P. Associations of fluid overload with mortality and kidney recovery in patients with acute kidney injury: A systematic review and meta-analysis. Journal of Critical Care. 30 (4), (2015).
- Simple Intensive Care Studies II - Full Text View. ClinicalTrials.gov Available from: https://clinicaltrials.gov/ct2/show/NCT03577405 (2018)
- Statistical analysis plan Simple Intensive Care Studies-I DETAILED STATISTICAL ANALYSIS PLAN (SAP) 1. Administrative information 1.1. Title, registration, versions and revisions. ClinicalTrials.gov Available from: https://clinicaltrials.gov/ProvidedDocs/24/NCT02912624/SAP_000.pdf (2018)
- Simple Observational Critical Care Studies - Full Text View - ClinicalTrials.gov. ClinicalTrials.gov Available from: https://clinicaltrials.gov/ct2/show/NCT03553069 (2018)
- Ait-Oufella, H., et al. Alteration of skin perfusion in mottling area during septic shock. Annals of Intensive Care. 3 (1), 31 (2013).
- Teasdale, G., Jennett, B. Assessment of Coma and Impaired Consciousness: A Practical Scale. The Lancet. 304 (7872), 81-84 (1974).
- Detsky, M. E., et al. Discriminative Accuracy of Physician and Nurse Predictions for Survival and Functional Outcomes 6 Months After an ICU Admission. JAMA. 317 (21), 2187 (2017).
- Lipson, A. R., Miano, S. J., Daly, B. J., Douglas, S. L. The Accuracy of Nurses' Predictions for Clinical Outcomes in the Chronically Critically Ill. Research & reviews. Journal of nursing and health sciences. 3 (2), 35-38 (2017).
- Lichtenstein, D. A. BLUE-protocol and FALLS-protocol: two applications of lung ultrasound in the critically ill. Chest. 147 (6), 1659-1670 (2015).
- Tang, W. H. W., Kitai, T. Intrarenal Venous Flow: A Window Into the Congestive Kidney Failure Phenotype of Heart Failure. JACC: Heart Failure. 4 (8), 683-686 (2016).
- Jeong, S. H., Jung, D. C., Kim, S. H., Kim, S. H. Renal venous doppler ultrasonography in normal subjects and patients with diabetic nephropathy: Value of venous impedance index measurements. Journal of Clinical Ultrasound. 39 (9), 512-518 (2011).
- Iida, N., et al. Clinical Implications of Intrarenal Hemodynamic Evaluation by Doppler Ultrasonography in Heart Failure. JACC: Heart Failure. 4 (8), 674-682 (2016).
- Lang, R. M., et al. Recommendations for Cardiac Chamber Quantification by Echocardiography in Adults: An Update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. European Heart Journal - Cardiovascular Imaging. 16 (3), 233-271 (2015).
- Hiemstra, B., Eck, R. J., Keus, F., van der Horst, I. C. C. Clinical examination for diagnosing circulatory shock. Current opinion in critical care. 23 (4), 293-301 (2017).
- Vignon, P., et al. Basic critical care echocardiography: validation of a curriculum dedicated to noncardiologist residents. Critical care medicine. 39 (4), 636-642 (2011).
- Jensen, M. B., Sloth, E., Larsen, K. M., Schmidt, M. B. Transthoracic echocardiography for cardiopulmonary monitoring in intensive care. European journal of anaesthesiology. 21 (9), 700-707 (2004).
- Koster, G., van der Horst, I. C. C. Critical care ultrasonography in circulatory shock. Current opinion in critical care. 23 (4), 326-333 (2017).
- Haitsma Mulier, J. L. G., et al. Renal resistive index as an early predictor and discriminator of acute kidney injury in critically ill patients; A prospective observational cohort study. PloS one. 13 (6), 0197967 (2018).
- Micek, S. T., et al. Fluid balance and cardiac function in septic shock as predictors of hospital mortality. Critical care. 17 (5), 246 (2013).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유