Method Article
Протокол обсервационного исследования для повторного клинического обследования и ультразвукового исследования в интенсивной терапии в рамках простых исследований интенсивной терапии
В этой статье
Резюме
Структурированные протоколы необходимы для получения ответов на исследовательские вопросы у пациентов в критическом состоянии. Простые исследования интенсивной терапии (SICS) обеспечивают инфраструктуру для повторных измерений у пациентов в критическом состоянии, включая клиническое обследование, биохимический анализ и ультразвуковое исследование. Проекты SICS имеют конкретную направленность, но их структура является гибкой для других исследований.
Аннотация
Продольная оценка пациентов в критическом состоянии с помощью комбинации клинического обследования, биохимического анализа и ультразвукового исследования в интенсивной терапии (УЗИ) может выявить нежелательные явления вмешательств, такие как перегрузка жидкостью, на ранней стадии. Simple Intensive Care Studies (SICS) — это исследовательская линия, направленная на прогностическую и диагностическую ценность комбинаций клинических переменных.
В исследовании SICS-I особое внимание уделялось использованию клинических переменных, полученных в течение 24 ч после острой госпитализации, для прогнозирования сердечного выброса (СО) и смертности. Его продолжение, SICS-II, фокусируется на повторных обследованиях во время поступления в отделение интенсивной терапии. Первое клиническое обследование обученными исследователями проводится в течение 3 часов после госпитализации, состоящее из физикального осмотра и обоснованных догадок. Второе клиническое обследование проводится в течение 24 часов после госпитализации и включает в себя физикальное обследование и обоснованное предположение, биохимический анализ и оценку CCUS сердца, легких, нижней полой вены (НПВ) и почек. Эту оценку повторяют на 3 и 5 день после госпитализации. Изображения CCUS проверяются независимым экспертом, а все данные регистрируются в защищенной онлайн-базе данных. Последующее наблюдение через 90 дней включает регистрацию осложнений и статуса выживаемости в соответствии с медицинскими картами пациента и регистром муниципальных лиц. Основным направлением SICS-II является связь между венозным застоем и дисфункцией органов.
Целью публикации данного протокола является предоставление подробной информации о структуре и методах данного продолжающегося проспективного обсервационного когортного исследования, позволяющего ответить на многочисленные исследовательские вопросы. Объяснен дизайн сбора данных комбинированного клинического обследования и оценки CCUS у пациентов в критическом состоянии. SICS-II открыт для участия других центров и открыт для других исследовательских вопросов, на которые можно ответить с помощью наших данных.
Введение
Пациенты, поступившие в отделение интенсивной терапии (ОИТ), являются наиболее тяжелобольными с высокими показателями сопутствующих и множественных заболеваний, независимо от их диагноза при поступлении. Таким образом, ОРИТ является местом для изучения ко- и мультиморбидности, их негативного влияния на исходы лечения пациентов и того, как критическое заболевание может привести к осложнениям, способствующим дополнительным мультиморбидам. Чтобы получить представление об этой разнородной группе пациентов, необходимо провести детальное обследование каждого отдельного пациента.
Исследовательская линия Simple Intensive Care Studies (SICS) разработана с целью оценки прогностической и диагностической ценности всестороннего набора клинических, гемодинамических и биохимических переменных у пациентов ОИТ, собранных специальной группой студентов-исследователей под руководством медицинских экспертов. Одной из основных целей исследования SICS-I является исследование комбинации результатов клинического обследования, наилучшим образом связанных с шоком, определяемым сердечным выбросом (CO), измеренным с помощью ультразвукового исследования интенсивной терапии (CCUS)1. SICS-II использует структуру SICS-I, но добавляет повторное клиническое обследование, биохимический анализ и CCUS. Основным направлением SICS-II является количественная оценка венозного застоя и определение переменных, которые могут способствовать его развитию. Повторные измерения дают динамическую информацию о течении болезни пациента. Исследования показывают, что перегрузка жидкостью присутствует у пациентов в критическом состоянии, а перегрузка жидкостью связана с новыми заболеваемостями. Таким образом, мы сосредоточимся на венозном застое у этих пациентов. Более того, несколько исследований предположили возможные негативные последствия чрезмерного введения жидкости 2,3,4,5,6. Перегрузка жидкостью может восприниматься как венозный застой или перегрузка венозной жидкостью, что может наблюдаться повышением центрального венозного давления (ЦВД) или периферическим отеком. Повышенное давление в центральной венозной системе может способствовать снижению перфузии органов с последующей органной недостаточностью, но точного определения венозного застоя не существует.
В предыдущих исследованиях, которые предполагали негативные эффекты, связанные с чрезмерным введением жидкости, использовались однократные суррогатные измерения венозного застоя, такие как CVP, сворачиваемость IVC, баланс жидкости и/или периферический отек 7,8,9,10. Насколько нам известно, SICS-II является первым исследованием, в котором были выполнены повторные CCUS нескольких органов в сочетании с результатами клинического обследования для оценки гемодинамического статуса пациентов ОИТ. Акцент на этом методе мультиорганной ультрасонографии важен, так как отказ органов или снижение функции органов всегда влияют на всю гемодинамическую систему. Мы ожидаем, что данные повторных обследований в СИХС-II помогут разгадать патофизиологию и последствия венозного застоя. Следовательно, это может помочь улучшить раннее выявление критически больных пациентов с риском венозного застоя и оптимизировать введение жидкости. Кроме того, можно изучить связь между венозным застоем и краткосрочной и долгосрочной органной недостаточностью. Наконец, успешная реализация протокола SICS-II сделает очевидным, что проведение крупного проспективного исследования с участием специальной группы студентов-исследователей возможно и может дать качественные данные для изучения клинических проблем.
Здесь демонстрируется методика проведения комплексного клинического обследования пациентов ОРИТ с целью измерения венозного застоя. Краткий протокол SICS-II был опубликован11 clinicaltrials.gov. После первого первичного клинического осмотра проводится не более трех дополнительных клинических обследований, биохимических анализов и CCUS. Физикальное обследование включает в себя переменные, отражающие периферическую перфузию/микроциркуляцию, такие как время наполнения капилляров (СРТ) или пятнистость, а также переменные макроциркуляции, такие как артериальное давление, частота сердечных сокращений и диурез. Кроме того, регистрируются стандартные лабораторные показатели лечения (например , лактат, pH). В последующем проводится ККУЗИ сердца, легких, НПВ и почек для получения информации о перфузии. Дальнейшие методы будут разработаны в рамках нашего плана статистического анализа, как это было сделано в SICS-I12.
На основании 138 пациентов, включенных в исследование в период с 14.05.2018 по 15.08.2018, повторные измерения широкого спектра клинических переменных в этой структуре представляются возможными. Мы также показываем, что независимая валидация возможна. SICS-II является примером ценной методологии, позволяющей исследователям точно регистрировать изменения в переменных, представляющих интерес, и, таким образом, может выступать в качестве руководства для проведения исследований, отражающих прогрессирование состояния пациентов, наблюдаемое в повседневной практике. Исследование SICS-II проводится ежедневно командой из 2-3 студентов-исследователей в любое время, а старший научный руководитель доступен по вызову. Эти студенты-исследователи обучены проведению физического осмотра и CCUS. Они выполняют все этапы данного протокола и отвечают за включение пациента как в рабочее время, так и в выходные дни. Кроме того, большая студенческая команда ОРИТ, состоящая из примерно 30 студентов, участвует в вечерних и ночных сменах для проведения первичного клинического осмотра (в течение 3 часов после поступления) новых пациентов. На рисунке 1 представлено схематическое резюме протокола исследования, а на рисунках 2 и 3 показаны формы описания клинического случая (CRF), используемые для регистрации данных при сборе.
протокол
Данное исследование проводится в соответствии с принципами Хельсинкской декларации (64-я версия, Бразилия 2013 г.) и в соответствии с Законом о медицинских исследованиях с участием человека (ВМО), руководящими принципами надлежащей клинической практики и местным институциональным наблюдательным советом (Medisch Ethische Toetsingscommissie; M18.228393).
1. Поступление пациента в отделение интенсивной терапии и скрининг
ЗАМЕТКА: Для скрининга цифровой список с минимальными данными о пациенте обновляется в течение дня, а включения и исключения регистрируются. Скрининговый лист хранится в защищенной электронной системе больницы с эксклюзивным доступом для исследователей. Чтобы защитить конфиденциальность пациентов, все физические копии списков уничтожаются в конце дня. Критерии включения: острая и незапланированная госпитализация; и пациенты старше 18 лет.
- Проверяйте систему ведения пациентов на предмет всех новых госпитализаций и проверяйте, соответствуют ли пациенты критериям включения.
- Немедленно исключите повторную госпитализацию, плановую госпитализацию, пациентов моложе 18 лет и тех, кто не сможет дать информированное согласие.
ЗАМЕТКА: Мы также исключили пациентов с нетравматической неврологической причиной госпитализации, поскольку мы установили несколько групп пациентов в SICS-I, в которых эта группа была гемодинамически стабильной, а госпитализация в ОРИТ касалась в основном неврологического лечения1. - Добавляйте возможные включения в постоянно обновляемый список пациентов. Используйте этот список для ежедневного планирования новых и повторных измерений в зависимости от времени поступления/включения.
2. Клиническое обследование 1
ЗАМЕТКА: Первое клиническое обследование проводится у всех пациентов, выполнивших критерии включения, в течение 3 ч после поступления. Это обследование проводится студентами-исследователями, если пациент поступает в дневную смену. Для пациентов, поступивших в вечернюю или ночную смену, это первое клиническое обследование проводится членом студенческой команды ОИТ, а данные обрабатываются и дорабатываются на следующий день студентами-исследователями. Полное описание протокола первого клинического осмотра см. в clinicaltrials.gov13. У постели больного, по возможности, пациента спрашивают, согласны ли они на клиническое обследование в данный момент. Письменное информированное согласие будет получено позже: инструкции см. в Шаге 1.2 и Шаге 7.
- Физикальное обследование
- Начните с обеспечения необходимых правил безопасности/изоляции для пациента: дезинфицируйте руки и запястья в соответствии со стандартными больничными процедурами 70% спиртом и используйте нестерильные перчатки и пластиковый фартук или дополнительные меры предосторожности, такие как изолирующий халат во время контакта с пациентом.
- Представьтесь и попросите у пациента разрешения на проведение обследования, если он не находится под действием седативных препаратов, находится в сознании и не адекватен. Объясните пациенту, что делается.
ЗАМЕТКА: Официальное информированное согласие запрашивается на более позднем этапе во время поступления в отделение интенсивной терапии или после выписки в палату либо от самого пациента, либо от ближайших родственников, если пациент не в состоянии это сделать. Более подробно это описано в шаге 7. - Зарегистрируйте гемодинамические переменные частоту сердечных сокращений, частоту дыхания, систолическое артериальное давление (САД), диастолическое артериальное давление (ДАД), среднее артериальное давление (MAP) и центральное венозное давление (ЦВД) с прикроватного монитора.
- Зарегистрируйте сатурацию кислорода (SpO2) и то, получает ли пациент неинвазивную респираторную поддержку или находится на искусственной вентиляции легких. Если это так, зарегистрируйте положительное конечное давление выдоха (PEEP) и долю вдыхаемого O2 (FiO2).
- Определяют реперфузию колена и грудины путем надавливания на 10 с на кожу и отпускания, затем отсчитывая количество секунд до полной реперфузии.
- Определите субъективную температуру кожи, пальпируя конечности руками, и оцените, холодные они или теплые.
- Запишите температуру мочевого пузыря с монитора, который показывает температуру, измеренную датчиком, прикрепленным к постоянному мочевому катетеру.
- Определите температуру кожи на тыльной стороне стопы, поместив дополнительный датчик температуры на середину спинки и подключив его к монитору. После этого измерения снова подключите датчик температуры мочевого пузыря к монитору.
- Оцените степень крапчатости, если она заметна, с помощью коленной шкалы Ait-Oufella14.
- Зарегистрируйте, получает ли пациент седативный препарат, и если да, то какой препарат, с какой скоростью помпы и в какой дозировке.
- Определение и регистрация шкалы комы Глазго (GCS) пациента15.
- Оцените выживаемость пациента в больнице, 6-месячную выживаемость и способность вернуться на свое первоначальное место жительства на основе обоснованного предположения и результатов этого клинического обследования16,17. Спросите у медсестры и врача их оценки и зарегистрируйте все оценки в ИРК.
3. Клинический осмотр 2
ЗАМЕТКА: Повторное клиническое обследование проводится в течение 24 часов после госпитализации и включает в себя измерения CCUS. Этот экзамен всегда проводится студентами-исследователями, прошедшими обучение в CCUS, а не членами студенческой команды ICU. Кроме того, у пациентов, которые соответствуют критериям включения и прошли клиническое обследование1, но позже выясняется, что они страдают исключительно неврологическим заболеванием (например, нетравматическим субарахноидальным кровоизлиянием), повторные измерения, включая CCUS, не проводятся, и в конечном итоге они исключаются.
- Получите информированное согласие.
ПРИМЕЧАНИЕ: В соответствии с правилами Университетской клиники Гронингена (UMCG) по наблюдательным измерениям, с 1 января 2016 года, ультразвуковые изображения, полученные во время клинического обследования, могут быть использованы без явного согласия. Тем не менее, политика исследования SICS-II заключается в том, чтобы получить информированное согласие пациентов как можно раньше, одновременно поддерживая принципы минимизации «стресса» для пациента, увеличения совместного принятия решений и предоставления пациенту достаточного времени для рассмотрения вопроса об участии. Поскольку большинство пациентов не могут дать согласие на раннем этапе пребывания в отделении интенсивной терапии, обычно получают «отсроченное» согласие. Если, наоборот, они смогут дать согласие или отказать в нем до или после проведения экспертиз, они либо не будут проведены, либо все уже полученные данные будут удалены, соответственно.- Перед началом обследования определите, находится ли пациент в сознании и способен ли он взаимодействовать со студентами-исследователями, определив его балл GCS. Предоставьте дееспособным пациентам объяснение относительно проводимого обследования и оставьте стандартное письменное письмо, которое они должны подписать.
- Если пациент не может получить согласие (из-за нарушения сознания, ограниченных умственных способностей и т. д.), ежедневно проверяйте его балл GCS и рассмотрите возможность получения согласия семьи, если члены семьи доступны, (как описано в шаге 7.1).
- Проведите физикальное обследование, следуя шагам, описанным для клинического осмотра 1.
- Проводят ККУЗИ сердца и легких.
ЗАМЕТКА: Данный протокол действителен при использовании ультразвукового аппарата в Таблица материалов, сердечный преобразователь для парастернального вида по длинной оси (PLAX) и сердечный преобразователь с фазированной решеткой для апикального четырех- и пятикамерного обзора (AP4CH, AP5CH). Для других ультразвуковых систем пользователям следует обратиться к руководствам по эксплуатации конкретного устройства.- Включите машину. Зарегистрируйте идентификатор анонимного исследования пациента, начните новое обследование и дождитесь, пока на экране отобразится автоматический режим 2D-визуализации.
- Если пациент одет, расстегните его халат, чтобы обнажить грудь. Разместите новые наклейки с электрокардиограммой (ЭКГ) и при необходимости подключите их к ультразвуковому аппарату.
- Подсоедините кабель ЭКГ от аппарата к прикроватному монитору пациента. Подождите, пока он стабилизируется и зарегистрируйте измеренную по ЭКГ частоту сердечных сокращений в CRF.
- По возможности расположите пациента слегка повернутым на левый бок. Это улучшает качество визуализации как сердца, так и почек.
ЗАМЕТКА: Технические соображения: Перед началом обследования нажмите кнопку «Настроить » и установите параметры изображения на пять сердечных циклов, глубину 10–15 см, ширину изображения 65° и частоту 1,7/3,4 МГц. Проверьте, правильно ли выбран зонд, нажав кнопку « Зонд ». - Нанесите достаточное количество геля для ультразвука на ультразвуковой датчик и поместите датчик слева от грудины, между 3-м и 5-м межреберьями, чтобы получить изображение PLAX в 2D-режиме. При необходимости отрегулируйте глубину для записи изображений для измерений выходного тракта левого желудочка и сохраните изображение.
ЗАМЕТКА: Максимальная ширина левого желудочка должна быть видна при максимальном открытии митрального клапана. Мышцы клапана не должны быть видны. Прежде чем поместить датчик на грудную клетку пациента, предупредите его о том, что гель холодный и может быть неприятным, а также что он почувствует некоторое давление (особенно в области грудины при записи изображений для выходного тракта левого желудочка (ЛЖТ). Имейте в виду, что у пациентов с реберными переломами следует избегать некоторых мест, так как это может быть неудобно для пациента). - В режиме 2D отрегулируйте глубину до 15–20 см, и поместите датчик над верхушкой сердца, каудально к левой ареоле. Получается вид AP4CH с четкой визуализацией всех четырех камер. Сохраните изображение.
- Перекатите трекбол так, чтобы курсор оказался на границе между трикуспидальным клапаном и стенкой правого желудочка, чтобы получить систолическую экскурсию трикуспидальной кольцевой плоскости (TAPSE). Нажмите кнопку M-Mode для получения правильного изображения и сохраните его, когда появятся определенные синусовые волны. Сохраните изображение.
- Наведите курсор на трехстворчатый клапан с трекболом. Уменьшите ширину изображения, чтобы увеличить количество кадров в секунду, необходимое для качества RV S. Нажмите сначала кнопку TVI , а затем кнопку PW , чтобы получить правильное изображение для RV S и сохранить его.
- С точки зрения AP4CH наклоните преобразователь вверх (т. е . выровняйте его), чтобы получить изображение AP5CH и отобразить корень аорты на экране. Сохраните изображение.
- Поместите курсор прямо над аортальным клапаном и нажмите кнопку PW, чтобы получить допплер пульсовой волны LVOT. Поместите курсор точно в то же место, где был измерен диаметр LVOT. Сохраните изображение с максимально высоким качеством (резкие границы доплеровских волн, полые с внутренней стороны и хорошо отличимые от ретроградного или митрального потока). Позже они будут использованы для вычисления интеграла скорости по времени (VTI), а затем CO.
ЗАМЕТКА: Всегда старайтесь получить по крайней мере три волны потока для каждого измерения. В случае нерегулярного ритма следует сохранить не менее пяти волн. - Приступайте к ультразвуковому исследованию легких с помощью того же сердечного датчика с фазированной решеткой и изменяя настройки на частоту 3,7 МГц, глубину до 15 см, и записывайте изображения только в течение 2 сердечных циклов. Разместите датчик в 6 разных местах, светом датчика в положении «12 часов», в соответствии с протоколом BLUE18. Убедитесь, что изображение всегда получено в одной и той же последовательности, чтобы избежать путаницы при просмотре изображений позже.
- Получите верхний передний среднеключичный вид легких, поместив датчик на межреберье2-го и3-го ребер с обеих сторон. Сохраните изображения для каждой стороны.
- Получите нижний передний среднеключичный вид легких, поместив датчик на 2-3 ребра ниже. Сохраните изображения для каждой стороны.
- Получите среднеосевой обзор легких, поместив датчик под подмышечные впадины пациента. Сохраните изображения для каждой стороны.
- После завершения визуализации сердца и легких сотрите излишки геля с грудной клетки пациента.
- Проводят ЦКУЗИ НПВ и почек.
- Нажмите кнопку « Зонд » и с помощью трекбола измените активный зонд на преобразователь с выпуклой/криволинейной решеткой (абдоминальный) для НПВ и исследования почек. Свет преобразователя, который может быть использован для ориентации, должен находиться в положении «12 часов» для обоих измерений.
- В 2D-режиме с настройками, установленными на глубину 10–20 см и частотой 2,5/5,0 МГц, поместите датчик чуть ниже мечевидного отростка и сместите его примерно на 2 см вправо от пациента. НПВ должен стать видимым. Сохраните изображение.
- Поместите курсор чуть выше верхней стенки IVC и за пределами просвета с помощью трекбола и нажмите кнопку M-Mode . Сохраните изображение.
- Для ультразвукового исследования почек начните с 2D-режима и отрегулируйте настройки на глубину 10–15 см и частоту 2,2/4,4 МГц. Расположите датчик дорсально и каудально от грудной клетки. Получите выбранный центр почки на изображении и сохраните его.
ЗАМЕТКА: Убедитесь, что датчик расположен как можно ближе к спине, чтобы отфильтровать ткани печени и петель кишечника. Для достоверного измерения длины почки границы почки должны быть четко видны, а расстояние между центральным синусовым комплексом (более эхогенным центром почки) и корой головного мозга должно быть одинаковым на всем изображении. - Нажмите кнопку «Цвет», чтобы получить цветное допплеровское изображение почки и определить кровоток в почечной сосудистой системе. Поместите курсор на любую артерию в кортикомедуллярном переходе в центре почки, где хорошо виден допплеровский кровоток с помощью трекбола.
- Отрегулируйте угол наклона курсора и нажмите кнопку PW . При необходимости отрегулируйте амплитуду сигнала и контрастность в активном режиме . Сохраните изображение.
- Определите, имеется ли также достаточный венозный сигнал (т.е. поток, видимый в отрицательной половине оси y), который необходим для последующих измерений. Если нет, повторите шаг 3.4.5 и наведите курсор на вену в кортикомедуллярном переходе посередине, где виден венозный поток. Сохраните изображение.
- После завершения визуализации отсоедините все кабели, сотрите излишки геля с пациента и датчика, оденьте или накройте пациента и очистите датчик дезинфицирующими салфетками, одобренными для ультразвука.
4. Клинические обследования 3 и 4
ЗАМЕТКА: Третье и четвертое клинические обследования проводятся на 3 и 5 день после поступления, если пациент все еще находится в отделении интенсивной терапии (т.е . смерть или перевод в палату не произошли).
- Физикальное обследование
- Проведите физикальное обследование, следуя шагам, описанным для клинического обследования 1.
- ККУЗИ сердца и легких
- Провести ультразвуковое исследование сердца и легких в соответствии с Шагом 3.3. Получите LVOT только один раз, так как это статическое измерение, и поэтому его не нужно регистрировать в клиническом обследовании 3 и 4.
- ЦКУЗ НПВ и почек
- Проводят ультразвуковое исследование НПВ и почек в соответствии с Шагом 3.4. Измеряйте длину почки только один раз, так как это статическое измерение, и поэтому его не нужно регистрировать в клиническом обследовании 3 и 4.
5. Измерения и анализ результатов ультразвуковых исследований
ЗАМЕТКА: Изображения, сохраненные во время клинического обследования, используются после каждого обследования для измерения желаемых переменных. Измеренные значения регистрируются в ИРК и транскрибируются в онлайн-систему управления клиническими данными о пациентах. Изображения, на которых выполнены измерения и которые видны, также должны быть сохранены в дополнение к исходным изображениям, которые впоследствии будут использоваться для проверки.
- Измерение LVOT
- Нажмите кнопку « Зонд », чтобы выбрать сердечный датчик и начать измерения.
- Используя изображение, сохраненное в шаге 3.3.5, приостановите изображение, когда клапаны будут полностью открыты.
- Нажмите кнопку «Измерить », а затем выберите параметры Cardiac-Dimension-LVOT в меню справа, чтобы начать измерение.
- Как только курсор появится, выберите две точки у основания аортального клапана, по одной с каждой стороны просвета, от внутреннего к внутреннему краю, во время конечной диастолы. Сохраните изображение.
ПРИМЕЧАНИЕ: Измерение LVOT должно быть выполнено и сохранено до измерения CO, чтобы машина могла автоматически определить его.
- Измерение CO
- Используя изображение, сохраненное в Шаге 3.3.10, проследите выход левого желудочка. Отрегулируйте горизонтальный стреловидный захват до 100 см/с.
- Выберите три полые волны правильной формы с четкими границами, которые совпадают с ЭКГ. Нажмите кнопку «Измерить » и с помощью трекбола выберите параметры кривой Cardiac-Aortic-LVOT .
- Проведите линию волны, начинающуюся и заканчивающуюся на базовой линии, и ультразвуковой аппарат автоматически рассчитает CO. Повторите это для трех волн и сохраните это изображение.
ЗАМЕТКА: В случае нерегулярного ритма запишите среднее значение CO, полученное за пять волн.
- ТАПСЕ
- Используя изображение в M-режиме, сохраненное на шаге 3.3.7, нажмите кнопку «Измерить » и используйте трекбол для выбора опций Cardiac-Dimension-TAPSE в меню справа.
- Поместите курсор сначала на самую низкую точку четко выраженной синусовой волны, а затем на самую высокую точку. Разница между ними (TAPSE) должна отображаться в верхнем левом углу экрана. Сделайте это в трех синусовых волнах и возьмите среднее значение трех измерений TAPSE. Сохраните изображение.
- Систолическое вмешательство правого желудочка (ПЖ S')
- Используя изображение, сохраненное на шаге 3.3.8, нажмите кнопку «Штангенциркуль » и поместите курсор на самый высокий пик четко определенной кривой. Делаем это в трех кривых и берем среднее значение. Сохраните изображение.
- Оценка артефактов B-линии Керли
ПРИМЕЧАНИЕ: Горизонтальные А-линии, представляющие нормальную поверхность легких, могут быть использованы в качестве эталонных при обнаружении В-линий. Они возникают из плевры и являются гиперэхогенными по сравнению с линиями А.- Отрегулируйте контрастность изображения и/или усиление. B-линии не всегда сразу видны на сохраненных изображениях.
- Определите и зарегистрируйте количество B-линий Керли для каждого из шести полученных изображений. Поскольку количество B-линий не сохраняется в машине, оно должно быть немедленно зарегистрировано в CRF (от 0 до 5).
- Диаметр и складность НПВ
- Нажмите кнопку « Зонд », чтобы выбрать датчик брюшной полости, чтобы начать измерения.
- Используя 2D-изображение, сохраненное в шаге 3.4.2, нажмите кнопку «Штангенциркуль » и измерьте расстояние между двумя стенками IVC на расстоянии 2 см от того места, где он входит в правое предсердие. Это диаметр IVC, сохраните это изображение.
- Используя изображение М-режима, сохраненное в шаге 3.4.3, нажмите кнопку «Штангенциркуль » и измерьте диаметры выдоха и вдоха IVC. Сохраните это изображение.
ЗАМЕТКА: Диаметры выдоха и вдоха НПВ являются максимальным и минимальным диаметрами, видимыми на изображении М-моды соответственно.
- Длина почек и кровоток
- Используя 2D-изображение, сохраненное в шаге 3.4.4, нажмите кнопку «Штангенциркуль » и нарисуйте самую длинную линию, проходящую от каудального до краниального концов почечной коры. Это длина почки в см, зарегистрируйте эту находку в ИРК. Сохраните это изображение.
- Используя допплеровское изображение, сохраненное на шаге 3.4.6, проанализируйте линию венозного кровотока, видимую ниже исходной линии, как непрерывную, монофазную или двухфазную. Зарегистрируйте результаты в ОФД.
- Используя изображение, сохраненное в шаге 3.4.6, нажмите кнопку «Измерить » и с помощью трекбола выберите параметры «Абдоминальный-Ренатальный-ПС/ЭД/РИ» в правом боковом меню.
- Поместите курсор на вершину и на самую низкую точку пульсирующей волны потока в положительной половине оси y.
ЗАМЕТКА: Аппарат G6 может автоматически рассчитать допплеровский индекс почечного сопротивления (RRI), если сохраняется непрерывная пульсирующая волна потока, используя формулу: RRI = (пиковая систолическая скорость — конечная диастолическая скорость)/пиковая систолическая скорость. Сохраните изображение с результатом измерения с ультразвукового аппарата на экране. - Используя изображение, сохраненное в шаге 3.4.6 или 3.4.7, нажмите кнопку «Штангенциркуль » и поместите курсор сначала на максимальную скорость потока, а затем на максимальную скорость потока в надире (т.е. в конце диастолического)19. Сохраните изображение после измерения.
ЗАМЕТКА: Индекс венозного импеданса (VII) рассчитывается по формуле: VII = (пиковая систолическая скорость — конечная диастолическая скорость) / пиковая систолическая скорость20,21. При монофазном потоке VII не регистрируется, так как в этом случае виден только один пик и диастолическая и систолическая фазы не различимы.
6. Регистрация, хранение и валидация данных ультразвуковых изображений
ЗАМЕТКА: Как показано на рисунке 1 , регистрация данных производится после каждого клинического обследования. Ниже описана процедура внесения данных, полученных в результате измерений, клинического обследования и биохимической информации (Таблица 2), извлеченной из электронной медицинской карты, в анонимизированный онлайн-файл субъекта исследования.
- Получите доступ к защищенной онлайн-системе управления пациентами и откройте досье недавно включенного пациента. Зарегистрируйте значения анализа газов крови, общие показатели сыворотки крови, сывороточные почечные показатели и анализ мочи за 24 часа. Список всех получаемых переменных и инструкции по их получению представлены в таблице 2.
- Проверьте изображения сердечного CCUS.
ПРИМЕЧАНИЕ: Эта валидация проводится независимыми экспертами Центральной лаборатории сердечно-сосудистой визуализации в соответствии с рекомендациями EACVI22. Качество изображений, полученных студентами-исследователями, оценивается и выполненные измерения повторяются для обеспечения требуемого качества размерных измерений и трассировки профилей скоростей.- Выполняйте измерения LVOT в конце диастолы, как видно на сигнале ЭКГ, непосредственно под аортальным клапаном.
- Отследите сигнал PW, полученный от LVOT, в проекции AP5CH, чтобы получить ударный объем левого желудочка и левый желудочковый CO.
- Подтвердите все изображения и измерения НПВ и почек. Это должен выполнять независимый опытный абдоминальный радиолог. В случае возникновения проблем с получением желаемых изображений во время клинического обследования, для проведения CCUS может быть вызван независимый абдоминальный радиолог, и в этом случае дальнейшая валидация не проводится.
7. Последующее наблюдение за пациентом
- Регистрация информированного согласия
- Если согласие пациента или его семьи получено во время любого из клинических обследований или после завершения протокола клинических обследований, но пациент все еще госпитализирован, зарегистрируйте его в системе управления данными пациента и загрузите подписанную от руки форму согласия.
- Если в согласии было отказано, зарегистрируйте это в системе управления данными пациента вместе с причиной неполучения согласия и сообщите об этом координатору исследования, который удалит все данные пациента.
- Данные о смертности
- Для пациентов, которые умирают во время госпитализации, регистрируйте смертность непосредственно из электронной карты пациента и связанной с ней причины смерти.
- Для пациентов без внутрибольничной смертности получите данные о смертности из муниципального реестра в Нидерландах, который обновляется каждые 90 дней.
Результаты
Цель этих репрезентативных результатов состоит в том, чтобы проиллюстрировать осуществимость протокола.
Пациентов
В период с 14-05-2018 по 15-08-2018 в отделение интенсивной терапии поступило 663 пациента. Из них 208 пациентов соответствовали критериям включения (причины исключения показаны на рисунке 4). Из группы было исключено 49 пациентов, так как из-за продолжающихся реанимационных мероприятий не было возможности провести ОКУС. Семь пациентов отказались от участия (без информированного согласия), а у четырех пациентов CCUS был невозможен, например, из-за положения лежа на животе для искусственной вентиляции легких или вакуумного закрытия больших ран, в результате чего 138 пациентов были включены с данными для анализа.
Валидация CCUS и качество изображения
Планируется обширная валидация визуализации сердца. Начата валидация ультразвукового исследования почек. На данный момент были проверены изображения 21 пациента (15%). У 18 пациентов (86%) снимки оказались достаточно качественными. Все причины неодобрения изображений были перечислены и возвращены для обратной связи исследователю, проводившему ультразвуковое исследование. Имя исследователя, проводившего ультразвуковое исследование, записывается для того, чтобы иметь возможность оценить меж- и внутринаблюдательную вариабельность с использованием внутриклассового коэффициента корреляции (ICC). Точные статистические методы будут описаны в нашем плане статистического анализа, как это было сделано в SICS-I12.
Пример из практики: Пациентка X, женщина среднего возраста
Пациентка Х была госпитализирована после того, как у нее было обнаружено нарушение сознания и низкое кровяное давление. Все полученные измерения приведены в таблице 1. Все переменные были получены в требуемое время без пропусков данных, что иллюстрирует возможную осуществимость данного протокола. В течение 3 часов после поступления был проведен первый клинический осмотр. Во время этого обследования пациенту была оказана седативная мера, интубирована и она нуждалась в вазопрессорном лечении. Второе клиническое обследование было проведено через десять часов и показало стабильные жизненные показатели после инфузии 700 мл жидкости. Вазопрессоры были снижены. ККУЗИ и биохимический анализ показали нормальную функцию сердца, НПВ и почек (Рисунок 5, Рисунок 6 и Рисунок 7). При Т3, через два дня, прием вазопрессоров был прекращен, но совокупный положительный баланс жидкости повысился до 6 литров, что сопровождалось повышенным угарным газом, расширением НПВ и снижением перфузии и функции почек, что отражалось на повышении креатинина сыворотки крови. При Т4, через 5 дней после госпитализации, баланс жидкости и креатинин сыворотки повысились еще больше, где у пациента развилось ОПП 3 стадии. Пациентка умерла через 2 дня из-за полиорганной недостаточности неясного происхождения, через 7 дней после поступления.
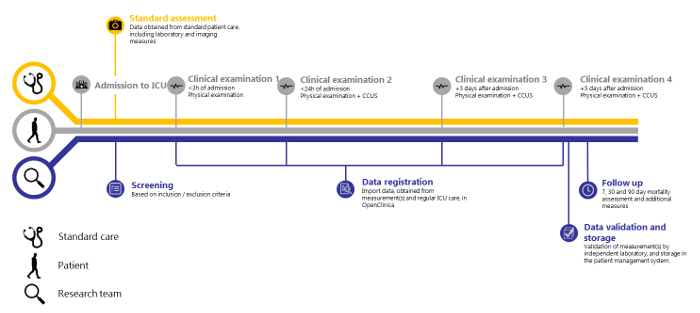
Рисунок 1: Обзор исследования SICS-II. Хронология исследования SICS-II от поступления пациента в отделение интенсивной терапии до финального этапа регистрации данных. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 2: Форма описания клинического случая (ОФК) для клинического обследования 1. ИРК заполняется студентами команды ОРИТ или студентами-исследователями при проведении первого клинического обследования. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 3: Форма описания клинического случая (CRF) для клинических обследований 2, 3 и 4. ИРК заполняется студентами команды ОРИТ или студентами-исследователями при проведении второго, третьего и четвертого клинических обследований. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
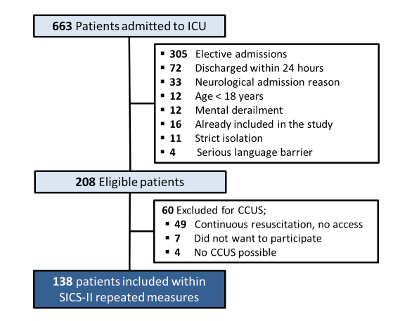
Рисунок 4: Таблица включения и исключения пациентов с SICS-II. Блок-схема с описанием критериев включения и исключения пациента из исследования SICS-II до 15.08.2018. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
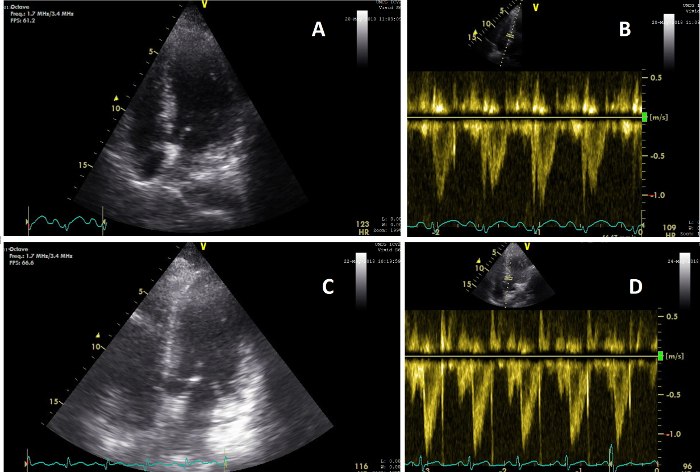
Рисунок 5: Апикальные изображения, показывающие изменение сердечной функции. (A) Изображение сердца на снимке AP4CH во время CCUS, проводимом во время клинического обследования 2 (T=2); (B) Изображение сигнала пульсовой волны сердца VTI на T=2, показывающее CO 5,6 л/мин; (C) Изображение сердца на снимке AP5CH во время CCUS, проводимом во время клинического обследования 3 (T=3); (D) Изображение сигнала пульсовой волны сердца VTI на T=3, показывающее CO 8,3 л/мин. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
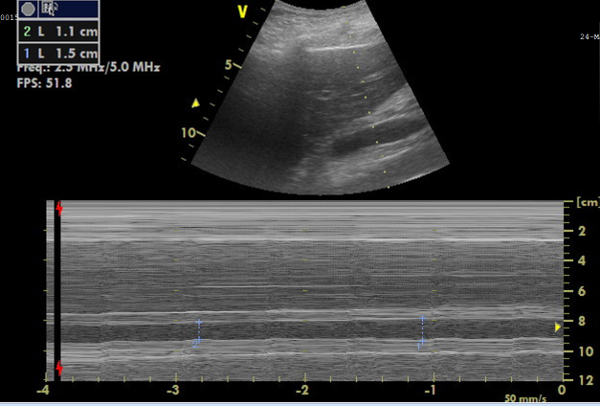
Иллюстрация 6: М-модное изображение нижней полой вены (НПВ) для измерения диаметра. Изображение, показывающее вверху IVC в режиме реального времени, а внизу изображение M-mode, представляющее изменения диаметра IVC, по которым можно рассчитать возможность сворачивания. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
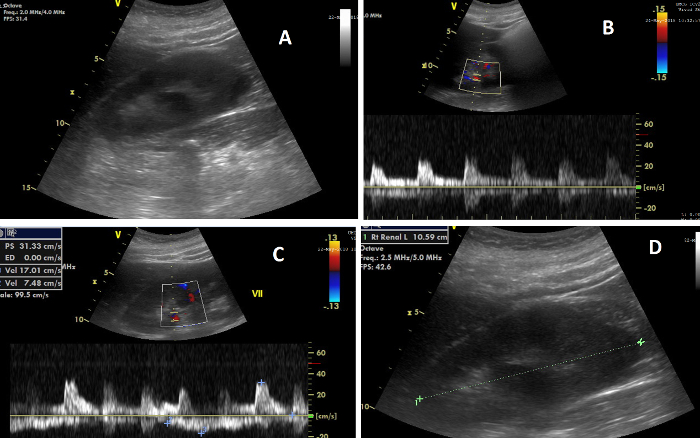
Рисунок 7: Различные элементы ультразвукового исследования почек. (А) Изображение правой почки во время ОКУИ; (В) Изображение, показывающее, вверху, допплеровский поток в почечных артериях, а внизу волну потока, из которой рассчитывается почечный резистивный индекс; (C) Изображение, показывающее, вверху, допплеровский поток в почечных венах, а внизу волну потока, из которой рассчитывается индекс венозного импеданса; (D) Изображение, иллюстрирующее измерение длины почек. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
| Переменная | Т1 День 1, в 00:38 | Т2 День 1, в 10:53 | Т3 День 3, в 10:14 | Т4 День 5, в 10:20 |
| Частота сердечных сокращений (уд/мин) | 110 | 124 | 122 | 98 |
| Частота дыхания (вдохов в минуту) | 24 | 15 | 26 | 12 |
| Систолическое артериальное давление (мм рт.ст.) | 100 | 115 | 130 | 118 |
| Диастолическое артериальное давление (мм рт.ст.) | 61 | 69 | 66 | 65 |
| Среднее артериальное давление (мм рт.ст.) | 73 | 80 | 84 | 81 |
| Кумулятивный баланс жидкости (мл) | 0 | 704 | 7272 | 12338 |
| Искусственная вентиляция | ПЭЭП 5, FiO2 40% | ПЭЭП 5, FiO2 40% | PEEP 5, FiO2 30% | PEEP 5, FiO2 30% |
| ЭЛТ-грудина (секунды) | 1.5 | 2 | 4 | 3 |
| Центральная температура (◦ C) | 37.6 | 37.5 | 38.0 | 37.4 |
| Диурез за предыдущий час (мл) | 117 | 60 | 0 | 10 |
| Вводимые инотропные препараты | Норадреналина 0,1 мг/мл 3,0 мл/ч | Норадреналина 0,1 мг/мл 1,0 мл/ч | никакой | никакой |
| Вводимые седативные средства | Пропофол 20 мг/мл 5,0 мл/ч | никакой | никакой | никакой |
| Оценка по APACHE IV | 92 | 88 | 87 | 90 |
| Оценка SOFA | 8 | 8 | 5 | 8 |
| LVOT (см) | Н.А. | 2.4 | 2.4 | 2.4 |
| Сердечный выброс (л/мин) | Н.А. | 5.6 | 8.34 | 9.89 |
| TAPSE (мм) | Н.А. | 25 | 26 | 21 |
| RV S' (см/с) | Н.А. | 14 | 15 | 12 |
| Диаметр вдоха НПВ (см) | Н.А. | 1.14 | 1.24 | 1.10 |
| Диаметр выдоха НПВ (см) | Н.А. | 1.27 | 1.38 | 1.50 |
| Маршруты Kerley B (всего) | Н.А. | 6 | 2 | 4 |
| Длина почек (см) | Н.А. | 10.59 | Н.А. | Н.А. |
| Схема внутрипочечного венозного кровотока | Н.А. | Непрерывный | Непрерывный | Непрерывный |
| Допплерография почечного RI | Н.А. | 0.61 | 0.75 | 0.70 |
| VII | Н.А. | 0.33 | 0.56 | 0.68 |
Таблица 1: Случайный пациент с SICS-II. Пациентка X, женщина среднего возраста, поступила в отделение интенсивной терапии после того, как у нее обнаружили нарушение сознания. Сокращения: уд/мин = ударов в минуту, CRT = время наполнения капилляров, LVOT = выходной тракт левого желудочка, TAPSE = систолическая экскурсия в трикуспидальной кольцевой плоскости, RV S' = систолическая экскурсия правого желудочка, IVC = нижняя полая вена, RRI = индекс почечного сопротивления, VII = индекс венозного импеданса, N.A. = не применяется.
| Переменная | Единица | Источник | Получено в |
| Лактат | ммоль/л | Анализ газов артериальной крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| Хлорид | ммоль/л | Анализ газов артериальной крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| pH | Анализ газов артериальной крови | От стандартного ухода, как можно ближе к каждому клиническому осмотру, макс. разница 12 хо | |
| PCO2 | кПа | Анализ газов артериальной крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| ПаО2 | кПа | Анализ газов артериальной крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| ОХС3- | ммоль/л | Анализ газов артериальной крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| Гемоглобин | ммоль/л | Анализ газов артериальной крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| Лейкоцитов | 10 x 10-9/л | Анализ сыворотки крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| Тромбоциты | 10 x 10-9/л | Анализ сыворотки крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| HS Тропонин | нг/л | Анализ сыворотки крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| АСАТ | /л | Анализ сыворотки крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| АЛЯТ | /л | Анализ сыворотки крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| Билирубин общий | uoml/L | Анализ сыворотки крови | От стандартного лечения, как можно ближе к каждому клиническому осмотру, максимальная разница 12 часов |
| Креатинина | мкмоль/л | Анализ сыворотки крови | Все измерения с начала поступления в отделение интенсивной терапии |
| Объем мочи | мл | Сбор мочи в течение 24 часов | Все измерения с начала поступления в отделение интенсивной терапии |
| Креатинина | ммоль/24 ч | Анализ мочи | Все измерения с начала поступления в отделение интенсивной терапии |
Таблица 2: Список полученных биохимических переменных. Все биохимические переменные пациента, собранные в ходе исследования, перечислены здесь.
Обсуждение
Все обследования должны проводиться в соответствии с протоколом. Физикальное обследование имеет ценность только в том случае, если оно проводится в соответствии с заранее определенными определениями23. Лабораторные показатели должны быть собраны в соответствии с протоколом для получения всех значений. Четкие, интерпретируемые изображения CCUS являются ключом к ответу на исследовательский вопрос данного исследования, как описано в шаге 3.3. Если получены изображения низкого качества, измерения и анализы, описанные в шаге 5, не могут быть выполнены, и цель повторных измерений прекращается. Для минимизации риска получения изображений низкого качества предпринимаются три важные меры. Во-первых, студенты-исследователи, которые проводят CCUS в нашем исследовании, проходят обучение у опытного кардиолога-реаниматолога. Литература показывает, что короткая программа обучения хорошо подходит для получения базовой компетенции по CCUS24. Во-вторых, студенты-исследователи находятся под наблюдением старшего студента-исследователя во время первых 20 экзаменов, чтобы они могли получить практическую обратную связь. Наконец, все полученные изображения сердца и почек будут повторно оценены и проверены независимым экспертом из основной лаборатории кардиологической визуализации и опытным абдоминальным радиологом соответственно, чтобы гарантировать надежность данных.
Чтобы обеспечить качество изображения, исследователям необходимо уделять внимание и другим аспектам. Иногда требуется повторное нанесение геля для ультразвука или изменение положения зонда таким образом, чтобы он лучше соприкасался с кожей пациента, чтобы обеспечить оптимальное качество изображения. Также важно уделить достаточно времени для получения наиболее оптимального изображения, и если есть сомнения, следует проконсультироваться со старшим научным сотрудником, т.е. с курирующим кардиологом-реаниматологом или основным лаборантом, прежде чем клиническое обследование будет завершено. Непрерывная оценка и валидация всех ультразвуковых изображений обеспечивается за счет применения протокольных шагов, показанных на рисунке 1. Кроме того, студенты-исследователи и эксперты часто обмениваются отзывами, что упрощает быстрое внесение изменений в протокол для дальнейшего повышения качества изображений и измерений. Такая частая проверка позволяет легко обнаруживать систематические ошибки, чтобы обучение CCUS для будущих студентов-исследователей могло быть соответствующим образом адаптировано. Кроме того, ежемесячные собрания, открытые для всех членов команды, позволяют тщательно оценить и (при необходимости) внести изменения в протокол.
Круглосуточная доступность для скрининга и инклюзии пациентов является еще одним ключевым элементом для успешной реализации этого исследования. Это может быть достигнуто только при наличии специальной команды студентов-исследователей, большой команды студентов для оказания поддержки и хорошей координации с лицами, ухаживающими за больными в отделении интенсивной терапии. Эта координация происходит путем регулярного контакта между лицами, осуществляющими уход, и исследователями о возможных улучшениях для оптимизации сотрудничества со стандартным уходом.
Ограничением этого протокола является то, что успешное проведение CCUS зависит от доступности заранее определенных позиций, где размещается зонд. Во время SICS-I уже было показано, что кардиологический CCUS не может быть выполнен, когда пациентам требуются дренажи, марлевые или раневые повязки, которые препятствуют теоретически оптимальному эхокардиографическому окну1. Кроме того, ранее было показано, что возможность получения надлежащего подреберного окна с помощью трансторакальной эхокардиографии, которая требуется для измерений НПВ, потенциально ограничена вобщей популяции ОИТ. Доступность 24/7, требуемая этим протоколом для проведения различных исследований в разные моменты времени, также является потенциальным ограничением, поскольку некоторые центры могут не иметь возможности для этого. Даже в такой крупной академической больнице, как UMCG, обеспечение этого привело к задержкам в начале исследования. Еще одним ограничением, присущим ультразвуковым измерениям, является вариабельность измерений между наблюдателями. Для того, чтобы включение пациента было гарантировано в режиме 24/7, невозможно, чтобы один исследователь провел все клинические обследования у всех включенных пациентов. Это исследование направлено на то, чтобы один и тот же исследователь проводил все ультразвуковые измерения у одного и того же пациента, чтобы свести к минимуму вариабельность на индивидуальном уровне, но для всей когорты вариабельность между наблюдателями остается проблемой.
Ультразвуковая визуализация нескольких органов может быть быстрой, безопасной и эффективной структурой для визуализации перфузии и функции органов. Это удобный инструмент, которым должны уметь пользоваться все медицинские работники, и для которого немногие измерения, основанные на простом стандартизированном протоколе, обычно должны обеспечивать надежные измерения.
Кроме того, большинство обсервационных исследований, оценивающих использование ультрасонографии, и в частности эхокардиографии, носят ретроспективный характер или включают лишь небольшое число пациентов. 26 Этот протокол позволяет проводить структурный скрининг в режиме 24/7 неотобранной когорты пациентов в критическом состоянии, из которых могут быть определены подпопуляции, представляющие интерес, что позволяет одновременно исследовать несколько исследовательских вопросов.
Более того, несмотря на то, что известно, что клинические переменные в интенсивной терапии очень динамичны и взаимно влияют друг на друга, в большинстве исследований изучалось только аддитивное значение единичных ультразвуковых измеренийконкретных органов. Это первый протокол, в котором основное внимание уделяется повторным измерениям, ультразвуковому исследованию всего тела и венозному застою. Мы ожидаем, что SICS-II обеспечит более точное отражение гемодинамического статуса пациентов во время госпитализации в ОРИТ.
Текущая структура, используемая в SICS, может быть применена к большому количеству настроек, а добавление других элементов в настоящее время изучается. Его сила заключается в сочетании базовой исследовательской линии и адаптивной линии, в которой новые переменные могут быть легко добавлены к CRF, чтобы можно было исследовать новые исследовательские вопросы. Примером такой приспособляемости является добавление в регулярный протокол у определенной подгруппы пациентов оценки обширной стенки желудочка с помощью визуализации деформации, т.е. краткосрочного напряжения.
Более того, включение пациентов в терапию в настоящее время происходит исключительно в отделении интенсивной терапии, и часть траектории ухода за пациентами теперь упущена. Пациенты ОРИТ часто сначала поступают в отделение неотложной помощи (ОНП), а после выписки из ОРИТ остаются в обычной больничной палате. Таким образом, SICS нацелен на включение пациентов на более ранней стадии, включая пациентов по прибытии в ОНП и регистрируя вмешательства и гемодинамическую функцию с момента первоначального поступления в больницу. Кроме того, также разрабатываются планы по проведению ОИТ после выписки из отделения интенсивной терапии в обычные палаты, чтобы все пациенты могли быть обследованы в каждое заранее определенное время исследования. Еще одним важным аспектом является возможность расширения протокола на другие центры: его простота позволяет легко адаптировать центры, которые могут сами начать включение.
Наконец, разработка и успешное внедрение структурированного протокола CCUS также может иметь клинические последствия. Несмотря на то, что он используется только в исследовательских целях, он может быть внедрен врачами в клиническую CCUS после предложенного короткого периода обучения. Затем было бы интересно оценить, приведет ли облегчение обучения CCUS для (неопытных) врачей к сокращению дополнительных диагностических тестов.
Раскрытие информации
Авторам нечего раскрывать.
Благодарности
Мы хотели бы поблагодарить всех членов исследовательской группы SICS, которые были вовлечены в работу SICS-I и приняли участие в мозговых штурмах по текущему протоколу. Мы также хотели бы поблагодарить исследовательское бюро нашего отделения интенсивной терапии и его координаторов за их поддержку; д-р В. Диперинк и М. Онруст. Кроме того, мы хотели бы поблагодарить студенческую команду ICU и студентов-исследователей, которые структурно включили пациентов в SICS-II до сих пор; J. A. de Bruin, B. E. Keuning, drs. K. Selles.
Материалы
| Name | Company | Catalog Number | Comments |
| Ultrasound machine | GE Healthcare | 0144VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 3507VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 0630VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound gel | Parker | 01-08 | Aquasonic 100 ultrasound transmission gel |
| Temperature probe | DeRoyal | 81-010400EU | Skin Temperature Sensor |
Ссылки
- Hiemstra, B., et al. Clinical examination, critical care ultrasonography and outcomes in the critically ill: cohort profile of the Simple Intensive Care Studies-I. BMJ open. 7 (9), 017170 (2017).
- Lee, J., et al. Association between fluid balance and survival in critically ill patients. Journal of Internal Medicine. 277 (4), 468-477 (2015).
- Perner, A., et al. Fluid management in acute kidney injury. Intensive Care Medicine. 43 (6), 807-815 (2017).
- Balakumar, V., et al. Both Positive and Negative Fluid Balance May Be Associated With Reduced Long-Term Survival in the Critically Ill. Critical care medicine. 45 (8), 749-757 (2017).
- Hjortrup, P. B., et al. Restricting volumes of resuscitation fluid in adults with septic shock after initial management: the CLASSIC randomised, parallel-group, multicentre feasibility trial. Intensive Care Medicine. 42 (11), 1695-1705 (2016).
- Prowle, J. R., Kirwan, C. J., Bellomo, R. Fluid management for the prevention and attenuation of acute kidney injury. Nature reviews. Nephrology. 10 (1), 37-47 (2014).
- Gambardella, I., et al. Congestive kidney failure in cardiac surgery: the relationship between central venous pressure and acute kidney injury. Interactive CardioVascular and Thoracic Surgery. 23 (5), 800-805 (2016).
- Chen, K. P., et al. Peripheral Edema, Central Venous Pressure, and Risk of AKI in Critical Illness. Clinical journal of the American Society of Nephrology : CJASN. 11 (4), 602-608 (2016).
- Song, J., et al. Value of the combination of renal resistance index and central venous pressure in the early prediction of sepsis-induced acute kidney injury. Journal of critical care. 45, 204-208 (2018).
- Zhang, L., Chen, Z., Diao, Y., Yang, Y., Fu, P. Associations of fluid overload with mortality and kidney recovery in patients with acute kidney injury: A systematic review and meta-analysis. Journal of Critical Care. 30 (4), (2015).
- Simple Intensive Care Studies II - Full Text View. ClinicalTrials.gov Available from: https://clinicaltrials.gov/ct2/show/NCT03577405 (2018)
- Statistical analysis plan Simple Intensive Care Studies-I DETAILED STATISTICAL ANALYSIS PLAN (SAP) 1. Administrative information 1.1. Title, registration, versions and revisions. ClinicalTrials.gov Available from: https://clinicaltrials.gov/ProvidedDocs/24/NCT02912624/SAP_000.pdf (2018)
- Simple Observational Critical Care Studies - Full Text View - ClinicalTrials.gov. ClinicalTrials.gov Available from: https://clinicaltrials.gov/ct2/show/NCT03553069 (2018)
- Ait-Oufella, H., et al. Alteration of skin perfusion in mottling area during septic shock. Annals of Intensive Care. 3 (1), 31 (2013).
- Teasdale, G., Jennett, B. Assessment of Coma and Impaired Consciousness: A Practical Scale. The Lancet. 304 (7872), 81-84 (1974).
- Detsky, M. E., et al. Discriminative Accuracy of Physician and Nurse Predictions for Survival and Functional Outcomes 6 Months After an ICU Admission. JAMA. 317 (21), 2187 (2017).
- Lipson, A. R., Miano, S. J., Daly, B. J., Douglas, S. L. The Accuracy of Nurses' Predictions for Clinical Outcomes in the Chronically Critically Ill. Research & reviews. Journal of nursing and health sciences. 3 (2), 35-38 (2017).
- Lichtenstein, D. A. BLUE-protocol and FALLS-protocol: two applications of lung ultrasound in the critically ill. Chest. 147 (6), 1659-1670 (2015).
- Tang, W. H. W., Kitai, T. Intrarenal Venous Flow: A Window Into the Congestive Kidney Failure Phenotype of Heart Failure. JACC: Heart Failure. 4 (8), 683-686 (2016).
- Jeong, S. H., Jung, D. C., Kim, S. H., Kim, S. H. Renal venous doppler ultrasonography in normal subjects and patients with diabetic nephropathy: Value of venous impedance index measurements. Journal of Clinical Ultrasound. 39 (9), 512-518 (2011).
- Iida, N., et al. Clinical Implications of Intrarenal Hemodynamic Evaluation by Doppler Ultrasonography in Heart Failure. JACC: Heart Failure. 4 (8), 674-682 (2016).
- Lang, R. M., et al. Recommendations for Cardiac Chamber Quantification by Echocardiography in Adults: An Update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. European Heart Journal - Cardiovascular Imaging. 16 (3), 233-271 (2015).
- Hiemstra, B., Eck, R. J., Keus, F., van der Horst, I. C. C. Clinical examination for diagnosing circulatory shock. Current opinion in critical care. 23 (4), 293-301 (2017).
- Vignon, P., et al. Basic critical care echocardiography: validation of a curriculum dedicated to noncardiologist residents. Critical care medicine. 39 (4), 636-642 (2011).
- Jensen, M. B., Sloth, E., Larsen, K. M., Schmidt, M. B. Transthoracic echocardiography for cardiopulmonary monitoring in intensive care. European journal of anaesthesiology. 21 (9), 700-707 (2004).
- Koster, G., van der Horst, I. C. C. Critical care ultrasonography in circulatory shock. Current opinion in critical care. 23 (4), 326-333 (2017).
- Haitsma Mulier, J. L. G., et al. Renal resistive index as an early predictor and discriminator of acute kidney injury in critically ill patients; A prospective observational cohort study. PloS one. 13 (6), 0197967 (2018).
- Micek, S. T., et al. Fluid balance and cardiac function in septic shock as predictors of hospital mortality. Critical care. 17 (5), 246 (2013).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены