Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Aislamiento escalable y purificación de vesículas extracelulares de Escherichia coli y otras bacterias
En este artículo
Resumen
Las bacterias secretan vesículas extracelulares (EV) de tamaño nanométrico que transportan moléculas biológicas bioactivas. La investigación EV se centra en comprender su biogénesis, su papel en las interacciones y enfermedades microbio-microbio y huésped-microbio, así como sus posibles aplicaciones terapéuticas. Se presenta un flujo de trabajo para el aislamiento escalable de vehículos eléctricos de varias bacterias para facilitar la estandarización de la investigación de vehículos eléctricos.
Resumen
Diversas especies bacterianas secretan ~20-300 nm vesículas extracelulares (EV), compuestas de lípidos, proteínas, ácidos nucleicos, glicanos y otras moléculas derivadas de las células parentales. Los EV funcionan como vectores de comunicación dentro y entre especies, al tiempo que contribuyen a la interacción entre bacterias y organismos huéspedes en el contexto de la infección y la colonización. Dada la multitud de funciones atribuidas a los EV en la salud y la enfermedad, existe un creciente interés en aislar los EV para estudios in vitro e in vivo . Se planteó la hipótesis de que la separación de EV basada en propiedades físicas, es decir, tamaño, facilitaría el aislamiento de vesículas de diversos cultivos bacterianos.
El flujo de trabajo de aislamiento consiste en centrifugación, filtración, ultrafiltración y cromatografía de exclusión de tamaño (SEC) para el aislamiento de EV de cultivos bacterianos. Se incorporó un paso de filtración de flujo tangencial (TFF) impulsado por bomba para mejorar la escalabilidad, lo que permite el aislamiento del material de los litros de cultivo celular inicial. Escherichia coli se utilizó como un sistema modelo que expresa nanoluciferasa asociada a EV y mCherry no asociada a EV como proteínas reporteras. La nanoluciferasa se dirigió a los EV fusionando su N-terminal con citolisina A. Las fracciones de cromatografía tempranas que contenían EV de 20-100 nm con citolisina A - nanoLuc asociadas eran distintas de las fracciones posteriores que contenían las proteínas libres. La presencia de nanoluciferasa asociada a EV se confirmó mediante etiquetado de inmunooro y microscopía electrónica de transmisión. Este flujo de trabajo de aislamiento EV es aplicable a otras especies bacterianas gramnegativas y grampositivas asociadas al intestino humano. En conclusión, la combinación de centrifugación, filtración, ultrafiltración / TFF y SEC permite el aislamiento escalable de EV de diversas especies bacterianas. El empleo de un flujo de trabajo de aislamiento estandarizado facilitará los estudios comparativos de EV microbianos entre especies.
Introducción
Las vesículas extracelulares (EV) son estructuras similares a liposomas de tamaño nanométrico compuestas de lípidos, proteínas, glicanos y ácidos nucleicos, secretados por células procariotas y eucariotas1. Desde los primeros estudios que visualizan la liberación de EV de bacterias gramnegativas2, el número de funciones biológicas atribuidas a las EV bacterianas (20-300 nm de diámetro) ha estado creciendo constantemente en las últimas décadas. Sus funciones incluyen la transferencia de resistencia a los antibióticos3, la formación de biopelículas4, la detección de quórum5 y la administración de toxinas6. También hay un creciente interés en el uso de EV bacterianas como terapéutica, especialmente en vacunología7 y terapia contra el cáncer8.
A pesar del creciente interés en la investigación de vehículos eléctricos, todavía existen desafíos técnicos con respecto a los métodos de aislamiento. Específicamente, existe la necesidad de métodos de aislamiento que sean reproducibles, escalables y compatibles con diversos organismos productores de EV. Para crear un conjunto unificado de principios para planificar y reportar el aislamiento de EV y los métodos de investigación, la Sociedad Internacional de Vesículas Extracelulares publica y actualiza el documento de posición MISEV9. Además, el consorcio EV-TRACK proporciona una plataforma abierta para informar metodologías detalladas para el aislamiento de EV utilizadas en manuscritos publicados para mejorar la transparencia10.
En este protocolo, se adaptaron metodologías previas utilizadas para el aislamiento de EVs a partir de cultivos celulares de mamíferos11,12 para permitir el aislamiento de EVs a partir de cultivo celular bacteriano. Buscamos emplear métodos que permitan el aislamiento de EV de una variedad de microbios, que pueden ser escalables, y equilibrar la pureza y el rendimiento de EV (como se discutió en el documento de posición9 de MISEV). Después de eliminar las células bacterianas y los desechos por centrifugación y filtración, el medio de cultivo se concentra mediante ultrafiltración del dispositivo centrífugo (para un volumen de hasta ~ 100 ml) o TFF accionado por bomba (para volúmenes más grandes). Los vehículos eléctricos son aislados por SEC utilizando columnas optimizadas para la purificación de pequeños vehículos eléctricos.
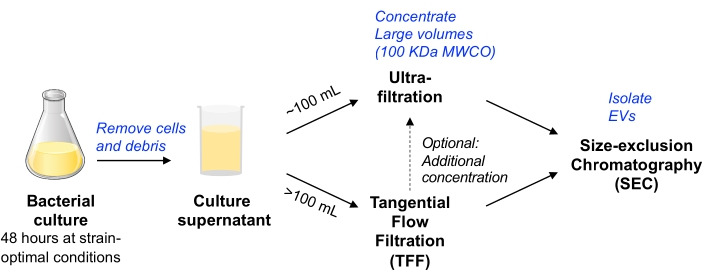
Figura 1: Descripción general del esquema del flujo de trabajo de aislamiento de EV bacteriano. Abreviaturas: EV = vesícula extracelular; TFF = filtración de flujo tangencial; SEC = cromatografía de exclusión de tamaño; MWCO = corte de peso molecular. Haga clic aquí para ver una versión más grande de esta figura.
Una cepa comensal de ratón de Escherichia coli (es decir, E. coli MP113) fue utilizada como organismo modelo y modificada para expresar nanoluciferasa asociada a EV por fusión a citolisina A, como se informó anteriormente14. Los métodos utilizados aquí pueden procesar al menos hasta varios litros de cultivos bacterianos y separar eficazmente las proteínas asociadas a EV de las no asociadas a EV. Finalmente, este método también se puede utilizar para otras especies bacterianas grampositivas y gramnegativas. Todos los datos relevantes de los experimentos reportados se enviaron a la base de conocimiento EV-TRACK (EV-TRACK ID: EV210211)10.
Protocolo
NOTA: Asegúrese de que todo el trabajo que involucre bacterias y ADN recombinante siga las mejores prácticas para la contención de bioseguridad apropiadas para el nivel de peligro de bioseguridad de cada cepa. El trabajo debe realizarse de acuerdo con las normas locales, nacionales e internacionales de seguridad de la biotecnología.
1. Cepas bacterianas y condiciones de cultivo
NOTA: Las cepas bacterianas utilizadas en este estudio fueron Escherichia coli MP113, Akkermansia mucinophila, Bacteroides thetaiotaomicron, Bifidobacterium breve y Bifidobacterium dentium.
- Para E. coli, use un asa estéril para inocular colonias individuales en 250 a 1,000 ml de caldo Luria-Bertani (LB) e incube aeróbicamente en una incubadora de agitación a 300 rpm y 37 ° C durante 48 h antes de procesar el cultivo. Para la cepa recombinante de E. coli MP1 que alberga p114-mCherry-Clyluc (método suplementario y figura suplementaria S1), agregue cloranfenicol al agar LB y al caldo a una concentración final de 17 μg / ml.
- Para A. mucinophila, B. thetaiotaomicron, B. breve y B. dentium, raye las placas de agar de infusión cerebral cardíaca (BHI) e incube anaeróbicamente dentro de una cámara anaeróbica de vinilo. Inocular colonias individuales en 100 ml de caldo de IHB prereducido e incubar durante 48 h anaeróbicamente.
2. Aislamiento EV
- Medio de cultivo bacteriano clarificador por centrifugación y filtración
- Transfiera los cultivos celulares bacterianos inoculados en el paso 1 para limpiar botellas de centrífuga de polipropileno de 250 ml o 500 ml vertiendo. Centrifugar las botellas en un rotor de ángulo fijo de gran capacidad a 4 °C y 5.000 × g durante 15 min. Transfiera el sobrenadante a las botellas de centrífuga limpias vertiendo con cuidado y centrifugar nuevamente a 10,000 × g durante 15 min.
NOTA: Reutilice las botellas después de una limpieza y descontaminación apropiadas para la bioseguridad.- Si hay grandes gránulos de células bacterianas después de la segunda centrifugación, repita la centrifugación en una botella limpia para eliminar aún más las células.
- Transfiera el sobrenadante a un dispositivo de filtro accionado por vacío de polietersulfona de 0,22 μm de tamaño apropiado vertiéndolo. Filtre conectando el dispositivo de filtración a un suministro de pared de vacío. Si la tasa de filtración disminuye significativamente, simplemente mueva cualquier material sin filtrar a un nuevo dispositivo. Conservar el medio filtrado a 4 °C durante la noche y continuar con el protocolo al día siguiente si lo desea.
NOTA: Las centrifugaciones anteriores generalmente permiten el procesamiento de ~ 2 veces el volumen indicado de cultivo celular a través de cada dispositivo. Por ejemplo, un solo dispositivo de filtro de 500 ml podría filtrar ~1.000 ml de cultivo precentrifugado. Estos dispositivos no suelen reutilizarse. El uso de filtros de jeringa en este paso no se recomienda sin optimización, ya que se observaron pérdidas significativas con los modelos probados. Este es un posible punto de parada. - Compruebe la eliminación completa de las células viables en este punto esparciendo una alícuota del sobrenadante filtrado en placas de agar adecuadas y asegúrese de la ausencia de colonias después de la incubación en condiciones óptimas para la cepa bacteriana. Si se detectan bacterias, optimice aún más el procedimiento anterior realizando centrifugaciones y / o filtraciones adicionales.
- Transfiera los cultivos celulares bacterianos inoculados en el paso 1 para limpiar botellas de centrífuga de polipropileno de 250 ml o 500 ml vertiendo. Centrifugar las botellas en un rotor de ángulo fijo de gran capacidad a 4 °C y 5.000 × g durante 15 min. Transfiera el sobrenadante a las botellas de centrífuga limpias vertiendo con cuidado y centrifugar nuevamente a 10,000 × g durante 15 min.
- Concentración del medio filtrado
- Si trabaja con volúmenes significativamente >100 ml, continúe con el paso 2.2.2. Si trabaja con volúmenes de ~100 ml, cargue 90 ml de medio de cultivo filtrado en el depósito de un dispositivo de ultrafiltración centrífuga de corte de peso molecular (MWCO) de capacidad respectiva de 100 kDa utilizando pipetas serológicas. Equilibre siempre con un dispositivo de ultrafiltración correspondiente y centrifugar en rotor de cangilón oscilante a 4 °C y 2.000 × g durante intervalos de 15-30 minutos, hasta que el volumen del medio en el depósito superior se haya concentrado a <0,5 ml.
- Rellene el depósito con cualquier medio de cultivo filtrado restante. Si está "rellenando", retire el flujo en la parte inferior del dispositivo y vuelva a equilibrar cualquier dispositivo.
NOTA: Se observó que el volumen máximo de medio de cultivo filtrado que se puede concentrar utilizando estos dispositivos es <2 veces el volumen recomendado. - Si la viscosidad del medio concentrado en el depósito aumenta visiblemente (material oscuro y viscoso), diluya con solución salina tamponada con fosfato (PBS) y vuelva a concentrar por centrifugación para diluir cualquier proteína no EV menor que el MWCO de 100 kDa.
NOTA: Este es un posible punto de parada. - Transfiera el medio concentrado a un tubo de baja unión a proteínas, guárdelo a 4 °C durante la noche y continúe el protocolo al día siguiente si lo desea.
- Rellene el depósito con cualquier medio de cultivo filtrado restante. Si está "rellenando", retire el flujo en la parte inferior del dispositivo y vuelva a equilibrar cualquier dispositivo.
- Si trabaja con volúmenes significativamente >100 ml, seleccione un dispositivo TFF del tamaño adecuado (100 kDa MWCO) para acomodar el volumen que se va a procesar.
NOTA: Los dispositivos de filtración para procesar de 100 ml a >1,000 ml están disponibles comercialmente. La disponibilidad local, el costo y la compatibilidad con la bomba y la tubería/conexiones dictarán qué modelos particulares serán más útiles. Se procesaron hasta 2 L de medio de cultivo con el dispositivo indicado en la Tabla de materiales antes de necesitar limpiar el filtro (consulte el paso 2.3 a continuación para el protocolo de limpieza).- Ensamble un circuito de filtración con tubo #16 de baja ligación/baja lixiviación, adaptadores de manguera-púa a Luer de 1/8 de pulgada, el dispositivo TFF y una bomba peristáltica, como se indica en la Figura Suplementaria S2.
NOTA: Realice TFF dentro de un gabinete de bioseguridad para minimizar el riesgo de contaminar la preparación EV con bacterias ambientales. - A temperatura ambiente, comience a circular el medio filtrado y acondicionado a aproximadamente 200 ml/min (mínimo 100 ml/min). Determine las RPM apropiadas correspondientes al caudal deseado bombeando 200 ml de PBS en un recipiente graduado. Cuando circule un medio filtrado y acondicionado, recoger las moléculas <100 kDa que atraviesan la membrana de ultrafiltración como residuos en un recipiente separado.
NOTA: El siguiente ejemplo supondrá un volumen inicial de 2 L de cultivo. - Continúe circulando el medio acondicionado hasta que su volumen se haya reducido a ~ 100-200 mL. Muévase a embarcaciones más pequeñas según sea necesario. Diluir 2 veces con PBS, y continuar circulando con la bomba, concentrándose hasta 75-100 mL. Diluir 2 veces con PBS y continuar circulando hasta un volumen final de 25 ml. Diluir 2 veces con PBS y continuar circulando hasta <10 ml.
- Levante el tubo de alimentación fuera del depósito de muestras y continúe bombeando para purgar el filtro y recuperar la cantidad máxima de muestra.
NOTA: Este es un posible punto de parada. - Transfiera la muestra concentrada a un tubo cónico y guárdela durante la noche a 4 °C si lo desea. Como alternativa, continúe con el protocolo.
- Mueva la muestra concentrada a un dispositivo de ultrafiltración centrífuga MWCO de 100 kDa de 15 ml de capacidad. Centrifugar en un rotor de cangilón oscilante a 4 °C y 2.000 × g durante intervalos de 15-30 min hasta que el volumen del medio en el depósito superior se haya concentrado a <2 ml.
NOTA: Este es un posible punto de parada. - Transfiera el medio concentrado a un tubo de baja unión a proteínas y guárdelo a 4 °C durante la noche, continuando el protocolo al día siguiente si lo desea.
- Ensamble un circuito de filtración con tubo #16 de baja ligación/baja lixiviación, adaptadores de manguera-púa a Luer de 1/8 de pulgada, el dispositivo TFF y una bomba peristáltica, como se indica en la Figura Suplementaria S2.
- Si trabaja con volúmenes significativamente >100 ml, continúe con el paso 2.2.2. Si trabaja con volúmenes de ~100 ml, cargue 90 ml de medio de cultivo filtrado en el depósito de un dispositivo de ultrafiltración centrífuga de corte de peso molecular (MWCO) de capacidad respectiva de 100 kDa utilizando pipetas serológicas. Equilibre siempre con un dispositivo de ultrafiltración correspondiente y centrifugar en rotor de cangilón oscilante a 4 °C y 2.000 × g durante intervalos de 15-30 minutos, hasta que el volumen del medio en el depósito superior se haya concentrado a <0,5 ml.
- Limpieza del dispositivo TFF (opcional)
NOTA: La tasa de filtración disminuye a medida que el dispositivo TFF comienza a "obstruirse" durante el proceso (ensuciamiento). Si es necesario, el dispositivo de filtro se puede limpiar para facilitar la filtración de muestras adicionales en la misma ejecución de purificación. Aunque teóricamente posible, un filtro TFF limpio no se ha utilizado para una ejecución de purificación diferente para evitar la contaminación cruzada.- Para limpiar, retire todos los tubos y tapas del dispositivo TFF y drene cualquier líquido residual.
- Utilice la bomba peristáltica y el tubo para inundar los compartimentos interior y exterior del dispositivo TFF (es decir, a través de los puertos paralelos y perpendiculares en el modelo enumerado en la Tabla de materiales) con ~ 100 ml de agua destilada. Retire todos los tubos/tapas y drene el dispositivo TFF.
- Tapa los puertos exteriores (perpendiculares, filtrados) y haz circular 250 ml de etanol al 20% en agua destilada a >200 ml/min durante 10 min a través del compartimento interior. Drenar, inundar con agua destilada y escurrir de nuevo como arriba.
- Hacer circular 250 ml de solución fresca de NaOH 0,5 N durante 30 minutos a través del compartimento interior y escurrir de nuevo.
- Vuelva a conectar todos los tubos y tapas a los puertos de entrada, salida y filtrado, como en la figura suplementaria S2, y haga circular nuevamente la solución de NaOH de 0,5 N hasta que un volumen de NaOH > área de superficie del filtro de 1 ml / cm2 penetre a través de la membrana del filtro y se recoja como filtrado/desecho.
- Enjuague el dispositivo TFF con agua destilada como se indica anteriormente. Use el dispositivo TFF inmediatamente o inunde el dispositivo con ~ 100 ml de etanol al 20% y guárdelo durante la noche a 4 ° C.
NOTA: Si se almacena en etanol, asegúrese de drenar, enjuagar con agua, drenar y hacer circular 250 ml de PBS a través del dispositivo hasta que un volumen de >1 ml / cm2 área de superficie del filtro penetre a través de la membrana del filtro y se recolecte como filtrado / desecho para eliminar el etanol residual antes del procesamiento de la muestra.
- Cromatografía de exclusión de tamaño (SEC)
NOTA: SEC se utiliza para aumentar la pureza de los EV y eliminar la proteína no vesicular.- Utilice una columna SEC pequeña (volumen de lecho de 10 ml) para el aislamiento de EV de <100 ml de material de partida y una columna más grande (volumen de lecho de 47 ml) para el aislamiento de EV de >100 ml de material de partida.
NOTA: En el ejemplo siguiente se enumerarán los volúmenes de la columna más grande, con los volúmenes de la columna más pequeña entre paréntesis. - Lleve la columna SEC y el PBS a temperatura ambiente durante varias horas. Estabilice la columna SEC en posición vertical utilizando un soporte y soporte de laboratorio estándar. Alternativamente, utilice soportes de columna de cromatografía comerciales.
- Antes de conectarlo a la columna SEC, hidrate el depósito de muestra permitiendo que 5 ml de PBS fluyan a través de la frita y hacia un contenedor de residuos. Desenrosque la tapa de entrada de la columna SEC, agregue 2 ml de PBS al depósito de muestra y conecte cuidadosamente el depósito a la columna a medida que el PBS gotea a través de la frita (no aplicable para columnas SEC pequeñas).
NOTA: Este paso anterior evita que las burbujas de aire queden atrapadas en la parte superior de la columna SEC. Si el aire está atrapado, retire el depósito, toque la columna para sacar la burbuja de aire y repita el procedimiento de conexión. Para la columna más pequeña, simplemente destape la parte superior de la columna SEC y coloque la tolva de muestra. - Agregue 47 ml (10 ml) de PBS al depósito de muestra y destape la parte inferior de la columna SEC. Permita que todo el búfer de muestra cargado fluya a través de la columna para el equilibrio. Deseche el flujo continuo.
- Cargue un máximo de 2 ml (0,5 ml) de muestra en el depósito de muestra, deseche el flujo y permita que la muestra entre completamente en la columna.
- Agregue inmediatamente PBS al depósito o tolva de muestra a un volumen de 14.25 ml menos el volumen de muestra (3 ml menos el volumen de muestra, para la columna pequeña). Permita que la solución fluya a través de la columna y deseche esta cantidad igual al volumen vacío de la columna.
NOTA: Para una muestra típica de 2 ml, la cantidad de PBS que se agregará al depósito o tolva de muestra será de 12.25 ml. - Coloque un microtubo de baja unión de 2 ml directamente debajo de la columna SEC. Agregue inmediatamente 2 ml (0,5 ml) de PBS al depósito de muestra y permita que entre en la columna. Etiquete estos primeros 2 ml (0,5 ml) de flujo continuo como fracción 1. Continúe agregando 2 ml (0.5 ml) a la vez al depósito de muestra para recolectar cada fracción subsiguiente.
NOTA: La mayoría de los EV bacterianos eluyen en las primeras 5 fracciones. Durante la optimización, se recolectaron las primeras 12 fracciones. - Conservar las fracciones a 4 °C para almacenamiento a corto plazo (días) o a -80 °C para almacenamiento a largo plazo.
- Limpieza y almacenamiento de las columnas SEC reutilizables
NOTA: Las columnas SEC descritas en este protocolo se pueden reutilizar hasta 5 veces según el fabricante. Si el caudal de las columnas SEC disminuye después de <5 usos, el fabricante recomienda centrifugar las muestras concentradas a 10.000 x g durante 10 minutos para eliminar cualquier agregado antes de SEC. A continuación, cargue el sobrenadante de esta centrifugación en la columna SEC para el aislamiento EV.- Para limpiar y almacenar la columna SEC después de cada uso, agregue 2 ml (0,5 ml) de NaOH 0,5 M y permita que entre en la columna por completo. Deje pasar 100 ml (20 ml) de etanol al 20% a través de la columna y guárdelo a 4 °C hasta el próximo uso. Antes del próximo uso, equilibre el etanol a temperatura ambiente como se mencionó anteriormente y cámbielo con un tampón de PBS pasando otros 150 ml (30 ml) de PBS a través de la columna.
- Para limpiar y reutilizar inmediatamente la columna SEC después de cada uso, agregue 2 ml (0,5 ml) de NaOH 0,5 M y permita que entre en la columna por completo. Ejecute aproximadamente 150 ml (30 ml) de tampón PBS para eliminar el NaOH. Cuando el pH del eluido es igual a PBS (~7), se puede cargar una nueva muestra.
- Utilice una columna SEC pequeña (volumen de lecho de 10 ml) para el aislamiento de EV de <100 ml de material de partida y una columna más grande (volumen de lecho de 47 ml) para el aislamiento de EV de >100 ml de material de partida.
3. Control de calidad de la preparación EV
- Pruebas de esterilidad
NOTA: Como estos EV provienen de cultivos bacterianos, es fundamental garantizar la esterilidad antes del uso posterior.- Obtener 100 μL (20 μL) de las fracciones a utilizar en los ensayos e inocular 3 mL del medio utilizado para cultivar la bacteria fuente. Cultivo en las respectivas condiciones óptimas durante al menos 3 días y observar turbidez. Alternativamente, aplique las muestras de fracción a las placas de agar que contienen el medio utilizado para cultivar las bacterias productoras y busque la formación de colonias.
NOTA: Si se detecta contaminación bacteriana, no se recomienda utilizar la preparación EV para la experimentación. En su lugar, repita el aislamiento, teniendo cuidado de minimizar el riesgo de contaminación bacteriana (a) realizando suficiente centrifugación / filtración de medio de cultivo celular bacteriano condicionado, (b) usando botellas limpias, tubos, filtros y columnas de cromatografía, y (c) empleando técnicas asépticas apropiadas.
- Obtener 100 μL (20 μL) de las fracciones a utilizar en los ensayos e inocular 3 mL del medio utilizado para cultivar la bacteria fuente. Cultivo en las respectivas condiciones óptimas durante al menos 3 días y observar turbidez. Alternativamente, aplique las muestras de fracción a las placas de agar que contienen el medio utilizado para cultivar las bacterias productoras y busque la formación de colonias.
- Cuantificación de proteínas
NOTA: Se utilizó un kit de cuantificación de proteínas basado en fluorescencia de alta sensibilidad (consulte la Tabla de materiales). El kit funciona con un fluorímetro patentado correspondiente a longitudes de onda de excitación/emisión de 485/590 nm.- Lleve todos los reactivos, patrones y muestras a temperatura ambiente.
- Preparar una mezcla maestra de reactivo proteico y tampón añadiendo 1 μL del reactivo a 199 μL de tampón para cada muestra y patrón a ensayar. Usando tubos de PCR de pared delgada de 0.5 ml, agregue 10 μL estándar + 190 μL de mezcla maestra a cada tubo estándar.
NOTA: Para estar dentro del rango del ensayo, la cantidad de cada fracción que se agregará a cada tubo de muestra depende del rendimiento proteico esperado de la purificación. Típicamente, se utilizaron 5 μL de cada fracción + 195 μL de mezcla maestra. El volumen final de la muestra + mezcla maestra debe ser de 200 μL. - Vortex los tubos de ensayo e incubar durante al menos 15 minutos a temperatura ambiente en la oscuridad.
- Mida los estándares en el fluorímetro patentado apropiado (consulte la Tabla de materiales) seleccionando la opción Ensayo de proteínas usando los botones de flecha y presionando el botón GO para confirmar. Siga las instrucciones en pantalla, inserte cada tubo estándar y presione GO.
- Inserte el tubo de muestra experimental; presione GO para leer; y observe el resultado mostrado, que es la concentración real de proteína en la mezcla tampón/muestra del ensayo. Para obtener la concentración de proteína en la muestra, utilice las teclas de flecha para seleccionar la opción Calcular concentración de muestra, pulse GO y utilice las teclas de flecha para seleccionar el volumen de muestra añadido al tampón de ensayo para la muestra dada. Presione GO y registre la concentración de proteína de la muestra. Repita este paso para cada muestra que se vaya a analizar.
- Conteo de partículas y distribución de tamaño
NOTA: Se utilizó la detección de pulso resistivo de microfluídica (MRPS) para cuantificar la concentración de EV y la distribución del tamaño.- Diluir las muestras en PBS suplementado con Tween-20 al 1% que se ha filtrado a través de un filtro de jeringa de 0,02 μm hasta una concentración de proteína de aproximadamente 0,1 μg/ml.
NOTA: El objetivo de la dilución es alcanzar una concentración de partículas esperada en el rango de 10a 10 partículas/ml en fracciones que contienen EV. Puede ser necesario determinar empíricamente la dilución óptima. Se esperan pocos vehículos eléctricos para fracciones posteriores (más allá de la fracción 6). Por lo tanto, la concentración de partículas probablemente será de <1010 partículas/ml a pesar del análisis a bajas diluciones. - Cargue 3 μL de cada muestra en el cartucho de microfluídica desechable con una micropipeta, inserte el cartucho en el instrumento MRPS y presione el botón metálico con un borde iluminado azul.
- Haga clic en Go! en el software de adquisición y espere a que el instrumento analice la muestra. Adquirir de 1.000 a 10.000 eventos de partículas para minimizar el error estadístico técnico del análisis. En este punto, haga clic en Detener y finalizar ejecución para completar la adquisición de muestra.
NOTA: Junto con los archivos de datos sin procesar, el instrumento genera una hoja de cálculo de resumen que enumera la concentración de partículas en la muestra. Corrija este valor de acuerdo con la dilución de la muestra realizada. - Utilizando software de análisis, cargue los datos en bruto y genere gráficos personalizados de distribución de tamaño.
- Diluir las muestras en PBS suplementado con Tween-20 al 1% que se ha filtrado a través de un filtro de jeringa de 0,02 μm hasta una concentración de proteína de aproximadamente 0,1 μg/ml.
4. Almacenamiento EV
- Alícuotas fracciones individuales o agrupadas al 25-50% del tamaño de la fracción individual (dependiendo del tamaño de la columna utilizada) en tubos de baja unión a proteínas y almacenar a -80 °C para evitar ciclos de congelación-descongelación.
NOTA: Diferentes aplicaciones pueden requerir alícuotas más pequeñas o más grandes dependiendo de la cantidad esperada utilizada en cada experimento. Esto tendrá que determinarse empíricamente. Las fracciones que no contienen EV pueden descartarse si no son aplicables a los objetivos de la investigación.
5. Microscopía electrónica de transmisión
- Tinción negativa
- Agregue 5 μL de la muestra EV a la rejilla de malla de cobre 400 recubierta de carbono e incube a temperatura ambiente durante 10 min. Lave el lado de la muestra con 5 gotas de tampón Tris de 5 mM (pH 7.1) y luego con 5 gotas de agua destilada.
- Mancha el lado de la muestra con 5 gotas de acetato de uranilo al 2%. Seque cualquier cantidad adicional de mancha con papel de filtro y deje que la rejilla se seque completamente durante varias horas o durante la noche. Visualice las muestras con un microscopio electrónico operado a 80 kV.
- Etiquetado Immunogold
- Aplicar 10 μL de la suspensión EV a una rejilla de malla formvar/carbon 400 e incubar a temperatura ambiente durante 1 h. Lave la rejilla en PBS tres veces y luego aplique paraformaldehído al 4% durante 10 minutos para fijar la muestra. Lave las rejillas cinco veces con PBS.
- Bloquee la rejilla con tres lavados de PBS que contienen 0,1% de albúmina sérica bovina (BSA). Luego, aplique 10 μL de un anticuerpo primario durante 40 min a temperatura ambiente (aquí, 1 μg/ml de anticuerpo nluc). Lavar tres veces más con PBS que contiene 0.1% de BSA.
- Agregue 10 μL de anticuerpo secundario marcado con oro a la rejilla e incube durante 40 minutos a temperatura ambiente. Lave las rejillas tres veces con PBS.
NOTA: Aquí, se utilizó un anticuerpo anti-ratón de cabra conjugado con nanopartículas de oro de 10 nm después de diluir 1:10 en el tampón de bloqueo. Si el etiquetado dorado oscurece la visualización EV, se pueden usar anticuerpos secundarios con nanopartículas de oro más pequeñas (por ejemplo, 5 nm) en su lugar. - Fije la rejilla con 10 μL de glutaraldehído al 2,5% durante 10 min a temperatura ambiente. Lavar tres veces en PBS. Realizar tinción negativa con acetato de uranilo al 2% (10 μL) durante 15 min. Incrustar las muestras en 10 μL de acetato de uranilo al 0,5% y solución de metilcelulosa al 0,13% durante 10 min.
- Deje que las rejillas de muestra se sequen durante la noche a temperatura ambiente antes de obtener imágenes en el microscopio electrónico.
- En el software de adquisición de microscopios, determine la exposición empíricamente para obtener la calidad óptima de la imagen (por ejemplo, 0.80851 s en esta configuración particular) y ajústela escribiendo este valor en el cuadro de opciones de tiempo de exposición . Seleccione la opción de 80 kV y haga clic en Iniciar adquisición para capturar la imagen.
Resultados
Para evaluar qué fracciones de cromatografía SEC se enriquecieron para EV, la columna SEC se cargó con 2 ml de medio de cultivo acondicionado con E. coli MP1 que había sido concentrado 1.000 veces por TFF, y se recolectaron fracciones secuenciales. Usando MRPS, se encontró que las fracciones 1-6 contenían la mayor cantidad de EV (Figura 2A). Las fracciones posteriores contenían muy pocos EVs, que comprendían proteínas libres de EV en lugar de EV (Figura...
Discusión
En el protocolo anterior, se describe un método que es escalable y aísla de manera confiable los EV de varias bacterias gramnegativas / positivas y aeróbicas / anaeróbicas. Tiene varios puntos de parada potenciales a lo largo del procedimiento, aunque es mejor evitar tomar más de 48 h para aislar los EV de los medios de cultivo bacteriano condicionados.
En primer lugar, consiste en cultivar bacterias para generar un medio de cultivo bacteriano condicionado. Se encontró que aumentar el ti...
Divulgaciones
Los autores no tienen conflictos de intereses que declarar.
Agradecimientos
La investigación descrita anteriormente fue apoyada por la subvención de capacitación NIH TL1 TR002549-03. Agradecemos a los doctores John C. Tilton y Zachary Troyer (Case Western Reserve University) por facilitar el acceso al instrumento analizador de tamaño de partículas; Lew Brown (Spectradyne) por su asistencia técnica con el análisis de los datos de distribución del tamaño de partícula; el Dr. David Putnam de la Universidad de Cornell por proporcionar el plásmido14 pClyA-GFP; y el Dr. Mark Goulian de la Universidad de Pensilvania por proporcionarnos la E. coli MP113.
Materiales
| Name | Company | Catalog Number | Comments |
| 0.5 mL flat cap, thin-walled PCR tubes | Thermo Scientific | 3430 | it is important to use thin-walled PCR tubes to obtain accurate readings with Qubit |
| 16% Paraformaldehyde (formaldehyde) aqueous solution | Electron microscopy sciences | 15700 | |
| 250 mL Fiberlite polypropylene centrifuge bottles | ThermoFisher | 010-1495 | |
| 500 mL Fiberlite polypropylene centrifuge bottles | ThermoFisher | 010-1493 | |
| 65 mm Polypropylene Round-Bottom/Conical Bottle Adapter | Beckman Coulter | 392077 | Allows Vivacell to fit in rotor |
| Akkermansia mucinophila | ATCC | BAA-835 | |
| Amicon-15 (100 kDa MWCO) | MilliporeSigma | UFC910024 | |
| Avanti J-20 XPI centrifuge | Beckman Coulter | No longer sold by Beckman. Avanti J-26XP is closest contemporary model. | |
| Bacteroides thetaiotaomicron VPI 5482 | ATCC | 29148 | |
| Bifidobacterium breve | NCIMB | B8807 | |
| Bifidobacterium dentium | ATCC | 27678 | |
| Brain Heart infusion (BHI) broth | Himedia | M2101 | After autoclaving, Both BHI broth and agar were introduced into the anaerobic chamber, supplemented with Menadione (1 µg/L), hematin (1.2 µg/L), and L-Cysteine Hydrochloride (0.05%). They were then incubated for at least 24 h under anaerobic conditions before inoculation with the anaerobic bacterial strains. |
| C-300 microfluidics cartridge | Spectradyne | ||
| Chloramphenicol | MP Biomedicals | ICN19032105 | |
| Electron microscope | FEI company | Tecnai G2 SpiritBT | |
| Escherichia coli HST08 (Steller competent cells) | Takara | 636763 | |
| Escherichia coli MP1 | Dr. Mark Goulian (gift) | commensal bacteria derived from mouse gut | |
| Fiberlite 500 mL to 250 mL adapter | ThermoFisher | 010-0151-05 | used with Fiberlite rotor to enable 250 mL bottles to be used for smaller size of starting bacterial culture |
| Fiberlite fixed-angle centrifuge rotor | ThermoFisher | F12-6x500-LEX | fits 6 x 500 mL bottles |
| Formvar Carbon Film 400 Mesh, Copper | Electron microscopy sciences | FCF-400-CU | |
| Glutaraldehyde (EM-grade, 10% aqeous solution) | Electron microscopy sciences | 16100 | |
| Hematin | ChemCruz | 207729B | Stock solution was made in 0.2 M L-histidine solution as 1.2 mg/mL |
| Infinite M Nano+ Microplate reader | Tecan | This equibment was used to measure the mCherry fluorescence | |
| In-Fusion HD Cloning Plus | Takara | 638909 | For cloning of the PCR fragements into the PCR-lineraized vectors |
| JS-5.3 AllSpin Swinging-Bucket Rotor | Beckman Coulter | 368690 | |
| Lauria Bertani (LB) broth, Miller | Difco | 244620 | |
| L-Cysteine Hydrochloride | J.T. Baker | 2071-05 | It should be weighed and added directly to the autoclaved BHI media inside the anaerobic chamber |
| Masterflex Fitting, Polypropylene, Straight, Female Luer to Hose Barb Adapter, 1/8" ID; 25/PK | cole-parmer - special | HV-30800-08 | connection adapters for filtration tubing circuit |
| Masterflex Fitting, Polypropylene, Straight, Male Luer to Hose Barb Adapter, 1/8" ID; 25/PK | cole-parmer - special | HV-30800-24 | connection adapters for filtration tubing circuit |
| Masterflex L/S Analog Variable-Speed Console Drive, 20 to 600 rpm | Masterflex | HV-07555-00 | |
| Masterflex L/S Easy-Load Head for Precision Tubing, 4-Roller, PARA Housing, SS Rotor | Masterflex | EW-07514-10 | |
| Masterflex L/S Precision Pump Tubing, PharmaPure, L/S 16; 25 ft | Cole Palmer | EW-06435-16 | low-binding/low-leaching tubing |
| Menadione (Vitamin K3) | MP | 102259 | Stock solution was made in ethanol as 1 mg/mL |
| MIDIKROS 41.5CM 100K MPES 0.5MM FLL X FLL 1/PK | Repligen | D04-E100-05-N | TFF device we have used to filter up to 2 L of E. coli culture supernatant |
| Nano-Glo Luciferase Assay System | Promega | N1110 | This assay kit was used to measure the luminescence of the nluc reporter protein |
| NanoLuc (Nluc) Luciferase Antibody, clone 965808 | R&D Systems | MAB10026 | |
| nCS1 microfluidics resistive pulse sensing instrument | Spectradyne | ||
| nCS1 Viewer | Spectradyne | Analysis software for particle size distribution | |
| OneTaq 2x Master Mix with Standard Buffer | NEB | M0482 | DNA polymerase master mix used to perform the routine PCR reactions for colony checking |
| Protein LoBind, 2.0 mL, PCR clean tubes | Eppendorf | 30108450 | |
| Q5 High-Fidelity 2x Master Mix | NEB | M0492 | DNA polymerase master mix used to perform the PCR reactions needed for cloning |
| qEV original, 35 nm | Izon | maximal loading volume of 0.5 mL | |
| qEV rack | Izon | for use with the qEV-original SEC columns | |
| qEV-2, 35 nm | Izon | maximal loading volume of 2 mL | |
| Qubit fluorometer | ThermoFisher | Item no longer available. Closest available product is Qubit 4.0 Fluorometer (cat. No. Q33238) | |
| Qubit protein assay kit | ThermoFisher | Q33211 | Store kit at room temperature. Standards are stored at 4 °C. |
| Sorvall Lynx 4000 centrifuge | ThermoFisher | 75006580 | |
| SpectraMax i3x Microplate reader | Molecular Devices | This equipment was used to measure the nanoluciferase bioluminescence | |
| Stericup Quick-release-GP Sterile Vacuum Filtration system (150, 250, or 500 mL) | MilliporeSigma | S2GPU01RE S2GPU02RE S2GPU05RE | One or multiple filters can be used to accommodate working volumes. In our experience, you can filter twice the volume listed on the product size. |
| Uranyl acetate | Electron microscopy sciences | 22400 | |
| Vinyl anaerobic chamber | Coy Lab | ||
| Vivacell 100, 100,000 MWCO PES | Sartorius | VC1042 | |
| Whatman Anotop 10 Plus syringe filters (0.02 micron) | MilliporeSigma | WHA68093002 | to filter MRPS diluent |
Referencias
- Yanez-Mo, M., et al. Biological properties of extracellular vesicles and their physiological functions. Journal of Extracellular Vesicles. 4, 27066 (2015).
- Chatterjee, S. N., Das, J. Electron microscopic observations on the excretion of cell-wall material by Vibrio cholerae. Journal of General Microbiology. 49 (1), 1-11 (1967).
- Ciofu, O., Beveridge, T. J., Kadurugamuwa, J., Walther-Rasmussen, J., Hoiby, N. Chromosomal beta-lactamase is packaged into membrane vesicles and secreted from Pseudomonas aeruginosa. Journal of Antimicrobial Chemotherapy. 45 (1), 9-13 (2000).
- Yonezawa, H., et al. Outer membrane vesicles of Helicobacter pylori TK1402 are involved in biofilm formation. BMC Microbiology. 9, 197 (2009).
- Mashburn, L. M., Whiteley, M. Membrane vesicles traffic signals and facilitate group activities in a prokaryote. Nature. 437 (7057), 422-425 (2005).
- Kato, S., Kowashi, Y., Demuth, D. R. Outer membrane-like vesicles secreted by Actinobacillus actinomycetemcomitans are enriched in leukotoxin. Microbial Pathogenesis. 32 (1), 1-13 (2002).
- Petousis-Harris, H., et al. Effectiveness of a group B outer membrane vesicle meningococcal vaccine against gonorrhoea in New Zealand: a retrospective case-control study. Lancet. 390 (10102), 1603-1610 (2017).
- Kim, O. Y., et al. Bacterial outer membrane vesicles suppress tumor by interferon-gamma-mediated antitumor response. Nature Communications. 8 (1), 626 (2017).
- Thery, C., et al. Minimal information for studies of extracellular vesicles 2018 (MISEV2018): a position statement of the International Society for Extracellular Vesicles and update of the MISEV2014 guidelines. Journal of Extracellular Vesicles. 7 (1), 1535750 (2018).
- Consortium, E. -. T., et al. EV-TRACK: transparent reporting and centralizing knowledge in extracellular vesicle research. Nature Methods. 14 (3), 228-232 (2017).
- Watson, D. C., et al. Efficient production and enhanced tumor delivery of engineered extracellular vesicles. Biomaterials. 105, 195-205 (2016).
- Watson, D. C., et al. Scalable, cGMP-compatible purification of extracellular vesicles carrying bioactive human heterodimeric IL-15/lactadherin complexes. Journal of Extracellular Vesicles. 7 (1), 1442088 (2018).
- Lasaro, M., et al. Escherichia coli isolate for studying colonization of the mouse intestine and its application to two-component signaling knockouts. Journal of Bacteriology. 196 (9), 1723-1732 (2014).
- Kim, J. Y., et al. Engineered bacterial outer membrane vesicles with enhanced functionality. Journal of Molecular Biology. 380 (1), 51-66 (2008).
- Beveridge, T. J. Structures of gram-negative cell walls and their derived membrane vesicles. Journal of Bacteriology. 181 (16), 4725-4733 (1999).
- Reimer, S. L., et al. Comparative analysis of outer membrane vesicle isolation methods with an Escherichia coli tolA mutant reveals a hypervesiculating phenotype with outer-inner membrane vesicle content. Frontiers in Microbiology. 12, 628801 (2021).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados