Method Article
La cristallisation des protéines membranaires dans des mésophases lipidique
Dans cet article
Résumé
Les protocoles décrivent les étapes essentielles pour obtenir des cristaux par diffraction de la qualité d'une protéine membranaire à partir de la reconstitution de la protéine dans une phase lipidique cubique (LCP), trouver les conditions initiales avec LCP-FRAP pré-cristallisation des essais, la mise en place des essais de cristallisation LCP et des cristaux de récolte .
Résumé
Les protéines membranaires exécuter des fonctions critiques dans les cellules vivantes liées à la transduction du signal, le transport et les transformations d'énergie, et, comme tels, sont impliqués dans une multitude de dysfonctionnements et maladies. Cependant, une compréhension structurale et fonctionnelle des protéines membranaires est fortement à la traîne de leurs partenaires solubles, principalement en raison de difficultés liées à leur solubilisation et la génération de cristaux de qualité de diffraction. Cristallisation dans mésophases lipidique (également connu sous le nom de la cristallisation méso ou LCP) est une technique prometteuse qui a été appliquée avec succès à obtenir des structures à haute résolution de rhodopsins microbienne, les protéines photosynthétiques, extérieur barils beta membrane et G récepteurs couplés aux protéines. En méso cristallisation profite d'un environnement de membrane native-like et produit généralement avec des cristaux de la teneur en solvant inférieure et une meilleure commande par rapport à la cristallisation traditionnels de solutions détergentes. La méthode n'est pas difficile, mais nécessite une compréhension du comportement phase lipidique et la pratique dans la manutention des matériaux mésophase visqueux. Ici nous démontrons une manière simple et efficace de faire de LCP et la reconstitution d'une protéine membranaire dans la bicouche lipidique du LCP utilisant un mélangeur à seringue, suivie par la distribution des portions du nanolitre LCP dans un essai ou une plaque de cristallisation, la conduite des essais de pré-cristallisation et la récolte des cristaux à partir la matrice LCP. Ces protocoles fournissent un guide de base pour aborder dans les essais de cristallisation méso; cependant, comme avec n'importe quel expérience de cristallisation, le dépistage étendu et l'optimisation sont nécessaires, et le succès n'est pas nécessairement garantie.
Protocole
Un plan typique d'une expérience de cristallisation dans le méso est montré à la Fig.1 1,2. Pré-cristallisation LCP-FRAP tests sont facultatifs, mais ils peuvent considérablement accélérer le processus de recherche de conditions de cristallisation initiale, particulièrement dans le cas des protéines membranaires difficiles 3.
1. Reconstitution des protéines dans les LCP
- Purifier une protéine membranaire d'intérêt dans une solution détergente et de concentrer les complexes protéine / détergent pour ~ 10 - 20 mg / ml, en prenant soin de ne pas trop concentrer les 1,4 détergent.
- Transfert ~ 25 mg d'un lipide d'hôte LCP (généralement monooléine) ou un mélange de lipides dans un tube de 1,5 ml en plastique et incuber à 40 ° C pendant quelques minutes jusqu'à ce que les lipides fond.
- Fixez un coupleur de la seringue pour une 100 uL étanche seringue.
- Charger la seringue avec le lipide fondu en utilisant une pipette de volume réglable. Noter le volume du lipide dans la seringue.
- Charger une autre seringue 100 pL avec la solution de protéine à une protéine solution à des lipides rapport 2 / 3 v / v.
- Connectez les deux seringues ensemble à travers le coupleur seringue.
- Poussez la seringue pistons en alternance pour déplacer les lipides et de protéines grâce à l'aiguille interne du coupleur, en arrière, jusqu'à ce que la mésophase lipides devient homogène. LCP forme spontanément lors du mélange mécanique, et la protéine devient reconstituée dans la bicouche lipidique du PAFR. Formation du LCP peut être vérifiée par sa cohérence et de transparence gel, et par l'absence de biréfringence lorsqu'on les examine sous un microscope équipé d'polariseurs croisés, ou, si possible, en utilisant X aux petits angles de diffraction des rayons 1.
2. LCP-FRAP pré-cristallisation Tests
LCP-FRAP tests sont conçus pour mesurer les propriétés de diffusion des protéines membranaires reconstitués dans LCP à une variété de conditions de dépistage 3. La diffusion à longue distance de protéines membranaires dans LCP est essentiel pour la cristallisation de succès, cependant, la microstructure de la LCP contraintes de diffusion des protéines de grande taille ou d'agrégats de protéines oligomériques. Une raison fréquente de l'échec d'une expérience de cristallisation dans le méso est une agrégation de protéines rapide conduisant à une perte de diffusion. Il a été démontré que le comportement d'agrégation d'une protéine dépend de la construction d'une protéine particulière, le lipide hôte et la composition de la solution 3 de dépistage.
- Étiquette de la protéine avec un colorant fluorescent (Cy3 ou similaire) à un ratio protéines / colorant de ~ 100 / 1, éliminer le colorant qui n'a pas réagi et se concentrer à la protéine de ~ 1 mg / mL. Étiquette soit amines libres ou thiols libres. Lors de l'étiquetage des amines libres, utilisez pH entre 7 et 7,5 à prédominance label gratuite N-terminale. Soyez conscient que l'étiquetage aminés peuvent également l'étiquette lipides co-purifiée avec la protéine 2,3.
- Reconstituer la protéine étiquetée LCP comme décrit dans la section 1).
- Mettre en place des plaques de dosage comme décrit dans la section 3) en utilisant des solutions de dépistage LCP-FRAP au lieu de 2 écrans cristallisation.
- Incuber les plaques à 20 ° C dans l'obscurité pendant au moins 12 heures pour atteindre un état d'équilibre.
- Placez l'une des plaques sur la station de LCP-FRAP et se concentrer sur le premier puits en utilisant un objectif 10x.
- Acquérir 5 images fluorescentes pour capturer les premières pré-blanchi de l'Etat.
- Déclencher le laser. La puissance du laser et du nombre d'impulsions doit être ajustée à l'eau de Javel ~ 30 - 70% de la protéine marquée au milieu de la tache blanchie.
- Immédiatement après le déclenchement du laser, commencer à enregistrer un rapide post-séquence de blanchiment de ~ 200 images à la cadence la plus rapide possible.
- Suivez avec l'enregistrement d'une lente après-javel séquence de ~ 50 images, la sélection du délai entre les images que 10 à 20 s, selon le taux de diffusion de la protéine.
- Intégrer l'intensité à l'intérieur de l'endroit l'eau de Javel dans tous les cadres et les corriger pour le blanchiment et la lumière des fluctuations d'intensité lors de l'acquisition en divisant l'intensité à l'intérieur de la tache blanchie par l'intensité moyenne d'un spot de référence en dehors de la zone au laser blanchi.
- Normaliser l'intensité corrigée pour rendre l'intensité de pré-blanchi égal à 1 et l'intensité initiale blanchi égal à 0.
- Monter la courbe de l'intensité normalisée en fonction du temps, F (t), en utilisant l'équation suivante 5:
F (t) = M x exp (-2T / t) x (I 0 (2T / t) + I 1 (2T / t)), (Eq.1)
où M est la fraction mobile de molécules diffusantes, T est le temps caractéristique de diffusion, t est le temps réel de chaque image enregistrée, I 0 et I 1 sont les e 0 et 1 er afin fonctions de Bessel modifiées. - Calculer le coefficient de diffusion, D, comme:
D = R 2 / 4T, (Eq.2)
où R est le rayon de la tache blanchie. - Déplacez to le bien suivant et répétez les étapes 2,5) - 2,13).
- Comparez les fractions mobiles et les coefficients de diffusion obtenus pour les conditions de dépistage différents. Conception nouvelle cristallisation des écrans basés sur les composants qui ont facilité la diffusion des protéines et des conditions d'exclusion pour lesquelles la diffusion de protéines n'a pas été observé. Si la protéine ne diffusent pas dans l'une des conditions dépistage, envisager d'élargir l'espace de dépistage ou d'essayer de construire une nouvelle protéine.
3. Configuration des essais de cristallisation LCP
- Reconstituer la protéine dans LCP comme décrit dans la section 1).
- Transfert du LCP protéines chargées dans un 10 uL étanche seringue fixée à un distributeur de seringues répétitives.
- Fixer une aiguille courte amovible (calibre 26, longueur 10 mm) à la seringue de 10 mL.
- Distribuer 200 nL bolus de LCP à la surface de quatre puits adjacents formant un carré de 2x2.
- Superposition de chacun des bolus LCP avec 1 ul de solution de cristallisation écran correspondant.
- Cap quatre puits chargé avec une lamelle de verre de 18 mm carrés. Appliquez une légère pression sur la lamelle pour sceller les puits.
- Répétez les étapes 3.4) -3.6) avec la prochaine série de 4 puits jusqu'à ce que la plaque entière est remplie.
- Incuber la plaque à une température constante, et vérifie périodiquement la formation de cristaux et de croissance.
4. Récolte Cristaux de LCP
- Placer une plaque avec des cristaux de protéines sous un microscope stéréo avec zoom variable, équipé d'un polariseur linéaire tournante et analyseur.
- Focus sur le bien d'intérêt en utilisant un zoom de faible puissance afin que le bien tout est placé dans le champ de vision.
- Score le verre lamelle en quatre coups faisant un carré à l'intérieur des limites bien en utilisant un angle vif d'une pierre de coupe capillaire en céramique.
- Appuyer sur le pourtour marqué avec une forte forte-point des pincettes pour propager les rayures grâce à l'épaisseur du verre couvre-objet.
- Percez deux petits trous aux coins opposés du carré marqué.
- Injecter uL quelques solution de précipitant à travers un des trous pour réduire la déshydratation au cours des étapes ultérieures.
- En utilisant une sonde d'aiguille à angle pointu briser le verre le long d'un ou deux côtés pour libérer la place découpe.
- Soulevez délicatement le regarder carrés de verre pour le bolus phase cubique. Si le bolus est collé à la lamelle, puis retournez le carré de verre et placez sur le fond du puits.
- Ajouter un supplément de quelques uL d'une solution de précipitant, complété par un cryo-protecteur, si nécessaire, au-dessus du bol phase cubique exposés dans le puits.
- Augmenter l'agrandissement du microscope et de se concentrer sur un cristal.
- Ajustez l'angle entre le polariseur et l'analyseur pour augmenter le contraste entre le cristal biréfringent et l'arrière-plan, tout en gardant assez de lumière pour voir la boucle de récolte.
- Sélectionner un MicroMount MiTeGen avec un diamètre correspondant à la taille des cristaux et ensuite récolter le cristal directement à partir du LCP en l'excavation dans le MicroMount.
- Flash geler les MicroMount avec le cristal récoltés dans l'azote liquide, et l'expédier à une ligne de lumière synchrotron à rayons X de collecte de données 6.
5. Les résultats représentatifs:
Une conçu beta 2-adrénergiques humains G récepteurs couplés aux protéines (β 2 AR-T4L) a été exprimée dans le baculovirus cellules d'insectes Sf9 infectées et purifié dans dodecylmaltoside (DDM) / cholestérol hémisuccinate (SHC) une solution de détergent lié à un agoniste partiel inverse carazolol 7. La protéine a été marquée avec Cy3 ester NHS et utilisés dans les LCP-FRAP pré-cristallisation des dosages (Figure 2). Écrans grille grossière basée sur plusieurs conditions sélectionnées à partir des résultats des tests de LCP-FRAP produite initiaux semblables à des cristaux frappe (figure 3). Optimisation des conditions de précipitation a donné des cristaux par diffraction de qualité (figure 4).
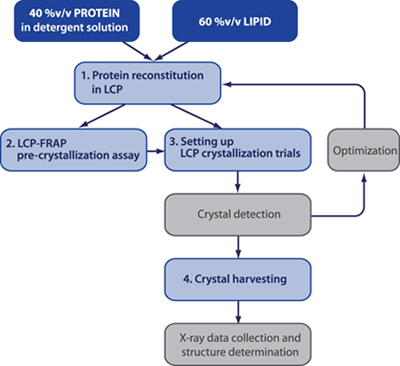
Figure 1. Organigramme d'une expérience de cristallisation LCP typique. Étapes dans les cases grises ne sont pas décrites dans les protocoles actuels.
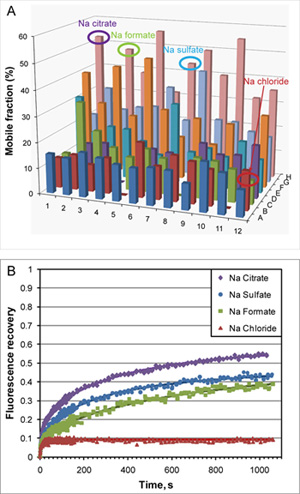
Figure 2. LCP-FRAP dosage avec β 2 AR-T4L/carazolol dans monooléine LCP base. A) les résultats d'un essai LCP-FRAP effectuées à une machine automatique à haut débit en mode, dans lequel chaque échantillon d'une plaque de 96 puits est blanchie séquentiellement et de recouvrement de fluorescence est mesurée après une incubation de 30 min. Le taux de récupération obtenus par fluorescence, qui représentent la fraction mobile dans chaque échantillon, sont tracées pour tous les 96 échantillons. Les solutions de criblage contiennent Tris 0,1 M pH 8, 30% v / v PEG 400 combiné avec 48 différents sels à deux concentrations différentes. B) Les profils de recouvrement de fluorescence pour rep plusieurssentant des conditions. Courbes en trait plein représentent s'adapte par l'Eq. 1.L fractions mobiles et les coefficients de diffusion sont déterminés en utilisant les équations. 1 et 2. La récupération rapide de moins de 10% dans l'échantillon contenant du chlorure de Na est due aux lipides marqués par fluorescence co-purifiée avec la protéine.
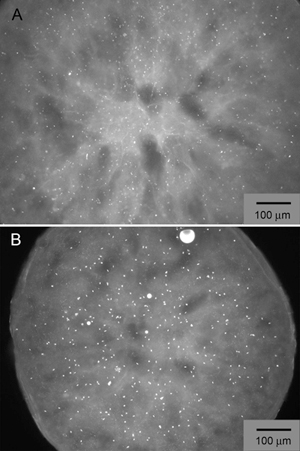
Figure 3. Coups de cristal initiale de β 2 AR-T4L/carazolol obtenue par une grille grossière de dépistage autour de la plupart des conditions prometteuses identifiées par LCP-FRAP, contenant du sulfate de Na (panneau A) et Na Formiate (panneau B). La protéine est étiqueté avec Cy3 ester NHS et les images fluorescentes sont prises en utilisant une excitation à 543 nm et émission à 605 nm.
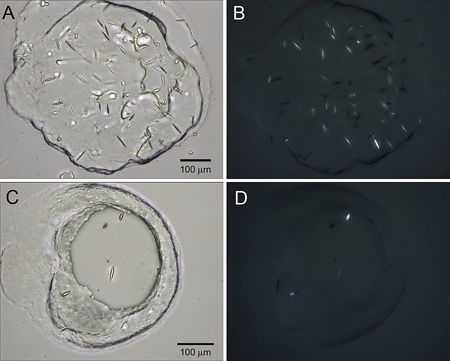
Figure 4. Cristaux optimisée des β 2 AR-T4L/carazolol. Les images de cristaux cultivés en présence de sulfate de Na (panneaux A et B) et K formate (panneaux C et D) sont prises en mode fond clair (panneaux A et C) et en utilisant polariseurs croisés (panneaux B et D).
Discussion
Les protocoles de fournir une orientation de base visuel pour les principales étapes à effectuer dans les expériences de cristallisation méso. Plus en profondeur les détails relatifs à ces protocoles, en soulignant les pièges possibles, des lacunes ou des itinéraires alternatifs sont disponibles nulle part ailleurs 1,2. En option LCP-FRAP tests peuvent aider lors des phases antérieures de choisir le concept le plus prometteur de protéines, de lipides et d'additifs d'hôte LCP lipides, ainsi que limiter la gamme des facteurs déclenchants possibles et les conditions de tampon 3. Une fois un succès cristallisation initiale est trouvé, il devrait être optimisé pour obtenir des cristaux de meilleure qualité. Optimisation des conditions de cristallisation dans le méso est essentiellement similaire à l'optimisation des conditions pour les protéines solubles avec l'ajout de paramètres supplémentaires associés à la composition de LCP 1. Des cristaux de protéines membranaires cultivées en mésophase lipidique sont généralement de plus petite taille que les cristaux obtenus dans une solution détergente, mais plus ordonnée, par conséquent, bénéficier fortement de l'aide microfoyer faisceaux disponibles auprès de sources synchrotron moderne 6.
La plupart des procédures liées à la cristallisation méso, y compris la mise en place des plaques de cristallisation ou de dosage, la conduite LCP-FRAP tests et la détection des cristaux, ont été semi ou entièrement automatique 1,2,8,9, permettant le dépistage d'une large gamme de conditions tout en consommant de petites quantités de protéines et de lipides. D'autre part, les reconstitutions de protéines dans LCP et la récolte de cristal reste des opérations manuelles fastidieuses et plus et, par conséquent, ont un besoin d'amélioration.
Déclarations de divulgation
Remerciements
Ce travail a été financé en partie par les subventions des NIH et de GM073197 RR025336.
matériels
| Name | Company | Catalog Number | Comments |
| 100 μL gas-tight syringe | Hamilton Co | 7656-01 | 2 syringes are required |
| 10 μL gas-tight syringe | Hamilton Co | 7653-01 | |
| Syringe coupler | Hamilton Co | 7770-02 30902 | The coupler can be made using available parts as described in refs. 10 |
| Repetitive syringe dispenser | Hamilton Co | 83700 | The repetitive syringe dispenser can be modified to reduce dispensing volume by ~3 times11 |
| Short (0.375”) flat-tipped removable needle (point style 3, gauge 26) | Hamilton Co | 7804-03 | |
| 96-well glass sandwich plate | Marienfeld | 08 900 03 | For manual operations it is more convenient to assemble the glass sandwich plate using a standard microscope glass slides and a double sticky tape with punched holes1,2,12. |
| Glass cover slip | Electron Microscopy Sciences | 63787-01 | |
| monoolein | Sigma-Aldrich | M7765 | |
| Crystallization screens | Hampton Research, Molecular Dimensions, Emerald Biosystems, Jena Bioscience | Most of available commercial screens can be used for initial screening. Conditions that consistently disrupt LCP can be diluted 2x for better compatibility13. | |
| Capillary cutting stone | Hampton Research | HR4-334 | |
| Fine point tweezers | Ted Pella, Inc. | 510 | |
| Angled sharp probe | Ted Pella, Inc. | 13650 | |
| MicroMounts | MiTeGen | M1-Lxx-xx | Select MicroMount diameter to match the crystal size |
Références
- Caffrey, M., Cherezov, V. Crystallizing membrane proteins using lipidic mesophases. Nat. Protoc. 4, 706-731 (2009).
- Cherezov, V., Abola, E., Stevens, R. C. Recent progress in the structure determination of GPCRs, a membrane protein family with high potential as pharmaceutical targets. Methods Mol. Biol. 654, 141-170 (2010).
- Cherezov, V., Liu, J., Hanson, M. A., Griffith, M. T., Stevens, R. C. LCP-FRAP assay for pre-screening membrane proteins for in meso crystallization. J. Cryst. Growth Design. 8, 4307-4315 (2008).
- Misquitta, Y., Caffrey, M. Detergents destabilize the cubic phase of monoolein: implications for membrane protein crystallization. Biophys. J. 79, 394-405 (2003).
- Soumpasis, D. M. Theoretical analysis of fluorescence photobleaching recovery experiments. Biophys. J. 41, 95-97 (1983).
- Cherezov, V., Hanson, M. A., Griffith, M. T., Hilgart, M. C., Sanishvili, R., Nagarajan, V., Stepanov, S., Fischetti, R. F., Kuhn, P., Stevens, R. C. Rastering strategy for screening and centering of microcrystal samples of human membrane proteins with a sub-10 micrometer size X-ray synchrotron beam. J. R. Soc. Interface. 6, S587-S597 (2009).
- Cherezov, V., Rosenbaum, D. M., Hanson, M. A., Rasmussen, S. G., Thian, F. S., Kobilka, T. S., Choi, H. J., Kuhn, P., Weis, W. I., Kobilka, B. K., Stevens, R. C. High-resolution crystal structure of an engineered human beta2-adrenergic G protein-coupled receptor. Science. 318, 1258-1265 (2007).
- Cherezov, V., Peddi, A., Muthusubramaniam, L., Zheng, Y. F., Caffrey, M. A robotic system for crystallizing membrane and soluble proteins in lipidic mesophases. Acta Crystallogr. D. 60, 1795-1807 (2004).
- Kissick, D. J., Gualtieri, E. J., Simpson, G. J., Cherezov, V. Nonlinear optical imaging of integral membrane protein crystals in lipidic mesophases. Anal. Chem. 82, 491-497 (2010).
- Cheng, A., Hummel, B., Qiu, H., Caffrey, M. A simple mechanical mixer for small viscous lipid-containing samples. Chem. Phys. Lipids. 95, 11-21 (1998).
- Cherezov, V., Caffrey, M. A simple and inexpensive nanoliter-volume dispenser for highly viscous materials used in membrane protein crystallization. J. Appl. Cryst. 38, 398-400 (2005).
- Cherezov, V., Caffrey, M. Nano-volume plates with excellent optical properties for fast, inexpensive crystallization screening of membrane proteins. J. Appl. Cryst. 36, 1372-1377 (2003).
- Cherezov, V., Fersi, H., Caffrey, M. Crystallization screens: compatibility with the lipidic cubic phase for in meso crystallization of membrane proteins. Biophys J. 81, 225-242 (2001).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon