Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Analyses quantitatives de tous influenza de type A hémagglutinines virales et les neuraminidases utilisant des anticorps Universal en simples essais slot blot
* Ces auteurs ont contribué à parts égales
Dans cet article
Erratum Notice
Résumé
Une méthode simple fente blot a été développé pour la quantification de l'hémagglutinine de la grippe virale et la neuraminidase utilisant des anticorps ciblant universelle leurs séquences les plus conservées identifiées par l'analyse bioinformatique. Cette approche innovatrice pourrait fournir une alternative utile pour la détermination quantitative de tous hémagglutinine et la neuraminidase virale.
Résumé
L'hémagglutinine (HA) et neuraminidase (NA) sont deux protéines de surface du virus de la grippe qui sont connus pour jouer un rôle important dans le cycle de vie du virus et l'induction de réponses immunitaires protectrices 1,2. Comme la principale cible des anticorps neutralisants, HA est actuellement utilisé comme marqueur de la puissance et le vaccin contre la grippe est mesurée par immunodiffusion radiale simple (SRID) 3. Cependant, la dépendance de SRID sur la disponibilité des immunsérums correspondants sous-type entraîne un minimum de 2-3 mois de retard pour la sortie de chaque nouveau vaccin. Par ailleurs, malgré les preuves que NA induit aussi une immunité protectrice 4, le montant de NA vaccins contre la grippe n'est pas encore standardisé en raison d'un manque de réactifs appropriés ou méthode analytique 5. Ainsi, de simples méthodes alternatives permettant de quantifier les antigènes HA et NA sont souhaitables pour une libération rapide et un meilleur contrôle de la qualité des vaccins antigrippaux.
Régions universellement conservées dans tous la grippe A disponible HA et NA séquences ont été identifiés par analyse bioinformatique 6-7. Une séquence (désigné comme Uni-1) a été identifié dans l'épitope ne universellement conservé de la HA, le peptide de fusion 6, tandis que deux séquences conservées ont été identifiées dans les neuraminidases, un proche du site enzymatique actif (désigné comme HCA-2) et le autre près de la N-terminale (désigné comme HCA-3) 7. Peptides avec ces séquences d'acides aminés ont été synthétisés et utilisés pour immuniser des lapins pour la production d'anticorps. L'anticorps dirigé contre l'épitope Uni-1 de HA a été en mesure de se lier à 13 sous-types de la grippe A HA (H1-H13) alors que les anticorps contre le HCA-2 et HCA-3 régions de NA ont été capables de se lier tous les 9 sous-types NA. Tous les anticorps ont une spécificité remarquable contre les séquences virales comme en témoigne le constat que pas de réactivité croisée aux protéines allantoïdien a été détectée. Ces anticorps ont ensuite été utilisés universelle pour développer des essais slot blot pour quantifier HA et NA dans les vaccins de grippe A sans la nécessité d'antisérums spécifiques 7,8. Échantillons de vaccin ont été appliquées sur une membrane de PVDF en utilisant un appareil de slot blot ainsi que des normes de référence dilué à différentes concentrations. Pour la détection de HA, les échantillons et les standards ont d'abord été dilué dans une solution saline tamponnée Tris (TBS) contenant de l'urée 4M tandis que pour la mesure de l'AN, ils ont été dilués dans du TBS contenant 0,01% Zwittergent que ces conditions a considérablement amélioré la sensibilité de détection. Suite à la détection de l'HA et NA antigènes par immunoblot avec leurs anticorps universel, intensités du signal ont été quantifiées par densitométrie. Montants des HA et NA dans les vaccins ont ensuite été calculées en utilisant une courbe standard établie avec les intensités du signal des différentes concentrations des références utilisées.
Étant donné que ces anticorps se lient à des épitopes universel en HA ou NA, les enquêteurs intéressés pourraient les utiliser comme outils de recherche dans les immunoessais autre que le slot blot seulement.
Protocole
1. Préparation des réactifs et du matériel
- Avant de commencer la procédure de slot blot, préparer 20_mls de solution d'urée 4M dans du Tris-solution saline tamponnée (Tris 20 mM, NaCl 137 mM, pH 7,6) (TBS) pour l'hémagglutinine ou HA, slot blot, ou d'un 20_mls% 0,01 Zwittergent solution dans le SCT pour la neuraminidase ou NA, slot blot. Alors que l'urée 4M doit être préparé à chaque fois, une solution stock à 10% en DH Zwittergent 2 O est stable pendant au moins 6 mois à température ambiante et peut donc être dilué à 0,01% dans le TBS avant chaque dosage.
- Préparer 2000 ml de tampon de lavage en ajoutant Tween-20 à une solution de TBS à une concentration finale de 0,1%. Préparer 80 ml de tampon de blocage en dissolvant la poudre de lait écrémé (buvard de grade non gras du lait en poudre) pour une concentration finale de 5% p / v dans du tampon de lavage.
- Activer la membrane de PVDF (pré-coupés à une taille de 9 x 12 cm) dans le méthanol pendant 15 secondes, suivie par une 2 minutes rincer dans le trou DDH 2 O. Faire tremper la membrane dans du TBS jusqu'à utilisation. Pré-humide 3 feuilles de Bio-Dot papier filtre dans SF SCT jusqu'à utilisation.
2. Préparation des échantillons et des vaccins contre la grippe standard de référence pour HA slot blot
Normes de référence de la grippe le vaccin avec un contenu HA pré-déterminé correspondant aux souches vaccinales pour être testés ont été obtenus à partir du Centre de recherche et d'évaluation des produits biologiques (CBER / FDA, États-Unis) ou le National Institute for Biological Standard et de contrôle (NIBSC, Royaume-Uni) et sont utilisés pour la quantification HA par slot blot. Les enquêteurs pourraient également préparer leurs propres normes d'antigènes en utilisant des procédures établies comme décrit dans les références 9 et 10.
- Pour les antigènes de référence HA et échantillons de vaccin test: Diluer le stock antigène HA de référence de l'urée 4M / SCT pour les concentrations suivantes: 0, 0,0938, 0,1875, 0,375, 0,75, 1,5, 3 et 6 ha pg / ml. Mélangez bien. Ensuite, diluer les échantillons de test de vaccins à usage humain obtenu par les producteurs de vaccin ou fait maison à des fins de recherche scientifique dans l'urée 4M / SCT et bien mélanger. Alors que des copies de l'antigène de référence et des échantillons de vaccin peut être exécuté, triples sont préférés. Préparer 3 dilutions de chaque échantillon (2 fois la différence) pour permettre à la concentration de l'échantillon pour tomber sous la courbe standard. Préparer 450 ul ul ou 650 de chaque antigène de référence ou la dilution de l'échantillon de test de vaccin pour lancer des doubles ou triples, respectivement. Un vaccin grippe monovalent peut être testé avec cette méthode slot blot. Le contenu HA des antigènes de référence a été précédemment déterminé à l'aide du SRID qui est le test actuellement utilisé pour les préparations standard de vaccin contre la grippe. Le contenu HA déterminé par SRID a été utilisé comme la concentration de référence antigène HA initiales d'actions pour la préparation des dilutions de la courbe de slot blot standard.
3. Préparation des échantillons vaccin contre la grippe et la norme de référence pour NA slot blot
Normes de référence de la grippe le vaccin correspondant aux souches vaccinales pour être testés ont été obtenus à partir du Centre de recherche et d'évaluation des produits biologiques (CBER / FDA, États-Unis) ou le National Institute for Biological Standard et de contrôle (NIBSC, Royaume-Uni) et sont utilisés pour la quantification de NA par slot blot. La teneur en Na de ces échantillons de référence a été déterminée par analyse SDS-PAGE des échantillons déglycosylé en conjonction avec l'analyse de densitométrie à balayage, comme décrit précédemment 9, 10 avec de légères modifications. En bref, les échantillons de référence déglycosylé vaccin (5 ug) ont été mélangés avec un tampon d'échantillon et chargées sur le gel. Le gel a été exécuté à 20 mA pendant environ 90 min jusqu'à ce que le colorant suivi exécutez simplement hors du gel, suivie d'une coloration Sypro. La quantification des protéines densitométrie a été réalisée en utilisant un système de documentation de gel Fluorchem (Alpha Innotech). Le montant de la NA a été déterminé en fonction du ratio des protéines NA aux protéines totales que déterminée par dosage de Lowry. Les échantillons de référence préparés en utilisant cette méthode peut ensuite être utilisé dans slot blot pour la quantification des matières NA dans des échantillons de vaccins auprès des fabricants de vaccins.
- Pour les antigènes de référence NA et échantillons de vaccin test: Diluer le stock NA antigène de référence de 0,01% Zwittergent / SCT pour les concentrations suivantes: 0, 0,039, 0,078, 0,1562, 0,3125, 0,625, 1,25, 2,5, 5 et 10 ug NA / ml. Mélangez bien. Ensuite, diluer les échantillons de test de vaccins à usage humain obtenu par les producteurs de vaccin ou fait maison à des fins de recherche scientifique dans 0,01% Zwittergent / SCT et bien mélanger. Alors que des copies de l'antigène de référence et des échantillons de vaccin peut être exécuté, triples sont préférés. Préparer 3 dilutions de chaque échantillon (2 fois la différence) pour permettre à la concentration de l'échantillon pour tomber sous la courbe standard. Préparer 450 ul ul ou 650 de chaque antigène de référence ou la dilution de l'échantillon de test de vaccin pour lancer des doubles ou triples, respectivement. Un vaccin grippe monovalent peut être testée d'esprith cette méthode slot blot.
4. Assemblée de l'appareil Bio-Dot microfiltration SF et buvard d'échantillons sur une membrane PVDF
- Réunir un préalablement nettoyées et séchées Bio-Dot appareil de microfiltration SF. Placer la plaque de support d'étanchéité dans le collecteur d'un aspirateur et placer le joint d'étanchéité sur les 3 top.Place humidifié feuilles de SF Bio-Dot filtre en papier sur le joint, suivie par la membrane pré-imbibé de PVDF. Placez le gabarit de l'échantillon sur le dessus de la membrane et le doigt-serrez les quatre vis en utilisant un modèle diagonal traversant pour assurer une application uniforme de la pression sur la surface de la membrane.
- Vérifiez que la vanne 3 voies est d'exposer le collecteur d'aspiration à la source de vide avant de se tourner uniquement sur la pompe et le raccordement du vide.
- Tournez sur la pompe et se connecter à l'appareil Bio-Dot. Assurez-vous que la vanne de flux est placé à un niveau inférieur au puits d'échantillon pour un drainage rapide et appropriée des échantillons dans les étapes suivantes.
- Répétez l'étape vis de serrage à l'aide de la diagonale traversant. Serrage des vis tandis que le vide est appliqué assure une meilleure étanchéité et empêche la contamination croisée entre les puits.
- Changer la vanne de débit afin d'exposer le collecteur d'air et de vide pour éteindre la pompe.
- Appliquer 100 ul de TBS à tous les puits à l'aide d'une pipette multicanaux pour réhydrater la membrane assurant ainsi contraignante uniforme de l'antigène. Des précautions doivent être prises pour éviter la formation de bulles et d'appliquer la solution dans le milieu du puits, au plus près que possible du fond, afin de couvrir la fente uniformément. Burst toute bulle d'air introduit accidentellement avec une pointe de pipette.
- Changer la vanne de débit afin d'exposer la variété à la fois à l'air et le vide, tourner sur la pompe, et doucement le tampon de vidange des puits en mettant un doigt sur le port exposé à l'air pour réguler la quantité de vide.
- Changer la vanne de débit afin d'exposer le collecteur d'air dès que le tampon est complètement vidé de tous les puits. Eteignez la pompe ou de débrancher l'aspirateur.
- Appliquer 200 ul de chaque norme ou la dilution des échantillons de vaccins par puits. Échantillons Pipet un à la fois, dans le centre de chaque puits, au plus près que possible du fond, en prenant soin d'éviter d'introduire des bulles d'air. Burst toute bulle d'air introduit accidentellement avec une pointe de pipette. Mettez 200 pi de tampon de dilution de l'échantillon (4M urée / SCT ou 0,01% Zwittergent / SCT) dans les puits inutilisés afin d'assurer à vide appropriée aux puits en usage.
- Régler la vanne de débit afin d'exposer la variété à la fois à l'air et le vide. Tournez sur la pompe (ou rebranchez l'aspirateur) et délicatement les échantillons permettent de vider complètement les puits en contrôlant la quantité de vide avec un doigt sur le port exposé à l'air. Retirer le doigt du port à libérer le vide dès que tous les échantillons ont drainé.
- Immédiatement ajouter 200 ul de TBS dans chaque puits à l'aide d'une pipette multicanaux. Appliquez un léger vide pour drainer et laver les puits en contrôlant la quantité de vide avec un doigt sur le port exposé à l'air.
- Répéter l'étape de lavage décrite à l'étape 4.11. Dès que les puits ont complètement vidé, desserrez les vis du gabarit de l'échantillon et éteignez le vide pour éviter le surséchage les puits. Procéder immédiatement à retirer la membrane.
- Placer la membrane dans un tampon bloquant et incuber une nuit à 4 ° C, avec doux balancement. Utiliser suffisamment de tampon de blocage pour couvrir complètement la membrane.
5. Immunoblot des antigènes HA et NA
- Après la nuit d'incubation dans un tampon bloquant, laver la membrane deux fois pendant 5 minutes avec TBS/0.1% Tween-20 tampon de lavage. Pour tous les lavages et les incubations, d'assurer la membrane est complètement recouverte de solution.
- Incuber la membrane avec un anticorps de lapin universelle contre HA (comme Uni-1) ou NA (comme HCA-2 ou HCA-3) dilué dans 5% p / v de BSA dans le tampon de lavage pendant une heure à température ambiante, avec douceur bascule. Concentrations d'anticorps optimal doivent être déterminés pour chaque stock d'anticorps. Les dilutions de 1:4000 de lapin anti-sérum a donné des résultats optimaux pour les anticorps ci-dessus mentionnés.
- Lavez la membrane à trois reprises, à température ambiante avec doux balancement pendant 15 minutes chaque fois, pour enlever toute anticorps primaires non liés.
- Incuber la membrane avec une HRP anti-lapin conjugué anticorps secondaire. Utiliser une dilution 1:50000 de la Chèvre Thermo ImmunoPure IgG anti-lapin, des anticorps peroxydase conjuguée au tampon de blocage et incuber à température ambiante pendant 30 minutes avec doux balancement.
- Lavez la membrane à trois reprises, se balancer pendant 15 minutes chaque fois, à température ambiante avec un tampon de lavage pour enlever tout anticorps non secondaire.
- Laver la membrane avec TBS pendant 5 minutes avec doux balancement pour éliminer les résidus de détergent Tween-20 à partir de la surface de la membrane.
- Préparer le substrat avec 3 ml de chaque reagent de l'Ouest SuperSignal Dura Durée kit Substrat étendue de Thermo Scientific et bien mélanger.
- Placer la membrane sur un papier tissu sec pour enlever délicatement toute l'excès de tampon TBS.
- Transférer la membrane d'un récipient sec et ajouter le substrat pour couvrir toute la membrane. Incuber 5 minutes avec doux balancement, à température ambiante.
- Retirez le substrat en excès en tamponnant délicatement la membrane sur du papier absorbant.
- Exposer la membrane d'un film chimiluminescence. La durée de l'exposition aura besoin d'être optimisé pour éviter une saturation du signal, mais sera généralement comprise entre 10 secondes et 10 minutes.
- Effectuer des analyses de densitométrie sur le film développé en utilisant un appareil d'imagerie de gel comme le système de documentation de gel Fluorchem (Alpha Innotech) suivant les instructions du fabricant. Les valeurs de densité pour chaque série de répétitions des antigènes de référence et des échantillons de vaccin test est ensuite calculée. Bien que les normes d'antigène et échantillons de vaccin peut être exécuté en double, triples sont préférés. Les valeurs de densité pour les répétitions doit être très semblable. Des différences significatives entre les répétitions indiquer un problème technique probable lors de la procédure. Une courbe standard dépendant de la concentration est établie en reportant les valeurs de densité moyenne par rapport à la quantité (en ng) d'HA ou de NA antigène mis dans chaque fente, de la norme de référence. L'utilisation appropriée d'ajustement de courbe de calibration dans les immunoessais est essentielle pour quantifier précisément HA et NA. La régression linéaire, obtenu en traçant la réponse (y) par rapport à la concentration (x) en utilisant la partie linéaire de la courbe de réponse (y = ax + b) est la méthode la plus simple pour la quantification des analytes. Si un plus large éventail d'analytes est considéré pour le calcul de la concentration, de la logistique à quatre paramètres (4PL) modèle pour immunodosages actuellement acceptées doivent être utilisés. Une variété de logiciels est disponible pour les chercheurs intéressés à envisager. Dans le cas de l'essai slot blot décrit, en convertissant les valeurs axe des x pour échelle log permet à la courbe à ajuster un modèle 4-PL et l'utilisation d'une pente de régression non linéaire variable pour calculer les montants des effacé HA et NA les échantillons vaccin testé est donc possible. Nous avons donc régulièrement utiliser ce modèle pour nos analyses. Comme les échantillons de vaccin tests ont été dilués dans l'urée 4M soit / SCT ou 0,01% Zwittergent / SCT avant d'être effacé sur la membrane, le facteur de dilution pour chaque échantillon doit être pris en compte pour déterminer le contenu HA et NA du test original échantillons de vaccin. Il est suggéré que chaque échantillon vaccin test sera exécuté dans trois dilutions différentes (2 fois la différence) dans le but pour un ensemble de valeurs de densité pour tomber sous la courbe standard. Les valeurs de densité supérieure à la plage courbe standard pour toutes les dilutions des échantillons testés vaccin doivent être diluée davantage pour HA ou la quantification précise de NA. Si les valeurs de densité sont en dessous du bas de la courbe, les échantillons doivent être dilués à un faible facteur de dilution.
6. Les résultats représentatifs:
Analyse bioinformatique de l'ensemble de la grippe A disponible séquences HA confirmé la N-terminale de la sous-unité HA2 (le peptide de fusion) que la seule région conservée de HA. La figure 1 montre le taux de conservation pour chaque position d'acide aminé de la séquence consensus identifiés. Deux variantes ont été identifiées à des positions 2 (L-> I) et 12 (G-> N) du 14 N-terminale d'acides aminés de la HA2, mais de telles variations ont été trouvés à ne pas affecter la liaison entre les anticorps et les variantes peptide 6 . L'épitope Uni-1 (GLFGAIAGFIEGGW) a été choisi pour développer un anticorps contre l'HA universelle. Cet anticorps a démontré une spécificité remarquable pour des séquences virales et est capable de se lier à 13 sous-types de grippe A HA (H1-H13) (figure 2).
En utilisant une approche similaire, deux séquences universellement conservées ont été identifiées dans tous grippe A NA, l'une à proximité du site enzymatiquement active (HCA-2) (figure 3A) et l'autre à l'extrémité N-terminale (HCA-3) (figure 3B) . Peptides avec ces séquences d'acides aminés ont été utilisés comme antigènes pour produire des anticorps contre le NA universelle. Les anticorps contre les deux épitopes sont capables de se lier à tous les 9 sous-types de NA et a montré très peu de réactivité croisée aux protéines allantoïdien ou cellulaire, démontrant ainsi une haute spécificité pour les séquences NA virale (figure 4).
La figure 5 montre un aperçu de la méthode de slot blot pour la quantification de la grippe HA et NA.
Exemples de HA et NA antigène slot blot sont illustrés aux figures 6 et 7. La figure 6A et 6C montre des résultats représentatifs après la détection de l'antigène HA dans une norme de référence de vaccin antigrippal et les échantillons de vaccin, respectivement. Chaque échantillon (standard ou d'un vaccin) a été exécuté en deux exemplaires, dans les puits adjacents. Les doublons doivent montrer similaintensités r suite à la détection. Optimisation des dilutions d'anticorps, l'incubation et la durée d'exposition peut être nécessaire selon les anticorps utilisés.
Un exemple d'une courbe typique standard obtenue suite à la détection de diverses concentrations de HA à partir d'un échantillon standard de référence est le vaccin le montre la figure 6B. La concentration de l'antigène HA est proportionnelle à l'intensité du signal suite à la détection par chimiluminescence de la tache à sous et correspond au modèle courbe 4-PL convenable pour cette gamme de concentration (0,0938 à 6 mg HA / ml).
La figure 7 montre des résultats représentatifs de la détection de l'antigène NA dans une norme de référence de vaccin antigrippal et dans des échantillons de vaccins. L'analyse a montré que la densité de l'intensité du signal obtenu par détection de l'antigène NA différentes dilutions d'une norme de référence vaccin par slot blot est proportionnelle à la concentration de SO (figure 7A). La courbe standard résultant ajuste un modèle 4-PL pour cette gamme de concentration (0,039 à 10 mg NA / ml), comme le montre la figure 7B. Figure 7C montre un exemple d'une analyse par transfert fente de la teneur en Na dans des échantillons de vaccin contre la grippe. Chaque échantillon a été dosé en double exemplaire, dans les puits adjacents.

Figure 1. Taux de conservation de l'épitope Uni-1 dans la région de peptide de fusion de la grippe A HA.
Analyse bioinformatique de l'ensemble de la grippe A disponible séquences HA a confirmé que le peptide de fusion (situé à l'extrémité N-terminale de la sous-unité HA2) est la seule région universellement conservé de la HA. Notez que les deux variantes à la position 2 (L-> I) et 12 (G-> N) ont été trouvés pour ne pas affecter la fixation des anticorps 6. Un anticorps universels capables de se lier 13 différents sous-types de la grippe A HA (H1-H13) a été développé en utilisant l'Uni-1 épitope (GLFGAIAGFIEGGW).
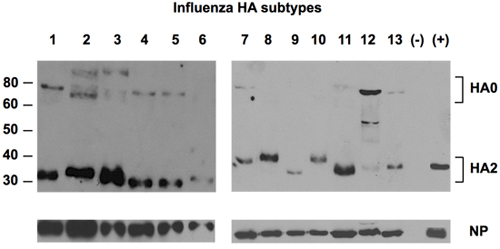
Figure 2. Détection des 13 sous-types de HA par des anticorps contre l'HA universelle.
Liquide allantoïdien de 13 sous-types de virus influenza A propagé dans des œufs embryonnés ont été fractionnés en SDS-PAGE, suivie par la détection des protéines HA en utilisant l'anticorps contre l'épitope universel Uni-1 de HA. Protéines NP a été détecté comme le contrôle du chargement à l'aide d'un lapin polyclonaux NP-anticorps spécifique. Contrôle négatif (-) a été fluide allantoïdien d'oeufs sains. Contrôle positif (+) était un étalon de référence de H1 à partir NIBSC, Royaume-Uni
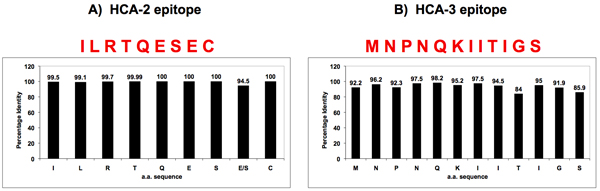
Figure 3. Homologie de séquence de la grippe A NA près du site enzymatiquement active et la N-terminale.
Deux séquences universellement conservées ont été identifiées dans la grippe A NA par la bioinformatique, l'un situé près du site enzymatique actif (HCA-2) (partie A), l'autre à l'extrémité N-terminale (HCA-3) (partie B). Peptides avec ces séquences d'acides aminés conservés ont été synthétisées et utilisées pour générer des anticorps contre le NA universelle.

Figure 4. Détection des 9 sous-types de NA NA par les anticorps.
Liquide allantoïdien des sous-types NA neuf des virus influenza A propagé dans des œufs embryonnés ont été fractionnés en SDS-PAGE, suivie par la détection des protéines NA utilisant le HCA-2 (partie A) et le HCA-3 (Groupe B) anticorps. Protéines NP a été détecté comme le contrôle du chargement à l'aide d'un lapin polyclonaux NP-anticorps spécifiques (Groupe C). Contrôle négatif (-) a été fluide allantoïdien d'oeufs sains. Contrôle positif (+) a été fluide allantoïdien dopés avec des ARN1 A / New Caledonia/20/99 et sondé avec les antisérums correspondants.

Figure 5. Diagramme de la procédure de slot blot pour la quantification des antigènes HA et NA dans les vaccins antigrippaux.
Les tampons nécessaires à la dilution de l'échantillon ainsi que pour le lavage et blocage de la membrane slot blot sont d'abord préparés et la membrane PVDF et papiers filtres nécessaires pour l'assemblage de l'appareil Bio-Dot microfiltration SF sont pré-trempées. Vaccin contre l'influenza et des échantillons standard de référence sont dilués dans le tampon optimal pour HA ou NA de détection par slot blot. L'appareil Bio-Dot microfiltration SF est assemblé selon les instructions du fabricant et les échantillons sont appliqués sur la membrane de PVDF. HA et NA antigènes sont détectés en utilisant des anticorps universelle contre chaque antigène. L'analyse densitométrique est effectuée sur les signaux chimioluminescence obtenue pour la quantification des HA et NA dans les échantillons testés.
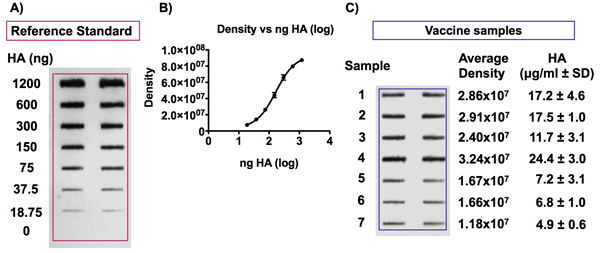
Figure 6. Détection de l'antigène HA dans les échantillons de vaccin contre la grippe et de se référerrence standard.
Le panneau A montre une tache représentatifs obtenus après immunodétection de l'antigène HA. L'antigène de référence HA a été diluée à concentrations de 0 à 6 mg HA / ml et les vaccins ont été dilués à une concentration de 0,375 mg HA / ml dans de l'urée 4M / SCT avant d'être appliquée à une membrane de PVDF avec un appareil Bio-Dot microfiltration SF . L'antigène HA a ensuite été détecté en utilisant l'anticorps Uni-1 universelle. Groupe B montre un exemple d'une courbe standard obtenue en détectant les signaux des concentrations différentes d'HA une norme de référence vaccin. L'intensité du signal est proportionnelle à la concentration de HA et de la courbe correspond à un modèle 4-PL.
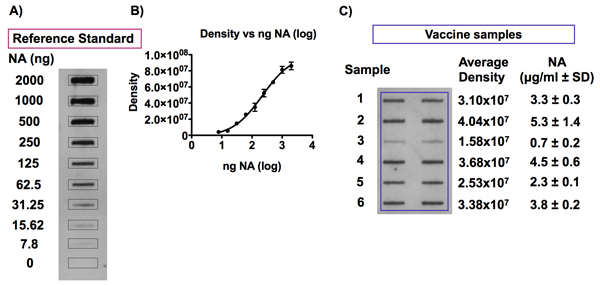
Figure 7. Détection de l'antigène NA dans les échantillons de vaccin contre la grippe et la norme de référence.
Panel A et B montrent représentatifs des signaux obtenus suite à la détection de NA dans une norme de référence de vaccin grippal dilué à des concentrations de NA allant de 0 à 10 ug NA / ml dans 0,01% Zwittergent / SCT et le 4-PL résultant courbe standard suivant analyse la densitométrie. Un exemple de signaux détectés par chimiluminescence typiques après une analyse de l'antigène de slot blot NA dans les échantillons de vaccin antigrippal est indiqué dans C. Les échantillons Panneau vaccin contre la grippe ont été dilués à une concentration de 1 ug HA / ml dans 0,01% Zwittergent / SCT et ont été transférés sur une membrane PVDF en utilisant un appareil Bio-Dot microfiltration SF. Dilutions de l'étalon de référence vaccin correspondant, avec des concentrations allant de 0 à 2,5 pg NA / ml, ont été inclus sur le même blot afin d'établir une courbe standard pour la quantification de l'antigène NA dans les échantillons de vaccin. L'antigène NA a été détecté avec l'anticorps HCA-2 universel contre NA et l'analyse des signaux de densitométrie chimioluminescence obtenue a été effectuée. Le montant de la NA dans chaque échantillon vaccin peut être calculée par rapport à la courbe 4-PL standard obtenue en traçant les valeurs de l'intensité du signal par rapport à la concentration de NA pour la norme de référence vaccin.
Discussion
La détermination quantitative de la grippe virale HA et NA sont essentiels pour la recherche de vaccins et le développement depuis ces deux protéines de surface sont plus importants composants viraux induire des réponses immunitaires 6-11. Auparavant rapporté des méthodes immunologiques pour la détection de ces protéines nécessitent anticorps spécifique à la souche. La méthode slot simple, reproductible et rapide blot pour quantifier les antigènes HA et NA décrits ici sont adaptés à tous la gr...
Déclarations de divulgation
Remerciements
Les auteurs tiennent à remercier Mme Monika Tocchi pour révision éditoriale du manuscrit. AMH est soutenu par une bourse de l'Université King Abdulaziz, à travers le Bureau culturel saoudien au Canada.
matériels
| Name | Company | Catalog Number | Comments |
| Nom du réactif ou de l'équipement | Société | Numéro de catalogue | Commentaires |
|---|---|---|---|
| Bio-Dot Appareil de microfiltration SF | Bio-Rad | 170-6542 | |
| Bio-Dot SF papier filtre | Bio-Rad | 162-0161 | |
| Immobilon-FL transfert de membrane (PVDF) | Millipore | IPFL00010 | |
| Pompe à vide | Millipore | WP6111560 | |
| Film Lumière chimiluminescence BioMax | Kodak | 178 8207 | |
| Système FluorChem documentation de gel | Alpha Innotech | 29 à 008-1896X | |
| Anticorps de lapin universelle contre HA et NA antigènes | Uni-1 (HA) HCA-2, HCA-3 (NA) | Les anticorps sont disponibles par le biais MTA ou peuvent être générées par les chercheurs intéressés, conformément aux procédures décrites précédemment 6,7. | |
| Antigènes de vaccins grippe de référence | CBER / FDA ou NIBSC | ||
| Échantillons vaccin contre la grippe | Couramment disponibles dans la plupart des pays | ||
| L'urée | Sigma-Aldrich | U1250 | |
| Zwittergent 3-14 détergent | Calbiochem | 693017 | |
| Tween-20 | Fisher Scientific | BP337-500 | |
| Blotting Blocker grade non-lait écrémé en poudre | Bio-Rad | 170-6404 | |
| ImmunoPure chèvre anti-lapin IgG (H + L), conjuguée à la peroxydase | Thermo Scientific | 31460 | |
| SuperSignal Ouest Dura Extended Substrat Durée | Thermo Scientific | 34075 |
Références
- Webster, R. G., Bean, W. J. Genetics of influenza virus. Annu Rev Genet. 12, 415-431 (1978).
- Skehel, J. J., Wiley, D. C. Receptor binding and membrane fusion in virus entry: the influenza hemagglutinin. Annu Rev Biochem. 69, 531-569 (2000).
- Wood, J. M. The influence of the host cell on standardisation of influenza vaccine potency. Dev Biol Stand. 98, 183-188 (1999).
- Sylte, M. J., Suarez, D. L. Influenza neuraminidase as a vaccine antigen. Curr Top Microbiol Immunol. 333, 227-241 (2009).
- Bright, R. A., Neuzil, K. M., Pervikov, Y., Palkonyay, L. WHO meeting on the role of neuraminidase in inducing protective immunity against influenza infection. Vaccine. 27, 6366-6369 (2008).
- Chun, S. Universal antibodies and their applications to the quantitative determination of virtually all subtypes of the influenza A viral hemagglutinins. Vaccine. 26, 6068-6076 (2008).
- Gravel, C. Qualitative and quantitative analyses of virtually all subtypes of influenza A and B viral neuraminidases using antibodies targeting the universally conserved sequences. Vaccine. 28, 5774-5784 (2010).
- Li, C. A simple slot blot for the detection of virtually all subtypes of the influenza A viral hemagglutinins using universal antibodies targeting the fusion peptide. Nat Protoc. 5, 14-19 (2010).
- Harvey, R., Wheeler, J. X., Wallis, C. L., Robertson, J. S., Engelhardt, O. G. Quantitation of haemagglutinin in H5N1 influenza viruses reveals low haemagglutinin content of vaccine virus NIBRG-14 (H5N1). Vaccine. 26, 6550-6554 (2008).
- Li, C. Application of deglycosylation and electrophoresis to the quantification of influenza viral hemagglutinins facilitating the production of 2009 pandemic influenza (H1N1) vaccines at multiple manufacturing sites in China. Biologicals. 38, 284-289 (2010).
- Johansson, B. E., Pokorny, B. A., Tiso, V. A. Supplementation of conventional trivalent influenza vaccine with purified viral N1 and N2 neuraminidases induces a balanced immune response without antigenic competition. Vaccine. 20, 1670-1674 (2002).
- Hashem, A. Universal antibodies against the highly conserved influenza fusion peptide cross-neutralize several subtypes of influenza A virus. Biochem Biophys Res Comm. , (2010).
Erratum
Formal Correction: Erratum: Quantitative Analyses of all Influenza Type A Viral Hemagglutinins and Neuraminidases using Universal Antibodies in Simple Slot Blot Assays
Posted by JoVE Editors on 11/13/2012. Citeable Link.
An author's affiliation was omitted from the publication of Quantitative Analyses of all Influenza Type A Viral Hemagglutinins and Neuraminidases using Universal Antibodies in Simple Slot Blot Assays.
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon