È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Analisi quantitativa di tutti influenza di tipo A Hemagglutinins e neuraminidasi virale utilizzando anticorpi Universale di saggi semplice Slot Blot
* Questi autori hanno contribuito in egual misura
In questo articolo
Erratum Notice
Riepilogo
Un metodo semplice macchia di slot è stato sviluppato per la quantificazione del emoagglutinina e neuraminidasi dell'influenza virale utilizzando anticorpi universali indirizzare le proprie sequenze più conservate identificate attraverso l'analisi bioinformatica. Questo approccio innovativo può fornire una valida alternativa alla determinazione quantitativa di tutti i emoagglutinina e neuraminidasi virale.
Abstract
Emoagglutinina (HA) e neuraminidasi (NA) sono due proteine di superficie dei virus influenzali, che sono noti per svolgere un ruolo importante nel ciclo di vita virale e l'induzione di risposta immunitaria protettiva 1,2. Come l'obiettivo principale per gli anticorpi neutralizzanti, HA è attualmente utilizzato come indicatore la potenza del vaccino influenzale ed è misurata dal singolo immunodiffusione radiale (SRID) 3. Tuttavia, la dipendenza della SRID sulla disponibilità del corrispondente sottotipo-specifici antisieri causa un minimo di 2-3 mesi di ritardo per il rilascio di ogni nuovo vaccino. Inoltre, nonostante le prove che la NA induce anche un'immunità protettiva 4, l'importo di NA nei vaccini influenzali non è ancora standardizzata a causa della mancanza di reagenti appropriati o metodo di analisi 5. Così, semplici metodi alternativi in grado di quantificare antigeni HA e NA sono desiderabili per rilascio rapido e miglior controllo della qualità dei vaccini antinfluenzali.
Regioni universalmente conservato in tutte le influenzale disponibile A HA e NA sequenze sono state identificate da analisi bioinformatiche 6-7. Una sequenza (designato come Uni-1) è stato identificato nel solo epitopo universalmente conservato di HA, il peptide di fusione 6, mentre due sequenze conservate sono stati identificati in neuraminidasi, una vicino al sito attivo enzimatico (designato come HCA-2) e il altro vicino alla N-terminale (designato come HCA-3) 7. Peptidi con queste sequenze di amminoacidi sono stati sintetizzati e usati per immunizzare i conigli per la produzione di anticorpi. L'anticorpo contro l'Uni-1 di epitopo HA è stato in grado di legarsi a 13 sottotipi di influenza A HA (H1-H13), mentre gli anticorpi contro l'HCA-2 e HCA-3 regioni di NA erano in grado di legare tutti i 9 sottotipi di NA. Tutti gli anticorpi hanno mostrato notevole specificità contro l'sequenze virali come dimostra l'osservazione che non cross-reattività alle proteine allantoide è stato rilevato. Questi anticorpi universale sono stati poi utilizzati per sviluppare test macchia di slot per quantificare HA e NA di influenza A vaccini senza la necessità di antisieri specifici 7,8. Campioni di vaccino sono stati applicati su una membrana PVDF con un apparato macchia di slot con standard di riferimento diluito a concentrazioni diverse. Per la rilevazione di HA, campioni e standard sono stati diluiti in tampone Tris salino (TBS) a base di urea 4M, mentre per la misura di NA sono stati diluiti in TBS contenente 0,01% Zwittergent come queste condizioni significativamente migliorato la sensibilità di rilevazione. In seguito al rilevamento di antigeni HA e NA da immunoblotting con i loro anticorpi rispettivi universale, intensità di segnale sono stati quantificati dalla densitometria. Quantità di HA e NA nel vaccino sono poi stati calcolati utilizzando una curva standard stabilito con l'intensità del segnale della varie concentrazioni dei riferimenti usati.
Dato che questi anticorpi si legano agli epitopi universale in HA o NA, gli investigatori hanno interessato potrà servirsene come strumenti di ricerca in saggi immunologici diversi macchia di slot solo.
Protocollo
1. Preparazione di reagenti e attrezzature
- Prima di iniziare la procedura di macchia slot, preparare 20_mls di soluzione di urea 4M in tampone Tris salino (20 mM Tris, 137 mM NaCl, pH 7.6) (TBS) per l'emoagglutinina, o HA, macchia slot, o 20_mls di un 0,01% Zwittergent soluzione in TBS per la neuraminidasi, o NA, macchia slot. Mentre urea 4M deve essere preparato fresco ogni volta, una soluzione al 10% in magazzino Zwittergent dH 2 O è stabile per almeno 6 mesi a temperatura ambiente e possono quindi essere diluito a 0,01% in TBS prima di ogni test.
- Preparare 2000 ml di soluzione di lavaggio con l'aggiunta di Tween-20 a una soluzione TBS ad una concentrazione finale del 0,1%. Preparare 80 ml di tampone di bloccaggio sciogliendo latte scremato in polvere (assorbente di grado non grassi del latte a secco) ad una concentrazione finale del 5% w / v in tampone di lavaggio.
- Attivare la membrana PVDF (pre-tagliati ad un x 9 12 dimensioni cm) in metanolo per 15 secondi, seguito da 2 minuti a sciacquare in DDH 2 O. Mettere a bagno la membrana in TBS fino al momento dell'uso. Pre-umido 3 fogli di Bio-Dot SF filtro di carta in TBS fino al momento dell'uso.
2. Preparazione dei campioni vaccino contro l'influenza e standard di riferimento per HA slot di macchia
Vaccino contro l'influenza standard di riferimento con pre-determinati contenuti HA corrispondenti ai ceppi del vaccino da testare sono stati ottenuti dal Centro di Valutazione e Ricerca Biologics (CBER / FDA, USA) o l'Istituto Nazionale di Standard e di controllo biologico (NIBSC, UK) e vengono utilizzati per la quantificazione HA da macchia slot. Gli investigatori potrebbe anche preparare i loro standard di antigene usando procedure stabilite, come descritto nei riferimenti 9 e 10.
- Per antigeni HA e campioni di riferimento vaccino di prova: Diluire il brodo di riferimento HA antigene in urea 4M / TBS per le seguenti concentrazioni: 0, 0,0938, 0,1875, 0,375, 0,75, 1,5, 3 e 6 HA mg / ml. Mescolare bene. Poi, diluire i campioni di prova vaccini per uso umano ottenuti da produttori di vaccini o fatti in casa per scopi di ricerca scientifica in urea 4M / TBS e mescolare bene. Mentre duplicati dell'antigene di riferimento ed i campioni vaccino può essere eseguito, triplica sono preferiti. Preparare 3 diluizioni di ogni campione (2 volte differenza) per consentire la concentrazione del campione a cadere all'interno della curva standard. Preparare 450 microlitri o 650 microlitri di ciascun antigene di riferimento o vaccino diluizione prova preliminare per eseguire duplicati o triplica rispettivamente. Un vaccini monovalenti influenza può essere provata con questo metodo macchia slot. Il contenuto degli antigeni HA riferimento precedentemente determinato utilizzando SRID che è il test attualmente utilizzato per le preparazioni standard di vaccino contro l'influenza. Il contenuto HA determinato da SRID è stata usata come iniziale concentrazione dell'antigene HA magazzino di riferimento per la preparazione delle diluizioni per la curva macchia slot standard.
3. Preparazione dei campioni vaccino contro l'influenza e standard di riferimento per NA slot di macchia
Influenza standard di riferimento vaccino corrispondenti ai ceppi del vaccino da testare sono stati ottenuti dal Centro di Valutazione e Ricerca Biologics (CBER / FDA, USA) o l'Istituto Nazionale di Standard e di controllo biologico (NIBSC, Regno Unito) e sono utilizzati per la quantificazione NA da macchia slot. Il contenuto NA di questi campioni di riferimento è stato determinato mediante SDS-PAGE analisi dei campioni di deglicosilata in collaborazione con l'analisi densitometria scansione, come descritto in precedenza 9, con lievi modifiche 10. In breve, il vaccino deglicosilata campioni di riferimento (5 mg) sono stati mescolati con il tampone del campione e caricato sul gel. Il gel è stato eseguito a 20 mA per circa 90 minuti fino a quando il colorante inseguimento appena esaurito il gel, seguita dalla colorazione Sypro. Densitometria quantificazione delle proteine è stata effettuata utilizzando un sistema di documentazione Fluorchem gel (Alpha Innotech). La quantità di NA è stato determinato in base al rapporto delle proteine NA per le proteine totali, come determinato mediante test Lowry. Campioni di riferimento preparato con questo metodo può essere utilizzato in blot slot per la quantificazione dei contenuti NA nei campioni di vaccino da produttori di vaccini.
- Per gli antigeni di riferimento NA ed i campioni del vaccino di prova: Diluire il brodo di riferimento NA antigene di 0,01% Zwittergent / TBS per le seguenti concentrazioni: 0, 0,039, 0,078, 0,1562, 0,3125, 0,625, 1,25, 2,5, 5 e 10 mcg NA / ml. Mescolare bene. Poi, diluire i campioni di prova vaccini per uso umano ottenuti da produttori di vaccini o fatti in casa per scopi di ricerca scientifica di 0,01% Zwittergent / TBS e mescolare bene. Mentre duplicati dell'antigene di riferimento ed i campioni vaccino può essere eseguito, triplica sono preferiti. Preparare 3 diluizioni di ogni campione (2 volte differenza) per consentire la concentrazione del campione a cadere all'interno della curva standard. Preparare 450 microlitri o 650 microlitri di ciascun antigene di riferimento o vaccino diluizione prova preliminare per eseguire duplicati o triplica rispettivamente. Vaccini monovalenti contro l'influenza A può essere testato spiritoh questo metodo macchia slot.
4. Assemblea della Bio-Dot apparato Microfiltrazione SF e blotting di campioni su membrana di PVDF
- Assemblare un precedentemente pulito e asciugato Bio-Dot apparato microfiltrazione SF. Posizionare la piastra di supporto guarnizione nel collettore di aspirazione e posizionare la guarnizione di tenuta sul bagnato top.Place i 3 fogli di Bio-Dot carta SF filtro sopra la guarnizione, seguito dal pre-impregnato membrana PVDF. Posizionare il modello di esempio in cima alla membrana e dita stringere le quattro viti con un diagonale che attraversano per garantire l'applicazione uniforme della pressione sulla superficie della membrana.
- Verificare che il 3-way valvola è tarata per esporre il collettore di aspirazione alla fonte di vuoto solo prima di accendere la pompa e collegare il vuoto.
- Accendere la pompa e la connessione a Bio-Dot apparato. Assicurarsi che la valvola di flusso è posizionato ad un livello al di sotto del campione pozzi per il drenaggio rapido e corretto dei campioni nei seguenti passaggi.
- Ripetere l'operazione utilizzando la vite di serraggio diagonale che attraversano. Serrando le viti, mentre il vuoto viene applicato assicura una tenuta migliore e impedisce la contaminazione incrociata tra pozzi.
- Cambiare la valvola di flusso per esporre il collettore di aspirazione dell'aria e spegnere la pompa.
- Applicare 100 ml di TBS a tutti i pozzetti utilizzando una pipetta multicanale per reidratare la membrana in modo da garantire vincolante uniforme dell'antigene. Si deve prestare attenzione per evitare la formazione di bolle e di applicare la soluzione nel mezzo del pozzo, il più vicino al fondo possibile, al fine di coprire la fessura in modo uniforme. Scoppiare una bolla d'aria accidentalmente introdotto con una punta pipettatore.
- Cambiare la valvola di flusso per esporre il collettore per l'aria e il vuoto, accendere la pompa, e delicatamente drenare il buffer dai pozzetti mettendo un dito sopra la porta esposta all'aria per regolare la quantità di vuoto.
- Cambiare la valvola di flusso per esporre il collettore all'aria non appena il buffer è completamente svuotato da tutti i pozzetti. Spegnere la pompa o scollegare il vuoto.
- Applicare 200 ml di ogni standard o campione di diluizione del vaccino per bene. Campioni Pipettare uno alla volta, al centro di ogni bene, il più vicino al fondo il più possibile, avendo cura di evitare l'introduzione di bolle d'aria. Scoppiare una bolla d'aria accidentalmente introdotto con una punta pipettatore. Mettere 200 ml di tampone di diluizione del campione (4M urea / TBS o 0,01% Zwittergent / TBS) in pozzi inutilizzati per garantire la depressione propria dei pozzi in uso.
- Regolare la valvola di flusso per esporre il collettore per l'aria e il vuoto. Accendere la pompa (o ricollegare il vuoto) e con delicatezza i campioni permettono di drenare completamente dai pozzi controllando la quantità di vuoto con un dito sul porto esposto all'aria. Togliere il dito dal porto di rilasciare il vuoto non appena tutti i campioni hanno drenato.
- Immediatamente aggiungere 200 ml di TBS in ogni pozzetto utilizzando una pipetta multicanale. Applicare un vuoto dolce per drenare e lavare i pozzi controllando la quantità di vuoto con un dito sul porto esposto all'aria.
- Ripetere la fase di lavaggio descritto al punto 4.11. Non appena i pozzi hanno completamente svuotato, allentare le viti del modello di esempio e spegnere il vuoto per evitare secchino troppo i pozzi. Prontamente alla rimozione della membrana.
- Posizionare la membrana in tampone di bloccaggio e incubare una notte a 4 ° C, con dolce dondolio. Usare abbastanza tampone di bloccaggio per coprire completamente la membrana.
5. Immunoblotting di antigeni HA e NA
- Dopo la notte di incubazione in tampone di bloccaggio, lavare la membrana due volte per 5 minuti con TBS/0.1% Tween-20 soluzione di lavaggio. Per tutti i lavaggi e le incubazioni, garantire la membrana è completamente coperto con una soluzione.
- Incubare la membrana con un anticorpo di coniglio universale contro HA (come Uni-1) o NA (come HCA-2 o HCA-3) diluito in 5% w / v BSA in tampone di lavaggio per un'ora a temperatura ambiente, con dolce dondolo. Le concentrazioni anticorpali ottimali devono essere determinati per ciascun titolo anticorpale. Diluizioni di 1:4000 di coniglio anti-siero ha dato ottimi risultati per gli anticorpi di cui sopra.
- Lavare la membrana per tre volte, a temperatura ambiente con dondolo dolce per 15 minuti ogni volta, per rimuovere eventuali anticorpi non legati primaria.
- Incubare la membrana con un HRP-coniugato anti-coniglio anticorpo secondario. Utilizzare una diluizione 1:50000 della Capra Thermo ImmunoPure anti-coniglio IgG, anticorpi perossidasi coniugato in tampone bloccante ed incubare a temperatura ambiente per 30 minuti con il dolce dondolio.
- Lavare la membrana per tre volte, a dondolo per 15 minuti ogni volta, a temperatura ambiente con il tampone di lavaggio per rimuovere ogni anticorpi non legati secondario.
- Lavare la membrana con TBS per 5 minuti con dondolo delicato per rimuovere residui di detergente Tween-20 dalla superficie della membrana.
- Preparare il supporto con 3 ml di ogni reagent dal kit Supersignal Durata Occidente estesa substrato Dura da Thermo Scientific e mescolare bene.
- Posizionare la membrana su una carta velina asciutta per rimuovere delicatamente ogni eccesso tampone TBS.
- Trasferire la membrana in un contenitore asciutto e aggiungere il supporto per coprire l'intera membrana. Incubare 5 minuti con dondolo dolce, a temperatura ambiente.
- Rimuovere il substrato in eccesso tamponando delicatamente la membrana su carta velina.
- Esporre la membrana di un film chemiluminescenza. La durata dell'esposizione sarà bisogno di essere ottimizzato per evitare la saturazione del segnale, ma in genere vanno da 10 secondi a 10 minuti.
- Eseguire analisi densitometria sul film sviluppato utilizzando un apparato di immagini di gel, come il sistema Fluorchem documentazione gel (Alpha Innotech) seguendo le istruzioni del produttore. I valori di densità per ogni set di repliche di antigeni di riferimento e un campione del vaccino di prova vengono poi mediati. Mentre gli standard ed i campioni antigene vaccino può essere eseguito in duplicato, triplicato sono preferiti. Valori di densità di replicazione dovrebbe essere molto simile. Differenze significative tra le repliche indicano un probabile problema tecnico durante la procedura. Una concentrazione-dipendente curva standard è stabilita tracciando i valori di densità media in funzione della quantità (in ng) di HA e NA antigene messo in ogni slot, dallo standard di riferimento. Utilizzando opportuni montaggio curva di calibrazione in immunodosaggi è fondamentale per quantificare con precisione HA e NA. Regressione lineare, ottenuta riportando la risposta (y) rispetto alla concentrazione (x) utilizzando la parte lineare della curva di risposta (y = mx + b) è il metodo più semplice per la quantificazione degli analiti. Se una più ampia gamma di analiti è considerato per il calcolo di concentramento, i quattro parametri logistici (4PL) modello attualmente accettato per gli immunodosaggi dovrebbe essere usato. Una varietà di software è disponibile per i ricercatori interessati a prendere in considerazione. Nel caso del test di slot descritto macchia, convertendo i valori dell'asse x per accedere scala permette la curva di montare un 4-PL modello e l'uso di una pendenza variabile non di regressione lineare per calcolare gli importi cancellati di HA e NA in i campioni di vaccino testato è quindi possibile. Siamo quindi di routine utilizzare questo modello per le nostre analisi. Come i campioni di prova del vaccino sono stati diluiti in entrambe urea 4M / TBS o 0,01% Zwittergent / TBS prima di essere cancellato sulla membrana, il fattore di diluizione per ogni campione deve essere presa in considerazione per determinare il contenuto di HA e NA del test originale vaccino campioni. Si suggerisce che ogni campione di test vaccino essere eseguito in tre diverse diluizioni (2 volte differenza) in modo che un insieme di valori di densità a cadere all'interno della curva standard. Valori di densità superiori al range curva standard per tutte le diluizioni dei campioni testati vaccino devono essere ulteriormente diluito per HA accurata o la quantificazione NA. Se i valori di densità sono al di sotto del gradino più basso della curva, campioni devono essere diluiti in un fattore di diluizione inferiore.
6. Rappresentante dei risultati:
Analisi bioinformatica di tutti influenza A disposizione sequenze HA confermato l'N-terminale della subunità HA2 (il peptide di fusione) come l'unica regione conservata di HA. La figura 1 mostra il tasso di conservazione per ogni posizione di aminoacidi della sequenza consenso identificati. Due varianti sono state identificate in posizioni 2 (L-> I) e 12 (G-> N) dei 14 aminoacidi N-terminale di HA2, ma tali variazioni sono state trovate non influenzare l'associazione tra gli anticorpi e le varianti peptide 6 . L'epitopo Uni-1 (GLFGAIAGFIEGGW) è stato scelto per sviluppare un anticorpo universale contro HA. Questo anticorpo ha dimostrato notevole specificità per le sequenze virali ed è in grado di legare a 13 differenti sottotipi di HA influenza A (H1-H13) (Figura 2).
Utilizzando un approccio simile, due sequenze universalmente conservate sono stati identificati in tutti influenza A NA, uno vicino al sito enzimaticamente attivo (HCA-2) (Figura 3A) e l'altro al N-terminale (HCA-3) (Figura 3B) . Peptidi con queste sequenze di amminoacidi sono stati utilizzati come antigeni per generare anticorpi universale contro NA. Gli anticorpi contro entrambi gli epitopi sono stati in grado di legarsi a tutti i 9 sottotipi di NA e ha mostrato molto poco cross-reattività alle proteine allantoide o cellulare, dimostrando così alta specificità per la sequenza virale NA (Figura 4).
La Figura 5 mostra una panoramica del metodo di slot blot per la quantificazione di influenza HA e NA.
Esempi di analisi antigene HA e NA di slot blot sono mostrati nelle figure 6 e 7. Figura 6A e 6C mostra i risultati di rappresentanza dopo il rilevamento dell'antigene HA in uno standard di riferimento vaccino antinfluenzale e campioni vaccino, rispettivamente. Ogni campione (standard o vaccino) è stato eseguito in duplice copia, in pozzetti adiacenti. Duplicati dovrebbe mostrare Similaintensità r seguito di rilevazione. Ottimizzazione delle diluizioni degli anticorpi, incubazione e tempo di esposizione può essere richiesto a seconda della anticorpi utilizzati.
Un esempio di una tipica curva standard ottenute in seguito all'individuazione di diverse concentrazioni di HA da un campione standard di vaccino di riferimento è mostrato in Figura 6B. La concentrazione dell'antigene HA è proporzionale all'intensità del segnale successivo rilevamento chemioluminescenza della macchia slot e si inserisce il 4-PL modello curve fitting per questa fascia di concentrazione (,0938-6 HA mcg / ml).
Figura 7 mostra i risultati rappresentante della rilevazione dell'antigene NA in uno standard di riferimento vaccino antinfluenzale e in campioni di vaccino. Analisi della densità ha mostrato che l'intensità del segnale ottenuto rilevando l'antigene NA in varie diluizioni di uno standard di riferimento da vaccino blot slot è proporzionale alla concentrazione di NA (Fig. 7A). La curva standard risultante si inserisce un 4-PL modello di questa fascia di concentrazione (0,039-10 NA mg / ml), come mostrato nella Figura 7B. La figura mostra 7C un esempio di analisi di slot blot dei contenuti NA nei campioni di vaccino contro l'influenza. Ogni campione è stato analizzato in duplicato, in pozzetti adiacenti.

Figura 1. Tasso di Conservazione della Uni-1 epitopo nella regione del peptide di fusione di influenza A HA.
Analisi bioinformatica di tutti influenza A disposizione sequenze HA confermato che il peptide di fusione (che si trova al N-terminale della subunità HA2) è l'unica regione universalmente conservato di HA. Si noti che le due variazioni in posizione 2 (L-> I) e 12 (G-> N) sono stati trovati non influenzare il legame degli anticorpi 6. Un anticorpo universale in grado di legare 13 diversi sottotipi di influenza A HA (H1-H13) è stato sviluppato utilizzando la Uni-1 epitopo (GLFGAIAGFIEGGW).
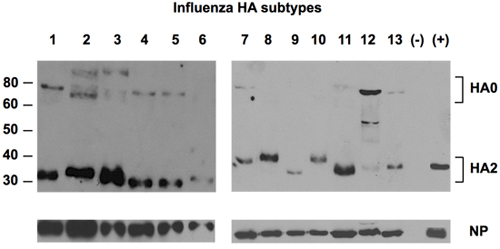
Figura 2. Rilevamento di 13 sottotipi di HA da anticorpi universale contro HA.
Fluidi allantoideo di 13 sottotipi del virus dell'influenza propagati in uova embrionate sono stati frazionati in SDS-PAGE, seguita dalla rilevazione delle proteine HA utilizzando l'anticorpo universale contro la Uni-1 di epitopo HA. Proteina NP è stato rilevato come il caricamento di controllo utilizzando un coniglio policlonale NP-specifici anticorpi. Controllo negativo (-) è stato liquido allantoico da uova infette. Controllo positivo (+) è uno standard di riferimento di H1 da NIBSC, UK
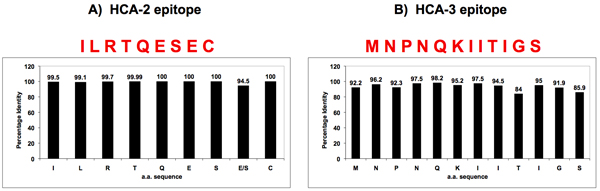
Figura 3. Omologia di sequenza di influenza A NA vicino al luogo enzimaticamente attiva e la N-terminale.
Due sequenze conservate universalmente sono stati identificati in influenza A NA da parte bioinformatica, uno situato in prossimità del sito attivo enzimatico (HCA-2) (Pannello A), l'altra al N-terminale (HCA-3) (Pannello B). Peptidi con tali sequenze conservate aminoacidi sono stati sintetizzati e utilizzati per generare gli anticorpi universale contro NA.

Figura 4. Rilevamento di 9 sottotipi di NA NA dagli anticorpi.
Fluidi allantoideo di nove sottotipi NA dei virus propagati in uova embrionate sono stati frazionati in SDS-PAGE, seguita dalla rilevazione delle proteine NA utilizzando l'HCA-2 (pannello A) e HCA-3 (pannello B) anticorpi. Proteina NP è stato rilevato come il caricamento di controllo utilizzando un coniglio policlonale NP-anticorpo specifico (Panel C). Controllo negativo (-) è stato liquido allantoico da uova infette. Controllo positivo (+) è liquido allantoico a spillo con rNA1 di A / New Caledonia/20/99 e sondato con gli antisieri corrispondenti.

Figura 5. Diagramma di flusso della procedura di slot blot per la determinazione quantitativa degli antigeni HA e NA di vaccini antinfluenzali.
I buffer necessaria per la diluizione del campione, nonché per il lavaggio e il blocco della membrana macchia slot sono prima preparato e la membrana PVDF e filtri di carta necessari per il montaggio del Bio-Dot apparato microfiltrazione SF sono pre-impregnati. Vaccino contro l'influenza e campioni standard di riferimento sono diluiti nel buffer ottimale per il rilevamento HA o NA da macchia slot. Il Bio-Dot apparato microfiltrazione SF sia montato secondo le istruzioni del produttore ed i campioni vengono applicati sulla membrana PVDF. Antigeni HA e NA sono individuati utilizzando gli anticorpi contro l'antigene universale. Analisi della densitometria viene eseguita sui segnali chemiluminescenza ottenuto per la quantificazione di HA e NA nei campioni testati.
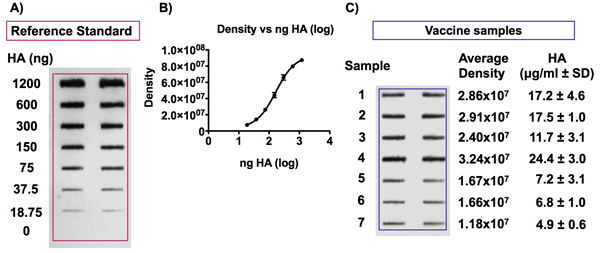
Figura 6. Rilevamento dell'antigene HA nei campioni di vaccino contro l'influenza e si riferisconoriferimento standard.
Pannello A mostra una macchia rappresentante ottenuti a seguito immunolocalizzazione dell'antigene HA. L'antigene di riferimento HA è stato diluito a concentrazioni di 0-6 mg sono stati diluiti HA / ml ed i vaccini ad una concentrazione di 0,375 mg di HA / ml in urea 4M / TBS prima di essere applicata a una membrana PVDF con un apparato bio-Dot microfiltrazione SF . L'antigene HA è stato poi rilevato utilizzando l'anticorpo Uni-1 universale. Pannello B mostra un esempio di una curva standard ottenuta rilevando i segnali di concentrazione HA diverse da uno standard di riferimento vaccino. L'intensità del segnale è proporzionale alla concentrazione di HA e la curva si inserisce un 4-PL modello.
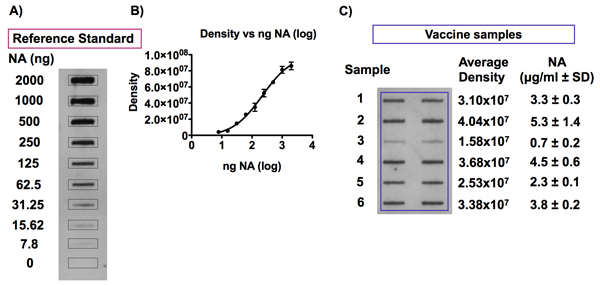
Figura 7. Rilevamento dell'antigene NA nei campioni di vaccino contro l'influenza e standard di riferimento.
Panel A e B mostrano rappresentante segnali ottenuti in seguito all'individuazione di NA in uno standard di riferimento influenza vaccino diluito a concentrazioni NA vanno da 0 a 10 mcg NA / ml a 0,01% Zwittergent / TBS e la risultante 4-PL curva standard che segue analizza la densitometria. Un esempio tipico di segnali di chemiluminescenza rilevati a seguito di una analisi di slot blot di antigene NA nei campioni di vaccino antinfluenzale è indicato nel Pannello di C. campioni di vaccino antinfluenzale sono stati diluiti a una concentrazione di 1 mg di HA / ml a 0,01% Zwittergent / TBS e sono stati cancellati su un PVDF membrana usando un apparato bio-Dot microfiltrazione SF. Diluizioni dello standard di riferimento corrispondente vaccino, con concentrazioni da 0 a 2,5 mcg NA / ml, sono stati inclusi sulla macchia stessa al fine di stabilire una curva standard per la quantificazione dell'antigene NA nei campioni di vaccino. L'antigene NA è stato rilevato con l'anticorpo HCA-2 universale contro NA densitometria e analisi dei segnali di chemiluminescenza ottenuto è stato eseguito. La quantità di NA in ogni campione vaccino può essere calcolato contro il 4-PL curva standard ottenuta riportando i valori di intensità di segnale rispetto alla concentrazione di NA per lo standard di riferimento vaccino.
Discussione
Determinazione quantitativa di influenza virale HA e NA sono fondamentali per la ricerca di vaccini e lo sviluppo dal momento che questi due proteine di superficie sono componenti virali più importanti che inducono risposte immunitarie 6-11. Riportato in precedenza metodi immunologici per la rilevazione di queste proteine richiedono anticorpi ceppo specifico. La semplice, riproducibile e veloce metodo blot slot per quantificare gli antigeni HA e NA qui descritti sono adatti per tutte l'influe...
Divulgazioni
Riconoscimenti
Gli autori desiderano ringraziare la signora Monika Tocchi per la revisione editoriale del manoscritto. AMH è supportato da una borsa di studio da King Abdulaziz University, attraverso l'Ufficio Cultura saudita in Canada.
Materiali
| Name | Company | Catalog Number | Comments |
| Nome del reagente o attrezzature | Azienda | Numero di catalogo | Commenti |
|---|---|---|---|
| Bio-Dot SF microfiltrazione Apparatus | Bio-Rad | 170-6542 | |
| Bio-Dot SF Carta da filtro | Bio-Rad | 162-0161 | |
| Immobilon-FL trasferimento a membrana (PVDF) | Millipore | IPFL00010 | |
| Pompa del vuoto | Millipore | WP6111560 | |
| Luce Film chemiluminescenza BioMax | Kodak | 178 8207 | |
| FluorChem Gel Documentazione di sistema | Alpha Innotech | 29-008-1896X | |
| Anticorpi di coniglio universale contro antigeni HA e NA | Uni-1 (HA) HCA-2, HCA-3 (NA) | Gli anticorpi sono disponibili tramite MTA o possono essere generati da ricercatori interessati secondo le modalità descritte in precedenza 6,7. | |
| Vaccino antinfluenzale antigene di riferimento | CBER / FDA o NIBSC | ||
| Vaccino antinfluenzale campioni | Comunemente disponibili in molti paesi | ||
| Urea | Sigma-Aldrich | U1250 | |
| Zwittergent 3-14 Detergente | Calbiochem | 693017 | |
| Tween-20 | Fisher Scientific | BP337-500 | |
| Blotting Grado Blocker non grassi del latte secco | Bio-Rad | 170-6404 | |
| ImmunoPure capra anti-coniglio IgG (H + L), perossidasi coniugato | Thermo Scientific | 31460 | |
| SuperSignal Occidente Dura estesa substrato Durata | Thermo Scientific | 34075 |
Riferimenti
- Webster, R. G., Bean, W. J. Genetics of influenza virus. Annu Rev Genet. 12, 415-431 (1978).
- Skehel, J. J., Wiley, D. C. Receptor binding and membrane fusion in virus entry: the influenza hemagglutinin. Annu Rev Biochem. 69, 531-569 (2000).
- Wood, J. M. The influence of the host cell on standardisation of influenza vaccine potency. Dev Biol Stand. 98, 183-188 (1999).
- Sylte, M. J., Suarez, D. L. Influenza neuraminidase as a vaccine antigen. Curr Top Microbiol Immunol. 333, 227-241 (2009).
- Bright, R. A., Neuzil, K. M., Pervikov, Y., Palkonyay, L. WHO meeting on the role of neuraminidase in inducing protective immunity against influenza infection. Vaccine. 27, 6366-6369 (2008).
- Chun, S. Universal antibodies and their applications to the quantitative determination of virtually all subtypes of the influenza A viral hemagglutinins. Vaccine. 26, 6068-6076 (2008).
- Gravel, C. Qualitative and quantitative analyses of virtually all subtypes of influenza A and B viral neuraminidases using antibodies targeting the universally conserved sequences. Vaccine. 28, 5774-5784 (2010).
- Li, C. A simple slot blot for the detection of virtually all subtypes of the influenza A viral hemagglutinins using universal antibodies targeting the fusion peptide. Nat Protoc. 5, 14-19 (2010).
- Harvey, R., Wheeler, J. X., Wallis, C. L., Robertson, J. S., Engelhardt, O. G. Quantitation of haemagglutinin in H5N1 influenza viruses reveals low haemagglutinin content of vaccine virus NIBRG-14 (H5N1). Vaccine. 26, 6550-6554 (2008).
- Li, C. Application of deglycosylation and electrophoresis to the quantification of influenza viral hemagglutinins facilitating the production of 2009 pandemic influenza (H1N1) vaccines at multiple manufacturing sites in China. Biologicals. 38, 284-289 (2010).
- Johansson, B. E., Pokorny, B. A., Tiso, V. A. Supplementation of conventional trivalent influenza vaccine with purified viral N1 and N2 neuraminidases induces a balanced immune response without antigenic competition. Vaccine. 20, 1670-1674 (2002).
- Hashem, A. Universal antibodies against the highly conserved influenza fusion peptide cross-neutralize several subtypes of influenza A virus. Biochem Biophys Res Comm. , (2010).
Erratum
Formal Correction: Erratum: Quantitative Analyses of all Influenza Type A Viral Hemagglutinins and Neuraminidases using Universal Antibodies in Simple Slot Blot Assays
Posted by JoVE Editors on 11/13/2012. Citeable Link.
An author's affiliation was omitted from the publication of Quantitative Analyses of all Influenza Type A Viral Hemagglutinins and Neuraminidases using Universal Antibodies in Simple Slot Blot Assays.
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon