Method Article
Nucléofection de rongeurs Neuroblastes à étudier neuroblaste migrations
Dans cet article
Résumé
la migration des neuroblastes est une étape cruciale dans la neurogenèse postnatale. Le protocole décrit ici peut être utilisé pour étudier le rôle des régulateurs candidats de la migration des neuroblastes en utilisant / petit ARN en épingle à cheveux d'ADN (shRNA) nucléofection et un test de migration 3D avec neuroblastes isolés du rongeur postnatale courant de migration rostrale.
Résumé
La zone sous-ventriculaire (SVZ) situé dans la paroi latérale des ventricules latéraux joue un rôle fondamental dans la neurogenèse adulte. Dans cette zone restreinte du cerveau, les cellules souches neurales prolifèrent et produisent constamment neuroblastes qui migrent tangentiellement dans les chaînes le long de la courant de migration rostrale (RMS) pour atteindre le bulbe olfactif (OB). Une fois dans l'OB, neuroblastes passer à la migration radiale puis se différencient en neurones matures capables d'intégrer dans le réseau neuronal préexistante. La migration des neuroblastes appropriée est une étape fondamentale dans la neurogenèse, assurer la maturation fonctionnelle correcte de nouveaux neurones. Compte tenu de la capacité des neuroblastes SVZ dérivés pour cibler les zones lésées dans le cerveau, l'étude des mécanismes intracellulaires sous-tendent leur motilité va non seulement améliorer la compréhension de la neurogenèse, mais peut également favoriser l'élaboration de stratégies neurorégénérateurs.
Ce manuscrit décrit une analyse détailléeprotocole pour la transfection de rongeur primaire RMS neuroblastes postnatals et l'analyse de leur motilité l'aide d'un test in vitro de migration 3D récapitulant leur mode de migration observée in vivo. Les neuroblastes de rats et de souris peuvent être rapidement et efficacement transfectées par nucléofection avec de l'ADN plasmidique, petite épingle à cheveux (sh) ARN interférent court ou (si) oligos ARN ciblant des gènes d'intérêt. Pour analyser la migration, les cellules sont agrégés de nouveau dans nucleofected «gouttes suspendues», puis noyées dans une matrice tridimensionnelle. Nucléofection en soi ne porte pas atteinte de façon significative la migration des neuroblastes. Le traitement pharmacologique de neuroblastes nucleofected et agrégés de nouveau peut également être effectuée pour étudier le rôle des voies de signalisation impliquées dans la migration des neuroblastes signalisation.
Introduction
En postnatal des mammifères cerveau, la production de nouveaux neurones (neurogenèse) se produit tout au long de la vie et est limitée à deux niches neurogène: la zone sous-ventriculaire (SVZ) des ventricules latéraux et la zone sous-granulaire du gyrus denté de l'hippocampe 1. Plusieurs études récentes ont montré l'importance du rôle de la neurogenèse adulte dans la facilitation des tâches d'apprentissage et de mémoire 2,3. En outre, la preuve de la prolifération et le recrutement de cellules progénitrices neurales suivants lésion cérébrale 4-7 soulève la possibilité d'activation pharmacologique de la neurogenèse dans la réparation neuronale.
La neurogenèse postnatale est strictement réglementée dans toutes ses phases, qui comprennent la prolifération de neurones progéniteurs, la migration, la différenciation, la survie et l'intégration synaptique finale des neurones nouvellement nés 8. Progéniteurs neuronaux (neuroblastes) dérivées de cellules souches dans le SVZ migrent sur une grande distance à travers la migration rostralecourant (RMS) vers le bulbe olfactif (OB) où elles se développent en neurones fonctionnels 9. Neuroblastes migrateurs sont principalement unipolaire, avec un corps cellulaire allongé s'étendant d'un processus de leader unique. Ces cellules se déplacent dans les chaînes d'une manière collective, en glissant sur l'autre 10. La migration est une étape cruciale pour la maturation ultérieure des progéniteurs SVZ dérivés en neurones fonctionnels 11 et est contrôlée par des facteurs multiples et des molécules de guidage, y compris: molécule polysialylés neurones d'adhésion cellulaire (PSA-NCAM) 12, Ephrines 13, les intégrines 14 fentes 15, Facteurs de croissance de 16 et 17 neurotransmetteurs, mais les mécanismes moléculaires qui sous-tendent ce processus ne sont pas pleinement compris. Enquêter sur les voies de signalisation intracellulaires régulant la migration des neuroblastes fournira non seulement une meilleure compréhension de la neurogenèse adulte, mais aussi de contribuer au développement de la nouvelle thérapeutiqueapproches pour favoriser la réparation du cerveau.
Ce manuscrit décrit un protocole détaillé pour étudier le rôle des régulateurs candidats de la migration des neuroblastes in vitro en utilisant nucléofection et un test de migration 3D. Nucléofection est une technique de transfection cellulaire basé sur un procédé perfectionné de l'électroporation. du type de cellule courant électrique spécifique et la solution de nucléofection permettent le transfert de macromolécules polyanioniques tels que des ADN et des vecteurs shRNA et de siRNA oligonucléotides directement dans le noyau cellulaire et transfection permis de diviser lentement ou cellules inactives sur le plan mitotique, comme les neurones embryonnaires de mammifères et 18. Cette méthode est rapide, relativement facile à réaliser et donne lieu à une transfection hautement reproductible d'un large éventail de types de cellules, y compris les neuroblastes et les neurones primaires de 19 à 21.
La dissociation du tissu RMS permet l'isolement des neuroblastes migratoires, qui peut être nucleofected avec succès avec l'ADN / SHRVecteurs NA ou oligos de siRNA ciblant des gènes d'intérêt. Suite à nucléofection, les neuroblastes sont agrégés de nouveau suspendu dans des gouttes et ensuite noyées dans une matrice de Matrigel en trois dimensions. Ces conditions permettent neuroblastes migrent sur les agrégats de cellules récapitulant le mode de migration observée in vivo, offrant ainsi un excellent modèle pour étudier les voies de signalisation impliquées dans la migration des neuroblastes et d'évaluer l'influence des traitements pharmacologiques sur la motilité de ces cellules.
Protocole
Cette procédure est conforme à Accueil Règlement Royaume-Uni bureau (ACT des procédures scientifiques des animaux, 1986). Les scientifiques doivent suivre les lignes directrices établies et approuvées par leurs organismes de réglementation animaux institutionnelles et nationales.
Une. Dissection et de dissociation de Rat RMS Neuroblastes
- Préparer les solutions nécessaires pour la dissection RMS et dissociation:
milieu de dissection (100 ml)
Solution saline équilibrée de Hank (HBSS) - 98,5 ml
5 M de HEPES pH 7,4 à 0,5 ml
Pénicilline-streptomycine (10 000 unités / ml et 10 000 pg / ml) - 1 ml
milieu de dissociation (2 ml)
HBSS - 1.760 ml
10x trypsine (2,5%) - 200 pl
DNAse1 (1 mg / ml) - 40 pl
Dulbecco modification moyenne de Eagle (DMEM) + 10% sérum de veau foetal (FCS) (40 ml)
DMEM -36 ml
FCS - 4 ml
Le milieu complet (12 ml)
Moyennes Neurobasal - 11,46 ml
B27 Supplément - 250 pi
L-glutamine (200 mM) - 125 pl
Glucose (45%) - 165 pl
2. Filtre à stériliser le% de FCS DMEM + 10 et le milieu complet et preequilibrate eux dans un rapport C / 5% de CO 2 incubateur à 37 °.
- Dissection
- Sacrifiez une litière de rat P6-P7 (environ 12 chiots) par dislocation cervicale et décapiter avec des ciseaux.
- Faire une incision antéro-postérieur à la peau le long de la suture mi-sagittal du nez au cervelet avec une lame de scalpel. Peler la peau et répéter la même incision le long du crâne.
- Retirez délicatement les volets crâniens avec une pince et retirer délicatement le cerveau d'une spatule, en prenant soin d'inclure les bulbes olfactifs.
- Couper la troisième plus caudale du cerveau et le jeter.
- Hacher ee tissu cérébral en 1,4 mm d'épaisseur à l'aide de coupes coronales un hachoir de tissu.
- Placer les tranches dans des boîtes contenant du milieu de dissection froide et les séparer soigneusement à l'aide d'une aiguille.
- Le RMS apparaît comme une triangulaire, zone translucide au centre de sections de OB et comme une petite zone circulaire en plus des tranches de cerveau caudale. Couper les RMS sur chaque tranche avec un couteau de microchirurgie, en prenant soin d'éviter d'inclure les tissus environnants. Dans les ratons P7, généralement les ~ 8 tranches les plus rostrales (y compris OB) contiennent les RMS.
- Recueillir les fragments RMS avec une pipette Pasteur en plastique et placez-les dans un petit plat contenant un milieu de dissection froide sur la glace.
- Lorsque la dissection est terminé, le transfert des fragments RMS dans un tube de 15 ml avec une pipette en plastique. Laissez fragments à se déposer au fond du tube.
- Dissociation
- Remplacer le milieu de dissection avec 2 ml de milieu de dissociation.
- Triturer les fragments RMS par doucement pipetting la suspension de haut en bas fragment environ 10x en utilisant une pipette P1000.
- Laisser le tube avec les fragments de tissus dans un bain d'eau à 37 ° pendant 2 min.
- Introduire à la pipette la solution de nouveau 10x et veiller à ce que les fragments ont dissocié (la suspension doit devenir trouble).
- Inactiver la trypsine en ajoutant 5 ml de DMEM préchauffé + 10% de FCS.
- Centrifuger la suspension de cellules à 433 xg pendant 5 min.
- Dans l'entre-temps aliquote de la quantité requise de siRNA / ADN dans des tubes Eppendorf (habituellement 3-5 pg d'ADN / shRNA ou 9.5 ug par siRNA oligo nucléofection cependant, la quantité d'ADN / siRNA peut nécessiter une optimisation).
- Retirer l'excès de milieu et remettre en suspension le culot cellulaire par pipetage doux dans 5 ml de DMEM préchauffé + 10% de FCS.
- Effectuer une numération cellulaire. Attendez ~ 1 x 10 6 cellules par rat chiot cerveau. Un minimum de 2,5 x 10 6 cellules sont nécessaires pour chaque nucléofection, tandis queles meilleurs résultats sont obtenus en utilisant 3-4 x 10 6 cellules par nucléofection.
- Centrifuger la suspension de cellules à 433 xg pendant 5 min. Assurez-vous d'enlever autant de support que possible.
2. Nucléofection
- Remettre en suspension immédiatement le culot cellulaire chez le rat (souris ou si l'on utilise des cellules de souris) solution de nucléofection neuronal préalablement incubé à la température ambiante. Utilisez 100 pi par nucléofection Remarque:. Généralement une portée de rat de 12 chiots est suffisante pour effectuer 4 nucleofections et une portée de souris (12 chiots) est suffisante pour effectuer 2 nucleofections.
- Transférer 100 ul de la suspension cellulaire dans chaque tube Eppendorf contenant siRNA / ADN et mélanger délicatement 2-3x par pipetage avec une pipette P200.
- Ajouter l'échantillon (cell-DNA/siRNA suspension) à la partie inférieure de la nucleofectioncuvette, en prenant soin d'éviter les bulles.
- Nucleofect utilisant le programme G-013 (pour les cellules de rat) ou O-005 (pourdes cellules de souris). Un nucléofection prend environ 5 sec.
- Ajouter rapidement 1 ml de DMEM préchauffé + 10% de FCS à l'échantillon nucleofected.
- Répétez les étapes 2.4 et 2.5 pour tous les autres échantillons. Remarque: pour des résultats optimaux, la procédure de nucléofection ensemble ne devrait pas durer plus de 5 minutes.
- Transférer chaque échantillon dans un tube de 15 ml contenant 5 ml de DMEM préchauffé + FCS à 10% en utilisant la pipette en plastique fourni par le kit de nucléofection. Éviter le transfert de tout débris cellulaire au tube.
- Centrifuger les échantillons à 433 g pendant 5 min.
- Retirez soigneusement tout excès de milieu et remettre le culot en 25-30 ul de DMEM préchauffé + 10% de FCS à l'aide d'une pipette P20. Ne pas utiliser plus de 30 pi de milieu.
- Introduire à la pipette la suspension comme une goutte sur la face intérieure d'un couvercle plat de p35.
- Inversez le couvercle sur le plat de p35 contenant 2 ml de milieu complet (voir aussi la figure 1).
- Ajouter dans l'incubateur (37 ° C / 5% CO 2) pendant aumoins 5 h et jusqu'à 7 h. Plus de temps d'incubation permet une meilleure ré-agrégation d'amas cellulaires.
- Transférer les gouttes de suspension du couvercle dans le milieu complet dans le plat à l'aide d'une pipette P1000 avec une pointe de coupe.
- Incuber à 37 ° C / 5% de CO 2 pendant 24 heures pour nucleofections d'ADN et 48 h pour nucleofections siRNA / shRNA.
3. Incorporation
- Préparer un milieu complet (25 ml) et il preequilibrate à 37 ° C / 5% CO 2 pendant quelques heures.
- Sortez les aliquotes congelées de la matrice de la membrane basale de -80 ° C congélateur et décongeler sur la glace dans la chambre froide.
- Pour chaque nucléofection préparer un plat de 6 cm contenant jusqu'à huit 13 mm coverlips stériles.
- Placez les plats sur une boîte de glace recouverte d'une pellicule de plastique. Il est important de maintenir les lamelles fraîche pour empêcher la solidification matrice durant la procédure d'enrobage.
- Pour maintenir l'humidité, placer une bande de tissu humide dans un plat de 15 cm que wmal être utilisés pour contenir jusqu'à trois plats 6 cm contenant les neuroblastes embarqués.
- Ajouter milieu complet à la matrice décongelé dans un rapport 1:3. Par exemple, mélanger 40 pi de milieu complet avec 120 pi de matrice à la pipette. Cette quantité de matrice est suffisante pour intégrer des agrégats sur huit 12 mm lamelles.
- Transférer les groupes de cellules agrégés de nouveau à un tube de 15 ml et centrifuger à 433 xg pendant 5 min.
- Retirer l'excès de milieu et remettre le culot dans 10 ul de milieu complet.
- Placez 2 pi de suspension cellulaire total sur chaque lamelle stérile et ajouter 18 ul de matrice / mélange milieu complet. Utilisez la pointe de la pipette pour répandre la matrice sur toute la lamelle.
- Placer immédiatement la capsule de 6 cm contenant les lamelles dans les 15 cm plat et laisser dans l'incubateur (37 ° C / 5% CO 2) pendant 15-20 min. Lorsque la matrice est solidifié, ajouter doucement 5 ml de milieu complet à chaque 6 cm prise de plat soins à pousserbas tout lamelle flottant avec une pointe de pipette.
- Incuber pendant 24 heures à 37 ° C / 5% CO 2 pour laisser neuroblastes migrent hors des agrégats de cellules.
4. 3D migrations Assay
- Préparer les solutions nécessaires pour immunologique.
- Préparer la solution de bloc:
solution de bloc de chèvre (50 ml)
Phosphate Buffered Saline (PBS) - 5 ml
Sérum de chèvre - 7,5 ml
10% de Triton X-100 - 1,5 ml
BSA - 50 mg
H 2 O - 36 ml - Filtrer et conserver à 4 ° C.
- Préparer la solution de fixation:
Solution de fixation (100 ml)
Paraformaldéhyde (PFA) - 4 g ATTENTION: manipulez toujours PFA sous une hotte
Saccharose - 20 g (en option)
PBS à 100 ml - Sur une plaque chauffante et sous agitation constante dissolution de la PFA dans 80 ml de PBS maintenue à 65 ° C.
- Une fois que le PFA a dissous, ajouter 20 g de saccharose.
- Ajuster le pH à7,4 (en général par l'addition de NaOH 60 M ~ 1 ul pour 100 ml de solution).
- Mettre à un volume total de 100 ml avec du PBS.
- Préparer la solution de bloc:
- Immunocoloration
- Placez les lamelles dans une plaque de 24 puits.
- Rincer les lamelles avec du PBS 2x.
- Fixer les neuroblastes agrégats RMS avec une solution de fixation pendant 45 min à température ambiante.
- Rincer les lamelles avec du PBS 3x (5 min / lavage - sur une plate-forme à bascule).
- Bloquer pendant 30-60 minutes avec une solution de bloc de chèvre.
- Diluer anticorps primaires dans la solution de bloc de chèvre et incuber pendant une nuit à 4 ° C. (Si on le souhaite, la phalloïdine fluorescente (1:400) et le colorant Hoechst (1:10000) peuvent également être ajoutés à la solution d'anticorps primaire à visualiser l'actine filamenteuse et des noyaux).
- Rincer les lamelles avec du PBS 3x (5 min / lavage).
- Diluer les anticorps secondaires dans la solution de bloc de chèvre et incuber pendant 2 heures à température ambiante.
- Rincer coverslips avec du PBS 3x (5 min / lavage)
- Mont lamelles couvre avec un milieu de montage fluorescent et laisser sécher une nuit à température ambiante.
- Analyse de la migration
- Capturez des images d'agrégats de neuroblastes RMS fixes avec un microscope à fluorescence en utilisant un objectif 10X. Inclure une barre d'échelle dans une image de l'échantillon.
- Pour configurer l'échelle de quantification, de mesurer la barre d'échelle dans l'image en sélectionnant la «ligne droite» outil sur la barre d'outils de ImageJ.
- Choisissez l'option «Analyser» et cliquez sur «définir l'échelle».
- Dans la fenêtre de l'échelle définir la «distance connue» et cochez la case «globale» de garder les mêmes paramètres pour toutes les mesures.
- Utilisez l'outil «ligne segmentée» sur la barre d'outils de ImageJ pour mesurer la distance entre le bord de l'ensemble de la neuroblaste le plus migré dans 6 secteurs différents autour de l'ensemble du total (figure 3B). Considérons seulement ag isolégregates pour analyse.
- Calculer une distance moyenne de 6 valeurs obtenues pour chaque agrégat de migration.
- Mesurer 10-20 agrégats pour chaque condition dans chaque expérience et piscine résultats indépendants d'un minimum de trois expériences indépendantes. Toujours inclure un contrôle nucléofection (p. ex. GFP ou une sh de contrôle / siRNA).
Résultats
Neuroblastes peuvent être isolés avec succès à partir de tissu disséqué RMS (figure 1A) et noyées dans une matrice à trois dimensions. Cellules isolées de rat ou dans le RMS postnataux de la souris sont immunopositif des marqueurs de neuroblastes migrateurs, tels que doublecortine (DCX), ßlll tubuline ou PSA-NCAM (figures 1B-C).
Neuroblastes dissociées peuvent être efficacement nucleofected avec de l'ADN (par ex. D'un plasmide codant pour la GFP, Figure 2) ou des plasmides shRNA (figure 4) pour atteindre l'épuisement protéine, qui peut être évaluée par analyse Western blot (figure 4B) ou immunofluorescence (non représenté) .
Cellules nucleofected avec des plasmides codant pour la GFP migrent radialement pôles de neuroblastes agrégés de nouveau (figure 3A). Quantification de la distance par rapport migré 24 heures après l'intégration (figure 3B) ne montre aucune différence de migration entre GFP-posit ive cellules et cellules nonnucleofected GFP-négatif (figure 3C), indiquant que nucléofection en soi ne perturbe pas la migration. Il ya aussi pas de différence significative dans la mesure de la migration entre les neuroblastes et neuroblastes nucleofected migrent directement des explants RMS (données non présentées).

Figure 1. Dissection de neuroblastes RMS. (A) Représentation schématique de RMS neuroblastes dissection. Pour une description détaillée s'il vous plaît se référer au texte. (B) Les cellules de RMS de rat isolés sont immunopositif pour les fabricants de neuroblastes migrateurs DCX et tubuline βlll. Bar, 20 um. (C) Les cellules migrent hors de souris RMS explants expriment neuroblaste migratoire Marqueurs DCX et PSA-NCAM. Bar, 20 um.0989/50989fig1highres.jpg "target =" _blank "> Cliquez ici pour agrandir l'image.
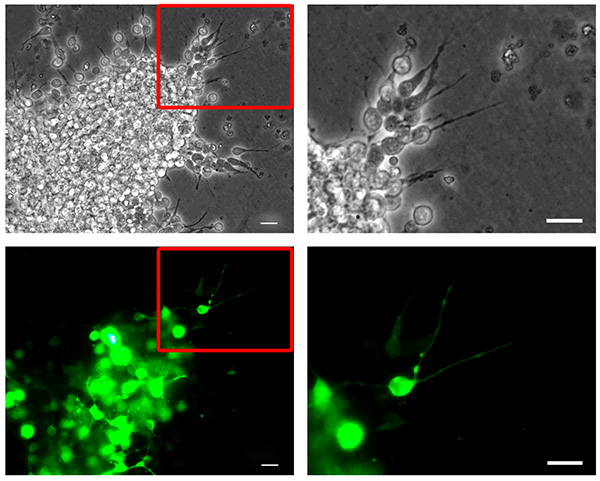
Figure 2. Souris neuroblastes nucléofection. Dissociées souris RMS neuroblastes sont nucleofected avec pMAX-GFP, agrégés de nouveau, noyées dans une matrice en trois dimensions et on a laissé migrer pendant 6 heures. Neuroblastes qui migrent d'un amas de cellules agrégés de nouveau (en haut, à contraste de phase photos) montrent l'efficacité de transfection élevée (en bas, le canal de la GFP photos). Les panneaux de la colonne de droite montrent des images de plus grossissement correspondant aux encarts en surbrillance dans les panneaux de la colonne de gauche. Bars, 20 um. Cliquez ici pour agrandir l'image .
ontenu-width = "6 po" src = "/ files/ftp_upload/50989/50989fig3.jpg" width = "500px" />
Figure 3. 3D essai de migration. (A) neuroblastes de rat ont été nucleofected avec pMAX-GFP (GFP) ou pCAG-IRES-EGFP 22 (EV), agrégés de nouveau, noyée dans la matrice et laissé migrer pendant 24 heures. Les cellules ont ensuite été fixées et immunocolorées pour la GFP (vert) et ßlll tubuline (rouge). Bar, 50 um. (B) mesure la distance de migration en utilisant ImageJ. L'amas de cellules agrégés de nouveau est divisé en 6 secteurs égaux. La distance entre le bord de la grappe (trait pointillé) et de la cellule migré plus loin est mesuré pour chaque secteur. (C) Quantification de la distance relative migré par les cellules nucleofected, des cellules nonnucleofected (GFP-positives) et de contrôle (GFP-négatif) . Cliquez ici pour agrandir l'image .
"Figure 4" fo: contenu width = "6 po" src = "/ files/ftp_upload/50989/50989fig4.jpg" width = "500px" />
Figure 4. Suivi migration des neuroblastes après shRNA nucléofection. (A) neuroblastes de rat ont été nucleofected avec un vecteur de commande shRNA (pCA-b-EGFPm5 Silencieux 3, qui exprime également EGFP 23) ou le même vecteur contenant un shRNA ciblant fascine, une protéine de l'actine-regroupement 24. Les cellules ont été agrégés de nouveau plus de 48 h, enrobées dans une matrice et de gauche à migrer pendant 24 heures. Les agrégats ont été ensuite fixées et immunocolorées pour la GFP (vert) et ßlll tubuline (rouge). Bar, 50 um. (B) fascine efficace épuisement peut être détectée 50 heures après shRNA nucléofection par analyse western blot. Actine est montrée ici comme un témoin de charge (C) L'analyse quantitative de la distance par rapport à la migration montrant que l'épuisement fascine entrave sérieusement la migration des neuroblastes. (Moyenne ± SEM; ** p <0,01, n = 3 expériences indépendantes). Cliquez ici pour agrandir l'image.
Discussion
La migration des neuroblastes le long des RMS à l'emplacement final dans l'OB est une étape fondamentale dans la neurogenèse postnatale. Cependant, les mécanismes moléculaires qui contrôlent ce processus complexe est loin d'être entièrement comprise.
La procédure expérimentale décrite ici permet l'étude de la migration des neuroblastes in vitro. Nous avons adapté un protocole précédemment publié pour isoler RMS neuroblastes de souris ou rat 25 postnatale précoce. Pour obtenir des résultats optimaux, il est important de maîtriser l'étape de dissection, car il est essentiel de maintenir l'intervalle de temps entre la dissection et nucléofection à un minimum. Après nucléofection, neuroblastes peuvent être agrégés de nouveau, noyées dans une matrice tridimensionnelle et de gauche à migrer sur une période de 24 heures. Sinon, pour des fins autres que la migration (par exemple immunofluorescence ou analyse Western blot), les cellules peuvent être immédiatement plaqué après nucléofection sur polyornithine/laminin-lamelles recouvertes, où ils survivent jusqu'à 4-5 jours. Souris et le rat neuroblastes migrent dans Matrigel dans une mesure similaire, mais des cellules de souris semblent avoir une plus forte tendance à migrer dans les chaînes que les cellules de rat.
En fonction de l'objectif de l'étude, les neuroblastes peuvent être nucleofected avec différents plasmides codant pour des protéines fluorescentes ou de type / mutant protéines sauvages d'intérêt. Pour optimales plasmides d'expression de la protéine avec un promoteur CAG (promoteur de β-actine par le CMV activateur et β-globine queue poly-A) 26 sont fortement recommandés. De plus, les oligos siARN ou des plasmides shRNA peuvent être nucleofected à knockdown cibles d'intérêt. L'appauvrissement de la protéine efficace peut être visualisée par immunofluorescence ou par western blot (lyse habituellement incorporés agrégats de 1 rat chiot avec 50 ul de tampon de lyse standard).
Nucléofection est une méthode relativement simple pour la transfection de neuroblastes primaires, offre une alternative plus facile et plus rapide à viral transfection médiée par un vecteur, et peut atteindre une haute (~ 70-80%) efficacité de la transfection. Il est essentiel de travailler rapidement au cours de la procédure de nucléofection, depuis le départ de neuroblastes dans la solution de nucléofection pendant une période prolongée réduit considérablement la viabilité cellulaire.
Le rendement moyen des cellules de dissection RMS est relativement faible pour les souris P7 (~ 5 x 10 5 cellules / cerveau) par rapport aux rats P7 (~ 1 x 10 6 cellules / cerveau) et d'au moins 3 x 10 6 cellules par nucléofection sont tenus pour réaliser la transfection avec ~ 50% de rendement. En outre, les neuroblastes de rat semblent mieux résister à nucléofection rapport à neuroblastes de souris. Par conséquent, les petits postnatale précoce (P6-P7) rat pourraient représenter une source de neuroblastes pratique, considérant également que l'organisation de RMS de rats et de souris sont remarquablement similaire 27 et que l'étendue de rat et de la souris migration des neuroblastes in vitro est également comparable. Il est conseillé de ne pas garder les groupes agrégés de nouveau de neuroblastes nucleofected en suspension pendant plus de 48 heures pour éviter les effets anormaux sur la morphologie et la migration cellulaire (nos observations non publiées).
Le test 3D décrit ici peut être utilisé pour quantifier la migration des neuroblastes à un point de temps fixe après incorporation dans la matrice (par exemple. 24 h). Les granulats de différentes tailles peuvent être utilisés dans l'analyse, car il n'existe pas de corrélation significative entre la taille des agrégats et de la distance de migration (nos observations non publiées). Pour visualiser et étudier plus la dynamique de la migration des neuroblastes, imagerie time-lapse peut être utilisé. Il est recommandé d'effectuer l'analyse de la migration dans un intervalle de 24 heures après l'intégration, car la vitesse de neuroblastes semble diminuer de façon drastique à des points de temps plus longues (nos observations non publiées).
Il ya des limites à ce protocole. En premier lieu, la mesure nucléofection peut être utilisé pour les premiers neuroblastes de rongeurs postnatales, alors que l'infection avec des vecteurs viraux méthode de transfection reste le plus efficace pour 28 neuroblastes adultes. En second lieu, l'analyse in vitro de migration ne reproduit pas entièrement l'architecture complexe des RMS observées in vivo. En effet, bien que les neuroblastes maintenir la capacité de migrer d'une manière similaire à leurs homologues in vivo, dans le montage expérimental décrit ici, ils n'ont pas d'interactions avec d'autres composants RMS telles que les astrocytes et les vaisseaux sanguins, ce qui contribue également à réguler leur motilité 9,29, 30. Ce problème peut être réglé à l'avenir par l'optimisation des systèmes de modèle de co-culture en trois dimensions.
En conclusion, la combinaison nucléofection avec un test de migration 3D représente un outil précieux pour mieux comprendre les mécanismes moléculaires sous-jacentsla migration des neuroblastes. Cette procédure expérimentale fournit une méthode initiale, rapide et relativement simple d'évaluer le rôle des régulateurs candidats de la migration des neuroblastes, qui peut encore être validées par d'autres approches comme in vivo postnatale électroporation et imagerie time-lapse de cultures tranche de cerveau 28,31,32 .
Déclarations de divulgation
Les auteurs n'ont rien à révéler.
Remerciements
Ce travail a été financé par une subvention de projet de fiducie Wellcome attribué à PD et GL (089236/Z/09/Z). SG a été soutenue par une bourse d'études de doctorat en biotechnologie et Conseil de recherches en sciences biologiques. Nous remercions Matthieu Vermeren pour le genre de cadeau du vecteur shRNA et Jennifer Shieh pour de précieux conseils sur neuroblastes nucléofection.
matériels
| Name | Company | Catalog Number | Comments |
| Hank’s Balanced Salt Solution (HBSS) | Invitrogen Life Technologies | 14175129 | |
| HEPES | Sigma-Aldrich | H3375-25G | |
| Penicillin-Streptomycin | Invitrogen Life Technologies | 15140-122 | |
| 2.5% Trypsin-EDTA (10x) | Gibco | 15090-046 | store 200 µl aliquots at -20 °C |
| DNAse I Vial (D2) | Worthington | LK003170 | ≥1,000 units per vial; store 50 µl aliquots at -20 °C |
| Dulbecco Modified Eagle's Medium (DMEM) | Gibco | 11960-044 | |
| Fetal Calf Serum (FCS) | Hyclone | SH3007902 | |
| Neurobasal medium | Gibco | 21103-049 | |
| B27 supplement | Invitrogen Life Technologies | 17504044 | |
| L-Glutamine (200 mM) | Invitrogen Life Technologies | 25030-081 | |
| D-(+)-Glucose solution (45%) | Sigma-Aldrich | G8769 | |
| Matrigel Basement Membrane Matrix, Growth Factor Reduced (GFR), Phenol Red-free, 10 ml, LDEV-Free | BD Biosciences | 356231 | prepare 120 µl aliquots at 4 °C, then store at -80 °C |
| PFA | Sigma-Aldrich | 441242 | |
| Sucrose | BDH | 102745C | |
| Goat serum | Sigma-Aldrich | 69023 | |
| Triton X-100 | VWR International Ltd. | 306324N | |
| BSA | Fisher Chemical | BPE9701-100 | |
| Dako fluorescence mounting medium | Dako | S3023 | |
| Rat neuron nucleofection kit | Lonza | VPG-1003 | |
| Mouse neuron nucleofection kit | Lonza | VPG-1001 | |
| Microsurgical knife | Angiotech | 7516 | |
| McIlwain tissue chopper | The Mickle Laboratory Engineering Company | ||
| Nucleofector II | Lonza |
Références
- Ming, G. L., Song, H. J. Adult Neurogenesis in the Mammalian Brain: Significant Answers and Significant Questions. Neuron. 70, 687-702 (2011).
- Alonso, M., et al. Activation of adult-born neurons facilitates learning and and memory. Nat. Neurosci. 15, 897-U127 (2012).
- Lazarini, F., Lledo, P. M. Is adult neurogenesis essential for olfaction?. Trends Neurosci. 34, 20-30 (2011).
- Arvidsson, A., Collin, T., Kirik, D., Kokaia, Z., Lindvall, O. Neuronal replacement from endogenous precursors in the adult brain after stroke. Nat. Med. 8, 963-970 (2002).
- Jin, K. L., et al. Evidence for stroke-induced neurogenesis in the human brain. Proc. Natl. Acad. Sci. U.S.A. 103, 13198-13202 (2006).
- Kim, Y., Szele, F. G. Activation of subventricular zone stem cells after neuronal injury. Cell Tissue Res. 331, 337-345 (2008).
- Massouh, M., Saghatelyan, A. De-routing neuronal precursors in the adult brain to sites of injury: Role of the vasculature. Neuropharmacology. 58, 877-883 (2010).
- Pathania, M., Yan, L. D., Bordey, A. A symphony of signals conducts early and late stages of adult neurogenesis. Neuropharmacology. 58, 865-876 (2010).
- Lois, C., Alvarez-Buylla, A. Long-Distance Neuronal Migration in the Adult Mammalian Brain. Science. 264, 1145-1148 (1994).
- Lois, C., Garcia-Verdugo, J. M., Alvarez-Buylla, A. Chain migration of neuronal precursors. Science. 271, 978-981 (1996).
- Belvindrah, R., Nissant, A., Lledo, P. M. Abnormal Neuronal Migration Changes the Fate of Developing Neurons in the Postnatal Olfactory Bulb. J. Neurosci. 31, 7551-7562 (2011).
- Battista, D., Rutishauser, U. Removal of Polysialic Acid Triggers Dispersion of Subventricularly Derived Neuroblasts into Surrounding CNS Tissues. J .Neurosci. 30, 3995-4003 (2010).
- Conover, J. C., et al. Disruption of Eph/ephrin signaling affects migration and proliferation in the adult subventricular zone. Nat. Neurosci. 3, 1091-1097 (2000).
- Mobley, A. K., McCarty, J. H. beta 8 Integrin is Essential for Neuroblast Migration in the Rostral Migratory Stream. Glia. 59, 1579-1587 (2011).
- Nguyen-Ba-Charvet, K. T., et al. Multiple roles for slits in the control of cell migration in the rostral migratory stream. J. Neurosci. 24, 1497-1506 (2004).
- Garzotto, D., Giacobini, P., Crepaldi, T., Fasolo, A., De Marchis, S. Hepatocyte growth factor regulates migration of olfactory interneuron precursors in the rostral migratory stream through Met-Grb2 coupling. J. Neurosci. 28, 5901-5909 (2008).
- Platel, J. C., Stamboulian, S., Nguyen, I., Bordey, A. Neurotransmitter signaling in postnatal neurogenesis: The first leg. Brain Res. Rev. 63, 60-71 (2010).
- Dityateva, G., et al. Rapid and efficient electroporation-based gene transfer into primary dissociated neurons. J. Neurosci. Meth. 130, 65-73 (2003).
- Shieh, J. C., Schaar, B. T., Srinivasan, K., Brodsky, F. M., McConnell, S. K. Endocytosis Regulates Cell Soma Translocation and the Distribution of Adhesion Proteins in Migrating Neurons. PloS One. 6, (2011).
- Viesselmann, C., Ballweg, J., Lumbard, D., Dent, E. W. Nucleofection and Primary Culture of Embryonic Mouse Hippocampal and Cortical Neurons. J. Vis. Exp. , e2373 (2011).
- Gartner, A., Collin, L., Lalli, G. Nucleofection of primary neurons. Method Enzymol. 406 (06), 374-388 (2006).
- Causeret, F., et al. The p21-Activated Kinase Is Required for Neuronal Migration in the Cerebral Cortex. Cereb. Cortex. 19, 861-875 (2009).
- Bron, R., Eickholt, B. J., Vermeren, M., Fragale, N., Cohen, J. Functional knockdown of neuropilin-1 in the developing chick nervous system by siRNA hairpins phenocopies genetic ablation in the mouse. Dev. Dynam. 230, 299-308 (2004).
- Sonego, M., et al. Fascin regulates the migration of subventricular zone-derived neuroblasts in the postnatal brain. J. Neurosci. 33, 12171-12185 (2013).
- Ward, M., Rao, Y. Investigations of neuronal migration in the central nervous system. Methods Mol. Biol. 294, 137-156 (2005).
- Niwa, H., Yamamura, K., Miyazaki, J. Efficient Selection for High-Expression Transfectants with a Novel Eukaryotic Vector. Gene. 108, 193-199 (1991).
- Peretto, P., Giachino, C., Aimar, P., Fasolo, A., Bonfanti, L. Chain formation and glial tube assembly in the shift from neonatal to adult subventricular zone of the rodent forebrain. J. Comp. Neurol. 487, 407-427 (2005).
- Khlghatyan, J., Saghatelyan, A. Time-lapse Imaging of Neuroblast Migration in Acute Slices of the Adult Mouse Forebrain. J. Vis. Exp. , e4061 (2012).
- Bozoyan, L., Khlghatyan, J., Saghatelyan, A. Astrocytes Control the Development of the Migration-Promoting Vasculature Scaffold in the Postnatal Brain via VEGF Signaling. J. Neurosci. 32, 1687-1704 (2012).
- Whitman, M. C., Fan, W., Rela, L., Rodriguez-Gil, D. J., Greer, C. A. Blood Vessels Form a Migratory Scaffold in the Rostral Migratory Stream. J. Comp. Neurol. 516, 94-104 (2009).
- Sonego, M., Ya, Z., Oudin, M. J., Doherty, P., Lalli, G. In vivo Postnatal Electroporation and Time-lapse Imaging of Neuroblast Migration in Mouse Acute Brain. J. Vis. Exp. , (2013).
- Feliciano, D. M., Lafourcade, C. A., Bordey, A., lique, Neonatal Subventricular Zone Electroporation. J. Vis. Exp. , e50197 (2013).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon