Method Article
Taches de sang séché - préparer et traiter pour utilisation dans les immunoessais et Techniques moléculaires
Dans cet article
Résumé
La préparation et le traitement des taches de sang séché (DBS) pour leur analyse finale sont encore mal standardisées pour la plupart des applications diagnostiques. Pour remédier à cette lacune, un protocole étape par étape complète est suggéré et évalué par la suite en ce qui concerne son efficacité pour la détection des marqueurs des infections virales.
Résumé
L’idée de collecte de sang sur une carte de papier et par la suite en utilisant les taches de sang séché (DBS) à des fins diagnostiques, son originaires il y a un siècle. Depuis lors, DBS stable pour des décennies, est resté principalement axée sur le diagnostic des maladies infectieuses, notamment dans les milieux de ressources limitées ou le dépistage systématique des nouveaux-nés pour les maladies métaboliques héréditaires et seulement récemment ont une variété de nouvelles et innovantes applications DBS commencées à émerger. Pendant de nombreuses années, pré-analytique variables étaient considérées comme uniquement de façon inappropriée dans le domaine des tests de DBS et aujourd'hui encore, à l’exception des nouveau-nés de dépistage, toute la phase pré-analytique, qui comprend la préparation et la transformation de DBS pour leur l’analyse finale n’a pas été normalisée. Dans ce contexte, un protocole complet étape par étape, qui porte sur al les phases essentielles, est proposé, c'est-à-dire, une accumulation de sang ; préparation des gouttes de sang ; séchage des gouttes de sang ; stockage et transport de DBS ; élution de DBS et enfin des analyses des éluats DBS. L’efficacité de ce protocole a été d’abord évaluée avec des paires de 1 762 sérum couplés/DBS pour la détection des marqueurs du virus de l’hépatite B, virus de l’hépatite C et les infections de virus de l’immunodéficience humaine sur une plateforme analytique automatisée. Dans un second temps, le protocole a été utilisé au cours d’une étude pilote, qui a été menée sur des toxicomanes actifs dans les villes allemandes de Berlin et Essen.
Introduction
L’idée d’utiliser le sang prélevé sur une carte de papier faite de cellulose est attribuée à Ivar Christian Bang (1869-1918), le père de microanalyse clinique moderne1, 2. En 1913, Bang déterminé le glucose à partir des mesures d’azote éluats de sang séché taches (DBS)3 et, plus tard, également réalisés à l’aide de la méthode de Kjeldahl avec cette technique de papier filtre2. Par la suite, plusieurs chercheurs ont observé sur l’utilisation de DBS pour les tests sérologiques pour diagnostiquer la syphilis2. Aussi tôt qu’en 1924, Chapman a résumé les avantages de DBS test quand il a souligné en particulier quatre éléments, qui sont encore valables aujourd'hui : ponction par rapport aux classiques (1), moins le volume sanguin est nécessaire et ce fait a été plus important en pédiatrie diagnostic ; (2) collecte de sang est simple, non invasif et peu coûteux ; (3) le risque de contamination bactérienne ou une hémolyse est minime ; et DBS (4) peuvent être conservées pendant de longues périodes avec presque aucune détérioration des analytes2, 4. Outre son utilisation dans le dépistage de la syphilis, outre les premières applications de la technique DBS inclus, par exemple, la détection d’anticorps contre la rougeole, les oreillons, poliovirus, virus parainfluenza et virus respiratoire syncytial (VRS) en 19532, l’identification des Shigella dans les excréments séchés sur du papier filtre et expédié par la poste de l’Indonésie à Leyde aux Pays-Bas ainsi que la détection des anticorps à Schistosoma dans DBS prises dans les zones d’endémie et analysé plus de trois mois plus tard5 . En 1963, cinquante ans après de Bang original communication2, 6, Guthrie a publié enfin sa célèbre méthode pour le diagnostic de la phénylcétonurie de DBS obtenue par une piqûre de talon de nouveaux-nés les7, 8.
Bien que depuis lors, DBS étaient considérés comme une méthode communément applicable pour rassembler, stocker, transporter et analyser une variété de fluides de corps humains5, leur utilisation dans le diagnostic reste principalement axée sur le diagnostic de infections surtout chez les ressources limitées et le dépistage systématique des nouveau-nés pour troubles métaboliques héréditaires pour des décennies les9, 10. Depuis 2005, cependant, une variété d’applications de DBS nouvelles et novatrices ont commencé à apparaître. Il en est résulté une augmentation presque exponentielle du nombre de publications scientifiques respectives sur DBS de 50 à près de 450 par an à l’heure actuelle. Parmi les applications émergentes sont des domaines aussi divers que la toxico - et les études de pharmacocinétique, profilage métabolique, suivi thérapeutique pharmacologique, toxicologie médico-légale ou pollution control10, 11.
Tests de DBS, ainsi, a une marche triomphale à travers des diagnostics en laboratoire clinique au cours des dernières années 1002. Comme en chimie clinique12, cependant, au cours de ce mois de mars pré-analytique variables ne étaient pas adéquatement considérées pendant de nombreuses années. En effet, même aujourd'hui, après des activités éminentes comme CDC papier-filtre évaluation projet13 ou l’élaboration d’une norme nationale pour la collecte de sang sur un papier filtre dans le cadre du dépistage14, la phase pré-analytique est encore largement sous-estimé dans la plupart des autres champs, dans laquelle DBS test est appliquée en5, 10.
Dans ce contexte, un protocole étape par étape complète14-16 pour utilisation dans les immunoessais et techniques moléculaires, qui couvre toutes les étapes essentielles, est suggéré pour la préparation et le traitement DBS dans la communication ci-après : (1) collecte de sang ; (2) préparation des gouttes de sang ; (3) séchage des gouttes de sang ; (4) le stockage et le transport ; (5) élution de DBS ; et enfin (6) analyses des éluats DBS. L’efficacité du protocole a été tout d’abord évaluée avec des paires de 1 762 sérum couplés/DBS pour détecter les virus de l’hépatite B (VHB) antigène de surface (AgHBs), anticorps dirigés contre l’antigène de noyau (anti-HBc), anticorps dirigés contre l’antigène de surface (anti-HB), l’ADN du VHB, anticorps pour le virus de l’hépatite C (VHC) (anti-VHC), essais de l’ARN du VHC et virus de l’immunodéficience humaine (VIH) 1-p24-antigène/anti-VIH 1/2 à l’aide d’une plate-forme entièrement automatisée ou qualitative sensible des acides nucléiques. 17. dans un deuxième temps, le protocole a été utilisé dans l’étude pilote « drogues et chronique Infectious Diseases » (« DRUCK Study ») qui a été menée par l’Institut Robert Koch-en étroite collaboration avec le Centre National de référence pour l’hépatite C sur actif usagers de drogue dans les villes allemandes de Berlin et Essen18.
Protocole
Étant donné que le protocole est conçu pour une utilisation dans le diagnostic médical, sa demande doit suivre les principes de la déclaration d’Helsinki19. Pour la première partie des résultats présentés dans la présente communication, les deux un accord séparé par les patients et l’approbation par un Comité d’éthique semblent être dispensable pour deux raisons : (1) « lors de l’admission » à l’hôpital universitaire d’Essen, « dispose de tous les patients consentement écrit de toutes les recherches biochimiques, bactériologiques et virologiques nécessaires. » 17 (2) « tous les échantillons utilisés tout au long de l’évaluation des tests de DBS ont été envoyés à l’Institut de virologie dans le processus de diagnostic clinique de routine. Ainsi, aucun des spécimens ont été recueilli spécifiquement dans le but de l’étude, pas une seule ponction supplémentaire a été effectuée et aucun des matériaux a été testé pour tout paramètre autre que celles requises par les médecins dans le cadre de la normale diagnostic « marche à suivre. 17 l’étude « Médicaments et maladies infectieuses chroniques » (DRUCK Study »)18, dans laquelle DBS essais enfin servait dans les villes allemandes de Berlin et Essen à évaluer ceux qui ont activement s’injectent des drogues, a été approuvé par le Commissaire fédéral aux données Protection et la liberté de l’Information (Berlin, Allemagne) et ainsi que par le Comité d’éthique de la Charité de l’Université médicale, (Berlin, Allemagne).
1. collecte de sang
- Ponction de14, 15, 20, 21
- Mettez des gants jetables en latex et nettoyer la zone de la ponction prévue (préférence la veine cubitale médiane dans la cubitale) avec un désinfectant approprié, par exemple, alcool isopropylique à 70 %.
- Appliquer un garrot 4 à 6 pouces au-dessus du site de ponction putatif à distendre les veines. Introduire l’aiguille dans la veine du patient et, une fois en place, remplir doucement le tube de sang connectés, qui contient l’EDTA comme anticoagulant.
- Dès la ponction veineuse est terminée, relâcher le garrot et retirer l’aiguille. Puis, appuyez sur une compresse sèche sur le site de ponction, qui par la suite peut être maintenu en place par un bandage.
- Perforation de la peau (Figure 1 a)13-15, 20, 22, 23
- Enfiler une paire de gants jetables en latex.
- Avant la perforation de la peau, le patient doit réchauffer ses mains. Le doigt est massé axonales l’enrichir le sang circuler vers de site de ponction.
- Nettoyer la peau de la face palmaire de la phalange distale de l’extrémité de la troisième ou quatrième doigt de la main non-écrit avec un désinfectant approprié, par exemple, alcool isopropylique à 70 %. Piquer la peau par une lancette à usage unique de sécurité. Le doigt se tiendrait dans une position telle que la gravité facilite la collecte de sang sur le bout des doigts.
- Lorsque le prélèvement du sang capillaire par ponction de la peau est terminée, placer un bandage sur le bout du doigt.
2. préparation des taches de sang
- Préparation à partir de sang prélevé par ponction veineuse15
- Repérer l’anti-coagulé (EDTA) ensemble veineux sang sur les cartes de filtre dès que possible. Ne préparez pas de taches de sang séché de plus de 24 heures après la ponction veineuse.
- Mettre toutes les informations nécessaires à l’identification du patient sur la carte de filtre. Une seule carte doit être repérée seulement avec le sang d’un individu.
- Mettez des gants jetables en latex.
- Retourner doucement le tube de prélèvement de sang 2 à 4 fois et ensuite ouvrir le bouchon avec précaution.
- Aspirer 50 µl de sang veineux tout en utilisant une pipette avec un embout jetable. Transférer le sang vers le centre d’un cercle sans toucher le papier filtre directement avec l’embout de la pipette. Essayer de saturer complètement le cercle.
- Répétez cette procédure pour remplir tous les cercles requises de la carte.
- Préparation du sang recueilli par peau percer (Figures 1 b et 1C)13-16, 23
- Essuyer la première goutte de sang avec un tampon de gaze parce qu’il peut contenir des liquides tissulaires excédentaire. Masser le doigt à nouveau pour augmenter le flux sanguin à la ponction. Transférer la baisse suivante à un des cercles d’une carte de filtre sans toucher la surface directement avec le bout des doigts. Permettre au sang d’être trempé dans la texture du filtre par des forces capillaires seulement.
- Laissez la prochaine grosse goutte de forme de sang capillaire sur le bout du doigt et ramasser en cercle suivant. Continuez cette procédure jusqu'à ce que tous les cercles nécessaires sont remplies ou la circulation sanguine s’arrête.
- Ne pas squeeze ou « lait » le doigt trop si le débit sanguin ne suffit pas à combler tous les cercles requises de la carte de filtre. En cas d’arrêt de la circulation sanguine, placer un bandage sur le bout du doigt. Effectuer une deuxième crevaison de peau sur un autre doigt si plus de sang est nécessaire pour l’examen.
3. séchage des taches de sang
- Pour sécher les taches de sang, mettre le filtre cartes sur un papier propre serviette dans une enceinte de sécurité biologique et les laisser sécher, préférence O/N (mais pour au moins 4 heures), à la droite en l’absence de toute source de chaleur externe. Lorsque le processus de séchage est terminé, les taches de sang ont une couleur brunâtre foncée uniformément et sans zones rouges sont visibles plus (Figure 1)13, 15, 16.
4. stockage et transport des taches de sang séché (DBS)
Remarque : Le traitement des taches de sang peut être interrompu après séchage. Les cartes de filtre peuvent désormais être stockées13-16, 23.
- Pour le stockage, mettre la carte de papier filtre dans un sac unique, gaz-imperméable à capuche, contenant 1 à 2 sachets déshydratants pour protéger les spécimens de l’humidité (Figure 1E). Ajouter éventuellement une carte d’indicateur d’humidité.
- Transférer ce sac dans un congélateur à une température de-20 ° C ou plus bas dès que possible. Si congélateurs ne sont pas disponibles dans des conditions naturelles, conservation à-4 ° C ou même à la température ambiante est possible jusqu'à 14 jours.
- Transport des échantillons congelés de DBS sur la glace sèche. Pour les cartes de filtre initialement maintenus à température ambiante, utilisent un système de triple emballage, qui comprend le sac fermeture éclair comme les réservoirs intérieurs ainsi qu’un intérieur et l’enveloppe extérieure. Non content de marquages sont requis sur l’enveloppe extérieure pour l’expédition par la poste, mais le symbole biohazard international doit être apposé sur le conteneur interne primaire16.
- Exclure les cartes filtre de traitement ultérieur si le dessiccateur et/ou de la carte d’indicateur humidité supplémentaire change d’une couleur rose.
5. l’élution du sang séché taches13, 15, 16, 23
- Percez un spot avec un dispositif à usage unique de 6 mm de chaque cercle sanglant de la carte de filtre de Grade 903 (Figure 1F). Transfert de tous les coups de poing des taches de sang séché d’un seul patient à un puits de la plaque de 12 puits.
- Remplir le puits avec une solution saline tamponnée au phosphate contenant 0,05 % Tween 20 et 0,08 % d’azide de sodium (Figure 1). Adapter le volume de tampon supplémentaire minime part aux exigences du test utilisé pour une analyse ultérieure des éluats de taches de sang séché.
- Répétez ces étapes pour obtenir une seconde série d’éluats tache de sang séché afin d’effectuer des analyses moléculaires.
- Mettre la plaque de culture cellulaire sur un agitateur de laboratoire et de laisser les taches de sang séché perforée éluer doucement pendant au moins 4 heures ou, de préférence, O/N (Figure 1 H).
- Le lendemain, les taches sont presque exempts de sang et des surnageants hémolytiques ont formé (Figure 1I). Transférer ces éluats microtubes à centrifuger. Ensuite, les soumettre à une centrifugation pendant 2 min à 10 500 g (Figure 1J) pour libérer les surnageants de tous les débris qui s’était formé au cours d’élution (Figure 1 K).
6. analyse des éluats
- Les éluats centrifugés sont maintenant prêts à être utilisés pour les analyses prévues. Étudier les éluats de marqueurs de l’hépatite B, virus de l’hépatite C et VIH en utilisant des kits disponibles dans le commerce et suivre attentivement les instructions des fabricants respectifs (Figure 1 L).
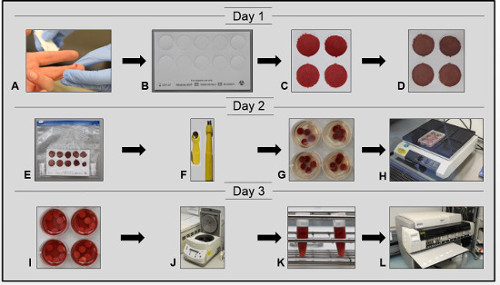
Figure 1. Graphique Sommaire du protocole proposé dans la présente communication pour la préparation et le traitement des taches de sang séché être utilisé dans les immunoessais et par des techniques moléculaires. Ensemble tube de prelevement sanguin et capillaire sanguin obtenu par ponction veineuse ou perforation de la peau par une lancette (A) peuvent servir d’échantillons pour l’analyse de tache de sang séché. Après le transfert du sang aux cercles d’une carte de filtre de Grade 903 (B, C), les échantillons doivent être séchés préférence O/N à la température ambiante sous une hotte à taches de forme d’une couleur uniformément brunâtre sans n’importe quel mélange de rouge de sécurité biohazard zones (D). Lors du séchage des taches de sang est terminé et le stockage est nécessaire, les cartes filtre peuvent être emballés dans des sacs à fermeture à glissière imperméable au gaz contenant de 1 à 2 sachets déshydratants (E). Traitement ultérieur de laboratoire de DBS constituent la génération des coups de poing par un dispositif à usage unique 6 mm depuis le Centre des cercles (F, G), l’élution des coups de poing dans un tampon PBS pendant au moins 4 heures ou, préférablement, O/N sur un agitateur (H ), la récupération des éluats (j’ai) et enfin centrifugation des coupes du laboratoire (J) pour libérer les éluats DBS de tout débris qui pourrait avoir son origine au cours du processus d’élution (K). Par la suite, les éluats DBS sont prêts pour des analyses qui ont été réalisées par une plate-forme entièrement automatisée (L) afin de détecter des marqueurs sérologiques des infections à VHB, VHC et VIH, respectivement. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
Résultats
L’efficacité du protocole proposé pour la préparation et le traitement de DBS a été tout d’abord évaluée par l’analyse de 1 762 paires de sérum couplés/DBS pour les marqueurs de l’infection à VHB, VHC et VIH. 17. à cet effet, DBS ont été préparés à partir de 100 µl de sang entier veineux (cf. points 2.1.1 – 2.1.6 du protocole précédent) et sont élués avec 1 000 µl de PBS-basée de la mémoire tampon, chacun, (cf. points 5.1 à 5.5 du protocole susmentionné) pour terminer le processus pour tous les sept paramètres dans deux opérations distinctes. Une telle approche sans optimisation minutieuse des conditions d’élution pour chaque analyte unique semble être inévitable car un débit assez élevé échantillon était prévu dans un temps relativement court pendant l’étude de terrain à paraître « drogues et chronique Infectious Diseases » (« DRUCK Study »).
Toutes les mesures ont adhéré aux recommandations du fabricant dans le cadre des analyses DBS, mais avaient dû être modifié en ce qui concerne les déterminations de l’AgHBs et l’anticorps anti-HBs pour compenser l’effet de l’hémolyse ou le résultat de la dilution. Avec une valeur de seuil de 0,05 UI/ml, tests AgHBs de DBS éluats conduisent à un taux de faux positifs de 14,7 % (52 sur 354) par rapport au sérum échantillons (Figure 2 a). Récepteur de fonctionnement caractéristique (ROC) analyse25, 26 des données indique qu’une augmentation du seuil à 0,15 UI/ml se traduirait par un idéal de la séparation de l’AgHBs positifs de HBsAg-négatifs (0,986 [sensibilité], 0,000 [1-spécificité], Figure 2 b). En revanche, avec un seuil de 10 UI/l pour la quantification d’anticorps anti-HBs, anticorps à qu'un taux de faux négatifs des mesures de 14,2 % (47 sur 331) a été enregistrent (Figure 2). Donc, après analyse ROC à nouveau, ce seuil a été abaissé à 1,5 UI/l pour obtenir une discrimination optimale des valeurs (0,917 [sensibilité], 0,007 [1-spécificité], Figure 2D).
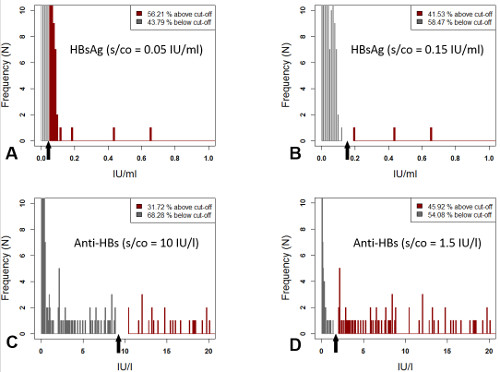
Figure 2. Ag HBs et anticorps anti-HBs test dans les éluats DBS (modifiés d’après17). L’augmentation de ROC-guidée de la valeur de seuil pour la quantification d’AgHBs de 0,05 UI/ml (A) à 0,15 UI/ml (B) réduit le taux de résultats faussement positifs de 14,7 % à 0 %. De même, l’analyse ROC des concentrations d’anticorps anti-HBs suggère une diminution du seuil respectif de 10 UI/l (C) à 1,5 UI/l (D), éliminant ainsi complètement faux-négatifs, qui représentait initialement 14,2 % de toutes les déterminations. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
Les résultats des analyses couplées sérum/DBS sont résumés dans le tableau 117. Aucun non-spécificité a été enregistrée au cours de la DBS stable pour tous les analytes de sept.
Lorsque les éluats DBS ont été étudiés pour la présence de l’AgHBs, i. e. le paramètre key sérologique d’une infection aiguë ou chronique par le VHB, une sensibilité analytique de 98,6 % a été déterminée. AgHBs concentrations dans les deux sérums faussement négatifs étaient 749 UI/ml et 6 UI/ml, respectivement. Anticorps anti-HBc ont été correctement détectés dans 176 sur 204 (i. e 86,3 %) Éluats DBS. Vingt-deux sur les 28 spécimens qui n'ont pas été détectés par les mesures provenaient de personnes co-infectées par le VIH. Donc, si les personnes séropositives ont été exclues du calcul, une sensibilité de 97,1 % a été atteint pour récupérer les anticorps anti-HBc de sang veineux entier séché éluée. Des observations similaires était vraies pour le dosage des anticorps anti-HBs. Même après ajustement de la valeur seuil du test à 1,5 UI/l, neuf résultats DBS sérum discordants s’est produite. Chez les patients ne pas co-infectés par le VIH, les concentrations sériques d’anticorps anti-HBs de 11 – 26 UI/l ont été trouvées, qui étaient trop faibles pour permettre une détection après élution du sang séché.
Anticorps anti-VHC sont révélateurs de soit une infection aiguë ou chronique ou résolue. Des résultats faussement négatifs anti-VHC (i. e. 2.2 %) seulement quatre ont été déterminées par les éluats DBS et autres analyses sérologiques et moléculaires a clairement démontré que les sérums respectifs proviennent très probablement de patients, dont les infections avaient depuis longtemps été résolu.
La détection des anticorps anti-VIH dans les éluats DBS avec le système entièrement automatisé a été un processus complètement lisse qui a rapporté une sensibilité analytique de 100 %.
« L’ADN du VHB moyenne concentration de sang éluats a été réalisée sur 100 spécimens (ADN concentration moyenne : 1 573 898 UI/ml, gamme : < 357 - > 17,860,000 UI/ml) et a donné une valeur de 93,0 %. Ainsi, sept échantillons avec des concentrations d’ADN-VHB sérique entre 409 et 3 643 UI/ml n’ont pas été détectés par la DBS stable. De 100 sérums qui s’étaient avérés positifs l’ARN du VHC (concentration de l’ARN du VHC moyenne : 1 415 944 UI/ml, gamme : 2 479 - > 7 692 000 UI/ml), correspondant aliquotes de sang étaient disponibles. L’enquête comparative a entraîné une sensibilité analytique de 100 % pour les déterminations de l’ARN du VHC d’éluats DBS. » 17
Pour tester le protocole indiqué pour préparer et traiter les DBS dans des conditions naturelles, il a été utilisé en étroite collaboration avec l’Institut Robert Koch-(Berlin, Allemagne) au cours de la phase pilote de l’étude « Drogues et chronique maladies infectieuses », qui a été menées sur les usagers de drogue actifs dans les villes allemandes de Berlin et Essen18. Tous les 534 participants inscrits (433 hommes et 101 femmes) a subi le prélèvement sanguin capillaire comme décrit en détail dans les sections 2.2.1 à 2.2.3 du protocole précédent, et DBS sont, encore une fois, éluées par addition de 1 000 µl de tampon PBS.
Deux personnes ont été diagnostiquées pour être une infection chronique par le VHB, et 39 a montré le modèle sérologique d’une infection à VHB résolu. En outre, quinze participants étaient positifs pour les anticorps anti-HBs (statut après la vaccination) et huit se sont révélés positifs pour les anticorps anti-HBc seul. La prévalence des anticorps anti-VHC parmi les participants était de 57,3 % (N = 193) à Berlin et à 73,0 % (N = 144) à Essen. De l’anticorps positifs des échantillons 65 % (N = 125) et 62 % (N = 89) ont été également virémique. Vingt-cinq sur les 534 personnes étaient positifs anti-VIH. Dix-neuf des infections étaient déjà connues et 24 d'entre eux ont été co-infectées par le VHC.
Les résultats obtenus lors d’essais de DBS ont été soigneusement comparés avec les données anamnestiques des participants à l’étude concernant le statut VHB et VHC auto-déclarés. Cette comparaison en conjonction avec les résultats des tests couplé paires de sérum/DBS a conduit à des modifications mineures de l’algorithme de test pour la phase principale de l’étude « DRUCK » qui va s’inscrire des toxicomanes actifs dans six autres grandes villes allemandes : « Individuals infectés par le VIH est toujours testé pour la présence d’ADN du VHB. Participants dont éluats DBS sont positifs pour les anticorps anti-HBc ou anti-HBs doivent être soumis à une ponction veineuse au cours d’une deuxième consultation pour clarifier définitivement leur statut d’anticorps anti-HBc/anti-HBs et, enfin, tous les éluats DBS seront projetés pour l’ARN du VHC Quelles que soient les résultats des tests d’anticorps anti-VHC. » 17
| Paramètres | Couplé sérums/DBS éluats (N) | Résultats discordants (N) | Raison des différences entre les tests sériques et les éluats DBS |
| VHB | |||
| AgHBs | 299 | 2 | Deux patients avec une infection chronique par le VHB. Ils étaient sous traitement antiviral et un d'entre eux était co-infectés par le VIH. Concentrations d’antigène HBs dans le sérum : 749 UI/ml et 6 UI/ml, respectivement. |
| Anticorps anti-HBc | 305 | 28 | Dans le sérum, vingt-deux patients avaient une infection par le VHB résolu. Six individus ont montré le résultat sérologique « anti-HBc seul ». Vingt-deux des patients ont été co-infectées par le VIH. Des « résolveurs VHB », vingt ans ont été évalués comme « Anti-HBs positif seul » en testant DBS et, par conséquent, étaient faussement classées comme « condition après la vaccination ». |
| Anticorps anti-HBs | 310 | 9 | Les quatre patients ne pas co-infectés par le VIH avaient sériques d’anticorps anti-HBs de ‑ 11 26 UI/l, qui étaient trop faibles pour permettre une détection des anticorps après élution des taches de sang séché. |
| ADN DU VHB | 150 | 7 | Les sérums respectifs ont été obtenus de sept patients avec des concentrations d’ADN-VHB sérique allant de 409 UI/ml à 3 643 UI/ml. |
| VHC | |||
| Anticorps anti-VHC | 339 | 4 | Ces quatre sérums ont été prises chez les patients, avec de longues depuis résolu par le VHC. |
| ARN DU VHC | 150 | 0 | – |
| VIH | |||
| VIH 1-p24/anti-VIH 1/2 | 209 | 0 | – |
Tableau 1 : Résultats obtenus à partir de 1 762 DBS, qui ont été préparés et transformés à base de qui suit le sang veineux tout le protocole proposé dans la présente communication, comparativement aux résultats dans des échantillons de sérum couplés comme référence.
Discussion
DBS ont été utilisés pour 100 ans2 mais, étonnamment, il n’y a encore aucun consensus sur leur préparation et le traitement. A ce jour, une normalisation suffisante de cette importante phase pré-analytique a seulement obtenue dans le domaine du dépistage néonatal14, une variété de différents protocoles existe pour toutes les autres applications de DBS test5, 16, 23. Pour surmonter cette hétérogénéité remarquable, un enseignement complet étape par étape pour préparer et traiter les DBS devant être utilisée dans les immunoessais et par des techniques moléculaires est présentée dans la présente communication et évaluée en ce qui concerne son efficacité pour la détection des marqueurs des infections à VHB, VHC et VIH. La mise au point de la discussion qui suit est principalement mis sur les différentes étapes du protocole suggéré.
Dans l’histoire de DBS essais nombreux papier-filtre différentes cartes ont été utilisées2 mais aujourd'hui seulement deux sources commerciales sont approuvés par la FDA comme dispositifs médicaux de classe II pour blood collection5, 16. Ces systèmes de carte de filtre sont très uniformes et ont des caractéristiques d’absorption très similaires afin que les résultats d’analyse obtenus à partir de sang capillaire préparé sur un d’eux ne diffèrent pas de plus de 4 % à 5 %,28. Il n’est pas surprenant, Masciotra et ses collègues29 détecté donc ARN du VIH-1 aussi bien avec un essai qualitatif après élution de cartes de collection de sang provenant de différentes sources. Compte tenu de ces données, il peut être pratiquement exclu que tout les écarts observés lors du test couplé paires de sérum/DBS pour marqueurs du VHB, VHC et VIH infection17 a été causée par le choix de la carte filtre seul. Toutefois, lorsqu’une quantification précise d’un analyte est indispensable, variation de la source à l’autre peut-être ne plus être négligeable et des techniques plus sophistiquées, par exemple, perforé DBS (PDB) comme méthode de Microprélèvement30 ou la préparation des taches de sérum séché (DSS)31 peut devraient s’appliquer au lieu de DBS classiques tests10.
Étant donné que de petites quantités de sang sont utilisées pour les essais de DBS (une goutte de sang capillaire se compose d’environ 50 µl)5, 16, variations dans le volume de l’échantillon sont essentiels et, certes, au moins une partie de l’écart entre les résultats sérologiques et du participant autodéclaré statut VHB et VHC enregistré pendant le pilotage de l’étude « DRUCK » sont imputables à cette variable. Le facteur le plus important pour réduire les « fluctuations » volume de l’échantillon est sans aucun doute une bonne technique de prélèvement sanguin capillaire, qui ne peut être atteint par une formation attentive et continue du personnel technique22. En outre, en tant que mesure de contrôle de la qualité, tous les laboratoires qui travaillent avec SRD devraient ont déjà lancé des procédures d’identification et par la suite, à l’exclusion des spécimens DBS qui doivent être considérées comme insatisfaisantes ou invalide16.
Des études menées principalement dans le contexte du VIH32 et dépistage néonatal33 ont montré que le taux d’humidité élevé peut conduire à une dégradation des analytes, mais jusqu’ici aucun consensus ne s’est dégagé au sujet de la question de combien de temps les DBS doit être séché à l’air . Un intervalle d’au moins 4 heures ou de préférence O/N est proposé dans la présente communication, qui a donc adopté des conditions qui ont servi dans la grande majorité de toutes les publications pertinentes32, 34 données sur le stockage de DBS à servir par la suite pour le VHB et le VHC test sont contradictoires. En 1981, Villa et ses collègues35, qui ont appliqué les techniques d’analyse contemporaines, a signalé que stockage à RT n’a pas affecté les résultats des analyses de VHB pendant la période d’observation complète de 180 jours si les titres d’anticorps étaient > 1/1 000, mais cette DBS est devenu borderline-positif ou négatif même après 15 jours, quand les titres dans le sérum sont seulement de 1/100. Stockage à-20 ° C ou 4 ° C n’a pas entraîné une amélioration substantielle. En revanche, une étude réalisée trente ans plus tard36 testé réplique d’un échantillon de VHB positifs, et les auteurs ont constaté qu’anti-HBc ainsi que les anticorps anti-HBs étaient stables jusqu'à 183 jours à ta, tandis qu’AgHBs dans les mêmes conditions est devenu faux-négatifs déjà après 63 jours. En ce qui concerne la détection de l’ADN du VHB d’éluats DBS, la concentration de l’acide nucléique viral a été stable pendant au moins sept jours à 37 ° C37 ou s’est avéré « résistants » au stockage à ta jusqu'à trois semaines38. Dépistage des anticorps anti-VHC à l’aide de deux disponible dans le commerce de troisième génération immunoessais39 a fourni des résultats précis pendant 117 jours en utilisant des échantillons DBS conservés à-20 ° C, 2 et 8 ° C et 20 – 25 ° C, respectivement. Stockage à-20 ° C, cependant, a entraîné la plus faible variation des densités optiques. Appliquer un anti-VHC de quatrième génération ELISA, c.-à-d. Monolisa HCV-Ag-Ab-ULTRA, dans le contexte de DBS, essais, Larrat et al. 40 a observé une diminution forte spécificité analytique après avoir mémorisé les spécimens DBS pendant plus de trois jours à température ambiante. En revanche, les résultats des tests précis ont été obtenus avec le même kit utilisant les échantillons déposés pendant 60 jours dans des conditions différentes (-20 ° C, 2 et 8 ° C et 22 à 26 ° C) par Brandao et collègues de travail41. Observations sur la baisse des concentrations de l’ARN du VHC dans DBS dans diverses conditions de stockage comprise entre aucune modification notable à RT pour jusqu'à un an42 et un changement décuplée après quatre semaines à température ambiante43. Prenant ces données plutôt contradictoires sur la stabilité du VHB et VHC antigènes, acides nucléiques et des anticorps en considération, il semblait raisonnable de se rétracter dans le projet de protocole à un consensus, ce qui a été défini précédemment pour le stockage des spécimens DBS à utiliser pour Dépistage de15, 30: pour les dépôts à court terme (jusqu'à deux semaines) anticorps, antigènes et l’acide nucléique viral sont considérés comme stables à RT, alors que des conditions de gel ideale pour des périodes plus longues.
Trois paramètres en règle générale, sont à considérer lors de la conception d’un protocole d’élution : (1) la mémoire tampon d’élution. (2) la durée et la température d’élution ; et (3) l’élution tome23. Dans la grande majorité de toutes les publications pertinentes solution saline tamponnée au phosphate (PBS) servait à élution de DBS, et la plupart des auteurs a ajouté une protéine, par exemple, l’albumine sérique bovine (BSA) ou Tween 20, un agent tensio-actif, afin d’améliorer le signal de test en stabilisant protéines, car ils vont dans la solution et en même temps blocage non-spécifiques sites23. Seuls quelques rapports qui comparer directement les tampons d’élution différents dans le cadre des essais de DBS, sont disponibles. Villar et al. capacités d’élution presque équivalent à tous les tampons utilisés, mais PBS/BSA a enregistré 36, par exemple, 0,5 % ont abouti à la plus faible de réactivité non spécifique. Une observation très similaire a été faite par Croom et ses collègues44 lorsque vous appliquez le diluant de l’échantillon de la Genetics Systems rLAV EIE pour l’élution des anticorps anti-VHC de DBS. Étant donné que le risque de dégradation de l’échantillon est extrêmement faible dans les premières heures après la préparation de DBS (voir ci-dessus), il a été décidé à incuber les taches O/N à la température ambiante et à soutenir le processus d’élution en mélangeant la fin plus douce. Cette approche a l’avantage de spécimens poinçonnés de la précédente journée peut être directement transférée au diagnostic de routine au début du prochain matin23. Il convient d’adapter le volume de la mémoire tampon d’élution minimal part aux exigences des essais utilisés pour les analyses suivantes afin de conserver le facteur de dilution aussi bas que possible. Toutefois, une optimisation minutieuse des conditions d’élution pour chaque analyte unique n’était pas possible dans l’évaluation précédente parce qu’un débit élevé échantillon devait être garanti en relativement peu de temps au cours de l' « Étude de DRUCK »17. Par conséquent, le volume plutôt défavorable de 1 000 µl de tampon PBS a été utilisé afin de compléter le processus entier d’élution pour tous les paramètres dans deux opérations distinctes.
Cette approche une part échoue « complètement dans le système anti-HBc/anti-HBs pour les personnes infectées par le VIH en raison de la concentration d’anticorps faible ; ... et il nécessaire procédures biologiques moléculaires avec une sensibilité analytique optimale en ce qui concerne l’ADN du VHB et l’ARN du VHC teste. » 17 en revanche, le volume d’élution élevé avéré pour être en aucune manière désavantageuse pour le dosage de l’antigène HBs, anticorps anti-VHC et anti-VIH par les kits utilisés tout au long de l’évaluation. « La détection de l’AgHBs positifs issus de sang total éluats a réussi avec une sensibilité de 98,6 %, à un degré élevé de même que dans les études précédentes, qui avait utilisé en partie d’un plus petit volume d’élution de 100 µl, 250 µl, 600 µl ou 500 µl »17 ,36, 45, 46. La sensibilité de 97,8 % constatés lors de l’enquête de 179 paires de sérum/DBS pour anticorps anti-VHC correspondaient aux résultats d’un existant rapporte24, 44, 47, 48, 49, qui avait travaillé avec un volume d’élution qui était inférieur d’un facteur de 5 à 10. « En outre, les protocoles pour la détection des anticorps anti-VHC avaient été convenablement optimisés... en précisant leurs propres points de coupure »,17, 24, 48, 49 « ou en augmentant les volumes d’échantillon de 20 µl à 100 µl. » 17, 49 Enfin, la spécificité analytique et la sensibilité (100 %) mis en place pour la détection des anti-VIH étaient égaux ou supérieurs à d’autres immuno-essais spécifiquement adaptés aux DBS essai50, 51 , les caractéristiques de performances « ou un pas à pas procédure avec l’utilisation combinée de plusieurs tests anti-VIH »17,52. « Ils ont, en effet, d’aussi dépassaient le record de performance d’un test qui a été spécialement développé et optimisé pour la détection des anticorps anti-VIH dans les éluats DBS (Q-Prevent HIV 1 + 2 kit de DBS). » 17, 53
Pris ensemble, le protocole étape par étape complète présenté dans la présente communication s’est avéré pour être un outil faisable et facile à utiliser pour la préparation et le traitement DBS et peut, ainsi, être utilisé avec fiabilité en virologie diagnostique. Il permet des approches utilisant automation 54 et en raison de ses caractéristiques excellentes performances a le potentiel pour servir en guise de première pierre pour un protocole futur consensus généralement reconnus dans le champ global de DBS, essais en laboratoire médecine.
Déclarations de divulgation
Dans le passé, la RSR a reçu d’honoraires permettant de présenter des conférences et un soutien financier pour son travail scientifique d’Abbott Diagnostics. NG et OM déclarent qu’ils n’ont pas d’intérêts contradictoires.
Remerciements
Cette communication est basée sur les résultats précédemment publiés dans Virology Journal17 en mode libre accès aux termes de la licence Creative Commons (http://creativecommons.org/licenses/by/2.0) avec BioMed Central comme un titulaire de licence. Les auteurs a remercient la collaboration fructueuse dans le cadre du pilotage de l’étude « Médicaments et maladies infectieuses chroniques » (« DRUCK Study »), avec U. Marcus, Cai W., W. Zhang et R. Zimmermann du Robert Koch Institute (Berlin, Allemagne) et sommes reconnaissants à S. Moyrer pour la photographier assemblés dans la Figure 1 , ainsi que D. F. Whybrew, Ph.d., (Göttingen, Allemagne) pour corriger le manuscrit. Ils expriment aussi leur gratitude pour l’assistance technique habile à J. Ackermann, E. Bayrambasi, U. Büttner, S. Dziubek, I. Jakobsche, B. Krellenberg, H. Krohn, P. Kusimski, A. Metcalf, J. Piejek, S. Saar, M. Schröter et K. Seidel. Cette étude a été financée en partie par une subvention du ministère allemand de la santé au Centre National de référence pour l’hépatite c.
matériels
| Name | Company | Catalog Number | Comments |
| Latex rubber gloves | Hartmann | #4049500041515 | |
| 70% isopropyl alcohol | Bode Chemie | #9768050 | |
| Mulifly safety cannula | Sarstedt | #85.1638 | |
| EDTA blood collection tube | Sarstedt | #02.1066.001 | |
| Adhesive bandage | Hartmann | #2994163 | |
| Dry gauze pad | Hartmann | #143213 | |
| Singel-use safety lancet | Owen Mumford | #3802421 | |
| Filter paper card | Whatman/sigmaaldrich | #10534612 | Filter paper card Grade 903 |
| Disposable pipette tips | Starlab | #S1126-7810, #S1120-8810 | |
| Zipper bag | Flexico | #20219 | |
| Mini desiccant bag | Tropack | #- | |
| Disposable Punch | pfmmedical | #48601 | 6.0 mm Disposable Biopsy Punch |
| Disposable Forceps | Servoprax | #H7301 | |
| 12 Well Cell Culture Plate | Greiner | #665180 | |
| PBS Buffer | Gibco | #14190-136 | |
| Tween 20 | Applichem | #A1389.0500 | |
| Sodium Azide | Merck | #66880250 | |
| Safe-Lock Tubes, 1.5 ml | Eppendorf | #30120086 | |
| ARCHITECT HBsAg (Quantitative) | Abbott | #6C3642 | |
| ARCHITECT anti-HBc II | Abbott | #8L4425 | |
| ARCHITECT anti-HBs | Abbott | #7C1825 | |
| ARCHITECT anti-HCV | Abbott | #6C3725 | |
| ARCHITECT HIV Ag/Ab Combo | Abbott | #4J2727 | |
| MagNA Pure 96 DNA and Viral NA Large Volume Kit | Roche | #6374891001 | |
| artus HBV LC PCR Kit | Qiagen | #4506063 (24 tests), #4506065 (96 tests) | |
| VERSANT HCV TMA Assay IVD | Siemens Healthcare | #2554311 |
Références
- Schmidt, V. Ivar Christian Bang (1869 - 1918), founder of modern clinical microchemistry. Clin Chem. 32 (1), 213-215 (1986).
- Hannon, W. H., Therell, B. L., Li, W., Lee, M. S. Overview of the history and applications of dried blood spot samples. Dried blood spots. Applications and techniques. 3, 3-15 (2014).
- Bang, I., Bergmann, J. F. . Der Blutzucker. , (1913).
- Chapman, O. D. The complement-fixation test for syphilis. Use of patient's whole blood dried on filter paper. Arch Derm Syphilol. 9 (5), 607-611 (1924).
- Smit, P. W., Elliott, I., Peeling, R. W., Mabey, D., Newton, P. N. An overview of the clinical use of filter paper in the diagnosis of tropical diseases. Am J Trop Med Hyg. 90 (2), 195-210 (2014).
- Kuehn, B. M. After 50 years, newborn screening continues to yield public health gains. JAMA. 309 (12), 1215-1217 (2013).
- Guthrie, R. Blood Screening for Phenylketonuria. JAMA. 178 (8), 863 (1961).
- Guthrie, R., Susi, A. A simple phenylalanine method for detecting phenylketonuria in large populations of newborn infants. Pediatrics. 32 (3), 338-343 (1963).
- Snijdewind, I. J., van Kampen, J. J., Fraaij, P. L., vander Ende, M. E., Osterhaus, A. D., Gruters, R. A. Current and future applications of dried blood spots in viral disease management. Antiviral Res. 93 (3), 309-321 (2012).
- Demirev, P. A. Dried blood spots: analysis and applications. Anal Chem. 85 (2), 779-789 (2013).
- Li, W., Lee, M. S., Li, W., Lee, M. S. Preface. Dried blood spots. Applications and techniques. , VIII-IX (2014).
- Guder, W. G., Narayanan, S., Wisser, H., Zawta, B. . Diagnostic Samples: From the Patient to the Laboratory. The Impact of Preanalytical Variables on the Quality of Laboratory Results. , (2009).
- Mei, J. V., Alexander, J. R., Adam, B. W., Hannon, W. H. Use of filter paper for the collection and analysis of human whole blood specimens. J Nutr. 131 (5), 1632S-1636S (2001).
- Mei, J., Lee, M. S., Li, W., Lee, M. S. Dried blood spots sample collection, storage, and transportation. Dried blood spots. Applications and techniques. , 21-31 (2014).
- Ross, R. S., et al. Detection of infections with hepatitis B virus, hepatitis C virus, and human immunodeficiency virus by analyses of dried blood spots. Performance characteristics of the ARCHITECT system and two commercial assays for nucleic acid amplification. Virol J. 10 (72), (2013).
- Zimmermann, R. DRUCK-Studie – Drogen und chronische Infektionskrankheiten in Deutschland. Ergebnisse der Pilotierung eines Sero- und Verhaltenssurveys bei i. v. Drogengebrauchern. Epidemiol Bull. 33, 335-339 (2012).
- . World Medical Association, Declaration of Helsinki. Ethical principles for medical research involving human subjects. JAMA. 310 (20), 2191-2194 (2013).
- Young, D. S., Bermes, E. W., Burtis, C. A., Ashwood, E. R., et al. Specimen collection and processing; sources of biological variation. Tietz textbook of clinical chemistry. 58, 58-101 (1994).
- McDade, T. W. Development and validation of assay protocols for use with dried blood spot samples. Am J Hum Biol. 26 (1), 1-9 (2014).
- Judd, A., et al. Evaluation of a modified commercial assay in detecting antibody to hepatitis C virus in oral fluids and dried blood spots. J Med Virol. 71 (1), 49-55 (2003).
- Zweig, M. H., Campbell, G. Receiver-operating characteristic (ROC) plots: A fundamental evaluation tool in clinical medicine. Clin Chem. 39 (4), 561-577 (1993).
- Greiner, M., Pfeiffer, D., Smith, R. D. Principles and practical application of the receiver-operating characteristic analysis for diagnostic tests. Prev Vet Med. 45 (1-2), 23-24 (2000).
- Clopper, C. J., Pearson, E. S. The use of confidence or fiducial limits illustrated in the case of the binominal. Biometrika. 26 (4), 404-413 (1934).
- Mei, J. V., Zobel, S. D., Hall, E. M., De Jesús, V. R., Adam, B. W., Hannon, W. H. Performance properties of filter paper devices for whole blood collection. Bioanalysis. 2 (8), 1403-1410 (2010).
- Masciotra, S., et al. Evaluation of blood collection filter papers for HIV-1 DNA PCR. J Clin Virol. 55 (2), 101-106 (2012).
- Li, F., Zulkoski, J., Fast, D., Michael, S. Perforated dried blood spots: a novel format for accurate microsampling. Bioanalysis. 3 (20), 2321-2333 (2011).
- Li, Y., Henion, J., Abbott, R., Wang, P. The use of a membrane filtration device to form dried plasma spots for the quantitative determination of guanfacine in whole blood. Rapid Commun Mass Spectrom. 26 (10), 1208-1212 (2012).
- Basavaraju, S. V., Pitman, J. P., Li, W., Lee, M. S. Dried blood spots for use in HIV-related epidemiological studies in resource-limited settings. Dried blood spots. Applications and techniques. , 76-94 (2014).
- Chace, D. H., Spitzer, A. R., De Jesus, V. R., Li, W., Lee, M. S. Applications of dried blood spots in newborn and metabolic screening. Dried blood spots for use in HIV-related epidemiological studies in resource-limited settings. Dried blood spots. Applications and techniques. 3, 53-75 (2014).
- Gakhar, H., Holodniy, M., Li, W., Lee, M. S. Use of dried blood spot samples in HCV-, HBV-, and influenza-related epidemiological studies. Dried blood spots. Applications and techniques. 3, 95-113 (2014).
- Villa, E., Cartolari, R., Bellentani, S., Rivasi, P., Casolo, G., Manenti, F. Hepatitis B virus markers on dried blood spots. A new tool for epidemiological research. J Clin Pathol. 34 (7), 809-812 (1981).
- Villar, L. M., de Oliveira, J. C., Cruz, H. M., Yoshida, C. F. T., Lampe, E., Lewis-Ximenez, L. L. Assessment of dried blood spot samples as a simple method for detection of hepatitis B virus markers. J Med Virol. 83 (9), 1529-1510 (2011).
- Lira, R., et al. Use of dried blood samples for monitoring hepatitis B virus infection. Virol J. 6 (1), 153 (2009).
- Jardi, R., et al. Usefulness of dried blood samples for quantification and molecular characterization of HBV-DNA. Hepatology. 40 (1), 133-139 (2004).
- Marques, B. L., et al. Dried blood spot samples: optimization of commercial EIAs for hepatitis C antibody detection and stability under different storage conditions. J Med Virol. 84 (10), 1600-1607 (2012).
- Larrat, S., et al. Performance of an antigen–antibody combined assay for hepatitis C virus testing without venipuncture. J Clin Virol. 55 (3), 220-225 (2012).
- Brandao, C. P., et al. Simultaneous detection of hepatitis C virus antigen and antibodies in dried blood spots. J Clin Virol. 57 (2), 98-102 (2013).
- Bennett, S., et al. Detection of hepatitis C virus RNA in dried blood spots. J Clin Virol. 54 (2), 106-109 (2012).
- Abe, K., Konomi, N. Hepatitis C virus RNA in dried serum spotted onto filter paper is stable at room temperature. J Clin Microbiol. 36 (10), 3070-3072 (1998).
- Croom, H. A., et al. Commercial enzyme immunoassay adapted for the detection of antibodies to hepatitis C virus in dried blood spots. J Clin Virol. 36 (1), 68-71 (2006).
- Mendy, M., et al. Hepatitis B surface antigenaemia and alpha-foetoprotein detection from dried blood spots: applications to field-based studies and to clinical care in hepatitis B virus endemic areas. J Viral Hepat. 12 (6), 642-647 (2005).
- Komas, N. P., Baï-Sepou, S., Manirakiza, A., Léal, J., Béré, A., Le Faou, A. The prevalence of hepatitis B virus markers in a cohort of students in Bangui, Central African Republic. BMC Infect Dis. 10, 226 (2010).
- Parker, S. P., Cubitt, W. D., Ades, A. E. A method for the detection and confirmation of antibodies to hepatitis C virus in dried blood spots. J Virol Methods. 68 (2), 199-205 (1997).
- McCarron, B., et al. Hepatitis C antibody detection in dried blood spots. J Viral Hepat. 6 (6), 453-456 (1999).
- Tuaillon, E., et al. Dried blood spot for hepatitis C virus serology and molecular testing. Hepatolog. 51 (3), 752-758 (2010).
- Solomon, S. S., et al. Dried blood spots (DBS): a valuable tool for HIV surveillance in developing/tropical countries. Int J STD AIDS. 13 (1), 25-28 (2002).
- Lakshmi, V., Sudha, T., Bhanurekha, M., Dandona, L. Evaluation of the Murex HIV Ag/Ab Combination assay when used with dried blood spots. Clin Microbiol Infect. 13 (11), 1136-1110 (2007).
- Sarge-Njie, R., et al. Evaluation of the dried blood spot filter paper technology and five testing strategies of HIV-1 and HIV-2 infections in West Africa. Scand J Infect Dis. 38 (11-12), 1050-1056 (2006).
- de Castro, A. C., Borges, L. G. d. o. s. A., de Souza, R. d. a. S., Grudzinski, M., D’Azevedo, P. A. Evaluation of the human immunodeficiency virus type 1 and 2 antibodies detection in dried whole blood spots (DBS) samples. Rev Inst Med Trop Sao Paulo. 50 (3), 151-156 (2006).
- Fan, L., Wan, K., Kavetskaia, O., Wu, H., Li, W., Lee, M. S. Automation in dried blood spot sample collection, processing, and analysis for quantitative bioanalysis in pharmaceutical industry. Dried blood spots. Applications and techniques. , 229-234 (2014).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon