Réaction de couplage catalysé au palladium
Vue d'ensemble
Source : Vy M. Dong et Faben Cruz, Department of Chemistry, University of California, Irvine, CA
Cette expérience démontrera le concept d’un couplage croisé catalysée par du palladium. La mise en place d’une réaction typique de couplage croisé catalysée par Pd sera illustrée. Les réactions de couplage croisé catalysée par le PD ont eu un effet profond sur les chimistes synthétiques comment créer des molécules. Ces réactions ont permis aux chimistes construire des liens de façons nouvelles et plus efficaces. Ces réactions ont trouvé de nombreuses utilisations dans l’industrie chimique et pharmaceutique fine. Les réactions de couplage croisé catalysée par le PD s’ajoute un autre outil de boîte à outils de la pharmacie pour construire des liaisons carbone-carbone, qui sont au cœur de la chimie organique. La combinaison de l’importance de faire des liaisons carbone-carbone et l’impact de couplage croisé catalysée par le Pd ont entraîné ces réactions faisant l’objet du prix Nobel de chimie 2010. Ei-ichi Negishi, un des lauréats du prix Nobel 2010 en chimie, a expliqué dans sa conférence Nobel que l’un de ses motivations pour développer cette chimie était de développer « largement simple Lego comme méthodes applicables pour accrocher deux différentes groupes organiques ».
Principles
Les réactions de couplage croisé catalysée par le PD se composent d’un électrophile (généralement un organohalogénure), un nucléophile (typiquement un composé organométallique ou un alcène) et un catalyseur au palladium. Indépendamment de l’électrophile ou nucléophile utilisé, tous les accouplements croisés catalysée par Pd s’appuient sur le Pd-catalyseur d’activer et de combiner les deux partenaires. De manière générale, une espèce de Pd(0) réagit avec l’organohalogénure via une addition oxydante pour former une espèce d’organopalladium (RPdX). Cette espèce d’organopalladium réagit alors avec le partenaire nucléophile pour générer une nouvelle espèce d’organopalladium et finalement de construire une nouvelle liaison carbone-carbone. En fonction de la partenaire nucléophile, le couplage croisé catalysé par le Pd est donné un nom spécifique (voir tableau 1 ci-dessous).
| Nucléophile | Nom de la réaction |
| Organoboré | Suzuki |
| Organostannane | Stille |
| Organozincique | Negishi |
| Organomagnésiens (réactif de Grignard) | Kumada |
| ORGANOSILANE | Hiyama |
| Oléfine/alcène | Estacade à claire-voie |
| Alcyne | Sonogashira |
Tableau 1 : Liste des noms de réaction de couplage croisé catalysée par le Pd et leurs partenaires nucléophiles.
Il y a deux mécanismes généraux associés à ces Pd-catalyseur croisent accouplements. Un pour la réaction de Heck et un pour l’autre croisent des réactions de couplage. Dans l’ensemble, la réaction de Heck est couplé un alcène à un organohalogénure pour générer une oléfine maintenant plus substituée (Figure 1). La première étape d’une réaction de Heck est la même chose que tous les autres raccords croisés catalysée par le Pd. Pour commencer, l’addition oxydante se produit entre le parti démocrate (0)-catalyseur et l’organohalogénure pour générer une espèce de organopalladium(II). Ensuite, les coordonnées d’oléfines à cette nouvellement forment organopalladium(II) espèces. Après coordination oléfine, carbopalladation se produit afin de générer une nouvelle liaison carbone-carbone et carbone-palladium. Ensuite, les bêta-hydrure élimination se produit afin de générer un Pd (II)-espèces hydrure et le produit de l’oléfine. Enfin, une élimination réductrice de HX régénère le parti démocrate (0)-catalyseur, qui peut continuer de couplage avec une autre molécule d’organohalogénure et d’oléfine.
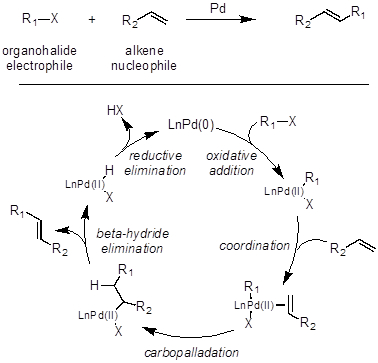
Figure 1 : La réaction de Heck est couplé un alcène à un organohalogénure pour générer une oléfine maintenant plus substituée.
Pour le reste des réactions de couplage, le mécanisme est le suivant (Figure 2). Addition oxydante entre l’organohalogénure et Pd(0) catalyseur entraîne la formation d’une espèce de organopalladium(II). Cette espèce de organopalladium(II) réagit avec les composés organométalliques nucléophile dans une étape appelée transmétallation pour générer une espèce de organopalladium(II) avec deux liaisons carbone-palladium. Enfin, une élimination réductrice se produit pour créer une nouvelle liaison carbone-carbone et régénérer le catalyseur de Pd(0).
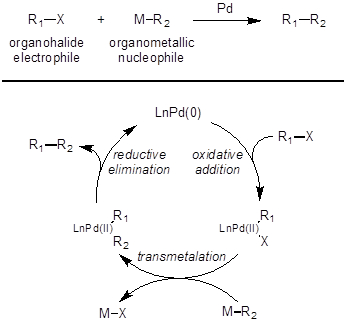
Figure 2 : Mécanisme pour les réactions de couplage croisé de restants.
Procédure
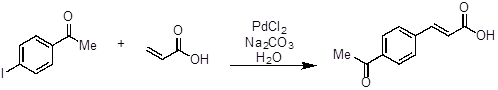
- Ajoutez 4-iodoacetophenone (246 mg, 1 équivalent, 1 mmol), acide acrylique (100 μL, 1,5 équivalent, 1,5 mmol), carbonate de sodium (Na2CO3, 318 mg, 3 équivalents, 3 mmol), PdCl2 (2 mg, équivalents de 0,01 0,01 mmol) et eau (5 mL, 0,2 M) à une ballon à fond rond (~ 20 mL) équipé d’un bar d’agitation magnétique.
- La chaleur de la réaction à environ 100 ° C et mélanger jusqu'à consommation complète de 4-iodoacetophenone (1 h environ).
- La réaction peut être surveillée par TLC.
- Refroidir le mélange réactionnel à la température ambiante après achèvement.
- Acidifier le mélange réactionnel avec 1 M de HCl aqueux à ~ pH de 1.
- Le pH du mélange réactionnel peut être vérifié avec le papier de tournesol.
- Un solide devrait précipiter.
- Recueillir le solide par filtration.
- Purifier la matière brute par recristallisation en utilisant un mélange 1:1 de méthanol et d’eau.
Résultats
Le produit devrait être un solide avec le spectre de RMN H suivi 1: 1H RMN (400 MHz, DMSO-d6) : δ (ppm) 2.60 (s, 3 H), 6,67 (d, J = 16,0 Hz, 1 H), 7,65 (d, J = 16,0 Hz, 1 H). 7.83 (d, J = 8,4 Hz, 2H). 7.97 (d, J = 8,4 Hz, 2H).
Applications et Résumé
Ces réactions de couplage croisé catalysée par le Pd ont changé la façon dont les molécules sont synthétisées dans les milieux académiques et industriels. L’impact de cette technologie peut être vu dans Comment chimistes construisent des structures complexes pour produits pharmaceutiques, produits chimiques agricoles et des matières. Au-delà des accouplements croisés catalysée par le Pd, catalyse de métaux de transition a changé (et continue à changer) la voie synthétiques chimistes préparent des molécules qui peut avoir un impact sur la société par le biais de leur usage thérapeutique potentielle.
Beaucoup de molécules d’intérêt pour le traitement des maladies ont des liens reliant les anneaux de constituant aromatique ou hétéro-aromatique. Palladium de croix, comme la réaction de Suzuki, les réactions de couplage ont trouvé usage répandu dans l’industrie pharmaceutique pour la fabrication de ces types de structures. Par exemple, Crizotinib (Xalkori), un médicament contre le cancer pour le traitement du carcinome du poumon non à petites cellules est synthétisé sur une échelle de plusieurs kilo à l’aide d’une Suzuki de couplage.
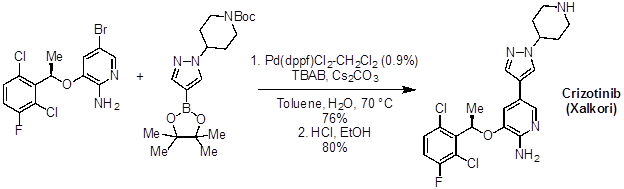
Figure 3 : Crizotinib (Xalkori), un médicament contre le cancer.
Palladium croisés accouplements ont également été appliqués vers la synthèse du Taxol (un médicament anticancéreux), Varenicline (un médicament contre le tabagisme) et précurseurs pour les résines électronique haute performance.
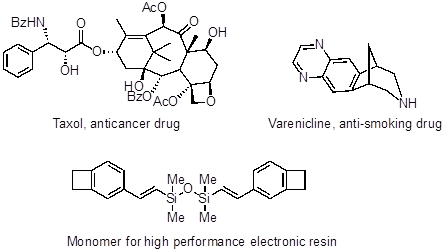
Figure 4 : Taxol (un médicament anticancéreux), Varenicline (un médicament contre le tabagisme) et précurseurs pour les résines électronique haute performance.
Passer à...
Vidéos de cette collection:

Now Playing
Réaction de couplage catalysé au palladium
Organic Chemistry II
34.4K Vues

Nettoyage de la verrerie
Organic Chemistry II
123.5K Vues

Substitution nucléophile
Organic Chemistry II
99.5K Vues

Agents reducteurs
Organic Chemistry II
43.1K Vues

Réaction de Grignard
Organic Chemistry II
149.1K Vues

Titrage du n-butyllithium
Organic Chemistry II
47.8K Vues

Appareil de Dean-Stark
Organic Chemistry II
100.3K Vues

Ozonolyse des alcènes
Organic Chemistry II
67.0K Vues

Organocatalyse
Organic Chemistry II
16.7K Vues

Synthèse en phase solide
Organic Chemistry II
41.0K Vues

Hydrogénation
Organic Chemistry II
49.6K Vues

Polymérisation
Organic Chemistry II
94.0K Vues

Point de fusion
Organic Chemistry II
149.9K Vues

Spectroscopie infrarouge
Organic Chemistry II
214.9K Vues

Polarimètre
Organic Chemistry II
99.9K Vues