È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Applicazione e metodologia della tecnica NMR Non distruttivo 19F dominio del tempo per misurare il contenuto in prodotti contenenti fluoro di droga
In questo articolo
Riepilogo
Una tecnica semplice e non distruttivo che misura il contenuto medio di sostanze farmacologiche in prodotti di droga formulati contenenti fluoro utilizzando basso campo fluoro-19 (19F) tempo-dominio (TD) a risonanza magnetica nucleare (NMR) è presentata qui. La tecnica può essere applicata allo sviluppo e alla produzione di farmaci nell'industria farmaceutica.
Abstract
Qui, descriviamo un protocollo sviluppato dal nostro gruppo che utilizza basso campo fluoro-19 (19F) tempo-dominio (TD) a risonanza magnetica nucleare (NMR) per misurare il contenuto medio di farmaci fluorurati nelle loro forme di prodotto formulato droga: compresse o capsule. Questo metodo è specifico di farmaci fluorurati perché rileva solo il contenuto di fluoro, evitando interferenze da eccipienti che la mancanza di fluoro. I vantaggi di misurare il contenuto attivo dei farmaci fluorurati con basso campo 19F TD-NMR contro ad alto campo 19F a stato solido (SS) NMR sono la semplicità del metodo; il basso costo; e la natura distruttiva della tecnica, con tutti i campioni recuperabili in forme intatte (ad es., polveri, compresse e capsule), rendendo questa tecnica alla portata di qualsiasi laboratorio.
Abbiamo testato il metodo con tre prodotti di droga fluorati disponibili sul mercato - cinacalcet, lansoprazolo e ciprofloxacina - con dosi che variano da 15 a 500 mg. I risultati delle analisi, misurate dal basso campo 19F TD-NMR, sostegno i reclami segnalati etichetta per il contenuto medio di droga.
Basato sulla semplicità e riproducibilità dell'analisi, immaginiamo questa metodologia attuata in qualsiasi laboratorio, tra cui impianti di produzione, come uno strumento (PAT) della tecnologia analitica di processo nell'industria farmaceutica.
Introduzione
Nell'industria farmaceutica, il contenuto di sostanze farmacologiche nelle loro forme di unità di dosaggio (ad es., compresse e capsule) deve essere all'interno della gamma sul reclamo dell'etichetta per soddisfare il controllo di qualità e linee guida sulle prestazioni. Cromatografia liquida ad alte prestazioni (HPLC) è la tecnica analitica convenzionale utilizzata per misurare l'uniformità di contenuto delle droghe nelle loro forme formulate. Tuttavia, il metodo è lunga e distruttiva, che richiedono la dissoluzione del farmaco nella sua forma formulato usando i solventi appropriati prima dell'analisi. Anche con l'automazione, il processo può richiedere 1-3 h per campione, a seconda dello sviluppo del metodo analitico appropriato1,2,3. Oltre a HPLC, vicino-infrarosso (NIR) è stato utilizzato per lo stesso scopo e come strumento di PAT, con l'avvertenza di richiedere l'analisi chemiometrica dei dati, rendendo la sua attuazione lunghe e più complesse4. Entrambe le tecniche sono distruttive, con la droga formulata scartata dopo l'analisi.
In questo manoscritto, descriviamo il protocollo passo passo di una metodologia precedentemente pubblicato da nostro gruppo5 per misurare il contenuto medio di farmaci fluorurati nelle loro forme di dosaggio (ad es., compresse e capsule) utilizzando basso campo 19F NMR. Nel corso degli anni, la percentuale di farmaci fluorurati sul mercato approvato dalle agenzie regolatorie in tutto il mondo come prodotti formulati droga è aumentata dal 2% nel 1970 al 25% in 20136. Pertanto, riteniamo che esiste una domanda di sviluppare un metodo più semplice ma più specifico rispetto ai metodi attualmente disponibili per il controllo di qualità del contenuto di gas fluorurati farmaci nelle loro forme formulate.
Farmaci contenenti fluoro-19 (19F) nelle loro strutture hanno il vantaggio di essere facilmente rilevato da 19F NMR dovuto la relativa sensibilità di abbondanza e l'83% del 100% rispetto a protoni7. Misura diretta di 1H. TD-NMR non è utile perché gli eccipienti e API hanno protoni, e il segnale totale protone proviene da tutti i componenti del farmaco, che lo rende poco pratico per misurare il contenuto di API in prodotti di droga utilizzando 1 H TD-NMR. Pertanto, la misurazione del contenuto di droga di fluorurati prodotti di droga utilizzando 19F TD-NMR ha il vantaggio di nessuna interferenza con eccipienti a causa della mancanza di fluoro. Per dimostrare la nostra metodologia di misurazione del contenuto di droga medio di prodotti fluorati droga, abbiamo selezionato tre prodotti di droga in commercio formulati contenenti fluoro in intervalli di dose diversa. Figura 1 illustra le strutture dei farmaci selezionati, dove due di loro - cinacalcet HCl8 e lansoprazolo9-dispone di un gruppo di trifluoromethyl (CF3) nelle loro strutture, con dosi che variano da 15 a 90 mg e il terzo uno - ciprofloxacin HCl monoidrato10 - contiene un atomo di fluoro attaccato un anello aromatico, con una dose di 500 mg.
Qui, dimostriamo la metodologia che abbiamo sviluppato5 per quantificare il contenuto di droga medio dei prodotti di droga fluorurati utilizzando uno strumento di basso campo benchtop TD-NMR (23,4 MHz per 1H e 22,0 MHz per 19F). Abbiamo anche confrontare due pacchetti di software (software di calibrazione RI e Mnova) che possono essere utilizzati per segnalare i risultati.
Protocollo
Attenzione: si prega di consultare tutte le schede di sicurezza pertinenti (MSDS) prima di utilizzare sostanze chimiche. Sostanze farmaceutiche in generale sono tossici e devono essere maneggiati con appropriati dispositivi di protezione individuale (PPE; ad esempio, guanti, occhiali di sicurezza, camice, pantaloni lunghi e scarpe chiuse), con particolare cautela quando si pesano i materiali in polvere. È consigliabile utilizzare un equilibrio collocato in un cappuccio con buon flusso d'aria per ridurre al minimo la polvere da materiali solidi diffondere fuori dalla zona che circonda l'equilibrio.
Nota: le istruzioni del software sono specifiche per la calibratura di RINMR, RI e Mnova. Per altri strumenti fornitore TD-NMR e pacchetti software, le istruzioni variano.
1. preparazione dei campioni prima a 19 F TD-NMR misura
- pesare i campioni per la calibrazione (sostanza medicinale in polvere o ingredienti farmaceutici attivi (API)) nei tubi NMR appropriati (2,5 - 3 - 5-, 10-, 18 e 25 mm OD NMR tubi) fino alla linea di marcatura (altezza della bobina per la sonda di NMR), o circa 30 mm di altezza. Si noti che l'altezza può dipendere la sonda.
Nota: Cinacalcet HCl è un esempio di un'API da utilizzare per la calibrazione per determinare il contenuto del farmaco in compresse commerciale cinacalcet. Il peso dipenderà la densità della polvere. Nel caso di cinacalcet HCl, i pesi dell'API sono intorno a 7.2, 3.5, 1.0, 0.3, 0,1 e 0,07 g quando si riempie l'altezza della bobina per 25 - 18-, 10-, 5-, 3- e tubi NMR 2,5 mm, rispettivamente. - Pesare i campioni di prodotto formulato droga (compresse o capsule) nei tubi NMR appropriati fino alla linea di marcatura (altezza della bobina per la sonda di NMR), o circa 30 mm di altezza, come indicato sopra.
Nota: tubi 25 o 18 mm sono adatti per medie e grandi compresse/capsule o quando abbastanza prodotto formulato droga è disponibile. Per piccole compresse/capsule o quando non abbastanza prodotto formulato farmaco è disponibile, ma il rapporto segnale-rumore può essere ancora sufficiente per la misurazione, utilizzare tubi di 10 mm. Misurare le compresse direttamente, o frantumare se lo si desidera. Nessuna osservazione delle variazioni nelle loro misurazioni sono stati osservati qui, come accennato nella discussione.- Quando preparazione commerciale compresse di cinacalcet, pesano circa quindici 90 mg compresse nel tubo di NMR di 25 mm (circa 9,2 g), cinquanta 30 mg compresse nel tubo di NMR di 25 mm (circa 9,6 g), compresse da 30 mg ventidue nella RMN 18mm tube (circa 4,2 g) e venti-tre compresse da 60 mg il tubo di NMR di 25 mm (circa 8,8 g).
2. Preparazione dello strumento per la misurazione NMR
- Tuning strumento NMR a 19 F
- trasportare tutte le misurazioni alla temperatura del magnete permanente nella RMN strumento. Utilizzare qui, 40 ° C; Nessun controllo della temperatura è disponibile per la sonda di 26 millimetri 19 F NMR usata qui. Tutte le misurazioni relative alla frequenza di 22,0 MHz per 19 F utilizzando lo strumento NMR 23-MHz (per 1 H).
- Mettere il campione standard di Teflon all'interno di un tubo di NMR di 25 o 26 mm e inserire la sonda all'interno del magnete. Consentire di equilibramento per circa 5-10 min e accordare lo strumento a 19 F. Selezionare " Auto O1 " sotto il " comandi " dal menu del software di RINMR. Ripetere la misurazione almeno 3 volte e prendere l'ultimo valore del parametro di 1 O (frequenza di offset).
- Calibrazione dell'impulso 90 gradi F 19
- calibrare l'impulso di 90 gradi per F-19 con il campione di Teflon standard utilizzando la sequenza di taratura automatica standard disponibile nello strumento. Selezionare " P90 Auto " sotto il " comandi " dal menu del software di RINMR.
Nota: Normalmente, l'impulso di 90 gradi non ha bisogno di essere misurato frequentemente a meno che non si esegue lo strumento o la sonda non è stata utilizzata per qualche tempo. Il valore di 90 gradi ottenuto per Teflon con la sonda di 26 millimetri 19 F NMR usata qui era 7,05 µs.
- calibrare l'impulso di 90 gradi per F-19 con il campione di Teflon standard utilizzando la sequenza di taratura automatica standard disponibile nello strumento. Selezionare " P90 Auto " sotto il " comandi " dal menu del software di RINMR.
3. Misurazione del tempo di rilassamento longitudinale o T 1 per campioni di API puro Standard
- per un migliore rapporto segnale-rumore, posizionare il campione di API preparato nel tubo NMR 25 mm all'interno della sonda di F-19 installato nel magnete e lasciarlo equilibrare per almeno 10 min.
- Misurare il tempo di rilassamento T 1, seguendo le istruzioni del manuale dello strumento, per ciascun campione di API utilizzando un esperimento standard per inversione-recupero dal software RINMR.
Nota: I parametri sperimentali raccomandati sono 16 scansioni raccolti con un tempo di sosta di 0,1 µs; punti 8 dati; un impulso di 90 gradi, come accennato in precedenza; e un tempo morto di 10 µs per la sonda di 26 millimetri di F-19. Una matrice di ritardi da 100 µs a 8 s (ad es., 100 µs, 500 µs, 10 ms, 100 ms, ms 300, 700 ms, 1 s, 2 s, 5 s e 8 s) per farmaci con CF 3 e ritardi da 100 µs a 20 s (es. 100 µs, 500 µs, 1 ms, 100 ms, 500 ms, 1 s, 5 s, 10 s, 15 s e 20 s) per farmaci con un gruppo di fluoro attaccato all'anello aromatico sono raccomandati.- In the RINMR software, carico la " invrec.exe " sequenza di impulso selezionando " caricare " sotto " sequenza " e facendo clic su " Open. " per controllare che i parametri di base sono i valori corretti facendo clic " A " o selezionando " Acquisizione " sotto il " parametri " menu.
- Selezionare " script " sotto il " strumenti " menù; una finestra pop-up. Selezionare la " T1.ris " scheda e fare clic sulla freccia verde; una finestra pop-up. Selezionare il file di elenco di ritardo con ritardi appropriati o creare l'elenco dopo aver cliccato " Open. " una volta l'elenco di ritardo è soddisfacente, fare clic su " OK. "
Nota: una finestra verrà visualizzata una richiesta per la creazione di un file per tutti gli spettri che sarà raccolti in al fine di calcolare il valore di T 1. La posizione e i nomi delle cartelle e dei file sono responsabilità dell'utente. - Fare clic su " salvare " per lo strumento avviare l'acquisizione dei dati e salvare automaticamente i file per i ritardi nella cartella selezionata.
Nota: Il software RIMNR creare le curve di rilassamento T 1 e calcolare i tempi di rilassamento T 1 per ogni caso. Una finestra pop-up con la curva di rilassamento T 1 e la costante di tempo o valore T 1 . Qui, il valore di T1 per cinacalcet HCl era 2.4 s.
4. Misure di campioni di calibrazione con Pure API
- misura l'API campioni per costruire la curva di taratura
- posto uno campione di calibrazione nel magnete per una particolare API. Equilibrare i campioni per un minimo di 5 min per i più piccoli tubi e 10 min per i più grandi tubi.
- Acquisire un deperimento libero di induzione (FID) o solido (90 x-90y FID) esperimento con i parametri appropriati seguendo le istruzioni riportate nel manuale dello strumento. Nel software RINMR, caricare il " solid.exe " (o " fid.exe ") sequenza di impulso selezionando " caricare " sotto " sequenza " e facendo clic su ". libera "
Nota: l'esperimento consigliata è solido per materiali solidi che sono Fast-rilassante con breve T 2 s (tempo di rilassamento trasversale). I parametri sperimentali raccomandati sono 128 scansioni raccolti, con un tempo di sosta 0,1 µs, punti 1.024 dati, un impulso di 90 gradi (7,05 µs in questo caso, capanoated utilizzando Teflon) e un tempo morto di 10 µs per la sonda di 26 millimetri 19 F. Un ritardo di riciclo di 7.5 s per farmaci con il gruppo di 3 CF e 20 s per farmaci con il gruppo F collegato ad un aromatico (a causa di tempi di rilassamento T 1) sono stati utilizzati per i casi presentati qui, basato sulla loro T 1 misure. - Misurare tutti i campioni preparati per ogni API dopo che essi sono equilibrati a temperatura del magnete per 5-10 min generare le curve di calibrazione di ogni campione di API. Salvare i dati in una cartella, dando un nome distinto per ogni esecuzione sperimentale.
- Calcolare la percentuale in peso dei campioni basati sulla quantità in ogni provetta e considerando la purezza del campione nel più grande tubo API.
5. Campioni di misura del farmaco in compresse
- luogo già preparato formulato campioni di prodotto di droga (compresse o capsule) nel magnete per misurarli uno alla volta. Equilibrare il campione per 5 min per piccoli tubi NMR o per 10 min per i campioni più grandi tubi NMR.
- Acquisire lo stesso NMR esperimento (cioè, solido) con le stesse condizioni per quanto riguarda i campioni calibrati per ogni particolare API.
6. Generazione della curva di calibrazione delle curve con puro esempi di API e aggiungendo i dati da campioni di prodotto di droga come compresse in curve di taratura
- In questi casi, selezionare la regione del solido esperimento da 5 a 300 punti per creare le curve di taratura. I dati possono essere analizzati in tre modi diversi, come descritto di seguito.
- Aprire il software di calibrazione del RI. Richiamare tutti i dati di tinta cliccando sul simbolo del clip per aprire il file FID o i solidi da una particolare API. Per tutti i campioni misurati, immettere le percentuali di peso sotto il “ Conc ” colonna e i pesi sotto la “ massa ” colonna. Selezionare la regione appropriata (5-300 punti) utilizzando il metodo average per costruire la curva di taratura (aprire l'icona di “ dati NMR Display ” per selezionare l'intervallo di punti per il calcolo). Salvare la curva di calibrazione.
Nota: La colonna di Cal fornirà la percentuale di farmaco nei campioni misurati. - In the RI Calibration software con la stessa regione selezionata (5-300 punti), utilizzare il metodo adatto per costruire la curva di taratura. Salvare la curva di calibrazione. Seguire le stesse istruzioni come al punto 4.2.2.
- Aprire il software (per esempio, Mnova). Trascinare tutti i solidi dati da una particolare API e immettere le percentuali di peso dei campioni di riferimento; manuale istruzioni possono essere trovate cliccando “ contenuto ” sotto la “ aiuto ” menu. Nella “ avanzate ” menu, selezionare “ Time Domain ” e poi “ quantificazione; ” una finestra pop-up. Fare clic sul segno più blu per selezionare l'area di integrazione. Integrare la regione appropriata (5-300 punti) utilizzando la modalità di grandezza per costruire la curva di taratura.
- Salvare la curva di calibrazione. Nella tabella, è necessario immettere le percentuali delle droghe per campione solo per gli standard sotto il “ concentrazione (x) ” colonna e i pesi per tutti i campioni sotto la “ massa (m) ” colonna; campioni di calibrazione dovrebbero essere in rosso (controllato). Assicurarsi che il “ funzione di segnale ” è “ y = s/m ” (per normalizzare a massa e del segnale).
- Per misurare la riproducibilità e ripetibilità, ogni campione 3 volte in giorni diversi e costruire la curva di calibrazione in entrambi i pacchetti software. Salvare la calibrazione curva file.
7. Calcolo della droga fluorurati API peso nel prodotto formulato droga utilizzando le curve di calibrazione
- per il calcolo dell'importo peso percentuale e media dosaggio per compressa/capsula di gas fluorurati ad API farmaco nel farmaco formulato prodotto
- uso il file per la curva di taratura dal software di calibrazione del RI e la media metodo. Leggere i dati NMR dal misurato compresse (o capsule) e inserire i pesi per determinare la percentuale in peso di gas fluorurati ad API nel formulato compresse o capsule sulla curva di calibrazione.
Nota: Il “ Cal ” colonna fornirà la percentuale di farmaco nei campioni misurati (calibrazione e commerciale compresse o incognite). Si noti che il parametro O1 deve essere lo stesso per i campioni di calibrazione e le compresse o capsule per il software di calibrazione RI. - Utilizzare il file per la curva di taratura dal software RI calibrazione con il metodo di misura. Leggi i dati NMR dal Tablet (o capsule) misurata e inserire loro pesi per determinare la percentuale in peso di gas fluorurati ad API nel formulato compresse o capsule dalla curva di taratura. Seguire le stesse istruzioni come al punto 5.2.1. Si noti che il parametro di 1 O deve essere lo stesso per i campioni di calibrazione e le compresse o capsule per il software di calibrazione RI.
- Utilizzare il file Mnova e trascinare i dati NMR acquisiti per l'API formulato (o li misura tutto il giorno stesso). Seguire le istruzioni al punto 4.2.4. Inserire i pesi per determinare la percentuale in peso di fluorurati API nel formulato compresse o capsule sulla curva di calibrazione.
Nota: Nella tabella, i campioni di taratura sarà in rosso (controllato) e le compresse/capsule sconosciute o commerciale in blu (non selezionata). Il “ concentrazione (x) ” colonna mostrerà i valori calcolati per le compresse commerciale dei campioni sconosciuti in base ai valori dei campioni di calibrazione in rosso blu. Avviso che il software non richiede l'uso dello stesso parametro per calcolare la percentuale di peso O1. - Calcolare la quantità di droga fluorurati per compressa o capsula come valore medio dall'equazione qui sotto (D = dose di API in mg, W NMR = percentuale in peso di API ottenuta dalla curva di taratura, w = peso totale di formulato prodotto dal peso della droga formulato provenienti da misurata compresse o capsule e N = numero di formulati compresse o capsule utilizzate per la misura) e confrontare con i valori calcolati dal software sulla base del curve di calibrazione:
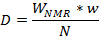
- uso il file per la curva di taratura dal software di calibrazione del RI e la media metodo. Leggere i dati NMR dal misurato compresse (o capsule) e inserire i pesi per determinare la percentuale in peso di gas fluorurati ad API nel formulato compresse o capsule sulla curva di calibrazione.
Risultati
Abbiamo testato basso campo 19F TD-NMR con tre prodotti di droga commerciale (cinacalcet, lansoprazolo e ciprofloxacina) per misurare il contenuto di droga medio dei prodotti fluorurati droga. La figura 1 Mostra le strutture dei farmaci testati, visualizzare le posizioni degli atomi di fluoro.
Abbiamo testato diversi lotti e forme di dosaggio (cioè, 30, 60 e 90 mg) di cinacalcet...
Discussione
Come più fluorurati farmaci stanno diventando disponibili sul mercato, abbiamo sviluppato una metodologia semplice e specifica per misurare il contenuto di droga medio dei prodotti di droga fluorurati utilizzando basso campo 19F TD-NMR5. Abbiamo testato questo metodo su tre prodotti di droga commerciale: compresse contenenti cinacalcet HCl, capsule contenenti lansoprazolo e compresse contenenti ciprofloxacin HCl monoidrato. I vantaggi di questo metodo sono sua specificità a causa dell...
Divulgazioni
Gli autori non hanno nulla a rivelare.
Riconoscimenti
Questo manoscritto è basato su un articolo precedentemente pubblicato5. Ristampato da5, copyright 2015, con il permesso da John Wiley & Sons.
Siamo grati al nostro management, Dr. Janet Cheetham, Dr. Francisco Alvarez, Dr. Arwinder Nagi e Dr. David Semin, per il loro supporto, interesse e incoraggiamento per eseguire questo progetto di ricerca e al Dr. Minhui Ma e Mr. Robert Munger, per averci con Cinacalcet HCl, formulati compresse e informazioni sul farmaco. Vogliamo anche ringraziare il Dr. Michael Bernstein, Dr. Manuel Perez e Dr. Santiago Dominguez per loro sostegno e costruttivi dibattiti sullo sviluppo della versione attualmente commerciale del software Mnova come si applica per la quantificazione dei dati TD-NMR. Inoltre, un ringraziamento speciale a Mr. film L. Marra F.N.P. per averci fornito con cipro generico compresse per condurre i nostri studi.
Materiali
| Name | Company | Catalog Number | Comments |
| MQC-23 | Oxford Instruments | 52-AM4044 | 23.4 MHz for 1H and 22.0 MHz for 19F |
| 26 mm Probe (19F) | Oxford Instruments | 52-AM4061 | 19F NMR probe |
| Cinacalcet HCl | Amgen | Lot 005002 M | Purity 99.8% |
| Cinacalcet commercial tablets | Amgen | Lot 0010021308 | 30 mg tablets |
| Cinacalcet commercial tablets | Amgen | Lot D1026396 | 30 mg tablets |
| Cinacalcet commercial tablets | Amgen | Lot D118714 | 30 mg tablets |
| Cinacalcet commercial tablets | Amgen | Lot D061829 | 60 mg tablets |
| Cinacalcet commercial tablets | Amgen | Lot 00100213 | 90 mg tablets |
| Cinacalcet commercial tablets | Amgen | Lot D064074 | 90 mg tablets |
| Cinacalcet commercial tablets | Amgen | Lot 1026356 | 90 mg tablets |
| Lansoprazole | Fluka | Lot LRAA1897 | Purity 99.7% |
| Brand name Lansoprazole | Novartis | Lot DV1891 | 15 mg capsules |
| Lansoprazole generic | SUPERVALUE INC | Lot 2GE2027 | 15 mg capsules |
| Ciprofloxacin free base | Fluka | Lot BCBM7969V | 99.9% purity |
| Ciprofloxacin HCl monohydrate | Fluka | Lot P500044 | 94% purity as HCl salt |
| Cipro generic | Pack Pharmaceuticals | Lot PUB3033 | 500 mg tablets |
| 25 mm NMR tube | New Era Enterprises | NE-25TD-200-FB | |
| 18 mm NMR tube | New Era Enterprises | NE-18TD-200-FB | |
| 10 mm NMR tube | New Era Enterprises | NE-10TD-200-FB | |
| 5 mm NMR tube | New Era Enterprises | NE-HL5-7 | |
| 3 mm NMR tube | New Era Enterprises | NE-H3-7 | |
| 2.5 mm NMR tube | New Era Enterprises | NE-H5/2.5 |
Riferimenti
- El-Yazigi, A., Wahab, F. A., Afrane, B. Stability Study and Content Uniformity of Prochloroperazine in Pharmaceutical Preparations by Liquid Chromatography. J Chromatogr A. 690, 71-76 (1995).
- Takeuchi, Y., Yoshida, M., Ito, A., Sunada, H. Uniformity of Drug Content During Pharmaceutical Dry Granulation by Roller Compaction and Tableting Processes. J Drug Del Sci Tech. 19 (2), 119-124 (2009).
- Toro, I., Dulsat, J. F., Fábregas, J. L., Claramunt, J. Development and Validation of a Fully Automated method of the Chromatographic Determination of Content Uniformity of Drug Tablets. J Pharm Biomed Anal. 36, 57-63 (2004).
- Shi, Z., Hermiller, J. G., Gunter, T. Z., Zhang, X., Reed, D. E. A Novel Sample Selection Strategy by Near-Infrared Spectroscopy-Based High Throughput Tablet Tester for Content Uniformity in Early-Phae Pharmaceutical Product Development. J Pharm Sci. 101 (7), 2502-2511 (2012).
- Silva Elipe, M. V., et al. Applications of 19F Time-Domain NMR to Measure Content in Fluorine-Containing Drug Products. Magn Reson Chem. 54 (6), 531-538 (2015).
- Wang, J., et al. Fluorine in Pharmaceutical Industry: Fluorine-Containing Drugs Introduced to the Market in the Last Decade (2001-2011). Chem Rev. 114, 2432-2506 (2014).
- Dolbier, W. R. . Guide to Fluorine NMR for Organic Chemists. , (2009).
- Barman, J. A., Scott, L. J. Cinacalcet Hydrochloride. Drugs. 65 (2), 271-282 (2005).
- Horn, J. The Proton-Pump Inhibitors: Similarities and Differences. Clin Ther. 22 (3), 266-280 (2000).
- LeBel, M. Ciprofloxacin: Chemistry, Mechanism of Action, Resistance, Antimicrobial Spectrum, Pharmacokinetics, Clinical Trials, and Adverse Reactions. Pharmacotherapy. 8 (1), 3-30 (1988).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon