Voltammetria ciclica
Panoramica
Fonte: Laboratorio della dott.à 18.0. Kayla Green — Texas Christian University
Un esperimento di voltammetria ciclica (CV) prevede la scansione di una gamma di tensioni potenziali durante la misurazione della corrente. Nell'esperimento CV, il potenziale di un elettrodo stazionario immerso viene scansionato da un potenziale iniziale predeterminato a un valore finale (chiamato potenziale di commutazione) e quindi si ottiene la scansione inversa. Questo dà una scansione "ciclica" dei potenziali e la curva corrente vs potenziale derivata dai dati è chiamata voltammogramma ciclico. La prima sweep è chiamata "scansione in avanti" e l'onda di ritorno è chiamata "scansione inversa". I potenziali estremi sono definiti "finestra di scansione". L'entità delle correnti di riduzione e ossidazione e la forma dei voltammogrammi dipendono fortemente dalla concentrazione di analiti, dai tassi di scansione e dalle condizioni sperimentali. Variando questi fattori, la voltammetria ciclica può fornire informazioni sulla stabilità dello stato di ossidazione dei metalli di transizione nella forma complessata, sulla reversibilità delle reazioni di trasferimento di elettroni e sulle informazioni relative alla reattività. Questo video spiegherà la configurazione di base per un esperimento di voltammetria ciclica che include la preparazione dell'analita e la configurazione della cella elettrochimica. Verrà presentato un semplice esperimento di voltammetria ciclica.
Procedura
1. Preparazione della soluzione elettrolitica
- Preparare una soluzione stock di elettrolita (10 mL) composta da 0,1 M [Bu4N][BF4] in CH3CN.
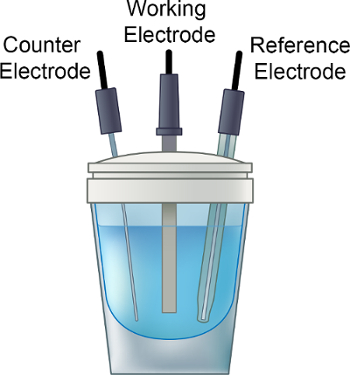
- Posizionare la soluzione elettrolitica nel flaconcino elettrochimico, aggiungere una piccola barra di agitazione e posizionare il tappo sul flaconcino come mostrato nella Figura 1.
- Verificare che il piombo di azoto sia nella soluzione elettrolitica. Mescolare e degassare la soluzione elettrolitica con un f
Risultati
È stata effettuata una scansione CV del ferrocene a 300 mV/s in acetonitrile e il voltammogramma corrispondente è mostrato nella Figura 2.
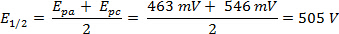
Il ΔE può essere derivato dai dati in Figura 2 in base alla differenza tra Epa ed Epc.
?...
Riferimenti
- Bard, A. J., Faulkner, L. A. Electrochemical methods: Fundamentals and Applications. 2nd ed. New York: Wiley; 833 p. (2001).
- Geiger, W. E., Connelly, N. G. Chemical Redox Agents for Organometallic Chemistry. Chem Rev. 96 (2), 877-910, (1996).