Method Article
組換えアデノ随伴ウイルスの血清型3つのベクトルによる肝癌細胞の高効率形質導入
要約
この記事では、我々はヒト肝癌細胞を標的とするための最も効率的なベクターとしてアデノ随伴ウイルス3型(AAV3)の識別について説明します。
要約
非病原性ヒトパルボウイルスに基づいて組換えベクターは、アデノ随伴ウイルス2(AAV2)を開発し、遺伝子治療臨床試験の数で現在使用されていますされています。さらに最近では、追加のAAV血清型の数も様々な大小の動物モデル1で組織親和性選択を示すことが示されている、単離されている。 10の最も一般的に使用されるAAV血清型のうち、AAV3は群を抜いて試験管内でだけでなく、in vivoでの細胞や組織を形質導入における最も効率的です。
AAV3がバインディングの共受容体の細胞としてのヒト肝細胞増殖因子受容体を使用しているため非常に効率的に細胞株 - 肝芽腫(HB)と肝細胞癌(HCC) - しかし、私たちの最近発表された研究で、我々はAAV3ベクターはヒト肝癌を伝達することが文書化されているこれらの細胞2,3のとエントリー。
この記事では、レポーター遺伝子を有する組換えAAV3ベクターによるヒト肝癌細胞の高効率伝達を達成するために必要な手順を説明します。治療用遺伝子を有する組換えAAV3ベクターの使用は、最終的にヒトの肝癌の潜在的な遺伝子治療につながる可能性があります。
プロトコル
1。組換えアデノ随伴ウイルス3型(rAAV3)ベクターのパッケージング
- ウェブサイトにアクセスしてください:" http://www.geguchadze.com/calc "とDNAの量を計算する。
- FBSと抗生物質を含まない培地中でプレミックスプラスミドpHelper(アデノウイルスヘルパー)、pACG2c3(AAVヘルパー)とpdsAAV - CB - EGFP(するrAAVベクトル)。総量は10 15センチメートル2プレート用8750μLにする必要があります。
- ステップ1.2のDNA溶液にPEIの1250μL(0.1%M / V、Polysciences、カタログ番号23966、pH4.5)を直接追加します。数秒間ボルテックスDNA - PEIのソリューション。
- インキュベートDNA - PEIは、溶液を室温で5分(RT)のための複合体を形成する。
- 15センチメートル2板あたりのDNA - PEI溶液1mLを追加。
- 新鮮な25mLの完全培地+10%FBS(C - DMEM)に置き換えて、4時間後に培地を取り外します。
- 七十二時間後にトランスフェクション、スクレープ細胞と250 mLのコニカル遠心チューブに分注する。
- 4℃、3000rpmでスピン、℃で10分間。上清を捨て。
- RB TMS緩衝液(50mMトリス- HCl、150mMのNaCl、pH8.0)を5mLに細胞ペレットを再懸濁する。新しい15 mLコニカルチューブに移す。
- 37℃で10分間解凍するためのドライアイス - エタノール浴で凍結℃で10分間。 3回繰り返します。
- 4.8 M MgCl 2とベンゾナーゼ2μL(25 U /μL、Novagen社、カタログ番号70664〜3)の1μLを追加。 37渦とインキュベート℃で40分間。
- 40分間4℃、4,000 rpmでCをスピンダウンして(ライセートを清澄化)上清を集める。
- 15%の2 mLの25%の2 mLの40%、1.5 mLおよび13 mLのクイックシールの遠心管(ベックマン、カタログ番号342413)、上から下への負荷イオジキサノール勾配(OptiPrep、カタログ番号1114542)で60%のイオジキサノール1.5mLの。イオジキサノール勾配の上清(ステップ1.12)ロードする。 RB TMS Bufferでチューブを埋める。
- ° Cベックマン90Tiローターを使用して、16で1時間75000 rpmで遠心する。
- 40〜60%の境界で注射器を挿入することにより40%イオジキサノール画分を集める。
- 1つの50 mLコニカルチューブに40%のイオジキサノール分画を転送し、バッファーを40 mLのために構成する(20mMトリス、15mMのNaClを、pHは8.5)。
- ハイトラップQ HPカラム(GE Healthcare社、カタログ番号17-1154-01)を使用してろ過装置を組み立てます。以下のバッファーでカラムを洗浄する:バッファーを25mL(20mMトリス、15mMのNaClを、pH 8.5)に、緩衝液B(10mMトリス、500mMのNaCl、pH 8.5)に25mLの、バッファー50 mLの。バッファ内のウイルスのサンプルを40 mLの、バッファー50 mLの(20mMトリス、15mMのNaClを、pH 8.5)に、緩衝液C(20mMトリス、175 mMのNaCl、pH 8.5)に20mLの。
- 20 mLのアポロコンセントレータ(オービタルサイエンス)のバッファCを収集する。 4℃、3,000 rpmで遠心する℃で10分間を。
- フロースルーを捨て、4℃、3000rpmで冷却したPBSおよび遠心の20 mLを加え℃で10分間を。
- フロースルーを捨て、冷却したPBS 500μLを加える。 -80小アリコートで凍結シリコン処理したエッペンドルフチューブとストアへの膜と転送℃からベクトルを洗い流す
2。 rAAV3ベクトルの力価の決定
- 氷上でエッペンドルフチューブに精製ウイルスの10μLを解凍。のddH 2 Oの40μLを追加
- ベンゾナーゼの0.2μL(25 U /μL、Novagen社、カタログ番号70664)を追加し、37℃で1時間。
- 別のエッペンドルフチューブにプラスミド標準(0.2 ng /μLの)50μLを取る。
- 65の各チューブとインキュベート℃で30分間に100 mMのNaOHを50μLを追加。
- 少なくとも5分間、直ちに氷上で冷やします。
- バイオドットろ紙(Bio - Rad社製、カタログ番号1620161)に応じて転写膜(ミリポア、カタログ番号INYC00010)をカット。 20分のための3つのフィルター紙で10 × SSCでメンブレンを洗浄します。
- スロットブロットSF装置(バイオドット、猫#170〜6542)を設定します。真空フラスコに接続し、スロットブロット装置に10倍のSSCの100μLを加える。
- ステップ2.5のサンプルのそれぞれに20 × SSCの100μLおよび6xローディング色素の1μLを追加。
- スロットブロット装置の膜上に各サンプル100μLをロードします。
- サンプルの各々に10倍のSSCの別の100μLを加える。
- すべてのサンプルがメンブレンを通過するまで、ステップ2.9および2.10を繰り返します。
- スロットブロット装置を分解して膜を取り除く。インスペクタのリンカSL - 1000 UV架橋剤に入れて。 "エネルギー"、"最適な架橋"(ショー1200)の電源を入れ、"開始"を押す。
- サケの精子の沸騰を1 mL(SS)DNA(フィッシャー、カタログ番号NC9753983)5分間。少なくとも5分間氷上で冷やします。
- のddH 2 O、20 × SSC、50 ×デンハルト溶液、20%SDS、1.25 mLを、ポリA 0.25mLのとステップ2.13からSS DNAを1mLの5 mLの15 mLのの27.5 mLを混合してプレハイブリダイゼーション溶液を調製します。
- 65でキャップガラスシリンダーとインキュベートでプレハイブリダイゼーション溶液で一晩ハイブリダイゼーションチャンバーのCの25 mLの膜を一時停止する。
- のddH 2 O10μlに50 ngの鋳型DNAを希釈する。 100℃沸騰℃で少なくとも5分間、直ちに氷上で5分間と寒さのため。
- 1分間、室温で3,000 rpmで遠心する。 10mMの3のdNTP(dCTPを欠いている)、ヘキサヌクレオチドミックスの2μL(Roche社、カタログ番号11277081001)、クレの1μL(Roche社、カタログ番号11008404001)とα-32 P - dCTPの5μLの2μLを加える。 37℃で10分間インキュベートする。
- 2分間、3,000 rpmでG - 50カラムを(GE Healthcare社、カタログ番号27-5330-01)心する。カラムにステップ2.17にプローブをロードする。 2分間、3,000 rpmで遠心し、フロースルーを収集する。
- 放射能をカウント。 ° C、直ちに氷上で5分間と寒さのために少なくとも5分間、100℃のプローブを沸騰。
- 膜とのプレハイブリダイゼーション溶液にプローブ(6 × 10 5 cpm / mlの)を追加します。
- ハイブリダイゼーションチャンバーで65℃で一晩インキュベートする。
- ハイブリダイゼーション溶液を捨て、15分間室温で2 × SSC 0.1パーセントSDSで膜をすすいでください。
- 液を捨て、℃で30分間65℃で0.1 × SSC 0.1パーセントSDSで膜をすすいでください。
- 液を捨て、室温で短時間で0.1 × SSCで膜をすすいでください。
- 6時間-80℃でフィルムを公開し、フィルムを開発する。典型的な結果を図1に示されています。
3。 rAAV3ベクターによる形質導入し、ヒト肝癌細胞における導入遺伝子発現
- 96ウェルプレートの各ウェル内のシード1 × 10 4細胞(したHuh7またはHep293TTのどちらか)。少なくとも18時間加湿CO 2インキュベーター内でインキュベートする。
- 96ウェルプレートから培地を取り除く。
- FBSと抗生物質を含まない培地50μLで細胞を2回洗浄し、削除する。
- 5000 VGS /細胞でFBSと抗生物質とするrAAVベクターを含まない培地50μLを加える。
- 4時間CO 2インキュベーターで培養する。
- 培地を捨てる。完全培地50μLで細胞を2回洗浄し、削除します。
- 各ウェルに、C - DMEMを150μLを追加し、72時間CO 2インキュベーター内でプレートをインキュベートし、蛍光顕微鏡(DMI 4000B、ライカマイクロシステムズ)を用いてEGFPの発現を可視化する。
- ウイルス感染細胞の3つのウエルからの画像は、ImageJの解析ソフト(NIH、ベセスダ、MD、米国)によって定量的に解析されています。
- 導入遺伝子の発現は、視野あたりの緑色蛍光の総面積(画素2)として評価される。典型的な結果を図2に示されています。
- 導入遺伝子の発現は、フローサイトメトリーによって決定することができる。
4。代表的な結果:
上記のプロトコルに続いて、一つは効率的にAAVの血清型のベクトルを生成することができます。典型的な収量は、ベクトルの株式を精製〜10 11 VGS /μLを含む〜500μLです。ベクトルの株式の純度は、ベンゾナーゼの消化がある場合とない場合の、定量的なDNAのスロットブロットでハイブリダイゼーションシグナルを比較することによって決定されます。効率的に細胞株 - 肝芽腫(HB)と肝細胞癌(HCC) - rAAV3ベクトル形質導入ヒト肝癌を精製。
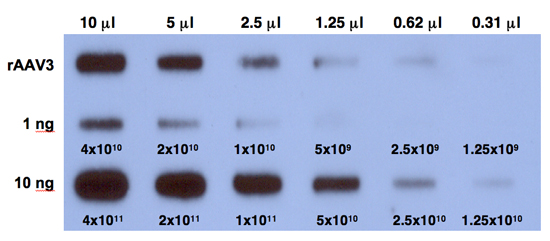
図1。rAAV3ベクトルの力価を決定するための定量的DNAスロット-ブロット分析。ベンゾナーゼ(一番上の行)で消化し たウイルス株を、精製の2倍希釈を32 P -標識したEGFP特異的DNAプローブを用いて定量的なDNAのスロットブロットで分析した。 AAV3ベクトルの力価は、1 ngの(中段)または膜にロードされたAAV - EGFPプラスミド基準の10ngの(一番下の行)との比較により決定した。数字は、DNAのコピーに対応しています。
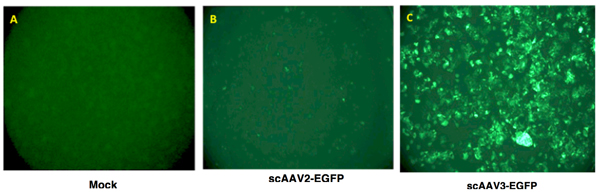
図2組換えAAVヒト肝癌細胞におけるベクターによる導入遺伝子の発現。 Hep293TT細胞、最近設立されたヒト肝芽細胞の4行目は 、どちらかのモック感染(左パネル)だった、または2時間、37℃でscAAV2 - EGFPまたはscAAV3 - EGFPベクターのどちらかの5000 VGS /セルで形質導入。導入遺伝子の発現は72時間後の形質導入は、蛍光顕微鏡を用いて可視化した。
ディスカッション
非病原性ヒトパルボウイルス、アデノ随伴ウイルス(AAV)に基づいて組換えベクターを開発し、遺伝子治療臨床試験5の数で現在使用されていますされています。以前は、10の最も一般的に使用されるAAV血清型の、一般的にAAV3ベクトルの導入効率は、in vitroおよび in vivo 1 の両方、特に低いことが報告されている。しかし、我々の最近非常によくAAV3ベクトル形質導入ヒト肝癌細胞株は、のようなフローサイトメトリー2で定量的に決定した観察、とAAV3はこれらの結合とエントリの細胞共受容体としてのヒト肝細胞増殖因子受容体(hHGFR)を利用しているセル3は 、強く、特に一般的にヒト肝細胞、およびヒト肝癌細胞に対してAAV3の選択的な組織親和性を示唆している。しかし、AAV3ベクターはまた、効率的に2正常ヒト肝細胞を形質導入するので、in vivoでのがんの遺伝子治療のアプリケーションでそれらの潜在的な利用に悪影響を及ぼす可能になります。この潜在的な問題を回避する一つの可能な戦略は選択的に腫瘍ではなく、正常な肝細胞によって産生される遺伝子産物を識別することによって癌細胞の転写標的を伴います。例えば、以前の研究は、正常な肝細胞は一般に非常に少量のを生成するのでα-フェトプロテイン(AFP)の血清レベルは、特定の存在を追跡するためのマーカー、進行、および/または肝臓癌の特定の種類の再発として使用されていることが示されているこのタンパク質。実際、我々は肝癌細胞ではなく、正常な肝細胞2、および研究において導入遺伝子の発現を標的とするAFPプロモーターを含むAAV3ベクトルを使用している現在、肝癌のマウス異種移植モデルでは、このアプローチの有効性をテストするために進行中です。私たちのさらなる研究では、我々は様々なAAVの血清型のベクターの導入効率が大幅に6月14日ウイルスキャプシドの表面に露出したチロシン残基の部位特異的突然変異誘発により増強することができることを観察した。 6 7の表面に露出したチロシンもAAV3に保存されているので、我々はこれらの残基の部位特異的突然変異誘発を実施し、チロシンに変異がAAV3ベクトルの導入効率が大幅にヒト肝癌細胞(未発表データ)に増強されることを観察した。研究はまた、ヒト肝と肝細胞癌のためのマウス異種移植モデルにおけるチロシン変異AAV3ベクトルの安全性と有効性を評価するために現在進行中であり、そして成功した場合、最適なチロシン変異AAV3の血清型のベクターは、ヒトの肝臓を標的とするために有用であることが証明されるかもしれない潜在的な遺伝子治療のためのがん。
開示事項
謝辞
我々は、博士に感謝する。寛大Hep293TT細胞を提供するための組換えAAV3とAAV - EGFPプラスミド、それぞれ、博士ゲイルトムリンソンの彼らの親切なギフトのためのR.ジュードSamulskiとシャオシャオ。この研究は国立衛生研究所からの公衆衛生サービス助成金助成金R01 HL - 076901、R01 HL - 097088、およびP01 DK - 058327(プロジェクト1)(ASの)によって部分的にサポートされていました。
資料
| Name | Company | Catalog Number | Comments |
| DMEM | Cellgro | 10-0170CM | |
| PEI | Polysciences, Inc. | 23966 | |
| Benzonase | Novagen, EMD Millipore | 70664-3 | |
| HiTrap Q HP column | GE Healthcare | 17-1154-01 | |
| Salmon sperm DNA | Fisher Scientific | NC9753983 | |
| Iodixanol gradient | OptiPrep | 1114542 | |
| G-50 Columns | GE Healthcare | 27-5330-01 |
参考文献
- Zincarelli, C., Soltys, S., Rengo, G., Rabinowitz, J. E. Analysis of AAV serotypes 1-9 mediated gene expression and tropism in mice after systemic injection. Mol Ther. 16, 1073-1080 (2008).
- Glushakova, L. G., Lisankie, M. J., Eruslanov, E. B., Ojano-Dirain, C., Zolotukhin, I., Liu, C., Srivastava, A., Stacpoole, P. W. AAV3-mediated transfer and expression of the pyruvate dehydrogenase E1 alpha subunit gene causes metabolic remodeling and apoptosis of human liver cancer cells. Mol Genet & Metabol. 98, 289-299 (2009).
- Ling, C., Lu, Y., Kalsi, J. K., Jayandharan, G. R., Li, B., Ma, W., Cheng, B., Gee, S. W., McGoogan, K. E., Govindasamy, L., Zhong, L., Agbandje-McKenna, M., Srivastava, A. Human hepatocyte growth factor receptor is a cellular coreceptor for adeno-associated virus serotype 3. Hum Gene Ther. 21, 1741-1747 (2010).
- Chen, T. T., Rakheja, D., Hung, J. Y., Hornsby, P. J., Tabaczewski, P., Malogolowkin, M., Feusner, J., Miskevich, F., Schultz, R., Tomlinson, G. E. Establishment and characterization of a cancer cell line derived from an aggressive childhood liver tumor. Pediatr Blood & Cancer. 53, 1040-1047 (2009).
- Daya, S., Berns, K. I. Gene therapy using adeno-associated virus vectors. Clin Microbiol Rev. 21, 583-593 (2008).
- Zhong, L., Li, B., Mah, C. S., Govindasamy, L., Agbandje-McKenna, M., Cooper, M., Herzog, R. W., Zolotukhin, I., Warrington, K. H., Weigel-Van Aken, K. A., Hobbs, J. A., Zolotukhin, S., Muzyczka, N., Srivastava, A. Next generation of adeno-associated virus 2 vectors: point mutations in tyrosines lead to high-efficiency transduction at lower doses. Proc Natl Acad Sci USA. 105, 7827-7832 (2008).
- Petrs-Silva, H., Dinculescu, A., Li, Q., Min, S. H., Chiodo, V., Pang, J. J., Zhong, L., Zolotukhin, S., Srivastava, A., Lewin, A. S., Hauswirth, W. W. High-efficiency transduction of the mouse retina by tyrosine-mutant AAV serotype vectors. Mol Ther. 17, 463-471 (2009).
- Jayandharan, G. R., Zhong, L., Sack, B. K., Rivers, A. E., Li, M., Li, B., Herzog, R. W., Srivastava, A. Optimized adeno-associated virus (AAV)-protein phosphatase-5 helper viruses for efficient liver transduction by single-stranded AAV vectors: therapeutic expression of factor IX at reduced vector doses. Hum. Gene Ther. 21, 271-283 (2010).
- Li, M., Jayandharan, G. R., Li, B., Ling, C., Ma, W., Srivastava, A., Zhong, L. High-efficiency transduction of fibroblasts and mesenchymal stem cells by tyrosine-mutant AAV2 vectors for their potential use in cellular therapy. Hum Gene Ther. 21, 1527-1543 (2010).
- Kauss, M. A., Smith, L. J., Zhong, L., Srivastava, A., Wong, K. K. J. r., Chatterjee, S. Enhanced long-term transduction and multilineage engraftment of human hematopoietic stem cells transduced with tyrosine-modified recombinant adeno-associated virus serotype 2. Hum Gene Ther. 21, 1129-1136 (2010).
- Qiao, C., Zhang, W., Yuan, Z., Shin, J. H., Li, J., Jayandharan, G. R., Zhong, L., Srivastava, A., Xiao, X., Duan, D. Adeno-associated virus serotype 6 capsid tyrosine-to-phenylalanine mutations improve gene transfer to skeletal muscle. Hum Gene Ther. 21, 1343-1348 (2010).
- Markusic, D. M., Herzog, R. W., Aslanidi, G. V., Hoffman, B. E., Li, B., Li, M., Jayandharan, G. R., Ling, C., Zolotukhin, I., Ma, W., Zolotukhin, S., Srivastava, A., Zhong, L. High-efficiency transduction and correction of murine hemophilia B using AAV2 vectors devoid of multiple surface-exposed tyrosines. Mol Ther. 18, 2048-2056 (2010).
- Ojano-Dirain, C., Glushakova, L. G., Zhong, L., Zolotukhin, S., Muzyczka, N., Srivastava, A., Stacpoole, P. W. An animal model of PDH deficiency using AAV8-siRNA vector-mediated knockdown of pyruvate dehydrogenase E1α. Mol Genet & Metabol. 101, 183-191 (2010).
- Petrs-Silva, H., Dinculescu, A., Li, Q., Deng, W. T., Pang, J. J., Min, S. H., Chiodo, V., Neeley, A. W., Govindasamy, L., Bennett, A., Agbandje-McKenna, M. Novel properties of tyrosine-mutant AAV2 vectors in the mouse retina. Mol Ther. , (2011).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved