Method Article
亜麻の花-DIP変換(
要約
ここでは、フローラルディップを経由してアグロバクテリウムによる植物の形質転換を用いて、亜麻を変換するプロトコルを提示する。このプロトコルは、実施が簡単で安価である、まだ亜麻の形質転換のために現在利用できる方法よりも高い変換率が得られます。
要約
フローラルディップを介してアグロバクテリウム媒介植物形質転換は、植物形質転換の分野で広く使用される技術であり、多くの植物種のために成功することが報告されている。しかし、フローラル·ディップによる亜麻( アマ )変換が報告されていない。このプロトコルの目的は、 アグロバクテリウムとフローラルディップ法、トランスジェニック亜麻を生成するために使用できることを確立することである。我々は、この技術は、簡単で安価な、効率的であり、より重要なことに、亜麻変換の現在利用可能な方法よりも高い変換率が得られることを示している。
2分-要するに、亜麻の花序1バイナリベクタープラスミド(T-DNA断片プラスアマ挿入シーケンス、LIS-1)を担持するアグロバクテリウムの溶液に浸漬した。植物は24時間彼らの側に平らに置いた。次いで、植物は、次の処理までの通常の増殖条件下で維持した。プロセスへ浸漬の間に14日間隔 - 約10で3回、 - 浸漬のsは2を繰り返した。 T1種子を収集し、土壌上で発芽させた。約2週間後、処理された子孫を直接PCRによって試験した。 2から3葉植物プラス適切なT-DNAプライマーごとに使用した。陽性の形質転換体を選択し、成熟するまで成長させた。陽性形質転換体である、処理された植物からの種子の60% - 変換率が50では、予想外に高かった。これは、フローラルディップ変換を用いて、シロイヌナズナ及び他の植物種について報告されたものよりも高い変換率である。また、形質転換のための他の方法を使用して亜麻形質転換のために、これまでに報告されている、最も高い。
概要
亜麻( アマ ) は、その繊維と油のため広く栽培重要な作物である。亜麻ゲノムの形質転換は、再生が続くバイオリスティック粒子または超音波処理を適用し、組織培養におけるそのような創傷、 アグロバクテリウム感染 、及び共培養のような技術により可能である。しかしながら、これらの技術は、多くの変異事象の傾向およびトランスジェニック系統を得るために長時間を含む多くの欠点を持っている。これらの方法のいくつかは、高価であり、低回収苗、その結果、器具の熟練した効率的な操作を必要とすることができる。最も重要なことは、これらの技術は、多くの場合、低い変換率2,6が生じる。
フローラルディップ経由アグロバクテリウムによる植物の形質転換は、トランスジェニック植物を生成するための簡単かつ効率的なアプローチである。それは、日常的にし、正常にそのようなシロイヌナズナthalianなど多くの植物種のために使用されてきた1,4、 ウマゴヤシのtruncatula 11、トマト12、小麦13とトウモロコシ10。しかし、それは、原因亜麻によって生成花少数など、いくつかの要因に亜麻の形質転換のための実行可能な技術は、それぞれの花から得られた種子の数が限られ、大きな種子サイズ、及び厚さの被膜として考えられていないまた、形質転換プロセスのために問題となる可能性がある。さらに、フローラルディップ技術の選択セグメントは、非形質転換子孫が発芽や発芽していないどちらながら変換し子孫は、発芽と緑に滞在する能力に基づいて区別して、抗生物質を含む植物メディアに変換された種子を発芽さが必要ですが、漂白剤出素早く死ぬ。現在の文献では、野生型亜麻ベースの偽陽性の結果を生成する、およびT1子孫の選択を行う、抗生物質選択の高濃度を脱出する傾向があることが指摘されている抗生物質耐性に6,14より難しい。また、抗生物質の高濃度は、選択培地に添加した場合、観測された変換率は劇的9ドロップ。
このプロトコルでは、そのゲノム3,5を変更することによって、環境におけるストレスに応答することが示されている繊維、亜麻、モント巻雲(応答性プラスチック)の行を変換するためにアグロバクテリウムとフローラルディップ法を用いた。抗生物質エスケープ問題を克服するために、我々は、植物培地に抗生物質を添加することによって、代わりの選択T1葉からのDNAの直接PCR検査を行うことを選択した。我々は、処理時に特定の花を追跡するために亜麻の簡単な解剖学的構造を利用した。この追跡システムは、抗生物質を添加することなく、土壌の特定の花および発芽の種子の選択を可能にした。陽性の形質転換体を、単に、迅速かつ効率的な方法を使用してoを葉から得られたDNAを試験することによって同定されたFダイレクトPCR。我々の結果は、フローラルディップ法は、亜麻のこの行に非常によく働いて、驚くべきことに、非常に高い変換率をもたらしたことを実証する-以前であると報告されたシロイヌナズナのために観察されるものよりも高い(50~60%)0.1から1 1%、および他の植物種10,12よりも高い。我々はまた、亜麻仁の別のさまざまな(オイル亜麻)、ベスーン(安定した非応答)をテストし、私たちの予備データはフローラル·ディップも、亜麻のこの品種のために働くことを示しています。
このプロトコルの目的は、 アグロバクテリウムとフローラルディップジェニック亜麻を生成するために使用できることを示すことである。我々は、この技術は、簡単で安価、および亜麻変換の他の方法よりも迅速であることを示している。さらに重要なことには、亜麻変換2,6の他の方法よりもはるかに高い変換率をもたらす。多くの枝や花を持つシロイヌナズナの解剖学、マサチューセッツ州KESが困難同じ植物に浸し、非浸し花を区別する。したがって、種子の多数は、植物当たり約2万種子は、陽性形質転換体8を同定するためにスクリーニングされる必要がある。亜麻は、一方では、個々の花を追跡すると、スクリーニングプロセスの間に、特定の種を選択することを可能にするもの、植物当たり約100個の種子を生産する、より少ない分岐(一方の主枝及び少数側枝)少ない花を有する。
私たちは、フローラル·ディップが亜麻のいずれかの近縁種、約200種の属を変換するために適用可能な方法であることを提案する。この方法は、亜麻変換の他の方法よりもはるかに高い変換率が得られる。また、T1葉DNAの直接PCRスクリーニングは、しばしば、多くの偽陽性を生じる抗生物質耐性のエスケープの問題を克服する効率的な方法であることを提案している。直接PCRスクリーニングは、任意の他の植物種に適用することができ、tは限定されるものではない亜麻O。このプロトコールで用いられる単純なシード追跡技術は、亜麻と類似の解剖学的構造を分岐して他の植物種に適用することができる。
プロトコル
1.植物を育て
- 6週間前浸漬し、土壌と5インチポットを記入し、亜麻の種子をまく¼(ポット当たり4の種子)、土壌に深くインチ。シードの上に土を固めるようにしてください。定期的に植物に水と長い昼光(14時間の明と10時間の暗闇)でそれらを維持する。
- 主要な花序(花「臓器のクラスター)を定期的に植物を確認してください。芽が表示され、ちょうど花序( 図1及び2)に形成されたときに植物が形質転換のための準備ができている。必要に応じて、芽を確認するには、その周りの葉をカット。
注:最高の花のステージを使用することが重要であると考察に詳述されている。- それはサイドbrachesより多くの花を生産するように実験的治療のための植物の主な枝を使用してください。コントロールとして(浸漬されるものではない)、または他の実験治療のためにどちらかの側枝を使用してください。
- また、メインとサイド枝を使用実験的治療のために同じ植物とコントロールとして、または他の実験的な治療のために別の植物を使用しています。個々の支店と日付と治療の種類と個々の花をマークするラベルを使用してください。
2.クローニングおよび形質転換大腸菌(E. coli)細胞の中
- T-DNAを保有植物バイナリーベクターのマルチクローニングサイトに目的の断片/遺伝子をクローニング。
- 1段階または2段階でクローニングを実行します。
- 直接植物バイナリーベクターには、このプロトコル(〜500 bp)の中に小さなインサートのクローンを作成する。このプロトコルでは、植物バイナリーベクター(PRI909)を使用します。それ以外の場合は、同様の戦略で、他の植物バイナリーベクターを使用しています。
- 最初の植物バイナリーベクターにサブクローニングその後、(特定の植物ではない)一般商業クローニングキットを使用して:あるいは、二段階で大きな挿入(≥6.5KB)をクローンする。
- 1段階または2段階でクローニングを実行します。
- PCR REACを設定ンは、目的の遺伝子を増幅した。 (使用中の植物バイナリーベクターのマルチクローニングサイトによれば)5 '末端に制限部位を有するプライマーを設計します。
- 以下のサイクリング条件で、標準的なPCRは、ゲノム亜麻DNAを使用して行う:24℃の初期保持し、その後、5秒間98℃の30サイクル、続いて94℃で2分間、15秒間60℃、および2分間72℃である。 4℃で無期限保留に続く5分間の72℃での最終伸長工程を実行します。
- 1%トリス/ホウ酸塩/ EDTA(TBE)アガロースゲル上の別々のPCR産物は、1時間、100Vでゲルを実行する。ゲルから製品を浄化し、ナノドロップを経由して定量化する。
- 商業クローニングベクターにPCR産物をクローニングする連結ミックスを設定します。製造業者のプロトコルに従ってください。
- 化学的にコンピテントに連結ミックスを変換する次のように大腸菌細胞 。
- CHの1バイアルにライゲーションミックス2μlのを追加します。emicallyテントE. coli細胞 。氷上で30分間インキュベートする。
- 熱は、42℃で30秒間細胞に衝撃を与える(熱ショック時間および温度は、使用する細胞の種類に依存する)。
- 氷上でインキュベートし、カタボライト抑制(SOC)培地でRTスーパー最適ブロス250μlを添加する。
- チューブをキャップと1時間、37℃で200rpmでオービタルシェーカーでインキュベートする。
- 10広がる - (37℃で予め温め)予め温めたLBプレート+適切な選択抗生物質の各形質転換からの50μlを(使用される市販のクローニングベクターの種類に基づいて、選択抗生物質を決定する)。 37℃CO / Nでプレートをインキュベートする。
- 市販のキットを使用して、ミニプレッププラスミド精製のために〜10個のコロニーを選択してください。ミニプレッププラスミド精製は、一般的に以下のように行われる。
注:バッファ名が使用される市販のキットに固有のものですが、その一般的な機能は似ています。- 2の単一のコロニーを接種- (使用した市販のベクターのタイプに基づいて決定される)適切な選択的抗生物質を含む5mlのLB培地。
- 激しく振盪(〜300 rpm)で、37℃で約8時間インキュベートする。
- 10分間6000×gでの遠心分離によって細胞を回収。
- 250μlの再懸濁緩衝液にペレットを再懸濁。ミックスと渦は完全にペレットを分散させる。
- 6回 - 溶解バッファー250μlのを追加して、細菌細胞を溶解は、チューブ4を反転させることによって完全に混合。
- 中和緩衝液中に溶解液を中和し、4反転 - 混合する6回。卓上型マイクロ遠心上〜17,900×gで10分間遠心。
- スピンカラムに前のステップからの上清を転送します。 60秒 - 30〜17,900×gで再び遠心し。
- 60秒 - 30 0.75ミリリットル洗浄緩衝液と遠心を追加することによって、スピンカラムを洗浄します。フロースルーを捨てます。
- レモへの追加1分間遠心残留洗浄バッファーVEの。新しい1.5 mlのマイクロ遠心チューブにスピンカラムを配置します。 DNAを溶出するために、各列の中央に50μlの水を加える。 1分間放置しましょう、と1分間遠心する。
3.インサートの存在のために精製されたプラスミドを分析
- 制限消化:
- インサートをクローニングするために使用される制限酵素でプラスミドを消化してインサートの存在を決定するために制限消化を設定する。次のように典型的な二重制限して反応をダイジェスト:精製プラスミド1μgの、それぞれの制限酵素の1μL、2μLの10倍の制限は、緩衝液+ 2μlのBSA(該当する場合)、(20μLの合計)Xμlの水を消化
- 穏やかに混合し、推奨温度(1酵素から別異なります)でインキュベート。
- 制限を1時間、100Vで実行、1%TBEアガロースゲル上で反応を消化し、適切な大きさのドロップアウトを探して分析する。
- PCR分析。
- INSERTまたはベクトルとインサートとの間の接合部の内側に増幅するために市販のベクター領域からプライマーを用いて、精製したプラスミドを用いてPCRを設定します。共通プライマーは、M13のフォワードおよびリバース及びT3 / T7プライマーである。
- このプロトコルでは、以下のPCRサイクル条件を使用し、その後、5秒、15秒、60℃、98℃で18サイクル、続いて94℃で2分間、および72℃、24℃の初期保持する2分間。 4℃で無期限保留に続く5分間の72℃での最終伸長工程を実行します。
- 1%TBEアガロースゲル上に負荷PCR産物と100して実行 - 1時間、120 V。
- シーケンシング:
- 分析し、インサートの存在を確認するために、市販のシークエンシング施設に精製したプラスミドを送信します。
- 正しい構築物が得られたら、(植物バイナリーベクターに)クローニングの第二段階のためにそれを使用。
注: - 3.3 2.3〜ステップクローニングは、一段階で完了している場合を排除することができる。
植物バイナリーベクター(PRI909)とE.へのクローニング4. 大腸菌の形質転換
- 二重制限を設定する植物バイナリーベクターを線状化し、プライマー( ステップ2.2)に添加し、同じ制限酵素部位を使用して、以前にクローニングされた挿入物を単離するための反応を消化する。
- 2時間 - 制限1、100 Vで動作し、ゲル電気泳動を用いて消化し、分析。ゲルからの挿入および線形化された植物バイナリーベクターをカット。
- ゲル製品を精製する市販のキットを使用してください。メーカーのマニュアルを参照してください。
- 植物バイナリーベクターへの挿入を連結する連結反応を設定します。ベクトル比インサートは、インサートのサイズや植物バイナリーベクターに依存します。このプロトコルではLIS1インサートは6.5キロバイトだったと植物バイナリーベクターは、9 KBでした。ベクトル比2のインサート:したがって、1を使用。 3 - >を繰り返して、2.4を繰り返します 。正しい構築物は(+植物バイナリーベクターを挿入)が得られると、 ステップ5でエレクトロポレーションに進みます。
アグロバクテリウムへ5.エレクトロポレーションは、電気的にコンピテント細胞ツメファシエンス
- アグロバクテリウムのバイアルを解凍すると、氷の上に電気的にコンピテント細胞ツメファシエンス 。
- 氷の上に、コンピテントセルの20μlにバイナリーベクタープラスミドDNAを1 ngのを追加し、穏やかに混合する。
- 氷の上0.1cmエレクトロポレーションキュベットを冷却。
- エレクトロポレーションキュベットにテントセル/ DNAミックスを移し、下部の混合物を収集するためにタップします。エレクトロ機やパルスでキュベットを入れて(電圧と時間の条件は、キュベットのサイズと使用エレクトロに依存)。
- 15mlチューブにSOC培地および転送細胞を1ml加える。
- 28から30で1時間インキュベートする100 rpmで振とう、℃。プレート50 - LB寒天+適切な選択抗生物質に対する細胞100μl(植物バイナリープラスミドと使用アグロバクテリウムの菌株に依存し、50μg/ mlのカナマイシンおよび100μg/ mlストレプトマイシン、このプロトコルの使用では。)。
- 30°C - 28で48時間までのプレートをインキュベートします。
- コロニーの選択とプラスミド精製の ための手順を繰り返し2.5。
- 手順3を繰り返して、プラスミドを分析し、フローラル·ディッピング用構 築物を用いて前に挿入し、T-DNAの整合性をチェックする。 ステップ3.3のように、全体のインサート地域全体とT-DNA領域を横断し、配列決定することにより、複数のPCRプライマーを用いて手順を繰り返し3.2、。
注:このプロトコルでは、4つの異なるプライマーは、T-DNAとインサート全体で10のプライマー間で設計されました。 - iを選択したアグロバクテリウムコロニー植物バイナリープラスミドの存在が確認されると、場所細胞-80℃でnは、50%グリセロール、店舗。彼らは一週間7内で使用される場合、ストアは、4℃でプレート上にコロニーを残り。
6.花ディップ
注:-ディッピング花の前に2日:
- 液体培地中でLB +適切な抗生物質に- (許容さ1〜0.5の間でOD 600)の固定相へのアグロバクテリウム細胞を成長させる。
注:これらの植物バイナリーベクター、使用アグロバクテリウム株の種類に基づいて、 工程5.6と同様の抗生物質である。 - 1で培養を開始:飽和(5ミリリットル)O / N培養の100希釈液と24育つ - 150 rpmで振とうしながら28〜30℃で48時間。文化はmidlogarithmic相に達している必要があり、より多くの可能性に近づいまたは固定相1になります。約0.8のOD(0.5〜1の間で再びODはすべて可)8。 5000 xで遠心分離して細胞を回収RTでグラム。
- 浸潤培地中の細胞( - 0.003%のSilwet L-77 5.0%スクロース+ 0.05)を懸濁する。浸漬の最初のラウンドでは、0.05%のシルウェット-77を使用しています。 2回目および3回目のために、( 議論で詳述)0.03%の濃度を低下させる。
- フローラルディップ工程に進みます。その側に工場を置き、1〜2分間浸透媒体にしか見え芽を浸す。その側に工場を残し、ドーム( 図3)で高湿度を維持するために、プラスチック製のラップでそれをカバーしています。
- 翌日、直立位置に植物を配置し、正常に維持する。
- 芽が(通常、約10の後に- 14日)大きくなるときは- 6.4、繰り返しは6.1を繰り返します 。 0.003%に60秒とシルウェット-77濃度 - 30に浸漬時間を削減します。
- 彼らの種子が成熟したとします( 図4)収集することができるの準備が整うまで、通常は植物を維持する。
ポジティブトラの7の選択直接PCRでnsformants
- ステップ1.1のように土壌上のT1種子をまく。
- 代替的に、水500ml中の寒天のMS培地+ 4グラムを2.2g添加することにより、MurashigeおよびSkoogの基礎塩培地(MS培地)を作る。オートクレーブ小さな植木鉢に注ぐ。使用するまで4℃で保管してください。
- 固化したMS培地上に置いて、種子をまく。長い日光(14時間の明と暗の10時間)の下で保管してください。 6日目( 図5) -種子は、約4で発芽する。
- 出発点として、それぞれの花から1シードを使用してください。陽性形質転換体が得られない場合には、花から別のシードを選ぶことによって、この手順を繰り返します。
注:いくつかのケースでは1花からではないすべての種子が変換されますので、同じ花から別の種をテストします。実験的な花から追加の種を選択すると、必要な場合がある。
- 定期的に苗に確認してください。約10では - 発芽後14日間、とき真葉は、開発し、直接PCRで植物をテストします。
- 3葉 - 2切断することにより、葉のDNA抽出物を準備 - 各苗から(5〜10 mg)をし、マイクロ遠心チューブに配置します。
- 各チューブに50 mMのNaOHを180μl添加し、そして95℃で10分間インキュベートする。
- 1 Mトリス-HCl(pH8.0)を20μl添加することにより抽出物を中和する。
- 陽性形質転換体を選択するために、T-DNAまたは挿入します( 図7)間で設計されたプライマーを用いて、直接PCR反応において抽出物の1μLを使用してください。
- このプロトコルでは、24°Cの初期保持と直接PCRを使用し、その後、10秒、15秒、アニーリング工程、及び68℃での伸長工程98℃(40サイクル、続いて98℃で2分C)。 4℃で無期限保留に続く5分間の68℃での最終伸長工程を実行します。 (サイクルのためのプライマー、アニーリング温度および伸長時間の詳細については、表1を参照してください)。
- 陽性形質転換体を特定し、成熟にそれらを育てる。種子はMS培地、大きな鍋で土壌に移植( 図5)で発芽させた場合。
結果
図1から4は、プロトコル内のステップのいくつかを示す。 図1及び図2に、花序の芽は、プロトコルを開発するために使用されたアグロバクテリウム細胞と異なる蕾ステージにそれらを公開するように切 断された葉の周り。 図3は、亜麻のフローラルディップのプロセスを示す。 図4示す追跡し、識別することができるか、メインとサイドブランチは標識することができ、どのように個々の花の例。 図5は、T1後代は、MSプラントメディア上で発芽させた後、成熟のために土壌に移植する方法を示しています。 図6は、どのように野生を示し型亜麻は文献6,9,14の前の所見を確認した、カナマイシンを高濃度で脱出することができます。
図7は、正のT1形質転換体からの直接PCR増幅の例を示している。 T1の花メートルから採取したシングルT0植物のAINとサイドのシュート。直接PCRから分かるように、8/12 T1植物を、PCRにより陽性であったし、T-DNA上の異なる領域を増幅している。私たちのプライマーはまた、LIS-1のインサートと複数のクローニング部位( 図7BおよびC)との間で設計されました。我々は、左の境界とNOSターミネーター(データは示していない)または右の境界と複数のクローニング部位( 図7D)のようなT-DNAの異なるセグメントを増幅するために植物バイナリーベクターからの追加のプライマーを用いた。 LIS-1のインサートに特異的なプライマーはまた、このプロトコルで使用された(データは示さず)。プライマーのリストは、 表1に提供されているが、これらのプライマーの配列は、T-DNAの植物バイナリーベクターフローラルディップに使用インサートの配列に依存する。また、主側枝から収集花との間の変換率に有意差がなかったことに留意。

Agrobacterim細胞にそれらを露出させるために、一次花序の芽の周りの葉を切断。(A)の芽を葉で覆われている。(B)の葉を図1にまとめて露光する芽の周りにカットされている。植物から(C)倍拡大画像芽を露出するように切 断後の(A)に。 この図の拡大版をご覧になるにはこちらをクリックしてください。

図2.フローラルディップのために使用するのに最適なステージを決定するために、このプロトコルで使用された別のつぼみの段階。(A)は 、初期段階の芽がapproximaです tely 2ミリメートル。(B)中段芽が約5ミリメートルである。(C)後期段階の芽は、約1cm程度である。 この図の拡大版をご覧になるにはこちらをクリックしてください。

図3.亜麻の花のディップのプロセス。 (A)一次花序は、 アグロバクテリウム細胞を含む浸潤培地中に浸漬されている。(B)(A)(C)から倍拡大浸し植物を翌日まで平らに置かれ、浸し枝を維持するために、プラスチックで覆われている高湿度。 この図の拡大版をご覧になるにはこちらをクリックしてください。

。図4. T0処理した植物から花の追跡および種子コレクションのプロセス、(A)メインブランチ(中央で最も高い枝)と植物全体の例と側枝(B - D)。アン。別の枝から花の例(E)は 、個々の花から採取した種子の例(ラベル- K)。メインブランチからのこの図の拡大版をご覧になるにはこちらをクリックしてください。

図5. T1実生は、抗生物質選択なしに増殖される。(A)T1種子である(B)陽性の形質転換。MSプラントメディア上で発芽させ、直接PCRによって決定されるように、土壌に移植し、成熟に成長している。 この図の拡大版をご覧になるにはこちらをクリックしてください。

図6抗生脱出、T1選択の問題は、直接PCRスクリーニングにより克服される。抗生物質なしMS植物培地上で発芽させ(A)野生型亜麻種子は、(B)野生型亜麻種子をMS植物培地+漸増濃度で発芽のカナマイシン(200μg/ mlの、600μgの/ mlで、1mg / ml)を、野生型亜麻およびT1から2mg / mlのカナマイシン(D)PCRでMS植物培地上で発芽(C)野生型亜麻仁すべてAMPL、カナマイシンプライマーを用いて苗カナマイシン遺伝子をified(凡例:EZ1:DNAマーカー、FlaxS、野生型flaxS、C: ""メインブランチ、SC、SD、Seを、Sfにから収集花からのT1子孫:非浸しブランチ、馬を制御します。 T1の側枝、Wから収集異なる花"C、D、E、F」の子孫:無DNA) この図の拡大版をご覧になるにはこちらをクリックしてください。
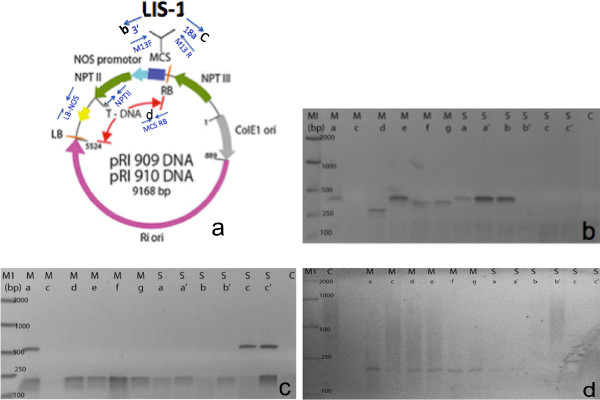
図7.直接PCR法を用いたT1子孫の成功PCR増幅の例植物バイナリーベクター+クローン化されたLIS-1挿入物の(A)図。ブルーの矢印は、(タカラから変更された)の直接PCRスクリーニングに使用されるPCRプライマーの位置を示す。プライマーM13R + 18aにM13Fは+ 3 '(C)PCRプライマーを用いた(B)PCR (D)プライマー右境界を用いたPCR(RB)とマルチクローニング部位(MCS)は**各レーンは、Cから収集し、個々の花からT1を表します。側枝の花のBC」。 この図の拡大版をご覧になるにはこちらをクリックしてください。
| フォワードプライマー配列源 | 配列5'-3 ' | リバースプライマー配列ソース | 配列5'-3 ' | アニーリングTemprature(℃) | 延長時間(秒) | 予想されるサイズ(bp)の |
| M13F(T-DNA) | CTGCAAGGCG ATTAAGTTGG | 3 '(LIS-1挿入) | GAGGATGGAA GATGAAGAAGG | 57 | 40 | 450 |
| 18A(LIS-1挿入) | TATTTTAACCC TATCTCCCAACAC | M13R(T-DNA) | ATTAGGCACC CCAGGCTTTA | 57 | 40 | 520 |
| MCS(T-DNA) | TGGTCATAGC TGTTTCCTGTG | RB(T-DNA) | TTTAAACTGA AGGCGGGAAA | 60 | 20 | 200 |
| LB(T-DNA) | TTTGATGGTG GTTCCGAAAT | NOS(T-DNA) | GAATCCTGTT GCCGGTCTT | 60 | 30 | 380 |
| NPTII(T-DNA) | GCGATACCGT AAAGCACGAG | NTPII(T-DNA) | GCTCGACGTT GTCACTGAAG | 65 | 45 | 502 |
表1.直接PCR検査のために使用したプライマーの一部。
ディスカッション
そのような亜麻( アマ )のようないくつかの植物種では、成功した植物形質転換は制限されてきた。以前は、亜麻で変換が負傷し、共培養、バイオリスティック粒子を適用するか、再生に続いて、超音波超音波処理を使用してアグロバクテリウム感染を必要としている。多くの変異事象を伴うことに長くがちでもあるプロセス。また、これらの技術の選択方法は、カナマイシンのような抗生物質選択マーカーの使用を必要とする。しかし、亜麻抗生物質6,9,14高濃度の脱出する傾向があるため、選択するこの方法は、多くの偽陽性を生じることが文献に記載されている。亜麻変換における従来の技術の別の欠点は、低い変換率は2,6であった。
ここに記載されているプロトコルでは、フローラル·ディッピング経由アグロバクテリウムによる植物の形質転換が示された(百分の50から60まで)亜麻のための高変換率をもたらすと。形質転換体は、メインとサイド枝から浸漬し、収集した花から入手した。陽性形質転換体の選択は単純に通過抗生物質選択を使用すること、土壌T1植物を成長させ、それらが発芽直後の葉をスクリーニングすることによって行われた、ステップは、以前に他の植物種のためのフローラルディップにおける標準として使用した。葉の直接PCRテストを実行し、適切なT-DNAプライマーを用いて、陽性形質転換体を迅速に選択することができる。この技術は、簡単で安価かつ容易に実施することが、まだ以前シロイヌナズナこの方法1,10,12を使用して、他の植物種について報告されたものよりもはるかに高い変換率をもたらす。また、亜麻の最高報告変換率である。
そのしかし、最高の花の段階の選択および最高の界面活性剤濃度を含む手順における重要なステップは、あるアグロバクテリウムは、花器官を殺すことなく、植物細胞に浸透することができる。初期の芽段は0.05%以下の高シルウェット-77濃度( 図2A)を使用した場合、花は種を開発したり設定しません。後期蕾ステージが( 図2C)を使用する場合、変換が動作するかもしれないが、それははるかに低いレートで発生する。同様の結果は、 シロイヌナズナフローラルディップ変換1,4で得られた。このプロトコルでは、すべての花のステージは、第二の浸漬で、続いて別のシルウェット-77の濃度で試験した、最高のステージは、第1の浸漬のための0.05%で、シルウェット-77との中間の芽の段階( 図2C)であることが決定された0.03%のわずかに減少シルウェット-77濃度の後期の芽段( 図2C)。変換はまた続いて、0.003%の低シルウェット-77濃度の初期の芽段( 図2A)を使用して、うまくいった0.05%の高いシルウェット-77濃度の中間の芽段( 図2B)と第二の浸漬。
このプロトコルでは、いくつかの他のパラメータは、変換速度を最適化しようとしたが、最終結果に影響を及ぼさないことが見出された。例としては、植物が彼らの側に置き、1日から2日後にプラスチックでカバーされていることを浸漬した後の時間を延長すること; アグロバクテリウム培養に1以上のODを使用する代わりに、0.5から1。 15分の代わりに1 - - 2分間5に浸漬時間を増大させる。ここでも我々はこれらの戦略を用いた形質転換率に影響を気づいていない。最も効果的な要因は、しかし、正確な花の段階で健康な植物を使用して、最良のSilwet-77濃度を用いていることが見出された。我々は2つの浸漬間隔は、1時間の浸漬でも動作するにもかかわらず、何らかの形でより良いより1時間を働くことに気づいた。
このプロトコルへの変更は、reducinによって達成することができる第二または第三の浸漬で、わずか0.003%にまでGのSilwet-77濃度。シルウェット-77は有毒であるため、花濃度が高すぎる結果がない種子収量をもたらし、不十分な発展途上。植物は健康見ていないと芽がよく開発されていない場合、第二又は第三の事象が解消して浸漬周波数は、一つに削減することができる。
この技術の主な制限は、亜麻、それぞれの花から得られた種子の数が限られ、亜麻の長いライフサイクルによって生成される花の数が少ないことである。 T1世代に到達するために10週間後に浸漬 - 最初の浸漬の準備が主な芽と追加の8を持っているシード播種から8週間 - それは、6かかります。合計で5〜6 - ヶ月T1世代を得るために必要とされる。他の植物種とは異なり、その年の花いつでも、いくつかの亜麻の品種特定の時間年間でより良い花。だから、この技術のための思慮深い計画が重要です。
、二つの異なる亜麻品種とのフローラルディップの我々の結果:繊維亜麻、ストアモントシーラス(応答性プラスチック)、およびオイル亜麻、ベスーン(安定した非応答)は、そのアグロバクテリウムを表示-フローラルディップを介して媒介植物形質転換は、亜麻の形質転換のために適用可能で効率的な方法であり、亜麻形質転換のために以前に使用されている技術を置き換えるために使用することができる。このプロトコルでフローラルディップ法の修正は、他の植物種での使用に適用し、亜麻、これらに限定されないであろう。
開示事項
The authors have nothing to disclose.
謝辞
This work was supported by the Ogelbay fund.
資料
| Name | Company | Catalog Number | Comments |
| Flax seeds of the original Stormont Cirrus variety (PL) | |||
| 5" pots | |||
| Potting soil | |||
| Greenhouse with appropriate light setting | |||
| Thermocycler | |||
| Agarose gel electropheresis equipment | |||
| Digital imaging setup | |||
| Silwet-77 | LEHLE SEEDS | VIS-01 | Toxic, wear gloves |
| GoTaq Green Master Mix | Promega | Part# 9PIM712 | |
| Terra PCR Direct Polymerase Mix | Clontech | 639270 | |
| Binary vector PRI 909 | Takara | 3260 | |
| Agrobacterium tumefaciens LBA4404 E | Takara | 9115 | |
| TOPO TA cloning kit | Invitrogen | K4595-01 | |
| Sucrose | Fisher Scientific | ||
| Electroporator and cuvettes | Bio-Rad | 165-2092 | |
| Shaker | |||
| Spinner | |||
| Plastic wrap and aluminum foil wrap | |||
| speedSTAR DNA polymerase | Takara | RR070A/B | |
| QlAquick gel extraction kit | Qiagen | 28704 | |
| QIAGEN plasmid mini kit | Qiagen | 12123 | |
| SalI-HF enzyme | NEB | R3138S | |
| SacI-HF enzyme | NEB | R3156S | |
| T4 DNA ligation kit | NEB | M0202 | |
| Murashige Skoog | Sigma | M5524 | |
| Agar | Fisher Scientific | A360-500 |
参考文献
- Bent, A. Arabidopsis thaliana floral dip transformation method. Methods Mol Biol. 343, 87-103 (2006).
- Beranova, M., Rakousky, S., Vavrova, Z., Skalicky, T. Sonication assisted Agrobacterium-mediated transformation enhances the transformation efficiency in flax (Linum usitatissimum L.). Plant Cell Tiss Organ Cult. 94, 253-259 (2008).
- Chen, Y., Schneeberger, R. G., Cullis, C. A. A site-specific insertion sequence in flax genotrophs induced by environment. New Phytol. 167, 171-180 (2005).
- Clough, S. J., Bent, A. F. Floral dip: a simplified method for Agrobacterium-mediated transformation of Arabidopsis thaliana. Plant J. 16 (6), 735-743 (1998).
- Cullis, C. A. Mechanisms and Control of Rapid Genomic Changes in Flax. Ann Bot. 95, 201-206 (2005).
- Dong, J. Z., McHughen, A. An improved procedure for production of transgenic flax plants using Agrobacterium tumefaciens. Plant Sci. 88, 61-71 (1993).
- Logemann, E., Birkenbihl, R. P., Ulker, B., Somssich, I. S. An improved method for preparing Agrobacterium cells that simplifies the Arabidopsis transformation protocol. Plant Methods. 2 (16), (2006).
- Mara, C., Grigorova, B., Liu, Z. Floral-dip transformation of Arabidopsis thaliana to examine pTSO2::β-glucuronidase reporter gene expression. J Vis Exp. (40), (2010).
- Mlynarova, L., Bauer, M., Nap, J. -P., Pretova, A. High efficiency Agrobacterium-mediated gene transfer to flax. Plant Cell Rep. 13, 282-285 (1994).
- Mu, G., et al. Genetic transformation of maize female inflorescence following floral dip method mediated by agrobacterium. Biotechnology. 11 (3), 178-183 (2012).
- Trieu, A. T., et al. Transformation of Medicago truncatula via infiltration of seedlings or flowering plants with Agrobacterium. Plant J. 22 (6), 531-541 (2000).
- Yasmeen, A., et al. In Planta transformation of tomato. Plant Mol Biol Rep. 27, 20-28 (2009).
- Zale, J. M., Agarwal, S., Loar, S., Steber, C. M. Evidence for stable transformation of wheat by floral dip in Agrobacterium tumefaciens. Plant Cell Rep. 28, 903-913 (2009).
- Zhan, X. C., Jones, D. A., Kerr, A. Regeneration of flax plants transformed by Agrobacterium rhizogenes. Plant Mol Biol. 11, 551-559 (1988).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved