Method Article
マウスの卵巣脂肪パッドに移植
要約
私たちは、女性の生殖器官の正常な形質転換上皮の研究に適した卵巣流行パッド移植アッセイを説明します。マウスの脂肪パッドは、大規模な組織片の移植を可能にする手術とイメージングのために簡単にアクセスでき、およびミュラー管由来の組織のための最も有利なネイティブ環境を提供します。
要約
Orthotopic transplantation assays in mice are invaluable for studies of cell regeneration and neoplastic transformation. Common approaches for orthotopic transplantation of ovarian surface and tubal epithelia include intraperitoneal and intrabursal administration of cells. The respective limitations of these methods include poorly defined location of injected cells and limited space volume. Furthermore, they are poorly suited for long-term structural preservation of transplanted organs. To address these challenges, we have developed an alternative approach, which is based on the introduction of cells and tissue fragments into the mouse fat pad. The mouse ovarian fat pad is located in the immediate vicinity of the ovary and uterine tube (aka oviduct, fallopian tube), and provides a familiar microenvironment for cells and tissues of these organs. In our approach fluorescence-labeled mouse and human cells, and fragments of the uterine tube are engrafted by using minimally traumatic dorsal incision surgery. Transplanted cells and their outgrowths are easily located in the ovarian fat pad for over 40 days. Long-term transplantation of the entire uterine tube allows correct preservation of all principle tissue components, and does not result in adverse side effects, such as fibrosis and inflammation. Our approach should be uniquely applicable for answering important biological questions such as differentiation, regenerative and neoplastic potential of specific cell populations. Furthermore, it should be suitable for studies of microenvironmental factors in normal development and cancer.
概要
マウスでの特定の身体部位への細胞および組織の導入を伴う移植アッセイは、組織再生および発癌の研究のために不可欠なアプローチを表します。細胞の同所性移植は、すなわち、天然の環境中へのそれらの配置は、成体幹細胞の特徴付けのために特に重要です。乳腺幹細胞の存在は、第1のマウスの腺無乳房脂肪パッドに上皮乳腺断片の移植によって示唆されました。ヒト化マウスの脂肪パッド2に移植アッセイは、ヒト初代乳房上皮細胞の再生能と正常な発達を再現するために使用しました。さらに、シリアルおよびクリア乳房脂肪パッドに、表現型の異なる細胞型の希釈移植を制限するには、自己再生能力および乳腺幹細胞3-5の多分化を試験することが重要でした。 combinatで移植アッセイ遺伝系統のトレースを持つイオンは乳腺発がん5に起源の細胞の証拠を提供しました。腎カプセル移植は、一般推定前立腺幹細胞6の特性を試験するために使用されます。正常及び腫瘍マウスおよびヒト膵臓オルガノイドの同所移植は、癌の進行7に変更された遺伝子および経路を明らかにしました。ネイティブ環境の重要性も後に、このような乳房脂肪パッド、肩脂肪パッド、および背中の皮膚8と異なる場所へ汗腺のengraftments多様な再生のデモンストレーションによってサポートされています。
腹腔および卵巣嚢は通常、女性の生殖管9-12の上皮細胞の同所移植のための場所として使用されています。これらの方法の両方は、多くの制限を有します。細胞の腹腔内注射は、腹腔の異なる領域にその注入をもたらし、それによってCOM細胞増殖を監視褶壁形成。また、微小環境の変化は、例えば、血管新生、神経支配および免疫細胞の表現の範囲として、腹腔内の異なる領域において非常に重要であり得ます。卵巣嚢は、液体のせいぜい10マイクロリットルの注入を可能にする、非常に限られた容積を有します。これは大幅に投与することができる細胞の量を制限します。また、卵嚢への注射は非常に技術的に挑戦することができ、手順はかなりの時間を必要とします。
これらの制限に対処するために、我々は、卵巣の脂肪パッドの特性を利用してきました。マウスの卵巣の脂肪パッドは、大きなサイズを有し、卵巣と卵管に隣接しており、手術で簡単にアクセスできます。ウマ栄養膜は、マウスの卵巣脂肪パッド13に移植できることが報告されています。しかし、この方法の詳細は記載されませんでした。また、この私の場合は報告されませんでしたTHODは成体細胞および組織に適用することができます。ここでは、女性の生殖器官のマウスおよびヒト細胞の移植のための信頼できる方法を説明し、この方法は、長期の臓器移植にも適用可能であることを示しています。
プロトコル
記載されている全てのin vivoでの作業は、コーネル大学の施設内動物管理使用委員会によって承認されています。
卵巣の脂肪パッドのアッセイのための1.サンプルの準備
- プライマリ卵管上皮の単離および培養(TE)細胞
- COにより8週齢の処女βアクチン強化緑色蛍光タンパク質(EFGP)またはβアクチンディスコソマ赤色蛍光タンパク質(DsRedの)マウスに頸椎脱臼に続いて2投与を供与6-安楽死させます。つま先のピンチによって成功した安楽死を確認します。
- 吸収性ドレープの個々のマウスを置き、腹側を上にしてから、70%エタノールで腹部を拭いてください。身体正中線で横切開を行うことで、指先がマウスの頭部と尾部に向かって切開部の上下に皮膚を引っ張ると皮膚を開きます。
- 鈍ピンセットを用いて腹膜を持ち、体腔を開くために細かいハサミでカットしてください。ゆっくりintestinのコイルをプッシュ脇電子と生殖器官を見つけます。
- 細かい鉗子で1子宮角をピックアップし、子宮角が分離点以上0.5cmにカット。子宮角を保持しながら、子宮角、卵管、卵巣および卵巣の脂肪パッドに取り付けられた結合組織を離れて解剖。 6ミリリットルの滅菌リン酸緩衝生理食塩水(PBS)で皿に解剖生殖器官を置きます。第二の生殖器官に進みます。
- バイオセーフティキャビネットに皿を移し、6ミリリットル滅菌PBSで組織を3回洗浄します。バイオセーフティキャビネットにある解剖顕微鏡下での作業を続行します。細かいピンセットで子宮角をつかみ、子宮卵管接合部で切断することによって卵管から子宮角を切断します。 25 G針を使用して卵巣を囲む卵嚢を切り取ります。
注:卵巣嚢を除去した後、切開が完了すると、個々の卵管にPBS溶液中に残ります。 - SINGLを転送3.5センチメートル皿にPBSの50μlのドロップでの電子の卵管と28ゲージの針を使用して、0.1ミリメートル片にミンチ。 200μlの消化緩衝液1(ダルベッコ改変イーグル培地300ユニットml -1のコラゲナーゼおよび100ユニットml -1のヒアルロニダーゼを補った(DMEM)F12(ハム)培地)に移し、5%CO中で37℃で1時間インキュベート2インキュベータ。
- インキュベーション後に1mlのを0.25%トリプシン - エチレンジアミン四酢酸(EDTA)を添加し、3分間、1mLのピペットチップ(別名ブルーチップ)の助けを借りて20倍溶液を中断する。 (ハム)培地は、2%ウシ胎児血清を含む5ミリリットル+ 4°C DMEM / F12を追加します。
- ((ハム)媒体は7ミリグラムml -1のディスパーゼIIおよび10μgml -1のデオキシリボヌクレアーゼIを補充し、遠心分離(600 RCF、5分間、室温(RT))、によって組織を収集し、1ミリリットルの消化緩衝液2(DMEM F12キーを追加します。 DNアーゼI))。 1ミリリットルピペットTIの助けを借りて、組織ペレットを20回サスペンドP。
- 5ミリリットルの無血清完全なマウス卵管上皮成長培地(M-TE-GM、表1)を追加します。
- 遠心分離(600 RCF、5分、RT)によって細胞を収集します。中断し、血球計数器により細胞をカウントし、1ミリリットルM-TE-GMを追加します。シード1×10 5 24ウェル低接着プレートでウェルあたり1ミリリットル中の細胞と4日間、5%CO 2インキュベーター中37℃でM-TE-GMでインキュベートします。
- 毎日培地を変更します。
- βアクチン-EGFPまたはβアクチンのDsRedマウスから培養された一次懸濁液TE細胞の単一細胞懸濁液を準備します。
- 24ウェル低接着プレートからTE懸濁培養物を収集します。遠心分離(600 RCF、5分、RT)、そして1mlの0.25%トリプシン-EDTAで細胞ペレットを懸濁します。 5%CO 2インキュベーター中、37℃で10分間インキュベートします。
- 5%ウシ胎児血清を含む(ハム)培地を5ミリリットルのDMEM / F12を追加することにより、トリプシン活性を停止します。遠心分離(600 RCF、5分、RT)によって細胞ペレットを収集します。
- 洗浄細胞ペレットを冷PBSで2回(4°C)の4ミリリットルで、細胞ペレットあたり1mlのPBSを追加し、一時停止します。血球計数器により細胞をカウントし、1.7ミリリットルの遠心分離管に移します。氷の上で作業し、10μlのPBSに1×10 5個の細胞を追加し、その後、10μlの基底膜マトリックスを追加します。動物室に氷上でサスペンドと輸送。
注意:滅菌条件下でバイオセーフティキャビネット内のすべての解剖および組織培養作業を実行します。
- 不死化ヒト細胞株の作製
- 別に成長レンチウイルス-EGFPと-mCherry標識ヒト不死化卵巣表面上皮細胞lineHIO118は80時まで- 5%CO 2インキュベーター内で37℃で10センチの皿に90%の密集度。
- 10 mlのPBSで二回洗浄皿、皿毎に1 mlの0.25%トリプシン-EDTAを添加し、5%CO 2インキュベーター中で37℃で10分間インキュベートします。 10 mlのDMEM / F12 5%ウシ胎児血清を含む(ハム)培地を添加することにより反応を停止させます。収集します遠心分離により細胞ペレット(600 RCF、5分、RT)。
- 洗浄細胞ペレットを冷PBSで2回(4°C)10mlで、細胞ペレットあたり1mlのPBSを追加し、一時停止します。血球計数器により細胞をカウントし、1.7ミリリットルの遠心分離管に移します。
- 氷の上で作業し、1.0×10 6レンチ-mCherryを標識細胞+ 1.0×10 6レンチ-EGFPは、10μlのPBSに細胞を標識した追加します。 10μlの基底膜マトリックスを追加します。動物室に氷上でサスペンドと輸送。
- 卵管の調製
- 1.1.1-1.1.5の手順で説明するように、6-から、PBS中の8週齢の処女βアクチンのDsRedマウスに個々の子宮管を解剖。解剖顕微鏡下で200μlのPBSのドロップに単一の子宮管を転送します。そっと卵管間膜、卵管のセグメントをサポートする広範な靱帯の部分を除去することにより、ピンセットと28ゲージの針の助けを借りて、子宮管をほどきます。 2のドロップで単一の非コイル状子宮チューブを入れます00μlの氷冷PBS受信者の卵巣の脂肪パッドが露出し、移植を受けるために準備されるまで。
2.卵巣の脂肪パッド移植
注:各動物の手術の間に器具を消毒します。事前にすべての機器を準備し、手配。これは脾臓を回避するように、右側の卵巣の脂肪パッドに背移植が優遇されています。ただし、受信者は両方の卵巣の脂肪パッドで移植を有することができます。
- 初代細胞のレシピエントとして同系マウスまたは重症複合免疫不全(SCID /のNCr)マウスを使用してください。ヒト細胞のようなHIO118細胞、使用NOD / SCID /γ(NSG)マウスまたはSCIDマウスの場合。
- 0.15ミリリットル/ 10g体重の用量で2,2,2-トリブロモエタノールの単一腹腔内注射でレシピエントマウスを麻酔。動物のフードに、加熱パッド上で動物を置き、ペダル反射(つま先ピンチ)の損失によって適切な麻酔を確認します。しばらく乾燥を防ぐために、目に獣医軟膏を適用します。動物は麻酔下です。術後疼痛のために治療するために、4ミリグラム/ g体重の用量で鎮痛剤ケトプロフェンと動物の皮下に注入します。
注:別の方法として、麻酔のためにイソフルランを使用しています。誘導室で動物を置き、0.8から1.5 L /分で2〜3%のイソフルラン気化器に酸素流量計を調整します。チャンバーから麻酔した動物を削除し、それがマスクからイソフルランを呼吸し、手術を開始した後、1.5%に0.4〜0.8リットル/分およびイソフルラン気化器に酸素流量計を設定してみましょう。 - #40バリカンで手術領域を剃ります。エリアから毛を取り除く2回手術領域、70%エタノールに続いポビドンヨードの3消毒スクラブで剃毛した皮膚を準備し、滅菌ドレープでカバー。
- バイオセーフティキャビネットにある解剖顕微鏡下で動物を移動します。直接卵巣の脂肪パッド上記背内側の位置で切開することにより生殖器官を公開します。
注:クリティカルiCalのステップ:正確な皮膚切開は創傷治癒を促進し、メスの使用は、ステップ2.4で推奨されています。 - 鈍細かい鉗子を使用すると、神経や主要な血管へのダメージを最小限に抑え、正中線に向かって切開によって慎重に卵巣の脂肪パッドを引き出します。
重要なステップ:出血が発生した場合は、手術を中止し、別の宿主動物に移植することを検討してください。 - 28ゲージベベル針の助けを借りて、解剖顕微鏡の制御下で3〜4ミリメートル卵巣の上に、卵巣の脂肪パッドに2〜4ミリメートルの深い切開を行います。
重要なステップ:切開だけ脂肪パッドの半分を通過していることを確認してください。底面までのすべての方法を穿刺して、漏れが発生します。迅速であることと、この工程の後遅滞なく進行します。 - 細胞移植のために、細胞基底膜マトリックス混合物の10から20μlのシリンジ(30ゲージの針)を記入し、脂肪パッドの切開部に注入します。卵管移植の場合、卵管のウィットを拾いますH細かい鉗子と10での場所 - 20μlの基底膜マトリックスは、氷上に保持しました。 0.1〜10/20μLをUsing XLは(3ミリメートル短縮)フィルターチップtissueと基底膜マトリックスサスペンションをピックアップし、脂肪パッド切開への放出を卒業しました。
- 基底膜マトリックスが固化し、バック腹膜への生殖器官を配置するための5分待ちます。 2外科手術用縫合糸のstichesと2小傷クリップまたは縫合糸で皮膚と筋肉を閉じます。
- 繰り返して、コントロールとなる動物の対側脂肪パッドにPBS-基底膜マトリックス混合物を移植するために2.4から2.8を繰り返します。
重要なステップ:熱損失は、麻酔したマウスで急速であるため、手術後、加熱パッド上に動物を配置します。 - 動物が本来のケージに加熱パッド上で回復し、麻酔から完全に目を覚ましまで動物を観察してみましょう。それは胸骨を維持するのに十分な意識を取り戻したまで無人の動物を放置しないでくださいリットルの横臥。完全に回復するまで、他の動物の会社に手術を受けた動物を返さないでください。
- 手術後のケージの上に食べ物を乾燥させるだけでなくケージの中にプリウェットフードペレットの一握りを置きます。必要に応じて、次の数日間、術後の鎮痛剤を適用し、毎日の傷を調べます。創傷感染が発生した場合、承認された動物プロトコルに従って抗生物質を適用します。傷が完全に閉じていたときに、10日手術後の創傷クリップを削除します。
3.組織学および画像取得
- グラフト収集と保存
- 26ミリリットルのddH 2 Oで4ミリリットル10×PBSおよび10ミリリットル16%パラホルムアルデヒド溶液を混合することにより、4%パラホルムアルデヒド溶液を準備します。
- 手順で説明するように、1つのブロック、移植した卵巣の脂肪パッド、卵巣、卵管0.5センチ子宮内解剖1.1.1-1.1.4。すぐに2ミリリットルの4%パラホルムアルデヒド中に入れ、室温で、2時間固定します。同じ動物から、非生着解剖対照としてPBS-基底膜マトリックス混合物を移植した反対側の卵巣の脂肪パッドシステム(ステップ2.9参照)。同じように修正して、プロセス。
- 固定の洗浄の後5分間、PBSで3回組織し、4℃でPBS中で一晩インキュベートします。
- 卵巣の脂肪パッドのホールマウントイメージングのために3.2.1に進みます。
注:画像取得組織を凍結(3.3.1)またはパラフィン包埋(3.3.2)のために処理することができた後。 4℃でPBS中30%スクロース中で一晩インキュベートし、凍結組織の品質を改善します。
- 画像収集
- 落射蛍光アタッチメントおよび高精細カラーカメラ4と、10倍対物レンズ、蛍光取り付け、カラーカメラとプランを備えた実体顕微鏡を備えた倒立顕微鏡を用いてPBS充填皿と、画像内の卵巣の脂肪パッドシステム全体マウント配置アポ1xWD70、EDプラン1.5xWD45目標。
- 組織学
- 以下ホールマウント画像取得(3.2.1)実験用フィルムの2×1cmの片に凍結組織標本のための媒体を埋め込み、鉗子を使用しての200から500μlのドロップを置き、ドロップに組織を移します。一方の縁でフィルムをピックアップし、1.8ミリリットルの低温バイアルに組織培地ドロップを転送します。バイアルを閉じて、液体窒素に突入。 -80℃で凍結組織を保管してください。
- 代わりに、標準的なパラフィン包埋を進めます。ステップごとに組織容積の20から40のボリュームを使用してください。
- 室温で穏やかに振盪しながら、30分間に一度65%エタノールで組織を浸し。
- 室温で穏やかに振盪しながら、30分間に一度、70%エタノールで組織を浸し。この段階で、サンプルを室温でヶ月間保存することができます。
- 室温で穏やかに振盪しながら、30分間に一度90%エタノールで組織を浸し。
- 室温で穏やかに振盪しながら、30分間に一度、95%エタノールで組織を浸し。
- 室温で穏やかに振盪しながら、30分間無水エタノール(200プルーフ)で二回組織を浸し。 <李>は室温で穏やかに振盪しながら、30分間、クロロホルムで二回組織を浸し。
- 58℃で穏やかに振盪しながら、30分間パラフィンに一度組織を浸し。
- 58℃で穏やかに振盪しながら、12時間、パラフィンに一度組織を浸し。
- 58℃で、3時間、パラフィンに一度組織を浸します。
- 金属組織学金型内の組織を置き、58℃のパラフィンと金型を埋めます。パラフィンの上にプラスチック製の組織学カセットを追加し、4℃にパラフィンをクールダウン。 RTでパラフィン組織ブロックや店舗を抽出します。
注:パラフィン温度は、免疫組織化学染色に適した組織の最適な保存のために58℃を超えてはなりません。
- また、検体処理ジェルとパラフィン包埋のために準備します。
- PBSを吸引し、70%エタノールにホールマウント組織を移します。 2時間室温でインキュベートします。水浴中、60℃に予熱検体処理ゲル中。
- Pipett実験用フィルムライニングペトリ皿上に検体処理ゲルのE 200μL。細かい解剖鉗子を使用すると、検体処理ゲルドロップにホールマウント組織システムを転送します。
- 検体処理ゲルプラグは室温で固化、または4℃で10分間のプラグを固化することができます。
- 生検フォームパッドの間に挟まれた組織学組織カセット内の検体処理ゲル包埋組織を置きます。ステップ3.3.2-3.3.2.10のようにパラフィンに埋め込みます。
注意:試料の処理ゲル埋め込みが損失を防止し、小さな脆弱な組織サンプルの保存を可能にします。
注:凍結またはパラフィン包埋によって保存組織は、免疫組織化学染色14,15に適しています。
結果
実験的細胞および組織を正確に解剖顕微鏡( 図1)の下で卵巣脂肪パッドに移植することができます。例としては、遍在EGFP( 図2A)またはDsRedの( 図2B)とHIO118 16,17細胞はmCherryをし、EGFPレンチウイルスで標識したヒト不死化卵巣表面上皮細胞( - F 図2C)を発現するマウス由来の初代マウス卵管上皮細胞が含まれます。アプローチはまた、マウスの卵管などの臓器の長期移植、( 図3)に適用可能です。免疫組織化学染色によると、(FOXJ1正14)繊毛および分泌の両方(PAX8正15)細胞が移植された組織( 図3DおよびE)の卵管上皮に保存されています。

図1:卵巣の脂肪パッド移植移植の(A)露出面積(矢印)。 (B)切開は28 G針(矢印)によって行われます。ピペットチップ(矢印)により、(C)UT /基底膜マトリックス混合物の生着。 (D)UT生着(矢印、明るい赤、βアクチンのDsRedマウスのUT)。 FP、脂肪パッド。 OV、卵巣; UT、卵管。スケールバー= 2ミリメートル。 この図の拡大版をご覧になるにはこちらをクリックしてください。
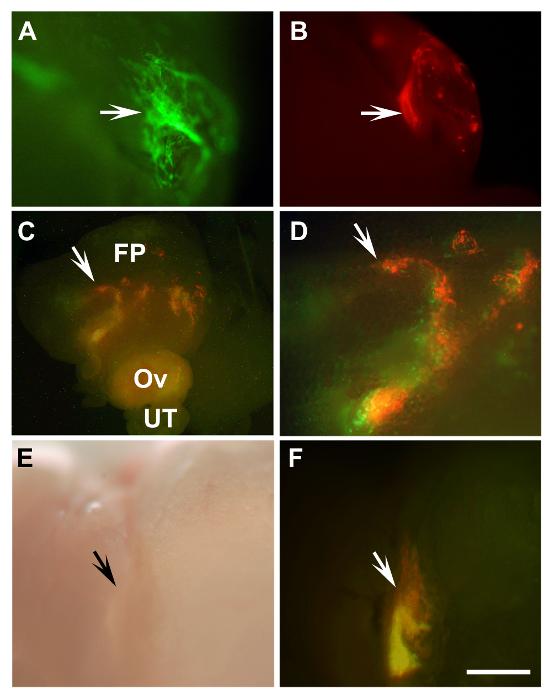
図2: 移植マウスプライマリ卵管上皮細胞の検出と人間が卵巣表面上皮細胞を不死化 (A、B)アウト。 8日同系マウスに移植した後、一次βアクチン-EGFPマウス (緑A)のマウス卵管上皮細胞(矢印)およびβアクチンのDsRed(B、赤)の成長。 (C、D)は、10日目移植後NSGマウスにレンチEGFP(緑色)またはレンチmCherryを(赤)のいずれかで標識された混合HIO118細胞(矢印)のEngraftments。 (D)(C、矢印)から拡大エリア。 (E、F)グラフトは、SCIDマウス(矢印)にD、Cのように43日、同じ細胞の移植後に発症しました。 AD、F、蛍光。 E、明視野、FP、脂肪パッド。 OV、卵巣; UT、卵管。 (A、B、DF)スケールバー=500μmの。 (C)スケールバー= 1600ミクロン。 この図の拡大版をご覧になるにはこちらをクリックしてください。
広告/ 54444 / 54444fig3.jpg "/>
図3: 卵管移植のキャラクタリゼーション。 (A)βアクチン-DsRedをマウス6日卵巣の脂肪パッドに移植した後の完全な卵管(矢印)(矢印を、明るい赤)。 (B)(A)に示される移植で脂肪パッドの蛍光凍結切片。レッド、のDsRed。ブルー、4 '、6-ジアミジノ-2-フェニルインドール(DAPI)、核対比染色。 (C)40日NSGレシピエントマウス(矢印)への移植後の子宮管移植片(矢印)。パラフィン切片。正しいすべての原則卵管コンポーネントの保存、および移植関連線維症および炎症性の欠如に注意してください。ヘマトキシリンおよびエオシン染色。 (D、E)検出卵管上皮マーカーペアボックス遺伝子8(PAX8)とフォークヘッドボックスJ1の(FOXJ1;茶色の核の色、矢頭)に示すグラフト(矢印)の細胞内で( C)。イムノシステム。メチルグリーンで対比染色。 FP、脂肪パッド。 OV、卵巣; UT、卵管。 (A)スケールバー=1000μmで。 (B)スケールバー=200μmの。 (CE)のスケールバー=100μmである。 この図の拡大版をご覧になるにはこちらをクリックしてください。
| 成分 | 1×DMEM F12(ハム)培地 |
| L-グルタミン | 2 mMの |
| ナトリウムpruvate | 1 mMの |
| 上皮成長因子 | 10 ngのmlの-1 |
| 塩基性線維芽細胞成長因子-2 | 10 ngのmlの-1 |
| ヒドロコルチゾン | 500 ngのmlの-1 |
| インスリン | 5μgのmlの-1 |
| トラnsferrin | 5μgのmlの-1 |
| 亜セレン酸ナトリウム | 5 ngのmlの-1 |
| ウシアルブミン | 0.10% |
| ペニシリン/ストレプトマイシン | 100単位ミリリットル-1 /100μgのミリリットル-1 |
| 最小必須培地イーグル(MEM)非必須アミノ酸 | 0.1 mMの |
| β-メルカプトエタノール | 10 -4 M |
表1:マウスの卵管Epithelim増殖培地(M-TE-GM)コンポーネント左の列に表示されているが、1×DMEM F12を示した濃度の(ハム)培地、右欄に溶解されています。最終的な培地組成は、無血清です。
ディスカッション
我々は、上皮細胞や組織の正確な配達および検出を可能にする卵巣の脂肪パッド移植アッセイを確立しています。卵巣の脂肪パッドアッセイ移植手順はintrabursal注入10-12未満技術的に困難であり、より均一で腹腔内注射9と比較して、移植された細胞の正確な位置を可能にします。それはまた、卵管などの臓器全体の長期移植に適しています。
重要なことは、卵巣の脂肪パッドは、女性の生殖器系の上皮のためのおなじみの微小環境を提供します。これは、再生および悪性形質転換の間に、ヒトおよびマウスの卵巣と卵管上皮細胞の分子および細胞特性の研究のために特に適していなければなりません。他の器官とは対照的に、いくつかの研究は、女性Rの上皮幹細胞の同定および特徴付けに焦点を当てていますeproductive管18,19。多くの癌は、成体幹細胞20に由来すると考えられるので、このような試験は特に重要です。しかし、上皮性卵巣癌の細胞の起源は、18非常に議論の余地が残ります。上皮性卵巣癌は、卵巣癌の大部分を占めると米国21の女性の全ての癌関連死の中で5位にあります。したがって、既存の移植技術に比べていくつかの利点を持つ同所アッセイの開発9-12が大幅にこの分野での研究を促進すべきです。
卵巣の脂肪パッドの表面的な場所を考えると、小動物イメージングシステムは、強い蛍光または生物発光レポーターで標識されたengraftmentsをフォローアップするために使用することができます。また、このような非線形顕微鏡22のような低侵襲性の高解像度ライブイメージングアッセイを確立することが可能であるべきです。卵巣の脂肪パッドも器官培養で維持することができ、それによって可能密接に細胞の組織と細胞外マトリックスを反復する条件の下で正常及び腫瘍性上皮の三次元培養をる。今後の研究では、これらの有望な可能性に対処すべきです。
いくつかの重要なステップを考慮しなければなりません。加熱パッドを提供し、手術中に暖かいげっ歯類を維持することが大幅に生存率を向上させます。脂肪パッドを扱う機器の無菌性は、移植されたシステムが無菌に保たれることが保証されます。我々の経験では、重大な出血は、移植の成長遅延をもたらします。重要なのは、脂肪パッドの切開が正確に脂肪パッドを引き裂くまたは出血の原因を介して穿刺するためなされるべきです。凝固剤は、必要に応じて出血を止めるために使用されるべきです。発達しないengraftments場合、注入された細胞のより高い濃度を考慮すべきです。最初に成功した派生物は、移植後1週間早けれとして観察され、最も目に見えるものでなければならないengraftmentsすることができます手続き後の月。移植のために、より大きな直径(23-25 G)を有する針は、大きなセル(直径10μm程度以上)の剪断を防止するために使用することができます。しかしながら、そのような針は、脂肪パッドに、より外傷性であってもよく、それらの使用は、事前に試験されるべきです。我々の実験のために我々は6〜8週齢のドナーとレシピエントマウスを使用しています。両方の目的のために、若いまたは古いマウスを使用することができます。しかし、注入した細胞の数を調整する必要があります。若年ドナーにおける卵巣の脂肪パッドの小型化も考慮される必要があります。
いずれの方法と同様に、マウスの卵巣の脂肪パッド移植アッセイのいくつかの制限があります。同系免疫適格マウスは、マウス初代細胞/組織のために使用することができますが、私たちの技術は、人間の体の移植のためのNSGまたはSCIDマウスが必要です。ヒト上皮細胞の増殖を支持するために脂肪パッドをヒト化することが可能と思われます。しかし、我々はまだこのアプローチをテストしていません。若いFEの使用男性は下繁殖コストをリードすることができ、しかし、成熟した処女雌マウス(年齢8〜10週間)は、それによって、より大きな標本の移植を可能にする、より大きな脂肪パッドを持っています。最後に、実験者は、手順のタイムリーで正常に実行されたことを確実にするために、動物の手術で訓練する必要があります。
開示事項
The authors have nothing to disclose.
謝辞
我々は、ヒト細胞HIO118を提供するために、博士アンドリューK.ゴドウィン、カンザス大学メディカルセンターに感謝したいと思います。 (; T028095 NYSTEM)と子の健康とAFNの人間開発(P50HD076210)の健康/国立研究所の国立研究所、およびNYSTEM(C028125、C024174からの助成金によってこれらの研究は、ニューヨーク幹細胞プログラムからの助成金によってサポートされていましたT028095)、アインへの健康/国立癌研究所(CA182413)および卵巣がん研究基金(327516)の国立研究所。
資料
| Name | Company | Catalog Number | Comments |
| 25 gauge needle | BD Becton Dickinson | 305122 | |
| 28 gauge needle (hypodermic syringe with attached needle) | Kendall | 30339 | Part Number: 8881500014 |
| basic fibroblast growth factor-2 | Sigma-Aldrich | F9786 | |
| basement membrane matrix (Geltrex) | Invitrogen | A1413202 | |
| β-actin-DsRed mice | The Jackson Laboratory | 6051 | B6.Cg-Tg(CAG-DsRed*MST)1Nagy/J |
| β-actin-EGFP mice | The Jackson Laboratory | 3291 | C57BL/6-Tg(CAG-eGFP)1Osb/J |
| β-mercaptoethanol | Sigma-Aldrich | M7522 | |
| bovine albumin | Sigma-Aldrich | A3311 | |
| chloroform | VWR | EM-CX1058-1 | |
| collagenase/hyaluronidase | Stem Cell Technologies | 7912 | |
| cryogenic vials | Thermo Scientific Nunc | 377267 | |
| dispase II | Worthington | NPRO2 | |
| DMEM F12 (HAM's) | Corning | 10-092-CV | |
| DNaseI (Deoxyribonuclease I) | Stem Cell Technologies | 7900 | |
| embedding medium for frozen tissue specimens (O. C. T.) | Sakura Finetek | 4583 | |
| epidermal growth factor | Sigma-Aldrich | E4127 | |
| ethanol 200 proof | Koptec | V1001 | to prepare 70% |
| fetal bovine serum | Sigma | F4135 | |
| filter tip 0.1-10/20 µl XL | USA Scientific | 1120-3810 | |
| FOXJ1 antibody | eBioscience | E10109-1632 | used at concentration 1:1,000 (no unmasking) |
| hydrocortisone | Sigma | H0135 | |
| Ketoprofen | Zoetis | 4396H | |
| laboratory film (Parafilm M) | American National Can | PM-999 | |
| L-Glutamine | Corning | 25-005-Cl | |
| insulin-transferin-sodium selenite | Sigma-Aldrich | I884 | |
| isoflurane, 250 ml | Santa Cruz Animal Health | sc-363629Rx | |
| low attachment plate 24-well | Costar | 3473 | |
| MEM non-essential amino acids | Corning | 25-025-Cl | |
| metal histology molds | Electron Microscopy Sciences | 62527-22 | |
| microscope, inverted | Nikon | Eclipse TS 100 | |
| microscope, stereo | Nikon | SMZ800 | |
| Nod/SCID/gamma (NSG) mice | The Jackson Laboratory | 05557 | NOD.Cg-PrkdcscidIl2rgtm1Wjl/SzJ |
| paraformaldehyde 16% solution | Electron Microscopy Sciences | 15710 | |
| paraffin (Paraplast, X-TRA) | Fisher Thermo Scientific | 23-021-401 | |
| PAX8 antibody | Proteintech | 10336-1-AP | used at concentration 1:1,000 (no unmasking) |
| PBS (Phosphate-Buffered Saline) | Corning | 21-030-CV | |
| penicillin streptomycin | Corning | 30-002-Cl | |
| severe combined immunodeficiency (SCID/NCr) mice, BALB/C background) | NCI-Frederick Animal Production Program | 01S11 | |
| sodium pyruvate | Corning | 25-000-Cl | |
| specimen processing gel (HISTOGEL) | Richard-Allan Scientific | HG-4000-012 | |
| sucrose | Sigma-Aldrich | S0389 | |
| Trypsin-EDTA, 25% | Corning | 25-053-Cl |
参考文献
- Deome, K. B., Faulkin, L. J., Bern, H. A., Blair, P. B. Development of mammary tumors from hyperplastic alveolar nodules transplanted into gland-free mammary fat pads of female C3H mice. Cancer Res. 19, 515-520 (1959).
- Proia, D. A., Kuperwasser, C. Reconstruction of human mammary tissues in a mouse model. Nature protocols. 1, 206-214 (2006).
- Shackleton, M., et al. Generation of a functional mammary gland from a single stem cell. Nature. 439, 84-88 (2006).
- Stingl, J., Caldas, C. Molecular heterogeneity of breast carcinomas and the cancer stem cell hypothesis. Nat Rev Cancer. 7, 791-799 (2007).
- Koren, S., et al. PIK3CA(H1047R) induces multipotency and multi-lineage mammary tumours. Nature. 525, 114-118 (2015).
- Nikitin, A. Y., Nafus, M. G., Zhou, Z., Liao, C. -. P., Roy-Burman, P., Bagley, R. G., Teicher, B. A. Prostate stem cells and cancer in animals. Stem Cells and Cancer. , 199-216 (2009).
- Boj, S. F., et al. Organoid models of human and mouse ductal pancreatic cancer. Cell. 160, 324-338 (2015).
- Lu, C. P., et al. Identification of stem cell populations in sweat glands and ducts reveals roles in homeostasis and wound repair. Cell. 150, 136-150 (2012).
- Flesken-Nikitin, A., et al. Ovarian surface epithelium at the junction area contains a cancer-prone stem cell niche. Nature. 495, 241-245 (2013).
- Orsulic, S., et al. Induction of ovarian cancer by defined multiple genetic changes in a mouse model system. Cancer Cell. 1, 53-62 (2002).
- Dawes, J., Liu, B., Mars, W., Michalopoulos, G., Khillan, J. S. Multiple ovarian transplants to rescue a transgenic line of mice. Lab Anim (NY). 39, 191-193 (2010).
- Cordero, A. B., Kwon, Y., Hua, X., Godwin, A. K. In vivo imaging and therapeutic treatments in an orthotopic mouse model of ovarian cancer. Journal of visualized experiments : JoVE. , (2010).
- Albihn, A., et al. Production of capsular material by equine trophoblast transplanted into immunodeficient mice. Reproduction. 125, 855-863 (2003).
- Muthusamy, N., Vijayakumar, A., Cheng, G., Ghashghaei, H. T. A knock-in Foxj1(CreERT2::GFP) mouse for recombination in epithelial cells with motile cilia. Genesis. 52, 350-358 (2014).
- Perets, R., et al. Transformation of the fallopian tube secretory epithelium leads to high-grade serous ovarian cancer in Brca;Tp53;Pten models. Cancer Cell. 24, 751-765 (2013).
- Capo-Chichi, C. D., et al. Dynamic alterations of the extracellular environment of ovarian surface epithelial cells in premalignant transformation, tumorigenicity, and metastasis. Cancer. 95, 1802-1815 (2002).
- Roland, I. H., et al. Loss of surface and cyst epithelial basement membranes and preneoplastic morphologic changes in prophylactic oophorectomies. Cancer. 98, 2607-2623 (2003).
- Flesken-Nikitin, A., Odai-Afotey, A. A., Nikitin, A. Y. Role of the stem cell niche in the pathogenesis of epithelial ovarian cancers. Mol Cell Oncol. 1, 963435 (2014).
- Ng, A., Barker, N. Ovary and fimbrial stem cells: biology, niche and cancer origins. Nat Rev Mol Cell Biol. 16, 625-638 (2015).
- Visvader, J. E. Cells of origin in cancer. Nature. 469, 314-322 (2011).
- Siegel, R. L., Miller, K. D., Jemal, A. Cancer statistics, 2015. CA Cancer J Clin. 65, 5-29 (2015).
- Williams, R. M., et al. Strategies for high-resolution imaging of epithelial ovarian cancer by laparoscopic nonlinear microscopy. Transl Oncol. 3, 181-194 (2010).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved