Method Article
ネイティブ、タグなしの Huntingtin Exon1 モノマーと相撲の融合戦略を使用して線維の生成
要約
ここでは、ネイティブなタグ無料モノマーのミリグラム量と小さなユビキチン関連修飾子 (相撲) の一時的な融合に基づくハンチンチン蛋白質 (Httex1) の exon1 の線維の生産のための堅牢な最適化されたプロトコルを提案する.
要約
ハンチントン病 (HD) CAG 拡張 (≥36) によって引き起こされる継承された致命的な神経変性疾患 HD 遺伝子の最初のエクソンの Huntingtin 蛋白質 (Htt) の式の結果、N 末端フラグメントそのポリグルタミン (polyQ) ストレッチ。
Huntingtin 蛋白質 (Httex1) の exon1 携帯で HD の機能の多くを繰り返す最小 Htt フラグメント、動物モデル、Htt の最も広く研究の断片の一つ。Httex1 の小型サイズになります実験生物物理特性より長いフラグメントまたはフルレングス Htt と比較して標準的な高解像度技術を使用してに従う義務があります。ただし、高凝集傾向変異体 Httex1 の (mHttex1) 増加 polyQ コンテンツ (≥42) で困難になっている効率的な式と十分な量のこれらの蛋白質を生産し、それらをアクセシブルにする浄水システムを開発するには融合蛋白質や蛋白質のネイティブのシーケンスを変更するその他の戦略を使用せずさまざまな分野からの科学者。堅牢かつ最適化されたメソッドをここで提案するネイティブのミリグラム単位の微量の生産のためタグ-無料 Httex1 小さなユビキチン関連修飾子 (相撲) の一時的な融合に基づきます。シンプルさと戦略の効率、Httex1、従ってこのタンパク質を研究者をよりアクセシブルにして異なる研究室の実験の再現性を向上のネイティブでないシーケンスを使用する必要はありません。これらの進歩も Htt と同様新規診断ツールの開発と治療治療または HD の進行を遅らせるの構造機能相関の解明を目指した今後の研究を容易にすることと考えています。
概要
Htt は 348 kDa タンパク質であり、いくつかの生理学的機能1に関与しています。Htt 以上 36 N 末端残基の拡張 polyQ 地域を含む、HD2,3が発生します。HD の病理学は、線条体、大脳皮質神経細胞死や影響を受ける組織4、5の萎縮につながる細胞介在物によって特徴付けられます。PolyQ 繰り返し管を含むいくつかの N 末端 Htt フラグメントは HD 患者の死後脳で検出され、huntingtin 蛋白質6のプロテアーゼによるプロセシングによって生成されると考えられています。最近の研究は、Httex1 が異常 mRNA スプライシングにより形成されることもお勧めします。病理学的 polyQ 変異を含み、動物の過剰発現 HD7、従って HD 病理と病の進行で6、このフラグメントの可能性の中心的役割を強調表示の主要な機能の多くを要約することができます Httex1 8,9。
高集計性向変異体 Httex1 (mHttex1) 拡張 polyQ 管と、ため既存式システムの大半はタンパク質 Httex1 の一時的な融合に基づいています (グルタチオン-S-トランスフェラーゼ (GST)、チオレドキシン (TRX) などやマルトース結合タンパク質 (MBP) やその表現、安定性、浄化および溶解度10、11,12,13,14 を向上させる特異的ペプチド (ポリ ヒスチジン) ,,1516,17,18,19,20,21,22,23 ,24,25,26,,2728。フュージョン パートナー、プロテアーゼ トリプシンなどの胸の谷間サイトを含む短いシーケンスと Httex1 にリンクして、タバコ etch ウイルス (TEV) プロテアーゼまたは胸の谷間と集計の開始前に Httex1 のリリースを許可する PreScission または浄化。これらのメソッドの欠点は、痕跡を残さない非胸の谷間のため追加残基と不完全な胸の谷間 (のための不均一性に加え Httex1 のシーケンス内での miscleavage により切り捨てられたフラグメントの作成を残しての可能性Viewegらの利点と制限事項このアプローチの詳細についてを参照してください)10.これらの制限に対処するため、我々 は最近コンストラクトの一時的な N 末端融合を用いた初めてのネイティブ タグ無料 Httex1 の生成を有効にする表現戦略を開発(Ssp)Httex110DnaB インテイン。インテイン胸の谷間は痕跡を残さないと特定蛋白質の mg 量が得られます、それまだ収量を減らすことができる 2 つの欠点に苦しむ: 式とで胸の谷間が発生するという事実の間に起こることができるインテインのすなわち、早すぎる胸の谷間特に拡張 polyQ 繰り返しで Httex1 の凝集による蛋白質の損失につながる可能性がいくつかの時間。
これらの制限に対処するため、ネイティブの生産のための我々 の戦略を絞り込むことに、相撲、Httex1 に酵母ホモログ Smt3 もっと丁度の一時的な融合に基づく新しい式システムを開発私たちタグ無料 Httex1。組換え蛋白質の生産のため相撲システムのアプリケーション 2004年29式の増加率と相撲融合タンパク質の溶解度を示した発表されました。相撲タグはユビキチン様タンパク質特定プロテアーゼ 1 (ULP1)、認識サイトを必要としないが、相撲の三次構造を認識し、miscleavage30の可能性を実質的に排除を切断することができます。さらに、ULP1 を介した胸の谷間は高速であり、痕跡を残さないと追加残余を残すありません。融合タグの早すぎる胸の谷間10自触媒インテインと完全に外部プロテアーゼの要件から敬遠です。相撲戦略は組換えタンパク質生産31,32,33で広く使用されますが、我々 は、不調である本質的の生成のために特に便利だ本稿で示すHttex1 のような集計が発生しやすいので、アミロイド蛋白質。シンプルさ、効率、相撲 fusion ベース手法の信頼性がネイティブなタグ無料 Httex1 をさまざまな分野からの研究者によりアクセスして Httex1の in vitroのネイティブでないシーケンスを使用する必要があることと考えています.これは、Httex1 の構造機能相関の解明に今後研究を容易にする重要な前進です。
プロトコルは細菌文化、12 L から Httex1 の浄化を記述が、プロトコルが小さいまたは大きいスケールの生産のため簡単に合わせることができます。プロトコル (23Q) 下 polyQ リピート長変異体 Httex1 と野生型 Httex1 (wtHttex1) の生産を説明します (mHttex1)、polyQ を繰り返します (43 q) 上の長さ (36Q) の病原性のしきい値。
プロトコル
1. 発現組換え Httex1 23Q と 43 q
- 必要なバッファーおよび解決を準備します。アンピシリン (アンプ、100 mg/mL) 原液、フィルター (0.2 μ m)、分注、-20 ° C でストア x 1000 を準備します。ホストゲノム スープ (LB) メディアの準備 (25 g ポンドあたり 1 L H2O ミラー)、オートクレーブ。1 M イソプロピル β-D-1thiogalactopyranoside (IPTG) 原液、フィルター (0.2 μ m)、因数およびストアを準備-20 ° C で
- 化学有能なエシェリヒア属大腸菌熱ショック法34の His6 相撲 N 末端タグに融合した人間の Httex1 を含む pTWIN1 ベクトルを持つ ER 2566 B を変換します。
注:エシェリヒア属大腸菌BL21 DE3 ひずみも使用されています。ただし、この場合は切り捨ての量の増加が観察されました。 - 1 LB 培地 200 mL に接種、寒天培地の滅菌ピペット チップから単一コロニーを追加して 1 L の三角フラスコにアンプ x。30 ° C と細菌のインキュベーターで 20 時間 (夜間) 180 rpm で文化を孵化させなさい。
- 滅菌ピペットと文化の 1 mL サンプルを取る。600 の光学濃度を測定使い捨てプラスチック キュベットと光度計 (測定範囲 0.1 ~ 1、LB 培地で希釈に応じて尊重) サンプルの nm (外径600)。3 L 文化で 0.05 の開始の OD600になります清酒の量を計算 (外径 φ600の清酒 = 50 mL を意味する 3)。
- 4 つのカルチャを接種する (1 LB 培地の各 3 L 5 L フラスコでアンプ x)、滅菌ピペットによる前処理の金額を追加することによって。37 ° C および細菌のインキュベーターで 180 rpm で文化を孵化させなさい。
- 30 分毎滅菌ピペットと文化の 1 mL サンプルを取る。使い捨てプラスチック キュベットと光度計で試料の外径600を測定します。外径 φ600 (通常 1-2 時間) 後 0.1 に達している、細菌の定温器の温度を 14 ° C に設定して冷却しながら培養を継続します。30 分毎滅菌ピペットと文化の 1 mL サンプルを取る。使い捨てプラスチック キュベットと光度計で試料の外径600を測定します。
注: 文化を冷却する時間によって異なります使用、インキュベーターため冷却を開始する時刻がインキュベータの種類によって適応する必要がありますに。ただし、温度勾配の変更のみが必要収量に影響は小さい相撲融合タンパク質は、かなり安定するいると思われるようです。 - 外径600は (通常 1-2 時間) 後 0.3 0.4 に達したとき、過剰の SDS-PAGE 解析のため文化の前誘導サンプルを取る。セルの対等な量を与えるサンプル サイズを計算し、Coomassie の良い信号染色 SDS-PAGE: のために 10 もゲル: ボリューム = 0.2600を OD15 よくゲルの半分を取る。
- 外径600細菌文化 = 0.4、取る 500 μ L。滅菌ピペットで細菌培養の計算された容積を取る。スピン ・ ダウン (18000 g、4 ° C、2 分 x) サンプルと上澄みを廃棄します。解析 (ステップ 1.11) に使用する準備ができるまで、-20 ° C でペレットを維持します。
- 各 3 L の培養液に 1 M IPTG ストック溶液の分注 1.2 mL でタンパク質の発現を誘導する (最終濃度 0.4 mM)。14 ° c 16 h (一晩) 文化の培養を続けます。
注: 温度が通常 ~ 20 ° C まで達しました IPTG を追加すると、インキュベーターの性能に応じて時間。 - 1.7 のステップで説明されている手順に従い、過剰発現の SDS-PAGE 解析のため文化の後誘導サンプルを取る。
- 1 L 管 (g, 4 ° C, 10 分 x 3993) 遠心分離によって細胞を収穫します。上澄みを廃棄し、氷の上細胞ペレットを浄化に直接進みます。
- SDS ページ35,36によって発現を分析します。20 μ L バッファーとローディングの染料 × 2 の 20 μ L を実行するのには、前と後の誘導サンプルを再懸濁します。熱ブロック 95 ° C で 5 分間のサンプルを加熱し、まだ熱い間 15% ゲルの 20 μ L をロードします。V. 染色ゲル Coomassie 染料メーカーの指示によると 180 で 90 分のためのゲルを実行します。図 1Cの代表的な結果を比較します。
注: プロトコルここで停止することができます、細胞ペレットを冷凍、数週間、-80 ° C で保存することができます。最適な結果を得るのためには、新鮮な細菌ペレットを使用し凍結を避けることをお勧めします。凍結融解は、細胞の換散および Httex1 の劣化をもたらすかもしれない。これは、収量およびタンパク質の品質を減らす可能性があります。
2. セル換散そして彼の6の浄化-相撲 Httex1 融合タンパク質固定化金属アフィニ ティー ・ クロマトグラフィー (IMAC)
- 2 L のガラス瓶の中のバッファーを準備 (50 mM トリス (ヒドロキシメチル)-aminomethan (Tris)、500 mM の NaCl、15 mM のイミダゾール)。(50 mM 500 mM の NaCl、トリス 500 mM のイミダゾール pH 7.4) のバッファー B のガラス瓶の中に、1 L を準備します。塩を溶解した後に、10 N 塩酸で pH 調整し、新鮮なボトルにソリューションをフィルター ボトル上部フィルター (0.65 μ m) と。1000 x phenylmethylsulfonyl フッ化物 (PMSF、0.3 M) を準備在庫ソリューション、-20 ° C で格納して 100 μ L 分注
注: プロトコルは、逆相高速液体クロマトグラフィー (クロマトグラフィー) 浄化し 8-9 h の内で凍結乾燥細菌のペレットの溶解からすべての手順を完了できるように設計されています。集計とタンパク質を制限、一時停止せず急速に動作し、4 ° c または氷の上のすべての手順を実行しますそれをお勧めします。 - 中古冷蔵バッファー A. 追加バッファーに細菌のペレットの 100 mL に PMSF 原液とプロテアーゼ阻害剤の 5 錠 (最終巻の 30 mL あたり 1) の 100 μ L を追加し、電磁攪拌棒で攪拌し、wi 上下ピペッティングによる懸濁液を均質化第 10 mL の滅菌ピペット (30 分程度)。
- 細菌懸濁液を 50 mL の使い捨てプラスチック チューブ 40 mL の因数に分割します。セル換散 (70% 振幅、合計超音波処理時間 5 分、超音波照射 30 s、30 s の一時停止の間隔) の水/氷バッチでそれぞれ因数を超音波照射します。
注: サンプルが超音波処理ステップの間に加熱していないことが重要です。超音波処理時の熱放散を改善するために氷風呂にいくつかの水を追加することをお勧めします。超音波処理の手順は、さまざまな楽器を使用する場合に適応する必要があります。フランス語プレスや、microfluidizer のような他の換散方法は同様に動作する必要があります、サンプル ・蛋白質集合体の加熱を避けるために有益である可能性があります。これらのデバイスは、私たちの研究室で利用できませんでした、私たちの超音波処理プロトコルで良い結果を得た。 - ナトリウム dodecyl 硫酸塩のポリアクリルアミドゲル電気泳動 (SDS-PAGE) 分析用溶解液 50 μ L のサンプルを取る。遠心分離機のサンプル (18000 g、4 ° C、2 分 x) と新しい試験管に可溶性のピペットします。ピペットとバッファー A の 50 μ L で不溶性画分を再懸濁します。SDS-PAGE 解析 (ステップ 2.6) まで氷のサンプルを保ちます。
- 遠心分離 (g, 4 ° C, 60 分 x 39191) によってライセートを明確に。
- 遠心分離のステップ中に SDS ページのセル換散一歩を分析します。ライセートの水溶性と不溶性分画に染料をそれぞれロード × 2 の 50 μ L を追加します。95 ° C で 5 分間加熱し、まだ熱い間 15% ゲルの 2 μ L をロードします。V. 染色ゲル Coomassie 染料メーカーの指示によると 180 で 90 分のためのゲルを実行します。図 1Cの代表的な結果を比較します。
- 上清 (0.45 μ m、シリンジ フィルター) をフィルター処理します。SDS-PAGE 解析 (ステップ 2.11) のフィルター処理された上澄みの 20 μ L のサンプルを取る。
注: 通常、明確にし、フィルター処理された上澄みの 90 から 100 ミリリットルのボリュームが取得されます。通常、3 つのシリンジ フィルターで十分です。ろ過が面倒な場合、遠心分離速度や時間を増やしてみてください。 - 固定化金属アフィニ ティー ・ クロマトグラフィー (IMAC) の 4 ° C37高速性能液体クロマトグラフィー (FPLC) システム上で明らかに細菌の lysate から His6 相撲 Httex1 融合タンパク質を分離します。
- 明らかにし埋める superloop および Ni NTA 列にロードにライセート (実行前の空白を推奨する除去、洗浄、製造元のマニュアルに従って再読み込み、) 10 mL/分洗浄するバッファー A の 2 mL/分を渡す 10 列ボリューム (CV、200 mL) でうち非連結蛋白質。
- 2.5 との融合タンパク質を溶出バッファー B 2 mL/分での 100% の CV (50 mL) 使用分数サイズの読み込みと洗浄 50 mL と 5 mL の溶出。結果を図 1Dの代表的な結果を比較します。
- SDS-PAGE 解析 (20 μ L) の各分画のサンプルを取るし、IMAC のクロマト グラムのピークによると融合タンパク質を含有する画分をプールします。追加 (2 s, 3 s) - 1, 4 - ビス (sulfanyl) ブタン-2, 3-ジオール (DTT) と L-システイン (最終濃度 100 mM) を粉末と軽くチューブを反転して解散。
注: 我々 の経験の異なる画分の融合蛋白質の純度は同等です。念のため、精製された融合タンパク質の画分を高濃度の分数の凝集を予防する IMAC 後すぐにプールする必要があります。さらに、相撲タグと HPLC 精製の胸の谷間に直接続行することをお勧めします。必要に応じて、プロトコルがここで停止できます。融合タンパク質の希釈液は液体窒素で凍結、-80 ° C で保存、収量を大幅に削減することがなく解凍後精製しました。24 h 4 ° C で融合タンパク質の希釈液の保管も同様の結果を与えます。 - SDS ページで IMAC を分析します。各サンプルにローディングの染料の 20 μ L を追加します。2 μ L の原料 (2.7)、非連結の割合、洗浄率と 15% ゲルの溶出ピークの各分画をロードします。V. 染色ゲル Coomassie 染料メーカーの指示によると 180 で 90 分のためのゲルを実行します。結果を図 1Dの代表的な結果を比較します。
3. 彼の胸の谷間6-相撲-タグと高速液体クロマトグラフィー精製
注意: トリフルオロ酢酸 (TFA) は揮発性の液体とことができます原因重症熱傷ので取り扱い注意。ヒューム フードのすべての処理を行い、適切な個人用保護具 (すなわち、使い捨てニトリル手袋、安全眼鏡、白衣) を着用します。
- 5 L ボトルで 5 L の水 (溶剤 a: H2O、0.1% (TFA) に TFA 5 mL プラスチック注射器を追加します。アセトニ トリルの 2.5 L ボトルに TFA 2.5 mL プラスチック注射器を追加 (溶剤 b: アセトニ トリル、0.1 %tfa)。
- 製造元が推奨する、高速液体クロマトグラフィー システムを準備します。きれいな列を確保するため空白を実行します。
- ULP1 高精度 (ステップ 3.5) によって開裂反応を監視するための加算の前に融合蛋白質の 100 μ L のサンプルを取る。
- 新しい 50 mL のチューブに融合蛋白質の 20 mL を転送 ULP1 ストック溶液 0.4 mL を追加、氷の上を孵化させなさい。氷の上の残りの融合蛋白質を保ちます。
注: 彼の付けられた触媒フラグメント 403 621 ユビキチン様特定プロテアーゼ 1 (ここで、"ULP1"と呼ばれる) は、相撲のタグを切断に使用されました。融合タンパク質は、劈開の Httex1 よりも安定です。バッチ全体が相撲タグを切断しないことをお勧めします。代わりに、HPLC カラムに直接、完全を適用できるサイズの因数を続行します。 - 10 分ごとには、超高性能液体クロマトグラフィー (高精度) で進行状況を監視する開裂反応の 100 μ L のサンプルを取る。遠心分離機のサンプル (18000 rpm、4 ° C、2 分) と分析による高精度 2 μ L (10% から 90% 溶剤 B 0.25 を 3 分間で、グラデーション、1 分間 10 %b 参照計測器の使用については、製造元の指示に従って)。サンプル ULP1 添加前に、と後に撮影サンプル得られたクロマト グラムを比較します。典型的な結果を図 2Bでの結果を比較します。
- 相撲胸の谷間が完了 (融合タンパク質のピーク高精度クロマト グラムの消えたし、は完全に新しく出現相撲と Httex1 ピークに変換されます)、サンプルのフィルター シリンジ フィルター (0.22 μ m)。
注: 相撲胸の谷間は通常非常に高速 (4 ° C で 10-20 分) したがって 4 分の実行時間の高精度解析は反応を監視するための貴重なツールです。高速液体クロマトグラフィーの前にサンプルをフィルタ リング浄化は、カラムの寿命を延ばすに主に予防策です。このサンプルは、濁水にしないでください。 - クロマトグラフィーによってフィルターが適用されたサンプルを浄化 (25-35% 溶剤 B 溶媒は、15 mL/分で 40 分以上の勾配 (0-10 分: 5%; 25 10 12.5 分: 5%; 12.5 52.5 分: 25 35%; 52.5 57.5 分 35 ~ 95%; 計測器の使用については、製造元の指示を参照してください)。結果を図 2Cの代表的な結果を比較します。
注: Httex1 と彼の6-クロマトグラフィーによってよく別相撲。ただし、ピークの前後で切り捨てられた Httex1 の少量があります。純粋な材料の最大量を取得する小さな分数を収集します。
注意: 使用時 (すなわち白衣、絶縁手袋、顔面シールド) 適切な安全装置低温流体を扱います。 - エレクトロ スプレー イオン化質量分析法による HPLC 分画を分析 (MS、オートサンプラー、10 μ L を注入、0.6 mL/分、溶媒の流れ: 計測器の使用については、製造元の指示を参照してくださいでは、列がない場合、20 %b) と高精度 (10% から 90% へのグラデーション0.25 〜 3 分、1 分間 10% B a B 溶媒は計測器の使用については、製造元の指示を参照。)50 mL プラスチック チューブのような純度の分数をプール、液体窒素で凍結、凍結乾燥します。重量を量ると 2 mL プラスチック チューブに凍結乾燥タンパク質を転送し、-20 ° C で保存
- 高精度、ESI MS、SDS-PAGE による精製材料を特徴付けます。1.5 mL チューブに端正 TFA の 8 μ L で凍結乾燥させた Httex1 の 100 μ g を溶解し、クローズド テスト チューブに室温で 20 分間インキュベートします。慎重に窒素またはアルゴンの流れとヒューム フードの下で TFA を蒸発させます。窒素・ アルゴンの低圧を使用すると、サンプルの損失を回避します。
- 高精度で H2o. 分析 2 μ L の 100 μ L と 3.8 の手順と ESI 質量 5 μ L のタンパク質を溶解します。ミックス 20 μ L タンパク質溶液のローディングの染料 × 2 の 20 μ L。
- SDS-PAGE により 10 μ g に 1 μ g の量を分析します。V. 染色ゲル Coomassie 染料メーカーの指示によると 180 で 90 分のためのゲルを実行します。結果を図 2Dの代表的な結果を比較します。
4. 解凝集および Httex1 タンパク質の Resolubilization
注意: TFA は揮発性の液体とことができます原因重症熱傷ので取り扱い注意。ヒューム フードのすべての処理を行い、適切な個人用保護具 (すなわち使い捨てニトリル手袋、安全眼鏡、白衣) を着用します。
- ダルベッコ リン酸緩衝生理食塩水 (DPBS) (137 mM NaCl、KCl 2.7 mM、10 mM Na2HPO4、2 mM KH2PO4、pH 7.4) 50 mL のチューブで予混合粉末からの 10 mL を準備します。各使用する前に 0.2 μ m のフィルターを通して DPBS ソリューションをフィルターします。
- 1.5 mL チューブに端正 TFA の 12 μ L で凍結乾燥させた Httex1 の 150 μ g を溶解し、クローズド テスト チューブに室温で 20 分間インキュベートします。慎重に窒素またはアルゴンの流れとヒューム フードの下で TFA を蒸発させます。サンプル38の損失を避けるために窒素・ アルゴンの低圧を使用します。
注: 一般に、溶解し、蛋白質の 50 μ g の分解および 4 μ L TFA を使用します。このプロシージャは内部の膜タンパク質を作成テスト チューブの壁。次の手順で Httex1 の即時集計を防ぐためには、予冷バッファーを使用、氷の上に常に蛋白質を保つため、高濃度を避けるため。 - 予冷 DPBS 1 mL で分解されたタンパク質を溶解し、1 M NaOH で 7.2 7.4 に pH を調整します。1.5 mL プラスチック チューブ (20000 x g、4 ° C、20 分) に 100 kDa 遠心フィルターを通して蛋白質の解決をフィルターします。
注: 計算される理論 Httex1 濃度は損失の可能性を考慮して必要な最終濃度より高いです。濾過手順中にタンパク質の分解を形成している可能性があります任意の集計を削除する必要です。 - アミノ酸分析 (λ214検出) に基づく高精度校正曲線を用いた Httex1 の濃度を決定して 2 μ g のタンパク質をアミノ酸分析濃度10を検証するために送信します。3 μ M の濃度を得るために追加する必要があります DPBS の量を計算 Httex1。
- テスト チューブに DPBS の金額を追加することによって 3 μ M にタンパク質を希釈します。集合のプロトコルの開始まで氷の上の管を保ちます。
注: Httex1 43 q をソリューションに格納しないでください。常に上記のプロトコルに基づく新鮮なタンパク質溶液を準備します。Httex1 蛋白質、-20 ° C の凍結乾燥粉末として格納されます最高
5. 監視、集計速度の Httex1 43 q 高精度と円二色性 (CD) の分光と透過電子顕微鏡 (TEM) による骨材の特性を使用しての
- 以前に報告された39として TEM のウラニル ギ酸ソリューションを準備します。
- Httex1 の集計を開始 37 ° c (分解プロトコルで上記溶液の 1 mL を使用) DPBS で 3 μ M ソリューションの孵化によって 43 q。
注: 実験の目的とニーズに応じてより高い濃度で Httex1 の集計を実行できます。 - (0、1、2、4、6、8、12、24、48 および 120 h) で示された時点で高精度を使用して水溶性の蛋白質の量を定量化します。これを行うには、35 μ L の因数を取る、遠心分離 (20000 g、4 ° C、20 分 x) によって不溶性の集計を削除します。上澄みの 4 μ L を高精度に注入します。計測器ソフトウェア40を使用してピーク面積の変更に基づく水溶性モノマーの比率を計算します。結果を図 3Aの代表的な結果を比較します。
- 0、48 h で CD 分光法を用いた二次構造の変化を特徴付けます。100 μ L を取るし、楕円率の測定 (1 mm 石英キュベット、195 nm ~ 250 nm、20 ° C、データ ポイントすべての 0.2 の nm、速度 10 nm/分、デジタル統合時間 2 s、帯域幅 1.0 nm)。サンプルと平均 6 スペクトルを取得し、99 のたたみ込み幅二項フィルターを用いた滑らかな。平均残基のモル楕円率 (θMRE)41としてスペクトルをプロットします。図 3Bの代表的な結果と結果を比較します。
- TEM による骨材の構造と形態学的特性を特徴付けます。グリッド上にホルムバール/炭素コーティング 200 メッシュ、グロー放電銅 1 分洗って一度を 0.7% (w/v) ウラニル蟻酸塩及び 30 の汚れ 15 μ、15 μ L 水で二回グリッドのタンパク質溶液 3 μ L を入れて 0.7 %w/v ウラニル ギ酸の 15 μ L と s。グリッドの TEM 分析を実行します。図 3Cに代表的な結果と結果を比較します。
結果
Httex1 は N ターミナルを持つ大腸菌で表される彼の6-相撲タグ。式および融合タンパク質の精製の代表の結果を図 1にまとめます。Met1 だ完全に裂かれた生体内で42Htt と Ala2、始まる 2 90 残基の Httex1 のシーケンスで構成されます。23Q バリアントは、アミノ酸の番号、図 1Aに表現された融合タンパク質の完全なシーケンスを示します。プラスミッドはコミュニティと共有する近い将来 Addgene に入金されます。プラスミッドおよび表現された融合タンパク質の概略図を図 1Bに示します。His6 相撲 Httex1 を中レベル (図 1C) 表現し、融合タンパク質のほとんどは、溶解、両方、23Q、43 q バリアントの後可溶性画分に存在です。融合タンパク質が予想よりも高い分子量に基づいて移行されます。これは相撲の強い倍もあって、たいがいは主にグルタミン、プロリン残基を含む Httex1 の異常なシーケンス構成。(23Q) 野生型と変異体 (43 q) 融合タンパク質濃縮 IMAC (図 1D) 共同ホスト蛋白質の浄化の存在が Httex1 と大きなサンプルの比較的低い発現レベルによって説明できる 〜 80% の純度にボリュームを列に適用します。
彼の胸の谷間6-相撲タグと Httex1 の精製を図 2Aに示します。高精度は、彼の胸の谷間を監視するための効率的なツール6-相撲タグ (図 2B)。融合蛋白質の元のピークが消費されると、彼に対応する 2 つの新しいと十分に分離ピーク6-相撲タグと Httex1 が表示されます。胸の谷間の反応は、10 〜 20 分に仕上がっています。西部のしみ (WB) が開裂反応を効率的に監視するには遅すぎるが、参考のため、相撲胸の谷間の完全性を示すための図に含まれています。両方の Httex1 23Q と 43 q は、彼からも分けることができます6-相撲クロマトグラフィー (図 2C) でタグを付けるし、高精度、MS、SDS-PAGE 分析 (図 2D) に示すように、高純度で得られました。
この法により作製した Httex1 蛋白質は Httex1 の予想集計プロパティを保持、沈降法による変異 Httex1 37 ° C の線維化動態を評価したことを説明するために CD による二次構造の変化を監視分光学、TEM による骨材の形態を特徴とします。MHttex1 線維形成沈降分析により凝集速度の代表的なデータ セットを図 3に示します。線維を形成するため、時間をかけて 43 q が高精度で, 定量化した水溶性の Httex1 の損失。培養 48 時間後の可溶性タンパク質の完全な枯渇を遵守します。さらに、CD 分光法 (図 3B) によるタンパク質の二次構造を決定します。構造化されていないから Httex1 43 q シフト (λmin 205 nm) 培養 48 時間後主に β シート豊富な立体配座 (λmin 215 nm) します。この構造変化は、48 時間 (図 3C) で TEM による観測として長い繊維集合体の形成を伴っている.
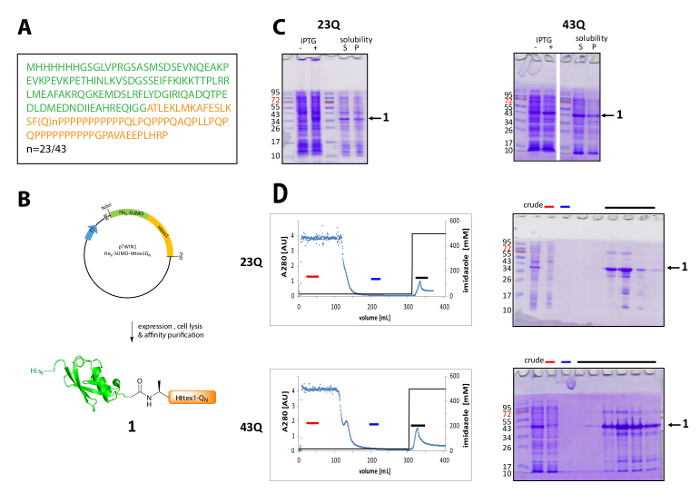
図 1.彼の発現と精製6-相撲 Httex1 融合タンパク質。
(A) 彼のアミノ酸シーケンス6-相撲-Httex1-QN融合コンストラクト (彼の6-緑色で相撲とオレンジの Httex1 QN );(B)発現と融合タンパク質の精製の図式的な概観(C) 式および換散; 後融合蛋白質の溶解度の SDS-PAGE 解析融合タンパク質の IMAC の精製と SDS-PAGE による端数の解析 (D) クロマト グラム (赤いバー: 非連結の割合、青いバー: 洗浄分数、黒いバー: 溶出ピークを含む画分);この図の拡大版を表示するのにはここをクリックしてください。

図 2.彼の胸の谷間6相撲タグとタグ無料 Httex1 QN蛋白質の浄化。
(A) 図式的な概観;(B) による高精度で ULP1 と相撲タグの胸の谷間 (青: ULP1; 添加前に黒: 20 分 (23Q)、ULP1 の付加の後でそれぞれ 10 分 (43 q)) と WB (MAB5492 集、二次ヤギ抗マウス抗体 1: 5000)Httex1; 分取クロマトグラフィー精製の (C) のクロマト グラムD: 解析、高精度で浄化された Httex1 の SDS-PAGE と MS;予想される分子量はそれぞれ 9943 Da (23Q) と 12506 Da (43 q です)。この図の拡大版を表示するのにはここをクリックしてください。
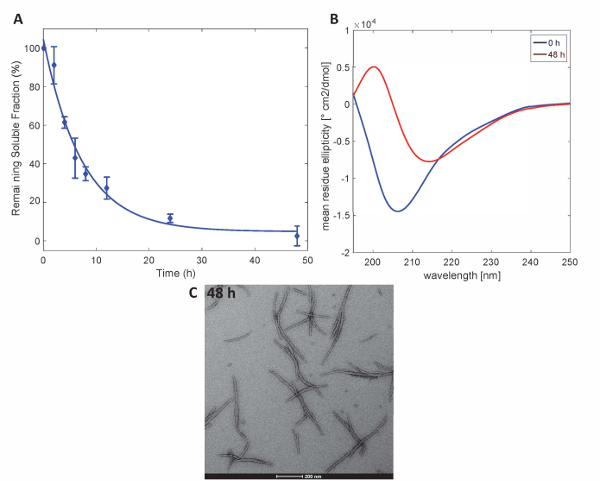
図 3.Httex1-43 q の集計:高精度に基づく (A) 沈降分析。(B) 0 h と 48 時間の集計の 48 h. (C) TEM 顕微鏡写真で二次構造の CD スペクトル (スケール バーは、200 nm)。この図の拡大版を表示するのにはここをクリックしてください。
ディスカッション
このプロトコルでタグなしのネイティブの取得ミリグラム量 Httex1 のための効率的な手順を概説した我々 23 または 43 のグルタミン残基を含みます。これは彼に C 末端融合として Httex1 を表現することによって達成された6-相撲タグ IMAC で細胞ライセートから融合タンパク質を分離する使用され、Httex1 の高速液体クロマトグラフィー精製前に切断します。相撲戦略は、いくつかの他のタンパク質の生産に使用されている、提案手法が、相撲を使用して本質的に生成することもできるユニークな特性を狂わせたら、集計が発生しやすいので、以前に証明しているアミロイド蛋白質表示されます。処理し、43,44を作り出す非常に困難。「行儀」タンパク質の生成は、わかりやすい、使いやすいプロトコルに匹敵するプロトコルを提案します。相撲可溶性し、式と IMAC の精製ステップ中に Httex1 を安定化します。タグ、インテイン戦略10集計と観察の時期尚早胸の谷間は、もはや問題なかった。
天然変性タンパク質は劣化に対して特に脆弱です。N17 地域の N 末端の劣化は、このプロトコルを使用して問題ではない、間 Httex1 PRD で切り捨てが発生します。切り捨てられた蛋白質が疎水性、料金、サイズ Httex1 に非常に類似している挑戦は、クロマト グラフの手段によってそれらを削除する、従ってそれは最初の場所でそれらの形成を防ぐために最善。プロトコルに密接にこだわり、常に氷に取り組んで、プロテアーゼ阻害剤の十分な量を使用して保つ必要がある観察打ち切りレベル非常に低い。Httex1 の C 末端融合タグを適用するので、削除でした切り捨て PRD の簡単に切り捨てられたタンパク質親和性タグも失うことになります。ただし、ネイティブのシーケンスは Httex1 終了プロリンと我々 の知る限り、このオプションは適用できませんを維持する必要がある場合、プロリン後痕跡を残さないと効率的な胸の谷間を誘導するために知られている C 末端融合タグがないです。
プロトコルの最も重要な部分は、解放後の相撲タグの胸の谷間 ULP1 によって Httex1 の処理です。タンパク質は、クロマトグラフィーによってすぐに浄化する必要があります。幸いなことに、これは通常 4 ° C で 10-20 分で完了する効率的かつ高速反応です。対照的に、インテイン戦略は不完全な胸の谷間と始まり集約トレードオフ収量を最大化するために必要となる、インテインの完全な胸の谷間にいくつかの時間を必要です。高速精密検査は、それが開始されます Httex1、突然変異体に必要な 23Q バリアントは、長い時間安定したに対し、開裂反応に比較的高濃度で集計します。クロマトグラフィー精製中に相撲の別の利点が明らかになります: Ssp DnaB インテインは疎水性カラムに強く棒、相撲は親水性と C4 逆相カラムから完全に示しています。商業 ULP1 は非常に高価ですが、タンパク質は、次の以前に発行されたプロトコル29高収率で簡単に製作可能します。
Httex1 を使用する前に分解のプロトコルを適用することの重要性をすることはできません十分に強調します。Httex1 のような凍結乾燥 polyQ 蛋白質が安定しているストアドの長い期間にすることができます、水やバッファーに完全に溶け合うことはありません。前もって形成されたオリゴマーや繊維の存在は、凝集速度とタンパク質45の生物物理特性に大きな影響を与える可能性があります。ここで説明した分解プロトコルでは、タンパク質の分解、前もって形成された集合体の除去と凍結乾燥のサンプルから単量体 Httex1 のソリューションの生成をことができます。相撲とインテイン戦略で得られた Httex1 の同様の集計速度と線維の形態を観察した.
Httex1 を生産する以前の方法と比較して、ここで説明した相撲戦略は、いくつかの利点を提供しています、構造を調査するための可能な研究の範囲と健康と病気のこの蛋白質の機能特性を拡大します。相撲 Httex1 融合タンパク質は扱いやすい、冷凍し、保存または周囲温度で 24 h のためのソリューション内に保持、無料の mHttex1 はすぐに集計できます。安定性と相撲 Httex1 融合タンパク質の高溶解性タンパク質を操作および/またはそれ以外の場合は不可能な胸の谷間の後 mHttex1 に酵素と化学の変更を導入するより大きい柔軟性を提供します。これは導入を含むポスト翻訳の修正、fluorophores が付いて、スピン ラベル、ビオチン タグ等紹介進歩すべき 1) Httex1; の構造-機能相関の解明に今後調査を促進します。2) Htt の集約と病理が広がっている; を調査するための新しいツールを生成します。3) 突然変異体 Httex1 の安定化し、その集計を防止する分子を同定する方法を新しいの開発を有効にします。・ 4) このタンパク質上で動作し、ハンティントンの病気のための治療法を見つけるに当社のクエストに参加させる他の分野から科学者を奨励します。
開示事項
著者は、この記事の内容との利害があるないことを宣言します。
謝辞
この作品 CHDI 財団やスイスの全米科学財団からの補助金によって主に資金を供給されました。ありがとう博士ソフィー Vieweg 有益な議論この新しい表現システムの開発と Lashuel グループの他のメンバーの間にこの式システムと彼らの経験を共有するため、その入力、貴重なフィードバック。我々 はまた、ULP1 プラスミドを提供する教授オリバー Hantschel を感謝します。著者原稿の批判的検討の博士ジョン B. ワーナーと博士 Senthil K. Thangaraj に感謝します。
資料
| Name | Company | Catalog Number | Comments |
| Uranyl formate (UO2(CHO2)2) | EMS | 22450 | |
| Formvar/carbon 200 mesh, Cu 50 grids | EMS | FCF200-Cu-50 | |
| High Precision Cell made of Quartz SUPRASIL 1 mm light path from Hellma Analytics | HellmaAnalytics | 110-1-40 | |
| Buffer Substance Dulbecco's (PBS w/o Ca and Mg) ancinne ref 47302 (RT) SERVA | Witech | SVA4730203 | |
| Ampicillin | AxonLab | A0839.0100 | |
| Luria Broth (Miller's LB Broth) | Chemie Brunschwig | 1551.05 | |
| Isopropyl β-D-1-thiogalactopyranoside (IPTG) | AxonLab | A1008.0025 | |
| E. coli B ER2566 | NEB | NEB# E4130 | |
| Imidazole | Sigma | 56750-500G | |
| cOmplete Protease Inhibitor Cocktail | Roche | 4693116001 | |
| Anti-Huntingtin Antibody, a.a. 1-82 | Merck Millipore Corporation | MAB5492 | |
| IRDye 680RD Goat anti-Mouse IgG (H + L) | Licor | 925-68070 | |
| PMSF | AxonLab | A0999.0005 | |
| HisPrep 16/10 column | GE Healthcare | 28936551 | |
| C4 HPLC column | Phenomenex | 00G-4168.P0 | 10 µm C4 300 Å, LC Column 250 x 21.2 mm, Phenomenex, 19x10 mm guard column, not temperature jacketed |
| Acetonitrile HPLC | MachereyNagel | C2502 | |
| Filtre seringue Filtropur S 0,45 ul sans prefiltre sterile | Sarstedt AG | 83.1826 | |
| Spectrophotometer semi-micro cuvette | Reactolab S.A. | 2534 | |
| Superloop, 1/16" fittings (ÄKTAdesign), 50 ml | GE Healthcare | 18111382 | |
| Trifluoroacetic acid | Sigma | 302031 | |
| GREINER Tubes fo FPLC 16 x 100 mm, cap. 12.0 ml | Greiner Bio-One | 7.160 102 | |
| 100 kD Microcon fast flow filters | Merck Millipore Corporation | MRCF0R100 | |
| Vibra-cell VCX130 ultrasonic liquid processor | Sonics | ||
| Äkta 900 equipped with a fraction collector | GE Healthcare | ||
| Jasco J-815 Circular Dichroism | Jasco | ||
| Waters UPLC system | Waters | C8 BEH acquity 2.1x100 mm 1.7 micron column , preheated column (40 °C), flow rate of 0.6 mL/min, injection volume of 4 μL | |
| waters HPLC system | Waters | 2489 UV detector and 2535 quaternary gradient module, 20 mL loop in a FlexInject housing | |
| ESI-MS: Finnigan LTQ | Thermo Fisher Scientific | ||
| lyophylizer instrument | FreeZone 2.5 Plus | ||
| Tecnai Spirit BioTWIN | FEI | electron microscope equipped with a LaB6 gun and a 4K x 4K FEI Eagle CCD camera (FEI) and operated at 80 kV | |
| 37 °C shaking incubator | Infors HT multitron Standard | ||
| Biophotometer plus | Eppendorf |
参考文献
- Saudou, F., Humbert, S. The Biology of Huntingtin. Neuron. 89 (5), 910-926 (2016).
- MacDonald, M. E., Gines, S., Gusella, J. F., Wheeler, V. C. Huntington's disease. Neuromolecular Medicine. 4 (1-2), 7-20 (2003).
- Li, S., Li, X. J. Multiple pathways contribute to the pathogenesis of Huntington disease. Molecular Neurodegeneration. 1, 19 (2006).
- DiFiglia, M. Aggregation of Huntingtin in Neuronal Intranuclear Inclusions and Dystrophic Neurites in Brain. Science. 277 (5334), 1990-1993 (1997).
- Atwal, R. S., et al. Huntingtin has a membrane association signal that can modulate huntingtin aggregation, nuclear entry and toxicity. Human Molecular Genetics. 16 (21), 2600-2615 (2007).
- Sathasivam, K., et al. Aberrant splicing of HTT generates the pathogenic exon 1 protein in Huntington disease. Proceedings of the National Academy of Sciences U S A. 110 (6), 2366-2370 (2013).
- Mangiarini, L., et al. Exon 1 of the HD gene with an expanded CAG repeat is sufficient to cause a progressive neurological phenotype in transgenic mice. Cell. 87 (3), 493-506 (1996).
- El-Daher, M. T., et al. Huntingtin proteolysis releases non-polyQ fragments that cause toxicity through dynamin 1 dysregulation. EMBO Journal. 34 (17), 2255-2271 (2015).
- Lunkes, A., et al. Proteases acting on mutant Huntingtin generate cleaved products that differentially build up cytoplasmic and nuclear inclusions. Molecular Cell. 10 (2), 259-269 (2002).
- Vieweg, S., Ansaloni, A., Wang, Z. M., Warner, J. B., Lashuel, H. A. An Intein-based Strategy for the Production of Tag-free Huntingtin Exon 1 Proteins Enables New Insights into the Polyglutamine Dependence of Httex1 Aggregation and Fibril Formation. Journal of Biological Chemistry. 291 (23), 12074-12086 (2016).
- Georgalis, Y., et al. Huntingtin aggregation monitored by dynamic light scattering. Proceedings of the National Academy of Sciences U S A. 95 (11), 6118-6121 (1998).
- Scherzinger, E., et al. Huntingtin-encoded polyglutamine expansions form amyloid-like protein aggregates in vitro and in vivo. Cell. 90 (3), 549-558 (1997).
- Scherzinger, E., et al. Self-assembly of polyglutamine-containing huntingtin fragments into amyloid-like fibrils: implications for Huntington's disease pathology. Proceedings of the National Academy of Sciences U S A. 96 (8), 4604-4609 (1999).
- Muchowski, P. J., et al. Hsp70 and hsp40 chaperones can inhibit self-assembly of polyglutamine proteins into amyloid-like fibrils. Proceedings of the National Academy of Sciences U S A. 97 (14), 7841-7846 (2000).
- Heiser, V., et al. Inhibition of huntingtin fibrillogenesis by specific antibodies and small molecules: implications for Huntington's disease therapy. Proceedings of the National Academy of Sciences U S A. 97 (12), 6739-6744 (2000).
- Bennett, E. J., Bence, N. F., Jayakumar, R., Kopito, R. R. Global impairment of the ubiquitin-proteasome system by nuclear or cytoplasmic protein aggregates precedes inclusion body formation. Molecular Cell. 17 (3), 351-365 (2005).
- Tam, S., et al. The chaperonin TRiC blocks a huntingtin sequence element that promotes the conformational switch to aggregation. Nature Structural & Molecular Biology. 16 (12), 1279-1285 (2009).
- Nekooki-Machida, Y., et al. Distinct conformations of in vitro and in vivo amyloids of huntingtin-exon1 show different cytotoxicity. Proceedings of the National Academy of Sciences U S A. 106 (24), 9679-9684 (2009).
- Wacker, J. L., Zareie, M. H., Fong, H., Sarikaya, M., Muchowski, P. J. Hsp70 and Hsp40 attenuate formation of spherical and annular polyglutamine oligomers by partitioning monomer. Nature Structural & Molecular Biology. 11 (12), 1215-1222 (2004).
- Legleiter, J., et al. Monoclonal antibodies recognize distinct conformational epitopes formed by polyglutamine in a mutant huntingtin fragment. Journal of Biological Chemistry. 284 (32), 21647-21658 (2009).
- Legleiter, J., et al. Mutant huntingtin fragments form oligomers in a polyglutamine length-dependent manner in vitro and in vivo. Journal of Biological Chemistry. 285 (19), 14777-14790 (2010).
- Nucifora, L. G., et al. Identification of novel potentially toxic oligomers formed in vitro. from mammalian-derived expanded huntingtin exon-1 protein. Journal of Biological Chemistry. 287 (19), 16017-16028 (2012).
- Dahlgren, P. R., et al. Atomic force microscopy analysis of the Huntington protein nanofibril formation. Nanomedicine. 1 (1), 52-57 (2005).
- Poirier, M. A., et al. Huntingtin spheroids and protofibrils as precursors in polyglutamine fibrilization. Journal of Biological Chemistry. 277 (43), 41032-41037 (2002).
- Duim, W. C., Chen, B., Frydman, J., Moerner, W. E. Sub-diffraction imaging of huntingtin protein aggregates by fluorescence blink-microscopy and atomic force microscopy. Chemphyschem. 12 (13), 2387-2390 (2011).
- Pieri, L., Madiona, K., Bousset, L., Melki, R. Fibrillar alpha-synuclein and huntingtin exon 1 assemblies are toxic to the cells. Biophysical Journal. 102 (12), 2894-2905 (2012).
- Monsellier, E., Redeker, V., Ruiz-Arlandis, G., Bousset, L., Melki, R. Molecular interaction between the chaperone Hsc70 and the N-terminal flank of huntingtin exon 1 modulates aggregation. Journal of Biological Chemistry. 290 (5), 2560-2576 (2015).
- Isas, J. M., Langen, R., Siemer, A. B. Solid-State Nuclear Magnetic Resonance on the Static and Dynamic Domains of Huntingtin Exon-1 Fibrils. Biochemistry. 54 (25), 3942-3949 (2015).
- Malakhov, M. P., et al. SUMO fusions and SUMO-specific protease for efficient expression and purification of proteins. Journal of Structural Function Genomics. 5 (1-2), 75-86 (2004).
- Mossessova, E., Lima, C. D. Ulp1-SUMO crystal structure and genetic analysis reveal conserved interactions and a regulatory element essential for cell growth in yeast. Molecular Cell. 5 (5), 865-876 (2000).
- Kumari, S., Pal, R. K., Gupta, R., Goel, M. High Resolution X-ray Diffraction Dataset for Bacillus licheniformis Gamma Glutamyl Transpeptidase-acivicin complex: SUMO-Tag Renders High Expression and Solubility. Protein Journakl. 36 (1), 7-16 (2017).
- Zhang, J., Sun, A., Dong, Y., Wei, D. Recombinant Production and Characterization of SAC, the Core Domain of Par-4, by SUMO Fusion System. Applied Biochemistry and Biotechnology. , (2017).
- Reif, A., et al. Semisynthesis of biologically active glycoforms of the human cytokine interleukin 6. Angewandte Chemie International Edition English. 53 (45), 12125-12131 (2014).
- Froger, A., Hall, J. E. Transformation of plasmid DNA into E. coli using the heat shock method. Journal of Visualized Experiments. (6), 253 (2007).
- Smith, B. J. SDS Polyacrylamide Gel Electrophoresis of Proteins. Methods in Molecular Biology. 1, 41-55 (1984).
- Lawrence, A. M., Besir, H. U. Staining of proteins in gels with Coomassie G-250 without organic solvent and acetic acid. Journal of Visualized Experiments. (30), (2009).
- Block, H., et al. Immobilized-metal affinity chromatography (IMAC): a review. Methods in Enzymology. 463, 439-473 (2009).
- Chen, S. M., Wetzel, R. Solubilization and disaggregation of polyglutamine peptides. Protein Science. 10 (4), 887-891 (2001).
- Booth, D. S., Avila-Sakar, A., Cheng, Y. Visualizing proteins and macromolecular complexes by negative stain EM: from grid preparation to image acquisition. Journal of Visualized Experiments. (58), (2011).
- O'Nuallain, B., et al. Kinetics and thermodynamics of amyloid assembly using a high-performance liquid chromatography-based sedimentation assay. Amyloid, Prions, and Other Protein Aggregates, Pt C. 413, 34-74 (2006).
- Greenfield, N. J. Analysis of circular dichroism data. Methods in Enzymology. 383, 282-317 (2004).
- Aiken, C. T., et al. Phosphorylation of threonine 3: implications for Huntingtin aggregation and neurotoxicity. Journal of Biological Chemistry. 284 (43), 29427-29436 (2009).
- Satakarni, M., Curtis, R. Production of recombinant peptides as fusions with SUMO. Protein Expression and Purification. 78 (2), 113-119 (2011).
- Davies, H. A., Wilkinson, M. C., Gibson, R. P., Middleton, D. A. Expression and purification of the aortic amyloid polypeptide medin. Protein Expression and Purification. 98, 32-37 (2014).
- Chen, S., Wetzel, R. Solubilization and disaggregation of polyglutamine peptides. Protein Science. 10 (4), 887-891 (2001).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved