Method Article
ヒト多形核白血球に対する黄色ブドウ球菌の細胞毒性の定量
Erratum Notice
要約
このプロトコルは、全ヒト血液からの多形核白血球の精製方法と、これらの重要な自然免疫細胞に対する黄色ブドウ球菌の細胞傷害性を定量化する2つの異なるアッセイについて説明する。
要約
黄色ブドウ球菌は、多形核白血球(PMNまたは好中球)の膜完全性を標的とし、破壊する広範囲の白血球分を分泌することができる。このプロトコルは、ヒトPMNの精製と、3つの異なるセクションにおけるPMNに対するS.オーレウス細胞毒性の定量の両方を記述する。セクション1では、密度遠心分離を用いたヒト血液からのPMNおよび血清の分離について詳述する。セクション2は、これらの精製されたヒトPMNに対してS.aureusによって産生される細胞外タンパク質の細胞傷害性を試験する。これらの手順は、細胞膜不透過性であるDNA結合フルオロフォアであるヨウ化プロピジウムで処理されたPMNのフローサイトメトリー分析を用いて、S.アウレウスロイコシジンによるPMN血漿膜完全性の破壊を測定する。総称して、これらの方法は、原発ヒトPMNに対するS.aureus細胞傷害性を迅速に試験する利点を有し、宿主病原体相互作用の他の側面を研究するために容易に適応することができる。
概要
黄色ブドウ球菌は、ヒトの疾患の広いスペクトルを引き起こすグラム陽性細菌です。この顕著な病原体は、感染の異なる側面に寄与する多数の毒性因子を産生する。これらには、S.aureusが異なるタイプの宿主組織1に付着することを可能にする表面分子、宿主免疫応答2を妨害する細胞外タンパク質、および異なるタイプの宿主細胞3を標的とする分泌毒素の配列が含まれる。本報告では、S.aureusによって産生される細胞外タンパク質の細胞傷害性をヒト多形核白血球(PMNまたは好中球)に対して定量する方法、宿主の主エフェクター細胞を先天性免疫応答とする。
PMNは哺乳類の中で最も豊富な白血球である。これらの循環免疫細胞は、常駐細胞または侵入微生物に特有の化合物によって産生される危険シグナルに応答して宿主組織侮辱の部位に迅速に募集される。これらの分子からの細胞外入力および外挿中に活性化された常駐宿主細胞との直接接触から、プライミング4、5として知られるプロセスにおけるPMNの活性化状態を増加させる。苦しんでいる組織に達したプライミングPMNは、感染の確立を防ぐために設計された重要な自然免疫応答を実行します。これらには、結合および内在化、または食細胞症、強力な抗菌化合物5の電池によって微生物破壊において立発する細胞内イベントのカスケードを引き起こす侵入微生物が含まれる。
PMNは、病原体の侵入からヒトを保護する重要な役割を果たし、S.aureus感染を防ぐために特に重要である4.しかし、この細菌は、異なるPMN機能を妨げる広範囲の毒性遺伝子を産生する。これらには、シグナル伝達分子の認識を遮断する細胞外タンパク質、宿主組織への付着防止、抗菌性化合物の産生抑制、および血漿膜完全性の侵害4が含まれる。S. aureusは、特定の環境手掛かりを認識する複数の2成分感覚システムからの集合的な入力を通じて、これらの毒性遺伝子の時間発現を調整する。SaeR/S 2成分システムは、感染時のS.アウレウス毒性遺伝子転写の主要なアップレギュレータである6,7,8,9,10,11.特に、この2成分系は、ヒトPMN12を特異的に標的とする二成分ロイコシジンの製造に重要であることが示されている。
このプロトコルは、3 つの異なるセクションに分かれています。第1セクションでは、Bøyum13およびNauseef14によって確立された方法から適応されたプロトコルを用いて密度勾配遠心分離を使用したヒト血液からのPMNの精製について説明する。第2および第3のセクションでは、S.アウレウス細胞毒性を調べる2つの異なる技術を詳述する。一方はS.aureusによって産生される細胞外タンパク質を有するPMNを中毒し、もう1つは食細胞症後にPMNに損傷を与える生菌の能力を調べる。これらの手順は、ヨウ化プロピジウムを使用して、S.アウレウス孔形成毒素によって引き起こされるPMN形質膜完全性の損失を測定する。ヨウ化プロピジウムは、通常は細胞膜不透過性であるが、S.アウレウス毒素によって破壊された形質膜を横断することができるDNA結合フルオロフォアである。フローサイトメトリー分析は、ヨウ化プロピジウム陽性PMNの迅速な定量を可能にし、S.アウレウス株の相対細胞毒性を測定する。メチシリン耐性S.アウレウス(MRSA)は、パルス場ゲル電気泳動型USA300およびこの株におけるsaeR/Sの等生欠失変異体(USA300ΔsaeR/S)として同定され、これらの手順がヒトPMNに対するS.オーレンスの細胞毒性を定量する方法を実証するモデルとして使用されている。
プロトコル
健康なドナーからのヘパリン化静脈血は、モンタナ州立大学のヒト被験者のための機関審査委員会によって承認されたプロトコルに従って収集されました.すべての寄付者は、この研究に参加することに書面による同意を提供した。
1. ヒト多形核白血球の精製とヒト血清の単離
注:すべての試薬は、市販のエンドトキシン検出キットを使用してエンドトキシンの存在を定期的にチェックする必要があり、PMNの不要なプライミングを防ぐために<25.0 pg/mLエンドトキシンを含める必要があります。
- 3% デキストラン-0.9% NaCl (w/v)の 50 mL、0.9% NaCl (w/v)の 35 mL、1.8% NaCl (w/v)の 20 mL、1.077 g/mL 密度勾配溶液の 12 mL、および 20 mL の注入または灌漑グレードの水を室温に持ち込みます。
- ヒト血清を単離するには、15mLガラス管内の37°Cで抗凝固剤を用いない新鮮に引き出されたヒト血液の4mLを30分間15mLのガラス管でインキュベートする。インキュベーション後、室温で10分間2,000~3,000×gで遠心分離試料を行う。上部血清層を新鮮な15 mL円錐円錐遠心管に移し、氷の上に置きます。
- 25 mL の新鮮なヘパリン化 (1000 単位/mL) 全ヒト血液を 25 mL の室温 3% デキストラン -0.9% NaCl (1:1 比) で 2 つの反復 50 mL 円錐形遠心管 (チューブあたり 50 mL 総容積) を組み合わせます。各50mL円錐形チューブを穏やかに揺らして混ぜ、30分間室温で放置します。
- 室温でインキュベーションすると、2つの別々の層が表示されます。各デキストラン血混合物の最上層を新しい50mL円錐管に移し、450 x gで低いまたはブレーキなしで室温で10分間遠心分離機を移す。
- 慎重に両方の上清を吸引し、細胞ペレットを邪魔することなく廃棄します。室温0.9%NaClの2 mLで各細胞ペレットを穏やかに再懸濁し、再懸濁ペレットを単一の50 mL円錐管に組み合わせ、残りの0.9%NaCl(35mLの最終容積)を加えます。
- 慎重にハンドピペットを使用して、セル懸濁液の下に1.077 g/mL密度勾配溶液の室温10 mLを下敷き。450 x gでスピンし、ブレーキが低いかブレーキなしで室温で30分間回転します。細胞ペレットを邪魔することなく、上清を穏やかに吸引する。上清は、先に説明した14のように回収できる末梢血単核細胞を含有する。
- 室温の水の20 mLで細胞ペレットを再サスペンドすることによって赤血球をリスする。30sのためにチューブを揺らして穏やかに混ぜます。赤血球のリンパは濁度の明確な減少を伴うであろう。
- 直ちに1.8%NaCl(室温[RT])の20 mLを加え、450×gで遠心分離試料を室温で10分間加えます。
注:PMNの収率を最大化し、PMNリシスおよび/または活性化を防ぐために、赤血球リシスの後にPMNが単独で水中に残される時間を最小限に抑することが重要です。 - 細胞ペレットを邪魔することなく、慎重に上清を吸引します。細胞ペレットをRT RPMI 1640培地の2mLで軽く再サスペンドし、氷の上に置きます。
- ヘモサイトメーターを使用して細胞をカウントします。精製されたPMNを氷冷RPMIで1 x 107セル/mLの濃度で再サスペンドし、氷の上に置いておきます。
- 精製PMN(1 x 106細胞)の100μLと、2つの反復フローサイトメトリーチューブに1μLのヨウ化プロピジウム染色を含む300°Lの氷冷ダルベッコのリン酸緩衝生理食塩水(DPBS)を組み合わせます。血漿膜損傷に対する陽性制御を行うには、40μLの0.5%Triton X-100溶液をフローサイトメトリーチューブの1つに加え、十分に混合します。
- フローサイトメトリーを使用して、精製細胞の前方散乱、側散乱、およびヨウ化プロピジウム染色(535/617 nmでの励起/発光最大値)を測定します(図1)。
注:前方および側面散乱解析は、リンパ球および単球の望ましくない集団を同定する。ヨウ化プロピジウムは、妥協した形質膜を有する細胞を染色し、ヨウ化プロピジウム陽性細胞の集団を顕著にした精製PMNのみを使用すべきではない。これらの研究では、精製PMNは、精製された細胞の>98%とヨウ化プロピジウムに対して<5%染色陽性を含む場合にのみ使用された。 - DPBSで希釈した20%単離ヒト血清の100μLでこのアッセイに使用される個々のウェルをコーティングすることにより、PMN細胞傷害性アッセイ用の96ウェルプレートを準備します。
メモ:PMNをプラスチックまたはガラスに直接めっきすると、細胞が活性化します。メディアのみを受信する少なくとも 1 つの負のコントロールウェルと、0.05% Triton X-100 を受け取る少なくとも 1 つの正のコントロールウェルを含めてください。 - プレートを37°Cで30分間インキュベートします。インキュベーション後、コーティングした井戸を氷冷DPBSで2回洗浄し、余分な血清を除去します。プレートを上下逆さまに軽くタップして、残留DPBSを取り除き、氷の上に置きます。
- 精製されたヒトPMNを1 x 107セル/mLで100μLをコーティングされた各ウェル(1 x 106 PMN/ウェル)にゆっくりと加えます。PMNが少なくとも5分間氷上のプレートをインキュベートして井戸に沈着することを許可します。
2. ヒト多形核白血球に対するS.アウレウス細胞外タンパク質の細胞毒性アッセイ
- 培養S.アウレウスは、37°Cに設定された振とうインキュベーターを用いてトリプティック大豆スープ(TSB)で一晩培養する。これらの研究では、別々の150 mLエルレンマイヤーフラスコ中のTSBの20mLを、S.アウレウス株USA300またはUSA300ΔsaeR/Sの凍結培養物で接種し、250rpmで振とうして約14時間成長させた。
- サブカルチャー S.アウレウスは、新鮮な媒体を用いて一晩の細菌培養の1:100希釈を行った。細菌が早期の静止成長期に達するまで振とう37°Cでインキュベートする。
注:これらの実験では、150mLエルレンマイヤーフラスコ中の20mLのトリプティック大豆ブロスを、一晩培養したUSA300またはUSA300ΔsaeR/Sの200μLで接種し、5時間250rpmで振としながら37°Cでインキュベートした。 - 細菌が早期の静止成長期に達したら、1mLのサブカルチャー S.aureusを1.5mLマイクロ遠心管に移し、室温で5分間5分間5,000×gで遠心分離機を移す。
- 遠心分離後、上清を3mLシリンジに転写する。0.22μmフィルターを通して上清を渡し、氷上の新しい1.5 mLマイクロ遠心管に入れます。
- S.アウレウスの培養に使用される氷冷媒体を用いて上清の連続希釈を行う。
注:示された実験のために、USA300およびUSA300ΔsaeR/Sからの上清は氷冷TSBとの4つの連続した1/2ログ希釈を受けた。 - ステップ1.15の氷上のPMNを含む96ウェルプレートの個々のウェルに、上清サンプルまたはメディアのみを(負および正のコントロールの場合)ゆっくりと追加します。これらの実験のために、USA300またはUSA300ΔsaeR/S上清サンプルの10μLを各ウェルに添加した。穏やかにロックプレートは、井戸に上清を配布し、37°でインキュベートします。
- 希望の時間に、インキュベーターからプレートを取り出し、氷の上に置きます。正のコントロールによく0.5%トリトンX-100の40 μLを加えます。
- 各ウェルでサンプルをゆっくりと上下にピペットし、プレートに付着したすべてのPMNを完全に取り除き、300μLの氷冷DPBSを含む氷上のサイトメトリーチューブをフローするようにサンプルを移します。
- フローサイトメトリーを用いてヨウ化プロピジウム陽性PMNの割合を測定する(図2A)。DNAに結合すると、ヨウ化プロピジウムは535/617 nmで励起/放出を有する。
3. 食細胞症後のヒト多形核白血球に対するS.アウレウス細胞毒性アッセイ
注:600 nm(OD600)の光学密度で定義された成長曲線と細菌の濃度は、このアッセイを開始する前に試験されるS.アウレウス株のために経験的に決定されなければならない。これらの実験の成功は、サブ培養細菌のOD600を使用して中等指数成長期に試験された各S.aureus株の等濃度の一貫した収穫を必要とする。
- ステップ2.1.1および2.1.2に記載されているように、S.アウレウス株およびサブカルチャー細菌の一晩培養を開始する。
- 1mLのマイクロ遠心管に1mLの培養細菌を移し、室温で5分間5,000×gで遠心分離することにより、培養中指数成長に達した場合にサブカルチャー S.アウレウスを収穫した。
注:当社の成長条件下では、USA300およびUSA300ΔsaeR/Sは、インキュベーション6の約135分後に中等指数成長期に達しました。 - 上清を吸引し、ペレット化された細菌をDPBSの1mLに再び沈下し、試料を30sでボルテックスし、室温で5分間5,000×gで遠心分離する。
- オプソニゼーションS.アウレウスは、DPBSで希釈した20%ヒト血清の1mLで細菌ペレットを再懸濁し、15分間攪拌で37°Cでインキュベートする。
- 遠心分離機は室温で5分間5,000 x gで細菌をオプソン化した。上清を吸引して遠心分離した後にS.aureusを洗浄し、ペレット化された細菌を1mL DPBSに再懸濁し、次いで細菌ペレットが完全に分解され、さらに30秒になるまでサンプルをボルテックスする。室温で5分間5,000×gで遠心分離細菌。
- 1 mL RPMIでオプソニドS.アウレウス株を再懸濁し、細菌ペレットが完全に分解されるまでサンプルをボルテックスし、さらに30sのために氷の上に細菌を置きます。
- 氷冷RPMIで所望の濃度にオプソニ化S.アウレウス株を希釈する。30sのための渦と氷の上に置きます。
- トリプティック大豆寒天に細菌の1:10連続希釈をめっきすることにより、オプソニングS.アウレウスの濃度を確認します。
注:このアッセイに使用される細菌の濃度の違いは、その後のPMN形質膜透過性(図3A)に大きな影響を与える可能性があるため、試験された各株の濃度が実験ごとに決定され、株間で同等であることは非常に重要です。 - ステップ1.14から氷上の96ウェルプレートのPMNに、各S.aureus株またはRPMI(正と負のコントロールの場合)の100 μL/ウェルをゆっくりと追加します。穏やかに岩板は、井戸にS.アウレウスを配布します。
- 食細胞症を同期させるのは、プレートを500×gで遠心分離し、4°C15で8分間分間同期させる。遠心分離直後の37°でプレートをインキュベートする(T =0)。
- 希望の時に、インキュベーターからプレートを取り出し、氷の上に置きます。正のコントロールによく0.5%トリトンX-100の40 μLを加えます。
- 各ウェルでサンプルをゆっくりと上下にピペットし、プレートに付着したすべてのPMNを完全に取り除き、200μLの氷冷DPBSを含む氷上に細胞測定チューブを流し、ヨウ化プロピジウムを1μLで流します。
- ステップ2.9に記載のフローサイトメトリーを用いてヨウ化プロピジウム染色のサンプルを分析する。
結果
我々は、MRSA PFGE型USA300およびこの株におけるsaeR/Sの等生欠欠変異体(USA300ΔsaeR/S)を用いてヒトPMNに対するS.aureusの細胞毒性を比較的定量するために上記の手順を使用する方法を実証した6.このプロトコルのセクション1に記載の手順を用いて単離されたPMNをヨウ化プロピジウムで染色し、フローサイトメトリーを用いて調べた。前方および側方散乱プロットは、単球またはリンパ球による精製PMNの汚染を例示するために使用され(図1A、B)およびPMN完全性は、ヨウ化プロピジウム染色を用いて決定した(図1C)。ヒトPMN精製の記載された方法は、一貫して0.5 x 107〜1x 108 PMNを生み出すことができ、それは>98%純粋で、>95%ヨウ化プロピジウム陰性である。
USA300およびUSA300ΔsaeR/Sによって産生される細胞外タンパク質の細胞毒性を、このプロトコルのセクション2に記載された手順に従って精製PMN(図2)に対して試験した。これらの実験は、USA300によって産生される細胞外タンパク質による中毒の30分後に精製されたPMNのヨウ化プロピジウム染色における濃度依存的な増加を示す(図2B)。これまでの研究では、SaeR/S 2成分系がヒトPMN6、10、11、16を標的とする多数の二成分ロイコシジンの発現にとって重要であることを実証している。これらの以前の知見と一致して、USA300ΔsaeR/Sによって産生される細胞外タンパク質への曝露後に、ヨウ化プロピジウム陽性PMNが検出されたごくわずかである(図2B)。さらなる実験は、約30分後にめっきされたUSA300細胞外タンパク質による中毒後のリンパの割合の着実な増加を実証した(図2C)。ヒトPMNの最小リンパは、USA300ΔsaeR/Sによって産生される細胞外タンパク質への曝露後、すべての時点で指摘された。これらの結果は、ヒトPMNに対する細胞外タンパク質による細胞傷害性の相対的定量に対するこのアッセイの有用性を示す。
このプロトコルのセクション3に記載されている食細胞症に続くヒトPMNに対するS.aureus細胞傷害性アッセイを用いて、USA300およびUSA300ΔsaeR/Sを試験した(図3)。USA300の食細胞症後90分でヨウ化プロピジウム陽性PMNの割合の濃度依存的な増加が観察された(図3A)。USA300ΔsaeR/Sの食素細胞症に続いてヨウ化プロピジウム陽性であったPMNの割合で有意な減少が認められた(図3A)、SaeR/Sの2成分系を示す他の結果を支持することは、ヒトPMNに対するS.aureusの細胞傷害性にとって重要である(図2)7、11。図3Aで既に述べたように、S.aureus濃度の違いは、食細胞症後のPMNリシスに顕著な影響を及ぼす。これらの各実験で使用されたUSA300およびUSA300ΔsaeR/S接種の列挙は、これらの株間の細胞傷害性のコントラストが使用される細菌の濃度の違いによるものではないことを実証した(図3B)。これらの知見は、食細胞症後のヒトPMNに対するS.オーレウス細胞傷害性アッセイを、ヒトPMN血漿膜完全性を損なう異なるS.aureus株の能力を評価するためにどのように使用できるかを示す。

図1:精製PMNのフローサイトメトリー分析(A)精製ヒトPMNおよび(B)PMNの代表的なフローサイトメトリードットプロットは、末梢血単核細胞で意図的に汚染された。(C) 代表的なフローサイトメトリーヒストグラムは、最小限のヨウ化プロピジウム染色を実証する(<1%)0.05% Triton X-100 (赤色のシェーディング) で処理された PMN と比較して、精製 PMN (シェーディング グレー)の。この図の大きなバージョンを表示するには、ここをクリックしてください。
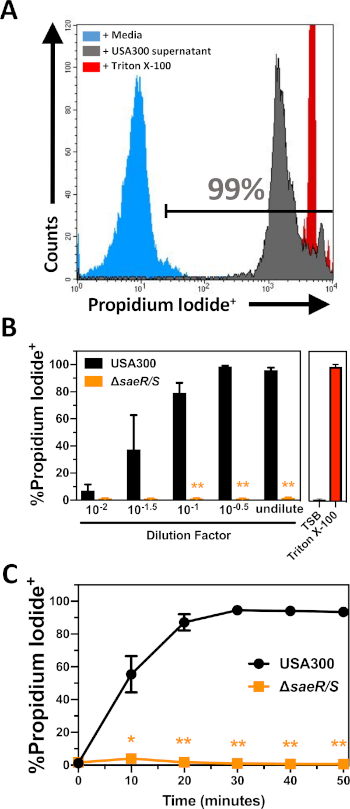
図2:S.アウレウスによって産生される細胞外タンパク質に酔い込んだPMNのフローサイトメトリー分析(A)代表的なフローサイトメトリーヒストグラムは、メディアコントロール(シェーディングブルー)によるインキュベーションの30分後にヨウ化プロピジウムで染色されたPMNのサイトメトリーヒストグラム、1:110(シェーディンググレー)の最終濃度でUSA300上清を濾過し、または0.05%トリトンX-100(陰の赤い陰の)を濾過した。(B)異なる濃度のUSA300またはUSA300°s上清を有するインキュベーションの30分後のヨウ化プロピジウム陽性PMNの割合。(C) ヨウ化プロピジウム陽性PMNの割合は、USA300またはUSA300°sを用いたインキュベーション後の経時の割合で、最終濃度1:110でデータは、両側t検定によって決定される*p ≤ 0.05および**p ≤ 0.005を用いた少なくとも3つの別々の実験の平均±SEMとして提示される。この図の大きなバージョンを表示するには、ここをクリックしてください。
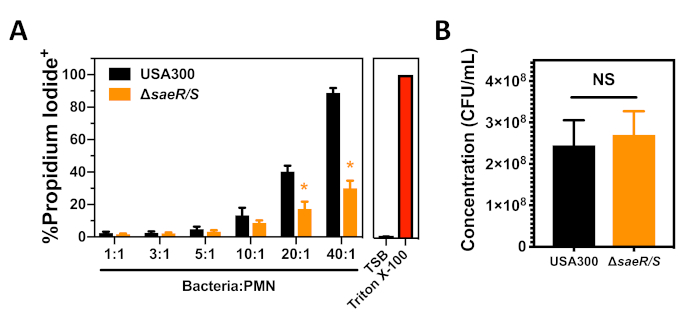
図3:S.アウレウスの食細胞症に続くPMNのフローサイトメトリー分析(A) ウサ300またはUSA300の異なる濃度の貪食後90分後にヨウ化プロピジウム陽性PMNの割合は、saeR/S. (B)パネルAに示す実験に用いられるOpson化S.アウレラス株の濃度は、p≤ 0.01で4回の別々の実験の平均±SEMとして提示される。この図の大きなバージョンを表示するには、ここをクリックしてください。
ディスカッション
このプロトコルは、ヒト血液からのPMNの精製と、これらの重要な自然免疫細胞に対するS.アウレウスの細胞毒性を定量するためにヨウ化プロピジウムを使用する2つの異なるアッセイを記述する。これらの手順の成功は、精製されたPMNの品質と、この病原体によって産生されるS.aureusおよび細胞外タンパク質の適切な調製に依存する。PMNの単離のためには、内毒素汚染のない試薬を使用し、細胞製剤を穏やかに処理し、細胞を適切な温度に保つことによって、精製中および精製後のPMN活性化を最小限に抑することが重要です。PMNの活性化を示す徴候は、精製中および単離された細胞の5%以上がヨウ化プロピジウムに対して陽性を染色する場合に細胞の塊を含む。PMNの寿命は比較的短いため、これらの細胞はヒトの血液から単離し、同じ日に検査されなければならない。PMNは、精製後に3時間以上氷の上に放置すると、自発的なアポトーシスの徴候を示し始めます。前述したように、すべてのPMN調製物は、単離細胞の純度と完全性を確保するために、前方および側散乱のフローサイトメトリー分析とヨウ化プロピジウム染色を使用して慎重に評価することが非常に重要です。
S.アウレウスによる二成分ロイコシジンの発現は、このプロトコルに記載されたアッセイを用いて観察される侵害されたPMN形質膜完全性の大部分を担っている。これらの毒素およびフェノール可溶性モジュリンのような他の細孔形成ペプチドの発現の変化は、S.aureusの株間でヒトPMNに対する細胞傷害性の違いを生じ得る。 さらに、食細胞症アッセイにおけるPINに対するS.aureusの比率は、その後のPMN血漿膜透過性(図3A)に大きな影響を及ぼし、これらの実験では、サブカルチャー属細菌のOD600を用いて中等指数成長期に試験された各S.アウレウス株の等濃度の一貫した収穫が必要である。これらの考慮事項を考えると、細胞傷害性アッセイを開始する前に調べるすべての株の成長曲線を定義することが非常に重要です。インビトロで有意な増殖差を示す株を用いたS.オーレウス細胞傷害性を分析するためのこれらの方法は推奨しない。
USA300は、ヒトPMN15に対して高い細胞傷害性であることが知られており、この株におけるSaeR/Sの喪失は、ヒトPMN6、12を標的とする多数の二成分ロイコシジンの転写を劇的に減少させ、記載されたアッセイを用いて細胞傷害性を比較するための理想的なモデルを作る。しかしながら、異なるS.aureus単離物とこれらのプロトコルに詳細に記載されているパラメータとの間に広範な遺伝的変異があり、他のS.aureus株を試験する際にヒトPMNに対する細胞毒性に実質的な変化をもたらさない可能性がある。増殖条件、添加された上清の体積、またはPMNに対する細菌の比率を調整することは、S.aureusの他の株を使用してこれらの方法で成功するために必要とされ得る。
開示事項
著者たちは何も開示する必要はない。
謝辞
この研究は、米国国立衛生研究所NIH-1R56AI135039-01A1、1R21A128295-01、U54GM115371、モンタナ州立大学農業試験場からの資金、マードック慈善信託からの設備交付金によって支援されました。.
資料
| Name | Company | Catalog Number | Comments |
| 0.9% Sodium Chloride Injection, USP, 500 mL VIAFLEX Plastic Container | Baxter | 2B1323Q | PMN purification |
| 1.5 mL micro-centrifuge tubes with Snap Caps | VWR | 89000-044 | Used in washing cells |
| 1.8% Sodium Chloride Solution | Sigma-Aldrich | S5150 | PMN purification |
| 12x75mm Culture tubes | VWR | 60818-430 | Used as flow cytometry tubes |
| 20% (w/w) Dextran | Sigma-Aldrich | D8802 | PMN purification |
| 3125 Hand Tally Counter | Traceable Products | 3125CC | For counting cells |
| 50 mL conical centrifuge tubes | VWR | 89039-656 | For dispensing media |
| Bacto Tryptic Soy Broth, Soybean-Casein Digest Medium | FischerScientific | 211823 | For growing cell cultures |
| BD Disposable Syringes with Luer-Lok Tips, 3 mL | FischerScientific | BD 309657 | For filtering supernatants |
| Bright-Line Hemocytometer | Sigma-Aldrich | Z359629 | Cell counting apparatus |
| DPBS, 1x (Dulbecco's Phosphate Buffered Saline) with calcium and magnesium | Corning | 21-030-CV | Used in washing cells |
| Ficoll-Paque PLUS | GE Healthcare | 17-1440-02 | PMN purification |
| Fisherbrand Sterile Polystyrene Disposable Serological Pipets | FischerScientific | 13-678-11E | For aspirating liquid |
| Greiner CELLSTAR 96 well plates | Millipore Sigma | M0687 | Plate for holding experimental samples |
| OMICRON Syringe Filters | Omicron Scientific | SFPV13R | For filtering supernatants |
| Propidium iodide | ThermoFisher Scientific | P3566 | Membrane impermeable DNA stain |
| PYREX Brand 4980 Erlenmeyer Flasks | Cole-Parmer | EW-34503-24 | For growing cell cultures |
| RPMI 1640, 1X without L-glutamine, phenol red | Corning | 17-105-CV | Used in resuspending cells |
| Sterile Water for Irrigation, USP | Baxter | 2F7113 | PMN purification |
| The Pipette Pump | Bel-Art Products | F37898 | For aspirating liquid |
| Triton X-100 | Sigma-Aldrich | X100 | Membrane integrity positive control |
参考文献
- Foster, T. J., Geoghegan, J. A., Ganesh, V. K., Höök, M. Adhesion, invasion and evasion: The many functions of the surface proteins of Staphylococcus aureus. Nature Reviews Microbiology. , (2014).
- Thammavongsa, V., Kim, H. K., Missiakas, D., Schneewind, O. Staphylococcal manipulation of host immune responses. Nature Reviews Microbiology. 13 (9), 529-543 (2015).
- Otto, M. Staphylococcus aureus toxins. Current Opinion in Microbiology. , (2014).
- Guerra, F. E., Borgogna, T. R., Patel, D. M., Sward, E. W., Voyich, J. M. Epic Immune Battles of History: Neutrophils vs. Staphylococcus aureus. Frontiers in Cellular and Infection Microbiology. 7, (2017).
- Nygaard, T., Malachowa, N., Kobayashi, S. D., DeLeo, F. R. Phagocytes. Management of Infections in the Immunocompromised Host. , 1-25 (2018).
- Nygaard, T. K., Pallister, K. B., Ruzevich, P., Griffith, S., Vuong, C., Voyich, J. M. SaeR Binds a Consensus Sequence within Virulence Gene Promoters to Advance USA300 Pathogenesis. The Journal of Infectious Diseases. 201 (2), 241-254 (2010).
- Voyich, J. M., et al. The SaeR/S gene regulatory system is essential for innate immune evasion by Staphylococcus aureus. J Infect Dis. 199 (11), 1698-1706 (2009).
- Borgogna, T. R., et al. Secondary Bacterial Pneumonia by Staphylococcus aureus Following Influenza A Infection Is SaeR/S Dependent. The Journal of Infectious Diseases. , (2018).
- Guerra, F. E., et al. Staphylococcus aureus SaeR/S-regulated factors reduce human neutrophil reactive oxygen species production. Journal of Leukocyte Biology. 100, 1-6 (2016).
- Zurek, O. W., et al. The role of innate immunity in promoting SaeR/S-mediated virulence in Staphylococcus aureus. J Innate Immun. 6 (1), 21-30 (2014).
- Nygaard, T. K., et al. Aspartic Acid Residue 51 of SaeR Is Essential for Staphylococcus aureus Virulence. Frontiers in Microbiology. 9, 3085 (2018).
- Spaan, A. N., Van Strijp, J. A. G., Torres, V. J. Leukocidins: Staphylococcal bi-component pore-forming toxins find their receptors. Nature Reviews Microbiology. , (2017).
- Bøyum, A. Isolation of mononuclear cells and granulocytes from human blood. Scandinavian Journal of Clinical and Laboratory. , (1968).
- Nauseef, W. M. Isolation of human neutrophils from venous blood. Methods in Molecular Biology. , (2014).
- Voyich, J. M., et al. Insights into mechanisms used by Staphylococcus aureus to avoid destruction by human neutrophils. J Immunol. 175 (6), 3907-3919 (2005).
- Voyich, J. M., et al. The SaeR/S gene regulatory system is essential for innate immune evasion by Staphylococcus aureus. The Journal of Infectious Diseases. 199 (11), 1698-1706 (2009).
Erratum
Formal Correction: Erratum: Quantifying the Cytotoxicity of Staphylococcus aureus Against Human Polymorphonuclear Leukocytes
Posted by JoVE Editors on 6/10/2021. Citeable Link.
An erratum was issued for: Quantifying the Cytotoxicity of Staphylococcus aureus Against Human Polymorphonuclear Leukocytes. The title was updated.
The title was updated from:
Quantifying the Cytotoxicity of Staphyloccus aureus Against Human Polymorphonuclear Leukocytes
to:
Quantifying the Cytotoxicity of Staphylococcus aureus Against Human Polymorphonuclear Leukocytes
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved