Method Article
PAR - 클립 - RNA 단백질의 바인딩 Transcriptome 전체 바인딩 사이트를 식별하는 방법
요약
RNA의 성적표는 횡단 행동 RNA 결합 단백질 (RBPs)의 다수에 의해 중재됩니다 광범위한 posttranscriptional 규정이 적용됩니다. 여기 우리는 정확하고 transcriptome 전체 규모 RBPs의 RNA 결합 사이트를 식별할 수있는 generalizable 방법을 제시.
초록
RNA의 성적은 RNA 결합 단백질의 수백 (RBPs)와 microRNA 함유 자주 dependently 셀 타입에 표현 ribonucleoprotein의 단지 (miRNPs를.)와 상호 작용하여 포스트 transcriptional 유전자 규정의 대상이 아르 이해하는 방법을 다음과 RNA 바인딩 요소의 상호 작용은 개인 성적, 생체내 단백질 - RNA 상호 작용 1 필요의 고해상도지도의 규정에 영향을 미칩니다.
유전자, 생화학 및 전산 접근 방식의 조합은 일반적으로 RNA - RBP 또는 RNA - RNP 상호 작용을 파악하기 위해 적용됩니다. immunopurified의 RBPs과 관련된 RNAS의 Microarray 프로 파일링 (RIP - 칩) 2 transcriptome 수준 목표를 정의하지만, 그 응용 프로그램은 kinetically 안정적인 상호 작용에만 드문 경우 3,4는 RBP 인식 요소 (RRE을 식별할 수의 특성으로 제한됩니다 ) 긴 목표 RNA 이내. 더 직접적인 RBP 대상 사이트 정보 가교 RNA 세그먼트와 cDNA 시퀀싱 (CLIP) 10의 절연 다음 immunoprecipitation 7-9로 생체내의 자외선 crosslinking 5,6에 결합하여 얻을 수 있습니다. 클립 RBPs 11-17의 다수의 대상을 식별하는 데 사용되었다. 그러나, 클립 UV 254 nm의 RNA - 단백질 crosslinking의 낮은 효율에 의해 제한되며, crosslink의 위치는 어려운 배경 이외의 가교에서 UV - 가교 대상 RNA 세그먼트를 분리하고, 합성 가교 조각 이내에 쉽게 식별이되지 않습니다 RNA는 또한 샘플에 존재 조각.
우리는 높은 해상도와 셀룰러 RBPs 및 miRNPs의 transcriptome 전체 바인딩 사이트에서 확인하기 위해 강력한 세포 기반 crosslinking 접근을 개발 우리가 용어 PAR - 클립 (Photoactivatable - Ribonucleoside 강화 Crosslinking 및 Immunoprecipitation) (개요에 대한 그림. 1A를 참조하십시오 방법). 방법은 살아있는 세포에 의해 초기 RNA의 성적에 같은 4 - thiouridine (4 - SU)과 6 - thioguanosine (6 - SG)로 photoreactive ribonucleoside의 analogs의 결합에 의존하고 있습니다. 365 NM의 자외선에 의한 세포의 방사선이 상호 작용 RBPs에 photoreactive 뉴클레오 - 라벨 세포 RNAS의 효율적 crosslinking을 유도. 관심 RBP의 Immunoprecipitation은 가교와 coimmunoprecipitated RNA의 분리옵니다. 절연 RNA는 cDNA 라이브러리로 변환하고 깊은 Solexa 기술을 사용하여 합성 수 있습니다. PAR - 클립 준비한 cDNA 라이브러리 중 하나 특징은 crosslinking의 정확한 위치가 합성 cDNA에 거주하는 돌연변이에 의해 식별 될 수있다는 것이다. 변이를 아데노신에 구아 노신 6 - SG 결과를 사용하는 반면 cytidine 전환 4 - SU을 사용하여, 가교 시퀀스 thymidine. 가교 시퀀스에있는 돌연변이의 존재는 그것이 가능한 풍부한 휴대 RNAS에서 파생 시퀀스의 배경에서 분리 수 있습니다.
다양한 RNA 바인딩 단백질의 숫자 방법의 응용은 Hafner 외에 보도되었다. 18
프로토콜
아래의 프로토콜 HEK293 세포가 깃발을 표현 / doxycycline와 유도시 IGF2BP1을 HA - 태그에 대한 PAR - 클립 절차를 설명합니다. 우리는 immunoprecipitation를위한 안티 - 플래그 항체를 사용합니다.
PAR - 클립 immunoprecipitation를위한 효율적인 항체를 사용할 경우 모든 세포주 관심의 RNA 결합 단백질 (RBP)를 태그가 지정되지 않은 내생의 감지 수준을 표현과 함께 작동합니다.
확대 셀
- 성장 매체 FlpIn-HEK293/TO/FLAG/HA-IGF2BP1 세포를 확장합니다. 우리는 출발점으로 100-400 X 10 6 세포 (약 10-40 15cm의 세포 배양 접시) 사이에 사용하는 것이 좋습니다. 약 80 % confluency로 성장합니다.
- crosslinking 전에 14 H는 직접 세포 배양 매체 100 μm의의 최종 농도 (1 M 4 thiouridine 주식 솔루션 1:1000 V / V)에) 4 thiouridine를 추가하고 B) 국기 / HA의 표현을 유도 doxycycline (10 MG / ML doxycycline 주식 솔루션의 1:10,000 V / V) 1 μg / ML를 추가로 IGF2BP1 태그. 참고 : 대신 4 thiouridine의 당신은 또한 6 thioguanosine 100 μm의를 사용할 수 있습니다.
UV - Crosslinking
- 판 당 10 ML 얼음처럼 차가운 PBS로 세포를 한 번 씻고 완전히 PBS를 제거합니다.
- 얼음 0.15 J / cm 2의 365 nm의 Stratalinker 2400에서 자외선 (Stratagene) 또는 유사한 장치와 덮개 비추다있는 트레이에 플레이스 번호판입니다.
- 50 ML의 원심 분리 튜브에 판, 전송 당 1 ML PBS에서 고무 경찰과 세포를 긁어 4 ° C에서 5 분 500 XG에서 원심 분리하여 수집하고 뜨는 폐기하십시오. 100 X 10 6 HEK293 세포 (10 15cm 접시) 약 얻을 것입니다. 서부 유럽 표준시 세포 펠렛 1 ML.
- (옵션)가 세포 lysis와 직접 계속하기를 원하지 않는다면, 충격 -80에서 액체 질소와 매장의 셀입니다 펠렛 ° C.를 동결 세포 펠렛은 최소한 12 개월 저장할 수 있습니다.
세포 용해와 RNaseT1 다이제스트
- 1X NP40 용해 버퍼 3 권 가교 세포의 세포 펠렛을 타고 10 분 얼음에 품어.
- 4 15 분 13,000 XG에서 원심 분리에 의해 삭제 세포 lysate ° C.
- 0.2 μm의 멤브레인 필터 주사기 (팔 Acrodisc 또는 이에 상응하는 금액)를 통해 필터링하여 더욱 lysate를 삭제합니다.
- 22 1 U / 15 분 물 목욕에 μl와 부화 ° C.의 최종 농도 RNase T1을 (Fermentas, 10,000 U / μl) 추가 계속하기 전에 얼음 5 분 이후 쿨 반응.
Immunoprecipitation 및 가교 대상 RNA 조각의 복구
자기 분리기를 사용하여
밖으로 건조에서 자기 구슬을 방지하기 위해 샘플 준비 전반에 걸쳐 다음 지침을 따르십시오.
- 1 2 분 동안 자기 증언대에 구슬이 들어있는 튜브를 놓습니다.
- 튜브는 자기 기호에있는 동안 튜브에 버퍼를 추가합니다.
- 튜브 뚜껑, 자석 구분에서 제거하고, 구슬을 resuspend. 당신은 손가락으로 튜브를 flicking하여 구슬을 resuspend 또는 5 6 세트 vortexer을 사용할 수 있습니다.
- 튜브 뚜껑에 남아있을 수있는 구슬을 수집하기 위해 간단히 원심 분리기.
- 필요에 따라 1-4 단계를 반복합니다.
자기 구슬의 준비
- Dynabeads의 단백질 G 자성 입자의 10 μl (Invitrogen) 당 ML 세포 lysate를 전송 (이것은되어야 일반적인 실험을 위해 약. 구슬 40 50 μl) 1.5 ML의 microfuge 튜브 있습니다. 구연 산염 인산 버퍼 1 ML로 두 번 구슬을 씻으십시오.
- 비드 정지의 원래 볼륨에 비해 구연 산염 인산 버퍼의 두 배 볼륨 Resuspend.
- 안티 - 플래그 M2 단클론 항체의 0.25 μg (시그마) 실온에서 40 분에 회전 바퀴에서 당 ML 서스펜션과 부화를 추가합니다.
- 언바운드 항체를 제거하는 구연 산염 인산 버퍼 1 ML에 두 구슬을 씻으십시오.
- 비드 정지의 원래 볼륨에 비해 구연 산염 인산 버퍼의 두 볼륨에 비즈를 Resuspend.
Immunoprecipitation (IP), 둘째 RNase T1의 소화 및 dephosphorylation
- 부분 RNase T1 취급 세포 lysate의 ML 당 신선한 항체 - 복합 자석 구슬 20 μl를 추가하고 4 1 H에 대한 회전 바퀴 15 ML의 원심 분리 튜브에 품어 ° C.
- 15 50 ML 원심 분리 튜브 (Invitrogen)에 대한 자성 입자 수집기에 자기 구슬을 모아 1.5 ML의 microfuge 튜브로 전송할 수 있습니다.
- IP 세척 버퍼 1 ML에 구슬에게 3 번 씻으십시오.
- 100 U / μl의 최종 농도 RNaseT1을 (Fermentas, 10,000 U / μl) 추가 22 15 분 물 목욕에 비드 현탁액을 품어 ° C. 얼음 이후 쿨5 분.
- 높은 소금 세척 버퍼 1 ML에 구슬에게 3 번 씻으십시오.
- dephosphorylation 버퍼 1 볼륨에 Resuspend 비즈
- 0.5 U / μl의 최종 농도 송아지 장 알칼리성 인산 가수 분해 효소 (채워, 코)을 추가, 37 10 분 정학을 품어 ° C.
- 인산 가수 분해 효소 세척 버퍼 1 ML 두 번 구슬 와시
- 두 폴리 뉴클레오 타이드 키나제 (PNK) 버퍼에 DTT (효소 반응에 필요한 DTT 농도 자기 구슬을 손상 정도로 높습니다)하지 않고 구슬을 씻으십시오.
- PNK 버퍼 중 하나가 원래 비즈 볼륨 Resuspend 비즈
immunoprecipitated 단백질 가교 RNA 세그먼트의 Radiolabeling
- 위에서 설명한 비드 중지, 1 U / 한 원래의 구슬 볼륨 μl을 0.5 μCi / μl와 T4 PNK의 최종 농도 (코)에 Υ - 32 P - ATP를 추가합니다. 37 30 분 정학을 품어 ° C.
- 100 μm의의 최종 농도를 구하고 37 또 다른 5 분 부화되지 않은 방사성 ATP를 추가 ° C.
- DTT없이 PNK 버퍼 800 μl와 자성 비즈에게 5 번 씻으십시오.
- SDS - PAGE 로딩 버퍼의 70 μl의 구슬을 Resuspend.
겔 조각에서 SDS - PAGE와 가교 RNA - 단백질 단지의 electroelution
- 95에서 열 블록에서 5 분 radiolabeled 정학을 품어 ° C 변성 및 가교 RNA와 와동과 immunoprecipitated RBP을 해제합니다.
- 분리기에 자성 비즈를 제거하고 깨끗한 1.5 ML의 microfuge 관에 뜨는을 전송하기만하면됩니다.
- 40 뜨는의 μl 당 우물 Novex 비스 - 트리스 4-12% (Invitrogen) 프리 캐스트의 polyacrylamide 젤을로드하고 200 55 분에 대한 겔을 실행 V.
- 겔 챔버를 해체하고 한 접시에 장착 떠나, 젤 해체. phosphorimager 용지 출력에 젤의 정렬을 촉진하기 위하여, 우리는 젤의 네 모퉁이의 세에 불균형 작은 세 개의 방사성 겔 조각을 이온 주입하는 것이 좋습니다. 방사성 젤 조각는 이전에 다음 ID로 radiolabeled 합성 oligonucleotides를 정화하는 데 사용되었다 젤에서 수집한 수 있습니다. 오염을 피하기 위해 플라스틱 필름 (예 : 사란 랩)에서 젤 싸서.
- 1 H에 대한 무시 phosphorimager 화면 젤 노출하고 phosphorimager에 시각화.
- 오리 엔테이션에 대한 이식 겔 조각을 사용하여 phosphorimager의 인쇄물 위에 젤 맞춥니다. RBP의 예상 크기 (IGF2BP1 약. 75 KDA)에 대응하고 D - 튜브 Dialyzer 미디 튜브로 전송 800 μl 1X SDS 실행 버퍼를 추가 밴드를 잘라 버릴거야.
- 2 H. 100 V에서 버퍼를 실행 1X SDS의 가교 RNA - RBP 복잡한 Electroelute 겔에서 excised 및 제조 업체의 지시에 따라 800 μl SDS 실행 버퍼에 D - 튜브 Dialyzer 미디 (Novagen)에 electroeluted.
Proteinase K의 소화
- 1.2 MG / ML의 최종 농도 Proteinase K (로체)의 또한 다음 electroeluate에 대하여 2X Proteinase K 버퍼의 동일한 볼륨을 추가합니다. 55 30 분 품어 ° C.
- 산성 페놀 / 클로로포름 / IAA 추출 (25:24:1, 산도 4.0) 클로로포름 추출에 의해 다음에 의해 RNA를 복구합니다. 글리코겐 1 μl를 (10 MG / ML 주식) 추가 에탄올 3 볼륨을 추가하여 RNA를 침전. 10.5 μl 물에 펠렛을 디졸브.
cDNA 라이브러리 준비와 깊은 시퀀싱
원래 작은 규제 RNAS 19 복제에 대한 설명 표준 cDNA 라이브러리 준비 프로토콜을 통해 복구된 RNA를 운반. 복구 RNA의 10.5 μl를 사용하여 20 μl 규모에서 설명하는 것처럼 첫 번째 단계, 3 '어댑터 내고이 진행되었습니다. Solexa 순서 어댑터 설명 집합을 사용합니다. 복구 RNA의 양에 따라 삽입하지 않고 5' - 어댑터 - 3' - 어댑터 제품은 추가 PCR 밴드로 cDNA의 증폭 후 검색됩니다. 이러한 경우에는, 소비세 3 % NuSieve에서 예상 크기의 긴 PCR 제품은 낮은 용융 점 아가로 오스 겔, Solexa 기술을 사용하여 GelElute 키트 (Qiagen)와 순서를 사용하여 겔 조각에서 PCR 제품을 elute. 한 Solexa 순서 실행은 보통 6 천만 순서 사이 내실수 RNA 바인딩 단백질의 바인딩 사이트의 transcriptome 넓은 범위에 대한 충분한 것을 읽습니다.
Bioinformatic 분석
순서주의 bioinformatic 분석 순서 대 번역되지 않은 코딩, 요구 사항 등 RNA 인식 요소 RBP이 가진 기본 바인딩 지역 (exonic 대 intronic으로 심사 RBP에 대한 RNA 구속력이 사이트에 의미있는 통찰력을 얻기 위해해야 할 일이 읽습니다 순서). 읽는 순서는 게놈과 동부 표준시 데이터베이스에 대해 정렬해야합니다. 우리는 일반적으로 읽습니다 mappi를 사용하여을 한 불일치, 삽입 또는 시퀀스 클러스터 구축을 삭제까지 고유 게놈에 NG가 나서 더 이상 분석 수 읽습니다. 클러스터 합성의 특성 변이의 빈도는 6 - SG를 사용할 때 전환 4 - SU와 G를 사용하는 경우, C 전환하기 위해 T를 읽는 성공적으로 가교 시퀀스 나타내는 있습니다. 우리의 경험에서 4 - SU으로 표시 uncrosslinked RNAS는 약 20 %의 배경 돌연변이 속도를 보여줍니다. 이 속도는 약으로 증가합니다. crosslinking시 50~80%.
bioinformatic 분석에 대한 자세한 설명은 Hafner 외 의해 출판의 보충 자료에서 찾을 수 있습니다. 18
선택 단계
총 RNA에 4 thiouridine의 정관 수준의 결정
안정 100 μm의 사전 수확 4SU 16 H와 보충 매체 성장 후 관심 RBP을 표현하는 세포 라인에서 총 RNA를 분리. 제어로, 수확 전지는 4SU 또한없는 성장. 제조 업체의 지침에 따라 세탁 세포 펠렛을 Trizol 시약 (시그마) 3 권 외에하여 총 RNA를 분리. 또한 제조 업체의 프로토콜에 따라 Qiagen RNeasy를 사용하여 총 RNA를 정화했다. RNA 분리 및 분석하는 동안 4SU의 산화를 방지하기 위해 세척 버퍼와 후속 효소 단계를 0.1 MM dithiothreitol (DTT)을 추가합니다. 다이제스트 및 HPLC 분석을 위해 하나의 nucleosides에 dephosphorylated 총 RNA는 20 전에 설명했다. 간단히, 30 μl 볼륨, 37 16 H에 대한 전체 RNA 투석을 40 μg을했다 품어 ° 0.4 U 세균 알칼리성 인산 가수 분해 효소 (생물 워싱턴)와 0.09 U의 뱀 독이와 C phosphodiesterase (워싱턴 생물). 참조 표준으로, 합성 4SU - 라벨 RNA (우리가 standardly CGUACGCGGAAUACUUCGA (4SU) U 사용) 또한 효소 소화를 완료하는 데 그것을 제목을 사용합니다. Supelco 디스커버리 C18 (보세 위상 실리카 5 μm의 입자, 250 X 4.6 mm) 반대 위상 열 (펠폰트 PA, 미국)의 HPLC에 의해 ribonucleosides의 결과 혼합물을 분리합니다. HPLC 버퍼는 3 % acetonitrile (A)와 물에 90 % acetonitrile (B)에 0.1 M TEAA 있습니다. 15 분, 20 분 0으로 10 % B, 30 분 10-100%의 B에 대한 0 % B : isocratic 그라데이션을 사용합니다. 사이에 적용 세척은 HPLC의 컬럼을 청소 실행 5 분 100 % B을 적용합니다.
대표 결과
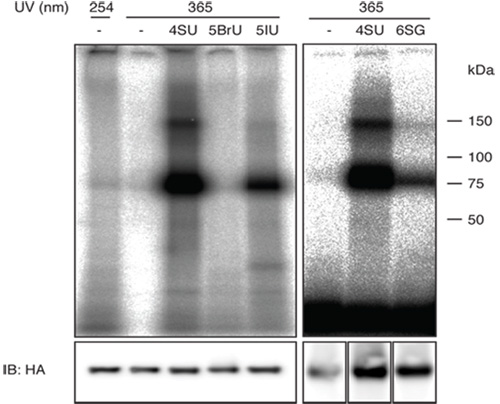
그림 1 (오른쪽 패널)은 세포 라인 플래그를 표현 / 4 - SU 6 - SG와 함께 IGF2BP1 HA - 태그와 수행 파 클립의 대표적인 결과를 보여줍니다. IGF2BP1 6 - SG의 crosslinking 효율 4 - SU에 대한 crosslinking 효율보다 낮은합니다. 낮은 crosslinking 효율 풍부한 세포 RNAS의 조각에서 파생된 시퀀스의 높은 배경에 결과되며, 따라서 덜 효율적인 photoreactive nucleosides를 사용할 때 실험을 축소 고려해야합니다.
그림 1의 왼쪽 패널은 잠재적으로 기존의 UV 254 나노미터 crosslinking에 비해 PAR - 클립에 사용할 수있는 다른 photoreactive 유리딘의 analogs를 사용하여 비교를 보여줍니다.
올바른 길이의 방사능 밴드의 강도는 당신에게 작은 RNA 순서 프로토콜 (소형의 cDNA 라이브러리 준비에 대한 단계별 설명을 통해 파 클립 실험이 효과가있다 당신이 수행하는 충분한 RNA을 고립 여부 좋은 생각을 제공합니다 RNAS 배열은) 19에서 찾을 수 있습니다. 6 - SG를 사용할 때 전환 4 - SU와 G를 사용하여 C 전환하는 합성 읽는, T의 특성 변이의 빈도는 성공적으로 가교 시퀀스 나타내는 있습니다. 우리의 경험에서 4 - SU으로 표시 uncrosslinked RNAS는 약 20 %의 배경 돌연변이 속도를 보여줍니다. 이 속도는 약으로 증가합니다. crosslinking시 50~80%.
공개
감사의 말
우리는 도움이 토론에 대한 Tuschl 연구소의 회원 감사합니다. MH는 도이쳐 Akademischer Austauschdienst (DAAD)가 지원됩니다. 이 작품은 스위스 국립 기금 부여 MZ에 # 3100A0 - 114001에 의해 지원되었다; TT는 HHMI의 조사이며, 자신의 실험실에서 연구는 NIH 보조금 GM073047과 MH08442과 스타 재단에 의해 지원되었다.
자료
버퍼 및 시약
성장 매체 HEK293 세포
- DMEM
- 10% FBS
- 이 MM L - 글루타민
- 100 U / ML 페니실린
- 100 U / ML 스트렙토 마이신
- 100 μg / ML hygromycin
- 15 μg / ML blasticidin
4 thiouridine 주식 솔루션 (1 M)
- 260.27 MG 4 thiouridine
- 1 ML DMSO
Doxycyclin 주식 (10 MG / ML)
- 10 MG doxycyclin
- 1 ML DMSO
1X NP40의 용해 버퍼
DTT와 단백 분해 효소 억제제없이 5 배 버퍼의 재고를 준비합니다. 직접 실험을하기 전에 DTT와 프로 테아제 억제제를 추가합니다.
- 50 MM HEPES, pH를 7.5
- 150 MM KCl
- 이 MM EDTA (에틸렌 다이아 민 테트라 초산)
- 1 ㎜ NaF
- 0.5 % (V / V) NP40
- 0.5 MM DTT
- 전체 EDTA (에틸렌 다이아 민 테트라 초산) - 무료 프로 테아제 억제제 칵테일 (로체)
구연 산염 인산 버퍼
- 4.7 g / L 구연산 산성
- 9.2 g / L 나 2 HPO 4
- 산도 5.0
IP - 세척 버퍼
- 50 MM HEPES - 코, 산도 7.5
- 300 MM KCl
- 0.05 % (V / V) NP40
- 0.5 MM DTT (실험 바로 앞에 추가)
- 전체 EDTA (에틸렌 다이아 민 테트라 초산) - 무료 프로 테아제 억제제 칵테일 (로체) (직접 실험을하기 전에 추가)
높은 소금 세척 버퍼
- 50 MM HEPES - 코, 산도 7.5
- 500 MM KCl
- 0.05 % (V / V) NP40
- 0.5 MM DTT (실험 바로 앞에 추가)
- 전체 EDTA (에틸렌 다이아 민 테트라 초산) - 무료 프로 테아제 억제제 칵테일 (로체) (실험 바로 앞에 추가)
Dephosphorylation 버퍼
- 50 MM 트리스 - HCL, pH를 7.9
- 100 MM NaCl
- 10 MM MgCl 2
- 1 ㎜ DTT
인산 가수 분해 효소 세척 버퍼
- 50 MM 트리스 - HCL, pH를 7.5
- 20 MM EGTA
- 0.5 % (V / V) NP40
DTT없이 폴리 뉴클레오 타이드의 키나제 (PNK) 버퍼
- 50 MM 트리스 - HCL, pH를 7.5
- 50 MM NaCl
- 10 MM MgCl 2
PNK 버퍼
- 50 MM 트리스 - HCL, pH를 7.5
- 50 MM NaCl
- 10 MM MgCl 2
- 5 MM DTT
SDS 페이지 로딩 버퍼
- 10 % 글리세롤 (V / V)
- 50 MM 트리스 - HCL, pH를 6.8
- 이 MM EDTA (에틸렌 다이아 민 테트라 초산)
- 2퍼센트 SDS (W / V)
- 100 MM DTT
- 0.1 % bromophenol 블루
2X Proteinase K 버퍼
- 100 MM 트리스 - HCL, pH를 7.5
- 150 MM NaCl
- 12.5 MM EDTA (에틸렌 다이아 민 테트라 초산)
- 2퍼센트 (W / V) SDS
참고문헌
- Keene, J. D. RNA regulons: coordination of post-transcriptional events. Nat. Rev. Genet. 8 (7), 533-533 (2007).
- Tenenbaum, S. A. Identifying mRNA subsets in messenger ribonucleoprotein complexes by using cDNA arrays. Proc. Nat. Acad. Sci. 97 (26), 14085-14085 (2000).
- Gerber, A. P. Genome-wide identification of mRNAs associated with the translational regulator PUMILIO in Drosophila melanogaster. Proc. Nat. Acad. Sci. 103 (12), 4487-4487 (2006).
- Lopez de Silanes, I. Identification of a target RNA motif for RNA-binding protein HuR. Proc. Nat. Acad. Sci. 101 (9), 2987-2987 (2004).
- Greenberg, J. R. Ultraviolet light-induced crosslinking of mRNA to proteins. Nucl. Acids Res. 6 (2), 715-715 (1979).
- Wagenmakers, A. J. Cross-linking of mRNA to proteins by irradiation of intact cells with ultraviolet light. Eur. J. Biochem. 112 (2), 323-323 (1980).
- Mayrand, S. Structure of nuclear ribonucleoprotein: identification of proteins in contact with poly(A)+ heterogeneous nuclear RNA in living HeLa cells. The Journal of Cell Biology. 90 (2), 380-380 (1981).
- Dreyfuss, G. Characterization of heterogeneous nuclear RNA-protein complexes in vivo with monoclonal antibodies. Mol. Cell. Biol. 4 (6), 1104-11 (1984).
- Adam, S. A., Dreyfuss, G. Adenovirus proteins associated with mRNA and hnRNA in infected HeLa cells. J. Virol. 61 (10), 3276-3276 (1987).
- Ule, J. CLIP identifies Nova-regulated RNA networks in the brain. Science. 302 (5648), 1212-1212 (2003).
- Licatalosi, D. D. HITS-CLIP yields genome-wide insights into brain alternative RNA processing. Nature. 456 (7221), 464-464 (2008).
- Yeo, G. W. An RNA code for the FOX2 splicing regulator revealed by mapping RNA-protein interactions in stem cells. Nat. Struct. Mol. Biol. 16 (2), 130-130 (2009).
- Sanford, J. R. Splicing factor SFRS1 recognizes a functionally diverse landscape of RNA transcripts. Genome Res. 19 (3), 381-381 (2009).
- Granneman, S. Identification of protein binding sites on U3 snoRNA and pre-rRNA by UV cross-linking and high-throughput analysis of cDNAs. Proc. Nat. Acad. Sci. , (2009).
- Guil, S., Caceres, J. F. The multifunctional RNA-binding protein hnRNP A1 is required for processing of miR-18a. Nat. Struct. Mol. Biol. 14 (7), 591-591 (2007).
- Chi, S. W. Argonaute HITS-CLIP decodes microRNA-mRNA interaction maps. Nature. 460 (7254), 479-479 (2009).
- Zisoulis, D. G. Comprehensive discovery of endogenous Argonaute binding sites in Caenorhabditis elegans. Nat. Struct. Mol. Biol. , (2010).
- Hafner, M. Transcriptome-wide identification of RNA-binding protein and microRNA target sites by PAR-CLIP. Cell. , (2010).
- Hafner, M. Identification of microRNAs and other small regulatory RNAs using cDNA library sequencing. Methods. 44 (1), 3-3 (2008).
- Andrus, A., Kuimelis, R. G. Base composition analysis of nucleosides using HPLC. Current Protocols in Nucleic Acid Chemistry. Chapter 10 (Unit 10.6), (2001).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유