Method Article
Síntese de funcionalizados 10 nm polímero-revestida com partículas de ouro para o direcionamento do endotélio e entrega da droga
Neste Artigo
Resumo
Nós descrevemos um método de síntese de nanopartículas de ouro 10 nm biocompatíveis, acrescidas por revestimento Poli-etileno glicol para a superfície. Estas partículas podem ser usados em vitro e em vivo para distribuir terapêutica a nanoescala celular e extracelular espaços que são difíceis de acesso com tamanhos convencionais de nanopartículas.
Resumo
Nanopartículas de ouro (AuNPs) têm sido amplamente utilizadas na pesquisa médica devido ao seu tamanho, biocompatibilidade e superfície pode ser modificado. Entrega de direcionamento e drogas específica são algumas das aplicações destes AuNPs, mas a captação de partículas as matrizes extracelulares endotelial propriedades defensivas cesto. Para resolver esse problema, nós descrevemos um método de síntese de nanopartículas de ouro manipulam melhorar a entrega vascular, com comprimentos de polímero para mais ajustes e personalizável de grupos funcionais. O protocolo rendimentos 2,5 nm AuNPs que são tampados com cloreto de tetrakis (hidroximetil) do phosphonium (THPC). A substituição de THPC com hétero-funcional polietileno glicol (PEG) na superfície da AuNP aumenta o raio hidrodinâmico para 10.5 nm, proporcionando vários grupos funcionais na superfície. A última parte do protocolo inclui adição opcional de um fluoróforo para permitir que o AuNPs ser visualizado sob fluorescência para controlar a absorção de nanopartículas. Diálise e liofilização foram usados para purificar e isolar o AuNPs. Essas nanopartículas fluorescentes podem ser visualizadas em experimentos in vitro e em vivo devido a biocompatível sondas PEG revestimento e fluorescente. Além disso, a escala do tamanho dessas nanopartículas tornem um candidato ideal para sondar o glicocálix sem interromper a função vasculatura normal, que pode levar a melhor entrega e terapêutica.
Introdução
Nanopartículas foram aplicadas à imagem por sua capacidade de navegar através do corpo para alcançar áreas alvo de interesse1,2e entrega da droga. As partículas podem se acumular dentro de tumores através da vasculatura gotejante ou localizar onde um ligante de destino é overexpressed e exposto. Ouro, especificamente, tornou-se um material de nanopartículas comumente utilizados devido às suas propriedades físicas e químicas únicas que afetam o transporte e lançamento de terapêutica3. Ouro é um material de nanopartículas eficaz porque sua superfície pode ser modificada para vincular a tióis e tem alta biocompatibilidade, devido à sua baixa toxicidade4. AuNPs são capazes de ser portadores de drogas grande biomolecular e foram bem sucedidos no fornecimento de peptídeos, ácidos nucleicos e proteínas, permitindo que AuNPs a ser favorável para o direcionamento de2,4.
Infelizmente, eficácia de entrega de droga de nanopartículas foi dificultada pelo glicocálix carregado negativamente, que é o casaco extracelular da membrana das células de mamíferos mais e tem tamanhos de poros de até 7 nm5,6. Este tamanho de poro é menor do que a maioria das transportadoras de drogas nanopartículas, que têm diâmetros típicos que variam de 50-200 nm. Sob condições de doença, estes poros glicocálix se tornam maiores devido à degradação, aumentando a permeabilidade através de células endoteliais. No entanto, a maioria das nanopartículas ainda são grandes demais para aproveitar esta mudança estrutural no glicocálix. Uma implicação deste tamanho desencontro é que convencionalmente tamanhos partículas não interagir favoravelmente com células endoteliais que revestem os vasos sanguíneos. Isso afeta a entrega de partículas administradas por via intravenosa em endotélio e também pode ser dito de transporte de partículas através do sangue cérebro barreira7,8,9,10.
Uma abordagem para combater esse problema é utilizar partículas menores para passar através dos pequenos poros no glicocálix. Aqui, podemos sintetizar um 10.5 nm manipulam ouro nanopartículas, que normalmente devem ser desencorajado por glicocálix intacto, saudável. Uma vez que o glicocálix começa a ficar comprometida, as nanopartículas devem penetrar facilmente as células através do aumento de tamanho dos poros. O protocolo neste trabalho detalha uma síntese de manipulam núcleo ouro revestido com PEG, o que aumenta a biocompatibilidade e reduz a liberação sistêmica4. O PEG também pode conter vários tipos de grupos funcionais, abrindo caminhos para a conjugação de direcionamento ligantes, fluorophores e terapêutica. Anteriormente publicados resultados indicam que essas nanopartículas manipulam tendem a ser tomada mais favoravelmente nas regiões de função de glicocálix endotelial interrompidos mesmo sem qualquer ativo visando4,11. Isto indica a viabilidade e a importância da utilização de partículas de tamanho correto para aplicações de entrega. O protocolo a seguir apresenta a síntese, purificação e caracterização de AuNPs o PEG-revestido (PEG-AuNP), com a discussão por adequar os grupos funcionais e conjugações de outros aplicativos.
Protocolo
1. preparação ou aquisição de soluções estoque (para ser armazenado em temperatura ambiente ou congelados até o uso)
- Prepare uma solução estoque de hidróxido de sódio (NaOH) 1M, dissolvendo-se 400 mg de NaOH em 10 mL de água ultrapura em temperatura ambiente e misturar os materiais bem.
Nota: Água ultrapura é definida como a água sem impurezas tais como partículas, bactérias, nucleases, íons ou vestígios de orgânicos. Um sistema de purificação é usado para obter a água ultrapura, resultando em sua resistividade de até 18,2 mΩ·cm, indicando uma baixa contaminação aniônica. Não se recomenda o uso de garrafas de água ultrapura comercialmente disponível. De agora em diante, esta água ultrapura será referida como a água, a menos que especificado de outra forma. - Preparar uma solução de NaOH de 6m, dissolvendo a 2,4 g de NaOH em 10 mL de água e armazenar a solução à temperatura ambiente.
- Prepare uma solução stock de 250 mM de Ácido cloroáurico (HAuCl4), dissolvendo 1 g de secas HAuCl4 em 10,16 mL de água. Dilua 1 mL de HAuCl4 de 250 mM com 9 mL de água para obter a concentração de trabalho de 25 mM HAuCl4. Armazene a solução de4 HAuCl à temperatura ambiente.
- Prepare um buffer de carbonato de 0,1 M em pH 8.8, dissolvendo 84 mg de bicarbonato de sódio em 10 mL de água e ajustar o pH a 8,8 adicionando 6 M NaOH da etapa 1.2. Armazene o buffer de carbonato na temperatura de quarto.
- Misturar 20 mL de tetrazólio sal composto, 3-(4,5-dimethylthiazol-2-yl)-5-(3-carboxymethoxyphenyl)-2-(4-sulfophenyl)-2H-tetrazolium (MTS), com um agente de estabilização, ethosulfate Fenazina (PES) (ver Tabela de materiais). Armazene a mistura MTS/PES em alíquotas (para um máximo de 10 ciclos de congelamento e descongelamento) a-20 ° C, no escuro.
2. síntese dos núcleos nanopartículas de ouro
- Preparar uma solução diluída de THPC adicionando 12 µ l de 80% THPC na água a 1 mL de água em um tubo de microcentrifugadora à temperatura ambiente.
- Fixe um balão de fundo redondo de 100 mL sobre o centro de uma placa de agitação magnética. Despeje o frasco com 45 mL de água e misture a água com 300 rpm usando uma barra pequena agitação magnética em forma de ovo. Adicione 0,5 mL de NaOH de M 1 e 1 mL de solução diluída de THPC. Continue a agitar a mistura vigorosamente por 5 min.
- Continue mexendo a mistura e adicionar 2 mL de solução de4 HAuCl de 25 mM. Mudará a cor da mistura do amarelo ao marrom escuro dentro de segundos, indicando que a formação de THPC tampado AuNPs com uma carga negativa. Agite a mistura para um 15min adicional permitir a formação completa dos núcleos ouro.
3. adição de polímero Corona em torno as nanopartículas de ouro
- Durante o período de 15 min descrito na etapa 2.3, preparar o PEG soluções dissolvendo-se cada uma das seguintes em 1 mL de água em frascos de vidro de 4 mL: 30 mg NH2-PEG-SH; 7,5 mg m-PEG-SH; 7,5 mg COOH-PEG-SH.
Nota: As concentrações resultantes devem ser de 8,8 M NH2-PEG-SH, 3,75 M m-PEG-SH e 3.75 M COOH-PEG-SH. - Depois de reduzir a velocidade de agita da solução num balão de fundo redondo de 100 rpm, adicionar o PEG soluções para a solução de THPC tampado AuNPs gota a gota. Continue a agitar a mistura suavemente durante a noite, à temperatura ambiente, para assegurar a remoção eficiente de THPC e a substituição por PEG.
- Para o próximo 72 h, use uma membrana de celulose corte de peso molecular de kDa 12-14 para urinar a mistura mexida contra um balde de 4 L de água agitada a 60 rpm. Amarre as pontas das membranas por clipes de diálise e transferir a solução através de uma pipeta.
Nota: Este processo de diálise com 12-14 kDa membrana corte remove apenas PEG não tenha reagida, THPC e outros reagentes químicos, por difusão ao longo de um gradiente de concentração. - Para manter o alto gradiente de concentração e promover a difusão contínua, trocar a água cada 2 h para as primeiras 6 horas e a cada 6-12 h para a restante 66 h.
Nota: O objetivo desta água alterar agendamento é acomodar a difusão rápida que ocorre logo no início, por causa da concentração elevada inicialmente dentro da amostra. O processo de diálise descrito acima folhas a solução de nanopartículas semi purificada, porque as nanopartículas, precipitados, agregados e outras impurezas de tamanho grande, não podem passar através dos poros da membrana corte kDa 12-14. - Filtre a solução de nanopartículas semi purificada em um tubo cónico de 50mL, usando um filtro de seringa 0,2 µm para remover os restantes precipitados, agregados e outras impurezas de tamanho grande.
- Coloque o tubo cônico em um freezer-80 ° C e permitir que a solução de PEGylated AuNP (PEG-AuNP) purificada congelar cerca de 5h.
- Use um secador de gelo para lyophilize o PEG-AuNP purificado.
- Armazene o PEG-AuNP seco, purificado a 4 ° C até o uso.
4. conjugação Fluorophores usando N-Hidroxisuccinimida (NHS) éster para os NH2 grupos sobre o PEG-AuNP
- Fixe um balão de fundo redondo de 50 mL sobre o centro de uma placa de agitação magnética. Encher o frasco com 18 mL de água e misture a água a 100 rpm usando uma barra de agitação magnética em forma de ovo.
- Pese 2 mg do PEG-AuNP liofilizado em um tubo cônico de 4 mL, usando uma escala de bancada de alta precisão. Use uma arma antiestática para eliminar a carga estática e o apego do PEG-AuNP pó na superfície do tubo. Adicione 2 mL de água para o tubo. Despeje a 2 mL de solução de PEG-AuNP o balão de fundo redondo para reconstituição em um total de 20 mL de água. Continue a agitar a mistura a 100 rpm usando uma barra de agitação magnética em forma de ovo.
- Adicionar 1 mL de 0,1 M, pH 8.8 carbonato de buffer para o 20 mL de leite reconstituído AuNP contido no balão de fundo redondo. Continue mexendo.
- Adicione 5 µ l de éster de NHS fluorescente 10 mg/mL em dimetilsulfóxido.
Nota: Qualquer tintura fluorescente pode ser usada neste processo. Misture o PEG fluorescente durante a noite. Mantê-lo em temperatura ambiente e coberto com papel de alumínio. - Para o próximo 72 h, remova excesso fluorophores usando o protocolo descrito na etapa 3.3. Brevemente, Dialize mexida mistura usando um balde de 4 L de água e uma membrana de celulose corte de peso molecular de kDa 12-14. Trocar a água a cada 2h para os primeiros 6 h e cada 6-12 h para a restante 66 h.
- Obter 1 mL a solução PEG-AuNP fluorescente purificada, deve ser usado para caracterização descrita abaixo na seção 5. Congelar e lyophilize o restante da solução para obter nanopartículas fluorescentes em forma de pó para armazenamento a 4 ° C, conforme descrito nas etapas 3.5-3.7.
- Use um filtro de seringa 0,2 µm para esterilizar e remover qualquer potenciais precipitados uma vez reconstituídos para aplicações de cultura de células.
5. caracterização de nanopartículas fluorescentes peguilado ouro
- Usando microscopia eletrônica de transmissão (TEM) para visualizar o núcleo de nanopartículas de ouro e quantificar os tamanhos
- Queda de 10 µ l da solução fluorescente PEG-AuNP purificada em uma grade TEM malha de carbono revestido.
- Depois de 5 min, use um pedaço de papel de filtro para pavio cuidadosamente o excesso de líquido fora da borda da grade TEM até um filme contendo o fluorescente que Peg-AuNPs é deixado para trás.
- Ver o PEG-AuNPs fluorescente em 80 kV e uma ampliação de 50.000-150, 000. Tire fotos digitais.
Nota: Apenas o núcleo de ouro será visível porque o PEG não é denso sobre a temperatura do elétron. - Usando um software de medição, definir a escala de medição em correlação com a barra de escala. Calcular os diâmetros de aproximadamente 20 núcleos de ouro e em seguida, determinar o diâmetro de núcleo ouro média.
Nota: O sistema de imagens TEM automaticamente coloca uma barra de escala nas fotos digitais.
- Medição de tamanho de nanopartículas hidrodinâmico usando Difusão dinâmica da luz (DLS)
- Transferi 1 mg de liofilizado AuNPs THPC-revestido em um tubo de microcentrifugadora usando a abordagem descrita na etapa 4.2. Transferi 1 mg de liofilizado PEG-AuNP num tubo separado. Adicionar 1 mL de água a cada tubo e transferir cada solução AuNP a um plástico transparente de 1 mL.
- Coloque uma cubeta num instrumento DLS e medir diâmetros hidrodinâmicos esféricos, usando o software de analisador de partícula que é incorporado ao sistema DLS.
- Traça os diâmetros hidrodinâmicos medidos usando um formato de histograma.
Nota: O histograma agrupará nanopartículas por tamanho. O maior grupo de nanopartículas esclarecerá o diâmetro que melhor descreve o tamanho da AuNPs sintetizado neste protocolo.
- Confirmação de fluorescência fluorométrica
Nota: A mesma amostra e cubeta da etapa 5.2 podem ser usados para medir o sinal fluorescente.- Remova o DLS a cubeta e inserir um spectrofluorometer. Conjunto o comprimento de onda de excitação a 633 nm e ler a fluorescência emitida sinais ao longo de uma faixa de comprimento de onda de 650-800 nm.
- Confirmar que o pico é aproximadamente 665 nm, que se correlaciona com o pico de emissão para NHS.
Nota: Ajuste os excitação e emissão de comprimentos de onda de acordo com o fluoróforo usado no processo.
- 11 para avaliar a biocompatibilidade de ensaios MTS
- Numa cultura clara de 96 poços de fundo de tecido estéril tratada placa, Pipetar 100 µ l de meio modificado águia de Dulbecco (DMEM; suplementado com 10% fetal bovino soro e 1% penicilina/estreptomicina) e 3.2 x 103 células em cada poço.
Nota: Neste estudo, as células endoteliais de rato do tecido são usadas. Um total de 21 poços são usados para permitir 3 repetições para cada uma das 7 concentrações diferentes de nanopartículas (ver passo 5.4.3 para concentrações específicas de interesse). - Permitir que as células a crescer a confluência na umidade e 5% CO2 controlada incubadoras em 37 ° C11.
- Prepare tubos microcentrifuga individuais, cada um contendo 300 µ l de DMEM com nanopartículas de várias concentrações. Este estudo requer 7 diferentes tubos de DMEM com as seguintes concentrações de PEG-AuNP: 0 µ g/mL, 10 µ g/mL, 50 µ g/mL, 100 mg/mL, 250 µ g/mL, 500 µ g/mL e 1.000 µ g/mL.
- Aspire o DMEM do tubo. Encha os poços em triplicado com 100 µ l de mídia DMEM contendo 0, 10, 50, 100, 250, 500 ou 1.000 µ g/mL de AuNP.
- Permitir que as células e nanopartículas de co incubar durante um período pré-determinado de tempo, aqui por 16 h.
- Perto do final do período de incubação, descongele mistura da etapa 1,5 MTS/PES.
- Após a incubação, Aspire o DMEM e as nanopartículas suspensas, vagamente anexadas dos poços. Adicione 100 µ l de DMEM fresco juntamente com 20 µ l de solução MTS/PES para obter 1:5 MTS/PES para relação DMEM de acordo com o protocolo do fabricante. Incube as celulas com MTS/PES a 37 ° C por 2 h.
Nota: Este tempo de incubação de 2 h é determinado pela atividade metabólica das células endoteliais e pode ser aumentado para até 4 h para outros tipos de células. No prazo de 2 h, a MTS é metabolizada pelas células endoteliais na colorida formazan que mistura com o DMEM. A probabilidade de viabilidade celular e biocompatibilidade do PEG-AuNP serão demonstradas com formazan mais colorida. Toxicidade do PEG-AuNP e a chance de que as células estão morrendo aparece com uma cor menos intensa. - Executar análise colorimétrica de cada poço por leitura de absorvância a 492 nm com um leitor de placas compatíveis.
- Para cada concentração de nanopartículas, calcule a absorbância média a valores de absorvância triplicado. Divida a absorvância média pelo valor obtido a partir de uma média de absorbância em poços contendo 0 µ g/mL nanopartículas.
Nota: Estes poços que não contêm nenhuma AuNPs servem como controles para calcular porcentagem viabilidade celular em resposta ao tratamento de nanopartículas administrado em outros poços.
- Numa cultura clara de 96 poços de fundo de tecido estéril tratada placa, Pipetar 100 µ l de meio modificado águia de Dulbecco (DMEM; suplementado com 10% fetal bovino soro e 1% penicilina/estreptomicina) e 3.2 x 103 células em cada poço.
- Avaliação de microscopia confocal de fluorescência de captação de nanopartículas nas células endoteliais aderentes com glicocálix intacta ou disfuncional11
- Semente 1.0 x 104 células/cm2 rato gordura células endoteliais para as lamelas de vidro de 12mm estéril da almofada e alimentar as células com DMEM suplementado com 10% fetal bovino soro e 1% penicilina/estreptomicina. Permitir que as células a crescer a confluência completa na umidade e incubadoras de CO2 controlada a 37 ° C, por aproximadamente 3 dias.
- Adicione tratamentos para modificar o glicocálix, se aplicável. Por exemplo, 2 h tratamento de culturas de células endoteliais com 2,5 x 10-6 IU heparinase enzima III degrada o glicocálix por clivagem especificamente seu componente de sulfato de heparan.
Nota: Glicocálix saudável pode ser modelado através do crescimento das células endoteliais, conforme descrito na etapa 5.5.1 sem a adição de enzimas de degradação. - Com o glicocálix endotelial intacta ou processado disfuncional, Incube as células endoteliais com AuNPs fluorescente em 550 µ g/mL para 16 h ou outra hora desejada.
- Lave delicadamente as células com 2 mL de 37 ° C 1% albumina de soro bovino em solução salina de tampão fosfato (PBS; contendo 100 mg/L cálcio e magnésio 100 mg/L). Mergulhe as células em 2 mL de paraformaldeído 2% e 0,1% de glutaraldeído em PBS e permitir que as células corrigir por 30 min à temperatura ambiente.
- Remover a solução de fixação de aldeído e lavar as células com temperatura PBS em 3 ciclos de 5 min.
- Antes da aplicação do anticorpo primário, expor as células endoteliais de soro de cabra de 2% em PBS durante 30 min à temperatura ambiente para bloquear sites de ligação não-específica. As células devem ser totalmente cobertas pela solução do bloqueio.
- Incube as células endoteliais durante a noite com o anticorpo primário de 1% anti-heparan sulfato em 2% de soro de cabra em PBS em 4 ° C para rotular o componente de sulfato de heparan do glicocálix. Certifique-se de que as células fixas são totalmente em contato com a solução de anticorpo.
- No dia seguinte, lave o anticorpo com temperatura PBS em 3 ciclos de 10 min.
- Incube as células endoteliais com 1:1,000 diluição do anticorpo secundário fluorescente apropriado por 30 min à temperatura ambiente, no escuro ou coberto com papel alumínio.
- Lave o anticorpo secundário com temperatura PBS em 3 ciclos de 10 min.
- Monte a lamela em corrediças do microscópio usando um meio de montagem de anti-desvaneça-se contendo 4' 6-diamidino-2-phenylindole, dicloridrato (DAPI) para coloração de núcleos. Sele as bordas da lamela usando esmalte.
- Imagem da célula endotelial fluorescente immunostained amostras com microscopia confocal, usando canais muito vermelhos, verdes e azuis para visualizar os núcleos, glicocálix sulfato de heparan e as nanopartículas, respectivamente.
Resultados
O AuNPs sintetizado, revestido com THPC ou PEG (figura 1A e figura 1B, respectivamente), são fotografada com temperatura e as partículas de tamanhos são medidos usando a temperatura e DLS para garantir a distribuição de tamanho adequado de nanopartículas. A Figura 2 mostra a imagem de temperatura de uma amostra de THPC-AuNP 80 kV e ampliação de x 150.000. Os diâmetros do intervalo de 2 a 3 nm, com base na barra de calibração em imagens TEM partículas THPC-AuNP. Este tamanho de THPC-AuNP também é evidente no histograma de medição DLS tamanho mostrado na Figura 2, em que o THPC revestido AuNP é mostrada para ter um pico em 2,5 nm. PEGylation não é visível sob temperatura como os polímeros não são elétron-densa. TEM imagem latente de PEG-AuNP amostras simplesmente confirma a presença de partículas dispersas individuais, que é esperada, pois a corona de polímero PEG ao redor as nanopartículas ajuda na prevenção da agregação. Para estas amostras de PEG-AuNP, o histograma de medição de tamanho DLS mostra uma mudança no pico, a aproximadamente 10.5 nm sobre a DLS. Anexos de ligantes ou drogas para grupos funcionais adicionais terá impacto sobre o tamanho da nanopartículas também e devem ser tida em conta quando se mede o diâmetro.
A adição de fluoróforo (Figura 1) é confirmada por meio de um dados para medir o sinal de fluorescência de uma amostra de nanopartículas, conforme mostrado na Figura 3. Quando animado com comprimento de onda 633 nm, a emissão é medido para ter no máximo entre 672 e 660 nm, que corresponde a informação de produto do fabricante de emissão máxima em 665 nm. Penhora de outras sondas fluorescentes deve ser verificada em uma maneira similar para garantir resposta fluorescente.
A biocompatibilidade das partículas e viabilidade celular relacionados são avaliados usando o ensaio MTS para verificar o metabolismo celular relativo de MTS após incubação de 16 h com diferentes concentrações das nanopartículas. O fluoróforo conjugado PEGylated AuNPs não mostra nenhuma toxicidade significativa, conforme indicado pelos níveis semelhantes de viabilidade celular em todas as concentrações de até 1 mg/mL (Figura 4A). Esta biocompatibilidade pode mudar dependendo da terapêutica ou anexado aos restantes grupos funcionais para personalizar ainda mais as partículas do ligante. Anexos de drogas tendem a aumentar a toxicidade, mas dependendo as concentrações de trabalho, não pode afetar a viabilidade de uma forma significativa.
Absorção de fluorescentes, PEGylated AuNPs (Figura 1) pelas células aderentes é avaliada utilizando células endoteliais do rato cultivadas do tecido com glicocálix intacta ou disfuncional (Figura 4B). As condições de glicocálix disfuncionais são obtidas adicionando heparinase enzima III para a cultura, resultando em uma degradação do componente glicocálix heparan sulfato e comprometer a matriz12. Figura 4B mostra os diferentes níveis de absorção de PEG-AuNPs, como pontos vermelhos na vista transversal das células endoteliais representativas. Uma saudável glicocálix dissuade absorção dessas nanopartículas de ouro, mas um aumento substancial é observado quando a enzima é independentes11. Este resultado evidencia o potencial dessas nanopartículas manipulam entregar terapêutica para as células endoteliais de forma controlada por interações distintas que são baseadas na saúde de glicocálix.
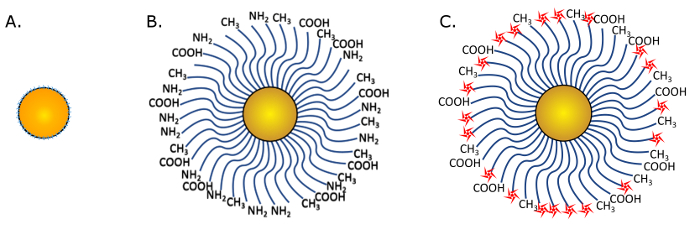
Figura 1: esquema de nanopartículas de ouro. (A) THPC revestido AuNP nanosphere antes da substituição de PEG. (B) PEGylated AuNP com 3 tipos de terminações de PEG, incluindo COOH, NH2e CH3. Ondas azuis representam o polímero. (C) conjugados nanopartículas para a imagem latente de fluorescência. Estrelas vermelhas mostram os fluorophores conjugada com NH2 grupos de funcionais. Clique aqui para ver uma versão maior desta figura.
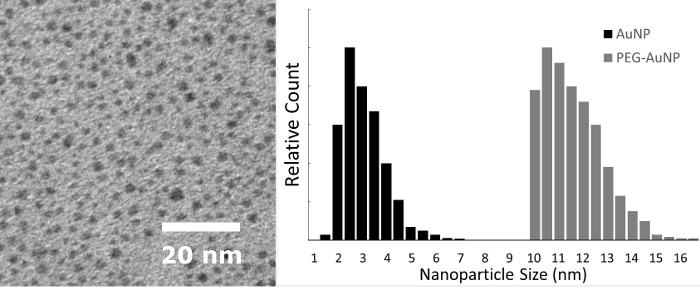
Figura 2: tamanho de medições de nanopartículas de ouro. Esquerda: TEM de nanopartículas de ouro antes da adição de PEG 80 kV e ampliação de 150.000 X, com a barra de escala mostrada. Direita: Histograma do tamanho de nanopartículas medido por DLS antes (AuNP) e depois (PEG-AuNP) o THPC substituição com PEG. Os resultados DLS para AuNP THPC-revestido quantificam o que é visualizado pela TEM. Os resultados de DLS PEG-revestido AuNP superar o desafio da incapacidade de Visualizar PEG pela TEM devido os polímeros não sendo elétron denso. Uma temperatura de PEG-AuNP mostrará apenas as nanopartículas de ouro do núcleo e terão a mesma aparência como um AuNP THPC-tampado. Clique aqui para ver uma versão maior desta figura.
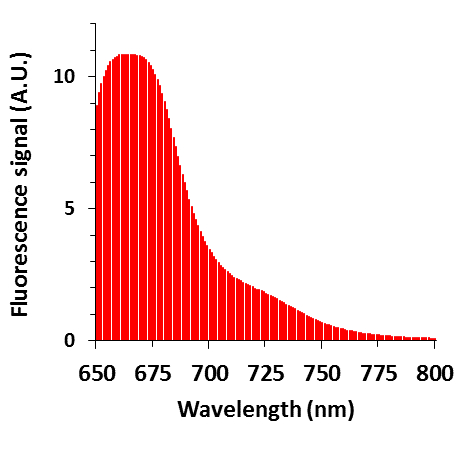
Figura 3: dados de fluorescência do fluorescente PEG-AuNP. O pico de fluorescência em 667 nm corresponde à emissão do fluoróforo conjugada a PEG-AuNP. U.A.: unidades arbitrárias.
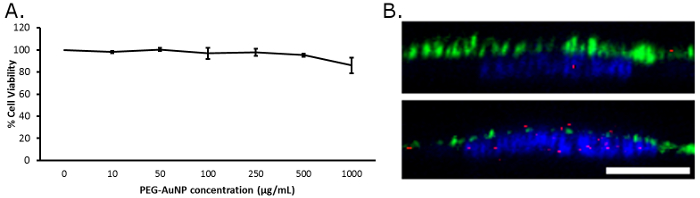
Figura 4: célula de interações com o PEG-AuNP fluorescente. (A) trama de viabilidade (metabolismo MTS) célula de gordura rato pad células endoteliais após 16 h co de incubação com PEG-AuNP fluorescente. (B) imagens transversais Confocal de gordura fixo rato almofada células endoteliais manchadas com DAPI para os núcleos (azuis) e anticorpo contra sulfato de heparan, um componente de glicocálix (verde). Imagem superior é uma saudável glicocálix e inferior é uma camada de glicocálix degradadas; Há significativamente mais fluorescência vermelha das nanopartículas na amostra com glicocálix degradada. Barra de escala é 10 µm. clique aqui para ver uma versão maior desta figura.
Discussão
Esta técnica é um método eficaz para a síntese de personalizável, que manipulam PEG revestido AuNPs. Uma parte importante deste processo é que a formação inicial de THPC tampado ouro nanopartículas, que podem ser confirmadas por alteração de cor de amarelo a marrom que ocorrerá depois HAuCl4 foi adicionado ao conteúdo do balão de fundo redondo (etapa de protocolo 2.3). Nenhuma mudança de cor indica que não há nenhum nanopartículas formadas e que os passos iniciais devem ser verificados e repetidos antes de prosseguir. No caso da que cor muda para algo diferente de marrom como vinho vermelho ou cinza, as partículas resultantes não provavelmente será em torno do alvo 2,5 nm e um novo lote deve ser feito também.
Após a formação do núcleo do ouro, a troca de THPC para PEG e os procedimentos de purificação contêm várias etapas-chave para a conclusão bem sucedida do protocolo. Permite a mistura durante a noite para a reação de substituição ir até a conclusão. Purificação de falha pode ocorrer se a água de diálise não é alterada com a frequência prescrita. Agregação e precipitação das partículas também podem ocorrer se as partículas são deixadas em diálise por mais de 72 h. Outros possíveis problemas podem ser observados durante a liofilização. Se o PEG manipulam revestido AuNP solução não estava completamente congelada ou o liofilizador não foi configurado corretamente, amostras podem ser perdidas. Consulte o manual do Liofilizador, como alguns equipamentos podem exigir preparações de amostra diferente.
A facilidade de síntese e a biocompatibilidade das partículas resultantes representam vantagens para a utilização destes PEG-AuNPs. Além disso, essas nanopartículas têm a vantagem de ser capaz de interagir com estruturas celulares de nanoescala, como demonstram a capacidade de identificar glicocálix degradada pela utilização dessas nanopartículas. Esta vantagem pode ser aproveitada para o desenvolvimento de novas terapias de aterosclerose e medidas preventivas. Além do que apresentamos aqui, uma outra vantagem deste protocolo é que ele permite a personalização extensiva das partículas bem como aumentou a estabilidade e recursos de armazenamento, anexando tiol contendo PEG para as nanopartículas de ouro4. A outra extremidade da cadeia PEG pode conter qualquer grupo funcional, e uma miríade de moléculas pode ser conjugada a esses grupos. Neste protocolo, todos os três grupos de funcionais comuns são anexados (metil, carboxila e amino). A relação entre a PEG é escolhido para priorizar a deteção fluorescente primeiro e, em seguida, a capacidade de incorporar um moiety alvo secundário usando o grupo ácido carboxílico. As relações desses grupos podem ser mexidas baseado no aplicativo, e os comprimentos e formas dos polímeros podem ser ajustadas.
Para medir a absorção de partículas, nós conjugados uma sonda fluorescente para um dos grupos funcionais. Note-se que qualquer conjugação além do que descrevemos irá resultar em uma mudança de propriedades superficiais de nanopartículas. Cada iteração das nanopartículas com relação a reações de conjugação e componentes adicionais deve ser testada para as propriedades desejadas.
Este método produz nanopartículas de ouro manipulam destinadas a superar as propriedades defensivas do glicocálix extracelular endotelial, o que dificulta a absorção de nanopartículas convencionalmente tamanhos. No entanto, o tamanho pequeno presta-se a dificuldade da imagem e o aspecto de carregamento de droga. Estas partículas são significativamente menores do que o intervalo de tamanho típico de nanopartículas, e como resultado a área da superfície disponível para anexos de terapêutica e direcionamento metades é diminuída extremamente. Isso pode levar a dificuldade de captar sinais individuais em aplicativos, de imagem, embora ainda aglomerados de partículas podem ser facilmente identificados, como mostrado nas imagens confocal. A superfície reduzida para anexos de direcionamento de ligantes e terapêutica pode exigir mais partículas a serem administrados para atingir os requisitos de dosagem de alvo. No entanto, as partículas menores será mais eficientes na entrega quando atendendo o glicocálix.
Estas partículas manipulam romance são capazes de entrega em difícil chegar nanoescala áreas dentro do corpo com interrupção mínima do microambiente. A adição de PEG permite maior biocompatibilidade e oferece grupos funcionais para personalização pesada das partículas para diversas aplicações. O tamanho menor em comparação com nanopartículas típicas vem com algumas deficiências, mas se desenvolveu estrategicamente, a partícula manipulam é uma abordagem promissora para alojamento dos difíceis de penetrar, glicocálix intrincada e frágil no vascular entrega de direcionamento e drogas.
Divulgações
Os autores declaram que eles têm não tem interesses financeiro concorrente.
Agradecimentos
Este trabalho foi financiado pelo departamento de engenharia de química Universidade Northeastern, fundos de start-up e uma bolsa de estudo piloto de 1 camada do escritório de reitor de Universidade do nordeste, NIH K01 HL125499 e NSF-IGERT concedem NSF/DGE-096843. Os autores também gostaria de agradecer Thomas J. Webster e seu laboratório para sua assistência, bem como a ciência Nanomedicine e centro de tecnologia e departamento de Ciências Farmacêuticas da Universidade de Northeastern.
Materiais
| Name | Company | Catalog Number | Comments |
| Sodium hydroxide (NaOH) | Sigma Aldrich | 795429 | |
| Gold (III) Chloride trihydrate (HAuCl4.3H2O) | Sigma Aldrich | 520918 | |
| Sodium bicarbonate | Sigma Aldrich | S5761 | |
| Tetrakis (hydroxymethyl) phosphnium chloride | Sigma Aldrich | 404861 | |
| Mono-functional mPEG-thiol | Layson Bio Inc. | MPEG-SH-2000-1g | Mw: 2,000 Da |
| hetero bi-functional anime-PEG-thiol | Layson Bio Inc. | NH2-PEG-SH-3400-1g | Mw: 3,400 Da |
| Carboxymethyl-PEG-thiol | Layson Bio Inc. | CM-PEG-SH-2000-1g | Mw: 2,000 Da |
| Cellulose dialysis membrane (12-14 kDa) | Sigma Aldrich | D9777 | |
| Zerostat anti-static instrument | Sigma Aldrich | Z108812 | |
| Alexa Fluor 647 (AF647) carboxylic acid succinimidyl ester | Fisher | A20006 | Fluorophore |
| Fisherbrand Qualitative Grade Plain Filter Paper Circles - P5 grade | Thermo Fisher Scientific | 09-801-B | |
| Transmission electron microscopy | JEOL USA | JEOL JEM-1000 | TEM |
| Dynamic Light Scattering | Brookhaven Instruments Corporation | Brookhaven 90 Plus Particle Size Analyzer | DLS |
| Fluorometer | Horiba Scientific | Jobin Yvon Fluromax 4 | Fluorometer |
| CellTiter 96 AQueous One Solution Cell Proliferation Assay (MTS) | Promega | G3582 | MTS |
| Plate reader | Molecular Devices | SpectraMax M4 | Plate reader |
| 10E4 epitope HS mouse monoclonal IgM antibody (primary antibody) | Amsbio | 370255 | Primary antibody |
| Alexa Fluor 488 goat anti-mouse IgG (secondary antibody) | Thermo Fisher Scientific | R37120 | Secondary antibody |
| VECTASHIELD mounting medium with DAPI | Vector Laboratories | H-1000 | With DAPI |
| Confocal Microscope | Carl Zeiss Meditex AG | Zeiss LSM 700 | Confocol microscopy |
Referências
- Veiseh, O., Gunn, J., Zhang, M. Design and fabrication of magnetic nanoparticles for targeted drug delivery and imaging. Adv. Drug Deliv. Rev. 62 (3), 284-304 (2010).
- Feng, X., et al. Conjugated polymer nanoparticles for drug delivery and imaging. ACS Appl. Mater. Interfaces. 2 (8), 2429-2435 (2010).
- Ghosh, P., Han, G., De, M., Kim, C. K., Rotello, V. M. Gold nanoparticles in delivery applications. Adv. Drug Deliv. Rev. 60 (11), 1307-1315 (2008).
- Kumar, R., et al. Third generation gold nanoplatform optimized for radiation therapy. Transl. Cancer Res. 2 (4), 1-18 (2013).
- Tarbell, J. M., Ebong, E. E. The endothelial glycocalyx: a mechano-sensor and -transducer. Sci. Signal. 1 (40), (2008).
- Reitsma, S., Slaaf, D. W., Vink, H., van Zandvoort, M., oude Egbrink, M. G. A. The endothelial glycocalyx: composition, functions, and visualization. Pflugers Arch. 454 (3), 345-359 (2007).
- Becker, B. F., Jacob, M., Leipert, S., Salmon, A. H., Chappell, D. Degradation of the endothelial glycocalyx in clinical settings: searching for the sheddases. Br. J. Clin. Pharmacol. 80 (3), 389-402 (2015).
- Muzykantov, V., Muro, S. Targeting delivery of drugs in the vascular system. Int. J. Transp. Phenom. 12 (1-2), 41-49 (2011).
- Simone, E., Ding, B. -. S., Muzykantov, V. Targeted delivery of therapeutics to endothelium. Cell Tissue Res. 335 (1), 283-300 (2009).
- Lockman, P. R., Mumper, R. J., Khan, M. A., Allen, D. D. Nanoparticle technology for drug delivery across the blood-brain barrier. Drug Dev. Ind. Pharm. 28 (1), 1-13 (2002).
- Cheng, M. J., Kumar, R., Sridhar, S., Webster, T. J., Ebong, E. E. Endothelial glycocalyx conditions influence nanoparticle uptake for passive targeting. Int. J. Nanomedicine. 11, 3305-3315 (2016).
- Fels, J., Jeggle, P., Liashkovich, I., Peters, W., Oberleithner, H. Nanomechanics of vascular endothelium. Cell Tissue Res. 355 (3), 727-737 (2014).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados