Method Article
Sistema Microfisiológico do Fígado Humano para Avaliação da Toxicidade Hepática Induzida por Drogas In Vitro
Neste Artigo
Resumo
A lesão hepática induzida por drogas (DILI) é uma das principais causas de insuficiência de drogas. Um protocolo foi desenvolvido para prever com precisão a responsabilidade DILI de um composto usando um sistema microfisiológico hepático (MPS). O modelo hepático utiliza a cocultura de células hepáticas primárias e desfechos translacionalmente relevantes para avaliar as respostas celulares ao tratamento.
Resumo
DILI é uma das principais causas de desgaste no desenvolvimento de medicamentos com mais de 1000 medicamentos aprovados pela FDA conhecidos por potencialmente causar DILI em humanos. Infelizmente, o DILI muitas vezes não é detectado até que os medicamentos tenham atingido estágios clínicos, arriscando a segurança dos pacientes e levando a perdas substanciais para a indústria farmacêutica. Tendo em conta que os modelos 2D padrão têm limitações na deteção de DILI, é essencial desenvolver modelos in vitro que sejam mais preditivos para melhorar a traduzibilidade dos dados. Para entender a causalidade e os aspectos mecanicistas da DILI em detalhes, uma MPS hepática humana consistindo de células parenquimatosas e não parenquimatosas hepáticas primárias humanas (NPCs) e cultivada em microtecidos 3D em um andaime modificado sob perfusão foi desenvolvida. Hepatócitos humanos primários criopreservados (PHHs) e células de Kupffer (HKCs) foram cocultivados como microtecidos na plataforma MPS por até duas semanas, e cada composto de interesse foi repetidamente dosado em microtecidos hepáticos em sete concentrações de teste por até quatro dias. Os desfechos funcionais específicos do fígado foram analisados (incluindo biomarcadores clínicos, como alanina aminotransferase, ALT) para avaliar a função hepática. A exposição aguda e crônica a compostos de várias gravidades DILI pode ser avaliada comparando as respostas a microtecidos de dose única e múltipla. A metodologia foi validada com um amplo conjunto de compostos graves e levemente hepatotóxicos. Aqui mostramos os dados para pioglitazona e troglitazona, compostos hepatotóxicos bem conhecidos retirados do mercado por causar insuficiência hepática. No geral, foi demonstrado que o modelo de MPS hepática pode ser uma ferramenta útil para avaliar a DILI e sua associação com alterações na função hepática. O modelo também pode ser usado para avaliar como novos compostos se comportam em subgrupos distintos de pacientes e como os perfis de toxicidade podem ser afetados por estados de doença hepática (por exemplo, hepatite viral, doença hepática gordurosa).
Introdução
O DILI continua sendo a causa mais comum de insuficiência hepática aguda nos EUA e na Europa e é uma das principais causas de desgaste de compostos no processo de desenvolvimento de medicamentos1. Quase todas as classes de medicamentos podem causar hepatotoxicidade, sendo os agentes do sistema nervoso central e os antibióticos de longe os tratamentos mais comuns que causam DILI em pacientes2. A hepatotoxicidade induzida por drogas é causada por uma complexa interação de fatores genéticos, não genéticos e ambientais, levando à morte de hepatócitos e outros tipos de células hepáticas, incluindo colangiócitos e células endoteliais 1,3.
Os agentes causadores de DILI podem ser classificados de duas maneiras: aqueles que causam danos hepáticos dependentes da dose previsível ou aqueles que causam DILI idiossincrático que é raro e se desenvolve independentemente da dose do medicamento, via ou duração da administração, mas é responsável por até um sexto de todas as insuficiência hepática aguda nos EUA apenas4. Infelizmente, o DILI muitas vezes não é detectado até que os medicamentos tenham atingido os estágios clínicos do processo de desenvolvimento de medicamentos. A classificação de lesão hepática induzida por drogas (ou DILIrank) consiste em mais de mil medicamentos aprovados pela FDA que são divididos em quatro classes de acordo com seu potencial de causar DILI, e seu uso em pacientes deve ser monitorado de perto5.
Estudar os mecanismos de hepatotoxicidade de drogas continua sendo muito desafiador e, portanto, muitos modelos pré-clínicos foram desenvolvidos para explorar os mecanismos de DILI. Os modelos in vitro e in vivo atuais usados para prever o DILI no desenvolvimento pré-clínico têm várias limitações para fornecer insights sobre as interações complexas e multifacetadas em um corpo humano vivo. Linhagens celulares hepáticas cancerosas (ou seja, HepG2, HepaRG) cultivadas em 2D ainda são usadas nos estágios iniciais do desenvolvimento de medicamentos para avaliar a toxicidade de compostos candidatos6. Mesmo assim, essas linhagens celulares provêm de doadores isolados e apresentam níveis anormais de função hepática, nem sempre apresentam alta sensibilidade para detecção de DILI 7,8. Como alternativa às linhagens celulares hepáticas cancerosas, as PHHs representam melhor a fisiologia hepática humana se cultivadas adequadamente in vitro, embora existam várias limitações com sua cultura, como curto tempo de incubação com drogas, vida útil relativamente curta, perda de expressão gênica hepática e alterações das funções metabólicas das drogas 9,10,11 . Os PHHs podem ser cultivados em proteínas da matriz extracelular em placas de cultura celular 2D padrão, mas, como desvantagem, o rápido declínio em sua função significa que eles têm baixa sensibilidade (<50%) para a predição de DILI12.
Por outro lado, os testes em modelos animais são lentos, caros e precisam de uma tradução entre espécies para extrapolar a previsão para os seres humanos. A maioria dos medicamentos recém-desenvolvidos não consegue obter aprovação, tornando esse processo caro e arriscado5. Além disso, para testar novas modalidades específicas para humanos, os modelos animais são menos adequados devido à sequência gênica ou às diferenças de resposta imunológica em relação aos humanos13.
Consequentemente, o interesse em modelos hepáticos tridimensionais (3D) mais avançados tem crescido exponencialmente. A cultura de PHHs como estruturas esferoidais geradas pela agregação gravitacional em gotas suspensas ou em superfícies de fixação ultrabaixas representa um método de alto rendimento para avaliar passivos compostos14. Os esferoides de PHH têm sido usados para avaliar a DILI em um contexto doente (por exemplo, esteatose e colestase)15. Uma grande variedade de modelos tem sido desenvolvida para incluir coculturas micropadronizadas chapeadas de hepatócitos com fibroblastos estromais16, tecidos hepáticos bioimpressos em 3D 17, culturas esferoides 3D com ou sem células hepáticas não parenquimatosas15. No entanto, todos esses métodos ainda apresentam desvantagens, e a cultura de PHHs em um microambiente fisiologicamente mais relevante poderia proporcionar-lhes níveis mais altos de funcionalidade por longos períodos de tempo para permitir a investigação da exposição prolongada a potenciais hepatotóxicos. Além disso, para melhorar a relevância translacional de qualquer cultura avançada de PHH in vitro, desfechos funcionais clinicamente relevantes ou biomarcadores de saída de toxicidade devem ser utilizados para permitir que os dados sejam comparados in vivo ou cenários clínicos18.
Neste estudo, avaliamos se um modelo hepático in vitro MPS, também conhecido como Organ-on-a-Chip (OOC), poderia ser usado para entender os aspectos mecanicistas detalhados da toxicidade hepática. O MPS já demonstrou manter microtecidos hepáticos 3D altamente funcionais, sob fluxo, por até 4 semanas19. O sistema foi recentemente testado pela FDA e demonstrou ter alta reprodutibilidade ao realizar toxicidade de drogas, metabolismo e acúmulo intracelular20. Além disso, quando comparado com as culturas de esferoides e sanduíches, o sistema apresentou função mais estável e maior sensibilidade na detecção da toxicidade de diversos fármacos20. Até o momento, a MPS tem sido usada em uma ampla gama de aplicações que abrangem ADME21, modelagem de doenças (HBV22, DHGNA 23,24,25) e interações medicamentosas 26, potencialmente tornando-a altamente adequada para avaliar DILI aguda e crônica. A tecnologia aqui apresentada oferece uma alternativa para fechar a lacuna entre culturas celulares mais tradicionais e modelos animais e ensaios clínicos em humanos, avançando para a simulação de condições biológicas humanas para apoiar a avaliação da toxicidade hepática de compostos candidatos em estágios pré-clínicos do processo de desenvolvimento de medicamentos.
Protocolo
Todo o trabalho foi realizado no laboratório seguindo rigorosos procedimentos de Saúde e Segurança e de acordo com suas próprias avaliações de risco laboratorial e POPs. Todos os equipamentos utilizados são reparados de acordo com as diretrizes da fabricação. Os gabinetes de segurança microbiológica (MBSCs) são atendidos anualmente e o Ki-Discus (iodeto de potássio) testado de acordo com os padrões britânicos. O protocolo segue o Código de Práticas e as diretrizes da Autoridade de Tecidos Humanos do Reino Unido (HTA) e usa células humanas primárias de origem ética fornecidas por fornecedores que cumprem plenamente os requisitos gerais de consentimento informado (45 CFR §46.116 e §46.117) e Boas Práticas Clínicas (GLP) (ICH E6) e comitês regulatórios e de ética.
1. Preparação de meios de cultura celular
NOTA: Preparar o meio DMEM avançado de semeadura no Dia -1 e armazenar a 4 °C. Prepare o meio DMEM Avançado de Manutenção no Dia 1 e armazene a 4 °C por até 1 semana.
- Meio DMEM Avançado de Semeadura para cocultura de PHHs e HKCs: Complementar um frasco de 500 mL de meio DMEM Avançado (Tabela de Materiais) com 18 mL de Coquetel A (concentração final de 3,6%) e com 25 mL de FBS (concentração final de 5%).
- Manutenção de meio DMEM avançado para cocultura de PHHs e HKCs: Complementar um frasco de 500 mL de meio DMEM avançado (Tabela de Materiais) com 20 mL de Coquetel B (concentração final de 4%) e hidrocortisona 500 nM.
NOTA: A hidrocortisona será feita fresca no dia de uso, e as etapas sobre como preparar a solução-mãe e as diluições necessárias são mencionadas abaixo. - Preparação de hidrocortisona 500 nM em Meio DMEM Avançado de Manutenção
- Preparação da solução-mãe de arranque (20 mM): Pesar 7,24 mg de hidrocortisona (Tabela de Materiais) num frasco para injetáveis de vidro de 1 ml. Registar a quantidade exacta de hidrocortisona pesada e determinar o volume de dimetilsulfóxido (DMSO) utilizando o seguinte cálculo:
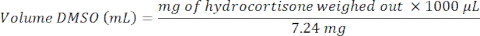
- Preparação da solução-mãe de hidrocortisona de trabalho a 100 μM: Adicionar 5 μL da solução-mãe de 20 mM inicial a 995 μL de DMEM avançado.
NOTA: A diluição de 25 μL da solução de DMSO a partir da etapa 1 em água ou meio resulta em concentração de DMSO a 0,5%. Na solução final, a concentração de DMSO será de 0,0025%. Neste caso, o volume adicional de 5 μL resulta em uma mudança insignificante no volume total. - Preparação da solução de hidrocortisona de 500 nM em Advanced DMEM: Para preparar 1 mL de solução de hidrocortisona de 500 nM em Advanced DMEM, adicione 5 μL da solução-mãe de hidrocortisona de 100 μM a 995 μL do meio DMEM Maintenance Advanced.
- Preparação da solução-mãe de arranque (20 mM): Pesar 7,24 mg de hidrocortisona (Tabela de Materiais) num frasco para injetáveis de vidro de 1 ml. Registar a quantidade exacta de hidrocortisona pesada e determinar o volume de dimetilsulfóxido (DMSO) utilizando o seguinte cálculo:
2. Configuração e priming do MPS (Dia -1)
- Conecte o controlador à sua casa de estação de ancoragem em uma incubadora de cultura de células e certifique-se de que o dessecante fresco (Tabela de Materiais) seja adicionado ao frasco dessecante localizado na parte de trás do controlador.
NOTA: A unidade controladora extrai umidade da incubadora ao longo do tempo e é mantida seca usando dessecante fresco. - Ligue o controlador pressionando o interruptor do balancim do barco localizado atrás dele e aguarde 5 minutos para que o sistema se estabilize e atinja a pressão. Em seguida, verifique a tela para o relatório pneumático para garantir: (i) A Saída do Reservatório de Pressão atingiu ~ 2000 mBar e (ii) A Saída do Reservatório de Vácuo atingiu ~ 850 mBar.
- Remova cada placa da embalagem e inspecione visualmente cada poço para verificar possíveis defeitos (andaimes ausentes, rachaduras, etc.).
- Insira um driver (com uma placa ligada) na estação de encaixe para verificar se o driver é reconhecido pela estação de encaixe e pelo controlador. Verifique se a Saída do Reservatório de Pressão caiu menos de 100 mBar e a Saída do Reservatório de Vácuo aumentou em menos de 500 mBar.
- Prepare cada poço adicionando 500 μL de meio DMEM avançado de semeadura (pré-aquecido a 37 °C) ao lado do reservatório.
- Selecione o programa Prime na tela do controlador (fluxo ascendente por 3 min a 2,5 μL/s) até que o fluido passe pelos suportes do filtro. NOTA: 'Fluxo ascendente' é uma configuração no controlador que permite que o meio flua do reservatório para cima através dos andaimes na placa LC12.
- Encha todos os poços com mais 1,1 mL de meio DMEM avançado de semeadura para cobrir o canal de superfície. Todos os poços estarão então em seu volume de trabalho total de 1,6 mL.
- Coloque os drivers com placas em uma incubadora de 37 °C e 5% de CO2 , conecte-se à estação de ancoragem e execute o programa Incubate .
NOTA: Todos os programas utilizados no experimento (Prime, Incubate, Seed, Media Change) são predefinidos no sistema MPS. Prepare as placas na incubadora até ficar pronto para semear.
3. Semeando células do fígado em MPS (Dia 0)
- Pré-valide todos os PHHS e HKCs. Todos os lotes de PHHs e HKCs são pré-validados internamente antes da realização do experimento de cultura celular (consulte Material Suplementar).
- Descongele os frascos para injetáveis de PHHs e células HKC (Tabela de Materiais) mantendo os frascos para injetáveis de forma constante num banho-maria de 37 °C até que apenas uma pequena lasca de gelo permaneça.
- Pipetar PHHs diretamente para um tubo de meio CHRM pré-aquecido (37 °C) Cryopreserve Hepatocyte Recovery Medium (dois frascos para injetáveis por tubo).
- Pipete as células suavemente e, em seguida, use 1 mL de CHRM para lavar as células restantes do criotubo. Seja muito gentil com as células ao descongelar e transferir para um tubo cônico.
CUIDADO Não agite os frascos para injetáveis durante o descongelamento e não pipete o seu conteúdo para cima e para baixo. - Pipetar células HKCs suavemente do criotubo para 10 mL de meio EMEM avançado de semeadura gelado em um tubo de centrífuga de 15 mL.
NOTA: Até 2 frascos para injetáveis de HKCs podem ser combinados. - Centrifugar ambos os tipos de células à temperatura ambiente (RT) a 100 x g durante 10 min. Remova o sobrenadante.
- Ressuspeite os PHHs em meio DMEM avançado de semeadura quente e HKCs em meio DMEM avançado de semeadura gelado (para ajudar a reduzir a aglomeração celular), usando 1 mL por frasco de células adicionadas ao tubo e coloque as células no gelo. Use uma ação de balanço suave para ressuspender as células.
CUIDADO: Não ressuscite os PHHs por ação da pipeta, pois isso pode levar à morte celular. - Combine as suspensões celulares de vários tubos (se aplicável - ou seja, se todos os PHHs forem do mesmo doador), mas não misture os tipos de células.
- Contagem de células. Registre a viabilidade (deve estar acima de 85% para ambos os tipos de células, PHHs e HKCs) e o número total de células. Se a viabilidade celular cair abaixo de 85%, descongele um novo frasco para injetáveis de células e reavalie a viabilidade celular.
- Calcule a viabilidade da célula usando a seguinte fórmula:
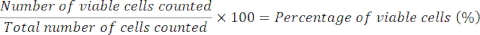
- Calcular o volume desejado da suspensão celular para semear em cada poço e o volume adicional de meio DMEM avançado de semeadura necessário para levar o volume total de semeadura a 400 μL. Número de células por poço: 0,4 x 10 6 PHHs e 0,04 x 10 6 HKCs por poço e densidade celular de 0,25 x 106 PHHs/mL, respectivamente 0,025 x 106 HKCs/mL.
- Desconecte o driver da docking station e coloque-o no MBSC.
- Aspirar o meio do andaime acima até o ponto de parada (descendo o entalhe profundo no anel de retenção), canal e reservatório. Deixe um "volume morto" de 0,2 mL no poço de cultura, atingindo logo acima do andaime. Deve-se tomar cuidado para não remover o meio total de cima do andaime para evitar a formação de bolhas de ar.
- Adicione 400 μL de meio DMEM avançado de semeadura na câmara do poço, devolva o driver à estação de ancoragem na incubadora e execute o programa Media Change por 3 min. O programa será pausado automaticamente após 3 min.
- Depois de concluído, desconecte o driver da estação de encaixe e coloque-o novamente no MBSC.
- Aspirar o meio do andaime acima até o ponto de parada e na extremidade do reservatório de cada poço.
- Ressuscite cuidadosamente os PHHs balançando suavemente o tubo e, em seguida, adicione o volume necessário da suspensão celular a cada poço de cultura. Pipete cuidadosamente a suspensão celular, certifique-se de que as células se dispersam uniformemente pelo andaime da placa.
NOTA: Para garantir uma boa cobertura em todo o andaime, use um movimento de redemoinho lento para pipetar as células para baixo no andaime. - Da mesma forma, ressuscite cuidadosamente os HKCs e adicione bem as suspensões celulares a cada cultura.
NOTA: Use um movimento de redemoinho lento para semear HKCs para garantir uma boa cobertura em todo o andaime. As duas subetapas de semeadura podem ser separadas, ou os dois tipos de células podem ser pré-misturados em uma densidade apropriada e semeados concomitantemente. - Quando todos os poços contiverem os dois tipos de células, coloque o driver MPS na estação de ancoragem da incubadora sem conectá-lo fisicamente e deixe-o repousar por 1 h.
- Após 1 h, encha cada poço com o volume necessário de meio DMEM Avançado de Semeadura adicional para atingir 400 μL e execute o programa Semente .
- Após 2 min, o programa pausará automaticamente, removerá o driver da incubadora e adicionará lentamente 1000 μL do meio DMEM Avançado de Semeadura ao canal (mais próximo da extremidade do reservatório do que da câmara do poço) para atingir um volume total de 1,4 mL (com mais 200 μL de volume morto nos canais).
- Mova as placas para a incubadora e execute o resto do programa Seed por 8 h.
NOTA: O fluxo mudará automaticamente para o programa Incubar após 8 h.
4. Mudança de mídia (Dia 1)
- Desconecte o driver da docking station e coloque-o no MBSC.
- Execute a Alteração de Mídia removendo a mídia DMEM Avançada de Semeadura na câmara do poço até o ponto de parada.
- Adicione 400 μL do meio DMEM Maintenance Advanced na câmara do poço, devolva o motorista à estação de ancoragem na incubadora e execute o programa Media Change por 3 min. O programa será pausado automaticamente após 3 min.
- Desconecte o motorista da estação de acoplamento e, no MBSC, aspirar a mídia para longe da câmara do reservatório, do canal e do ponto de parada acima do andaime. Neste ponto, o poço da cultura será devolvido ao volume morto.
- Encha a câmara do reservatório com 1,4 mL de meio DMEM avançado de manutenção pré-aquecido fresco (37 °C).
- Devolva o motorista à estação de ancoragem na incubadora e execute o programa Incubate .
5. Controle de qualidade do microtecido hepático (QC), coleta de mídia, mudança de mídia e dosagem de medicamentos (Dia 4)
- No dia 4, execute uma Mudança de Mídia usando o meio DMEM Avançado de Manutenção e as verificações de QC para garantir que a semeadura tenha sido bem-sucedida.
NOTA: QC é um processo usado para verificar a saúde dos microtecidos formados através da medição de lactato desidrogenase (LDH) e ureia. - Antes de executar o QC, prepare novas soluções de estoque para cada composto a ser testado (seja em meio DMEM Avançado de Manutenção ou meio DMEM Avançado de Manutenção contendo DMSO de 0,1%, dependendo da solubilidade de cada composto). Preparar as diluições em conformidade para produzir concentrações de ensaio para cada composto.
- Desconecte o driver e a placa da estação de encaixe e transfira para um MBSC.
- Transfira 50 μL de meios de cada poço usando uma pipeta para uma placa de 96 poços para realizar um ensaio de LDH (Tabela de Materiais) antes da amostragem e 25 μL para um ensaio de Ureia (Tabela de Materiais).
NOTA: Os ensaios de LDH e ureia serão realizados de acordo com as instruções do fabricante. - Continue o experimento após o QC se as leituras de LDH forem inferiores a 2 AU/10 6 células e a ureia estiver acima de 40 μg/dia/106 células.
NOTA: A albumina não é usada como QC porque é um ensaio longo para ser executado no dia e será ensaiado mais tarde, uma vez que o experimento esteja completo a partir das amostras retiradas no Dia 4. - Se algum poço falhar no QC, remova-o do projeto experimental.
- Uma vez confirmado o layout experimental, apresente a amostra do meio restante de cada poço, certificando-se de não perturbar a cultura celular tocando o andaime. Conservar o meio recolhido (rotulado como amostras pré-dose) a -80 °C para ensaios posteriores.
- Execute a alteração de mídia em um MBSC seguindo as etapas 4.3-4.5. Alterar os poços para o meio DMEM Avançado de Manutenção com a concentração correta do fármaco de acordo com o desenho experimental.
- Uma vez concluído, devolva o motorista à estação de ancoragem na incubadora e execute o programa Incubate .
6. Coleta de mídia, mudança de mídia e dosagem de drogas (Dia 6)
- Preparar novas soluções de estoque para cada composto a ser testado (seja em meio DMEM Avançado de Manutenção ou meio DMEM Avançado de Manutenção contendo DMSO de 0,1%, dependendo da solubilidade de cada composto). Preparar as diluições em conformidade para produzir concentrações de ensaio para cada composto de acordo com o plano em placa.
- Desconecte o driver e a placa da estação de encaixe e transfira para um MBSC.
- Recolha os meios de cada poço (~1 ml) manualmente com uma pipeta certificando-se de não perturbar a cultura celular tocando no andaime, ensaio para LDH e Ureia. Armazenar o resto do meio recolhido a -80 °C para ensaios posteriores e rotulá-los 48 h após a dose.
- Re-dose de cada poço com a mesma concentração de droga que no Dia 4 e de acordo com o plano de placa, realizando a Mudança de Mídia seguindo as etapas 4.3-4.5.
- Uma vez concluído, devolva o motorista à estação de ancoragem na incubadora e execute o programa Incubate .
7. Terminando o experimento (Dia 8)
- Desconecte o driver e a placa da estação de encaixe e transfira para um MBSC.
- Prove o meio de cada poço manualmente usando uma pipeta, certificando-se de não perturbar a cultura celular tocando no andaime.
- Ensaio dos meios retirados para LDH e ureia e armazenar o resto dos meios recolhidos a -80 °C para ensaios posteriores.
- Executando o ensaio CYP3A4-glo.
- Medir os efeitos dos fármacos testados na atividade do citocromo P450 CYP3A4 em PHHs no final da experiência utilizando este ensaio.
- Reconstituir o reagente de deteção (para o ensaio do CYP3A4, ver Tabela de Materiais) seguindo as instruções do fabricante. Se o reagente de detecção tiver sido previamente reconstituído e congelado, retire-o do congelador a -20 °C e deixe-o descongelar no RT.
- Preparar a norma D-luciferina de 20 mM de reserva seguindo as instruções do fabricante.
- Preparar o meio de substrato luminogênico de trabalho com diluição 1:1000 de Luciferin IPA em meio DMEM Maintenance Advanced (2 mL de meio substrato luminogênico por poço).
- Execute uma Mudança de Mídia conforme descrito nas etapas 4.3-4.5 com meio de substrato luminogênico. Salvar 500 μL do meio do substrato luminogênico em um frasco para injetáveis de vidro de 1,5 mL (Tabela de Materiais) como material de entrada.
- Devolva o motorista à docking station na incubadora e execute o programa Incubate por 1,5 h.
- Preparar a curva padrão de D-luciferina em meio de cultura em tubos de 1,5 mL seguindo as instruções do fabricante e pipetar 50 μL de cada padrão em duplicata em uma placa branca opaca de 96 poços (ver Tabela de Materiais), usando meio de cultura como branco ou 0 μM.
- Decorrido o tempo, remova o condutor da estação de ancoragem e do suporte de amostra para o ensaio CYP3A4 seguindo os passos 7.4.9-7.4.13.
- Após a incubação, transferir 50 μL do meio de amostra de cada poço e material de entrada para a placa de luminômetro branco opaco de 96 poços contendo padrões. Tome cuidado para deixar pelo menos duas fileiras vazias na placa opaca entre as normas e as amostras para evitar o transporte leve entre as normas superiores e as leituras das amostras.
- Adicione 50 μL de Reagente de Detecção de Lúciferina a cada poço para iniciar uma reação luminescente.
- Incubar a placa em RT em um agitador de placa por 20 min no escuro para estabilizar o sinal luminescente.
- Registre a luminescência usando um luminômetro ou uma câmera CCD.
- Plote a curva padrão tomando a média de cada ponto e, em seguida, subtraindo a média dos espaços em branco. Use a equação da linha para calcular a taxa metabólica (pmol/min/106 células) no restante das amostras, lembrando-se de incluir quaisquer diluições feitas.
- Retire os andaimes das placas usando um par de pinças e coloque-os em uma placa de 24 poços contendo 500 μL de D-PBS (Sem Ca++ e Mg++) em cada poço, tomando cuidado para não perturbar o microtecido.
- Tire instantâneos de cada andaime usando um microscópio de luz invertida na ampliação 10x.
- Executando o ensaio ATP (consulte Tabela de materiais) seguindo as instruções do fabricante:
- Descongele o reagente na RT.
- Lave os andaimes duas vezes com 500 μL de D-PBS (Sem Ca++ e Mg++) para cada etapa de lavagem.
- Adicione 120 μL de reagente e 120 μL de PBS a cada andaime e os mesmos volumes a um poço vazio (este servirá como em branco). Coloque a placa coberta com papel alumínio em um agitador e agite vigorosamente (500 rpm) por 5 minutos seguido de 30 min de incubação para estabilizar o sinal de luminescência.
- Transferir 100 μL das amostras lisadas em duplicata para uma placa de ensaio de fundo plano transparente de 96 poços para medição. Certifique-se de que os poços em branco não sejam colocados ao lado dos outros poços de medição de alta luminescência.
- Registre a luminescência usando um leitor de microplacas.
- Comparar a luminescência das amostras com a luminescência das normas para determinar o ATP detectado pelo reagente nas amostras.
Resultados
O manuscrito descreve um modelo de MPS hepático usado para avaliar o DILI. O MPS facilita a geração de microtecidos hepáticos 3D que são mantidos altamente funcionais sob fluxo por até 4 semanas. PHHs / HKCs são semeados em andaimes revestidos de colágeno para formar microtecidos hepáticos que são perfundidos com um meio de crescimento e, depois de passar na verificação QC, são dosados com compostos. Aqui, mostramos dados para troglitazona e pioglitazona, dois compostos estruturalmente semelhantes, mas com diferentes gravidades DILI.
No Dia 4, antes da dosagem do medicamento, uma verificação QC dos microtecidos hepáticos formados é avaliada e consiste em liberação de LDH e síntese de ureia (Figura 1A). O QC visa confirmar que a MPS hepática produz microtecidos hepáticos altamente consistentes e funcionais. Os dados aqui apresentados são gerados a partir de três experimentos e mostram bons níveis de reprodutibilidade com baixa variabilidade intra e interestudo. Após uma cultura de 8 dias, múltiplas métricas de saúde e hepáticas (albumina, ureia, CYP3A4, ATP) são avaliadas e os microtecidos de controle apresentam altos níveis de funcionalidade e reprodutibilidade hepática (Figura 1B,C). A microscopia de fase de contraste e a coloração IF dos microtecidos hepáticos (Ver Material Suplementar) mostram alta consistência de semeadura em todos os microcanais do andaime e revelam a distribuição de HKCs nos microtecidos PHH (Figura 1D)
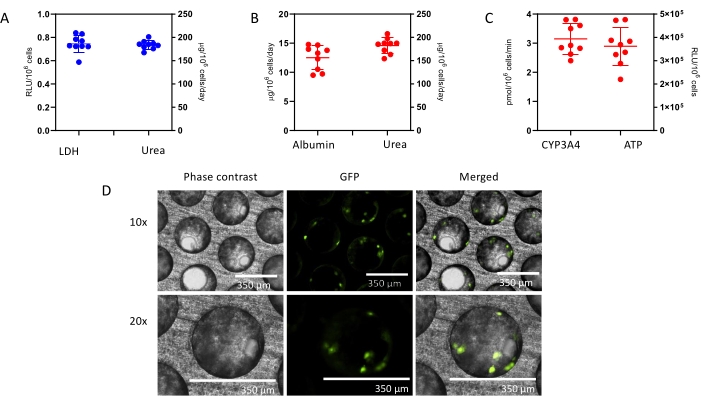
Figura 1: A MPS hepática produz dados altamente reprodutíveis e microtecidos consistentes. (A) Métricas de QC de microtecido hepático 3D no Dia 4 e avaliação da funcionalidade no final do estudo no Dia 8 -(B) Albumina e Ureia, (C) CY3A4 e ATP). Os dados são coletados de 3 experimentos; em cada experimento, houve 3 repetições de controle do veículo. Os dados apresentados são Média ± DP, N = 9. (D) Microscopia de contraste de fase (10x e 20x) e FI de microtecidos hepáticos 3D gerados pela cocultura de PHHs e HKCs na plataforma de MPS hepática para avaliação de DILI. Para visualizar os HKCs, antes da semeadura, os HKCs foram transduzidos com um vetor adenoviral que expressa eGFP (ver Material Suplementar). Fotomicrografias representativas são mostradas. A transdução e a imagem foram realizadas como um experimento autônomo para demonstrar a localização celular e não foram feitas com o protocolo DILI descrito. As células HKCs são pré-validadas internamente antes do uso em cultura celular experimental e devem ter baixos níveis de ativação pós-descongelamento; isso é avaliado pela medição dos biomarcadores IL-6 e TNF-alfa. Por favor, clique aqui para ver uma versão maior desta figura.
Sabe-se que a troglitazona causa DILI grave; após a sua licença para o tratamento da diabetes tipo 2, foi retirado pela FDA após 3 anos no mercado devido à frequência de lesão hepática associada ao seu uso. Até o momento, estudos publicados em animais não conseguiram prever o potencial da troglitazona para causar lesões hepáticas graves. A toxicidade deste composto também não foi detectada em ensaios hepáticos 2D padrão in vitro 14.
Os microtecidos hepáticos da MPS foram dosados com troglitazona por 96 h, o que causou uma resposta tóxica aguda, Cmáx , que foi detectada pela liberação de ALT e LDH e uma rápida redução na produção de albumina e ureia, em torno de 15 x Cmax, após exposição aguda à troglitazona (Figura 2A). O objetivo celular (teor de ATP) e a atividade do CYP3A4 (para avaliar a biotransformação metabólica), amostrados após 96 h de exposição, toxicidade confirmada adicional causada pela troglitazona e valores de EC:50 foram altamente comparáveis a outros parâmetros de avaliação (Figura 2B). Imagens de microscopia de campo brilhante obtidas após 8 dias de cultura no MPS revelam um microtecido hepático saudável, uniformemente semeado em todo o andaime (controle do veículo) em contraste com a morte/degradação tecidual generalizada, como visto nas replicações tratadas com controle positivo e troglitazona nas duas principais concentrações de teste (Figura 2C).
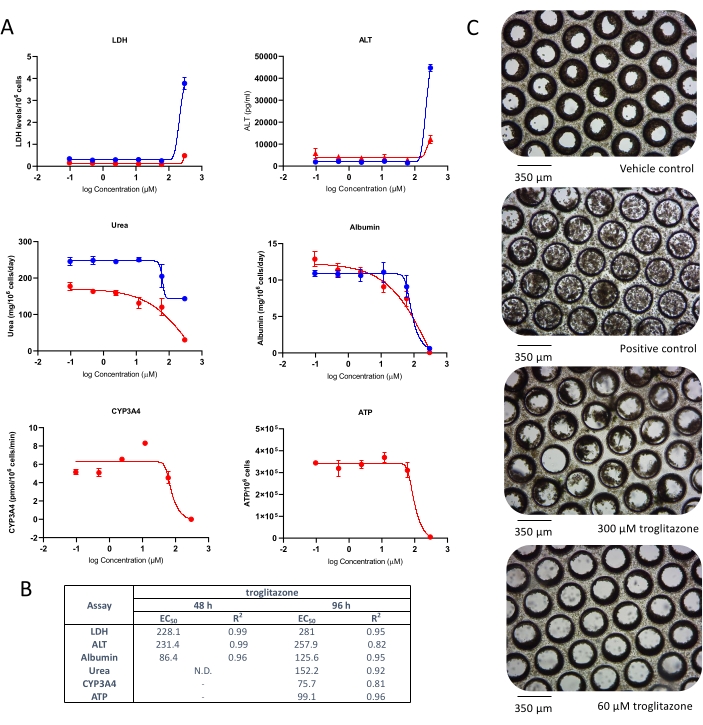
Figura 2: Determinação do risco de troglitazona por DILI utilizando múltiplos parâmetros de avaliação hepatotóxicos. Os microtecidos hepáticos foram expostos a sete concentrações de teste de troglitazona por 96 h e comparados para (A) liberação de LDH, liberação de ALT, produção de albumina, síntese de ureia, atividade do CYP3A4 e conteúdo de ATP. Linhas azuis - exposição de 48 h (apenas pontos de extremidade da mídia), linhas vermelhas - exposição de 96 h. O controle positivo foi de clorpromazina 100 μM. Todos os desfechos são medidos a partir das mesmas culturas de MPS hepática. Os dados apresentados são médios ± DP, N = 3. (B) Resumo dos números E:50 gerados a partir de dados. N.D. = dados não plotáveis. Linha = não ensaiada. (C) Microscopia representativa de campo brilhante dos microtecidos hepáticos após 8 dias de cultura (ampliação de 10x). Por favor, clique aqui para ver uma versão maior desta figura.
A toxicidade hepática após a exposição à pioglitazona também foi investigada. A pioglitazona é um composto sabidamente de baixa preocupação com DILI4 e não exerceu hepatotoxicidade em culturas clássicas de hepatócitos primários 2D e mesmo em alguns modelos 3D mais avançados10,11. Efeitos hepatotóxicos leves foram observados em ambos os momentos testados (Figura 3). Nenhuma liberação de LDH ou ALT foi detectada; entretanto, após 48 h, observou-se leve redução na produção de albumina e ureia, em aprox. 25x Cmax (Figura 3A). Redução muito pequena no teor de ATP também foi observada em altas concentrações de pioglitazona, mas isso não foi significativo. Os valores de EC:50 gerados a partir de curvas dose-resposta são apresentados na Figura 3B. A microscopia revelou discreta alteração microtecidual após 96 h de exposição à pioglitazona nas duas maiores concentrações testadas (Figura 3C). Os resultados demonstram a capacidade da MPS hepática de detectar a toxicidade de compostos com leve preocupação com DILI.
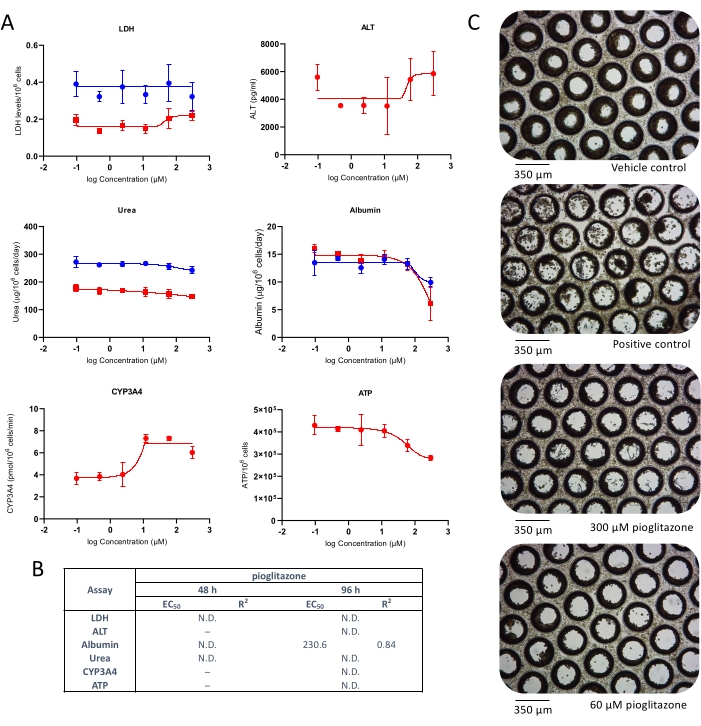
Figura 3: Determinação do risco de pioglitazona por DILI utilizando múltiplos parâmetros de avaliação hepatotóxicos. Os microtecidos hepáticos foram expostos a sete concentrações de teste de pioglitazona por 96 h e comparados para (A) liberação de LDH, liberação de ALT, produção de albumina, síntese de ureia, atividade do CYP3A4 e conteúdo de ATP. Linhas azuis - exposição de 48 h (apenas pontos de extremidade da mídia), linhas vermelhas - exposição de 96 h. O controle positivo foi de clorpromazina 100 μM. Todos os desfechos são medidos a partir das mesmas culturas de MPS hepática. Os dados apresentados são médios ± DP, N = 3. (B) Resumo dos números EC:50 gerados a partir de dados. N.D. = dados não plotáveis. Linha = não ensaiada. (C) Microscopia representativa de campo brilhante dos microtecidos hepáticos após 8 dias de cultura (ampliação de 10x). Por favor, clique aqui para ver uma versão maior desta figura.
Ao avaliar todos os parâmetros de avaliação funcionais e biomarcadores de saída de toxicidade que possam representar cenários in vivo ou clínicos (libertação de LDH, síntese de ureia, produção de albumina, atividade do CYP3A4, teor de ATP, libertação de ALT) e corroborando os dados gerados para ambos os compostos testados dosados num intervalo de dose de sete pontos durante 48 h e 96 h, foi gerado um mapa de calor para produzir uma "assinatura de hepatotoxicidade", ajudando a identificar compostos com diferentes níveis de preocupação com DILI (Figura 4).
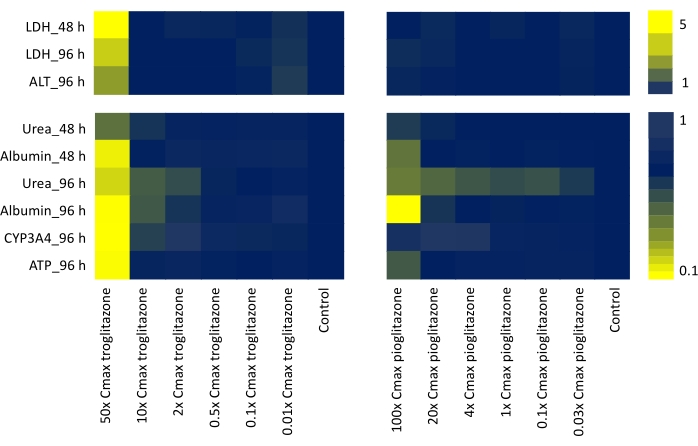
Figura 4: Determinação da "assinatura de toxicidade" com MPS hepática. Mapa de calor mostrando troglitazona e pioglitazona de seis desfechos funcionais específicos do fígado (liberação de LDH, síntese de ureia, produção de albumina, liberação de ALT, atividade do CYP3A4 e conteúdo de ATP) após 48 horas e 96 h de exposição a uma faixa de dose de sete pontos. Cada valor é gerado como Média, N = 3 e normalizado para amostras de controle. Os valores nas barras de cores representam um aumento de dobra em relação aos controles de linha de base. Por favor, clique aqui para ver uma versão maior desta figura.
Material Suplementar: Imagem em microscópio fluorescente de microtecidos e avaliação de pré-qualificação de células. Clique aqui para baixar este arquivo.
Discussão
Os MPS são projetados para recapitular unidades funcionais de órgãos humanos in vitro e foram desenvolvidos para abordar as limitações dos modelos convencionais de cultura de células 3D27. O fígado é um dos órgãos mais modelados usando MPS, e uma grande variedade de sistemas foram desenvolvidos. O fígado humano é responsável pelo metabolismo de fármacos e geração de metabólitos tóxicos de fármacos, e sua função é um elemento-chave para o modelo de desenvolvimento de fármacos, incluindo a avaliação da responsabilidade de compostos por DILI28. Aqui introduzimos um novo método para avaliar DILI usando um MPS hepático; o protocolo permite que insights mecanicistas sejam buscados para cada composto ensaiado para determinar como ele pode causar DILI, além de ser um ensaio altamente sensível e robusto. Os microtecidos hepáticos são formados nas placas de MPS, que são uma cocultura de PHH e HKCs e são altamente funcionais com altos níveis de produção de albumina e ureia, bem como alta atividade do CYP3A4 em comparação com os modelos hepáticos in vitro padrão20.
Embora o modelo DILI descrito aqui possa servir como uma ferramenta útil em estágios posteriores de testes pré-clínicos no processo de desenvolvimento de medicamentos, ele também tem várias limitações. Como a maioria dos MPS atualmente disponíveis no mercado, é uma plataforma de baixo rendimento e, portanto, mais difícil de usar para atividades de triagem de drogas em larga escala. Consistindo de microtecidos formados por PHHs e HKCs coculturais, o modelo DILI também não pode capturar inteiramente a complexidade do fígado humano, e uma otimização adicional incorporando diferentes tipos de células (por exemplo, células imunes) seria benéfica para agregar valor ao modelo existente. Este MPS de órgão único também pode ser combinado com outras plataformas de órgãos que podem compartilhar um meio comum e permitir o crosstalk de órgãos no nível celular ou endócrino, e que podem ajudar a entender melhor os insights mecanicistas da toxicidade não limitados apenas ao próprio fígado. Além disso, como qualquer tecnologia relativamente nova, pode ser considerada dispendiosa e, por conseguinte, de acessibilidade limitada.
MPS é uma plataforma usada para desenvolver modelos organotípicos de tecidos humanos únicos ou múltiplos. O sistema é composto por um controlador, cabo umbilical e driver MPS no qual a placa é inserida (Figura 5A). Cada placa MPS hepática tem 12 poços abertos independentes para a cultura de células hepáticas primárias em 3D em andaimes modificados. Em resumo, o sistema é verificado por QC, e as placas são preparadas no Dia -1, os PHHs e HKCs são semeados nas placas no Dia zero (Figura 5B, ver 1). As microbombas incorporadas facilitam a circulação de meios de cultura celular através dos andaimes para facilitar a formação de microtecidos 3D (Figura 5B, ver 2). Os microtecidos formados são QC'd no Dia 4, dosados com diferentes concentrações de cada composto a cada 48 h durante 4 dias e ensaiados para biomarcadores de desfecho no Dia 8 (Figura 5C). A linha do tempo experimental do ensaio DILI na placa MPS está representada na Figura 5D.
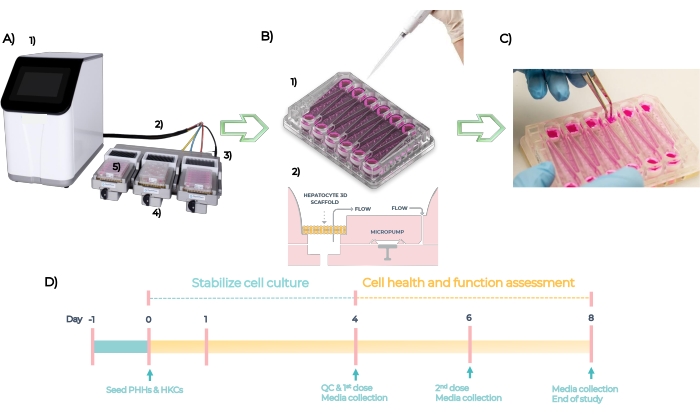
Figura 5: O sistema microfisiológico e a linha do tempo experimental de um ensaio DILI padrão. (A) O sistema microfisiológico com seus componentes: controlador (1), cabo umbilical (2), docking station (3), driver MPS (4) e placa LC12 (5). (B) A semeadura de PHHs e HKCs na placa de CL12 no Dia 1 (1) e microbombas embutidas facilitam a circulação de meios de cultura celular com taxas de fluxo ajustáveis através dos microtecidos 3D semeados nos andaimes (2). (C) Derrubar os andaimes no final do estudo. (D) Linha do tempo experimental. Por favor, clique aqui para ver uma versão maior desta figura.
Ao executar o protocolo, é importante que uma verificação robusta do QC do sistema seja realizada antes do início, verificando se o sistema está funcionando pneumaticamente corretamente e as placas consumíveis são inspecionadas visualmente e preparadas de forma eficiente para garantir a funcionalidade uniforme em todos os poços. Ter células humanas primárias de alta qualidade é essencial para este protocolo, com hepatócitos conhecidos por aderirem consistentemente em experimentos de cultura de células e formarem interações 3D. O descongelamento dessas células também é um passo crítico, pois os hepatócitos primários não devem ser ressuspensos por ação de pipetagem, pois isso pode levar rapidamente à morte celular. Ter viabilidade celular acima de 85% é fundamental para uma semeadura bem-sucedida, pois grandes quantidades de detritos celulares interferirão na formação de microtecidos 3D. A verificação do QC dos microtecidos hepáticos formados no Dia 4 também é importante, e o usuário precisa garantir que os níveis aceitáveis de LDH e Ureia sejam medidos, pois os parâmetros fora do alcance podem ser indicativos de formação de tecido de baixa qualidade e permitir a solução de problemas direta. Finalmente, a hidrocortisona utilizada no meio de cultura celular deve ser preparada fresca no dia do uso para evitar qualquer degradação indesejada que possa afetar a funcionalidade da cultura celular, pois é necessária para manter a funcionalidade metabólica dos hepatócitos.
Apesar de ter uma complexidade significativa, o MPS do fígado não contém todos os tipos de células do fígado humano. É possível adicionar mais tipos de células ao modelo24,29 para aumentar a relevância fisiológica, mas estas só devem ser adicionadas com uma justificativa clara para o contexto de uso. Para o estudo DILI PHH são o tipo de célula chave, e a incorporação de HKCs neste modelo permite que algumas respostas imunológicas sejam determinadas. Deve-se notar também que PHHs isolados de fígados humanos e PHHs criopreservados comercialmente disponíveis tendem a demonstrar algumas variações de lote para lote. Demonstramos aqui que este protocolo produz resultados reprodutíveis quando usado com preparações de células de alta qualidade. No entanto, alguma variação de lote seria esperada, e isso poderia ser ainda mais superado usando lotes agrupados de vários doadores. Essas limitações poderiam ser superadas com o uso de células semelhantes a hepatócitos diferenciadas de iPSC que recapitulam muitas propriedades funcionais dos PHHs e que têm sido utilizadas no processo de desenvolvimento de fármacos30. Os HKCs também mostram muita variabilidade e um alto nível de ativação após o descongelamento; portanto, os doadores de HKCs são pré-validados internamente antes do uso em cultura celular experimental (cocultura com PHHs validados) e devem ter baixos níveis de ativação pós-descongelamento; isto é avaliado através da medição de biomarcadores IL-6 e TNF-alfa (ver Material Suplementar).
Os dados aqui apresentados confirmam que o ensaio pode detectar DILI com precisão, ajudando a identificar hepatotóxicos que podem não ser detectados por modelos 2D10,11 e até mesmo por alguns modelos 3D. Os dados gerados a partir da MPS ainda não são utilizados como padrão pela indústria farmacêutica para submissões regulatórias ou para fins de triagem de medicamentos, devido à falta de padronização e harmonização de processos, incluindo a reprodutibilidade entre os locais20. Os dados e as abordagens experimentais aqui demonstrados abordam isso, mostrando que o modelo hepático pode ser usado rotineiramente e robustamente em telas DILI para prever com precisão a responsabilidade de novos compostos.
Medindo uma gama de parâmetros de avaliação para produzir uma "assinatura de hepatotoxicidade", ajudando a identificar compostos com diferentes níveis de preocupação DILI (incluindo compostos não detectáveis por outros métodos in vitro) e os seus mecanismos de toxicidade revelados. Esta tecnologia pode fechar a lacuna entre a cultura celular tradicional e os modelos animais de um lado e os ensaios clínicos em humanos, avançando para a simulação de condições biológicas humanas para a avaliação pré-clínica da toxicidade hepática como parte do processo de desenvolvimento de medicamentos.
Divulgações
Todos os autores são funcionários da CN Bio Innovations Limited.
Agradecimentos
A CN Bio Innovations Ltd. financiou este estudo.
Materiais
| Name | Company | Catalog Number | Comments |
| 24 well cell culture cluster plates flat bottom | Corning | 3524 | |
| 96 well clear assay plates, flat bottom clear plastic | Greiner | 655101 | |
| 96 well plates black flat bottom | Corning | 3915 | |
| 96 Well White/Clear Bottom Plate, TC Surface | ThermoScientific | 165306 | |
| Advanced DMEM (1x) | Gibco | 12491015 | Cell culture media. |
| AssayMax Albumin ELISA Kit | AssayPro | EA3201-1 | Dilution 1:250. Time point Day 4, 6, and 8. |
| Cell Maintenance Cocktail B, (Primary Hepatocyte Maintenance Supplements) | Gibco | CM4000 | |
| CellTiter-Glo 3D Cell Viability Assay | Promega | G9682 | Dilution 1:1. Time point Day 8. |
| Chlorpromazine HCl | Sigma Aldrich | C8138 | |
| Chromacol blue lids, 9 mm Autosampler Vial Screw Thread Caps | ThermoScientific | 9-SCK(B)-ST1 | glass vial |
| Chromacol vials, 9 mm Clear Glass Screw Thread Vials | ThermoScientific | 2-SVW | |
| Class 2 Microbiological Safety Cabinets - Trimat2 1500 exhaust | Contained Air Solutions | ||
| Conical tubes 50 mL | Greiner | 227261 | |
| Cryopreserved Hepatocyte Recovery Medium (CHRM) | ThermoFisher Scientific | Gibco CM7000 | |
| Cryopreserved primary human hepatocytes | BioIVT Europe | Lot. RAS | |
| CytoTox 96 Cytotoxicty (LDH) Assay Kit | Promega | G1781 | Dilution - none. Time point Day 4, 6 and 8 |
| >Data analysis model used to generate the graph and EC:50 curves was nonlinear regression (curve fit) asymmetric sigmoidal, 5PL, where X is log(concentration | GraphPad Prism 9 | ||
| Disposable PES Filter Units 500mL | Fisher Scientific | 15913307 | |
| Disposable Pipette Basins 50ml | Fisher Scientific | 12369175 | |
| DMSO (Dimethyl sulfoxide) | Sigma-Aldrich | Sigma D2650 | |
| Dulbeco’s Phosphate Buffered Saline without Ca2+ and Mg2+ (D-PBS) | ThermoFisher Scientific | 14190-144 | |
| Easy Reader Conical Polypropylene Centrifuge Tubes 15 mL | Fisher Scientific | 11889640 | |
| Foetal bovine serum | Gibco | 10500064 | |
| Human ALT ELISA Kit | Abcam | ab 234578 | Dilution 1:5. Time point Day 6 and 8. |
| Human Cryopreserved Kupffer Cells | Lonza Europe | Lot. 190088KC | |
| hydrocortisone | Merck | H0888-1G | |
| Incubators models: New Brunswick Galaxy 170 S, New Brunswick Galaxy 170 R and CellXpert® C170. | Eppendorf | All serviced yearly; paperwork available upon request. | |
| Inverted Microscope | Leica DMIL LED | ||
| MPS know as Organ-on-a-Chip (OOC) | CN Bio Innovations Ltd. | ||
| MPS LC-12 plate | CN Bio Innovations Ltd. | ||
| Neubauer Improved C-Chip Disposable Haemocytometer (2 channel) | Cambridge Bioscience | DHC-N01-50 | |
| P450-Glo CYP3A4 Assay and Screening System | Promega | V9002 | Dilution - none. Time point Day 8 |
| PhysioMimix MPS platform | CN Bio Innovations Ltd. | ||
| Pioglitazone | MedChemExpress Tocris | HY-13956/CS-1700 | |
| Quantichrom Urea Assay Kit – Bioassay systems | Bioassay Systems | DY970-05 | Dilution 1:2 if initial reading is too high. Time point Day 4, 6 and 8. |
| Silica gel | Sigma-Aldrich | S7625 | |
| Software used to analyse and generate all the graphs was | GraphPad Prism 9 | ||
| Stripettes 10 mL | Fisher Scientific | 11839660 | |
| Stripettes 25 mL | Fisher Scientific | 11839181 | |
| Thawing plate Cocktail A, (Primary Hepatocyte Thawing and Plating Supplements) | Gibco | CM3000 | |
| Troglitazone | MedChemExpress Tocris | 97322-87-7 | |
| Trypan Blue Solution, 0.4% | Gibco | 15250061 | |
| Tubes 1.5 mL | Greiner | 616201 | |
| Weighing balance - model PA214C and AV213C | Ohaus Corp |
Referências
- Lisi, D. M. Drug-induced liver injury: An overview. US Pharmacist. 41 (12), 30-34 (2016).
- Kuna, L., et al. Models of drug induced liver injury (DILI)-current issues and future perspectives. Current Drug Metabolism. 19 (10), 830-838 (2018).
- Katarey, D., Verma, S. Drug-induced liver injury. Clinical Medicine. 16 (6), 104-109 (2016).
- Kullak-Ublick, G. A., et al. Drug-induced liver injury: recent advances in diagnosis and risk assessment Recent advances in clinical practice. Gut. 66, 1154-1164 (2017).
- Dirven, H., et al. Performance of pre-clinical models in predicting drug-induced liver injury in humans: a systematic review. Scientific Reports. 11 (1), 6403 (2021).
- Donato, M. T., Lahoz, A., Castell, J. V., Gomez-Lechon, M. J. Cell lines: a tool for in vitro drug metabolism studies. Current Drug Metabolism. 9 (1), 1-11 (2008).
- Wilkening, S., Stahl, F., Bader, A. Comparison of primary human hepatocytes and hepatoma cell line HepG2 with regard to their biotransformation properties. Drug Metabolism and Disposition. 31 (8), 1035-1042 (2003).
- Gerets, H. H. J., et al. Characterization of primary human hepatocytes, HepG2 cells, and HepaRG cells at the mRNA level and CYP activity in response to inducers and their predictivity for the detection of human hepatotoxins. Cell Biology and Toxicology. 28 (2), 69-87 (2012).
- Grainger, C. I., Greenwell, L. L., Lockley, D. J., Martin, G. P., Forbes, B. Culture of Calu-3 cells at the air interface provides a representative model of the airway epithelial barrier. Pharmaceutical Research. 23 (7), 1482-1490 (2006).
- Li, F., Cao, L., Parikh, S., Zuo, R. Three-dimensional spheroids with primary human liver cells and differential roles of kupffer cells in drug-induced liver injury. Journal of Pharmaceutical Sciences. 109 (6), 1912-1923 (2020).
- Proctor, W. R., et al. Utility of spherical human liver microtissues for prediction of clinical drug-induced liver injury. Archives of Toxicology. 91 (8), 2849-2863 (2017).
- Lin, C., Khetani, S. R. Advances in engineered liver models for investigating drug-induced liver injury. BioMed Research International. 2016, 1829148 (2016).
- Olson, H., et al. Concordance of the toxicity of pharmaceuticals in humans and in animals. Regulatory Toxicology and Pharmacology. 32 (1), 56-67 (2000).
- Bell, C. C., et al. Comparison of hepatic 2D sandwich cultures and 3D spheroids for long-term toxicity applications: A multicenter study. Toxicological Sciences. 162 (2), 655-666 (2018).
- Bell, C. C., et al. Characterization of primary human hepatocyte spheroids as a model system for drug-induced liver injury, liver function and disease. Scientific Reports. 6, 25187 (2016).
- Khetani, S. R., et al. Use of micropatterned co-cultures to detect compounds that cause drug-induced liver injury in humans. Toxicological Sciences. 132 (1), 107-117 (2013).
- Ma, X., et al. Deterministically patterned biomimetic human iPSC-derived hepatic model via rapid 3D bioprinting. Proceedings of the National Academy of Sciences of the united States of America. 113 (8), 2206-2211 (2016).
- Dieterle, P. Y. M., Dieterle, F. Tissue-specific, non-invasive toxicity biomarkers: translation from pre-clinical safety assessment to clinical safety monitoring. Expert Opinion on Drug Metabolism & Toxicology. 5 (9), 1023-1038 (2009).
- Rowe, C., et al. Perfused human hepatocyte microtissues identify reactive metabolite-forming and mitochondria-perturbing hepatotoxins. Toxicology in Vitro. 46, 29-38 (2018).
- Rubiano, A., et al. Characterizing the reproducibility in using a liver microphysiological system for assaying drug toxicity, metabolism, and accumulation. Clinical and Translational Science. 14 (3), 1049-1061 (2021).
- Tsamandouras, N., Kostrzewski, T., Stokes, C. L., Griffith, L. G., Hughes, D. J., Cirit, M. Quantitative assessment of population variability in hepatic drug metabolism using a perfused three-dimensional human liver microphysiological system. Journal of Pharmacology and Experimental Therapeutics. 360 (1), 95-105 (2017).
- Ortega-Prieto, A. M., et al. 3D microfluidic liver cultures as a physiological pre-clinical tool for hepatitis B virus infection. Nature Communications. 9 (1), 682 (2018).
- Kostrzewski, T., et al. Three-dimensional perfused human in vitro model of non-alcoholic fatty liver disease. World Journal of Gastroenterology. 23 (2), 204-215 (2017).
- Kostrzewski, T., et al. A microphysiological system for studying nonalcoholic steatohepatitis. Hepatology Communications. 4 (1), 77-91 (2020).
- Vacca, M., et al. Bone morphogenetic protein 8B promotes the progression of non-alcoholic steatohepatitis. Nature Metabolism. 2 (6), 514-531 (2020).
- Long, T. J., et al. Modeling therapeutic antibody-small molecule drug-drug interactions using a three-dimensional perfusable human liver co-culture platforms. Drug Metabolism and Disposition. 44, 1940-1948 (2016).
- Bai, J., Wang, C. Organoids and microphysiological systems: New tools for ophthalmic drug discovery. Frontiers in Pharmacology. 11, 407 (2020).
- Ribeiro, A. J. S., Yang, X., Patel, V., Madabushi, R., Strauss, D. G. Liver microphysiological systems for predicting and evaluating drug effects. Clinical Pharmacology & Therapeutics. 106 (1), 139-147 (2019).
- Clark, A. M., et al. A microphysiological system model of therapy for liver micrometastases hhs public access. Experimental Biology and Medicine (Maywood). 239 (9), 1170-1179 (2014).
- Qosa, H., Ribeiro, A. J. S., Hartman, N. R., Volpe, D. A. Characterization of a commercially available line of iPSC hepatocytes as models of hepatocyte function and toxicity for regulatory purposes. Journal of Pharmacological and Toxicological Methods. 110, 107083 (2021).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados