Case Report
Técnica híbrida nova e inovadora para dissecção da aorta tipo A
Neste Artigo
Resumo
O protocolo descreve a substituição da aorta ascendente combinada com cobertura endovascular de todo o arco aórtico com endoprótese fenestrada em um paciente com dissecção aguda da aorta tipo A na ausência de ruptura do arco aórtico.
Resumo
A dissecção aguda da aorta tipo A de Stanford (TAAD) é uma emergência cirúrgica caracterizada por uma alta taxa de mortalidade e inúmeras complicações. No tratamento do TAAD, o momento da cirurgia e a escolha do procedimento cirúrgico são de suma importância. A reconstrução total aberta do arco aórtico continua sendo o padrão-ouro para a cirurgia do arco aórtico e é um dos procedimentos mais desafiadores. No entanto, essa abordagem é invasiva, relativamente demorada e associada a sangramento substancial, o que requer altos níveis de habilidade do operador e acarreta o risco de múltiplas complicações, principalmente neurológicas. Este relato descreve um novo procedimento híbrido denominado Substituição Aberta da Aorta Ascendente Combinada com Implante de Stent no Arco Aórtico Total Fenestrado. Foi selecionado um caso em que a lesão não envolvia o arco aórtico, pelo menos no lado de maior curvatura do arco. Foi realizada substituição da aorta ascendente, seguida de intervenção do arco com endopróteses automodificadas para preservar os ramos nativos do arco aórtico. Essa abordagem permite uma rápida simplificação do procedimento, evita hipotermia profunda ou parada circulatória associada à cirurgia aberta convencional e atenua as complicações neurológicas.
Introdução
A dissecção da aorta é uma emergência cardiovascular rara associada a uma alta taxa de mortalidade; no entanto, sua incidência aumentou nos últimos anos, enquanto a idade de início diminuiu, particularmente para a dissecção da aorta tipo A de Stanford (TAAD)1,2. O implante aórtico continua sendo o procedimento mais utilizado para o TAAD3. Inúmeras complicações pós-operatórias são encontradas e as taxas de mortalidade são elevadas devido a trauma significativo e parada circulatória hipotérmica prolongada 4,5.
O desenvolvimento do reparo endovascular da aorta torácica (TEVAR) levou ao surgimento da cirurgia híbrida 6,7,8, tornando o procedimento minimamente invasivo e menos complexo. Embora existam indicações estritas, a redução da perda sanguínea, o menor tempo operatório e a ausência de parada hipotérmica profunda atenuam o alto risco de complicações pós-operatórias.
A cirurgia híbrida visa encurtar o tempo de recuperação funcional. A porção ascendente da aorta foi substituída, independentemente de a raiz ter sido manejada. O arco foi fenestrado com endopróteses (SGs), e um stent cobriu a porção descendente para ampliar a luz verdadeira. Essa técnica híbrida resulta em menor tempo operatório, diminuição da perda sanguínea e o risco de eventos neurológicos pós-operatórios e complicações significativas são comparáveis ou menores do que aqueles associados à substituição aberta. As etapas cirúrgicas são simplificadas por meio do manejo reduzido dos três ramos do arco, em comparação com outras cirurgias híbridas anteriores9. Estudos anteriores demonstraram que a cirurgia híbrida é caracterizada por trauma reduzido e recuperação acelerada. Reconhece-se que inúmeras variações podem existir em quase todas as etapas do procedimento10,11.
Este estudo apresenta uma abordagem para a cirurgia híbrida que incorpora TEVAR. A identificação precisa e o alinhamento cuidadoso, particularmente dos três ramos do supra-arco, são críticos. Este caso envolve um homem de 55 anos que apresentou dor torácica intensa. A angiotomografia computadorizada (angio-TC) sugeriu TAAD sem ruptura do arco. O paciente consentiu em ser submetido à cirurgia híbrida, seguida de substituição da aorta ascendente e arcada total usando implante de SGs fenestrados automodificados (Figura 1), e acabou recebendo alta hospitalar.
APRESENTAÇÃO DO CASO:
Paciente do sexo masculino, 55 anos, apresentou aperto no peito e dor iniciada há 11 horas, sem nenhum gatilho aparente. Ele tinha uma história de hipertensão de 3 anos, com pressão arterial máxima de 150/100 mmHg, e não estava tomando nenhum medicamento para controlar sua pressão arterial. Ele também tinha uma história de gota de 20 anos, sem história de hiperlipidemia, diabetes mellitus, hepatite B ou tuberculose. Negava cirurgia prévia, transfusões de sangue, alergias a medicamentos ou alimentos e não relatava história familiar significativa. Na admissão, o paciente estava alerta e orientado e recebia oxigênio por meio de cânula nasal. A monitorização cardíaca revelou frequência cardíaca de 68 batimentos por minuto, saturação de oxigênio de 100%, frequência respiratória de 16 respirações por minuto e pressão arterial de 126/83 mmHg no membro superior esquerdo, 139/79 mmHg no membro superior direito, 135/80 mmHg no membro inferior esquerdo e 150/84 mmHg no membro inferior direito. A temperatura da pele dos membros superiores era fria, mais ainda do lado direito. Ambas as pupilas eram iguais em tamanho, redondas e com aproximadamente 3 mm de diâmetro, e eram reativas à luz. Os murmúrios vesiculares de ambos os pulmões eram claros na ausculta, sem estertores secos ou úmidos. As bulhas cardíacas eram normais e não se ouviam sopros patológicos em nenhum dos sítios de ausculta valvar. O abdômen estava macio, sem sensibilidade ou dor na rebote. O fígado e o baço não eram palpáveis abaixo da caixa torácica. Os membros mostraram força muscular normal e nenhum edema foi observado nos membros inferiores. Os pulsos pediosos dorsais eram palpáveis e nenhum sinal patológico foi eliciado.
Diagnóstico, avaliação e plano:
Após a admissão do paciente, foram realizados exames e investigações adequadas. O ecocardiograma cardíaco revelou os seguintes diagnósticos: 1. hipertrofia ventricular esquerda, 2. dilatação proximal da aorta ascendente. A aorta mostrou-se anormal, e o exame de angiotomografia confirmou o diagnóstico de dissecção da aorta (tipo Stanford A) sem ruptura da aorta ascendente ou arco. A dissecção envolveu a artéria mesentérica superior, as artérias ilíacas comuns bilaterais e a artéria ilíaca externa direita. A artéria renal direita foi suprida pela pseudocavidade, e derrames pleurais bilaterais e expansão inadequada dos lobos pulmonares inferiores foram observados. Foi administrado tratamento sintomático, incluindo controle da pressão arterial e da frequência cardíaca e analgesia. O diagnóstico do paciente foi confirmado, um exame de cabeça e abdome foi realizado, as contraindicações à cirurgia foram excluídas e a família do paciente recebeu informações detalhadas para facilitar o preparo pré-operatório.
Protocolo
O consentimento informado por escrito foi obtido do paciente para o procedimento, e foi dada concordância para a substituição da aorta ascendente com os GEs fenestrados. Este estudo foi conduzido em conformidade com todas as diretrizes institucionais, nacionais e internacionais de bem-estar humano12 e recebeu aprovação do Comitê de Ética da Faculdade de Medicina de Tongji, Universidade de Ciência e Tecnologia de Huazhong (documento do Conselho de Revisão Institucional número TJ-IRB20220124). O consentimento informado por escrito dos pacientes foi obtido para a publicação do manuscrito e das imagens que o acompanham.
1. Avaliação pré-operatória da angio-TC
- A fenestração foi desenhada de acordo com as características da lesão, a medida precisa antes da operação e a configuração do GE (Figura 2).
- Os diâmetros da aorta e das três principais artérias ramificadas foram medidos por meio de imagens de angio-TC, empregando-se o diâmetro circular ou o diâmetro médio elíptico das artérias. As medidas foram realizadas em vários pontos anatômicos, com atenção especial ao arco aórtico e seus ramos, que são cruciais para o planejamento da cirurgia híbrida para TAAD.
- Para obter medições precisas, uma linha central foi definida primeiro ao longo do comprimento da aorta e seus ramos. Para cada artéria, o diâmetro foi medido no plano da seção transversal perpendicular que cruzou a linha central no local de medição escolhido para evitar artefatos ou irregularidades na parede do vaso que pudessem influenciar a precisão das medidas.
- A aorta foi medida em pontos-chave, incluindo a aorta ascendente, o arco aórtico (distal à origem da artéria braquiocefálica) e a aorta torácica descendente. Da mesma forma, os diâmetros dos ramos maiores (artérias braquiocefálica, carótida comum esquerda e subclávia esquerda) foram medidos na origem e nos pontos distais ao longo do arco, garantindo consistência na técnica de medição. As medições foram obtidas usando uma ferramenta de software calibrada capaz de gerar visualizações transversais precisas e permitir uma avaliação confiável do diâmetro.
- O ângulo do arco aórtico é o ângulo entre a linha entre as extremidades proximal e distal do arco aórtico e o plano horizontal. O ângulo do arco foi determinado com o paciente em decúbito dorsal. Este ângulo determina o ângulo de projeção do bulbo quando o arco aórtico é implantado. Geralmente é oblíquo anterior esquerdo 30°-60°, com uma média de 45°.
2. Substituição da aorta ascendente
- O enxerto vascular artificial (AVG) adequado foi selecionado com base no diâmetro natural do vaso, medido por angio-TC.
- A condição da secção do seio aórtico, a íntima da raiz aórtica, o óstio da artéria coronária e as estruturas do folheto valvar aórtico foram avaliadas para determinar se o segmento mais proximal deveria ser tratado.
- Neste caso, a valva aórtica estava envolvida na lesão, incluindo envolvimento do anel aórtico e regurgitação da valva. Após a administração de heparina para obter anticoagulação adequada, a circulação extracorpórea (CEC) foi estabelecida através das artérias axilar e femoral e o paciente não foi submetido a parada cardíaca hipotérmica profunda. A CEC foi assistida para realizar a intervenção cirúrgica com segurança.
- A aorta ascendente foi então excisada, e um enxerto artificial personalizado (30 mm), selecionado com base nas medidas pré-operatórias da angio-TC, foi suturado no local para substituir o segmento aórtico doente. Ao mesmo tempo, a valva aórtica foi substituída por uma prótese valvar mecânica para tratar a disfunção valvar e garantir a estabilidade hemodinâmica a longo prazo.
- Durante todo o procedimento, a integridade do óstio da artéria coronária foi preservada, evitando-se essa zona para operações cirúrgicas e as estruturas radiculares da aorta foram cuidadosamente inspecionadas para garantir o alinhamento adequado do enxerto e da válvula. O procedimento teve como objetivo alcançar sucesso imediato e a longo prazo na restauração da integridade e função da aorta.
3. Fenestração dos SGs
- Após a conclusão da substituição da aorta ascendente, o tórax foi deliberadamente deixado aberto para facilitar a avaliação subsequente da anastomose distal. Para garantir a identificação precisa do local da anastomose para avaliação posterior, pinças de Kelly ou clipes de titânio foram colocados no local da anastomose distal. Esses marcadores servem como pontos de referência anatômicos claros para exames de imagem e intervenções cirúrgicas subsequentes.
- Após a colocação dos marcadores, foi realizada a angiografia por subtração digital (DSA)13 para avaliar a integridade e a perviedade do segmento aórtico recém-construído (Figura 3). A técnica de imagem DSA foi empregada para obter imagens de alta resolução e em tempo real da anastomose distal, permitindo uma avaliação precisa da dinâmica do fluxo sanguíneo e a ausência de complicações como estenose, vazamento ou mau posicionamento. O processo de subtração digital aumenta a visibilidade das estruturas vasculares, eliminando o tecido de fundo e destacando o lúmen cheio de contraste.
- A posição e o comprimento das aberturas do GV foram determinados com base em imagens intraoperatórias e dados de angiotomografia pré-operatória. Nesse caso, a localização da ruptura descendente foi próxima à artéria subclávia esquerda.
- Para evitar vazamento e manejo incompleto da lesão, foi planejado o envidraçamento in situ para a artéria subclávia esquerda para implantar o Viabahn, e a fenestração in vitro foi planejada para os dois ramos restantes do arco.
- Primeiro, a extremidade anterior do stent foi coberta e excedeu a anastomose aórtica distal em 10-15 mm. O comprimento da janela dos GVs foi definido pela extremidade proximal do óstio do tronco braquiocefálico e pela extremidade distal do óstio da artéria carótida comum esquerda. A largura da janela foi determinada principalmente pelo diâmetro dos vasos no arco e sua posição relativa entre si.
- Para posicionar com precisão as janelas dos SGs com os ramos correspondentes do arco aórtico, foram utilizadas suturas fixas de materiais radiopacos, como fio de aço inoxidável ou placas metálicas finas, em ambas as extremidades da janela do SG. Esses materiais são escolhidos por sua radiopacidade, o que permite uma visualização clara sob orientação fluoroscópica durante o procedimento.
- A sutura foi realizada com a colocação cuidadosa de suturas interrompidas ou contínuas através dos SGs nas bordas da janela. O fio ou folha metálica foi fixado ao stent nesses pontos para garantir o posicionamento estável e o alinhamento preciso da janela modificada com os vasos do arco, principalmente ao nível do tronco braquiocefálico e da artéria carótida comum esquerda, para minimizar o risco de complicações como reestenose ou desalinhamento do óstio do ramo.
- Se os galhos estivessem mais distantes na proa, janelas separadas eram usadas para cada um dos três ramos, exigindo medições precisas de uma imagem 3D.
4. Implantação de SGs
- Os GVs modificados foram implantados através da artéria femoral (Figura 4).
- A alça dos SGs foi girada e o SG foi liberado antes de desembainhar lentamente e abrir o suporte para a posição inicial da sobreposição do suporte. O lado do SG correspondente ao ponto branco na alça é identificado como o lado de abertura, e o marcador lateral de abertura foi confirmado.
- As posições anterior e posterior da janela de abertura também podem ser marcadas usando os segmentos SG correspondentes. A posição do arco aórtico e do ramo dentro do arco foi determinada repetidamente marcando o arco aórtico e dois ramos com marcadores de tela e marcadores correspondentes no osso.
- Um fio-guia foi avançado através da bainha até a artéria subclávia esquerda, com fluoroscopia em tempo real orientando o procedimento para garantir a colocação precisa do cateter no local correspondente aos SGs previamente implantados, após o qual um cateter-balão foi introduzido através da bainha e avançado para o óstio da artéria subclávia.
- A dilatação do balão foi cuidadosamente realizada no local dos SGs para otimizar a expansão do stent, melhorar a aposição à parede da aorta e restaurar o fluxo na aorta dissecada. O balão foi inflado gradualmente e a pressão foi cuidadosamente monitorada para evitar lesões nos vasos, garantindo a expansão adequada do stent. Após a dilatação bem-sucedida do balão, uma endoprótese coberta com Viabahn foi implantada em todo o local para minimizar o risco de vazamento e garantir a posição dos SGs.
- Dependendo da necessidade do paciente, um segundo stent foi implantado na aorta descendente para eliminar o máximo possível da falsa luz.
5. Posicionamento do fio-guia
- No procedimento TEVAR para TAAD, o implante de SGs requer manuseio meticuloso do fio-guia para garantir a implantação precisa do stent. Inicialmente, um fio-guia foi selecionado e cuidadosamente moldado para corresponder à anatomia da aorta. Para apoiar o fio-guia adequadamente e evitar complicações durante o avanço, foi utilizado um AVG ramificado ou pré-tratado.
- Uma vez que o fio-guia estava firmemente no lugar, o SG foi avançado sobre o fio-guia, garantindo uma implantação suave e controlada no local alvo usando orientação fluoroscópica.
- Neste caso de cirurgia híbrida para TAAD, o implante da endoprótese (SG) foi complicado por uma troca curta de enxerto aórtico (AVG) e pela presença de uma valva aórtica mecânica, o que impediu a passagem do fio-guia pela valva. Para superar esse desafio, foi utilizado um AVG ramificado ou pré-tratado, que permitiu que o fio-guia fosse posicionado acima da valva aórtica, evitando a interação direta com os componentes mecânicos da valva.
- O AVG foi cuidadosamente avançado para que o fio-guia se projetasse do enxerto, ancorado fora da luz da valva aórtica. Isso forneceu um caminho estável e seguro para o avanço do fio-guia através da aorta, evitando qualquer dano potencial à válvula ou interrupção de sua função. A posição do fio-guia foi cuidadosamente monitorada por fluoroscopia para garantir sua colocação adequada acima da válvula.
- Além disso, como a AVG de substituição é curta e a valva aórtica não foi substituída, o fio-guia foi estendido para o ventrículo. A ponta foi pré-tratada para garantir que fosse curvada, reduzindo o risco de danos cardíacos. No entanto, quando a AVG de substituição tem comprimento ideal, a valva aórtica não afeta o fio-guia, sendo colocada diretamente no vaso.
6. DSA pós-operatório
- Após o procedimento cirúrgico, a DSA foi realizada para avaliar o resultado do reparo híbrido no paciente. A DSA forneceu imagens de alta resolução, permitindo a visualização detalhada de toda a aorta, incluindo os três principais ramos do arco aórtico (tronco braquiocefálico, artéria carótida comum esquerda e artéria subclávia esquerda). Isso foi crucial para garantir que o arco aórtico estivesse bem patente, sem evidências de estenose ou qualquer comprometimento do fluxo de sangue para a cabeça, pescoço e membros superiores.
- Além disso, o DSA permite a avaliação dos SGs recém-implantados, confirmando que eles foram posicionados corretamente sem dobras ou deslocamentos. O procedimento também foi fundamental na detecção de possíveis complicações, como vazamento interno, migração de stent ou vazamentos, que poderiam comprometer o reparo e necessitar de intervenção adicional. O fluxo sanguíneo suave e desobstruído através do arco aórtico e nos ramos foi usado como um indicador de um resultado bem-sucedido, garantindo que o procedimento híbrido tenha efetivamente restaurado a hemodinâmica normal.
- Após a DSA confirmar a ausência de qualquer vazamento e a colocação bem-sucedida da endoprótese, o tórax foi então fechado em camadas. Isso envolve o fechamento cuidadoso do pericárdio, seguido da reaproximação dos músculos da parede torácica, fáscia e pele, garantindo a hemostasia adequada e minimizando o risco de complicações pós-operatórias, como infecção ou deiscência da ferida.
Resultados
Os resultados representativos deste caso demonstram o sucesso técnico e a viabilidade da abordagem híbrida do TAAD. A operação foi concluída em um período de tempo razoável de 6 h com uma perda sanguínea controlada de 500 mL, refletindo a natureza minimamente invasiva da abordagem híbrida em comparação com a cirurgia aberta tradicional. A rápida recuperação do paciente, acordando apenas 3 h após o operatório sem nenhuma anormalidade sensorial ou motora, é um importante indicador da eficácia do procedimento na manutenção da integridade neural e vascular. A ausência de complicações como déficits neurológicos e o fato de o paciente não necessitar de hipotermia profunda durante o procedimento evidencia a redução do estresse fisiológico imposto pela técnica híbrida.
Além disso, a angiotomografia pós-operatória (Figura 5), que não mostrou vazamento significativo de contraste, nenhum deslocamento do stent e fluxo sanguíneo suave nos três ramos do arco aórtico, apoia o sucesso técnico da colocação do stent e confirma a perviedade e estabilidade do reparo. Esses resultados de imagem são críticos para demonstrar a eficácia do procedimento híbrido no reparo do TAAD e na restauração do fluxo sanguíneo normal para a cabeça, pescoço e membros superiores. O paciente recebeu alta no 11º dia de pós-operatório sem complicações maiores, reforçando ainda mais o resultado favorável e a rápida recuperação associada a essa abordagem.
Para analisar o desfecho, é importante avaliar tanto os resultados pós-operatórios imediatos, como visto nos dados de imagem e recuperação, quanto o acompanhamento a longo prazo para avaliar a durabilidade da endoprótese e a possibilidade de complicações tardias, como vazamentos ou reestenose. Além disso, comparar essa abordagem híbrida com as técnicas cirúrgicas tradicionais em termos de tempo operatório, perda de sangue e taxas de complicações pode fornecer informações valiosas sobre os benefícios da cirurgia híbrida no TAAD.
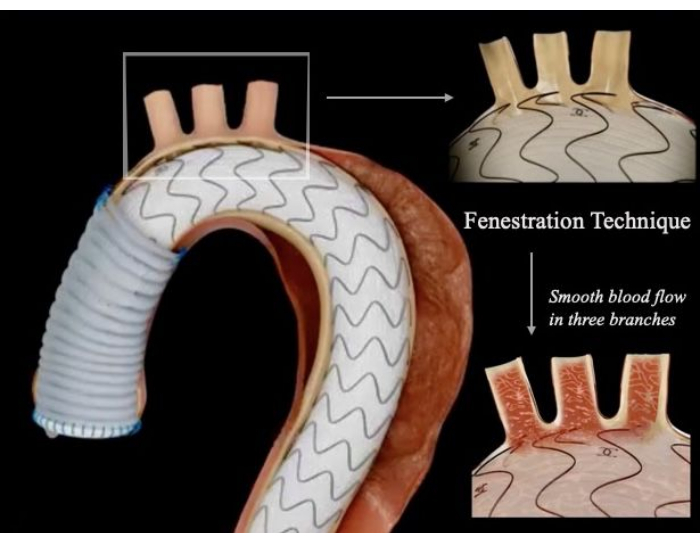
Figura 1: Diagrama esquemático da técnica híbrida de substituição da aorta ascendente combinada com endoprótese fenestrada. O local fenestrado foi precisamente alinhado com os ramos do arco, permitindo fluxo sanguíneo suave para a cabeça, pescoço e extremidades superiores e remoção completa da lesão aórtica sem endoleak. Clique aqui para ver uma versão maior desta figura.
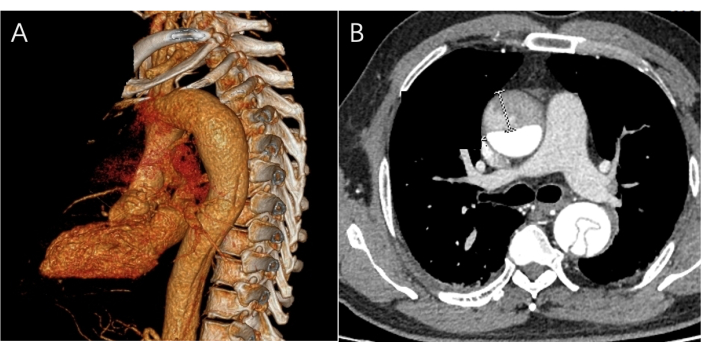
Figura 2: Imagens da angio-TC pré-operatória. (A) Uma imagem tridimensional de TCA do local da lesão é visível, mas não há rupturas na aorta. (B) A imagem do plano transversal da angio-TC mostra as partes ascendente e descendente da aorta apresentando um duplo lúmen com um retalho intimal. Clique aqui para ver uma versão maior desta figura.
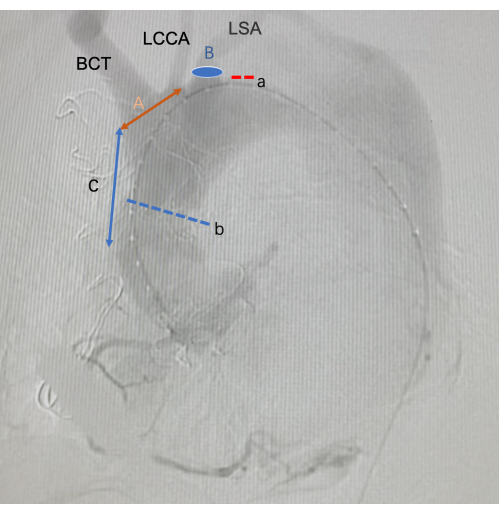
Figura 3: Imagens da DSA intraoperatória. a é a ruptura da dissecção da aorta. b é a anastomose distal de um enxerto vascular artificial. A é o comprimento da fenestração in vitro . B é a posição da fenestração do traje. C é o comprimento da posição inicial da fenestração do GV a partir da extremidade anterior do GV. Abreviaturas: BCT = tronco braquiocefálico; ACCE = artéria carótida comum esquerda; LSA = Artéria subclávia esquerda Clique aqui para ver uma versão maior desta figura.
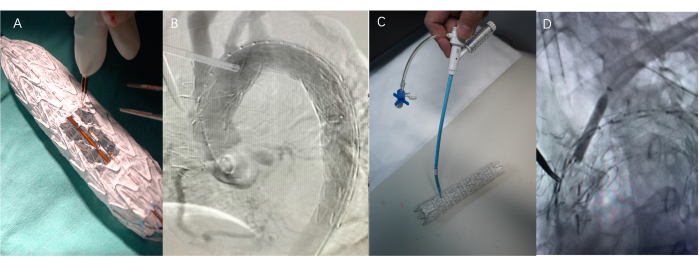
Figura 4: Procedimento cirúrgico. (A) Automodificação de endopróteses com caneta cautérica ou bisturi - Cirurgia fenestrada. O comprimento da janela é o comprimento total das saliências dos galhos e a largura é o diâmetro dos galhos. (B) O processo de implantação de uma endoprótese (SG). (C) Agulhas de dobra e perfuração ajustáveis usadas na tecnologia de fenestração in-situ. Este dispositivo pode ajustar de forma flexível o ângulo e a posição da extremidade frontal. (D) Use um balão para dilatar o local da punção para facilitar a implantação do Viabahn após a agulha ter passado pelo stent coberto. Clique aqui para ver uma versão maior desta figura.
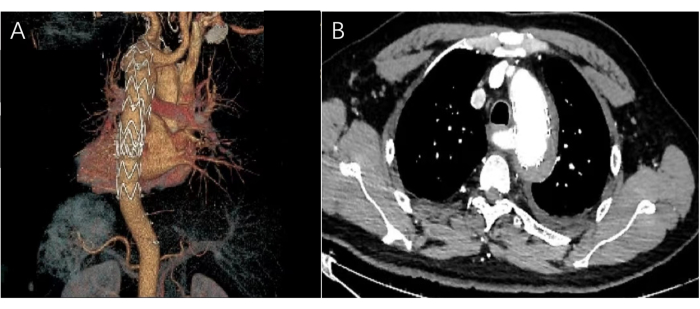
Figura 5: Imagens da angio-TC pós-operatória. (A) A imagem tridimensional da angio-TC pós-operatória mostra que o stent aórtico está no arco aórtico e a ruptura da artéria subclávia esquerda está completamente fechada. (B) A imagem horizontal da angio-TC mostra a sombra do stent sem hematoma ou vazamento de contraste. Clique aqui para ver uma versão maior desta figura.
Discussão
Atualmente, esse procedimento é indicado para pacientes selecionados com arcos aórticos de qualidade, como aqueles com 1) rupturas na aorta descendente e/ou ascendente, onde o arco aórtico está suficientemente íntegro para permitir o uso de pinça bloqueadora, sem rupturas no lado da curvatura maior e sem aprisionamento dos ramos supra-arteriais; 2) mesmo que haja rupturas no arco, elas ficam confinadas ao lado de menor curvatura e o procedimento TEVAR isolará as rupturas, minimizando o risco de vazamento interno. As principais etapas do procedimento de fenestração são as seguintes: substituição da aorta ascendente, exame de DSA intraoperatório, fenestração dos SGs, implante de SGs modificados que cobrem e estendem a anastomose em 10-15 mm, localização e encaixe no ramo do arco e uso de um fio-guia super-rígido.
Esse procedimento requer menos anastomoses, reduz o número de passos cirúrgicos, é de fácil execução e evita parada circulatória hipotérmica profunda14. No TEVAR, o tórax não é suturado e apenas uma membrana adesiva é usada, principalmente para evitar a re-heparinização e a readministração de protamina, o que aumenta o risco de sangramento torácico e falha na detecção de sangramento a tempo. Além disso, a membrana adesiva fornece um ponto de apoio se o stent tiver dificuldade em cruzar a anastomose distal. Em caso de mau posicionamento, o problema pode ser resolvido prontamente, por exemplo, criando um bypass ou realizando uma punção com agulha na membrana. Além das complicações cirúrgicas usuais, as complicações neurológicas devem ser monitoradas de perto no pós-operatório15,16. O tratamento do arco pode afetar o suprimento de sangue para a cabeça, pescoço e extremidades superiores. Devido a esse risco, um DSA é realizado pelo menos no pós-operatório na sala de cirurgia para avaliar o suprimento de sangue para os ramos do arco. A função motora e sensorial do membro afetado deve ser avaliada o mais rápido possível quando o paciente estiver acordado. A estabilidade dos SGs pode ser comprometida após cirurgia aberta no stent sobrejacente, e há risco de migração do SG. Este procedimento híbrido requer um alto nível de habilidade do cirurgião cardíaco, que não deve apenas ser proficiente em técnicas cirúrgicas abertas, mas também ter habilidades endovasculares avançadas.
Ao garantir que a zona de ancoragem seja suficientemente longa, o uso de um stent de sobreposição pode minimizar o número de etapas do procedimento17. O desenho do stent de sobreposição pode ser adaptado às características da lesão do paciente18. Por exemplo, se os três ramos do arco supra-aórtico estiverem muito espaçados, janelas duplas ou triplas podem ser selecionadas para manter a estabilidade do stent. Quando os ramos supra-aórticos do arco estão envolvidos, como no caso de uma artéria infraclavicular clicada, a fenestração in vitro combinada com a fenestração in situ pode ser usada para implantar um stent de ramo no vaso, reduzindo assim o risco de endoleak. Essa abordagem pode ajudar a garantir a estabilidade do stent, como demonstrado neste caso.
A cirurgia híbrida é viável, mas futuros estudos prospectivos são necessários para validar essa abordagem. A técnica descrita, em combinação com medidas adequadas de angiotomografia computadorizada e localização precisa da ruptura, pode oferecer uma alternativa valiosa tanto à cirurgia aberta tradicional quanto aos procedimentos híbridos clássicos. Mais estudos são necessários para comparar os resultados de curto e longo prazo desse procedimento híbrido com os da cirurgia aberta e da cirurgia híbrida clássica.
Divulgações
Os autores não têm nada a divulgar.
Agradecimentos
Os autores não têm agradecimentos.
Materiais
| Name | Company | Catalog Number | Comments |
| Adjustable bend | Lifetech | 106938370117414.00 | The Lifetech Adjustable Bend is constructed from high-quality, biocompatible materials, ensuring both flexibility and durability. The outer layer is typically composed of a polyurethane or similar material that is resistant to kinking, while the inner components include a nickel-titanium alloy (nitinol), known for its superelastic properties, which allow the catheter to return to its original shape after bending to improve the navigability and adaptability of endovascular procedures in challenging vascular anatomies. |
| Artificial vascular graft | Terumo | 734006 | The artificial vascular graft used in this study is made from expanded polytetrafluoroethylene (ePTFE), a biocompatible synthetic material used in vascular surgeries. |
| Balloon catheter | Boston Scientific | H74939171060410 | The Boston Scientific B-Balloon Catheter is a highly advanced, precision-engineered device designed for use in percutaneous transluminal angioplasty (PTA) procedures, particularly in vascular interventions. Its key feature is the balloon catheter technology, which allows for the effective dilation of stenotic lesions in both peripheral and coronary arteries. |
| Guidewire | Cook Medical | G14544 | The Cook Guidewire is a high-performance medical device used to navigate and guide catheters, balloons, and other devices in interventional procedures. It is made from durable materials such as stainless steel and nickel-titanium alloy and is available in a range of sizes and designs tailored to specific clinical needs. The guidewire features a flexible, torqueable, and pushable structure that allows precise navigation through challenging anatomical pathways. |
| Mechanical valve | Medtronic | A7700 | The mechanical heart valve is a widely used prosthetic device designed for the replacement of damaged or diseased heart valves and is particularly suitable for younger patients who require a long-lasting solution for valve replacement, with a proven clinical track record of over 20 years of durability. |
| Pigtail catheter | Cook Medical | G11916 | The Cook Pigtail Catheter is constructed from radiopaque materials, allowing for clear visualization under fluoroscopy,and a versatile, reliable device that enhances the effectiveness of various diagnostic and therapeutic interventions. Its flexible, radiopaque design and pigtail shape provide stability and ease of navigation, making it a valuable tool for clinicians performing cardiac and vascular procedures. |
| Stent-graft | Lifetech | (01)06938370139126 | The Lifetech Stent-Graft is a highly effective and reliable solution for the endovascular treatment of a variety of vascular conditions, particularly aortic dissection.It has a discontinuous, non-radiopaque metal strip on the back.Its hybrid design, incorporating a self-expanding nitinol stent with a durable, biocompatible graft, provides both structural support and sealing, offering significant advantages over traditional open surgery in terms of patient recovery and procedural risk. |
| Stent-graft | Medtronic | VAMF3232C200TE | The Medtronic Stent-Graft represents a significant advancement in the field of endovascular surgery, offering a safe and effective alternative to open surgical repair for patients with complex vascular pathologies such as aortic dissection. The combination of a self-expanding nitinol stent with a durable, biocompatible graft provides optimal sealing and long-term durability. |
| Viabahn | Gore | VBHR080202W | The Gore Viabahn Stent-Graft is composed of a stainless steel or nitinol stent covered by a ePTFE (expanded polytetrafluoroethylene) graft.The Viabahn combines the mechanical support of a self-expanding stent with the sealing capabilities of a biocompatible graft, providing a durable, minimally invasive solution to treat complex vascular lesions. |
Referências
- Zhu, Y., et al. Type A aortic dissection-experience over 5 decades: JACC historical breakthroughs in perspective. J Am Coll Cardiol. 76 (14), 1703-1713 (2020).
- Kallenbach, K., et al. Treatment of the aortic root in acute aortic dissection type A: insights from the German registry for acute aortic dissection type A. Eur J Cardiothorac Surg. , ezac261 (2022).
- Hagan, P. G., et al. The international registry of acute aortic dissection (IRAD): new insights into an old disease. JAMA. 283 (7), 897-903 (2000).
- Mousavizadeh, M., et al. Hypothermic circulatory arrest time affects neurological outcomes of frozen elephant trunk for acute type A aortic dissection: A systematic review and meta-analysis. J Card Surg. 36 (9), 3337-3351 (2021).
- Pupovac, S. S., et al. Moderate versus deep hypothermia in type A acute aortic dissection repair: Insights from the international registry of acute aortic dissection. Ann Thorac Surg. 112 (6), 1893-1899 (2021).
- National Society of Vascular Surgery, China. Chinese expert consensus on hybrid technique on treating thoracic aortic pathologies involving the aortic arch. Chinese Circ J. 35 (2), 124-130 (2020).
- National Committee of Experts on Cardiovascular Diseases. The Chinese expert consensus on hybridization techniques for treatment of aortic diseases involving the arch. Chinese J Circ. 35 (2), 124-130 (2020).
- Zhang, L., et al. Hybrid and frozen elephant trunk for total arch replacement in DeBakey type I dissection. J Thorac Cardiovasc Surg. 158 (5), 1285-1292 (2019).
- Liu, X., et al. Hybrid total arch replacement via ministernotomy for Stanford type A aortic dissection. Front Cardiovasc Med. 10, 1231905 (2023).
- Liu, Y., et al. Early outcomes of hybrid type II arch repair versus total arch replacement with frozen elephant trunk in acute DeBakey type I aortic dissection: a propensity score-matched analysis. Interact Cardiovasc Thorac Surg. 31 (4), 565-572 (2020).
- Liu, S., et al. Midterm outcomes of one-stage hybrid aortic arch repair for stanford type A aortic dissection: A single center's experience. Semin Thorac Cardiovasc Surg. 35 (2), 311-321 (2023).
- World Medical Association. World Medical Association Declaration of Helsinki: ethical principles for medical research involving human subjects. JAMA. 310 (20), 2191-2194 (2013).
- Dai, L., et al. Safety and effectiveness of the sutureless integrated stented graft prosthesis in an animal model. Heliyon. 10 (9), e30323 (2024).
- Sirota, D. A., et al. Hybrid technologies for reconstruction of proximal aortic dissection. Sovrem Tekhnologii Med. 15 (3), 42-51 (2023).
- Jensen, C. W., Chen, E. P. Management of brain malperfusion in acute type A aortic dissection. Asian Cardiovasc Thorac Ann. 30 (3), 364-370 (2022).
- Gaul, C., Dietrich, W., Erbguth, F. J. Neurological symptoms in aortic dissection: a challenge for neurologists. Cerebrovasc Dis. 26 (1), 1-8 (2008).
- Kuzniar, M. K., Wanhainen, A., Tegler, G., Mani, K. Endovascular treatment of chronic aortic dissection with fenestrated and branched stent grafts. J Vasc Surg. 73 (5), 1573-1582 (2021).
- Tenorio, E. R., et al. Fenestrated and branched aortic research Consortium investigators. Outcomes of endovascular repair of chronic postdissection compared with degenerative thoracoabdominal aortic aneurysms using fenestrated-branched stent grafts. J Vasc Surg. 72 (3), 822-836.e9 (2020).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados