Method Article
Обнаружение инвазивный легочный аспергиллез в гематологических больных злокачественных новообразований с помощью бокового потока технологии
В этой статье
Резюме
Быстрый и точный момент оказания медицинской помощи тест на инвазивный легочный аспергиллез представлен. Он использует боковой поток технологий с использованием специфических моноклональных антител, которые связываются с Aspergillus Антигена выделяется при легочных инфекций. Анализ совместим с сывороткой и brochoalveolar промывание и представляет собой новый тест дополнения для диагностики заболеваний.
Аннотация
Invasive pulmonary aspergillosis (IPA) is a leading cause of morbidity and mortality in haematological malignancy patients and hematopoietic stem cell transplant recipients1. Detection of IPA represents a formidable diagnostic challenge and, in the absence of a 'gold standard', relies on a combination of clinical data and microbiology and histopathology where feasible. Diagnosis of IPA must conform to the European Organization for Research and Treatment of Cancer and the National Institute of Allergy and Infectious Diseases Mycology Study Group (EORTC/MSG) consensus defining "proven", "probable", and "possible" invasive fungal diseases2. Currently, no nucleic acid-based tests have been externally validated for IPA detection and so polymerase chain reaction (PCR) is not included in current EORTC/MSG diagnostic criteria.
Identification of Aspergillus in histological sections is problematic because of similarities in hyphal morphologies with other invasive fungal pathogens3, and proven identification requires isolation of the etiologic agent in pure culture. Culture-based approaches rely on the availability of biopsy samples, but these are not always accessible in sick patients, and do not always yield viable propagules for culture when obtained.
An important feature in the pathogenesis of Aspergillus is angio-invasion, a trait that provides opportunities to track the fungus immunologically using tests that detect characteristic antigenic signatures molecules in serum and bronchoalveolar lavage (BAL) fluids. This has led to the development of the Platelia enzyme immunoassay (GM-EIA) that detects Aspergillus galactomannan and a 'pan-fungal' assay (Fungitell test) that detects the conserved fungal cell wall component (1 →3)-β-D-glucan, but not in the mucorales that lack this component in their cell walls1,4. Issues surrounding the accuracy of these tests1,4-6 has led to the recent development of next-generation monoclonal antibody (MAb)-based assays that detect surrogate markers of infection1,5.
Thornton5 recently described the generation of an Aspergillus-specific MAb (JF5) using hybridoma technology and its use to develop an immuno-chromatographic lateral-flow device (LFD) for the point-of-care (POC) diagnosis of IPA. A major advantage of the LFD is its ability to detect activity since MAb JF5 binds to an extracellular glycoprotein antigen that is secreted during active growth of the fungus only5. This is an important consideration when using fluids such as lung BAL for diagnosing IPA since Aspergillus spores are a common component of inhaled air. The utility of the device in diagnosing IPA has been demonstrated using an animal model of infection, where the LFD displayed improved sensitivity and specificity compared to the Platelia GM and Fungitell (1 → 3)-β-D-glucan assays7.
Here, we present a simple LFD procedure to detect Aspergillus antigen in human serum and BAL fluids. Its speed and accuracy provides a novel adjunct point-of-care test for diagnosis of IPA in haematological malignancy patients.
протокол
1. Сбора, хранения и подготовки сыворотки и жидкости бронхоальвеолярного лаважа
- Сбор сыворотки из необработанных образцов крови, позволяя крови сворачиваться при температуре 4 ° С, и хранить сыворотку в качестве аликвоты при -20 ° C до использования. Бронхоальвеолярного лаважа жидкости (БАЛ), также должны быть сохранены как аликвоты при -20 ° C. Примечание: Хранение сыворотке и БАЛ как аликвоты ограничивает возможности деградации целевого антигена повторного замораживания-оттаивания образцов во время повторного тестирования.
- Оттепель образцов и смешивать в сыворотке и БАЛ образцы тщательно встряхивая и центрифуги в течение 1 мин при 14000 оборотах в минуту.
- Для обычного человека тестирование образцов сыворотки, разбавленной сыворотки 1:1 (объем / объем) с тканевой культурой среды (TCM). TCM состоит из RPMI-1640, 10% (объем / объем) эмбриональной телячьей сыворотки, 1% (объем / объем) 200 мм L-глютамин решение, и азид натрия (0,02% вес / объем) в качестве консерванта. Среда готовится заранее и может храниться при температуре 4 ° С в течение нескольких месяцев. Применяют по 100 мкл dilutред сыворотки LFD.
- Для человека BAL жидкости, так и для BAL жидкости из животных, применяют по 100 мкл образца аккуратным LFD, без предварительной обработки.
- Для сыворотки животных, разведите сыворотку 1:2 (объем / объем) с фосфатным буферным раствором, содержащий 4% (вес / объем) ЭДТА, тепла для 3 минуты в кипящей водяной бане, центрифуги в течение 5 мин при 14000 оборотах в минуту, и применять 100 мкл надосадочной аккуратно, чтобы LFD устройства.
2. Применение сыворотки и BAL на боковой поток устройств
- Хранить боковой поток устройств при комнатной температуре (23 ° C). При этой температуре, устройства стабильны в течение 12 месяцев. Удаление устройства из сумки и место на ровной поверхности.
- Используя стерильный наконечник пипетки, применяются 100 мкл предварительно обработанной сыворотке или БАЛ аккуратный образца выпуска порту устройства.
- Дайте анализ запустить в течение 15 мин при комнатной температуре, после чего результаты испытаний должны регистрироваться. Примечание: В течение нескольких секунд жидкость будет таковойан мигрировать под действием капиллярных сил вдоль нитроцеллюлозные мембраны в смотровое окно.
3. Учет и интерпретация результатов LFD
- LFD состоит из внутренней линии контроля (обозначается буквой С на пластиковый корпус) и тестовой линии (обозначается буквой Т). Контрольная полоска должна всегда появляются независимо от антигена Aspergillus в сыворотке или БАЛ образца. Это показывает, что анализ был работать правильно.
- Если антиген Aspergillus присутствуют в сыворотке или БАЛ образца, испытание линии также появятся в 15 минут в пример приложения. Поскольку интенсивность тест линии пропорциональна количеству антигена Aspergillus в образце, тестовая линия может появиться как слабый положительный (+), умеренная положительная (+ +) или как сильный положительный (+ + +) . Тем не менее, любой положительный тест линии, независимо от интенсивности, что указывает на наличие антигена Aspergillus в образце. В йэлектронной отсутствие антигена Aspergillus, ни один тест не появится строка, а результат записывается в виде отрицательной (-).
4. Представитель Результаты
Типичные примеры отрицательные, слабая положительная, умеренная положительная, и сильные положительные результаты с LFD БАЛ и сыворотке крови показано на рисунке 1.
Результаты антиген-положительных LFD тестов (слабое и сильное) или отрицательным LFD тестов с использованием BAL жидкости от острой миелоидной лейкемией (ОМЛ) пациентов, диагностированных по EORTC / MSG диагностические критерии приведены в таблице 1. В эту таблицу соответствующие клинические и микологические (галактоманнана и культуры) данные, и результаты Aspergillus-ПЦР тест, разработанный в Санкт-Bartholomews больницу 8, для каждого пациента. Диагностика заболевания основывается на множество факторов (нейтропения, длительное применение кортикостероидов, лечение с другими признанными Т-клеток immunosuppressants), клинические критерии и GM положительности для BAL (здесь определяется как значение индекса GM> 0,8). В 2002 году EORTC / MSG принципов 10 пациентов 12, 13 и 16 с диагнозом "возможно" И.А. на основе факторов хозяина и клинические критерии или GM положительности. В соответствии с пересмотренным (2008) EORTC / MSG принципы 2, факторы хозяина и GM положительности в одиночку или хозяин факторов и клинических критериев сам по себе не будет означать "возможно" инвазивной грибковой инфекции без сопровождения доказательств из клинических данных и микологии соответственно. Пациент 6 был поставлен диагноз «вероятные» И.А. в 2002 и 2008, потому что принципы принимающей факторов, больших и малых клинических признаков и GM положительности. Отметим, что в то время как ни LFD ни ПЦР в настоящее время включены в EORTC / MSG принципы, есть сильное соглашение между двумя анализов и коммерческих тест галактоманнана указывающие на наличие антигена Aspergillus и нуклеиновых кислот в BAL образец пациентов с 6 до 12 лет. Дополнительные результаты исследования демонстрируют эффективность LFD и ПЦР в диагностике МПА могут быть найдены в Джонсон и др. 8.
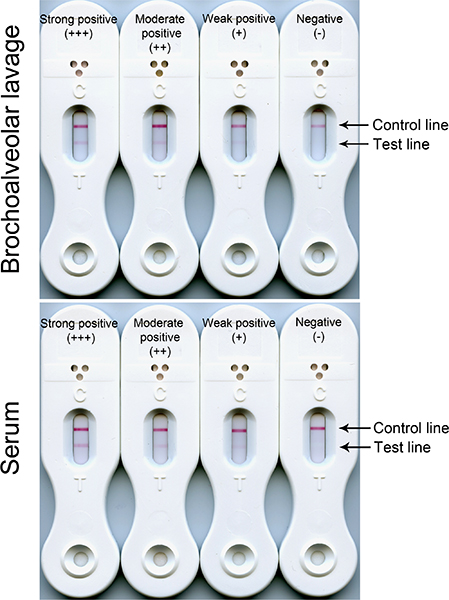
Рисунок 1. Отрицательный (контроль линий) и положительного (контроль и тест линии) результатов LFD тесты с использованием сыворотки крови и БАЛ. Интенсивность реакции тестовой линии пропорциональна концентрации антигена-мишени в сыворотке и БАЛ образцов. Реакция обычно колеблется от слабой (+) по умеренной (+ +) сильным (+ + +). Независимо от того, тест интенсивности линии, все три сыворотки положительных реакций будет означать инвазивных заболеваний легких аспергиллез в связи с наличием циркулирующих Aspergillus антигена в крови. Положительная реакция БАЛ (слабая, умеренная или сильная) будет означать прорастание спор и развитие потенциально патогенных гифы в легких.
| Пациент нет. | ПатиЛОР-информация | Клинические критерии 1 | BAL культуры 2 | GM ОВОС индекса 3 | EORTC / MSG (2002) 4 | EORTC / MSG (2008) 5 | Aspergillus ПЦР результат | LFD результат |
| 6 | - | Основные признаки CT (узелок и гало) и один несовершеннолетний | Отрицательный | 0,9 (положительный) | Вероятный | Вероятный | Положительный | Слабый положительный (+) |
| 12 | Предполагаемые предыдущие грибковые инфекции | Никаких серьезных, один несовершеннолетний | Candida glabrata | 6,43 (сильный положительный) | Возможное | Никто | Положительный | Сильная положительная (+ + +) |
| 13 | Коагулазонегативные Staphylococcus и Е. палочки в крови | Никаких серьезных, два небольших | Отрицательный | 0.25 (отрицательный) | Возможное | Никто | Отрицательный | Отрицательный (-) |
| 16 | Инфекция грудной клетки | 3 мелких критериев, включая новый проникнуть плюс множественного выпот | Отрицательный | 0.16 (отрицательный) | Возможное | Никто | Отрицательный | Отрицательный (-) |
1 Узлы или ореолов на компьютерной томографии это свидетельствует о грибковой инфекции
2 Candida glabrata в БАЛ будет рассматриваться в качестве загрязнителя, так как это второй наиболее распространенной дрожжи изолированы как часть нормальной человеческой флоры 9
3 индекс> 0,8 в тесте GM ОВОС БАЛ свидетельствует о Aspergillus инфекции
4 На основании 2002 EORTC / MSG диагностических критериев "possiblе ',' вероятно 'или' проверенные 'инвазивных грибковых заболеваний 10
5 На основе пересмотренных (2008) EORTC / MSG диагностические критерии для «возможного», «вероятные» и «проверенных» инвазивных грибковых заболеваний 2
Таблица 1. Результаты испытаний LFD БАЛ образцы острой миелоидной лейкемией пациентов с вероятным МПА и от контроля больных ОМЛ (без признаков инфекции) и EORTC / MSG диагностики инфекции.
Обсуждение
Окончательное определение МПА может действительно быть достигнуто путем выделения этиологического агента из образцов биопсии, но восстановление подходящих образцов часто не представляется возможным в очень больных и Aspergillus редко извлекаемые из крови. В то время как основные успехи были достигнуты при использовании компьютерной томографии сканирование грудной клетки в МПА диагностики, характеристики, указывающие на легочную МПА, таких как "гало" или "воздух-полумесяц" знаки либо временной или может быть связано с дыханием артефактов или другими грибковыми инфекциями 11,12. Такие данные, таким образом, дополнить серологические методы, которые направлены на выявление подпись молекул (GM и β-глюкан), из грибов, которые циркулируют в сыворотке крови пациента или которые находятся в BAL жидкости, мокроты или мочи 13. Хотя эти тесты обладать достаточной чувствительностью, они не имеют достаточной точностью, или страдать от помех при определенных условиях 1,6 .
LFD тест для обнаружения МПА представленные здесь дает диагноз "точка-в-помощь" МПА и подвиги технологии, которая использовалась до сих пор в тестах на обнаружение вирусов, бактерий, паразитов и токсинов, 14-19 и, наиболее известный, для домашних тестов на беременность впервые введено Unipath в 1988 году. В Aspergillus LFD описано здесь, Aspergillus конкретных MAb JF5 заблокирован для захвата зоны (тест линии) на пористую мембрану нитроцеллюлозы. Anti-мышиного иммуноглобулина иммобилизованным на мембране в отдельной зоне служил внутреннего контроля (контрольная линия). С добавлением сыворотки или БАЛ к порту релиз, MAb JF5-коллоидного золота сопряжена в освобождении площадки связывается с антигена-мишени и сложная затем проходит вдоль пористую мембрану под действием капиллярных сил. MAb JF5 иммобилизованных в захвате зоны связывается с JF5-коллоидное золото-антиген в результате красная линия испытаний. Любой свободный JF5-коллоидного золотаконъюгат связывается с внутреннего контроля, о том, что анализ был работать правильно. Это приводит к красной линии контроля.
Тест быстро, взяв с собой только 15 минут для выполнения, это дешевле, чем в сыворотке и БАЛ тесты, основанные на GM и β-глюкан обнаружения, и не требует дорогостоящего оборудования и обширные лабораторные бежать. Кроме того, MAb JF5 не перекрестно реагируют с наркотиками или загрязняющих веществ, что было показано, что причиной ложно-положительную реакцию в GM и β-глюкан испытания 1,4,6. Дополнительных главных преимуществ по сравнению с нынешним диагностических тестов LFDs способность обнаруживать активность, что указывает на рост инвазивных видов Aspergillus.
Важным шагом в LFD процедуры является необходимость читать результаты через 15 мин после применения сыворотки или BAL образец устройства. Испытания не должны оставаться дольше, чем за 15 минут до записи результатов, так как это может смещения результате interpretatiо. Слабая реакция не будет усилено за счет расширения инкубационного периода. Термическая обработка сыворотки животных моделях инфекции было установлено, улучшить анализ чувствительности. Ограничение теста является то, что качественные, и зависит от оператора, чтобы субъективные оценки позитивности. Интенсивность тестовой линии варьируется в зависимости от содержания антигена в сыворотке крови и БАЛ образцов (рис. 1). Однако, любая позитивная реакция (определяется путем сравнения с известными негативов) указывает на наличие антигена Aspergillus и поэтому инфекция. Чтобы ограничить субъективность LFD анализы, портативные устройства доступны, которые позволяют количественно LFD интенсивности тестовой линии и включить определение пороговых значений для выявления антигена 20.
Будущее развитие LFD включить ее коммерциализации и развития мультиплекс LFD, который позволяет одновременное обнаружение других инвазивных грибковых патогеновиспользование весьма специфические моноклональные антитела 3.
Раскрытие информации
Нам нечего раскрывать.
Благодарности
Финансирование для доктор Торнтон от Pfizer Лимитед благодарностью.
Материалы
| Name | Company | Catalog Number | Comments |
| Название реагента | Компания | Номер по каталогу | Комментарии |
| Aspergillus LFD | Университет Эксетер | Доступна с соответствующим автором по запросу | |
| RPMI-1640 | Сигма | R0883 | |
| L-Глютамин | Сигма | G7513 | |
| Эмбриональной телячьей сыворотки | Biosera | S9100 | Другие источники эмбриональной телячьей сыворотки могут быть использованы при подготовке TCM |
| ЭДТА | Fisher Scientific | BPE120-1 |
Ссылки
- Thornton, C. R. Detection of invasive aspergillosis. Adv. Appl. Microbiol. 70, 187-216 (2010).
- De Pauw, B., Walsh, T. J., Donnelly, J. P. Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of Cancer/Invasive Fungal Infections Cooperative Group and the National Institute of Allergy and Infectious Diseases Mycology Study Group (EORTC/MSG) concensus group. Clin. Infect. Dis. 46, 1813-1821 (2008).
- Thornton, C. R. Tracking the emerging human pathogen Pseudallescheria boydii by using highly specific monoclonal antibodies. Clin. Vacc. Immunol. 16, 756-764 (2009).
- Pickering, J. W. Evaluation of a (1 -> 3)-β-D-glucan assay for diagnosis of invasive fungal infections. J. Clin. Microbiol. 43, 5957-5962 (2005).
- Thornton, C. R. Development of an immunochromatographic lateral-flow device for rapid serodiagnosis of invasive aspergillosis. Clin. Vacc. Immunol. 15, 1095-1105 (2008).
- Verweij, P. E., Mennink-Kersten, M. A. S. H. Issues with galactomannan testing. Med. Mycol. 44, 179-183 (2006).
- Wiederhold, N. P. Comparison of lateral flow technology and galactomannan and (1 -> 3)-β-D-glucan assays for detection of invasive pulmonary aspergillosis. Clin. Vacc. Immunol. 16, 1844-1846 (2009).
- Johnson, G. L., Bibby, D., Bustin, S. Detection of Aspergillus in broncho-alveolar lavage fluid using two biological assays; evidence of active infection. Mycoses. 54, 130-131 (2011).
- Malani, A. Candida glabrata fungemia: experience in a tertiary care centre. Clin. Infect. Dis. 41, 975-981 (2005).
- Ascioglu, S. Defining opportunistic invasive fungal infection in immunocompromised patients with cancer and hematopoietic stem cell transplants: an international concensus. Clin. Infect. Dis. 34, 71-74 (2002).
- Denning, D. Early diagnosis of invasive aspergillosis. Lancet. 355, 423-424 (2000).
- Greene, R., Shibuya, K., Ando, T., Latge, J. -. P., Steinbach, W. J. . Aspergillus fumigatus and Aspergillosis. , 353-363 (2009).
- Klont, R. R., Mennink-Kersten, M. A. S. H., Verweij, P. E. Utility of Aspergillus antigen detection in specimens other than serum samples. Clin. Infect. Dis. 39, 1467-1474 (2004).
- Iweala, O. I. HIV diagnostic tests: an overview. Contraception. 70, 141-147 (2004).
- Ketema, F., Zeh, C., Edelman, D. C. Assessment of the performance of a rapid, lateral flow assay for the detection of antibodies to HIV. J. Acquir. Immune Defic. Syndr. 27, 63-70 (2001).
- Moody, A. Rapid diagnostic tests for malaria parasites. Clin. Microbiol. Rev. 15, 66-78 (2002).
- Parkash, O. Performance of a lateral flow test for the detection of leprosy patients in India. J. Med. Microbiol. 57, 130-132 (2008).
- Sharma, S. K. Evaluation of lateral-flow Clostridium botulinum neurotoxin detection kits for food analysis. Appl. Environ. Microbiol. 71, 3935-3941 (2005).
- Smits, H. L. Lateral-flow assay for rapid serodiagnosis of human leptospirosis. Clin. Diagn. Lab. Immunol. 8, 166-169 (2001).
- Faulstich, K., Wong, R., Tse, H. . Lateral Flow Immunoassay. , 157-185 (2009).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены