Method Article
Лапароскопическая Pancreatoduodenectomy с модифицированных Blumgart Pancreaticojejunostomy
В этой статье
Резюме
Лапароскопическая pancreatoduodenctomy (LPD) могут предложить преимущества над открытым pancreatoduodenectomy, включая ранние послеоперационные мобилизации, меньше задержка опорожнения желудка и короткие пребывания в больнице. Однако система LPD технически сложной и не хорошо стандартизированных, особенно относительно поджелудочной железы анастомоза. Мы описываем стандартного метода для поджелудочной железы анастомоза во время LPD: изменение Blumgart pancreaticojejunostomy.
Аннотация
Малоинвазивные резекций поджелудочной железы являются технически сложных но быстро растет в популярности. В отличие от лапароскопическая дистальной диализата лапароскопическая pancreatoduodenectomy (LPD) еще не получили широкого признания, вероятно из-за технических проблем, особенно в отношении поджелудочной железы анастомоза.
Исследование описывает и демонстрирует все шаги LPD, включая изменение pancreaticojejunostomy Blumgart. Показания для LPD являются все опухоли поджелудочной железы и пери ампуллы без сосудистых участия. Относительные противопоказания, индекс массы тела > 35 кг/м2, хронический панкреатит, середины cholangiocarcinomas и большого дуоденального рака.
Пациент находится в позицию Франции, 6 trocars размещены и Анатомирование выполняется с использованием (шарнирное) уплотняющие устройства. Изменение pancreaticojejunostomy конец в бок Blumgart проводится с 4 больших иглы (3/0) колючая транс поджелудочной швы и 4-6 воздуховод к слизистой оболочке швы с помощью рассасывающихся мультифиламентные 5/0 в сочетании с 12 см, 6 или 8 Fr внутренней стент с помощью 3D Лапароскопия. Две хирургические водостоки размещены рядом с pancreaticojejunostomy.
Описывается методика LPD, включая изменение Blumgart pancreatico Еюноилеостомия хорошо стандартизирован, и его заслуги в настоящее время изучаются в рандомизированных контролируемых многоцентрового судебного разбирательства. Этот комплекс операция должна выполняться в центрах больших объемов, где хирурги имеют обширный опыт в открытой хирургии поджелудочной железы и передовые лапароскопической хирургии желудочно-кишечного тракта.
Введение
Лапароскопическая хирургия имеет быструю эволюцию в течение последних десятилетий и выполняется для все более сложных хирургических процедур. Несмотря на растущее признание преимущества этого подхода, большинство хирургов поджелудочной железы остаются неопределенными о преимуществах этой техники1,2,3,4,5 . Лапароскопическая дистальной Панкреатэктомия теперь доказано быть безопасными и доступными, хотя его использование в лечении аденокарциномы до сих пор обсуждается2,4,6,7. После представления первого доклада по лапароскопической pancreatoduodenectomy (LPD) в 1994 году8несколько исследований описали технику9,10,,1112. Не рандомизированные исследования сообщили о сокращении задержки опорожнения желудка и оценкам интраоперационной кровопотери сообщалось LPD, по сравнению с открытым pancreatoduodenectomy13,14. Одно рандомизированное испытание и систематический обзор сообщил, что система LPD может уменьшить пребывания в больнице, без увеличения общей цене15,16. К сожалению система LPD, как представляется, связаны с более высокой частотой послеоперационных панкреатической фистулы и реадмиссии, особенно в низком объеме центров17. Лучшая техника поджелудочной железы анастомоза все еще открыт для обсуждения. Наиболее распространенными анастомозов, выполненных во время открытого pancreatoduodenectomy воспроизводятся в LPD. Однако что касается открытой хирургии поджелудочной железы, результаты, полученные с LPD являются спорными. Безопасность, осуществимость, воспроизводимость и простота поджелудочной железы анастомоза имеют решающую роль в распространении этой техники и в результатах хирургического.
Поджелудочной железы анастомоза Blumgart это простой и эффективный метод, который сочетает в себе принцип воздуховодов к слизистой оболочке анастомоза с тощей кишки, охватывающих по сырой поверхности поджелудочной железы18. Анастомоз Blumgart был связан с низкой ставкой панкреатической фистулы в чем другие методы19.
Эта статья призвана продемонстрировать безопасности и целесообразности LPD и специально pancreaticojejunostomy (PJ) с модифицированных Blumgart анастомоза и его хирургические онкологических результат у пациентов с ампуллы опухоли.
протокол
Поскольку эта операция была выполнена в рутинной медицинской помощи требуется одобрение без конкретных этики. Пациентом стал 67-летняя женщина с опухолью ампуллы 1 см, представляя с механической желтухи, бледные табуретки цветные, темного цвета мочи, зуд и 10 кг потеря веса в 1 год. Истории болезни пациента показывает гипертонии и типа сахарного диабета II. Эндоскопическое УЗИ (EUS) показывает большой ножке полипоидных поражения ампула.
1. Отбора пациентов
- Выберите пациентов на основе опухолью поджелудочной железы или Пери ампуллы без каких-либо признаков участия крупных сосудов на последних (Макс 4 недель) контраст расширенной КТ сканирования.
- Изучите CT для любого сосудистые аномалии, такие как аномальным курс право печёночной артерии.
- Во время обучения, исключают пациентов с индексом массы тела > 35 кг/м2, рецидивирующий острый или хронический панкреатит, предыдущих основных абдоминальной хирургии, ориентированные на поджелудочной железы лучевая терапия, середины cholangiocarcinomas и большого дуоденального рака, из-за Ожидается, что технические трудности. Получив богатый опыт работы с LPD, сосудистая резекции возможны также во время LPD20.
2. пациент подготовка
- Выполните предоперационный эндоскопическая ретроградная холангиопанкреатография (ERCP) для облегчения механической желтухи.
- Место 7Fr пластиковых желчных стента и взять биопсию. Патологии показывает tubulovillous аденома общего желчного протока (КБР) с фокуса высококачественных дисплазия. Рисунок 1 иллюстрирует появление поражения на КТ.
3. Хирургическая техника
- Настройка
- Место пациента в французском положении с нагревательным устройством на матрасе короткое зерно с и правую руку в левую руку, похищенных на 90°.
- В стерильные экспозиции помните надлобковой области бесплатно Пфанненштилю удалить образец. Первый хирург стоит между ног пациента, 1-й и 2-й помощник на левой и правой стороны, соответственно. Используйте технику 6-порт для выполнения процедуры, см. Рисунок 2.
- После создания пневмоперитонеума место югу пупочной 12 мм троакар и затем 4 trocars вдоль плоскости полукруглые (два trocars 12 мм слева и справа пупок, два trocars 5 мм, четыре пальца онкогорошину слева и право в передней подмышечной линии).
- Место 6й троакара просто суб xiphoidal (рис. 2) для печени опровержения.
- Выберите выделенные (шарнирное) уплотняющие устройства, наряду с лапароскопической крюк монополярная и лапароскопическая биполярного зажима диатермия.
- Этап разведки
- Выполните диагностическая лапароскопия исключить брюшной полости и печени метастазов. Место прямые иглы аутогенных в регионе эпигастральной области, вокруг связки Терес отозвать связки в брюшной стенки живота.
- Вскрыть рубчика желчного пузыря и кистозная артерия и затем разделить протока между клипами и шовные Hartmann в мешочек к брюшному брюшной стенки для дальнейшего печени ретракции и воздействия гепато двенадцатиперстной связки.
- Рассечение фаза
- Откройте меньшей sac, разделив связки Гастроколический 2 см дистальной из судов gastroepiploic. Бесплатный желудка из поджелудочной железы и пусть помощник втягивать живот кпереди. Мобилизовать печеночная прогиба. После этого левый помощник отзывает двенадцатиперстную кишку пациента в левую сторону, в то время как право помощник толкает толстой кишки caudo медиально с марлей.
- Маневр Кохер
- Выполняют широкий Kocher маневр, подвергая нижней caval Вены, происхождение превосходной верхней брыжеечной артерии (SMA) и связки Treitz. Предоставляют также Улучшенный брыжеечных вен (СМВ) и ее слияния с gastroepiploic Вену. Вскрыть последний и разрез, используя клипы и формулирование герметик.
- Поджелудочной железы туннель
- Теперь создайте начало широкой поджелудочной железы туннеля.
- Далее свободный дистальной части желудка, всего 1 см проксимальнее пилоруса и разрез с помощью endostapler, после того, как трубка через назогастральный зонд вытащил обратно. На краниальной стороне поджелудочной железы вскрыть станции Лимфоузел печёночной артерии (номер 8а) и отправить его для патологии. Далее определите печеночной артерии, воротной вены и артерии гастродуоденальной.
- Окружить гастродуоденальной артерии с петлей судна и разделить его, оставляя 2 блокировки клипы на стороне и 1 на стороне образца пациента. Завершите поджелудочной железы туннеля, тупым рассечение, используя формулирование sealer и слинг поджелудочной железы с четверти длины судна цикла, закрепив его с пластиковой самоблокирующихся клип.
- Связки Treitz резекции
- Мобилизовать duodenojejunal прогиба (связки Treitz) и делят первую петлю тощей кишки с endostapler с помощью сосудистой картриджа. Теперь заполните мобилизации первого цикла до верхней брыжеечной корня. Далее шовные две бесплатные концы тощую друг к другу и пройти оба под корнем брыжеечных пациента по правой стороне.
- Резекция поджелудочной железы
- Для поджелудочной железы головы рассечение Переместите камеру право двусторонняя 12-мм троакар как это дает более четкое представление о SMA и СМВ. Вскрыть крючковатыми процесса с формулирование герметик с наружной стороны СМВ и первый филиал тощей кишки. Работа в слои от вентральный спинной, при отзыве SMV медиально подвергать SMA.
- Разрез поджелудочной железы с помощью монополярной диатермия, управлять кровотечение с биполярной диатермия.
- Разрез проток поджелудочной железы с ножницами, чтобы избежать уплотнения протока. Проанализируем все забрюшинной узлы, при визуализации SMA.
- Резекция желчных протоков
- Следить за общей печёночной артерии правой печеночной артерии и заботиться в случае ошибочной сосудистой анатомии. Далее окружить печеночный проток с петлей судна и разделить его между лапароскопическая бульдог на проксимальной протоков печени и пластиковые фиксирующий зажим (или второй бульдог) на дистальной печеночный проток.
- Далее Поместите образец в мешке пластиковых извлечения и временно оставить его в нижней части живота. Удаление образца позднее одновременно с желчного пузыря. Взять короткий перерыв до начала этапа восстановления.
- Этап восстановления
- Поджелудочной железы анастомоза
- С 3D лапароскопии, начало этапа восстановления, выполняя PJ, согласно модифицированных Blumgart технику, с 4 колючая швов (большой тупой иглой, 3/0, длина 23 см) (рис. 3).
- Передайте швы через поджелудочной железы около 1 см от края разреза, а затем передать их дорзально через кишечник и обратно через поджелудочной железы. После прохождения, привода иглы через свой цикл, затянуть и поместите его далеко от поджелудочной железы.
- Повторите эту процедуру для каждого шва, заботиться, чтобы не препятствовать протока поджелудочной железы (рис.1). Легко иглы и ушивание способствует 3D лапароскопии.
- Воздуховод к слизистой оболочке анастомоза
- Создайте 2 мм enterotomy в тощей кишки, используя диатермия крюк (около 5 мм от проток поджелудочной железы).
- Впоследствии место 4-6 воздуховод к слизистой оболочке швы с помощью небольшой тупой иглой (5/0). В случае четырех швов поместите их в 8, 5, 11 и 2 часов. Выберите положение для того, чтобы преодолеть сложнее ушивание типичный 9 и 3 часа швы в мелких протоков поджелудочной железы.
- Во-первых место 8 и 5 часов швами с узел внутри. Место 12 см, 6 или 8 Fr педиатрического через назогастральный зонд трубку как внутренние поджелудочной железы стента (Рисунок 3.2).
- Далее место 11 и 2 часов швами с узлом вне. Заполните анастомоза собирание вентральной стороне тощей кишки с оригинальной четыре колючая швы, вставляя их сначала кпереди через стенку тощей кишки и затем обратно через вентральной стороне поджелудочной железы, и втягивания к селезенке для предотвращения разрывая поджелудочной железы.
- Безопасность каждого шва с зажимом на поверхности поджелудочной железы до резки (рис. 3.3 и 3.4).
- Желчных анастомоза
- Приблизительно 5-7 см. далее на петлю тощей кишки, создайте enterotomy антимезентериальном 2-4 мм с диатермия крючком.
- Выполните конец в бок Геа (HJ) с Прерванный рассасывающихся резьбовые нитей (5/0), начиная с шов между 6 часов на желчных протоков в 12 часов в enterotomy.
- Продолжать его из хвостового черепной чередующихся между левым и правым краями HJ. Шовный материал, выпустив напряженности могут быть помещены между петлю тощей кишки и желчного пузыря кровати. В случае широкого толстостенный желчных протоков используют работает шовный материал с хирургом, стоя на левой или правой стороны пациента.
- Место хирургические стока от правой онкогорошину пространства через отверстия Уинслоу, заканчивая превосходной границы PJ. Завершить холецистэктомии и желчного пузыря в вторую сумку поиска. Потяните вверх первую петлю тощей кишки в желудок.
- Желудочный анастомоз
- После небольшой enterotomy и малых гастростомия просто брюшной от основной линии выполняют сшитых side-to-side antecolic gastrojejunostomy (ГДЖ). Закройте оставшиеся часы с одного шва с колючей шов 3/0.
- Создайте Пфанненштилю 5 см для извлечения образца pancreatoduodenectomy и желчного пузыря. Закройте этот разрез в слоях и insufflate живот поставить второй сливной через наиболее право двусторонняя троакар 5 мм на нижней границе PJ, с наконечником под GJ.
- Обложка, PJ и пней GDA с большого сальника. Закройте фасции трех trocars 12 мм. Закройте все разрезы, внутрикожные швы (4/0) (Рисунок 4).
- Поджелудочной железы анастомоза
Результаты
Время операции было 6 часов с 150 мл кровопотерь. Пациента послеоперационный курс был неосложненной. Был обнаружен не послеоперационной панкреатической фистулы. Послеоперационные сутки, 3 уровень амилазы в обоих стоки были 1373 U/L и 804 U/L, который нормализовалась на 5 день после стоки были удалены. Пациент был выписан по 6й послеоперационные сутки. Оценке патологии выявлено 1,5 см tubulovillous аденома фатерова сосочка с дисплазия. Микроскопически радикал (R0) и ни один из тринадцати лимфатических узлов, которые собирают были вовлечены на опухолевые клетки поля резекции.
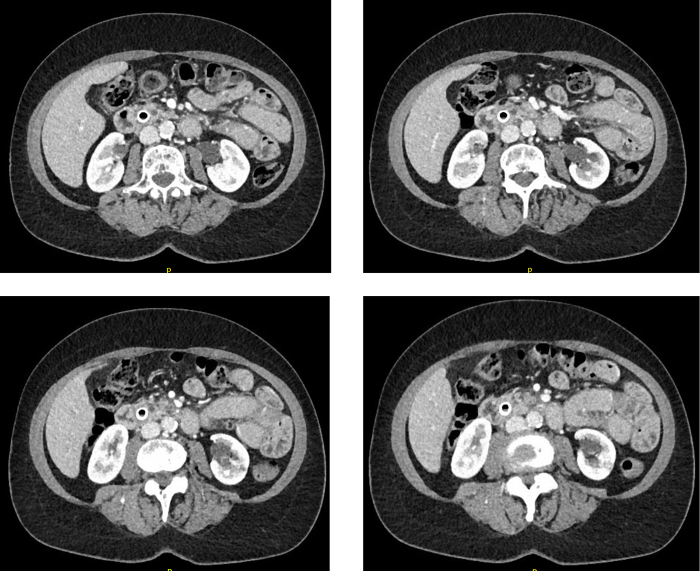
Рисунок 1 Больных КТ сканирования
На снимках ампуллы опухоли, вызывая механической желтухи. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
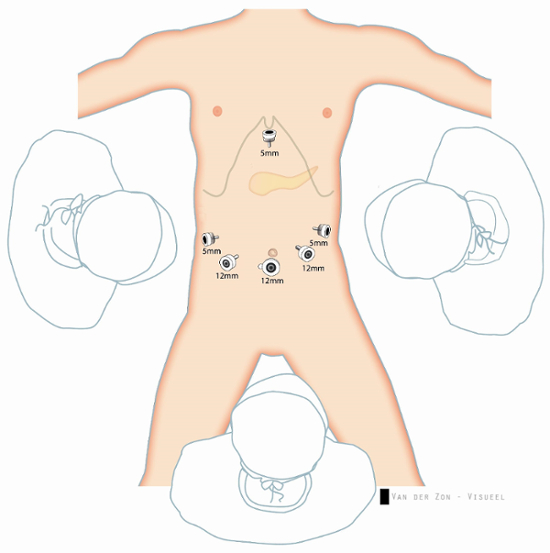
Рисунок 2 Настройка пациента
Оператор находится между ног, 1-й и 2-й помощник слева и справа, соответственно. Процедура выполняется с помощью метода 6-порт. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
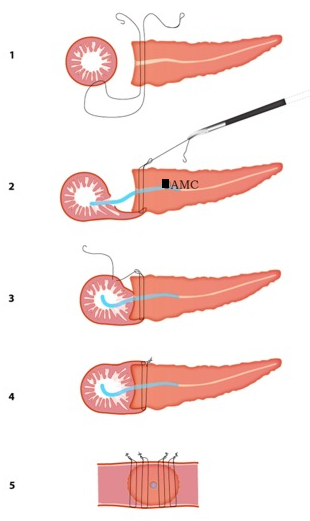
Рисунок 3 Pancreaticojejunostomy согласно модифицированных Blumgart техника
Изменение pancreaticojejunostomy Blumgart производится с четырьмя колючая швами (3/0), крупные иглы, для transpancreatic U-швы (3.1). 12 см внутренние 6 или 8 Fr поджелудочной железы стента помещается и воздуховодов к слизистой оболочке анастомоза производится с использованием 4-6 рассасывающиеся резьбой 5/0 зашивается с небольшой тупой иглой (3.2). Анастомоза завершается, подбирая вентральной стороне тощей кишки с оригинальной четыре колючая швы (3.3, 3.4). Боковой вид конечного результата (3.5).
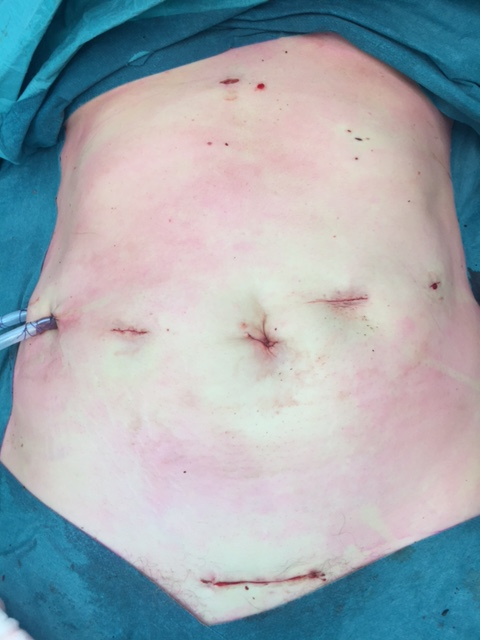
Рисунок 4 После операции результат
Это конечный результат после лапароскопической pancreatoduodenectomy с модифицированных Blumgart pancreaticojejunostomy.
Обсуждение
LPD является технически сложной, но хорошо стандартизированных, безопасной и воспроизводимые процедуры. Система LPD может предложить преимущества малоинвазивной подходов, включая мобилизацию раннего, раннего возвращения функции кишечника и короткие больница пребывания21. Широко признается, что лапароскопию предлагает лучшее качество визуализации, расширяя все детали операционного поля и минимальным манипуляции ткани22. Патологических результатов также сопоставимы между LPD и открытых технику. В частности же R0 резекции и лимфоузлов урожай ставки были сообщила10.
Использование позицию Франции, 6-порт техники, 3D лапароскопии (особенно на этапе анастомоза) и соответствующие лапароскопическая устройства может уменьшить препятствия минимально инвазивный подход. Мы предлагаем также некоторые технические советы, описанных выше, Palanivelu и др. 23 например чрескожная иглы в эпигастральной области отозвать Терес связки или шов Хартманн мешочек к брюшному брюшной стенки, для повышения воздействия hepatoduodeneal связки.
К сожалению есть цена оплачивается; Этот комплекс операция должна быть выполнена на высокой громкости центрах, где хирурги имеют обширный опыт в открытых резекций поджелудочной железы и продвинутых лапароскопических процедур15. Хотя изменение pancreaticojejunostomy Blumgart воспроизводимый метод для выполнения поджелудочной железы анастомоза, тщательно операции не требуется. Хирург должен заботиться, чтобы не препятствовать протока поджелудочной железы с колючей швы. Необходимо также тщательно размещены швы воздуховодов к слизистой оболочке. Каждый шов под прямой визуализации, но не нужно быть затянуты сразу и может храниться первоначально для тяги. Первоначально, режа проток поджелудочной железы, он может храниться несколько больше времени, чтобы облегчить эти швы.
Лапароскопическая pancreaticoduodenectomy требует лапароскопическая навыки и богатый опыт работы с открытой хирургии поджелудочной железы. Дальнейшие исследования должны расследовать онкологические результаты этой методики. Ли минимально инвазивный подход является безопасным и полезным для этих пациентов должен установить в рандомизированных обстановке. В Нидерландах Леопард-2 (судебного реестра NTR5689) многоцентрового суда является в настоящее время случайной больных между минимально инвазивных и открытые pancreatoduodenectomy с использованием описанных техника24.
Раскрытие информации
Авторы не имеют ничего сообщать.
Благодарности
Авторы имеют без подтверждений. Описывается методика используется в обоих учреждений авторов.
Материалы
| Name | Company | Catalog Number | Comments |
| Bair Hugger | 3M COMPANY | 79500 | Patient Warming Unit, Model 795, 120V-ENG-E, Refurbished 79500 |
| ENSEAL | Ethicon Endo-Surgery, Cincinnati, OH, USA | NSLG2C45 | articulating sealing device |
| Weck Hem-o-lok Polymer Ligation System - Automatic | Weck Surgical Instruments, Teleflex Medical, Durham, NC | 543965 | The Weck Hem-o-lok Auto Endo5 delivers 15 true Medium-Large clips on a 5mm platform. The Medium-Large clip is designed for 3-10 mm size vessels. Designed for security, the non-absorbable locking polymer clip is inert, nonconductive, radiolucent, and does not interfere with CT or X-ray diagnostics. |
| ECHELON FLEX Powered Plus Stapler | Ethicon Endo-Surgery, Cincinnati, OH, USA | PLEE60A | The ECHELON FLEX GST System controls tissue movement |
| Echelon black | Ethicon Endo-Surgery, Cincinnati, OH, USA | GST60T | Black reload intended for use in very thick tissue |
| Echelon blue | Ethicon Endo-Surgery, Cincinnati, OH, USA | GST60B | Blue reload intended for use in regular tissue |
| V-Loc | Covidien | VLOCM1824 | The V-Loc wound closure device is a revolutionary technology that supports optimal patient outcomes by closing wounds securely without the need to tie knots. |
| VICRYL Suture | ETHICON | J303H | Suture USP: 5-0 Brand: Coated Vicryl Suture Color: Violet Strands per Pack: 1 Suture Length (Inches): 27 Needle Type: RB-1 |
Ссылки
- de Rooij, T., et al. Impact of a Nationwide Training Program in Minimally Invasive Distal Pancreatectomy (LAELAPS). Ann Surg. , (2016).
- van Hilst, J., et al. Worldwide survey on opinions and use of minimally invasive pancreatic resection. HPB (Oxford). , (2017).
- de Rooij, T., et al. Laparoscopic Distal Pancreatectomy for Pancreatic Ductal Adenocarcinoma: Time for a Randomized Controlled Trial? Results of an All-inclusive National Observational Study. Ann Surg. , (2016).
- de Rooij, T., et al. Pan-European survey on the implementation of minimally invasive pancreatic surgery with emphasis on cancer. HPB (Oxford). 18 (2), 170-176 (2016).
- Hogg, M. E., et al. Training in Minimally Invasive Pancreatic Resections: a paradigm shift away from "See one, Do one, Teach one". HPB (Oxford). 19 (3), 234-245 (2017).
- Magge, D., et al. Comparative effectiveness of minimally invasive and open distal pancreatectomy for ductal adenocarcinoma. JAMA Surg. 148 (6), 525-531 (2013).
- Venkat, R., et al. Laparoscopic distal pancreatectomy is associated with significantly less overall morbidity compared to the open technique: a systematic review and meta-analysis. Ann Surg. 255 (6), 1048-1059 (2012).
- Gagner, M., Pomp, A. Laparoscopic pylorus-preserving pancreatoduodenectomy. Surg Endosc. 8 (5), 408-410 (1994).
- Boggi, U., et al. Laparoscopic pancreaticoduodenectomy: a systematic literature review. Surg Endosc. 29 (1), 9-23 (2015).
- Mendoza, A. S., Han, H. S., Yoon, Y. S., Cho, J. Y., Choi, Y. Laparoscopy-assisted pancreaticoduodenectomy as minimally invasive surgery for periampullary tumors: a comparison of short-term clinical outcomes of laparoscopy-assisted pancreaticoduodenectomy and open pancreaticoduodenectomy. J Hepatobiliary Pancreat Sci. 22 (12), 819-824 (2015).
- Asbun, H. J., Stauffer, J. A. Laparoscopic vs open pancreaticoduodenectomy: overall outcomes and severity of complications using the Accordion Severity Grading System. J Am Coll Surg. 215 (6), 810-819 (2012).
- Palanivelu, C., et al. Laparoscopic pancreaticoduodenectomy: technique and outcomes. J Am Coll Surg. 205 (2), 222-230 (2007).
- de Rooij, T., et al. Outcomes of a Multicenter Training Program in Laparoscopic Pancreatoduodenectomy (LAELAPS-2). Ann Surg. , (2017).
- de Rooij, T., et al. Laparoscopic pancreatic surgery for benign and malignant disease. Nat Rev Gastroenterol Hepatol. 13 (4), 227-238 (2016).
- de Rooij, T., et al. Minimally Invasive Versus Open Pancreatoduodenectomy: Systematic Review and Meta-analysis of Comparative Cohort and Registry Studies. Ann Surg. 264 (2), 257-267 (2016).
- Palanivelu, C., et al. Randomized clinical trial of laparoscopic versus open pancreatoduodenectomy for periampullary tumours. Br J Surg. 104 (11), 1443-1450 (2017).
- Nassour, I., et al. Minimally Invasive Versus Open Pancreaticoduodenectomy: A Propensity-Matched Study From a National Cohort of Patients. Ann Surg. , (2017).
- Grobmyer, S. R., Kooby, D. A., Hochwald, S. N., Blumgart, L. H. Blumgart anastomosis for pancreaticojejunostomy minimizes severe complications after pancreatic head resection. Br J Surg. 97 (1), 134-135 (2010).
- Wang, S. E., Chen, S. C., Shyr, B. U., Shyr, Y. M. Comparison of Modified Blumgart pancreaticojejunostomy and pancreaticogastrostomy after pancreaticoduodenectomy. HPB (Oxford). 18 (3), 229-235 (2016).
- Croome, K. P., et al. Pancreaticoduodenectomy with major vascular resection: a comparison of laparoscopic versus open approaches. J Gastrointest Surg. 19 (1), 189-194 (2015).
- Kendrick, M. L., et al. Minimally invasive pancreatoduodenectomy. HPB (Oxford). 19 (3), 215-224 (2017).
- Song, K. B., et al. Matched Case-Control Analysis Comparing Laparoscopic and Open Pylorus-preserving Pancreaticoduodenectomy in Patients With Periampullary Tumors. Ann Surg. 262 (1), 146-155 (2015).
- Palanivelu, C., et al. Evolution in techniques of laparoscopic pancreaticoduodenectomy: a decade long experience from a tertiary center. J Hepatobiliary Pancreat Surg. 16 (6), 731-740 (2009).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены