Method Article
Человеческого Colonoid монослои для изучения взаимодействия между патогенов, Комменсалами и принимающих кишечного эпителия
В этой статье
Резюме
Здесь мы представляем протокол к культуре человека enteroid или colonoid монослои, которые имеют нетронутыми барьерную функцию для изучения принимающей эпителиальных микробиоты взаимодействия на уровне клеточных и биохимических.
Аннотация
Человека 3-мерные (3D) enteroid или colonoid культуры производный от крипты базовый стволовых клеток являются в настоящее время самые передовые модели ex vivo кишечного эпителия. Благодаря их закрытых структур и значительной поддержки внеклеточного матрикса 3D культуры не являются идеальными для исследования хост патогена. Enteroids или colonoids можно выращивать как эпителиального монослои на проницаемой ткани культуры мембраны позволяет управлять как Люминал и базолатеральной клеток поверхности, так и сопровождающих жидкости. Этот повышения Люминал поверхности доступность облегчает моделирования бактерий хост эпителиальных взаимодействиями, такими как способность унижающего достоинство слизь энтерогеморрагические E. coli (EHEC) на толстой эпителия. Описан метод для 3D культуры фрагментации, однослойная посева и измерения электрического сопротивления (тер) transepithelial для контроля за прогрессом на пути к confluency и дифференциации. Colonoid монослой дифференциации дает выделяется слизь, которая может быть изучен иммунофлюоресценции или immunoblotting методов. В целом enteroid или colonoid монослои позволяют физиологически соответствующие платформы для оценки конкретных клеточных популяций, которые могут быть объектом патогенных или синантропных микробиоты.
Введение
Кишечные organoids, enteroids и colonoids привели к многие достижения в понимании поведения стволовых клеток, кишечные развития, функции барьера/транспорта и клеточной дифференциации. 1 однако 3D культуры ограничивает исследования хост эпителия возбудитель взаимодействия потому что просвета не является напрямую доступной для бактерий или факторы вирулентности, если закрытые структуры подвергаются микроинъекции. 2 , 3 Кроме того, выделяется материалы, такие как малые молекулы, белки, или слизь нельзя легко брались 3D культуры для анализа ниже по течению. Воздействие патогенных агентов на эпителиальные барьер функция4 и ионного транспорта5 был оценен в 3D с использованием флуоресцентных красителей и time-lapse микроскопии культуре, но поддаются монослои, выращенных на проницаемой ткани культуры поддерживает Дополнительные методы, такие как измерение тер и Ussing палаты/напряжение зажим записи. 6 , 7
Многочисленные публикации описал протоколы для 2D или монослоя культуры enteroids/colonoids. Материалы, найденные для содействия эпителиальных клеток вложение включают коллаген гидрогели,8,9 0.1% желатина,10 тонкослойная мышиных саркома производные базальной мембраны матрица (BMM),,11,12 13 и человеческого коллагена IV. 6 , 7 , 14 , 15 , 16 , 17 посев подходы включают механические фрагментации, закупорить6,,1415 или диссоциации факторов адгезии клеток с помощью трипсина,10,11 dispase,13 или ЭДТА. 9 несколько протоколов использовать не пористых культуры ткани пластик для заполнения, но это ограничивает базолатеральной доступ, поэтому большинство приложений зависят от вставки проницаемых культуры ткани. Документация стабильной вырожденная монослоя формирования и поддержания варьируется среди публикаций. Кроме того рост и дифференцировку СМИ композиции для человеческих культур отличаются среди различных групп и продолжать развиваться как больше исследователей принять и скорректировать методологию с учетом их применения и имеющихся ресурсов.
Для устранения ограничений 3D кишечного эпителия культуры в хост возбудитель взаимодействия исследования, мы представляем измененного Протокола для преобразования 3D человеческого enteroids или colonoids в монослоя. После достижения confluency в состоянии склеп как незрелые, вывод факторов роста WNT3A, RSPO1 и ингибиторы A-83-01 и SB 202190 приводит к дифференциации представитель малого кишечных ворсинок или поверхности эпителия кишечника. Мы описываем идеальный матрица, человеческого коллагена типа IV, чтобы покрыть вставками и получить равномерное enteroid или colonoid фрагментов для покрытия. Мы показываем, что этот протокол производит вырожденная монослой с высоким Colonoid Тер монослои выделяют густой слизи апикальной слой, позволяя ex vivo исследований взаимодействия возбудителя слизи через immunoblotting или иммуноокрашивания. Изменение фиксации для сохранения кишечника слизи слой для иммуноокрашивания также описан. Этот метод призван обеспечить шансов справиться с возникающими модель для изучения ранних кишечных хост возбудитель взаимодействия после инфекции.
протокол
Этот протокол основан на ранее опубликованные авторы исследования. 6 , 7 , 14 , 15 , 16 следующие шаги должны осуществляться в кабинете стерильных биобезопасности, с помощью надлежащего асептических методов. Все методы, с участием человека образцы были одобрены институционального обзора Совет из Джона Хопкинса университета Школа медицины (IRB NA_00038329).
1. Покройте вставки культуры клеток с внеклеточного матрикса
- Подготовьте 5 мл раствора (1 мг/мл) запасов коллаген IV в 100 мм уксусной кислоты. Пусть стоять на 4 ° C приблизительно 4 ч до полностью гидрата/растворить.
- Аликвота коллаген IV складе решения и хранить при 4 ° C (≤ 1 месяц) или от-20 ° C (> 1 месяц).
- Непосредственно перед покрытием, разбавляют коллаген IV Стоковый раствор в стерильных культуры ткани класса воды до конечной концентрации 34 мкг/мл. Для 24-ну плиты вставляет культуры клеток, пальто, каждая вставка с 100 мкл раствора, который соответствует 10 мкг/см2.
- Инкубировать пластины в стандартной CO2 культуры ткани инкубатора при 37 ° C ≥ 2 часа, или для удобства, уплотнение края пластины с парафином пленкой и инкубировать на 4 ° C на ночь или до 1 недели.
2. Изолируйте enteroids/colonoids от 3D культуры
Примечание: Enteroids или colonoids от доноров биопсии и ведется в 3D культуры согласно стандартные протоколы, в описанный ранее. 14 , 18 кратко, склепы собирают из кишечное биопсии или резекции через комплексообразования и механических агитации. Склепы промывают, собирают и покрытие в BMM. Расширение средств массовой информации (описано в шаге 4.2) добавляется к культуре и заменены каждые 2 дня. Формирование культуры 3D виден в течение часов после покрытия.
- Аспирационная питательной среды от 24-ну пластины и заменить ледяной уборки раствором 1 мл (см. Таблицу материалы) в колодец.
- Используйте мини-клеток скребок для выбить и распада базальной мембраны матрица гранулы, уделяя особое внимание любого материала по краям хорошо.
- Агитируйте пластину на орбитальный шейкер на примерно 200 об/мин, 4 ° C на 30-45 мин.
3. отделить 3D enteroids/colonoids
- Используйте Р200 Одноканальные Пипетки или многоканальные пипетки с стерильных фильтр советы для нарезанных суспензию клеток.
- Объединить ячейку когда в коническую пробирку 15 мл. Используйте несколько флаконов, если объем всего подвеска > 6 мл.
- Добавить равное количество Advanced DMEM/F12 носитель, содержащий 10 мм HEPES, L-аланил L-глютамин дипептид (1 x) и пенициллин стрептомицином (1 x) (мыть средний). Инвертировать трубку 3 - 4 раза для смешивания. Центрифуга 300 x g, 10 мин, 4 ° C.
- При необходимости, аспирационная мыть среднего и заменить 0,5 мл/хорошо трипсина (см. Таблицу материалы). Ресуспензируйте colonoids с пипеткой P200, крышка трубки и место в ванну воды 37 ° C приблизительно в 2 мин немедленно снять трубку, добавить мыть среднего окончательный объём 10 мл, и повторять центрифугирования как шаг 3.3.
Примечание: Этот шаг может быть предпочтительным, если Тритурация не приводит к равномерно размера фрагментов.
- При необходимости, аспирационная мыть среднего и заменить 0,5 мл/хорошо трипсина (см. Таблицу материалы). Ресуспензируйте colonoids с пипеткой P200, крышка трубки и место в ванну воды 37 ° C приблизительно в 2 мин немедленно снять трубку, добавить мыть среднего окончательный объём 10 мл, и повторять центрифугирования как шаг 3.3.
4. гальваническое подвеска enteroid/colonoid
- Если покрытием вставок хранились при температуре 4 ° C, сбалансировать в 37 °C/5% CO2 культуры ткани инкубатор для по крайней мере 30 минут до ячейки покрытия.
- Для каждой вставки с покрытием подготовить 1 мл теплой (между 25-37 ° C) расширение среднего (ЭМ) и добавить 10 мкм Y-27632 и 10 мкм ЧИР 99021.
Примечание: EM состоит из передовых среде DMEM/F12 содержащие B27 (1 x), 50% WNT3A кондиционером среднего, средний RSPO1 кондиционером 15%, 10% льют кондиционером средний, 50 человека EGF нг/мл, 500 Нм A-83-01, 10 мкм SB 202190, антибиотик/противогрибковое коктейль (1 x), 10 мм HEPES, L-аланил L-глютамин дипептид (1 x) и пенициллин стрептомицином (1 x) (см. Таблицу материалы). - Аспирационная мыть среднего от трубка, содержащая ячейку гранулы и Ресуспензируйте в объеме EM достаточно, чтобы принести по крайней мере 100 мкл/вставить.
- Аспирационная коллаген IV решения от каждой вставки и мыть дважды с 150 мкл мыть среды за вставки.
- Накапайте 600 мкл EM в пространство под каждой вставки.
- Накапайте 100 мкл суспензии клеток в каждой вставки.
- Возвращение пластину в инкубатор культуры ткани и оставить в покое в течение 12 часов.
Примечание: Избегайте тряски или резко наклона пластины для предотвращения неравномерное распределение colonoid фрагментов на вставки мембраны. - Контролировать ячейки вложение и распространение сформировать вырожденная монослоя, поместив пластину на световой микроскоп фазово контрастной под 2,5 x-10 x объектив.
- После 1-2 дня большинство фрагментов следует придерживаться коллагеновой матрицы. Обновите питательной среды и прекратить лечение с Y-27632 и ЧИР 99021. Продолжать обновлять носитель каждые 2-3 дня до притока. Confluency обычно достигается через 7-10 дней.
5. мера электрического сопротивления transepithelial
- Приложите электрод приводит и мощности на эпителиальных Волътомметры (EVOM). Убедитесь, что функция измерения присвоено ом.
- Электрод советы кратко в 70% этанола окунуться и протирают сухой салфеткой лаборатории. Сбалансировать электрод в 5 мл мыть среды для примерно 5 мин.
- Погружать короче электрода в средстве вставки и ориентировать больше электрода в нижней пластины хорошо. Поддерживать электрода в полную вертикальную ориентацию до тех пор, пока EVOM чтение является относительно стабильным, или не более чем 60 s.
Примечание: Если Ассамблея электрода при наклоне далеко от вертикальной, или неправильно корректируется высота оголовка, кончик короче может вступить в контакт с и нарушить монослое клеток. - Сравните EVOM измерения для значения, полученного из свободных ячеек вставки, погруженной в питательной среды для оценки прогресса в достижении confluency или дифференциации.
6. дифференциация вырожденная монослои enteroid/colonoid
- Обмен EM для дифференциации среднего (DM) и продолжать обновлять СМИ каждые два дня до дня 5. DM-ет, что не хватает WNT3A, RSPO1, A-83-01 и SB 202190.
- Продолжать следить за Тер для проверки, что дифференциация идет, как ожидалось. ТЕЖ будет продолжать расти в течение 1-5 дней дифференциации. Монослои могут продолжать увеличить тер и сохраняют жизнеспособность за день 5-6 но exhibit максимальное и наиболее воспроизводимые результаты при использовании в день 5-6.
7. бактериальные инфекции с синантропных или патогенной кишечной палочки
- Один день до проведения инфекции, вымыть и кормить монослои с антибиотиками-EM или DM.
- Используйте цикл стерильные микробиологии осторожно очистите поверхности замороженных бактериальных глицерин запас и прививать 2 мл LB отвара. Передать трубку стандарт, пожимая инкубатора при 37 ° C для 12-16 ч.
- Развести 50 мкл закваски в 5 мл свежего LB отвара (1: 100) и продолжить инкубации встряхивании 90 мин. Это даст этапа культуры журнала с плотностью 105-106 образуя колонии единиц (cfu) / мл.
- При необходимости подтвердите бактериальных концентратов, измерения оптической плотности на 600 Нм (OD600) в спектрофотометре.
- Уменьшается бактериальной культуры на 12000 g x 10 мин, удалить супернатант и Ресуспензируйте бактерий в антибиотик-EM или DM до конечной концентрации 107 кое/мл.
- Добавьте 10 мкл бактериальной подвески для вставки (конечная концентрация 106 кое/мл). Накапайте медленно, чтобы смешивать и не мешать слой внеклеточной слизи.
- Возвращение пластину в инкубатор культуры ткани на период желаемого инфекции.
8. Фиксация для сохранения и имунноконтраст слизь
- Лифт, который клеточной культуры вставляет от 24-ну пластины, тщательно инвертировать на бумаге ткани лаборатории для удаления апикальной носителя и обтереть прочь внешние жидкости, цепляясь за вставки.
- В новой пластинкой 24-ну погружайте Вставка в раствор 1:3 уксусной кислоты кристаллизированной в абсолютного этанола (Кларк в раствор) для 10 мин при комнатной температуре.
- Инвертируйте Вставка Снимите фиксатор и увлажняет клетки в 1 x PBS на 10 мин продолжайте со стандартным иммуноокрашивания протоколами.
- Используйте лезвие бритвы вырезать по периметру вставки мембраны. Передача мембраны стекло микроскопа с помощью щипцов и прикрепите coverglass с монтажа средних.
9. Подготовка lysates клетки для immunoblotting
Примечание: Выполните следующие шаги на льду или в холодной комнате.
- Аспирационная среднего и мыть раз вставить с PBS.
- Добавить 150 мкл лизис буфера содержащие ингибиторы протеазы (см. таблицу материалы) для вставки и дать постоять 5-10 мин литического буфера содержит 50 мм трис pH 8, 150 мм NaCl, 1% IGEPAL CA-630, 0,5% Дезоксихолат натрия, 0.1% SDS, коктейль ингибитор протеазы масштаба 1: 100.
- Использовать мини-клеток скребок для удаления клеток из вставки, а затем использовать пипетку Р200 для кратко нарезанных подвеска и передачи пробки microcentrifuge.
- Sonicate подвеска с 5 x 1 s импульсов на 20% амплитуды, с помощью microtip зонд (см. Таблицу материалы).
- Добавить SDS-PAGE загрузки буфера, если немедленно выполняет электрофореза или Алиготе и хранить лизатов при-20 ° C.
Результаты
Человеческого enteroid и colonoid культуры выращивается как трехмерных структур, затем отделить и фрагментарный характер для покрытий на вставки культуры IV-покрытием клеток человеческого коллагена. Прогресс формирование монослоя легко отслеживается на ежедневной основе через светлые области микроскопии, иммунофлюоресценции, окрашивание (рис. 1) и устойчивый рост электрического сопротивления transepithelial (тер) (Рисунок 2), который отражает проницаемость плотные соединения ионов и коррелирует с confluency монослоя. ТЕЖ вставкой пустых 24-ну примерно 50-100 Ω·cm2и по достижении confluency возрастает до примерно 400-500 Ω·cm2. Все клетки эпителия в вырожденная монослои связаны соединительной комплексов определяется F-актина кольцо по периметру ячейки (рис. 1). Монослои в полном фактор роста СМИ представляют пролиферативной склеп как эпителий, состоит главным образом из активно делящихся клеток, которые включают нуклеозидный аналог Эду (рис. 2). Снятие факторов роста, WNT3A и RSPO1 способствует дифференциации, ведущих к ворсинок подобных культур, которые не имеют пролиферирующих клеток. Дифференцированные монослои содержат enterocytes (enteroids) или colonocytes (colonoids) и разработать специализированные эпителиальные клетки кишечника, как было показано в 3D культур,18 , включая бокал и enteroendocrine клетки. 15 дифференцированная монослои также демонстрируют значительное увеличение тер (> 1000 Ω·cm2) (рис. 2), указывающее Зрелые плотные соединения.
В нормальной физиологии человека кишечного эпителия слой отделяет питательных веществ и Микроб обогащенный Люминал пространства от стерильного серозных окружающей среды. Эпителий жестко регулирует перекрестных помех между этими двумя отсеками. Enteroid и colonoid монослои сохранить этот важный фрагментарность собственности как показано протеомного анализа в Таблица 1. Существуют значительные различия между состав белков в апикальной и базолатеральной кондиционером СМИ, собранных из монослои дифференцированных enteroid. Доступ к обеим апикальной и базолатеральной позволяет коллекции обоим supernatants зависимым образом время для измерения дифференциального секреции других молекул, таких как цитокинов и chemokines. 15 , 17
Монослои являются удобным и весьма воспроизводимые модели для обнаружения изменений в выражении протеина используя immunoblotting и иммуноокрашивания. Таким образом, изменения в муцина 2 (MUC2) выражение, индуцируемый нокдаун (KD) могут быть обнаружены с помощью обоих методов (рис. 3). Индуцируемый трансдукции была выполнена на 3D colonoids и поддерживается в антибиотик выбор средств массовой информации. После проверки KD, colonoids может быть непрерывно сохранить как 3D культур или покрытием как монослои для экспериментальных целей. Кроме того MUC2 KD не влияет на эффективность формирования монослоя, по сравнению с строке родительского colonoid дикого типа. Коллекция монослои для immunoblotting является простой и аналогичные протоколы, описанные для линий человеческих эпителиальных клеток аденокарциномы производные. Как правило около 50 мкг, или более общего белка могут быть извлечены из одного 0,33 см2 Вставка выросли монослоя. Как показано на рисунке 3, MUC2 едва выявляется в недифференцированных монослои colonoid WT (UD), но весьма выражается в дифференцированных монослои WT (DF). MUC2 находится ниже уровня обнаружения в UD и DF colonoid монослои преобразованы с MUC2 индуцируемый.
Важно отметить, что монослои являются подходящей модели для изучения хост микробных взаимодействий на апикальной поверхности эпителия. Colonoid монослои образуют толстый слой слизи прилагаемый MUC2-позитивных по дифференциации, которая легко не пронизана синантропных бактерий E. coli HS (рис. 4), похож на то, что было предложено в нормальных человеческих Колон. 19 однако, энтерогеморрагические E. coli (EHEC), человеческий патоген толстой, было показано имеют возможность разрушить слой MUC2-обогащенный прилагаемый слизь достичь апикальной поверхности эпителия (рис. 4). 14 , 20 оставшиеся MUC2 присутствует только внутри бокаловидных клеток.
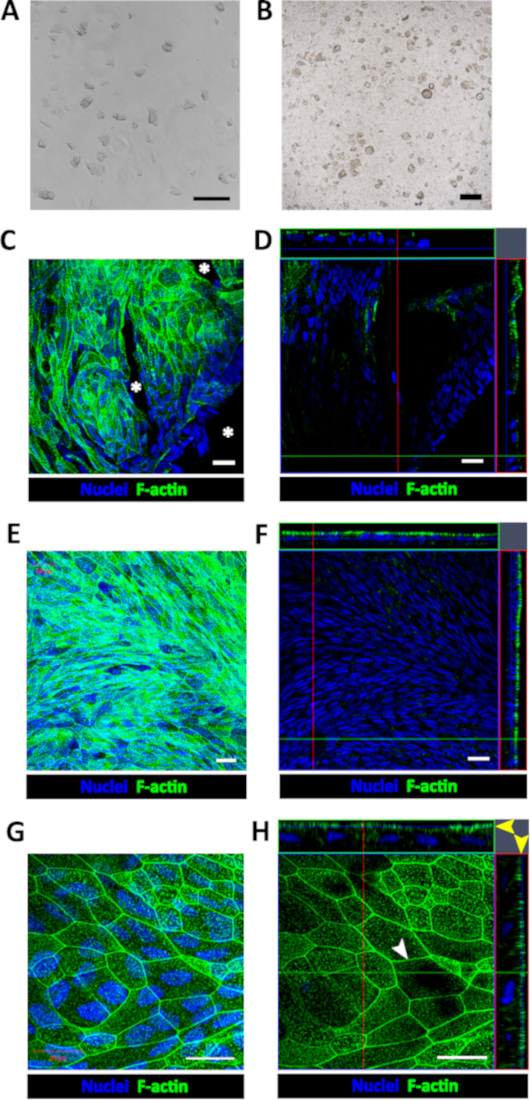
Рисунок 1: Создание человека монослои enteroid/colonoid. (A) пример colonoid фрагменты после распада BMM и Тритурация. (B) пример вставки сразу же после покрытия colonoid фрагментов. Масштаб бар (A-B) = 200 мкм. Представитель проекции максимальная сила света (C) и (D) конфокальный оптических Z-секции с соответствующего ортогональной проекции показывают colonoid фрагменты посеян человеческого коллагена IV-покрытием фильтры форму несколько монослоя острова 2-4 дней после посева. Ячейки свободно OBLASTей (звездочка) опознаваемые отсутствие обеих ядерных (Hoechst 33342, синий) и апикального F-актина (Фаллоидин, зеленый) пятнать в C и D. Представитель проекция максимальной интенсивности (E) и (F) конфокальный оптический раздел с соответствующего ортогональной проекции показывают вырожденная colonoid монослой с непрерывной апикальной поверхности определяется F-актина иммуноокрашивания около 1 недели после посева. (G) большого увеличения (H) конфокальный оптических секции с соответствующего ортогональной проекции и представитель максимальная интенсивность проекции показывают, что клетки в монослои вырожденная colonoid образуют perijunctional F-актина кольца (белая стрелка) и незрелых апикальной кисть границы (желтая стрелка голов). Масштаб бар (C-H) = 20 мкм. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
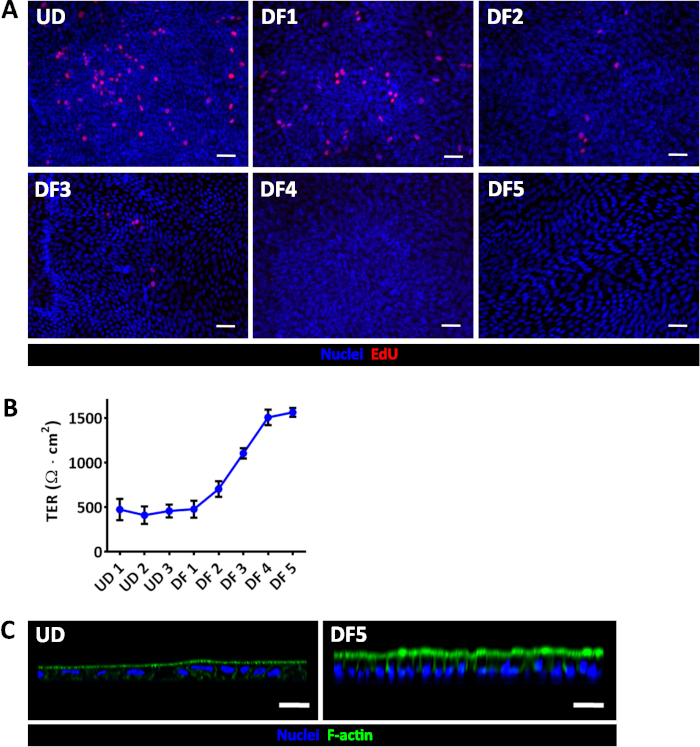
Рисунок 2: Оценка дифференцировки enteroid/colonoid монослоя. (A) Эду (красный) инкорпорации демонстрирует прогрессирующая потеря распространения во время дифференциация монослоя тощей кишки. (B) средняя Тер измерения в монослои вырожденная тощей кишки в расширение или дифференциации среднего. Планки погрешностей представляют SEM. UD, недифференцированный; DF, продифференцировано. Номера соответствуют дней согласно указанному условию; UD1 был в первый день confluency, примерно в 1 неделю после посева. (C) UD тощей кишки монослои имеют широкие, короче клетки и чем DF день 5 тощей кишки монослои менее зрелые апикальной на основе актина кисть границы. Масштаб бар (A, C) = 50 мкм. Все монослои были изображены по крайней мере 1 недели после посева и были вырожденная до начала дифференциации. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
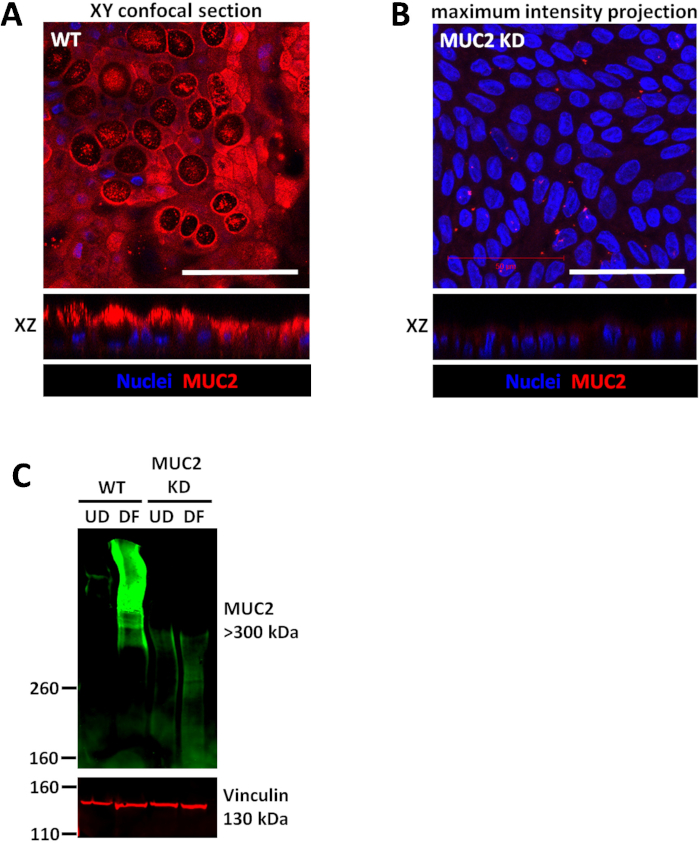
Рисунок 3: Colonoids дикого типа и индуцируемый преобразованы нокдаун (KD) colonoids каждой формы вырожденная монослои. (A) представитель образы дикого типа (WT) человека вырожденная colonoid монослоя дифференцированы на 5 дней и (B) аналогично вырос монослои, производные от MUC2 KD colonoid культур. Масштаб бар (A-B) = 50 мкм (C) представитель immunoblot colonoid культур, преобразованы с платные индуцируемый или MUC2 индуцируемый показывает, что изменения в выражении протеина благодаря KD можно предел, immunoblot. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
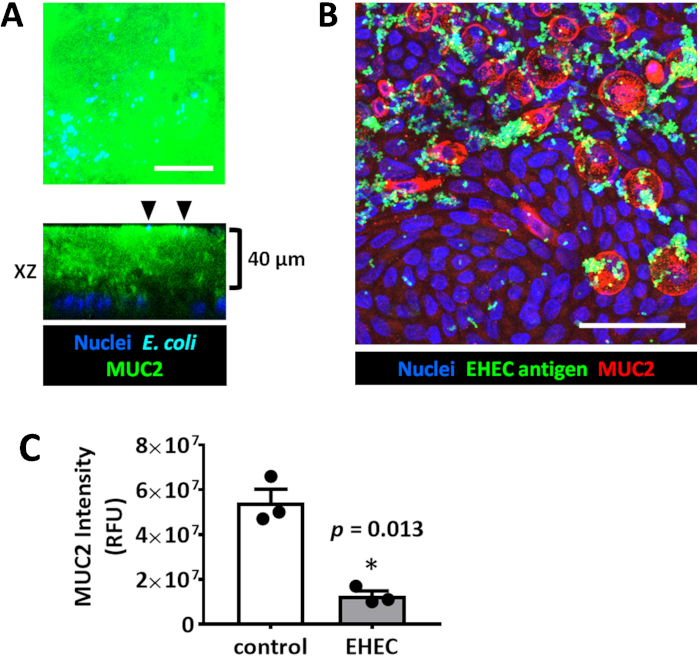
Рисунок 4: Enteroid/colonoid монослои являются подходящей модели для изучения взаимодействия Люминал Микроб хост. (A) представитель максимальная интенсивность проекции и ортогональных оптических секции colonoid монослоя показывает толстые апикальной MUC2-позитивных слизь слой, который не проницаемой для е. coli HS (черные стрелки) сидя на апикальной слизь поверхности. Монослой был заражен 6 часов с 106 кое/мл HS. (B) представитель максимальная интенсивность проекции человека colonoid монослоя вершине инфицированных ЭГКП (106 кое/мл, 6 часов). Масштаб бар (A-B) = 50 мкм. (C) MUC2 иммунофлюоресценции интенсивности измерения показывают значительное снижение MUC2 в монослои ЭГКП инфицированных colonoid, по сравнению с неинфицированным элементов управления. Планки погрешностей представляют SEM. пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
| Белка | Присоединение номер | Изобилие пептида |
| Базолатеральной СМИ | ||
| белок, связывающий жирные кислоты печени [Homo sapiens] | NP_001434.1 | 1299 |
| Профилин-1 [Homo sapiens] | NP_005013.1 | 797 |
| аполипопротеина А-IV прекурсоров [Homo sapiens] | NP_000473.2 | 744 |
| Экто ADP-ribosyltransferase 4 прекурсоров [Homo sapiens] | NP_066549.2 | 633 |
| Глицеральдегид-3-фосфат дегидрогеназа изоформы 1 [Homo sapiens] | NP_002037.2 (+ 1) | 616 |
| serotransferrin прекурсоров [Homo sapiens] | NP_001054.1 (+ 1) | 572 |
| Витамин D связывания белка изоформы 3 прекурсоров [Homo sapiens] | NP_001191236.1 (+ 2) | 567 |
| каталаза [Homo sapiens] | NP_001743.1 | 427 |
| agrin изоформы 1 прекурсоров [Homo sapiens] | NP_940978.2 (+ 1) | 377 |
| lactotransferrin изоформы 1 прекурсоров [Homo sapiens] | NP_002334.2 (+ 1) | 262 |
| Верхушечный СМИ | ||
| трилистник фактор 3 прекурсоров [Homo sapiens] | NP_003217.3 | 326 |
| трилистник фактор 1 прекурсоров [Homo sapiens] | NP_003216.1 | 304 |
| базальной мембраны конкретных heparan сульфат протеогликана основной белок изоформы предвестником [Homo sapiens] | NP_001278789.1 (+ 3) | 303 |
| filamin-B изоформы 1 [Homo sapiens] | NP_001157789.1 (+ 2) | 240 |
| трилистник фактор 2 прекурсоров [Homo sapiens] | NP_005414.1 | 182 |
| удалена в мозг злокачественных опухолей 1 белок изоформы b прекурсоров [Homo sapiens] | NP_015568.2 (+ 3) | 169 |
| кератин, тип II цитоскелета 1 [Homo sapiens] | NP_006112.3 | 157 |
| миозин-9 [Homo sapiens] | NP_002464.1 | 150 |
| aminopeptidase N прекурсоров [Homo sapiens] | NP_001141.2 (+ 1) | 145 |
| agrin прекурсоров [Homo sapiens] | NP_940978.2 (+ 1) | 112 |
Таблица 1. Частичный список пептидов, выявленные жидкостной хроматографии/тандемные масс-спектрометрии в апикальной и базолатеральной жидкости, отобранных из дифференцированной монослои тощей кишки.
Обсуждение
Критические параметры для успешного формирования enteroid/colonoid монослои включают 1) здоровым, размножающихся 3D культур как исходного материала; 2) покрытие поверхности вставить культуры клеток с человеческого коллагена IV до монослоя посева; 3) фрагментация 3D культур механически или энзиматического, но не на уровне отдельной ячейки.
Во время изоляции 3D enteroids/colonoids оптимальной пожимая скорость может варьироваться в зависимости от вращения диаметр данного шейкер модели. Целью является не только агитировать пластину для эффективного смешивания, но также избежать разбрызгивания суспензию клеток на крышке плита или в соседних скважин. Инкубационный период < 30 мин могут принести остаточного BMM цепляясь клетки, которые могут препятствовать привязанность и формирование единой клетки монослои когда покрытием на вставок. Обширные инкубации (≥ 1 h) даст жизнеспособность клеток значительно снизилась.
Степень Тритурация требуется отделить 3D enteroids/colonoids может варьироваться с поршневой жесткость и пользователя ловкость. Периодическое рассмотрение хорошо содержимого на световой микроскоп фазово контрастной рекомендуется для определения однородности фрагмент во время Тритурация, с целью приблизительно 30 ячеек на фрагмент. Вместо или в дополнение к Тритурация подвески можно кратко переваривается трипсином для получения меньшего единообразных фрагментов. Трипсин дайджест может быть желательным, если монослои содержат большое количество 3D-подобных структур среди противном случае однослойного эпителия. Однако диссоциации в отдельные ячейки не желательно, поскольку это значительно сокращает жизнеспособность клеток. Один хорошо культивированный в капельки BMM 35 мкл enteroids/colonoids будет достаточно, чтобы заполнить 2-3 вставки, но этот фактор может варьироваться в зависимости от числа и средний размер enteroids/colonoids.
Colonoid монослои может поглощать значительный объем апикальной среды как они дифференцируют. Это можно обойти путем применения дополнительных DM в верхней вставить камеру (150-200 мкл), хотя подсушки верхней палаты не представляется, отрицательно сказаться на жизнеспособности монослоя или функции в нижнем течении анализов. После примерно 4-5 дней дифференциации colonoid монослои развивать внеклеточной слизи, которая может быть видна как толстый/желатиновой материала на поверхности клеток после тщательного стремления дм.
Для инфекции ЭГКП взаимодействия с внешней слизь слой мы регулярно использовать бактериальных титр и инкубационного периода, указанного в протоколе. Однако уникальных штаммов бактерий первоначально быть assayed на несколько концентрации и инкубационных периодов определить соответствующие параметры для желаемого эффекта.
Во время фиксации слизи аспирационных апикальной среднего, скорее всего, удалить большую часть слоя внеклеточной слизи неприсоединенной. Таким образом важно тщательно слейте среды. Если среда сохраняется в Вставка поверхностное натяжение, используйте углу ткани сложить Лаборатория сломать поверхностное натяжение и фитиль от большинства среды. После фиксации и окраски слой слизи может непреднамеренно выбили или плоский во время монтажа coverglass над вставка фильтра. Чтобы сохранить высоту слизи, установите фильтр на падение монтажа СМИ и тщательно место coverglass на фильтре. Не коснитесь или нажмите вниз на coverglass, как это может значительно сгладить слой слизи.
Сформировать поляризованные монослоя от клеток в культуре 3D, это необходимо воспроизводить взаимодействие между базолатеральной интегринов мембраны клеток кишечного эпителия и белков внеклеточного матрикса (ECM). Ламинин, IV коллаген, фибронектин и массив протеогликаны составляют кишечного эпителия ECM. 21 , 22 мы сравнивали человеческих клеток, полученных Ламинин, фибронектин, коллаген IV и мышиным производные BMM как вставка покрытия. Коллаген IV поддерживается формирование стабильного, долгосрочного (до 4 недель) только вырожденная монослои enteroid/colonoid (рисунки 1-2). Небольшие участки монослоя как роста были получены на каждом из других протестированных матриц, но эти регионы не прогрессировали в confluency. Использование человеческого коллагена IV как суррогат ECM имеет ряд преимуществ. БММ производных от Engelbreth-холм-Рой (EHS), мышиных саркома клетки являются не человеческого происхождения, тогда как человеческий коллаген IV является коммерчески доступных и обычно более экономически эффективным. Кроме того BMM представляет собой сложную смесь белков с присущих изменчивости и могут содержать факторы роста, выделяемый саркома, которые влияют на экспрессию генов. 23
По-прежнему неполно понимается взаимодействие клеток кишечного эпителия и базовой ECM в кишечного эпителия реституции. Было предложено значение коллаген IV, но не Ламинин, как сцепления лигандом для человека colonocytes24 и усилитель кишечные крипты эпителиальных клеток реституции25 с использованием антител против коллаген IV, позволявшая вложений . Эпителиально выразил β1-Интегрин представляется важным для ECM взаимодействия, как антител специфических для β1-Интегрин значительно заблокирован адгезию colonocytes для типа IV коллагена. 24 а коллаген IV обеспечивает надежный ECM для enteroid/colonoid монослой формирования на вставок, эпителиальные Ремоделирование ECM со временем не еще была оценена в этой модели, ни влияние более сложных и определенных смесей ECM Коллаген IV, Ламинин и фибронектин.
Человеческого enteroids/colonoids в монослое формате (рисунки 1-4) включение манипуляции и выборки, будет громоздким или невозможно достичь с помощью 3D матрицы встроенный культур. 3D enteroids/colonoids различаются по размеру, структурной сложности и просветный тома, и таким образом трудно точно quantitate микроинъекции микробов или малых молекул. Кроме того в отличие от монослои (Таблица 1), 3D культур предотвратить прямой доступ к Люминал и базолатеральной поверхностей для измерения ионов, питательных веществ, цитокинов или выделяется факторы, связанные с физиологической или патофизиологические процессов . Confluency (рисунки 1-2) является одним из главных свойств enteroid/colonoid монослой, необходимых для создания не только физиологическое градиенты питательных веществ, ионов и других макромолекул,16 , но также создание надлежащего барьера между Люминал микробиоту и стерильные мезенхимальных/иммунной клетки заполняется серозных средах. Эти аспекты являются важными для будущих исследований, которые включают монослои enteroid/colonoid с типов мезенхимы, иммунитет или нейрональных клеток для построения более сложных физиологических моделей.
Отметил ограничения модели Вставка культуры клеток, описанной здесь включают в себя отсутствие физической силы, такие как жидкости касательное напряжение и механическое растяжение/сжатие (перистальтики), а анаэробных апикальной среды, обычно сталкиваются кишечника эпителия в естественных условиях. Эти элементы имеют потенциал, чтобы решать более сложные платформы microphysiological,26 , но они также требуют дополнительных затрат, оборудование и опыт для реализации. 3D и монослоя культуры являются также без взаимодействия с или взносов кишечная микрофлора, популяции стромальных клеток и иммунной системы, если целенаправленно добавлены эти компоненты.
Будущих приложений монослоя enteroid/colonoid на коллаген IV-покрытием клетки культуры вставок могут включать в себя другие исследования патогенных или синантропных микробной взаимодействия, наркотиков или питательных поглощения, токсичности, метаболизм, барьерные функции и функциональные повышение катализируемой Сопредседатель культуры с типами дополнительные клеток кишечника. Оценок могут быть сделаны не только в пределах эпителия здоровых доноров, но и от физических лиц с генетической мутации или кишечных расстройств, в естественных условиях фенотипов устанавливаются должны быть сохранены в ex vivo enteroid/colonoid культуры.
Раскрытие информации
Авторы не имеют ничего сообщать.
Благодарности
Эта работа была поддержана NIH грантов P01 AI125181, K01 DK106323 (JGI) и K01 DK113043 (JFA). Мы благодарим Джеймса капер (Университет штата Мэриленд, Балтимор, MD, США) за предоставление E. coli штамм ЭГКП и HS. Мы также признаем комплексной физиологии и изображений ядра Хопкинс Конте пищеварительные болезни основных и переводческая исследовательский центр Core (P30 DK089502) и Джонса Хопкинса масс-спектрометрии и Proteomics ядро.
Материалы
| Name | Company | Catalog Number | Comments |
| 2-Amino-2-(hydroxymethyl)-1,3-propanediol | Sigma | T4661 | Tris base, Component of lysis buffer |
| A-83-01 | Tocris | 2939 | ALK4/5/7 inhibitor |
| Acetic acid, glacial | Fisher Scientific | A38 | |
| Advanced DMEM/F12 | Life Technologies | 12634-010 | Component of growth medium |
| Alexa Fluor 488 phalloidin | Life Technologies | A12379 | Fluorescent probe for F-actin |
| Antibiotic/antimycotic cocktail | Invivogen | ant-pm-2 | Primocin (100x) |
| B27, 50x | Life Technologies | 17504-044 | Component of growth medium |
| Cell culture inserts | Corning | 3470 | Transwell, PET membrane, 0.4 μm pore, 24-well plate |
| CHIR 99021 | Tocris | 4423 | GSK3β inhibitor |
| Click-iT Plus EdU Alexa Fluor 594 Imaging Kit | Life Technologies | C10639 | |
| Collagen IV, from human placenta | Sigma | C5533 | |
| Cultrex Organoid Harvesting Solution | Trevigen | 3700-100-01 | Depolymerizes basement membrane matrix |
| Enterohemorrhagic Escherichia coli (EHEC) | Kaper lab, University of Maryland | ||
| Epithelial voltohmmeter | World Precision Instruments | EVOM2 | |
| Epithelial voltohmmeter electrode | World Precision Instruments | STX3 | |
| Escherichia coli strain HS | Kaper lab, University of Maryland | ||
| Ethanol, absolute | Pharmco | 111000200 | |
| FluorSave mounting medium | Millipore | 345789 | For mounting insert membrane on microscope slide |
| GlutaMAX | Life Technologies | 35050-061 | L-alanyl-L-glutamine dipeptide, 200 mM |
| HEK293T/Noggin-Fc cell line | van den Brink lab, Tytgat Institute for Liver and Intestinal Research | For production of Noggin conditioned medium | |
| HEK293T/RSPO1-Fc-HA cell line | Trevigen | 3710-001-K | For production of Rspondin-1 conditioned medium |
| HEPES, 1 M | Life Technologies | 15630-080 | Component of growth medium |
| Heraeus Multifuge X1R Centrifuge | Thermo Fisher Scientific | 75004250 | |
| Hoechst 33342 | Life Technologies | H3570 | Fluorescent nuclear dye |
| Human epidermal growth factor (EGF) | R&D Systems | 236-EG-01M | Component of growth medium |
| IGEPAL CA-630 | Sigma | I8896 | Component of lysis buffer |
| Inverted cell culture light microscope | Olympus | CKX51 | |
| LB broth | EMD Millipore | 1.10285.0500 | |
| L-WNT3A cell line | ATCC | CRL-2647 | For production of Wnt3a conditioned medium |
| Matrigel, growth factor reduced | Corning | 356231 | Basement membrane matrix for 3D culture |
| Mini cell scraper | United BioSystems | MCS-200 | |
| MUC2 antibody, mouse monoclonal | Abcam | ab11197 | Use at 1:100 for immunostaining, 1:500 for immunoblotting |
| MUC2 shRNA lentiviral particles | GE Dharmacon | RHS4531 | GIPZ lentiviral shRNA, ID: 4583 |
| Orbital shaker | Grant Instruments | PSU-10i | |
| Penicillin-streptomycin, 100x | Life Technologies | 15140-122 | Component of growth medium |
| Phosphate buffered saline | Corning | 21-031 | |
| Probe sonicator with microtip | Branson Ultrasonics | 450 | |
| Protease inhibitor cocktail for mammalian cells | Sigma | P8340 | Component of lysis buffer |
| SB 202190 | Tocris | 1264 | p38 MAPK inhibitor |
| Sodium chloride | Sigma | S3014 | Component of lysis buffer |
| Sodium dexoycholate | Sigma | D6750 | Component of lysis buffer |
| Sodium dodecyl sulfate | Sigma | L3771 | Component of lysis buffer |
| TrypLE Express, 1x | Life Technologies | 12605-010 | Trypsin, for digesting enteroid/colonoid fragments |
| Vinculin antibody, rabbit monoclonal | Abcam | ab129002 | Use at 1:1000 for immunoblotting |
| Water, tissue culture grade, sterile filtered | Corning | 25-055 | |
| Y-27632 | Tocris | 1254 | RhoA/ROCK inhibitor |
Ссылки
- In, J. G., et al. Human mini-guts: new insights into intestinal physiology and host-pathogen interactions. Nature Reviews Gastroenterology & Hepatology. 13, 633-642 (2016).
- Hill, D. R., et al. Bacterial colonization stimulates a complex physiological response in the immature human intestinal epithelium. eLife. 6, e29132 (2017).
- Williamson, I. A., et al. A High-Throughput Organoid Microinjection Platform to Study Gastrointestinal Microbiota and Luminal Physiology. Cellular and Molecular Gastroenterology and Hepatology. 6, 301-319 (2018).
- Leslie, J. L., et al. Persistence and Toxin Production by Clostridium difficile within Human Intestinal Organoids Result in Disruption of Epithelial Paracellular Barrier Function. Infection and Immunity. 83, 138 (2015).
- Foulke-Abel, J., et al. Human Enteroids as a Model of Upper Small Intestinal Ion Transport Physiology and Pathophysiology. Gastroenterology. 150, (2016).
- Yin, J., et al. Molecular Basis and Differentiation-Associated Alterations of Anion Secretion in Human Duodenal Enteroid Monolayers. Cellular and Molecular Gastroenterology and Hepatology. 5, 591-609 (2018).
- Tse, C., et al. Enterohemorrhagic E. coli (EHEC)—Secreted Serine Protease EspP Stimulates Electrogenic Ion Transport in Human Colonoid Monolayers. Toxins. 10, 351 (2018).
- Jabaji, Z., et al. Use of collagen gel as an alternative extracellular matrix for the in vitro and in vivo growth of murine small intestinal epithelium. Tissue engineering. Part C, Methods. 19, 961-969 (2013).
- Wang, Y., et al. Self-renewing Monolayer of Primary Colonic or Rectal Epithelial Cells. Cellular and Molecular Gastroenterology and Hepatology. 4, 165-182 (2017).
- Moon, C., VanDussen, K. L., Miyoshi, H., Stappenbeck, T. S. Development of a primary mouse intestinal epithelial cell monolayer culture system to evaluate factors that modulate IgA transcytosis. Mucosal Immunology. 7, 818-828 (2014).
- VanDussen, K. L., et al. Development of an enhanced human gastrointestinal epithelial culture system to facilitate patient-based assays. Gut. 64, 911 (2015).
- Ettayebi, K., et al. Replication of human noroviruses in stem cell–derived human enteroids. Science. 353, 1387 (2016).
- Kozuka, K., et al. Development and Characterization of a Human and Mouse Intestinal Epithelial Cell Monolayer Platform. Stem Cell Reports. 9, 1976-1990 (2017).
- In, J., et al. Enterohemorrhagic Escherichia coli Reduces Mucus and Intermicrovillar Bridges in Human Stem Cell-Derived Colonoids. Cellular and Molecular Gastroenterology and Hepatology. 2, 48-62 (2016).
- Noel, G., et al. A primary human macrophage-enteroid co-culture model to investigate mucosal gut physiology and host-pathogen interactions. Scientific Reports. 7, 45270 (2017).
- Vernetti, L., et al. Functional Coupling of Human Microphysiology Systems: Intestine, Liver, Kidney Proximal Tubule, Blood-Brain Barrier and Skeletal Muscle. Scientific Reports. 7, 42296 (2017).
- Noel, G., et al. Enterotoxigenic Escherichia coli is phagocytosed by macrophages underlying villus-like intestinal epithelial cells: modeling ex vivo innate immune defenses of the human gut. Gut Microbes. 9, 382-389 (2018).
- Sato, T., et al. Long-term Expansion of Epithelial Organoids From Human Colon, Adenoma, Adenocarcinoma, and Barrett's Epithelium. Gastroenterology. 141, 1762-1772 (2011).
- Johansson, M. E. V., Sjövall, H., Hansson, G. C. The gastrointestinal mucus system in health and disease. Nature Reviews Gastroenterology & Hepatology. 10, 352-361 (2013).
- Hews, C. L., et al. The StcE metalloprotease of enterohaemorrhagic Escherichia coli reduces the inner mucus layer and promotes adherence to human colonic epithelium ex vivo. Cellular Microbiology. 19, e12717 (2017).
- Laurie, G. W., Leblond, C. P., Martin, G. R. Localization of type IV collagen, laminin, heparan sulfate proteoglycan, and fibronectin to the basal lamina of basement membranes. The Journal of Cell Biology. 95, 340 (1982).
- Timpl, R. Macromolecular organization of basement membranes. Current Opinion in Cell Biology. 8, 618-624 (1996).
- Hughes, C. S., Postovit, L. M., Lajoie, G. A. Matrigel: A complex protein mixture required for optimal growth of cell culture. Proteomics. 10, 1886-1890 (2010).
- Ishii, S., et al. Normal colonic epithelium adheres to carcinoembryonic antigen and type IV collagen. Gastroenterology. 106, 1242-1250 (1994).
- Moore, R., Madri, J., Carlson, S., Madara, J. L. Collagens facilitate epithelial migration in restitution of native guinea pig intestinal epithelium. Gastroenterology. 102, 119-130 (1992).
- Bein, A., et al. Microfluidic Organ-on-a-Chip Models of Human Intestine. Cellular and Molecular Gastroenterology and Hepatology. 5, 659-668 (2018).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены