Method Article
Производство рекомбинантных белков PRMT с использованием векторной системы экспрессии бакуловируса
В этой статье
Резюме
Векторная система экспрессии бакуловируса (BEVS) является надежной платформой для скрининга экспрессии и производства белковых аргининметилтрансфераз (PRMT), которые будут использоваться для биохимических, биофизических и структурных исследований. Миллиграммовые количества материала могут быть получены для большинства PRMT и других белков, представляющих интерес, требующих платформы эукариотической экспрессии.
Аннотация
Белковые аргининметилтрансферазы (PRMT) метилат аргинина остатки на широком спектре белков, которые играют роль в многочисленных клеточных процессах. PRMT могут либо моно-, либо диметилат аргинин гуанидиновых групп симметрично или асимметрично. Энзимология этих белков представляет собой сложную и интенсивно исследуемую область, которая требует миллиграммового количества высококачественного рекомбинантного белка. Векторная система экспрессии бакуловируса (BEVS), использующая клетки насекомых Autographa californica multiple nucleopolyhedrovirus (AcMNPV) и Spodoptera frugiperda 9 (Sf9), использовалась для скрининга экспрессии и производства многих PRMT, включая PRMT 1, 2 и 4-9. Для одновременного скрининга экспрессии нескольких конструкций этих белков, включая домены и усеченные фрагменты, а также полноразмерные белки, мы применили масштабируемые методы с использованием регулируемых и программируемых многоканальных пипеток в сочетании с 24- и 96-скважинными пластинами и блоками. В целом, эти корректировки метода позволили крупномасштабную генерацию ДНК bacmid, рекомбинантных вирусов и скрининг экспрессии белка. Использование емкостей для культивирования с большим объемом клеточной суспензии Sf9 помогло преодолеть ограничения пространства в производственном конвейере для односерийного крупномасштабного производства белка. Здесь мы описываем подробные протоколы для эффективной и экономичной экспрессии функциональных PRMT для биохимических, биофизических и структурных исследований.
Введение
Белковые аргининметилтрансферазы (PRMT) метилат аргинина остатки монометилового или симметричного/асимметричного диметилового виде. Повторяющиеся последовательности RG/RGG/GRG являются весьма предпочтительными для большинства PRMT и содержатся в широком спектре белков1,2. Аргининовые метилированные белки, такие как гистоны или факторы транскрипции и факторы сплайсинга, регулируют транскрипцию, сплайсинг и структуру хроматина3,4. Растущие знания о разнообразной регуляции использования субстрата и кофактора, оборота и кинетики PRMT, а также генерации селективных ингибиторов пролили механистический свет на эти ферменты и их комплексы5,6. Однако не все члены семьи ПРМТ изучаются в одинаковой степени; например, PRMT9 только недавно был обнаружен как член семейства PRMT1. Исследования структуры и функции ферментов для этих белков требуют достаточного, часто миллиграммового, количества рекомбинантного белка, чтобы быть доступным.
Система экспрессии прокариотической экспрессии Escherichia coli (E. coli)обычно является первым выбором для скрининга экспрессии с использованием нескольких конструкций для данного белка7,8,9. Однако экспрессия на основе E. coliне всегда приводит к достаточному количеству белков PRMT в их активных формах, как мы отметили, в частности, для PRMT5 и PRMT7 (см. Ниже). Таким образом, PRMT, которые не смогли экспрессироваться в E. coli или должны были быть получены механизмом эукариотической экспрессии, были субклонированы в векторы, подходящие для скрининга экспрессии в альтернативной системе векторов экспрессии бакуловируса (BEVS). В то время как экспрессируемые E. coli образцы PRMT1, PRMT3 и PRMT8 широко использовались для анализов in vitro и кристаллографии, другие PRMT, такие как PRMT5, который требует партнера по связыванию MEP50 своего двойного метилтрансферазного домена, и PRMT, такие как PRMT7 и 9, требуют экспрессии клеток насекомых для получения достаточного количества активного белка. В целом, стандартизированные среднепроизводительный анализ метилтрансферазы для PRMT4, 5, 6, 7 и 9 использовали BEVS в клетках насекомых6. Векторная система экспрессии бакуловируса (BEVS) является универсальной платформой для получения рекомбинантных белков, требующих механизма эукариотической экспрессии, который позволяет осуществлять постперекренческие модификации, необходимые для биохимических, биофизических и структурных исследований10,11,12. Несколько BEVS стали коммерчески доступными с момента первого сообщения об использовании бакуловирусов в 1983 году для экспрессии белка13. Большинство из этих протоколов используют различные стратегии для передачи экспрессии плазмиды в клетки насекомых. К ним относятся Bac-to-Bac, flashBAC, BaculoGOLD Bright, BacVector-3000, BacMagic, BacPAK и т. Д. Наш протокол основан на наиболее часто используемой системе в BEVS, системе Bac-to-Bac14,которая предназначена для передачи гена / кДНК, кодирующей интересуяще белок (POI, здесь PRMT), в геном бакуловируса, поддерживаемый в специализированном штамме E. coli посредством сайт-специфической транспозиции15.
Вкратце, переносной вектор плазмиды, содержащий интересующий ген, был преобразован в клетки, компетентные DH10Bac E. coli, для генерации рекомбинантной вирусной днк bacmid. Затем адгезивные клетки Sf9 были трансфектованы ДНК bacmid. Через четыре-пять дней после трансфекции первоначальные рекомбинантные бакуловирусы, секретируемые в среду клеточной культуры, были восстановлены и помечены как вирус P1. Запасы бакуловируса P1 затем использовались для амплификации вируса (т. Е. Генерации запасов бакуловируса P2) и скрининга экспрессии белка. На основе результатов скрининга экспрессии вирусы P2 для наилучшей экспрессии белка были идентифицированы и использованы для создания культур суспензии инфицированных бакуловирусом клеток насекомых (SCBIIS) для крупномасштабного производства белка. Здесь мы описываем наши подробные протоколы и описываем обоснование нашего выбора реагентов и сосудов для культивирования для поддержки нашей стратегии разработки более эффективной по времени, экономичности и масштабируемости методологии для получения достаточного количества желаемых рекомбинантных белков.
протокол
ПРИМЕЧАНИЕ: Обзор этапов протокола BEVS приведен на рисунке 1.
1. Генерация рекомбинантной бакмидной ДНК
- Подготовка селективных пластин агара LB для трансформации DH10Bac
- Подготовьте агаровые пластины LB, содержащие: 50 мкг/мл канамицина, 7 мкг/мл гентамицина, 10 мкг/мл тетрациклина, 200 мкг/мл Bluo-gal и 40 мкг/мл IPTG для выбора трансформантов DH10Bac.
- Взвесьте 25 г предварительно смешанный бульон LB и 13 г бакто-агара и поместите в колбу 2 л. Доведите объем до 1 л с дистиллированной водой и автоклавом в течение 15-30 мин при 121 °C.
- Установите водяную баню при 50 °C и охладите раствор автоклавного агара на водяной бане в течение 40-60 минут до его охлаждения до 50-55 °C.
- К охлаждаемой основе добавляют гентамицин до конечной концентрации 7 мкг/мл, канамицин до конечной концентрации 50 мкг/мл, тетрациклин до конечной концентрации 10 мкг/мл, Блюо-гал до конечной концентрации 200 мкг/мл и ИПТГ до конечной концентрации 40 мкг/мл.
- Смешайте раствор агара и аликвоту по 7-10 мл среды с каждой пластиной 60 мм с помощью пипетки 50 мл. Дайте плитам постоять при комнатной температуре (2 ч) для затвердевать. Инвертировать, заворачивать и хранить при 4 °C. Пластины, содержащие антибиотики, стабильны до 4 недель.
- Превращение плазмиды в dh10Bac E. coli компетентные клетки
- Рассчитайте необходимый объем грамотных ячеек.
- Разморозить грамотные клетки на льду, осторожно раскрутить и повторно суспендируйте обратно нежным постукиванием.
- Используйте 12-канальный пипетку для дозирования 4 мкл клеток в каждую скважину 96-скважинной ПЦР-пластины.
- Добавьте ~ 0,3-0,5 мкг рекомбинантной плазмидной ДНК к компетентным клеткам и аккуратно перемешайте постукиванием. Инкубировать смесь на льду в течение 10-15 мин.
- Тепловой удар смеси в ПЦР-машине при 42 °C в течение 45 с. Охладить на льду в течение 2 мин.
- Дозировать по 0,5 мл soc-среды в каждую скважину из 96 блоков скважин (скважина глубиной 96 2,4 мл).
- Используйте 12-канальную пипетку для переноса преобразованной бактериальной суспензии в соответствующий колодец блока и накройте его листом воздушной поры.
- Поместите блок в встряхивательный инкубатор при 37 °C со средним перемешиванием (205 об/мин) в течение 4-5 ч.
- Равномерно распределите 30-50 мкл культуры по поверхности агаровой пластины LB с помощью стерильных стеклянных шариков. Храните остальную часть культуры при 4 °C.
- Инкубируют пластины при 37 °C до тех пор, пока не будет различим цвет сине-белых колоний (40-48 ч). Откажитесь от культуры, когда на тарелке получится достаточно белых, крупных колоний.
- Чтобы гарантировать, что белые колонии содержат только рекомбинантную ДНК bacmid, повторно проложите одну изолированную белую колонию на свежие пластины агара LB, содержащие антибиотики, bluo-gal и IPTG для проверки фенотипа.
- Инкубировать в течение 48 ч при 37 °C.
- Выберите одну проверенную белую колонию из повторно расчищеной пластины для извлечения рекомбинантной днк bacmid.
- Выделение рекомбинантной бакмидной ДНК
- Инокулируют одну изолированную белую колонию в 3 мл среды LB, дополненной 50 мкг/мл канамицина, 7 мкг/мл гентамицина и 10 мкг/мл тетрациклина в 24-скважинных блоках (24-скважинные блоки с круглым дном) и покрывают листом воздушной поры.
- Растите при 37 °C в течение ночи с встряхиванием при 250 об/мин.
- Центрифугировать 24-скважинные блоки при 2 100 х г в течение 10 мин. Декантируйте супернатант, переверните блок и осторожно постучите по абсорбирующей папиросной бумаге. Добавьте 250 мкл раствора 1 (раствор для повторного суспензии клеток) в каждую скважину.
- Запечатайте блоки ленточными прокладками или любыми другими уплотнительными пленками и поместите их на встряхивающую платформу при 75 об/мин в течение 5-10 мин. Проверьте каждую скважину, чтобы обеспечить надлежащий лизис клеток, и при необходимости повторно суспендируйте, используя наконечник 1 мл.
- Добавляют 250 мкл раствора 2 (раствор клеточного лизиса) в каждую скважину, герметизируют блоки и помещают на встряхивающую платформу при 75 об/мин в течение 30 с (во избежание перекрестного загрязнения образцов не инвертировать 24-скважинные блоки), инкубируя при комнатной температуре в течение 4 мин.
- Добавьте 250 мкл раствора 3 (нейтрализующего раствора), запечатайте блоки и поместите на встряхивательную платформу со скоростью 75 об/мин в течение 30 с. Образуется густой белый осадок белка и геномной ДНК E. coli. Поместите образец на лед на 10-15 мин.
- Центрифуга в течение 60 мин при 2,100 х г при 4 °C плотно гранулирует белый осадочный материал. Во время центрифугирования маркируют новую микроцентрифужную трубку и добавляют 0,8 мл абсолютного изопропанола.
- Осторожно перенесите супернатант в пробирку, содержащую изопропанол, избегая любого белого осажденного материала. Перемешайте, осторожно перевернутый тюбик несколько раз, а затем поместите на лед на 5-10 минут. На этом этапе образец может храниться при -20 °C в течение ночи.
- Центрифугировать образец в течение 15 мин при 14 000 х г при 4 °C. Удалите супернатант и добавьте 0,5 мл 70% этанола в каждую пробирку. Переверяйте трубку несколько раз, чтобы промыть гранулу. Центрифуга в течение 5 мин при 14 000 х г при комнатной температуре. (Опционально: повторная стирка)
- Занесите образцы внутрь ламинарного проточного капота, чтобы обеспечить стерильность препарата плазмиды и удалить как можно больше супернатанта.
ПРИМЕЧАНИЕ: Гранула может сместиться со дна трубки, поэтому внимательно следите за гранулой при выбросе супернатанта. - Высушите гранулу на воздухе внутри ламинарной проточной вытяжки в течение 15 - 20 мин и растворите ДНК в 50 мкл фильтрованного буфера элюирования, 10 мМ Tris-Cl, рН 8,5 (убедитесь, что гранулы не пересушены).
- Поскольку рекомбинантная днк бакмида имеет размер более 135 кб, чтобы избежать сдвига ДНК, растворите гранулу мягким постукиванием.
- Чтобы проверить наличие гена, представляющий интерес, в ДНК бакмида, настройте реакционную смесь ПЦР в 96-скважинную ПЦР-пластину.
- Готовят смесь ПЦР следующим образом: 1 мкл буфера, 0,2 мкл (по 10 мМ) дНТП, 0,1 мкл ДНК-полимеразы Taq, 0,1 мкл (25 мкМ) прямого и обратного праймеров (BACV2FWD: tattccggattattcataccg; BACV2REV: ctctacaaatgtggtatggggc), 1 мкл ДНК бакмида и 8 мкл воды.
- Выполняют амплификацию генов-мишеней с начальной денатурацией в течение 2 мин при 95 °C, затем 25 циклов 94 °C в течение 30 с, 55 °C в течение 30 с и 72 °C в течение 1 мин/кб.
- Прекращают реакцию после окончательного продления в течение 7 мин при 72 °C.
- Электрофорезом анализируют 10 мкл продукта амплификации на 1% (мас./об.) агарозном геле, содержащем раствор для окрашивания нуклеиновой кислотой.
- Храните проверенные ДНК bacmid при 4 °C.
2. Генерация рекомбинантных бакуловирусных запасов
ПРИМЕЧАНИЕ: Используйте экспоненциально растущие клетки Sf9 с жизнеспособностью 95% или более для любого этапа протокола экспрессии бакуловируса, включая трансфекцию клеток для генерации бакуловируса, амплификацию объема бакуловируса, скрининг экспрессии белка и производство белка.
- Трансфекция клеток Sf9 с ДНК Bacmid и трансфекционными реагентами (T.R.), такими как JetPrime или X-tremeGENE 9.
ПРИМЕЧАНИЕ: Окрашивание Trypan Blue и гемоцитометр могут быть использованы для определения количества жизнеспособных клеток и % жизнеспособности клеток. Нежизные клетки занимают пятно и кажутся синими под микроскопом, в то время как жизнеспособные клетки остаются незапятнанными. Чтобы рассчитать % жизнеспособности клеток, получается общее количество клеток (неокрашивых и окрашенных), а количество жизнеспособных клеток делится на общее количество клеток и умножается на 100.- Разбавьте экспоненциально растущие клетки Sf9 до конечной плотности клеток 4 х 105 клеток/мл в сывороточных свободных от насекомых средах и вылейте в резервуар стерильных реагентов.
- Используйте программируемую многоканальную пипетку для засева 0,5 мл разбавленных ячеек Sf9 в каждую скважину 24-скважинной пластины.
- Пометьте один колодец пластины как контрольный (нетрансфессированный) и используйте его в качестве контроля для сравнения трансфекционных и нетрансфекционных клеток для оценки потенциальных признаков инфекций.
- После засева клеток в пластины осторожно раскачивайте пластины вперед и назад несколько раз, чтобы обеспечить равномерный монослой клеток. Не закручивайте пластины, потому что клетки будут группироваться в центре колодца.
- Инкубируют пластины при 27 °C в течение, по меньшей мере, 1 ч, чтобы обеспечить прикрепление клеток к пластинам культуры.
- Хорошо перемешать флакон трансфекционного реагента. Для каждой трансфекции добавляют 2 мкл трансфекционного реагента к 100 мкл трансфекционного буфера. Также можно использовать любую другую необечаемую среду для насекомых. Нанесите разбавленный трансфекционный реагент в резервуар стерильного реагента и осторожно перемешайте в течение 10 с.
- Используя 12-канальный пипетку, переведите 102 мкл разбавленного трансфекционного реагента в стерильную 96-микролуночную пластину.
- Перенесите 10 мкл раствора рекомбинантной бакмидной ДНК 0,2 мкг/мкл в соответствующий колодец 96-скважинной микролуночной пластины и перемешайте, осторожно встряхнув (постукивая) пластину с боков.
- Инкубировать трансфекционную смесь в течение 15-20 мин, чтобы обеспечить образование комплекса.
- Используя регулируемую 6-канальный пипетку, предназначенную для переноса между 96- и 24-скважинными пластинами, добавляют трансфекционную смесь на ячейки по каплям в соответствующие колодцы трансфекционных пластин и инкубируют в течение 4-5 ч при 27 °C.
- Осторожно раскачивайте пластины вперед и назад несколько раз в течение времени инкубации, чтобы обеспечить равномерное распределение трансфекционной смеси по монослою ячейки.
- Через 4-5 ч после трансфекции добавляют 1,5 мл безымянного от насекомых среды, дополненного 10% (v/v) финалом инактивированной фетальной фетальной бычий сыворотки и антибиотико-антимикотической до 1% (v/v) конечного объема (100 ед/мл пенициллина, 100 мкг/мл стрептомицина и 0,25 мкг/мл амфотерицина B).
- Инкубируют клетки в инкубаторе при 27 °C в течение 72-96 ч. Осторожно раскачивая трансфекционные пластины один раз в день, когда это возможно.
- Ищите признаки инфекции (SOI), проявивающиеся в трансфектированных клетках через 72-96 ч после трансфекции(рисунок 2). Имейте в виду, что трансфектированные клетки начнут продуцировать вирус и в дальнейшем заразят культуру; таким образом, ищите признаки инфекции.
ПРИМЕЧАНИЕ: Признаками инфекции являются структурные изменения в клетках насекомых, такие как увеличение диаметра клеток на 25-50%, увеличение ядер клеток, равномерно округлая форма, потеря пролиферации и прилипания к поверхности чашки культуры, а также снижение жизнеспособности клеток(рисунок 2. Бакуловирус Инфицированные и неинфицированные клетки Sf9).
3. Маломасштабный скрининг экспрессии белка и амплификация вируса
- Инфицирование клеток Sf9 бакуловирусными запасами P1.
ПРИМЕЧАНИЕ: через 4-5 дней после трансфекции признаки инфекции должны быть очевидны в трансфектированных клетках по сравнению с контрольными (нетрансфектными) клетками под инвертированной микроскопией. Исходные рекомбинантные бакуловирусы, секретируемые в культурную среду клеток, должны быть готовы к сбору.- Семена 2 х 105 экспоненциально растущих клеток Sf9 в сывороточных средах насекомых в каждую скважину из 24-скважинных пластин в общем объеме 2 мл для заражения вирусами P1 для усиления объема вируса (в результате чего генерируются вирусы P2).
- После пипетки ячеек в пластины аккуратно раскачивайте пластины, используя движение вперед и назад, чтобы обеспечить ровный монослой. Не закручивайте пластины, потому что клетки будут группироваться в центре колодца.
- Инкубируют пластины при 27 °C в течение не менее 1 ч, чтобы обеспечить клеточное прилипастание к пластине.
- Дозировать 4 мл клеток Sf9 при плотности 3,5-4 х 106 в среде, свободной от насекомых, в каждую скважину из 24-скважинных блоков для заражения вирусами P1 для скрининга экспрессии белка.
ПРИМЕЧАНИЕ: Пометьте одну скважину из 24-скважинных пластин и 24-скважинных блоков в качестве контрольной и используйте в качестве неинфицированного контроля для сравнения инфицированных и неинфицированных клеток при поиске SOI. - Используйте программируемую электронную многоканальность, позволяющую одновременный сбор вирусов P1 (этап 2.1.13), заражение свежезасеянных клеток Sf9 (этап 3.1.1) и заражение клеток суспензии в 24-скважинных блоках (этап 3.1.4) 150 мкл вирусов P1.
- Открутите остальные собранные вирусные запасы P1 в течение 15 мин при 17 970 х г,переложите их в микроцентрифужные трубки и храните в темноте при 4 °C.
- Аккуратно раскачивают 24-скважинные пластины (этап 3.1.1) на поршневой шейкер для обеспечения равномерного распределения добавленных вирусов P1 по клеточным монослою; повторите это несколько раз во время инкубации.
- Накрыть 24-скважинные блоки суспензией культуры инфицированных клеток Sf9 (этап 3.1.4) листом воздушной полотнища.
- Инкубировать 24-скважинные блоки при 27 °C, встряхивая при 245 об/мин в течение 72-96 ч.
- Ищите SOI в течение 72-96 ч после заражения в 24-скважинных пластинах с вирусами P2 (шаг 3.1.1) и в 24-скважинных блоках (этап 3.1.4) с инфицированными клетками для скрининга экспрессии.
ПРИМЕЧАНИЕ: через 4-5 дней после заражения клеток Sf9 вирусами P1 SOI должен проявляться в инфицированных клетках по сравнению с неинфицируемыми контрольными клетками под инвертируемым микроскопом. - Соберите вирусы P2 из 24-скважинных пластин, центрифугируют в течение 15 мин при 17 970 х г,переложат их в микроцентрифужные трубки и хранят в темноте при 4 °C.
- Через 72-96 ч после заражения распылите на 24-скважинные блоки 70% этанола, внесите в ламинарную вытяжку и проверьте плотность и жизнеспособность клеток в нескольких скважинах с помощью окрашивания Trypan Blue.
- Приступают к очистке белка, если клетки имеют признаки инфекции и жизнеспособность близка к 70-75%, как оценивается окрашиванием Trypan Blue.
- Гранулировать ячейки центрифугированием 24-скважинных блоков при 525 х г при 4 °C в течение 15 мин. Откажитесь от супернатанта и тщательно повторно суспендируем гранулы в 1 мл лизисного буфера, включающего 25 мМ Tris pH 8,0, 300 мМ NaCl, 0,6 % NP-40, 2 мМ имидазола, 5% глицерина (v/v) и 1x коктейль ингибитора протеазы (коктейль ингибитора протеазы 100x содержит апротинин 0,25 мг/мл, леупептид 0,25 мг/мл, пепстатин А 0,25 мг/мл; Е-64 0,25 мг/мл).
- Хранить клеточную суспензию при -80°С для последующей тестовой очистки (см. раздел 3.2.2).
- Очистка белка из замороженной клеточной суспензии в 24-скважинных тест-экспрессионных блоках.
- Сборка связующего блока(рисунок 3).
- Поместите 3 перекрывающихся слоя парапленки на верхнюю часть блока скважины глубиной 96 (скважина глубиной 96 2,4 мл).
- Поместите фильтрующая пластину с 96 скважинами (фильтрующая микропластилина, 96-скважинный, полипропилен с 25-мкм сверхвысокомолекулярной полиэтиленовой мембраной) поверх блока скважины глубиной 96.
- Опуститесь вниз фильтрующей пластиной, чтобы закрепить наконечники в парапленке, чтобы изолировать фильтрующей пластину от блока глубиной 96 скважин.
- Переложите 50 мкл предварительно уравновешенной 50% смолы Ni-NTA в каждую скважину фильтрующей пластины.
- Процедура тестового выражения
- Поместите замороженную клеточную суспензию (этап 3.1.15), присутствуют в 24-скважинных блоках, на водяную баню при RT в течение 5-10 мин, затем встряхните при 450 об/мин в течение 20 мин.
- Центрифугировать 24-скважинные блоки при 3 275 х г в течение 15 мин.
- Используя многоканальную пипетку, перенесите очищенные лизаты в фильтровальную пластину, содержащую 50 мкл предварительно уравновешенной 50% смолы Ni-NTA (этап 3.2.1.4) и запечатайте фильтрующей пластиной с помощью 96-скважинного колпачкового мата (96-скважинный колпачок, для использования с квадратной скважиной, 2 мл).
ПРИМЕЧАНИЕ: Используйте несколько резинок, чтобы удерживать блок связывания вместе во время этапов инкубации и центрифугирования. - Поместите защищенный связующий блок на 45-60 мин в ротатор в холодном помещении для инкубации очищенных лизатов с смолой Ni-NTA.
- После инкубации осторожно поднимите фильтрующий лист и удалите слой парапленки с поверхности блока скважины глубиной 96 (этап 3.2.1.1).
- Поместите фильтрующую пластину обратно на блок скважин глубиной 96 и раскрутите защищенный блок связывания в течение 2 мин при 235 х г.
- Промывная связь Ni-NTA смолы 2x с 2 мл промывочного буфера, содержащего 25 мМ Tris pH 8,0, 300 мМ NaCl, 5% глицерин и имидазол 15 мМ.
- Отращивание блока с буфером промывки каждый раз в течение 5 мин при 235 х г, чтобы обеспечить полное удаление остаточной жидкости.
- Переложите фильтрующей пластины на верхнюю часть 96-скважинной ПЦР-пластины, содержащей 10 мкл 4-кратного загрузочного красителя.
- Добавьте 40 мкл элюдионного буфера (25 мМ Tris pH 8,0, 300 мМ NaCl, 5% глицерина, 500 мМ имидазола) в каждую скважину фильтрующей пластины и инкубируют в течение 5 мин.
- Вращайте блок, чтобы элюировать белки в 96-скважинную ПЦР-пластину при 235 х г в течение 10 мин.
- Запечатайте 96-скважинную ПЦР-пластину с помощью термостойкой чечетки и нагревайте при 98 °C в течение 3 мин.
- Загрузите 15 мкл элюированных белковых образцов в стандартный буфер Laemmli на 4-20% гель SDS-PAGE рядом с белковой лестницей и запустите гель со стандартным буфером, содержащим SDS.
- Окрась гель синим цветом Coomassie и обезболить водой. Анализируйте результаты тестового выражения, чтобы определить наилучшие выразимые конструкции для крупномасштабного производства.
- Сборка связующего блока(рисунок 3).
4. Препараты бакуловирус-инфицированных клеток насекомых (SCBIIC) для производства белка
- За 4 дня до запланированного времени производства разделить экспоненциально растущие клетки Sf9 до конечной плотности клеток 2х 10 6 клеток/мл на 125 мл / 250 мл / 500 мл стеклянные колбы Эрленмейера с перегородками в 50 мл / 100 мл / 200 мл среды без насекомых, содержащей 1% (v/v) конечный антибиотик-антимикотический.
- Добавьте 0,150 мл / 0,300 мл / 0,6 мл соответствующих вирусов P2, инкубирует инфицированные клетки со скоростью 165 об/мин на орбитальном шейкере с однодюймовым ходом и при более низкой температуре 25 °C для замедления деления клеток.
- Через 4 дня после заражения проверьте клетки под микроскопом на SOI и приступайте к производству, если жизнеспособность клеток, подтвержденная пятном Trypan Blue, близка к 70-75%.
5. Клеточные препараты Sf9 для крупномасштабного производства белка
- За 4 дня до запланированного времени производства рассчитайте необходимый объем клеток Sf9 для крупномасштабной продуцировании белка.
- Посейте 2 л экспоненциально растущих клеток Sf9 в среде без сыворотки насекомых до плотности клеток 1 х 106 клеток / мл в 2,8 л колбы Фернбаха.
- Инкубировать колбы при 27 °C с встряхиванием при 150 об/мин.
ПРИМЕЧАНИЕ: Для предотвращения бактериального загрязнения в культуре клеток Sf9 используют гентамицин до конечной концентрации 10 мкг/мл или пенициллин/стрептомицин до 50 Ед/мл и 50 мкг/мл соответственно.
6. Инфицирование клеток Sf9 SCBIIS для крупномасштабного производства белка
- Разделите 2 л или 4 л экспоненциально растущих клеток Sf9 в среде без сыворотки насекомых до конечной плотности клеток 4 x 106 клеток/мл в колбах Tunair объемом 2,5 л или бутылках с реагентами объемом 5 л.
- Добавьте 10-12 мл/л культуры суспензии клеток насекомых, инфицированных бакуловирусом (SCBIIC).
- Инкубируют инфицированную культуру клеток Sf9 на шейкере со скоростью 145 об/мин при более низкой температуре 25 °C (для замедления деления клеток) в течение 72-96 ч.
- Через 72 ч после заражения проверьте клетки под микроскопом на SOI и оцените жизнеспособность клеток.
- Обычно, примерно через 72 ч после заражения, жизнеспособность клеток Sf9 падает до 70%-75% (измеряется с помощью пятна Trypan Blue). Собирайте зараженные клетки Sf9 в полипропиленовой бутылке объемом 1 л путем центрифугирования при 900 х г в течение 15 мин при 4 °C.
- Повторно суспендируют клеточную гранулу, собранную из 1 л культуры продуцированной клетки с 20-25 мл 1x PBS, путем осторожного закручивание и переноса в конические трубки объемом 50 мл.
- Открутите клеточную суспензию при 900 х г в течение 15 мин и выбросьте раствор PBS.
- Повторно суспендировать промытую ячейку гранулы 20-25 мл суспензионного буфера (20 мМ Tris-HCl pH 8,0, 500 мМ NaCl, 5% глицерин, 1x ингибитор протеазы коктейль) и мгновенно заморозить в жидком азоте; хранить при −80 °C до очистки.
ПРИМЕЧАНИЕ: Процедуры очистки PRMT были подробно описаны в опубликованном SGC документе6.
Результаты
Обзор протокола BEVS приведен на рисунке 1. Множественные конструкции экспрессии PRMT, включая полноразмерные, домены и усеченные фрагменты, были сгенерированы в Консорциуме структурной геномики (SGC, Торонто) в соответствии с стратегиями in-house с попыткой увеличить показатель успеха для идентификации растворимых и стабильных белков с относительно высоким уровнем экспрессии7,9. Заинтересованным читателям предлагается ознакомиться с определениями и методологией SGC по проектированию «фрагмента» как сегмента последовательности генов, включенного в клон экспрессии, «домена» как аннотированного PFAM структурного домена и «конструкции» как фрагмента, клонированного в векторе экспрессии, все из которых были подробно описаны в более ранней публикации7. Конструкции экспрессии PRMT, представленные в этом протоколе, предназначены для получения белков, помеченных полигистидином, клонированных в вектор pFBOH-MHL, который является производным вектора pFastBac1. На рисунке 4представлен анализ SDS-PAGE растворимых конструкций PRMT1, 2, 4-9, очищенных из гранул, собранных после 4 мл продукции в ячейках Sf9 (этап 3.1.4). Полноразмерные (FL) PRMT1 и PRMT9 не представлены в этом геле, так как FL PRMT1 был произведен из E. coli,а FL PRMT9, полученный из BEVS, был очищен Flag-tag6. Усеченные конструкции PRMT1, FL PRMT4 и всех конструкций PRMT8 показывают относительно высокий выход, но элюаты белка содержат фракции коочищенных загрязняющих веществ. Эти конструкции требуют дальнейшей оптимизации протоколов очистки. Таким образом, для повышения чистоты этих белков от масштабных производств требуются дополнительные подходы, такие как уменьшение количества никелевых шариков на стадии инкубации с осветленным лизатом; повышение концентрации имидазола в промывных буферах; расщепление His-метки с протеазой TEV с последующим нанесением на Ni-аффинную смолу; и дополнительные этапы очистки, такие как исключение размера и ионная хроматография. Конструкции PRMT2 показывают значительно более низкий выход по сравнению с другими белками и полноразмерным белком PRMT2, сопровождаемым сильной полосой загрязняющих веществ. Масштабирование производства и две ступени очистки, такие как IMAC и исключение размера, подтвердили низкий уровень экспрессии для этой конструкции наряду с постоянным присутствием коочистающего загрязнителя для белка FL. Чистые белки были получены для комплекса PRMT5, произведенного и очищенного с его партнером по связыванию облигатов, MEP50. Усеченная конструкция PRMT9 имеет почти в два или три раза более низкий уровень экспрессии, близкий к 1,5 мг/л, по сравнению с другими PRMT. Тем не менее, рекомбинантные вирусные запасы этой конструкции были использованы для масштабирования производства, были получены дифрактируемые кристаллы, и структура была решена для этого белка вместе с PRMT4, 6 и 7(Рисунок 5).
Для масштабирования производства соответствующие вирусы P2 использовались для заражения культуры суспензии клеток насекомых Sf9. Этот этап генерирует 50/100/200 мл инфицированных бакуловирусом клеток, содержащих инфицированные клетки и вирусы P3 в супернатанте. Для крупномасштабного производства белка 2 л клеток Sf9 культивировали в каждой из 2,8 л колбы Fernbach shake при 150 об/мин, 27 °C(рисунок 6). В день производства 2 л клеток Sf9 (жизнеспособность клеток > 97%) в колбах Tunair объемом 2,5 л или 4 л в флаконах с реагентами по 5 л разбавляли до плотности ячейки 4 х10 6/мл. Эти клетки были инфицированы непосредственно 10-12 мл / л суспензии культуры инфицированных бакуловирусом клеток насекомых и инкубированы при пониженной температуре 25 ° C при 145 оборотах в минуту. Заражение производственной партии непосредственно суспензионной культурой зараженных бакуловирусом клеток насекомых значительно снижало трудоемкие и трудоемкие этапы амплификации объема вируса, исключая дополнительную обработку инфицированных клеток, и избегало снижения титра и деградации вируса. Поддержание клеточной культуры SF9 и масштабирование производства были выполнены в сосудах для культивирования с большим объемом заполнения для принятия крупномасштабного производства белка в одной партии(рисунок 6).
Полноразмерные PRMT 4, 5 (в комплексе с белками MEP50), 6, 7 и 9, полученные из опосредоопосредования бакуловирусной производственной платформы, использовались для кинетической характеристики и скрининга ингибиторных соединений в SGC6. Кристаллические структуры решали и депонировали в Банк данных о белках (PDB) для полноразмерных или усеченных форм белков PRMT 4, 6, 7 и 9 с различными химическими зондами и ингибиторами. Экспрессионные плазмиды для этих PRMT были депонированы в репозиторий плазмид Addgene (Addgene является дистрибьютором SGC, https://www.addgene.org/) и доступны исследовательским сообществу(рисунок 5).
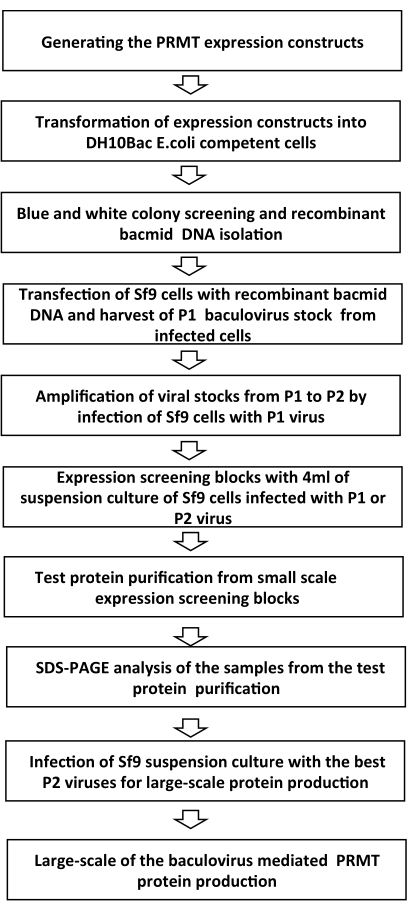
Рисунок 1:Схематический обзор этапов процесса экспрессии бакуловируса Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 2:Бакуловирус Инфицированные и неинфицированные клетки Sf9. Признаками инфекции являются структурные изменения в клетках насекомых, такие как увеличение диаметра клеток на 25-50%, увеличение клеточных ядер, равномерно округлая форма, потеря пролиферации и прилипания к поверхности чашки культуры, а также снижение жизнеспособности клеток. Белая шкала 200 мкм. Признаки инфекции, представленные здесь, одинаковы для трансфектированных клеток, использующих оба трансфекционных реагента, JetPrime и X-tremeGene 9. Конкретный пример приведен для трансфекционного реагента JetPrime. (A) Неинфицированные клетки Sf9 в качестве контроля. (B) Бакуловирус-инфицированные клетки Sf9. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 3:Сборка связующей пластины для быстрой очистки белков тестовой экспрессии. Пожалуйста, смотрите текст для деталей, шаги 3.2.1-2 Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
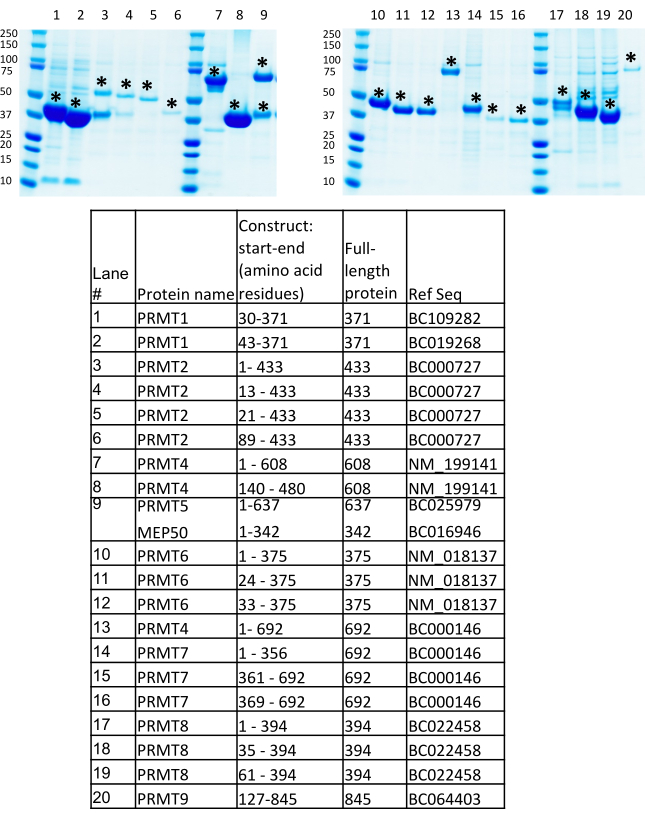
Рисунок 4:Результаты скрининга экспрессии белка. Результаты скрининга экспрессии белка опосредования бакуловирусом производства белка в 4 мл культуры суспензии Sf9, инфицированной соответствующими рекомбинантными вирусами P1 для различных PRMT и комплекса PRMT5-MEP50. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
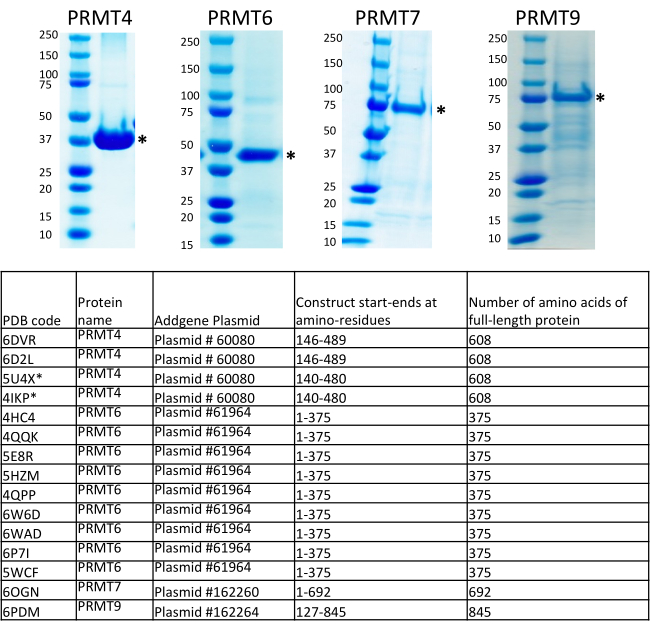
Рисунок 5:Краткое изложение конструкций экспрессии для PRMT4, 6, 7 и 9, используемых для исследований кристаллической структуры в Консорциуме структурной геномики, Торонто (SGC). Кристаллические структуры решали и депонировали в Банк белковых данных (PDB) для полноразмерных или усеченных форм белков PRMT 4, 6, 7 и 9 с различными химическими зондами и ингибиторами. Экспрессионные плазмиды для этих PRMT были депонированы в репозиторий плазмид Addgene и доступны исследовательского сообщества (Addgene является дистрибьютором SGC, https://www.addgene.org/). Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 6:Sf9 поддержание клеток насекомых и производство белка в различных сосудах культуры: (A) 2,8 л колбы Фернбаха для поддержания клеток и производства белка. Использование 72% объема заполнения увеличивает пропускную способность в 2,5 раза на одной встряхиваемой платформе. (B) Колбы для встряхивания Tunair (на этом рисунке представлено только 9 колб из 10) и бутылки с реагентами с объемом заполнения 80% резко увеличивают производственную мощность встряхивающей платформы. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Обсуждение
Одним из преимуществ BEVS в клетках насекомых является способность механизма постпереводной модификации обеспечивать более сложные модификации, такие как фосфорилирование, миристоилирование и гликозилирование. Вместе с высокоэффективным сворачиванию белков млекопитающих эти модификации способствуют большому количеству модифицированного и свернутого белка, подходящего для физиологически значимых последующих экспериментов16.
Здесь мы описали подробные протоколы BEVS, подчеркивающие критические элементы для успешного скрининга экспрессии множественных конструкций белков PRMT и крупномасштабной продукции белка PRMT в платформе экспрессии бакуловируса: 1) Использование регулярных, регулируемых и программируемых многоканальных пипеток для переноса биологических материалов между 24- и 96-клеточными культурами пластин и блоков на этапах генерации ДНК и вируса bacmid; сбор рекомбинантных вирусов, амплификация вирусных объемов рекомбинантных вирусов и подготовка блоков скрининга экспрессии белка. 2) Высокоэффективные и экономичные трансфекционные реагенты для генерации рекомбинантных вирусов. 3) Культура суспензии клеток насекомых, инфицированных бакуловирусом (SCBIIC) для крупномасштабного производства белка. 4) Использование колб fernbach с высоким объемом наполнения 2,8 л для поддержания культуры суспензии Sf9 и колб для коктейлей Tunair объемом 2,5 л и флаконов с реагентами 5 л для крупномасштабного производства белка.
Особые соображения и обоснование этапов преобразования и трансфекции.
Хотя коммерческий протокол рекомендует использовать 100 мкл компетентных клеток для одной трансформации14,эффективность трансформации коммерческих компетентных клеток DH10Bac E. coli составляет 1 х 108 КОЕ / мкг ДНК, поэтому мы используем только 4 мкл. Этого достаточно для каждого трансформанта, чтобы получить изолированные белые рекомбинантные колонии для выделения ДНК бакмида. Адгезивные клетки Sf9 в 24-скважинной трансфекционной пластине засевали при плотности клеток 2 х 105 /мл в 0,5 мл среды насекомых без сыворотки. Этого объема достаточно, чтобы обеспечить равномерное покрытие рабочей поверхности скважины. В то же время он не разбавляет трансфекционную смесь слишком сильно, что повышает эффективность трансфекции. Трансфекционные реагенты не токсичны для клеток Sf9, и обмен сред не нужен. Вместо изменения среды в трансфекционную пластину добавляют дополнительные 1,5 мл среды, содержащей 10% (v/v) FBS через 4-5 часов после трансфекции, чтобы облегчить рост клеток. Эффективность трансфекции обоих трансфекционных реагентов высока. Тем не менее, при X-tremeGene 9 признаки инфекции в трансфеферированных клетках(рисунок 2)появляются на 10-12 ч раньше, чем при реагенте JetPrime, поэтому мы выбираем между этими реагентами в зависимости от рабочего графика следующих шагов в протоколах, что обеспечивает некоторую гибкость в общем процессе.
Скрининг экспрессии белка может быть настроен с вирусами P2, если количество исходных рекомбинантных вирусов, собранных из трансфекционной пластины и помеченных как P1, является ограничивающим фактором для использования для скрининга экспрессии белка.
Рекомендации при переходе от малых к большим объемам языка и культуры.
Исторически считалось, что оптимальный рост клеток требует большого воздушного пространства в культуре суспензии клеток Sf9 и масштабирования производства. Однако в 2014 году сообщалось, что высокое воздушное пространство в культурных судах менее критично, чем считалосьранее 17. Культуральный сосуд, настроенный с использованием соответствующим образом отрегулированной скорости встряхивания до орбитального броска встряхивающей платформы, обеспечит достаточный перенос кислорода даже в культуре суспензии с высоким объемом заполнения, создавая и поддерживая небольшие пузырьки воздуха в течение более длительного времени. При таком подходе коммерчески доступные клетки насекомых можно культивируем с более высокой скоростью встряхивания в пределах нормального диапазона времени удвоения клеток без ущерба для высокой жизнеспособности клеток.
Таким образом, 6 лет назад мы начали увеличивать объем культуры суспензии в трясущейся колбе во время поддержания клеток и ввели другой тип культурального сосуда для производства белка при корректировке и мониторинге условий встряхивания(рисунок 6). Чтобы установить оптимальные условия в этих сосудах культуры, мы контролировали параметры культуры клеток Sf9, такие как время удвоения клеток, а также жизнеспособность клеток, размер и форма, состояние агрегации и инфекционность клеток.
Например, для поддержания клеток Sf9 в колбах для встряхивания Фернбаха 2,8 л мы культивируем 2 л вместо 0,8 л суспензионных клеток Sf9, трясущихся при 150 об/мин при 27 °C, а жизнеспособность клеток большую часть времени близка к 99%, с равномерной формой здоровых делящихся клеток. Для масштабного производства мы заражаем 4 л клеток в 5 л реагентных флаконах, встряхивающихся с высокой скоростью до 145 оборотов в минуту при пониженной температуре 25 °C. Наиболее часто используемые инкубаторы со встроенной встряхивающей платформой могут вмещать 6 x 2,8 л колб для коктейлей или 6 x 5 л реагентных бутылок, или 10 x 2,5 л колб Tunair. Таким образом, емкость одной встряхивающей платформы, если мы заполняем колбы и бутылки с реагентами Fernbach до 1/3 по сравнению с большим объемом наполнения сосудов, составляет 4,8 л против 12 л при использовании 2,8 л колб для коктейлей Fernbach и 10 л против 24 л при использовании 5 л реагентных бутылок(рисунок 6). Поддержание культуры суспензии и масштабирование производства в сосудах культуры с высоким объемом заполнения помогли нам преодолеть ограничения объемов производства и принять крупномасштабную платформу. Таким образом, это очень полезно для лабораторий, не имеющих доступа к биореакторам и / или ограниченного пространства в производственных конвейерах.
Этот протокол может быть легко адаптирован для производства и очистки белковых конструкций с различными метками сродства путем использования соответствующих смол и модификации буферов очистки, как было описано в опубликованной SGC статье6 для помеченных флагом полноразмерных белков PRMT4, 7, 9 и комплекса PRMT5-MEP50 и PRMT6 с метками His. Хотя мы описываем протокол BEVS для семейства белков PRMT, тот же подход может быть применен к любому другому семейству белков.
Раскрытие информации
Авторы заявляют об отсутствии конфликта интересов.
Благодарности
Авторы хотели бы поблагодарить Далию Барсайт-Лавджой за то, что она удостоилась времени, чтобы предоставить ценные отзывы и критические комментарии к рукописи, а также всех наших коллег из SGC, которые работали с семейством белков PRMT, выраженным из векторной системы экспрессии бакуловируса.
SGC является зарегистрированной благотворительной организацией (номер 1097737), которая получает средства от AbbVie, Bayer AG, Boehringer Ingelheim, Genentech, Genome Canada через Институт геномики Онтарио [OGI-196], ЕС и EFPIA через совместное предприятие Innovative Medicines Initiative 2 [грант EUbOPEN 875510], Janssen, Merck KGaA (aka EMD в Канаде и США), Pfizer, Takeda и Wellcome Trust [106169/ZZ14/Z].
Материалы
| Name | Company | Catalog Number | Comments |
| 2.8L Nalgene Fernbach Culture Flask, Polycarbonate, | Nalgene | 29171-854 | For large scale maintenance of suspension culture of Sf9 cells |
| 24-Well Blocks RB | Qiagen | 19583 | For incubation of 4ml of suspension Sf9 cells for protein expression screening |
| 4-20 Criterion TGX Gel 26W 15 ul | Biorad | 5671095 | For SDS-PAGe analysis of the purified proteins |
| 50ml Reagent Reservoir | Celltreat Scientific Products | 229290 | Reservoir used for diluted transfection reagent and Sf9 cells suspension |
| 96-well cap mat, for use with square well, 2 mL | Greiner Bio-One | 381080 | Used to cover 96 well block |
| 96 well PCR plate | Eppendorf | 30129300 | |
| Bacto agar | BD | 214010 | For LB-agar selection paltes |
| Airpore Tape Sheets | Qiagen | 19571 | To cover 24 well blocks for protein expression screening |
| Allega X-15R Centrifuge | Beckman Coulter | 392932 | |
| Antibiotic Antimycotic (100x) | Gibco | 15240112 | |
| Bacmid DNA | in-house | non-catalog item | Bacmid DNA for baculovirus production |
| Bluo-Gal, 1g | Thermo Fisher | 15519028 | |
| Beckman JLA 8.1000 | |||
| Cell Culture Plates, 24-Well, with lid, flat bottom, sterile | Eppendorf | 30722116 | Tissue culture treated plate |
| Cell Resuspension Solution 0.5 L | Millipore Sigma | LSKCRS500 | For Bacmid DNA extraction |
| Cell Lysis Solution 0.5 L | Millipore Sigma | LSKCLS500 | For Bacmid DNA extraction |
| CELLSTAR Tissue Culture Plates, 96 well | Greiner Bio-One | 655180 | For transfection mix |
| ClipTip 1250, filter reload, sterile | ThermoFisher Scientific | 94420818 | Tips for programmable and adjustable multichannel pipette |
| dNTP Mix (25 mM each) | Thermo Fisher Scientific | R1121 | |
| E1-ClipTip Electronic Adjustable Tip Spacing Multichannel Equalizer Pipette, 15 to 1250 μL | ThermoFisher Scientific | 4672090BT | Programmable and adjustable multichannel pipette |
| E4 XLS adjustable spacer 6-channel pipette, 20-300 μL | Ranin | LTS EA6-300XLS | Ranin adjustable multichannel pipette |
| Filter microplate, 96-well, polypropylene, with 25 µm ultra high molecular weight polyethylene membrane | Agilent | 201005-100 | For protein purification in expression screening |
| Full-Baffle Flask Kit Tunair, 2.5L | IBI Scientific | SS-6003C | For large scale protein production in suspension culture of SF9 cells |
| Gentamicin 10x10ml | BioShop | 15750078 | |
| Heat Inactivated Fetal Bovine Serum | Wisent Biocenter | 080-450 | |
| I-Max Insect Media W/ L-Glutamine, 1 L | Wisent Biocenter | 301-045-LL | Serum free insect cells growth medium |
| InstantBlue, Ultrafast Protein Stain | Expedeon Protein Solutions | ISB1L-1L | For protein gel (SDS-PAGE) staining |
| Iptg, Ultra Pure, Dioxane Free, Min 99.5% | BioShop | IPT001.100 | |
| JetPRIME Transfection Reagent Provided with jetPRIME buffer | POLYPLUS TRANSFECTION Inc | 114-01 | For Sf9 cells transfection to generate baculovirus |
| Kanamycin Monosulfate | BioShop | KAN201.100 | |
| Lb Broth (Lennox), Powder Microbial Gro& | Sigma | L3022-1KG | |
| Masterblock 96 deep well 2.4mL | Greiner Bio-One | 780285-FD | Used in the transformation and expression screening procedures |
| Max Efficiency DH10Bac Competent Cells , 0.5ml | Thermo Fisher | 10361012 | Competent cells for bacmid DNA generation |
| mLINE 12-Channel Pipette, adjustable 30 - 300 uL | Sartorius | Sartorius 725240 | 12 channel pipette |
| Neutralization Solution, 0.5 L | Millipore Sigma | LSKNS0500 | For bacmid DNA extraction |
| New Brunswick Innova 44R, 120V, orbit 2.5 cm (1 in) | Eppendorf | M1282-0004 | Shaker incubator for incubaion of suspension of Sf9 cells |
| Ni-NTA Agarose | Qiagen | 30250 | For protein purification |
| Penicillin-Streptomycin (10,000 U/mL) | Gibco | LS15140122 | |
| PYREX Delong Shaker Erlenmeyer Flask with Baffles, Corning 500ml | Pyrex | 4444-500 | For suspension culture of Sf9 cells |
| PYREX Delong Shaker Erlenmeyer Flask with Baffles, Corning 125ml | Pyrex | 4444-125 | For suspension culture of Sf9 cells |
| PYREX Delong Shaker Erlenmeyer Flask with Baffles, Corning 250ml | Pyrex | 4444-250 | For suspension culture of Sf9 cells |
| RedSafe Nucleic Acid Staining Solution | Froggabio | 21141 | |
| RNase A, 0.9 mL | Millipore Sigma | LSKPMRN30 | For suspension buffer for bacmid DNA extraction |
| Roll & Grow Spherical Glass Plating Beads | MP Biomedicals | 115000550 | For spread of bacterial cells across the surface of an agar plate. |
| RT-LTS-A-300μL-768/8 (tips) | Ranin | 30389253 | Tips for ranin multichannel pipette |
| S.O.C. Medium | Thermo Fisher Scientific | 15544034 | |
| Serum, Cell Culture, Fetal Bovine Serum (Fbs), Hyclone, Characterized Canadian | cytivalifesciences | SH3039602 | Addition to the serum free medim for the transfected cells |
| Sf9 cells | Thermo Fisher | 12659017 | Insect cells |
| Sfx-Insect Cell Culture Media | Cytiva (Formerly GE Healthcare Life Sciences) | SH3027802 | Serum free insect cells growth medium |
| Tape Pad | Qiagen | 19570 | Tape Pad |
| Taq DNA Polymerase with ThermoPol Buffer - 2,000 units | New England Biolabs | M0267L | |
| Tetracycline Hcl | BioShop | TET701.10 | |
| Trypan Blue 0.4% Solution | Gibco | 15250061 | For assessment of cell viability |
| VITLAB Reagent Bottles, PP with Screw Caps, PP, BrandTech, 5L | VITLAB | V100889 | For large scale protein production in suspension culture of Sf9 cells |
| VWR Digital Mini Incubator | VWR | 10055-006 | Incubator for adherent Sf9 cells |
| VWR Incubating Microplate Shaker | VWR | 97043-606 | Incubator for suspension culture of Sf9 cells in 24 well blocks |
| VWR Petri Dishes | VWR | CA73370-037 | |
| X-tremeGene 9 DNA Transfection Reagent 1.0 M | Roche | 6365787001 | For Sf9 cells transfection to generate recombinant baculovirus |
Ссылки
- Guccione, E., Richard, S. The regulation, functions and relevance of arginine methylation. Nature Reviews in Molecular Cell Biology. 20 (10), 642-657 (2019).
- Thandapani, P., O'Connor, T. R., Bailey, T. L., Richard, S. Defining the RGG/RG motif. Molecular Cell. 50 (5), 613-623 (2013).
- Lorton, B. M., Shechter, D. Cellular consequences of arginine methylation. Cell and Molecular Life Sciences. 76 (15), 2933-2956 (2019).
- Bedford, M. T., Clarke, S. G. Protein arginine methylation in mammals: Who, what, and why. Molecular Cell. 33 (1), 1-13 (2008).
- Frankel, A., Brown, J. I. Evaluation of kinetic data: What the numbers tell us about PRMTs. Biochimica Biophysica Acta Proteins Proteomics. 1867 (3), 306-316 (2018).
- Li, A. S. M., Li, F., Eram, M. S., Bolotokova, A., Dela Seña, C. C., Vedadi, M. Chemical probes for protein arginine methyltransferases. Methods. 175, 30-43 (2020).
- Savitsky, P., et al. High-throughput production of human proteins for crystallization: The SGC experience. Journal of Structural Biology. 172, 3-13 (2010).
- Gileadi, O., et al. Expressing the human proteome for affinity proteomics: Optimizing expression of soluble protein domains and in vivo biotinylation. New Biotechnology. 29 (5), 515-525 (2012).
- Graslund, S., et al. Protein production and purification. Nature Methods. 5, 135(2008).
- Kost, T. A., Condreay, J. P., Jarvis, D. L. Baculovirus as versatile vectors for protein expression in insect and mammalian cells. Nature Biotechnology. 23, 567-575 (2005).
- Jarvis, D. L. Baculovirus-insect cell expression systems. Methods in Enzymology. 463, 191-222 (2009).
- Shrestha, B., et al. Baculovirus expression vector system: an emerging host for high-throughput eukaryotic protein expression. Methods in Molecular Biology. 439, 269-289 (2008).
- Smith, G. E., Summers, M. D., Fraser, M. J. Production of human beta interferon in insect cells infected with a baculovirus expression vector. Molecular Cell Biology. 3, 2156-2165 (1983).
- Invitrogen Life Technologies. Invitrogen, Bac-to-Bac Baculovirus expression system. , Invitrogen Life Technologies. Carlsbad. (2010).
- Luckow, V. A., Lee, S. C., Barry, G. F., Olins, P. O. Efficient generation of infectious recombinant baculoviruses by site-specific transposon-mediated insertion of foreign genes into a baculovirus genome propagated in Escherichia coli. Journal of Virology. 67, 4566-4579 (1993).
- Irons, S. L., Chambers, A. C., Lissina, O., King, L. A., Possee, R. D. Protein Production Using the Baculovirus Expression System. Current Protocol in Protein Sciences. 91, 1-22 (2018).
- Rieffel, S., et al. Insect cell culture in reagent bottles. MethodsX. 1, 155-161 (2014).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены