Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Структурная МРТ легких с использованием визуализации со свободным дыханием, самостробированием и ультракоротким эхо-временем
В этой статье
Резюме
Описан протокол создания структурных изображений легких с высоким разрешением с использованием магнитно-резонансной томографии (МРТ) с ультракоротким эхо-временем (UTE). Этот протокол позволяет получать изображения с помощью простой последовательности импульсов МРТ во время свободного дыхания.
Аннотация
Высокое качество МРТ легких осложняется низкой плотностью тканей, быстрым ослаблением сигнала МРТ, а также дыхательной и сердечной моторизацией. По этим причинам структурная визуализация легких выполняется почти исключительно с помощью компьютерной томографии (КТ). Тем не менее, компьютерная томография обеспечивает ионизирующее излучение и, таким образом, менее подходит для определенных уязвимых групп населения (например, педиатрии) или для исследовательских целей. В качестве альтернативы вызывает интерес МРТ с использованием ультракороткого времени эха (UTE). Эта техника может быть выполнена во время свободного дыхания в течение ~5-10 минут сканирования. Информация о движении дыхания кодируется вместе с изображениями; Эта информация может быть использована для «самозагрузки» изображений. Таким образом, самостробирование устраняет необходимость в расширенном программировании последовательности импульсов МРТ или использовании дыхательных сильфонов, что упрощает получение изображений. В этом протоколе представлены простые, надежные и вычислительно эффективные методы сбора и реконструкции для получения высококачественной МРТ легких UTE. Этот протокол был разработан для использования на 3T MRI сканере, но те же принципы могут быть реализованы и при более низкой напряженности магнитного поля. Протокол включает в себя рекомендуемые настройки параметров для получения 3D-радиальных изображений UTE, а также указания для самостробированной реконструкции изображений для получения изображений в отдельных фазах дыхания. Благодаря реализации этого протокола пользователи могут создавать изображения легких с высоким разрешением с минимальными или минимальными или отсутствующими артефактами движения. Эти изображения могут быть использованы для оценки структуры легких, что может быть использовано для исследовательского использования при различных легочных заболеваниях.
Введение
Визуализация структуры легких с высоким разрешением является важной частью диагностических обследований при многих легочных заболеваниях. Как правило, это выполняется с помощью компьютерной томографии (КТ), которая идеально подходит для получения изображений легких с высоким разрешением1. Тем не менее, компьютерная томография обеспечивает нетривиальную дозу ионизирующего излучения, что делает ее плохо подходящей для регулярной повторной визуализации, визуализации нескольких различных фаз дыхания или визуализации определенных групп населения (например, педиатрии). Магнитно-резонансная томография (МРТ) не несет в себе такого же риска ионизирующего излучения, и поэтому подходит для таких задач визуализации. Тем не менее, визуализировать легкие с помощью МРТ сложно из-за низкой плотности тканей, дыхательных и сердечных движений, а также очень быстрой релаксации сигнала 2,3,4.
Одним из методов МРТ, который способен смягчить эти проблемы, является МРТ с ультракоротким эхо-временем (UTE) 4,5,6. При МРТ UTE сигнал МРТ дискретизируется сразу после возбуждения сигнала, что снижает влияние быстрой релаксации сигнала. Более того, этот метод осуществляет выборку k-пространства от центра к внешним горизонтам, что приводит к значительной избыточной дискретизации в центре k-пространства. Эта избыточная дискретизация в центре k-пространства делает этот метод визуализации устойчивым к движению. В дополнение к этой присущей ему устойчивости к движению, повторная дискретизация центра k-пространства кодирует информацию о движении дыхания, что делает возможным самостробирование изображений 7,8,9. Это самостробирование может быть использовано для создания изображений на различных фазах дыхания. Поскольку люди проводят большую часть дыхательной фазы на выдохе, обычно создается изображение для конца выдоха, поскольку на этой фазе получено больше всего данных визуализации.
Существует множество стратегий самозаторбирования дыхания при МРТ легких. Первое различие, которое следует сделать, это различие, основанное на изображении и . k-пространственное стробирование10 (рисунок 1). При стробировании на основе изображений набор изображений с высоким временным разрешением создается путем реконструкции небольших временных подмножеств данных изображения. Впоследствии положение диафрагмы на этих изображениях используется для идентификации фазы дыхания для заданного набора проекций изображения10,11. В гейтинге, основанном на k-пространстве, данные из центра k-пространства («k0») исследуются 8,9,12. Интенсивность сигнала изображения кодируется в k0, и, таким образом, интенсивность точки k0 изменяется в зависимости от дыхания. Таким образом, проекции могут быть разбиты на различные дыхательные фазы в зависимости от интенсивности k0. Как в стробировании на основе изображений, так и в k-пространстве проекции с фазами, похожими на дыхательные, группируются для реконструкции изображений. Было высказано предположение, что стробирование на основе изображений обеспечивает повышенную точность оценки дыхательной фазы, тем самым обеспечивая изображения с уменьшенным размытием10,13.
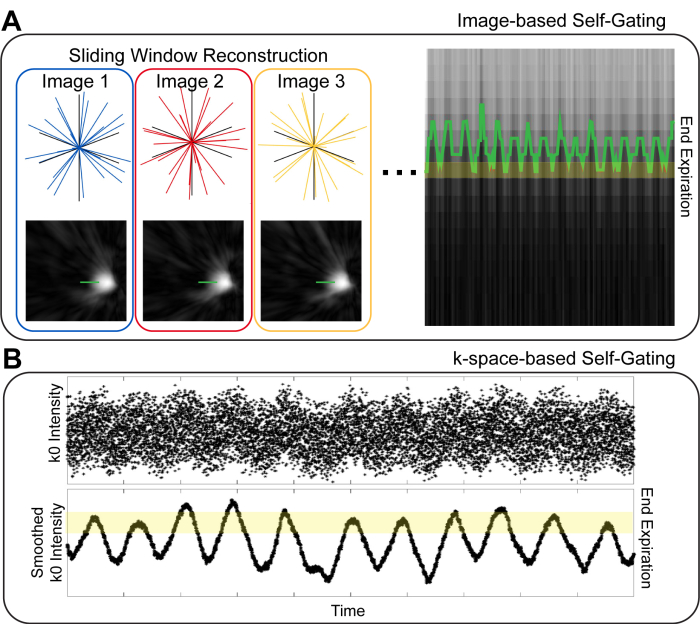
Рисунок 1: Методы самостробирования на основе изображений и k-пространства. (A) При стробировании на основе изображений изображения с низким пространственным разрешением и высоким временным разрешением, показывающие диафрагму, генерируются из временных подмножеств общих данных. Используя линию над диафрагмой, можно визуализировать дыхательные движения и сгруппировать их для реконструкции изображения. (B) В стробировании на основе k-пространства первая точка на проекции k-пространства по центру («k0») используется для визуализации дыхательных движений. После сглаживания k0 различия в интенсивности сигнала, основанные на дыхательном цикле, хорошо видны и могут быть использованы для идентификации различных фаз дыхания. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
Стробирование на основе изображения и k-пространства может быть выполнено с использованием либо жесткого стробирования, либо мягкого стробирования11,14. При жестком гейтинге реконструируются только проекции, соответствующие желаемой фазе дыхания. Однако такое отбрасывание нежелательных проекций может привести к снижению отношения сигнал/шум изображения (SNR) и увеличению артефактов недостаточной дискретизации. Эти нежелательные эффекты можно смягчить с помощью мягкого стробирования. При мягком стробировании все проекции используются для реконструкции изображения, но проекции из нежелательной дыхательной фазы утяжеляются таким образом, чтобы они оказывали меньшее влияние на итоговое изображение. При этом изображения могут быть реконструированы с минимальными артефактами и высоким отношением сигнал/шум, при этом подавляя воздействие дыхательных движений.
Благодаря сочетанию МРТ-сканирования UTE с самостробированием после регистрации можно получить высококачественные изображения, которые, хотя и не эквивалентны КТ, имеют контрастность и разрешение, приближающиеся к КТ-визуализации 6,15,16,17,18,19. В настоящем документе представлен простой протокол для сбора и реконструкции изображений МРТ UTE для получения высококачественных изображений легочной структуры.
Этот протокол написан в первую очередь для 3T MRI сканеров; 3T — это наиболее распространенная напряженность поля, используемая для исследовательской МРТ. Более низкая напряженность магнитного поля, такая как 1,5 Тл или недавно доступная 0,55 Тл20 , может обеспечить улучшенное качество изображения и интенсивность сигнала в легких, поскольку релаксация сигнала в легких происходит медленнее при этих напряженных полях.
Несмотря на то, что были предприняты все усилия для обеспечения ясности и простоты этого протокола и предоставленного кода реконструкции изображения, протокол, вероятно, потребует специального физика МРТ (или аналогичного эксперта по МРТ) для установления соответствующей последовательности МРТ UTE на МРТ-сканере. Последовательность МРТ должна реализовывать стратегию 3D-недекартова кодирования с траекториями k-пространства Center-out. Примеры включают 3D радиальную или 3D спиральную (например, "FLORET")21,22 последовательности изображений. Важно отметить, что порядок проекций должен обладать хорошей временной стабильностью: в течение любого данного подмножества времени проекции должны охватывать весь диапазон k-пространства23. Примерами стратегий упорядочивания проекций с хорошей временной стабильностью являются золотые средние или рандомизированная спираль Хэлтона. Если используется порядок проекции с плохой временной стабильностью, самостробирование после сбора данных приведет к пропуску больших областей k-пространства, что приведет к артефактам изображения. Наконец, последовательность должна быть способна достигать времени эхо-сигнала (TE) <100 μс. Время релаксации T2* в легких при 3 T составляет <1 мс24, поэтому использование очень короткого TE имеет важное значение для получения высококачественных изображений.
протокол
Вся визуализация человека была выполнена с одобрения KUMC IRB. Письменное информированное согласие было получено от всех участников. Изображения в этом исследовании были получены в соответствии с общим протоколом технической разработки, а критерии включения/исключения были намеренно широкими. Критерии включения: возраст ≥ 18 лет. Критерии исключения: МРТ противопоказано на основании ответов на скрининговый опросник МРТ и беременность. Аксессуары и оборудование, использованные для этого исследования, перечислены в Таблице материалов.
1. Получение изображений с помощью UTE
- Подготовьте последовательность изображений. Подготовьте последовательность изображений один раз и используйте эту же последовательность для всех участников.
- Задайте параметры в соответствии с таблицей 1.
- Поместите фантом МРТ в центр МРТ и выполните последовательность визуализации.
ПРИМЕЧАНИЕ: Поскольку эта последовательность требует быстрой градиентной производительности и большого количества радиочастотных импульсов, важно убедиться, что настройка протокола может быть выполнена до тестирования на человеке.
- Подготовьте участника к МРТ. Используйте стандартный скрининг безопасности МРТ, чтобы убедиться, что участник может безопасно войти на МРТ.
- Расположите участника на кровати для МРТ и поместите грудную катушку на туловище участника. Расположите катушку близко к подбородку участника, чтобы обеспечить полное покрытие верхушек легких.
- Переместите участника в МРТ-сканер. Расположите позиционный ориентир чуть ниже грудины участника.
- Соберите сканирование с помощью локализатора, чтобы убедиться, что легкие участника находятся в поле зрения для сканирования UTE. Не перемещайте геометрию скана UTE. Если легкие участника не находятся в поле зрения, переместите участника и сделайте дополнительные сканирования локализатором, пока легкие полностью не окажутся в поле зрения.
- Запустите последовательность UTE. Во время этой последовательности участник может нормально дышать.
- Экспортируйте необработанные данные со сканера. В зависимости от используемой последовательности изображений, сканер может воспроизводить или не восстанавливать изображения на сканере. Для предлагаемой ретроспективной реконструкции стробирования требуются необработанные данные изображения, чтобы определить, генерируются ли изображения на сканере. Обратите внимание, что исходные данные будут большими (>10 ГБ).
- Экспорт или расчет траекторий в k-пространстве (т.е. местоположение в k-пространстве каждой точки исходных данных).
ПРИМЕЧАНИЕ: Для некоторых последовательностей изображений траектории k-пространства могут храниться вместе с необработанными данными на МРТ-сканере и могут быть напрямую экспортированы. Для других последовательностей визуализации траектории k-пространства должны быть рассчитаны на основе параметров визуализации.
| Параметр | Общие рекомендуемые настройки | Настройки, реализованные здесь |
| Последовательность визуализации | 3D недекартовы траектории с центрированием в k-пространстве | Заказ 3D радиальной проекции с золотыми средними |
| Поле зрения | 400 x 400 x 400 мм3 | 400 x 400 x 400 мм3 |
| Размер матрицы | По желанию для целевого разрешения | 320 x 320 x 320 (изотропное разрешение 1,25 мм) |
| Пропускная способность | По мере необходимости для длительности считывания < 1,0 мс | 888 Гц/пиксель |
| ТЭ | < 0,1 мс | 0,07 мс |
| ТР | Минимум (цель 3 – 4 мс) | 3,5 мс |
| Угол поворота | Приблизительно 5° | 4.8° |
| Количество проекций | Минимум 100 000 | 1,35,386 |
| Продолжительность изображения | Минимум 5 мин | 7 мин, 54 с |
Таблица 1: Рекомендуемые настройки для создания образов UTE. Предоставляются общие рекомендуемые настройки, которые можно использовать для настройки протокола. Также приведены конкретные рекомендуемые настройки, которые использовались для данных, как показано в качестве репрезентативных результатов. Спецификации параметров являются общими для всех поставщиков, за исключением пропускной способности. Некоторые крупные поставщики МРТ указывают полосу пропускания как Гц/пиксель. Другие крупные поставщики МРТ указывают абсолютную пропускную способность. Рекомендуемая ширина полосы пропускания (888 Гц/пиксель) соответствует абсолютной полосе пропускания 284 160 Гц.
2. Реконструкция изображения UTE с использованием мягкого гейтирования дыхания на основе изображений
ПРИМЕЧАНИЕ: Код MATLAB для выполнения следующих шагов предоставляется в https://github.com/pniedbalski3/UTE_Reconstruction.
- Импортируйте данные и траектории k-пространства в MATLAB. Код для импорта необработанных данных МРТ доступен для всех основных поставщиков МРТ.
- Отбросьте первые 1000 проекций, чтобы убедиться, что данные находятся в стационарном состоянии намагниченности.
ПРИМЕЧАНИЕ: Если используемая последовательность визуализации включает фиктивные сканирования до сбора данных, этот шаг можно пропустить. - Реконструируйте изображение с низким разрешением, используя очень маленькое подмножество данных.
- Восстановите изображение с помощью неравномерного быстрого преобразования Фурье до размера матрицы 96 x 96 x 96.
- Используйте приблизительно 200 проекций, соответствующих данным за 0,6–0,8 с.
- Реконструируйте и сохраняйте изображения со всех элементов катушки, а также окончательное комбинированное изображение.
- В полученном изображении с помощью катушки выберите корональный срез , на котором четко видна диафрагма.
ПРИМЕЧАНИЕ: Предоставленный код предложит пользователю выбрать срез, содержащий диафрагму. - После того, как этот срез будет выбран, просмотрите отдельные изображения катушек для этого среза и выберите один или два элемента катушки , которые лучше всего показывают диафрагму (рис. 2).
ПРИМЕЧАНИЕ: Предоставленный код предложит пользователю выбрать элементы катушки. - Реконструируйте изображения с помощью скользящего окна для создания изображений с временным разрешением ~0,5 с (рис. 2).
- Восстановите только данные из элементов катушки, выбранных на шаге 2.4.
ПРИМЕЧАНИЕ: В то время как все элементы катушки могут быть реконструированы, только элементы, расположенные ближе всего к диафрагме, необходимы для визуализации мембраны с целью самостробирования дыхания. Благодаря реконструкции только тех элементов катушки, которые находятся ближе всего к диаграмме, время реконструкции и вычислительная нагрузка значительно сокращаются. - Используйте первые 200 проекций для реконструкции изображения с помощью неравномерного быстрого преобразования Фурье (рисунок 2). Сохраните только срез, показывающий диафрагму (как показано в шаге 2.4).
ПРИМЕЧАНИЕ: В конечном итоге будет сгенерировано до 1500 изображений; Для визуализации положения диафрагмы требуется только 2D-срез, а хранение 3D-изображений для каждой из ступеней скользящего окна было бы непомерно затруднительным. - Сдвиг на 100 проекций (т.е. первое изображение реконструируется с помощью проекций 1-200. Второй реконструируют с помощью проекций (101 - 300) и реконструируют дополнительное изображение, сохраняя выбранный на шаге 2.4 срез.
- Продолжайте до тех пор, пока все проекции не будут использованы для создания изображений.
- Восстановите только данные из элементов катушки, выбранных на шаге 2.4.
- Выберите линию над диафрагмой на первом из изображений в виде скользящего окна. Следите за тем, чтобы линия была достаточно длинной, чтобы простираться в легкие на 5-10 вокселей и в диафрагму на 5-10 вокселей.
- Визуализируйте дыхательные движения, просматривая этот навигатор дыхания для всех проекций.
- Определите расположение диафрагмы для всех дыхательных навигаторов. Существует множество способов сделать это, но простой метод заключается в использовании метода25 Оцу для разделения темной стороны (легких) и более светлой стороны (диафрагмы).
- Используйте положение диафрагмы, чтобы обозначить выступы как принадлежащие данному дыхательному бункеру. Если данный респираторный навигатор показывает диафрагму в «положении 1», то 200 проекций, использованных для создания изображения для этого навигатора, будут принадлежать «ячейке 1».
ПРИМЕЧАНИЕ: Поскольку изображения были созданы с использованием скользящего окна с перекрытием 100 проекций, некоторые проекции могут быть помечены как принадлежащие нескольким ячейкам. Грубое пространственное разрешение изображений скользящих окон приводит к тому, что в общей сложности получается ~4-6 ячеек, которые охватывают весь диапазон от вдоха до истечения срока годности. - Выберите ячейку для восстановления, определив, какая ячейка имеет наибольшее количество проекций, которые должны соответствовать окончанию срока действия.
- В качестве альтернативы можно реконструировать изображения для желаемых фаз дыхания на основе визуального осмотра дыхательного навигатора.
- Генерация весов для мягкого стробирования14.
- Используйте экспоненциальный фильтр , чтобы обеспечить вес 1 для проекций в пределах основного бункера и резко уменьшающий вес для проекций в различных дыхательных бункерах.
- Используйте набор инструментов Berkely Advanced Reconstruction Toolbox (BART; https://mrirecon.github.io/bart/)26,27 для восстановления изображения с высоким разрешением в нужном респираторном отсеке.
ПРИМЕЧАНИЕ: BART — это свободно доступный набор инструментов для реконструкции изображений МРТ.- Вычисление весов компенсации плотности с помощью итерационной комбинации плотностей.
- Масштабируйте грузы компенсации плотности с помощью весов с мягким стробированием.
- Данные шкалы на основе компенсации плотности и весов с мягким стробированием
- Выполните базовое неравномерное быстрое преобразование Фурье (NUFFT) для облегчения комбинации катушек.
- Преобразуйте изображение NUFFT в k-пространство с сеткой, которое будет использоваться для комбинации катушек.
- Сгенерируйте матрицу комбинации катушек и используйте ее для объединения катушек как для исходных данных, так и для сетки k-пространства.
- Оцените чувствительность катушки.
- Выполняйте параллельную реконструкцию сжатого чувства с использованием взвешенной компенсации плотности, комбинированных данных катушки и карт чувствительности катушки.
- Сохраните итоговое изображение. Формат NIFTI легко реализуется. Если изображение должно быть загружено в систему PACs, может потребоваться формат DICOM.
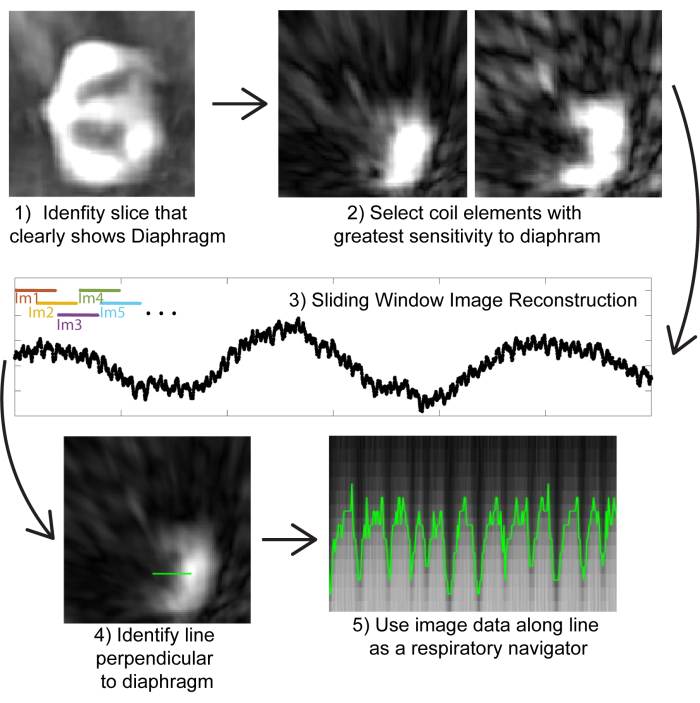
Рисунок 2: Самостробирование на основе изображений. (1) Используя изображение с низким разрешением, восстановленное из небольшого числа проекций (для вычислительной эффективности), определите корональный срез, на котором четко видна диафрагма. (2) Изучив изображения с отдельных элементов катушки, выберите элементы катушки, которые находятся ближе всего к диафрагме. (3) Выполнение реконструкции скользящего окна только тех элементов катушки, которые находятся ближе всего к диафрагме (для вычислительной эффективности). Изображения могут быть сгенерированы из подмножеств из 200 проекций (что соответствует ~0,8 с); Перекрывая проекции, можно достичь псевдовременного разрешения ~0,5 с на изображениях. (4) Определение линии, перпендикулярной диафрагме, которая будет использоваться в качестве дыхательного навигатора. (5) Визуализация данных изображения на этой линии показывает дыхательные движения, которые могут быть использованы для корзины изображений. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
3. Реконструкция изображения UTE с использованием мягкого гейтирования дыхания на базе k-space
- Выполните шаги 2.1-2.4, чтобы можно было определить ближайший к мембране элемент катушки.
- Создание трассировки временных рядов k0 с использованием абсолютного значения первой точки на проекции для всех проекций для выбранного элемента катушки. Это обеспечит визуализацию формы дыхательной волны.
- С шагом в 5000 проекций нормализуем k0 на среднюю интенсивность сигнала тех же k0 точек28. Это уменьшает дрейф интенсивности сигнала с течением времени и обеспечивает улучшенную возможность количественного группирования проекций.
- Обозначьте каждую точку k0 как происходящую во время вдоха или выдоха.
- Сгладьте временной ряд k0 и возьмите производную для оценки наклона для каждой точки на кривой стробирования.
- Наносите метки вдохновения на основе знака склона. Положительный наклон соответствует выдоху, в то время как отрицательный наклон соответствует вдоху.
- Проекции ячеек на основе интенсивности сигнала. Поскольку глубина дыхания может быть переменной, проекции бункера основаны на амплитуде сигнала, а не на местоположении в фазе дыхания.
Примечание: Простым и быстрым методом достижения этой цели является реализация кластеризации k-средних для определения различных уровней интенсивности сигнала. - Для ячеек, промежуточных между окончанием вдоха и окончанием срока действия, определите проекции, возникающие во время вдоха и истечения срока действия, на основе шага 3.4.
- Завершите реконструкцию изображения, следуя шагам, описанным в шагах с 2.10 по 2.13.
- При желании восстановите изображения для всех дыхательных контейнеров, а не только в конце срока годности.
Результаты
Репрезентативные результаты (рис. 3) были получены с использованием настроек, показанных в таблице 1. Используемая продолжительность визуализации обеспечивает высокое качество изображений, которое воспринимается большинством участников.
...Обсуждение
При выполнении визуализации легких с помощью UTE можно использовать множество вариантов как получения, так и реконструкции для получения изображений легких. Этот протокол ориентирован на простоту реализации и вычислительную эффективность. Визуализация с помощью 3D rad...
Раскрытие информации
Питер Недбальски получает финансирование на исследования от Национального фонда склеродермии, Американской кардиологической ассоциации и NIH. Он является консультантом компании Polarean Imaging Plc., которая разрабатывает технологию гиперполяризованной МРТ 129Xe.
Благодарности
Разработка этого протокола и изображений, показанных в качестве репрезентативных результатов, была поддержана Национальным фондом склеродермии.
Материалы
| Name | Company | Catalog Number | Comments |
| Chest MRI Coil | Siemens, GE, Philips,, Other Clinical MRI Imaging Coil Vendor | N/A | A 26 - 32 channel Chest coil should be used |
| High Performance Workstation | HP, Apple, or other Computer Hardware company | N/A | A computer with a minimum of 64 GB of Memory is needed for image reconstruction |
| Matlab | Mathworks | R2016A or newer | A Matlab license is needed to run the provided computer code |
| MRI Phantom | Siemens, GE, Philips, or Other MRI Phantom Vendor | N/A | Any Phantom can be used to test the MRI sequence prior to its use in human subjects. |
| MRI Scanner | Siemens, GE, Philips, or Other Clinical MRI Scanner Vendor | N/A | The protocol was developed on a 3T scanner, but 1.5T or 0.55T would also work with minimal adaptation |
Ссылки
- Raju, S., Ghosh, S., Mehta, A. C. Chest ct signs in pulmonary disease: A pictorial review. Chest. 151 (6), 1356-1374 (2017).
- Biederer, J., et al. MRI of the lung (2/3). Why, when, how. Insights Imaging. 3 (4), 355-371 (2012).
- Biederer, J., et al. MRI of the lung (3/3)-current applications and future perspectives. Insights Imaging. 3 (4), 373-386 (2012).
- Johnson, K. M., Fain, S. B., Schiebler, M. L., Nagle, S. Optimized 3D ultrashort echo time pulmonary MRI. Magn Reson Med. 70 (5), 1241-1250 (2013).
- Ma, W., et al. Ultra-short echo-time pulmonary MRI: Evaluation and reproducibility in COPD subjects with and without bronchiectasis. J Magn Reson Imaging. 41 (5), 1465-1474 (2015).
- Roach, D. J., et al. Ultrashort echo-time magnetic resonance imaging is a sensitive method for the evaluation of early cystic fibrosis lung disease. Ann Am Thorac Soc. 13 (11), 1923-1931 (2016).
- Tibiletti, M., et al. Multistage three-dimensional UTE lung imaging by image-based self-gating. Magn Reson Med. 75 (3), 1324-1332 (2016).
- Weick, S., et al. Dc-gated high-resolution three-dimensional lung imaging during free-breathing. J Magn Reson Imaging. 37 (3), 727-732 (2013).
- Fischer, A., et al. Self-gated non-contrast-enhanced functional lung imaging (SENCEFUL) using a quasi-random fast low-angle shot (FLASH) sequence and proton MRI. NMR Biomed. 27 (8), 907-917 (2014).
- Tibiletti, M., et al. Respiratory self-gated 3D UTE for lung imaging in small animal MRI. Magn Reson Med. 78 (2), 739-745 (2017).
- Jiang, W., et al. Motion robust high resolution 3D free-breathing pulmonary MRI using dynamic 3D image self-navigator. Magn Reson Med. 79 (6), 2954-2967 (2018).
- Higano, N. S., et al. Retrospective respiratory self-gating and removal of bulk motion in pulmonary UTE MRI of neonates and adults. Magn Reson Med. 77 (3), 1284-1295 (2016).
- Metze, P., et al. Non-uniform self-gating in 2D lung imaging. Front Phys. 10, (2022).
- Gandhi, D. B., et al. Comparison of weighting algorithms to mitigate respiratory motion in free-breathing neonatal pulmonary radial UTE-MRI. Biomed Phys Eng Express. 10 (3), 035030 (2024).
- Fauveau, V., et al. Performance of spiral UTE-MRI of the lung in post-covid patients. Magn Reson Imaging. 96, 135-143 (2023).
- Metz, C., et al. Comparison of diagnostic quality of 3D ultrashort-echo-time techniques for pulmonary magnetic resonance imaging in free-breathing. Acta Radiologica. 64 (5), 1851-1858 (2023).
- Periaswamy, G., et al. Comparison of ultrashort TE lung MRI and HRCT lungs for detection of pulmonary nodules in oncology patients. Indian J Radiol Imaging. 32 (04), 497-504 (2022).
- Darçot, E., et al. Comparison between magnetic resonance imaging and computed tomography in the detection and volumetric assessment of lung nodules: A prospective study. Frontiers in Medicine. 9, 858731 (2022).
- Dournes, G., et al. 3D ultrashort echo time MRI of the lung using stack-of-spirals and spherical k-space coverages: Evaluation in healthy volunteers and parenchymal diseases. J Magn Reson Imaging. 48 (6), 1489-1497 (2018).
- Campbell-Washburn, A. E. 2019 American Thoracic Society Bear Cage winning proposal: Lung imaging using high-performance low-field magnetic resonance imaging. Am J Respir Crit Care Med. 201 (11), 1333-1336 (2020).
- Robison, R. K., Anderson, A. G., Pipe, J. G. Three-dimensional ultrashort echo-time imaging using a FLORET trajectory. Magn Reson Med. 78 (3), 1038-1049 (2017).
- Willmering, M. M., Robison, R. K., Wang, H., Pipe, J. G., Woods, J. C. Implementation of the FLORET sequence for lung imaging. Magn Reson Med. 82 (3), 1091-1100 (2019).
- Chan, R. W., Ramsay, E. A., Cunningham, C. H., Plewes, D. B. Temporal stability of adaptive 3D radial MRI using multidimensional golden means. Magn Reson Med. 61 (2), 354-363 (2009).
- Yu, J., Xue, Y., Song, H. K. Comparison of lung T2* during free-breathing at 1.5 T and 3.0 T with ultrashort echo time imaging. Magn Reson Med. 66 (1), 248-254 (2011).
- Otsu, N. A threshold selection method from gray-level histograms. IEEE Trans Syst Man Cybern. 9 (1), 62-66 (1979).
- Martin Uecker, F. O., et al. Berkely advanced reconstruction toolbox. Proc Intl Soc Magn Reson Med. 23, 2486 (2015).
- . . Bart Toolbox for Computational Magnetic Resonance Imaging. , (2024).
- Munidasa, S. . Treatment monitoring of pediatric cystic fibrosis lung disease using free breathing lung MRI. , (2024).
- Zhu, X., Chan, M., Lustig, M., Johnson, K. M., Larson, P. E. Z. Iterative motion-compensation reconstruction ultra-short TE (IMOCO UTE) for high-resolution free-breathing pulmonary MRI. Magn Reson Med. 83 (4), 1208-1221 (2020).
- Tan, F., et al. Motion-compensated low-rank reconstruction for simultaneous structural and functional UTE lung MRI. Magn Reson Med. 90 (3), 1101-1113 (2023).
- Bhattacharya, I., et al. Oxygen-enhanced functional lung imaging using a contemporary 0.55 T MRI system. NMR Biomed. 34 (8), e4562 (2021).
- Kim, M., et al. Feasibility of dynamic T2*-based oxygen-enhanced lung MRI at 3T. Magn Reson Med. 91 (3), 972-986 (2024).
- Klimeš, F., et al. 3D phase-resolved functional lung ventilation MR imaging in healthy volunteers and patients with chronic pulmonary disease. Magn Reson Med. 85 (2), 912-925 (2021).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены