É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Imobilização planária, irradiação parcial e Transplante de Tecidos
Neste Artigo
Resumo
Um método eficaz para enxerto de tecido de tamanho definido e consistente entre planaria é descrito. Também incluído é uma descrição de como a técnica de imobilização utilizado para transplante pode ser adaptado, em conjugação com escudos de chumbo, para a irradiação parcial de animais vivos.
Resumo
A planária, um verme de água doce, tem provado ser um poderoso sistema para dissecar regeneração metazoários e haste 1,2 biologia celular. Regeneração planária de quaisquer tecidos danificados ou ausentes é tornada possível pelas células estaminais adultas denominado neoblasts 3. Embora essas células-tronco foram definitivamente demonstrou ser pluripotentes e singularmente capaz de reconstituição de um animal inteiro 4, a heterogeneidade dentro da população de células-tronco ea dinâmica de seus comportamentos celulares permanecem sem solução. Devido ao grande número e distribuição ampla de células-tronco ao longo do plano do corpo planária, métodos avançados para a manipulação de subpopulações de células estaminais para o estudo molecular e funcional in vivo são necessários.
Transplante de tecidos e irradiação parcial são dois métodos pelos quais uma subpopulação de células-tronco planária podem ser isoladas para estudo posterior. Cada técnica tem vantagens distintas. Ttransplante questão permite a introdução das células estaminais, num hospedeiro ingénuos, que são inerentemente qualquer geneticamente distintas ou que tenham sido previamente tratados farmacologicamente. Alternativamente, a irradiação parcial permite o isolamento de células-tronco dentro de um hospedeiro, justaposta ao tecido desprovido de células estaminais, sem a introdução de uma ferida ou qualquer culatra em integridade do tecido. Usando estes dois métodos, pode-se investigar os fatores celulares autónomos e não autónomos que controlam funções de células-tronco, tais como a proliferação, diferenciação e migração.
Tanto o tecido transplante 5,6 e irradiação parcial 7 têm sido usado historicamente na definição de muitas das questões sobre regeneração planária que permanecem em estudo hoje. No entanto, estas técnicas têm permanecido subutilizada devido à natureza trabalhoso e inconsistente de métodos anteriores. Os protocolos apresentados aqui representam um grande passo na diminuição do tempond esforço necessário para gerar reproduzível um grande número de animais enxertados ou parcialmente irradiada com eficácias que se aproximam de 100 por cento. Nós cobrimos a cultura de animais de grande porte, imobilização, a preparação para irradiação parcial, o transplante de tecidos, ea otimização da recuperação de animais. Além disso, o trabalho aqui descrito demonstra a primeira aplicação do método de irradiação parcial para uso com o planária mais amplamente estudados, Schmidtea mediterranea. Além disso, o tecido eficiente enxertia em planaria abre a porta para o teste funcional de subpopulações de células-tronco ingênuos ou tratados nos ensaios de repovoamento, que tem sido o método padrão-ouro de se avaliar o potencial das células-tronco adultas em mamíferos 8. A ampla adoção destas técnicas irá sem dúvida levar a uma melhor compreensão dos comportamentos celulares de células-tronco adultas durante a homeostase e regeneração tecidual.
Protocolo
Nota: este protocolo sugere a utilização de materiais potencialmente perigosos (chumbo e chloretone). Adquira, leia e siga FDS para todos os materiais potencialmente perigosos.
1. Cultura Animal, Seleção e Preparação
- Para a cultura animal e água manuseamento planária utilização (1X sais Montjuïc 9) e pipetas de transferência de plástico.
- Sexual biótipo Schmidtea mediterranea pode ser usado quando levantada no laboratório sob condições de cultura normal 10. Para produzir amostras de tamanho assexuadas requisito, S. mediterranea levantado à temperatura ambiente sob condições normais 9 deve ser alimentado ao dobro de frequência normal triplo (2-3 vezes por semana) por um a dois meses antes da utilização. Alternativamente, os animais alimentados com uma frequência assexuadas normal pode ser mantida a 10 graus Celsius indefinidamente, a fim de aumentar o seu tamanho médio.
- Seleccionar animais que estão entre 1 a 2 cm emcomprimento e mais largo do que 2 mm, em seguida, fome animais 3-7 dias antes da utilização.
- Se efectuar quaisquer tratamentos farmacológicos ou radiológica em hosts destinados, doadores, ou animais irradiados parcialmente, realizar o tratamento (s) neste momento.
- Se os tratamentos farmacológicos foram realizados à exigida a alimentação dos animais, starve animais um período adicional de 3 a 7 dias antes da utilização.
2. Preparação de Soluções e materiais
- Preparar a solução chloretone, um anestésico local, leve, por dissolução de 0,1-0,2% w / v em água chloretone planária e arrefecimento a solução sobre gelo.
- Se realizar a irradiação parcial apenas, avance para o passo 2.7. Para o transplante de tecidos continue no passo 2.3.
- Usando um bico de Bunsen, dobre 0,75 mm de diâmetro interior, utilizados para o corte do tecido do enxerto, e 0,7 mm de diâmetro exterior, usado para a criação de um buraco no hospedeiro que irá receber o enxerto, tubos capilares a um ângulo de 90 ° em 1-2 cm a partir da extremidade de bistubo ch. Para poupar material, dobre ambas as extremidades de cada tubo capilar e quebrar-los em meio para produzir duas ferramentas. Tome cuidado para não chama os confins dos tubos.
- Corte os seguintes documentos para os tamanhos indicados:
- Negro de papel de filtro (cortado em rectângulos de aprox. 2,5 cm x 1,5 cm)
- Whatman # 3 papel de filtro (cortado em rectângulos de aprox. 2 cm x 0,5 cm)
- Kimwipe (dobrado e cortado em aprox chumaços. 3 cm x 0,5 cm x 4 ply)
- Papel de cigarro rolando (remova a tira de goma e corte em retângulos. Aproximadamente 3 cm x 2 cm)
- Preparar solução modificada de Holtfreter (3,5 g / L de NaCl, 0,2 g / L de NaHCO3, 0,05 g / L de KCl, 0,2 g / L MgSO4, 0,1 g / L de CaCl2, pH 7,0-7,5) e solução saturada de caseína Holtfreter e frio tanto a 4 ° C.
- Anexar uma Kimwipe dobrado a um quadrado de Parafilm e coloque sobre Peltier placa refrigerador ou outro dispositivo de resfriamento situada sob um microscópio de dissecação. Saturar o Kimwipe com Holtf refrigeradossolução de reter e coloque dois retângulos pretos de papel de filtro sobre o Kimwipe.
- Linha de pratos de Petri com papel Whatman n º 2 do filtro. Umedeça o papel de filtro com a solução Holtfreter e relaxar os pratos de gelo. Para a irradiação parcial um prato maior eo revestimento de papel de filtro pode ser usado.
3. Anestesiados e Imobilização
- Encha uma placa de Petri com solução chloretone refrigerados e vermes pipeta no prato. Para o transplante apenas anestesiar um hospedeiro e um doador de cada vez. Para irradiação parcial muitos (n> 10) os animais podem ser anestesiados de uma só vez.
- Permitir vermes de molho na solução chloretone até que se tornem imóvel (5-10 minutos).
- Lavar vermes pipetando-los em um prato cheio com solução refrigerada de Holtfreter.
- Imobilizar animais pipetando-los em papel de filtro preto saturado com solução Holtfreter refrigerados e orientá-los lado ventral para baixo com uma pinça. Se os animais são capazes de locomote, absorva o excesso da solução Holtfreter, diminuir um pouco a temperatura do seu Peltier ou placa fria, ou aumentar a duração do tratamento chloretone.
4. Irradiação parcial
Nota: Siga estes passos para preparar animais para irradiação parcial. Se realizar o transplante em vez disso, vá para a seção 5.
- Coloque uma placa de Petri refrigeradas a partir do passo 2,7 no gelo em um balde de gelo que vai caber dentro de uma fonte superior de raios-X irradiador.
- Dispor animais anestesiados em uma placa de Petri, movendo o papel preto filtro sobre a qual estão imobilizados. Utilizando uma pinça para mover vermes anestesiados directamente, podem prejudicá-las.
- Transporte dispostas animais para um topo fonte de raios-X irradiador e situar o balde de gelo de tal modo que a distância do tubo de cátodo para os animais é minimizado, maximizando assim a taxa de dose eficaz.
- Posição de chumbo blindagem (s) (Figura 1) entre os animais e para o cátodo tUbe, como desejado. Escudos deve ser de 4,5 a 6 mm de espessura para permitir a 97-99% de atenuação de um raio-X 325kV feixe 11.
- Entregar X-ray dose. Se ablação completa de células-tronco a partir de regiões não-blindados é desejada, entregar 30 Gy ou mais usando um irradiador de raios-X. Para referência, 30 Gy é equivalente a 3,6 minutos a 320 kilovolts e 10 miliamperes em uma precisão X-Ray Inc. XRAD320 com uma distância de campo-a-fonte de 30 centímetros.
- Imediatamente após a administração é completa, lidar com vermes pelo filtro de papel preto, animais de transferência em água refrigerada planária. Permitir que a água planária aquecer até à temperatura ambiente e os animais para desalojar-se a partir do papel de filtro preto. O procedimento de irradiação parcial está concluída.
5. Transplante de Tecidos
- Usando uma pipeta de transferência e fórceps, organizar anfitrião anestesiados e vermes doadores em retângulos de papel separadas filtro preto no Kimwipe que tem sido arrefecido no Peltier ou resfriador sob o microscópio de dissecação.
- Usando um tubo de 0,75 milímetros de diâmetro interno capilar cortar a ficha enxerto do doador e, usando uma pinça, coloque-o sobre um fora da porção caminho do host. Se o material do enxerto fica preso no tubo capilar, desalojar com uma pinça.
- Usando um tubo de 0,7 milímetros de diâmetro exterior capilar remover um tampão a partir do hospedeiro e usando fórceps posição do enxerto dentro do orifício que é deixado para trás.
- Transfira o anfitrião transplantado em seu retângulo de papel preto do filtro em placa de Petri preparada no passo 2.7.
- Molhar um pedaço de papel de rolamento com uma solução de caseína Holtfreter saturada e colocá-lo na parte superior do hospedeiro transplantado como ilustrado na Figura 2A.
- Embeber quatro pedaços de papel de filtro em solução saturada de caseína Holtfreter e envolvem o hospedeiro transplantado como ilustrado na Figura 2B.
- Mergulhe quatro maços de Kimwipe corte em caseína solução saturada Holtfreter e colocá-los sobreo papel de filtro a partir do passo 5.6 (Figura 2B). Colocar a tampa e colocar a placa de Petri sobre gelo.
- Transfira o worm doador em água planária para recuperar, curar e regenerar.
- Quando todos os transplantes são completadas, colocar os vermes transplantadas para um incubador a 10 ° C durante a noite.
- Na manhã seguinte, tomando cuidado para não perturbar o enxerto, descobrir a minhoca e transferi-lo (em seu papel preto filtro) para uma placa de Petri com água planaria.
- Permitir que o worm para desalojar-se do papel de filtro ou removê-lo suavemente com uma pinça.
- Troque a água planária uma vez a cada 2-3 dias.
6. Os resultados representativos
Imediatamente após planaria irradiação parcial vai parecer normal e não afetado. Dependendo da dose administrada e da geometria da blindagem usado, tecido irradiado pode regredir e até mesmo se desintegram 7. Tecido blindado deve permanecer intacta. Follregressão tecido devido e uma perda da integridade dos tecidos, uma blastema irá formar estruturas e ausentes serão regenerada (Figura 3A). Se uma amputação é feita na região parcialmente irradiado, o tecido irradiado será resgatado (isto é impedido de regressão ou de desintegração) (Figura 3B). Em ambos os não lesionado e à regeneração caso amputado será atrasada, em comparação com um amputado não irradiado planaria (Figura 3C). Se uma dose de raios-X de 30 Gy foi entregue eo animal foi parcialmente irradiado não lesionado, a ablação de células estaminais bem sucedida em um padrão correspondente com o escudo de chumbo utilizado pode ser confirmado 2 a 3 dias após a irradiação parcial por hibridização in situ para a célula haste marcador Smed-piwi-1 12 (aka smedwi-1) (Figura 4).
Na manhã após o transplante, um enxerto bem sucedida do tecido transplantado deve ser w óbviasithin o tecido do hospedeiro, tendo adere a ambas as superfícies dorsal e ventral do hospedeiro (Figura 5A). Ocasionalmente, o enxerto irá aderir ao apenas a superfície ventral ou dorsal. Se o transplante foi completamente bem sucedida, nenhum sinal do enxerto será visível a partir de qualquer superfície dorsal ou ventral do hospedeiro (Figura 5B). Pouco tempo depois de um enxerto bem sucedida de não irradiado tecido num hospedeiro que tinha sido ablated de células estaminais por irradiação letal 13,14, hibridização in situ para Smed-piwi-1 irá revelar que as células estaminais estão presentes principalmente dentro do enxerto (Figura 5C ). Além disso, os enxertos de sucesso de tecido não irradiado em hospedeiros letalmente irradiados irá resultar em salvamento do tecido do hospedeiro e sobrevivência a longo prazo do hospedeiro 15.

Figura 1. Arranjo geral do componente básicos para irradiação parcial. Em um irradiador de raios-X com um topo posicionado fonte de raios X (tubo de cátodo) a planária anestesiados está posicionado directamente por baixo da fonte de raios X no interior do campo de irradiação. A fim de maximizar a taxa de dose de raios-X, a distância entre a planária ea fonte de raios-X deve ser minimizada. Um escudo de chumbo deve ser posicionado entre o tubo de cátodo e do verme anestesiados, o mais próximo do verme como prático. O escudo de chumbo deve ser projetado, fabricado, e posicionado de modo que ele protege o tecido desejado, mas completamente expõe o resto do worm. Muitos comercial fabrica irá produzir escudos de chumbo personalizados a partir do diagrama de design simples, temos utilizado com sucesso Alpha Systems Corp (Bluffdale, UT). O chumbo deve ser suficientemente espessa para permitir a quantidade desejada de blindagem. Por exemplo, se quase completa da blindagem de um kV 320 feixe de raios X é desejado, o chumbo deve ser de 4,5 a 6 mm de espessura. A planária e escudo são posicionadas sobrepapel embebido um Holtfreter do filtro alinhada placa de Petri, que descansa em um balde de gelo. Dado um campo de irradiação suficientemente grande de raios-X e um número de escudos de chumbo idênticas, as amostras de muitos pode ser parcialmente irradiadas a um tempo (não ilustrado).
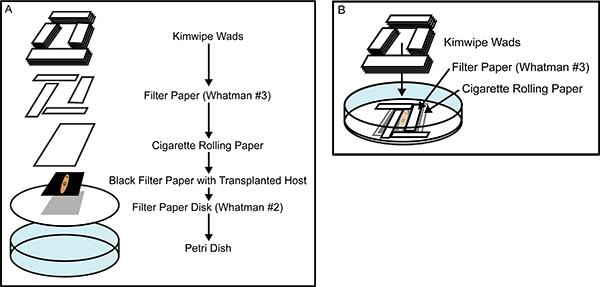
Figura 2. Construindo a câmara de recuperação. (A) Uma vista explodida da câmara de recuperação do tecido do transplante, mostrando todos os componentes que são mergulhados no topo de uma outra depois de ser embebido em solução saturada de caseína Holtfreter do. (B) Uma câmara de recuperação quase completa, ilustrando a colocação de encravamento da Whatman # 3 rectângulos de papel de filtro que se ajustem envolvem o planária anestesiados, impedindo o movimento durante a cura. A construção cuidadosa da câmara de recuperação impede o movimento dos animais e dessecação, promovendo uma rápida cicatrização e maior eficácia dos transplantes de tecidos.

Figura 3. Resultados representativos de irradiação posterior parcial simples. Como Dubois descritos 7, (A) quando a metade posterior da planárias foram protegidos com chumbo e em seguida exposto a irradiação de raios-x do tecido anterior foi observada a regredir de volta para o limite entre o irradiado e blindado tecido em que blastemas ponto sem pigmento formado e os animais começaram a regenerar. (B) Por outro lado, quando os animais foram decapitados após a irradiação mesmo parcial realizada em (A), regressão do tecido não foi observada eo tecido irradiado restante anterior foi resgatado. O decapitados animais irradiados parcialmente cabeças regenerada (B), no entanto, a regeneração foi significativamente retardada em comparação com controlos não irradiados decapitados (C).

Figura 4. Representante outcome de ablação parcial de células estaminais na sequência de irradiação parcial. montagem Whole-A hibridação in situ (pedido) para o marcador de células estaminais Smed-piwi-1 revela que planaria tipo selvagem têm células estaminais distribuído por todo o corpo com a excepção de o tecido anterior à fotorreceptores (ponta de seta) e da faringe adequada (asterisco) 14. (A) Desejo de Smed-piwi-1 no controle irradiado mas totalmente blindado planaria fixado três dias após a irradiação apresenta uma distribuição de células-tronco que é indistinguível da planaria tipo selvagem. (B) Por outro lado, desejam para Smed-piwi-1 em animais que foram apenas parcialmente protegidos, deixando o exposto anterior e posterior, mas também foram fixadas três dias a seguir mostra irradiação que as células estaminais são ablacionados a partir das regiões não blindados . Barras de escala são 500 microns.

Figura 5. Examples de transplante de tecido com sucesso e insucesso. (A) ao vivo imagens de vistas dorsal e ventral de uma planária transplantado com sucesso três dias após o transplante. O enxerto (indicado) é claramente visível em ambas as superfícies dorsal e ventral e está rodeada com o tecido não pigmentado característica na interface enxerto-hospedeiro. (B) correspondente, transplantes mal sucedidos não apresentam qualquer tecido do enxerto visível no local de transplante (indicada) e, em vez mostrar um curada, ferida, despigmentado lateral do transplante falhou. Um enxerto que adere à apenas dorsal ou a superfície ventral pode assemelhar-se um transplante bem sucedido (A) quando visto de um lado e um transplante de insucesso (B) quando visto a partir do outro. (C) Quando tecidual de tipo selvagem (wt) é enxertado em um hospedeiro que tenha sido irradiado ablated de células estaminais residentes e as células transplantadas são posteriormente revelado por desejo de Smed-piwi-1 de dois dias após o transplante eo sucesso do transplante é claramente mostrado pela presença específica de células-tronco só ou em torno da localização do enxerto (pontas de seta). Barras de escala são 500 microns.
Discussão
Importância da imobilização
A imobilização é, de longe, o passo mais crítico para a conclusão com êxito de qualquer destes processos. Se planaria são indevidamente imobilizado antes da irradiação parcial, podem mover-se sob o escudo de chumbo, produzindo resultados inconsistentes e de confusão. Além disso, se os animais são insuficientemente imobilizada após o transplante, o verme hospedeiro provavelmente afastar-se do tecido do enxerto, o que resulta numa falha do enxerto para ...
Divulgações
Não há conflitos de interesse declarados.
Agradecimentos
Os autores gostariam de agradecer a Chiyoko Kobayashi e Kiyokazu Agata para conselhos úteis sobre transplante planária, bem como membros do passado e do presente do laboratório Sánchez para discussões valiosas durante o desenvolvimento dessas técnicas. Este trabalho foi financiado pelo NIH Training Grant (5T32 HD0791) para OCG e R37GM057260 NIH para ASA. ASA é um Howard Hughes Medical Institute.
Materiais
| Name | Company | Catalog Number | Comments |
| Nome do reagente | Companhia | Número de catálogo | |
| General Purpose Transferência Pipetar | Samco | 691 | |
| Os tubos capilares (milímetros ID 0,75) | FHC | 30-30-0 | |
| Os tubos capilares (OD 0,7 mm) | FHC | 30-50-08 | |
| Parafilm M | VWR | 52858-076 | |
| Kimwipes 34155 | VWR | 500029-891 | |
| Papel de filtro preto | Schleicher & Schuell | 10310809 | |
| Whatman n º 2 1002-055 papel de filtro | Fisher Scientific | 09-810B | |
| Whatman # 3 papel de filtro 1003-185 | Fisher Scientific | 09-820E | |
| Papel de cigarro rolando | Zig-Zag, original | NA | |
| Petripratos | VWR | 82050-544 | |
| Pinças DUMONT, INOX # 5 | FST | 11251-20 | |
| Chloretone | Sigma Aldrich | 112054 | |
| Caseína | Sigma Aldrich | C3400 | |
| Chumbo Shields | Alfa Systems Corp, Bluffdale, UT | Design personalizado | |
| XRAD-320 Irradiador Biológica | Precision X-Ray, North Branford, CT | NA |
Referências
- Morgan, T. Experimental studies of the regeneration of Planaria maculata. Arch. Entw. Mech. Org. 7, 364-397 .
- Reddien, P. W., Sanchez Alvarado, A. Fundamentals of planarian regeneration. Annu Rev Cell Dev Biol. 20, 725-757 (2004).
- Randolph, H. The regeneration of the tail in lumbriculus. J. Morphol. 7, 317-344 .
- Wagner, D. E., Wang, I. E., Reddien, P. W. Clonogenic neoblasts are pluripotent adult stem cells that underlie planarian regeneration. Science. 332, 811-816 (2011).
- Santos, F. Studies on transplantation in planaria. Biological Bulletin. 57, 188-197 (1929).
- Morgan, L. Regeneration of grafted pieces of planarians. J. Exp. Zoöl. 3, 269-294 (1906).
- Dubois, F. Contribution á l 'ètude de la migration des cellules de règènèration chez les Planaires dulcicoles. Bull. Biol. Fr. Belg. 83, 213-283 (1949).
- Purton, L. E., Scadden, D. T. Limiting factors in murine hematopoietic stem cell assays. Cell Stem Cell. 1, 263-270 (2007).
- Cebria, F., Newmark, P. A. Planarian homologs of netrin and netrin receptor are required for proper regeneration of the central nervous system and the maintenance of nervous system architecture. Development. , 132-3691 (2005).
- Newmark, P. A., Sánchez Alvarado, A. Bromodeoxyuridine specifically labels the regenerative stem cells of planarians. Dev. Biol. 220, 142-153 (2000).
- Miller, W., Kennedy, R. J. X-ray attenuation in lead, aluminum, and concrete in the range 275 to 525 kilovolts. Radiology. 65, 920-925 (1955).
- Pearson, B. J. Formaldehyde-based whole-mount in situ hybridization method for planarians. Dev. Dyn. 238, 443-450 (2009).
- Hayashi, T., Asami, M., Higuchi, S., Shibata, N., Agata, K. Isolation of planarian X-ray-sensitive stem cells by fluorescence-activated cell sorting. Dev. Growth Differ. 48, 371-380 (2006).
- Reddien, P. W., Oviedo, N. J., Jennings, J. R., Jenkin, J. C., Sánchez Alvarado, A. SMEDWI-2 is a PIWI-like protein that regulates planarian stem cells. Science. 310, 1327-1330 (2005).
- Stéphan-Dubois, F. Les cellules de régénération chez la planaire Dendrocoleum lacteum. Bulletin de la Société Zooologique de France. 86, 172-185 (1961).
- Gurley, K. A. Expression of secreted Wnt pathway components reveals unexpected complexity of the planarian amputation response. Dev. Biol. 347, 24-39 (2010).
- Salvetti, A. Adult stem cell plasticity: neoblast repopulation in non-lethally irradiated planarians. Dev. Biol. 328, 305-314 (2009).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados